Method Article
Atténuation de la néphropathie à IgA médiée par la dioscine en inhibant l’activation des lymphocytes B in vivo et en diminuant la production d’IgA1 déficiente en galactose in vitro
Dans cet article
Résumé
Cette étude fournit des données expérimentales pour le traitement de la néphropathie à immunoglobuline A (IgAN) avec de la dioscine (DIO), l’ingrédient actif du rhizomas de Dioscoreae Nipponicae (DNR), et un paradigme pour étudier les effets de la phytothérapie et les mécanismes sous-jacents in vivo et in vitro.
Résumé
L’augmentation des IgA1 circulantes déficientes en galactose (Gd-IgA1) est causée par une activation excessive des cellules sécrétoires IgA positives dans le processus de réponses immunitaires de la muqueuse, qui est un lien essentiel dans la pathogenèse de la néphropathie à IgA (IgAN). Le patch de Peyer, l’endroit proéminent où les lymphocytes B sont transformés en plasmocytes sécrétant des IgA, est la principale source d’IgA. De plus, l’expression plus faible de la 1β-1,3-galactosyltransférase (C1GalT1) et de son chaperon moléculaire, le chaperon moléculaire spécifique de C1GalT1 (Cosmc), est liée à une glycosylation anormale des IgA1 chez les patients IgAN. Notre expérience clinique montre que la phytothérapie de Dioscoreae Nipponicae Rhizoma (DNR) peut soulager la protéinurie et l’hématurie et améliorer la fonction rénale chez les patients IgAN. La dioscine (DIO) est l’un des principaux ingrédients actifs de la DNR, qui a diverses activités pharmacologiques. Cette étude explore le mécanisme possible de DIO dans le traitement des IgAN.Le modèle de souris IgAN a été établi par induction immunitaire muqueuse. Les souris ont été divisées en groupes de contrôle, de modèle et de gavage DIO. Le dépôt glomérulaire d’IgA chez la souris, les changements pathologiques rénaux et l’expression des marqueurs de cellules B CD20 et CXCR5 dans le patch de Peyer ont été détectés par immunofluorescence et immunohistochimie. Après la stimulation par lipopolysaccharide (LPS), les effets de DIO sur la prolifération des cellules DAKIKI, la sécrétion d’IgA et de Gd-IgA1, l’expression de C1GalT1 et de Cosmc ont été étudiés à l’aide d’un kit de comptage cellulaire (CCK-8), d’un test ELISA (Enzyme-linked immunosorbent test), d’une réaction en chaîne par polymérase quantitative en temps réel (QRT-PCR) et d’un western blot (WB). Dans des études in vivo , le dépôt d’IgA accompagné d’une hyperplasie mésangiale glomérulaire et d’une expression accrue de CD20 et CXCR5 dans le patch de Peyer chez la souris modèle IgAN a été atténué par DIO. Des études in vitro ont montré qu’une injection directe de 0,25 μg/mL à 1,0 μg/mL inhibait la prolifération des cellules DAKIKI induite par le LPS, la sécrétion d’IgA et de Gd-IgA1, et régulait à la hausse l’expression de l’ARNm et des protéines C1GalT1 et Cosmc. Cette étude démontre que la DIO peut réduire la production de Gd-IgA1 en inhibant l’activation excessive des cellules sécrétant des IgA et en régulant à la hausse l’expression de C1GALT1/Cosmc.
Introduction
La néphropathie à IgA (IgAN) est le type le plus courant de glomérulonéphrite primitive, pour laquelle il n’existe pas de traitement spécifique, et elle reste une cause importante d’insuffisance rénale terminale1. Bien que la pathogenèse de l’IgAN ne soit pas encore entièrement comprise, l’hypothèse des « coups multiples » est généralement acceptée et étayée par un grand nombre de preuves de recherche clinique et expérimentale2. La pathogenèse des IgAN implique l’activation des lymphocytes B et la production d’IgA1 déficientes en galactose (Gd-IgA1)3. L’augmentation des Gd-IgA1 circulantes due à la prolifération et à l’activation excessives des cellules sécrétant des IgA pendant la réponse immunitaire de la muqueuse est un lien critique dans la pathogenèse des IgAN 4,5,6. En tant que lieu central pour la prolifération et l’activation de la conversion du phénotype des lymphocytes B en cellules sécrétant des IgA, le patch de Peyer est la principale source de sécrétion d’IgA, étroitement liée à l’apparition et au développement des IgAN 7,8. De plus, la prolifération des cellules sécrétant des IgA1, ainsi que l’expression de la Core 1β-1,3-galactosyltransférase (C1GalT1) et du chaperon moléculaire spécifique de C1GalT1 (Cosmc), ont été associées à une glycosylation anormale des IgA1, ce qui provoque la production de GD-IgA1 chez les patients IgAN 6,9.
L’étude clinique sur le traitement par IgAN par phytothérapie a progressé ces dernières années. Yiqi Qingjie Formula est une formule essentielle pour le traitement des IgAN par le Département de néphrologie de l’hôpital Guang’anmen. L’étude précédente de notre groupe a révélé que la Gd-IgA1 diminuait dans le sérum des patients IgAN après un traitement avec Yiqi Qingjie Formula. En tant que l’une des herbes les plus utilisées dans la formule Yiqi Qingjie, Dioscoreae Nipponicae Rhizoma (DNR) est le rhizome séché de Dioscorea Nipponica Makino, qui a diverses fonctions telles que la régulation de l’immunité, la suppression de l’inflammation, le soulagement de la toux et de l’asthme10,11. Plusieurs chercheurs ont traité les IgAN avec DNR et ont obtenu de bons résultats 12,13,14. En tant que principal ingrédient actif de DNR15, la dioscine (DIO) abaisse l’acide urique, inhibe la fibrose, inhibe la réponse inflammatoire et le stress antioxydant16,17. Par conséquent, la DIO peut avoir un nouveau mécanisme d’action pour inhiber la sécrétion cellulaire d’un excès de Gd-IgA1 et exercer des effets spécifiques de protection rénale. Pourtant, aucune étude n’a été rapportée sur le mécanisme d’action de DIO pour traiter les IgAN.
Afin d’explorer le mécanisme thérapeutique potentiel de la DIO sur les IgAN et de fournir une nouvelle méthode pour le traitement des IgAN, nous avons mené des expériences sur les effets thérapeutiques de la DIO sur les IgAN in vivo et in vitro.
Protocole
Le comité d’éthique de l’hôpital de Guanganmen a approuvé cette expérience (numéro d’approbation éthique de l’expérimentation animale : IACUC-GAMH-2023-003).
1. Préparation des souris à la procédure expérimentale
- Élever 22 souris Balb/c mâles de grade SPF (âgées de 6 à 7 semaines, poids corporel de 20 à 25 g) dans l’animalerie de l’hôpital ou du centre de recherche. Répartissez les animaux en groupes témoins (n = 8) et modèles (n = 14) à l’aide de la méthode de la table de nombres aléatoires.
- Après 1 semaine d’élevage adaptatif en cage de laboratoire, nourrir le groupe modèle (groupe IgAN) avec une solution de gammaglobulines bovines (BGG) à 0,1 % dans de l’eau acidifiée contenant 6 mmol/L de HCl pendant 9 semaines selon le protocole de modélisation de Zou et al.18.
- Injecter 0,1 mL de solution saline de BGG à 0,1 % dans la veine de la queue pendant 3 jours consécutifs tout en continuant à boire la solution de BGG pour préparer un modèle de souris expérimental d’IgAN18.
- Laissez le groupe témoin boire librement 6 mmol/L d’eau acidifiée HCl sans BGG pendant 9 semaines. Injectez le volume correspondant de solution saline dans la veine de la queue pendant 3 jours consécutifs.
REMARQUE : Les groupes de contrôle et de modèle ont été nourris avec la même qualité que l’alimentation normale. - Après l’injection dans la veine caudale, sélectionnez au hasard 2 souris dans le groupe témoin et 2 souris dans le groupe modèle et examinez-les par protéinurie, microscopie optique et immunofluorescence pour déterminer si la modélisation a réussi.
REMARQUE : Aucune nourriture n’est fournie aux animaux, mais ils ne sont pas interdits d’eau ; Enregistrer le débit d’urine. - Recueillir l’urine pendant 24 h par des cages métaboliques et la centrifuger à 400 x g pendant 5 min ; jeter les sédiments d’urine. Après une dilution de 10 fois du surnageant, mesurer la concentration de protéinurie à l’aide d’un kit de dosage des protéines urinaires, puis multiplier par le facteur de dilution et le volume urinaire pour obtenir 24 h de protéines urinaires totales.
REMARQUE : Les méthodes de microscopie et d’immunofluorescence sont présentées dans les sections 3 et 4, respectivement. - Après avoir préparé le modèle avec succès, divisez 12 souris du groupe de modèles en 6 souris, chacune dans le groupe de modèles (groupe IgAN) et le groupe de gavage DIO (groupe DIO), selon la méthode de la table de nombres aléatoires.
- Que le groupe témoin continue à boire 6 mmol/L d’eau acidifiée HCl sans BGG, et le groupe modèle une solution BGG à 0,1 % composée d’eau acidifiée contenant 6 mmol/L de HCl. Calculer la dose d’administration par gavage du groupe DIO selon la formule de conversion de dose de la méthodologie expérimentale pharmacologique (convertie en fonction de la masse corporelle humaine de 70 kg)19. Gavage DIO comprimés 0,06 g/kg une fois par jour pendant 8 semaines.
- Après 8 semaines de gavage, anesthésier les souris par voie intrapéritonéale avec 0,4 % de pentobarbital sodique (60 mg/kg), et après avoir confirmé l’anesthésie appropriée par pincement des orteils, isolez les reins et le patch de Peyer pour des analyses ultérieures de microscopie optique et d’immunohistochimie.
REMARQUE : Le schéma du modèle in vivo est présenté à la figure supplémentaire 1.
2. Analyse histologique
- Coupes de paraffine pour les reins et le patch de Peyer
- Fixer des tissus rénaux de 3 mm d’épaisseur ou 1 patch de Peyer avec 4% de paraformaldéhyde pendant 24 h, déshydrater avec de l’éthanol dégradé et du xylène. Tremper dans la cire pendant 2 h, sceller et congeler.
- Coupez des sections de reins de 2 m d’épaisseur et des sections de patch de Peyer de 4 m d’épaisseur et étalez-les dans de l’eau tiède. Ramassez les tranches dépliées à l’aide d’une lame en verre propre et faites-les cuire dans un four à température constante à 40 °C pendant 1 h. Commencer la coloration après le prétraitement de l’échantillon.
REMARQUE : Prenez la surface coronale de la partie hilaire du rein, avec une épaisseur de bloc de tissu de 3 mm.
- Décaffinez et colorez les sections de paraffine à température ambiante (RT) pendant 10 min avec une solution acide périodique, en évitant la lumière. Rincez à l’eau distillée et essuyez à sec avec la solution de coloration Schiff’s pendant 20 à 30 min, en évitant la lumière. Rincer à l’eau distillée jusqu’à ce que les sections soient rouges au microscope.
- Placez les sections dans une solution de coloration à l’hématoxyline, colorez les noyaux pendant 3 minutes (les noyaux trop profondément colorés peuvent être divisés par du chlorhydrate d’éthanol) et rincez à l’eau courante jusqu’à ce que les lames soient incolores.
- Effectuez une déshydratation de routine avec des concentrations dégradées d’éthanol et de xylène, scellez les sections avec de la gomme neutre et observez au microscope. Le PAS-positif est rouge et le noyau est bleu.
3. Analyse immunohistochimique du patch de Peyer
- Préparez des sections de paraffine du patch de Peyer comme décrit à l’étape 2.1.
REMARQUE : L’épaisseur des sections pour l’immunohistochimie et l’immunofluorescence ultérieure est de 4 μm. - Décaffinez les sections de paraffine :
- Placez les sections dans le xylène I pendant 5 min, le xylène II pendant 5 min et le xylène III pendant 5 min.
- De plus, rincez les lames dans de l’éthanol anhydre I pendant 5 min, de l’éthanol anhydre II pendant 5 min, de l’alcool à 85 % pendant 5 min, de l’alcool à 75 % pendant 5 min. Rincez ensuite les lames à l’eau distillée.
- Récupération d’antigènes
- Préparez une solution mère de citrate de sodium 50x et diluez-la avec de l’eau distillée à 1x pour l’utilisation. Chauffez-le dans un autoclave pendant 2 min, puis placez les tranches dans l’autoclave en veillant à ce que le niveau de liquide dépasse le niveau des tranches.
- Faites chauffer à haute température pendant 5 min, puis laissez les lames refroidir naturellement. Lavez les tranches trois fois avec la solution PBS pendant 5 minutes chacune.
- Blocage de la peroxydase endogène : Marquez les bords du tissu dans un cercle avec un stylo immunohistochimique. Incuber les sections dans une solution de peroxyde d’hydrogène à 3 % pendant 15 minutes à l’heure de l’art, à l’abri de la lumière, et laver les sections trois fois avec une solution PBS pendant 5 minutes à chaque fois.
- Blocage du sérum : Bloquez les sections en déposant 10 % de sérum de chèvre sur les sections de tissus marquées pendant 30 minutes à RT. Assurez-vous que les sections sont uniformément recouvertes de la tache.
- Incubation de l’anticorps primaire : Secouez doucement la solution bloquante et ajoutez une proportion de l’anticorps primaire préparé (CD20 [1:800] ; CXCR5 [1:800]) à la section. Placez la section à plat dans une boîte humide et incubez toute la nuit à 4 °C.
REMARQUE : Ajoutez une petite quantité d’eau dans la boîte humide pour éviter l’évaporation de l’anticorps. - Incubation secondaire d’anticorps : Lavez les sections trois fois avec une solution de PBS pendant 5 minutes à chaque fois. Retirez le PBS en secouant les sections pour les sécher, couvrez le tissu avec une goutte d’anticorps secondaire (HRP-label) de l’espèce apparentée de l’anticorps primaire, et incubez à RT pendant 50 min.
- Homogénéisation de la 3,3'-diaminobenzidine (DAB) : Laver les sections avec une solution de PBS trois fois pendant 5 minutes chacune. Après avoir secoué les sections pour les sécher, déposez la solution chromogène DAB fraîchement préparée sur les sections. Observer le temps de développement des couleurs au microscope ; Le positif est jaune brunâtre. Rincer à l’eau du robinet pour terminer le développement de la couleur.
- Coloration des noyaux : Colorez à nouveau avec de l’hématoxyline pendant environ 1 min, lavez à l’eau du robinet, puis rincez pendant 10 min à l’eau du robinet pour revenir au bleu.
- Déshydratation et scellement :
- Placez les sections dans de l’alcool à 75 % pendant 5 min et à 85 % d’alcool pendant 5 min. Placez les sections dans de l’éthanol anhydre I pendant 5 min, de l’éthanol anhydre II pendant 5 min et de l’éthanol anhydre III pendant 5 min.
- Lavez les sections dans du xylène I pendant 5 min, sortez-les pour les faire sécher légèrement et scellez les sections avec de la gomme neutre.
- Acquisition d’images : Collectez des images par examen microscopique et analysez-les à l’aide d’un logiciel halo pour l’analyse d’images panoramiques du tissu.
REMARQUE : Les noyaux colorés à l’hématoxyline sont bleus, et l’expression positive du DAB est observée sous forme de jaune brunâtre.
4. Immunofluorescence rénale IgA
- Préparez des coupes de paraffine pour les reins comme décrit à l’étape 2.1.
- Décaffiner les sections de paraffine :
- Placez les sections dans le xylène I pendant 5 min, le xylène II pendant 5 min et le xylène III pendant 5 min. Traitez les sections avec de l’éthanol anhydre I, de l’éthanol anhydre II, de l’éthanol à 95 %, de l’éthanol à 90 %, de l’éthanol à 80 %, de l’éthanol à 70 % et de l’éthanol à 50 %, pendant 5 min, et lavez-les à l’eau distillée.
- Récupération de la protéinase K : Secouez les sections pour les sécher et tracez un cercle autour de la section de tissu avec un stylo histochimique. Ajouter la solution de travail de protéinase K (rapport 1:9 de la solution mère et du PBS) goutte à goutte pour couvrir le tissu et incuber à 37 °C pendant 30 min. Lavez les sections trois fois avec du PBS pendant 5 minutes chacune.
- Pénétration de la membrane cellulaire : Secouez légèrement les sections pour les sécher, puis couvrez-les de Triton à 0,1 %. Incuber pendant 20 min à RT et laver les sections trois fois avec du PBS pendant 5 min chacune.
- Blocage : Ajouter 10 % de sérum de chèvre goutte à goutte pour couvrir uniformément les tissus pour le blocage à la RT pendant 30 min.
- Incubation primaire de l’anticorps : Ajouter une quantité appropriée d’anticorps IgA conjugués anti-souris AF488 de chèvre (1:500) goutte à goutte pour couvrir uniformément le tissu et incuber toute la nuit à 4 °C.
- Coloration des noyaux : Lavez les tranches trois fois avec du PBS pendant 5 minutes chacune. Après avoir retiré le PBS, ajoutez le colorant 4′,6-diamidino-2-phénylindole (DAPI) goutte à goutte sur les sections et incubez pendant 15 min à RT, à l’abri de la lumière.
- Laver et sceller les sections : Lavez les sections trois fois avec du PBS pendant 5 min, puis scellez-les avec un support de montage anti-décoloration.
- Microscopie et photographie : Observez les coupes au microscope fluorescent et prenez des images.
REMARQUE : Pour DAPI, l’excitation ultraviolette est de longueur d’onde 330-380 nm et la longueur d’onde d’émission est de 420 nm, lumière bleue. La longueur d’onde d’excitation de l’isothiocyanate de fluorescéine (FITC) est de 465 à 495 nm et la longueur d’onde d’émission est de 515 à 555 nm, lumière verte.
5. Culture cellulaire
- Obtenir la lignée de lymphocytes B humains DAKIKI auprès de l’ATCC, aux États-Unis. Culture de cellules DAKIKI dans un milieu RPMI-1640 complété par 10% de FBS et 1% de pénicilline-streptomycine.
- Cultivez les cellules dans un incubateur à 37 °C, 5% de CO2 et sous-cultivez-les tous les 2-3 jours. Utilisez des cellules en phase de croissance logarithmique pour toutes les expériences.
- À 70 %-80 % de confluence, prélever les cellules à l’aide d’une pipette stérile et centrifuger les cellules à 140 x g pendant 5 min. Jetez le surnageant, mettez-le en suspension avec le milieu sans sérum et, après 24 heures, laissez toutes les cellules dans une période de repos pour un traitement ultérieur.
6. Tests de cytotoxicité LDH pour le dépistage de concentrations sûres de DIO sur des cellules DAKIKI normales
- Ensemencez les cellules DAKIKI dans des plaques de 96 puits à une densité de 4x105 cellules/puits et mettez en place un groupe témoin faible, un groupe témoin élevé et différentes concentrations de DIO (0,25, 0,5, 1,0, 2,0, 4,0, 8,0 μg/mL). Incuber dans un incubateur à 5% de CO2, 37 °C pendant 24 h après le traitement correspondant selon la méthode de regroupement.
- Selon les instructions du kit de détection de la cytotoxicité, ajoutez 5 μL de lysat par puits dans le groupe témoin élevé, puis placez la plaque dans un incubateur à 5 % de CO2, 37 °C pendant 15 min.
- Sortez la plaque, ajoutez 100 μL du mélange réactionnel dans chaque puits, incubez dans l’obscurité pendant 10 min à RT, puis ajoutez 50 μL de la solution d’arrêt de la réaction. Mesurez la valeur OD à 490 nm sur le lecteur de microplaques dès que possible.
- Calculer le taux de libération de LDH de différentes concentrations de DIO et de ≤10 % comme dose maximale administrée selon la formule : Taux de libération de LDH = (LDH bien expérimentale - LDH faiblement témoin) / (LDH haute maîtrise - LDH faible) x 100 %.
7. Test CCK-8 pour détecter l’effet de DIO sur la prolifération cellulaire DAKIKI
- Sur la base des résultats de nos expériences précédentes20, établissez un modèle IgAN utilisant LPS 40 μg/mL pour induire des cellules DAKIKI.
- Ensuite, ensemencez 4 x 105 cellules/puits dans des plaques de 96 puits et divisez-les en groupes de contrôle, de modèle et d’ID numériques à faible, moyenne et haute concentration (0,25 μg/mL, 0,5 μg/mL et 1,0 μg/mL). Incuber les plaques dans un incubateur à 5 % de CO2, 37 °C pendant 24 h.
- Ensuite, ajoutez 20 μL de réactif CCK-8 dans chaque puits et remettez les plaques dans l’incubateur (5 % CO2, 37 °C) pendant 2 h. Après l’incubation, détectez le DO à une longueur d’onde de 450 nm sur le lecteur de microplaques dès que possible.
8. ELISA pour détecter l’effet de la DIO sur la sécrétion d’IgA et de Gd-IgA1 par les cellules DAKIKI
- Ensemencez les cellules DAKIKI dans des plaques de 6 puits à une densité de 6x106 cellules/puits, puis regroupez et traitez les cellules selon l’étape 7.2. Cultiver les cellules pendant 24 h, puis centrifuger à 850 x g pendant 10 min à 4 °C pour obtenir le surnageant.
- Détectez les concentrations d’IgA et de Gd-IgA1 conformément aux instructions du kit.
9.qRT-PCR pour détecter l’effet de la DIO sur les niveaux d’ARNm C1GALT1 et Cosmc dans les cellules DAKIKI
- Ensemencez les cellules DAKIKI à une densité de 6x106 cellules/puits dans une plaque à 6 puits, regroupez et traitez les cellules comme CCK8 mentionné à l’étape 7.2, et incubez pendant 24 h. Extrayez l’ARN total des cellules DAKIKI selon les instructions du kit d’extraction d’ARN total.
- Après avoir prélevé 1 μL d’ARN extrait de chaque groupe d’échantillons et mesuré sa concentration, transcrivez inversement 1 μg d’ARN total de chaque échantillon en ADNc selon les instructions du kit.
- Ensuite, effectuez une amplification RT-PCR pour détecter l’expression de chaque gène (95 °C pendant 15 min, 95 °C pendant 10 s et 60 °C pendant 30 s). Calculez le niveau d’expression de chaque gène à l’aide de la méthode 2-ΔΔCT avec la β-actine comme référence interne.
REMARQUE : Les séquences d’amorce étaient les suivantes :
C1GALT1 : 5'-AAGGTTGACACCCAGCCTAA-3', 5'-CTTTGACGTGTGTGGCCTTT-3' ;
Cosmc : 5'-GCTCCTTTTTGAAGGGTGTG-3', 5'-TACTGCAGCCCAAAGACTCA-3' ;
β-actine : 5'-TCACCCACACTGTGCCCATCTACGA-3', 5'-CAGCGGAACCGCTCTCATTGCCAATGG-3'.
10. Western blot pour examiner l’effet de DIO sur l’expression des protéines C1GALT1 et Cosmc dans les cellules DAKIKI
- Ensemencez les cellules DAKIKI à une densité de 6x106 cellules/puits dans une plaque à 6 puits. Regroupez-les et traitez-les comme mentionné à l’étape 7.2. Après 24 h d’incubation, prélever chaque groupe de cellules.
- Ajouter une quantité appropriée de solution de lyse cellulaire (PMSF : inhibiteur de la phosphatase : solution de lyse RIPA = 1:1:100) et incuber sur glace pendant 30 min. Ensuite, centrifuger à 13 500 x g pendant 10 min à 4 °C et recueillir le surnageant.
- Déterminez la concentration en protéines à l’aide du kit de dosage de la concentration en protéines BCA.
- Mélangez les échantillons de protéines avec 5 tampons de chargement SDS-PAGE à 4:1 par vortex, et chauffez les échantillons mélangés à 100 °C pendant 5 min pour dénaturer la protéine.
- Pour détecter des protéines de poids moléculaires différents, ajoutez le marqueur protéique (5 μL/puits) et des échantillons (20 μg/puits) dans différentes voies d’un gel SDS-PAGE à 12 %, effectuez une électrophorèse SDS-PAGE et transférez le gel sur des membranes PVDF.
- Bloquer les membranes avec du lait écrémé à 5 % pendant 2 h à la RT et incuber avec les anticorps primaires correspondants (C1GALT1 [1:1000], Cosmc [1:2000]) pendant 24 h. Utiliser l’anticorps β-actine (1:100000) comme contrôle interne.
- Laver la membrane en fluorure de polyvinylidène (PVDF) avec 1x sérum physiologique tamponné Tris, détergent Tween 20 à 0,1 % (TBST) trois fois (10 min/temps), puis incuber avec l’anticorps IgG anti-lapin secondaire de chèvre correspondant (1:10000) à RT pendant 2 h.
- Lavez de nouveau la membrane avec du TBST (trois fois pendant 10 minutes chacune) et traitez-la avec une quantité appropriée de solution de travail à chimiluminescence améliorée (ECL) (selon les instructions du fabricant) pour la détection des bandes protéiques.
- Capturez les images à l’aide du système d’imagerie par chimiluminescence et effectuez une analyse semi-quantitative des valeurs de gris des protéines à l’aide du système d’analyse d’images Image J.
11. Aéroport internationalAnalyse statistique
- Utilisez un logiciel approprié pour analyser les données. Exprimez toutes les données comme moyennes ± écart-type (écart-type) et évaluez plusieurs échantillons à l’aide d’un test ANOVA à un facteur pour la comparaison entre les groupes.
REMARQUE : Le logiciel statistique SPSS 26.0 a été utilisé pour l’analyse statistique. La méthode LSD a été utilisée pour les comparaisons à deux facteurs entre les groupes lorsque les variances étaient égales, et la méthode Dunnett T3 a été utilisée pour les comparaisons à deux facteurs entre les groupes lorsque les variances n’étaient pas égales. P<0,05 a été considéré comme indiquant une différence statistiquement significative.
Résultats
Effet de la DIO sur le tissu rénal dans un modèle de souris IgAN
Par rapport au groupe témoin, le modèle de souris IgAN induites par l’immunité muqueuse (groupe modèle) a présenté une augmentation significative de la protéinurie (Figure supplémentaire 2), le dépôt d’IgA était visible dans la région mésangiale, la fluorescence était uniformément distribuée en grappes dans toute la région mésangiale (Figure 1A), la coloration PAS du tissu rénal a montré une prolifération de cellules mésangiales et une hyperplasie stromale (Figure 1B), qui a été réduite dans le groupe gavage DIO (groupe DIO).
Effet de la DIO sur les lymphocytes B dans le patch de Peyer
Le patch de Peyer est le principal site de conversion des lymphocytes B en cellules sécrétant des IgA. Nous avons pris le patch de Peyer comme objet de recherche pour observer l’effet de la DIO sur les lymphocytes B en détectant l’expression des marqueurs de cellules B CD20 et CXCR5. Les résultats immunohistochimiques ont montré que l’expression de CD20 et CXCR5 était significativement plus élevée dans le groupe modèle que dans le groupe témoin. La DIO pourrait inhiber l’expression des marqueurs moléculaires ci-dessus (Figure 2A,B).
La plage de concentration sûre de l’IDO sur les cellules DAKIKI
La LDH est un marqueur de l’intégrité de la membrane plasmique et un indicateur de la mort cellulaire, avec des taux de libération de LDH plus élevés indiquant des dommages cellulaires plus graves. Le test de libération de LDH a été utilisé pour déterminer la plage de concentration sûre de DIO. La concentration maximale sans danger de DIO a été déterminée par un taux de libération de LDH inférieur à 10 %. Les résultats (figure 3) n’ont montré aucune cytotoxicité significative induite par l’IOD à des concentrations de 0,25 à 1,0 μg/mL. Par conséquent, l’étude suivante a utilisé 0,25, 0,5 et 1,0 μg/mL d’IDO comme niveau de dosage.
Effets de la DIO sur la prolifération cellulaire DAKIKI
Les résultats expérimentaux (Figure 4) ont montré que, par rapport au groupe modèle (groupe stimulé par le LPS), DIO inhibait la prolifération des cellules DAKIKI induite par le LPS d’une manière dépendante de la concentration. L’IOD à des concentrations de 0,5 et 1,0 μg/mL a inhibé de manière significative la prolifération des cellules DAKIKI induite par le LPS (P < 0,01).
Effets de la DIO sur la fonction sécrétoire des cellules DAKIKI
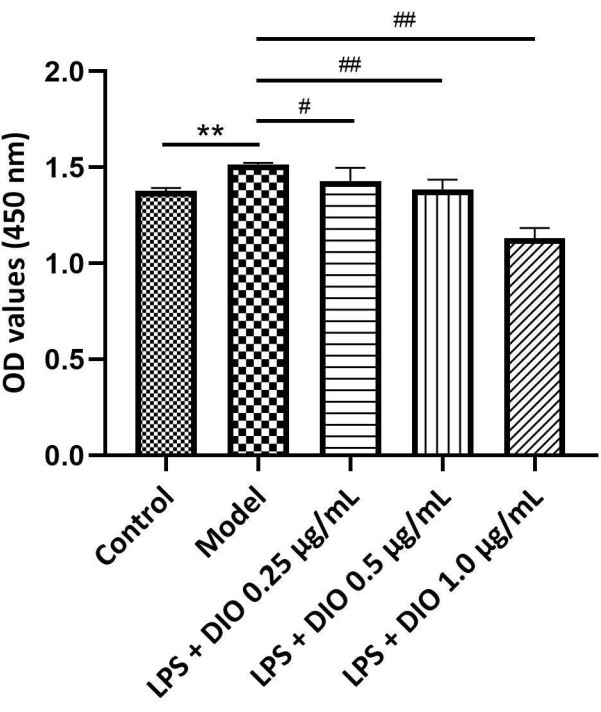
Les niveaux de Gd-IgA1 sont étroitement liés au processus pathologique des IgAN, et les IgA totales sont testées ensemble comme indicateur de la fonction sécrétoire cellulaire. Un test ELISA a été utilisé pour détecter le contenu en IgA et Gd-IgA1 dans le surnageant de la culture cellulaire DAKIKI. Les résultats ont montré (Figure 5A,B) que les cellules DAKIKI stimulées par le LPS sécrétaient plus d’IgA par rapport au groupe témoin (P < 0,01). En comparaison, DIO a inhibé de manière significative la sécrétion d’IgA par les cellules DAKIKI (P < 0,01) de manière dépendante de la concentration. Par rapport au groupe témoin, les cellules DAKIKI stimulées par le LPS ont sécrété plus de Gd-IgA1 avec une tendance statistique (P < 0,10), et DIO a inhibé la sécrétion de Gd-IgA1 à partir des cellules DAKIKI stimulées par le LPS de manière dépendante de la concentration (P < 0,05 et P < 0,01), parmi lesquelles DIO à 1,0 μg/mL a inhibé de manière significative la sécrétion de Gd-IgA1 avec le taux inhibé de 25%.
Le mécanisme de la DIO inhibe la sécrétion de Gd-IgA1 par les cellules DAKIKI
Pour étudier plus en détail le mécanisme possible de l’inhibition de la sécrétion excessive de Gd-IgA1 par les cellules DAKIKI, les niveaux d’ARNm de la C1GALT1 de la glycosylée transférase et de la protéine chaperonne Cosmc dans les cellules DAKIKI ont été détectés par qRT-PCR, et les résultats ont montré (Figure 6A,B) que l’expression relative de l’ARNm de C1GALT1 et de Cosmc était régulée à la baisse dans les cellules DAKIKI du groupe modèle par rapport au groupe témoin (P < 0,01). DIO a régulé à la hausse l’expression relative de l’ARNm de C1GALT1 et de Cosmc à des degrés différents par rapport au groupe modèle, avec DIO 1,0 μg / mL significativement régulé à la hausse l’expression relative de l’ARNm de C1GALT1 et Cosmc (P < 0,05).
Dans le même temps, la méthode WB a été utilisée pour détecter l’effet de DIO sur l’expression protéique de C1GALT1 et Cosmc dans les cellules DAKIKI. Par rapport au groupe témoin, l’expression protéique de C1GALT1 et de Cosmc dans les cellules DAKIKI du groupe modèle a diminué de manière évidente (P < 0,05). Par rapport au groupe modèle, l’expression protéique de C1GALT1 et de Cosmc après l’intervention DIO a été régulée à la hausse. L’expression protéique de C1GALT1 et de Cosmc a été significativement régulée à la hausse par DIO à une concentration de 1,0 μg/mL (P < 0,05) (figures 7A-C).
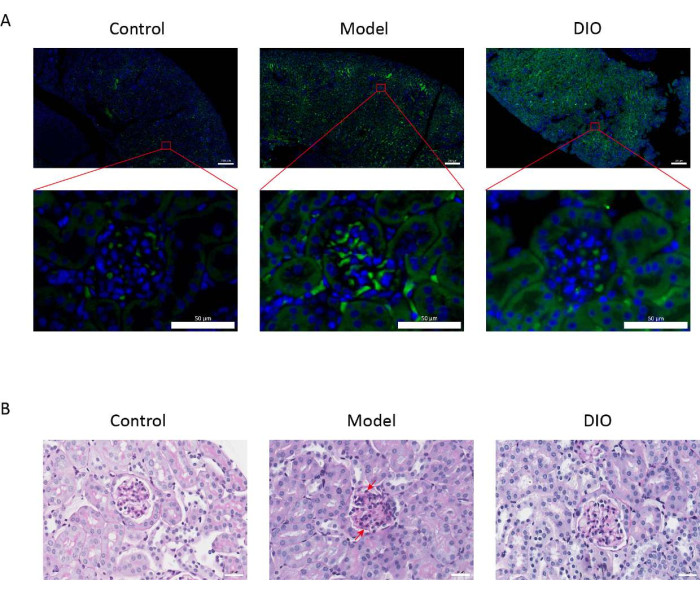
Figure 1 : Histopathologie des reins. (A) Microscope à immunofluorescence. Des coupes de reins de souris de chaque groupe ont été colorées avec des anti-IgA (vert) et du DAPI (bleu). La barre d’échelle d’image ci-dessus = 200 μm. La barre d’échelle de l’image ci-dessous = 50 μm. n = 6 par groupe. (B) Des images représentatives de la coloration PAS du tissu rénal chez les souris des groupes Contrôle, Modèle et DIO. Barre d’échelle = 30 μm. La flèche vers le bas montre les cellules mésangiales et la flèche vers le haut montre le stroma. Barre d’échelle = 30 μm. n = 6 par groupe. Veuillez cliquer ici pour voir une version agrandie de cette figure.
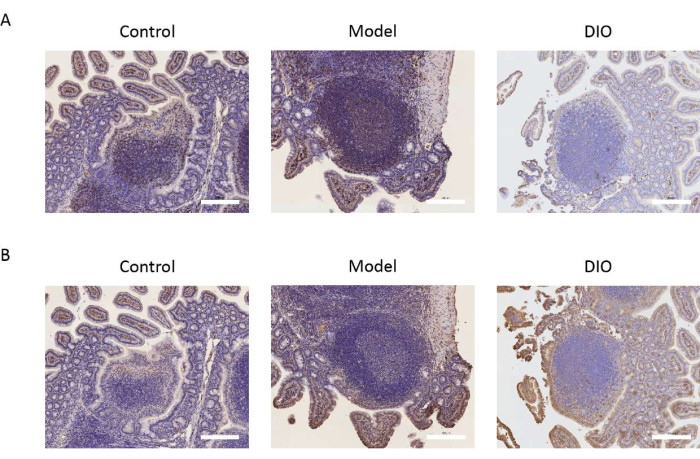
Figure 2 : Effet de la DIO sur les marqueurs des lymphocytes B. (A) L’expression de CD20 dans le patch de Peyer. Barre d’échelle = 200 μm. n = 6 par groupe. (B) L’expression de CXCR5 dans le patch de Peyer. Les barres d’échelle se trouvent dans le coin inférieur droit de l’image. Barre d’échelle = 200 μm. n = 6 par groupe. Veuillez cliquer ici pour voir une version agrandie de cette figure.
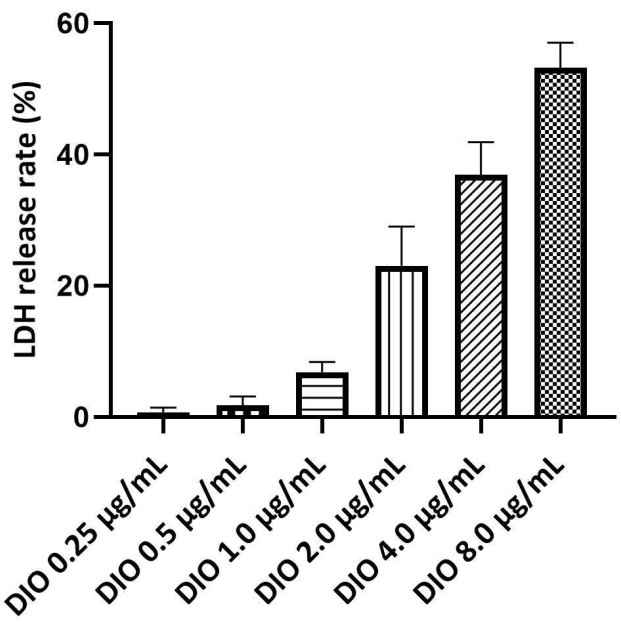
Graphique 3. Criblage de la concentration sûre de DIO sur les cellules DAKIKI. Les valeurs statistiques sont exprimées en moyenne ± ET à partir de trois expériences indépendantes. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Graphique 4. Différentes concentrations de DIO affectent la prolifération des cellules DAKIKI. Les données ont été exprimées en moyenne ±ET. Par rapport au groupe témoin, **P < 0,01 ; par rapport au groupe modèle, #P < 0,05' ##P < 0,01 ; Les résultats de toutes les expériences ont été répétés trois fois. Veuillez cliquer ici pour voir une version agrandie de cette figure.
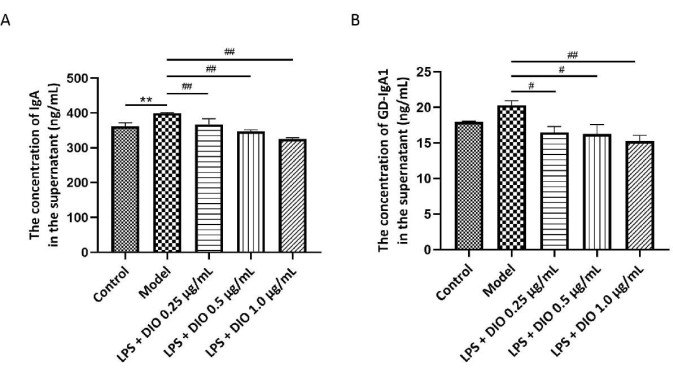
Graphique 5. DIO inhibe la sécrétion d’IgA et de Gd-IgA1 par les cellules DAKIKI. (A) La méthode ELISA a détecté l’expression des IgA dans chaque groupe. (B) La méthode ELISA a détecté l’expression de Gd-IgA1 dans chaque groupe. Les données ont été exprimées en moyenne ± écart-type. Par rapport au groupe témoin, **P < 0,01 ; par rapport au groupe modèle, #P < 0,05, ##P < 0,01 ; Tous les résultats expérimentaux ont été répétés trois fois. Veuillez cliquer ici pour voir une version agrandie de cette figure.
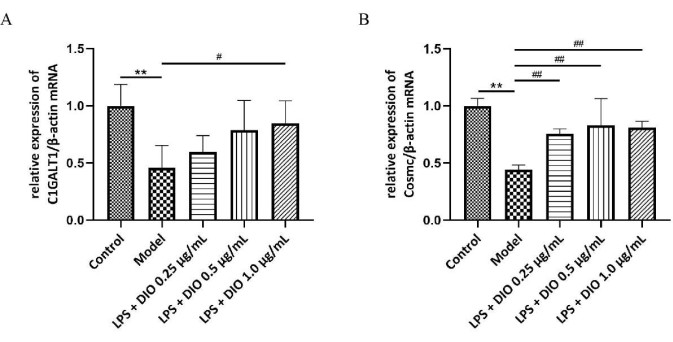
Graphique 6. Le mécanisme de DIO inhibe la sécrétion excessive de Gd-IgA1 par les cellules DAKIKI. (A) QRT-PCR a détecté l’expression de l’ARNm de C1GALT1. (B) QRT-PCR a détecté l’expression de l’ARNm de Cosmc. Les données ont été exprimées en moyenne ± écart-type. Par rapport au groupe témoin, **P<0,01 ; par rapport au groupe modèle, #P < 0,05, ##P < 0,01 ; Tous les résultats expérimentaux ont été répétés trois fois. Veuillez cliquer ici pour voir une version agrandie de cette figure.
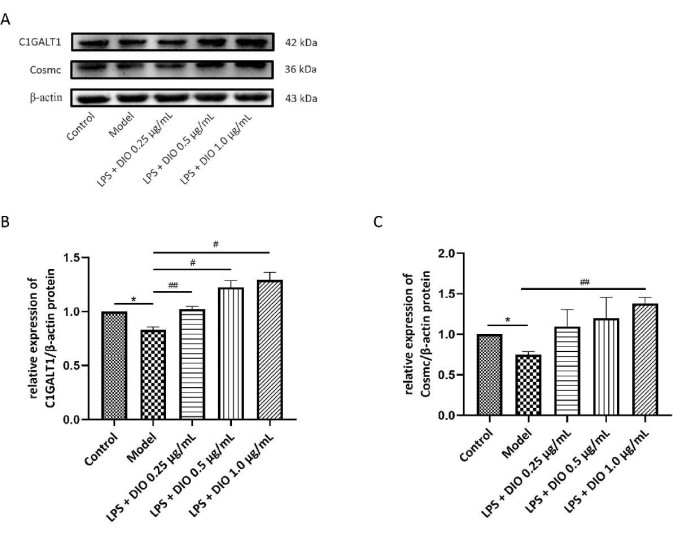
Graphique 7. DIO affecte l’expression protéique de C1GALT1 et Cosmc dans les cellules DAKIKI. (A) WB a vérifié la régulation à la hausse de l’expression protéique de C1GALT1 et Cosmc par DIO. (B) Une analyse semi-quantitative de l’expression de C1GALT1 a été réalisée à l’aide de l’image J. (C) Une analyse semi-quantitative de l’expression de Cosmc à l’aide de l’image J. Les données ont été exprimées en moyenne ± écart-type. Par rapport au groupe témoin*, P < 0,05 ; par rapport au groupe modèle, #P < 0,05, ##P < 0,01, tous les résultats expérimentaux ont été répétés trois fois. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Figure supplémentaire 1. Le schéma du modèle in vivo. Veuillez cliquer ici pour télécharger cette figure.
Figure supplémentaire 2. Modifications de la protéinurie. Les données ont été exprimées en moyenne ± écart-type ; n = 6 par groupe. Veuillez cliquer ici pour télécharger cette figure.
Discussion
La caractéristique pathologique des IgAN est le dépôt de complexes immuns contenant des IgA1 et GD-IgA1 dans la région mésangiale du glomérule21,22. La réduction de la formation de complexes immunitaires peut réduire les lésions rénales et atténuer les symptômes cliniques des IgAN. Dans une expérience in vivo, nous avons étudié les effets thérapeutiques de la DIO sur les IgAN, et nous avons constaté que la DIO peut réduire le dépôt d’IgA dans le rein de souris modèles d’IgAN. Il est démontré que l’accumulation de cellules sécrétant des IgA dans le rein est liée à la pathogenèse des IgAN23. En tant que site important de prolifération et d’activation des lymphocytes B, le patch de Peyer est une source importante de cellules sécrétant des IgA, nous avons donc examiné l’expression des marqueurs de lymphocytes B (CD20, CXCR5) dans le patch de Peyer et avons constaté que DIO pouvait inhiber l’expression des lymphocytes B dans le patch de Peyer du modèle de souris IgAN. Ces résultats expérimentaux pourraient servir de base à l’application de la DIO dans le traitement des IgAN.
Nous avons réalisé les expériences suivantes in vitro pour étudier davantage le mécanisme d’action de la DIO sur les IgAN. Tout d’abord, il a été démontré précédemment que DAKIKI, une lignée de lymphocytes B immortalisée par l’EBV qui sécrète de l’IgA1, dont une partie est GD-IgA124, est idéale pour la recherche in vitro du mécanisme d’action du médicament sur l’IgAN. Nous avons choisi des cellules DAKIKI pour étudier le mécanisme moléculaire de la DIO dans le traitement des IgAN. De plus, la réponse immunitaire inflammatoire de la muqueuse joue un rôle essentiel dans la pathogenèse des IgAN. Comme mentionné ci-dessus, nous utilisons le LPS pour stimuler les cellules DAKIKI, qui peuvent libérer des facteurs pro-inflammatoires et médier les réponses inflammatoires, ce qui peut mieux imiter le mécanisme des réponses immunitaires de la muqueuse dans les IgAN. Le modèle cellulaire in vitro peut aider à étudier la possibilité et le mécanisme d’autres médicaments pour traiter les IgAN. Les résultats ont montré que la DIO inhibait la prolifération des cellules DAKIKI stimulées par le LPS de manière dépendante de la concentration. DIO pourrait inhiber la sécrétion d’IgA et de Gd-IgA1 dans les cellules DAKIKI causée par la stimulation LPS et réguler à la hausse l’expression de l’ARNm et de la protéine C1GalT1 et de son chaperon Cosmc dans les cellules DAKIKI, suggérant que DIO pourrait réduire la sécrétion de Gd-IgA1 en régulant à la hausse l’expression de C1GALT1/Cosmc et ainsi inhiber l’activation excessive des cellules DAKIKI.
Les étapes clés doivent être notées au cours des procédures expérimentales. La concentration de Gd-IgA1 dans le surnageant cellulaire DAKIKI n’est pas dans la plage de détection du kit ELISA (1,56 ~ 100 ng/mL), et le surnageant collecté doit être centrifugé par un tube d’ultrafiltration pour obtenir le Gd-IgA1 concentré. Assurez-vous également que le volume de surnageant provenant de chaque groupe est le même et que le volume final de concentré obtenu après l’ultrafiltration est le même.
Dans cette étude, nous avons utilisé simultanément des méthodes in vitro et in vivo , qui peuvent se soutenir mutuellement dans les effets pharmacologiques et fournir un exemple pour l’étude des effets et de leurs mécanismes de la phytothérapie. Certaines choses pourraient être améliorées dans ce protocole. Tout d’abord, nous n’avons pas détecté de concentrations sanguines dans le groupe de gavage DIO des souris ; par conséquent, la concentration de DIO équivalente aux concentrations sanguines n’est pas utilisée dans les expériences in vitro . Deuxièmement, seul le monomère DIO, le composant actif de la DNR, a été étudié ; les effets d’autres composants de la DNR sur les IgAN doivent encore être étudiés plus avant.
En conclusion, cette étude fournit une base expérimentale pour le traitement des IgAN avec DIO, l’ingrédient actif de la DNR. Cette étude a permis d’établir un modèle cellulaire pathologique des IgAN en mimant la réponse immunitaire muqueuse des IgAN à la fois in vitro et in vivo. Il donne une nouvelle idée pour étudier la médecine traditionnelle chinoise pour prévenir et traiter les IgAN.
Déclarations de divulgation
Les auteurs déclarent qu’ils n’ont pas d’intérêts financiers concurrents.
Remerciements
Ce travail a été soutenu par la Fondation nationale des sciences naturelles de Chine (81973675).
matériels
| Name | Company | Catalog Number | Comments |
| Anti-CD20/MS4A1 Antibody | Boster Biotechnology Company | A03780-3 | |
| Antifade mounting medium | Beyotime, Shanghai, China | P0128S | |
| Balb/c mice | Beijing Weitong Lihua Laboratory Animal Technology Co., Ltd. | 110322220101424000 | |
| blocking serum | Solarbio, Beijing, China | SL038 | |
| Bovine gamma globulin | ShangHai YuanYe Biotechnology Company | S12031 | |
| C1GALT1 polyclonal antibody | Proteintech Group, Inc,USA | 27569-1-AP | |
| Citrate antigen retrieval solution(50×) | Phygene Biotechnology Company | PH0422 | |
| COSMC polyclonal antibody | Proteintech Group, Inc,USA | 19254-1-AP | |
| Cytotoxiciy detection kit | Roche Company | 4744926001 | |
| Dako REAL EnVision detection system, Peroxidase/DAB+ | Dako | K5007 | |
| DAPI | Invitrogen | D1306 | |
| Dioscin | National Institute For Food and Drug Control | 111707-201703 | |
| DIO tablets | Chengdu No 1 Pharmaceutical Co. Ltd. | H51023866 | |
| ECL working solution | Merck Biotechnology, Inc | WBKLS0100 | |
| Enhanced cell counting kit-8 | Beyotime, Shanghai, China | C0043 | |
| Fasking one-step removal of gene cDNA first-strand synthesis premix | TIANGEN,Beijing, China | KR118-02 | |
| Glycogen Periodic acid Schiff (PAS) stain kit | BaSO Biotechnology Company | BA4080A | |
| Goat anti-mouse IgA-AF488 | SouthernBiotech | 1040-30 | |
| Goat anti-rabbit IgG antibody (H+L), HRP conjugated | BeiJing Bioss Biotechnology Company | BS-0295G-HRP | |
| Human Gd-IgA1 ELISA kit | IBL | 27600 | |
| Human IgA ELISA kit | MultiSciences (LiankeBio) | 70-EK174-96 | |
| Pierce BCA protein assay kit | Thermo Scientific | 23227 | |
| PMSF solution | Beyotime, Shanghai, China | ST507 | |
| Proteinase K | Phygene Biotechnology Company | PH1521 | |
| Rabbit anti-CXCR5 polyclonal antibody | BeiJing Bioss Biotechnology Company | bs-23570R | |
| RIPA lysis buffer | Beyotime, Shanghai, China | P0013B | |
| RNAsimple total RNA extraction kit | TIANGEN,Beijing, China | DP419 | |
| RPMI Medium 1640 | Solarbio, Beijing, China | 31800 | |
| Super-Bradford protein assay kit | CWBIO, Beijing, China | CW0013 | |
| Triton X-100 | Beyotime, Shanghai, China | ST795 | |
| β-Actin Rabbit mAb | Abclonal, Wuhan, China | AC026 |
Références
- Knoppova, B., et al. The origin and activities of IgA1-containing immune complexes in IgA nephropathy. Frontiers in Immunology. 7, 117 (2016).
- Suzuki, H., et al. The pathophysiology of IgA nephropathy. Journal of The American Society of Nephrology. 22 (10), 1795-1803 (2011).
- He, L., et al. Synthetic double-stranded RNA poly(I:C) aggravates IgA nephropathy by triggering IgA class switching recombination through the TLR3-BAFF axis. American Journal of Nephrology. 42 (3), 185-197 (2015).
- Zhao, N., et al. The level of galactose-deficient IgA1 in the sera of patients with IgA nephropathy is associated with disease progression. Kidney International. 82 (7), 790-796 (2012).
- Xing, Y., et al. C1GALT1 expression is associated with galactosylation of IgA1 in peripheral B lymphocyte in immunoglobulin a nephropathy. BMC Nephrology. 21 (1), 18 (2020).
- Qin, W., et al. External suppression causes the low expression of the Cosmc gene in IgA nephropathy. Nephrology Dialysis Transplantation. 23 (5), 1608-1614 (2008).
- Sakai, F., et al. Lactobacillus gasseri SBT2055 induces TGF-β expression in dendritic cells and activates TLR2 signal to produce IgA in the small intestine. PLoS One. 9 (8), 105370 (2014).
- Gutzeit, C., Magri, G., Cerutti, A. Intestinal IgA production and its role in host-microbe interaction. Immunological Reviews. 260 (1), 76-85 (2014).
- Serino, G., et al. In a retrospective international study, circulating miR-148b and let-7b were found to be serum markers for detecting primary IgA nephropathy. Kidney International. 89 (3), 683-692 (2016).
- Lu, F., et al. Therapeutic effect of Rhizoma Dioscoreae Nipponicae on gouty arthritis based on the SDF-1/CXCR 4 and p38 MAPK pathway: an in vivo and in vitro study. Phytotherapy research: PTR. 28 (2), 280-288 (2014).
- Wang, W., Xu, L., Zhou, L., Wan, S., Jiang, L. A Network pharmacology approach to reveal the underlying mechanisms of Rhizoma Dioscoreae Nipponicae in the treatment of asthma. Evidence-Based Complementary and Alternative Medicine: eCAM. 2022, 4749613 (2022).
- Tian, W. W., Wei, Y. Professor TONG Xiaolin used the experience of Dioscoreae Nipponicae. Jilin Journal of Chinese Medicine. 40 (05), 589-592 (2020).
- Rao, X. R., Bai, Y. W. Das Xiwen's experience in treating IgA nephropathy. Beijing Journal of Traditional Chinese Medicine. 9, 691-693 (2008).
- Si, Y., Zhang, Y. A data mining study on the pattern of medication use in the treatment of IgA nephropathy by Professor Zhang Yu. Journal of Chinese Physician. 20 (01), 109-111 (2018).
- Jiang, H., et al. Optimization of the enzymatic extraction technology of Diosgenin from Dioscorea nipponica. Chinese Traditional Patent Medicine. 39 (03), 621-624 (2017).
- Qi, M., et al. Dioscin alleviates lipopolysaccharide-induced inflammatory kidney injury via the microRNA let-7i/TLR4/MyD88 signaling pathway. Pharmacological Research. 111, 509-522 (2016).
- Yang, L., et al. Recent advances in the pharmacological activities of Dioscin. BioMed Research International. 2019, 5763602 (2019).
- Nal Zou, J., et al. Toll-like receptor 4 signaling pathway in the protective effect of Pioglitazone on experimental immunoglobulin A nephropathy. Chinese Medical Journal. 130 (8), 906-913 (2017).
- Xu, S. Y., Bian, R. L., Chen, X. Pharmacological experiments methodology. Chinese Pharmacological Bulletin. 1, 19 (1992).
- Shen, J. C., Ren, Y., Rao, X. R., You, Y., Li, S. Network pharmacology, molecular docking, and in vitro experiments to explore the molecular mechanism of Dioscorea Nipponica Makion in the treatment of IgA nephropathy. World Journal of Integrated Traditional and Western Medicine. 16 (12), 2246-2254 (2021).
- Mestecky, J., et al. IgA nephropathy: molecular mechanisms of the disease. Annual Review of Pathology. 8, 217-240 (2013).
- Novak, J., et al. IgA1-containing immune complexes in IgA nephropathy differentially affect proliferation of mesangial cells. Kidney International. 67 (2), 504-513 (2005).
- Nihei, Y., et al. Identification of IgA autoantibodies targeting mesangial cells redefines the pathogenesis of IgA nephropathy. Science Advances. 9 (12), (2023).
- Raska, M., et al. Identification and characterization of CMP-NeuAc: GalNAc-IgA1 alpha2,6-sialyltransferase in IgA1-producing cells. Journal of Molecular Biology. 369 (1), 69-78 (2007).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon