Method Article
형광 기반의 뉴 라미니다 아제 억제 분석은 항 바이러스제의 뉴 라미니다 아제 억제제 클래스에 인플루엔자 바이러스의 감수성을 평가하기 위해
요약
우리는 항 바이러스의 뉴 라미니다 제 억제제 클래스 인플루엔자 A 및 B 바이러스의 감수성을 평가하는 표현형 형광 계 뉴 라미 억제 분석의 사용을 설명한다.
초록
뉴 라미니다 (NA) 억제제는 현재 순환 계통에 대한 효과적인 인플루엔자의 치료 및 예방을 위해 승인 된 항 바이러스제의 유일한 클래스입니다. 계절 인플루엔자 치료에의 사용뿐만 아니라, NA 억제제는 세계적 유행병의 경우에 사용하는 국가들에 의해 비축되었다. 항 바이러스제의이 클래스에 인플루엔자 바이러스 순환의 감수성을 모니터링하는 것이 중요하다. 거기 NA 억제제 인플루엔자 바이러스의 민감성을 평가하기 위해 사용될 수있는 분석의 종류가 있지만, 형광 기판 또는 화학 발광 기질을 사용하여 효소 저해 분석은 가장 널리 사용하고 권장된다. 이 프로토콜은 NA 억제제에 인플루엔자 바이러스 감수성을 평가하는 형광 기반 분석의 사용을 설명한다. MUNANA ((4- Methylumbelliferyl) -α-D- N -acetylneuraminic 산 - 상기 분석은 2 '절단 개구 효소에 기초) 형광 생성물 4- 메틸 움 (4-MU)를 해제 기판. 따라서, 인플루엔자 바이러스 NA NA에 대한 억제제의 억제 효과는 IC 50 값으로 주어진 NA 활성의 50 % 감소하는 데 필요한 NA 억제제의 농도에 따라 결정된다.
서문
헤 마글 루티 닌 (HA)과 뉴 라미니다 제 (NA)는 인플루엔자 A 및 B 바이러스의 두 가지 주요 표면 당 단백질이다. 개구가 세포 표면에 1 갈락토스로부터 시알 산을 절단하여 바이러스를 방출하면서 HA는 세포 표면 당 단백질이나 당지질의 시알 산 - 갈락토스 결합한다. NA 억제제는 합리적하여 바이러스 자손의 방출 및 확산을 방지 NA의 효소 활성 부위에 단단하게 결합하도록 설계되었습니다 인플루엔자 항 바이러스제의 클래스입니다. 오셀 타미 비르와 자 나미 비르는 치료 및 인플루엔자의 예방을 위해 전 세계적으로 많은 국가에서 승인 된 두 NA 억제제이다. 최근 몇 년 동안, 두 개의 추가 NA 억제제, peramivir 및 laninamivir은 제한된 수의 국가에서 사용이 승인되었다. NA 억제제 감수성 및 내성을 부여하는 돌연변이의 식별을 위해 인플루엔자 바이러스의 스크리닝과 결정 effectiv 모니터링에 중요항 바이러스제의이 클래스의 eness.
16 강 년, 형광 기반 NA 억제 분석은 인플루엔자 바이러스 순환 중 바이러스 감수성의 변화 경향을 모니터링 인플루엔자 멜버른 (멜버른 WHOCCRRI)의 참조 및 연구 협력 센터 WHO에서 정기적으로 수행되었다. 매년 2,000 개 이상의 인플루엔자 바이러스는 항 바이러스 감수성 검사를하고 있습니다. 2007-2008 북반구 독감 시즌 동안, 전 계절 A (H1N1) 바이러스의 수가 급증이 있었지만 대부분의 인플루엔자 시즌에서 바이러스> 98 %는 네 NA 억제제 2, 3, 4에 취약 그 오셀 타미 비르 (5)에 감수성을 감소했다. 2008 년 말에 의해 세계의 나머지 확산 NA 아미노산 치환의 H275Y 포함 된 바이러스의이 그룹,,, 오셀 타미 비르의 inappropri을이 바이러스의 치료를 위해 전 세계적으로 먹었다. 현재 인플루엔자 B, 인플루엔자 A (H3N2) 및 인플루엔자 A 순환 대다수 (H1N1) pdm09 균주 오셀에 취약, 비록 오셀 감소 부여 개구 아미노산 치환 H275Y 함유 A (H1N1) pdm09 변형 커뮤니티 클러스터 및 peramivir 감수성, 세계 6, 7의 여러 부분에서보고되었다.
때문에 충분히 높은 바이러스 역가의 필요성, (동물 비강 세척 포함) 임상 검체 중 하나를 세포 배양에서 계대 또는 바이러스 감수성 검사 이전에 계란을 발육해야합니다. 이 문서에서 설명하는 NA 억제 분석은 세 부분으로 나눌 수있다 :
특정 형광의 형광 생성물 4- 메틸 움 (4-MU)에 대한 선형 범위를 결정
때문에 fluorometers 사이의 고유 한 차이, t그 형광 최종 생성물 4-MU 및 상대적인 형광 단위 (RFU) 선형 범위를 확립 할 필요가있다. 4-MU 용 선형 범위가 설정되면, 최적의 목표 신호는 인플루엔자 바이러스의 농도가 NA 활성 분석에서 조정되는 선택된다. 특정 형광 완료되면이 반복 할 필요가 없습니다.
바이러스의 NA 활동을 결정
바이러스 순차적 희석 (4-Methylumbelliferyl) -α-D- N -acetylneuraminic 산 (MUNANA) 기판 - 개구 활성 분석은 (2 ')의 추가를 포함하는 간단한 분석이다. 개구 의해 MUNANA의 분해에서 생성 된 형광 최종 생성물 4-MU의 양은 형광 분석기를 사용하여 측정된다. 개구 억제 분석에 사용할 수있는 적절한 바이러스는 바이러스 희석 희석 대해 형광 단위를 플로팅하여 선택된다. 생성 된 S 자형 곡선에서 선형 부분의 중간 지점에 대응한다형광 분석기의 4-MU 선형 범위 제 1 항에서 결정 부 (3)에 사용되는 바이러스의 적정 농도를 알릴 것이다.
개구 억제 분석을 이용하여 NA 억제제 평가 바이러스 감수성
특정 NA 억제제로 바이러스의 민감성을 평가하기 위해, (2)에서 판정 된 희석 바이러스 NA 억제제 농도의 범위와 함께 배양된다. MUNANA와 후속 배양 후, 억제되지 않은 바이러스에 의해 생성 된 4-MU는 형광 RFU 의해 측정된다. 바이러스의 NA 효소 활성의 NA 억제제의 억제 효과는 IC 50 값으로 주어진 NA 활성의 50 % 감소하는 데 필요한 NA 억제제 농도에 따라 계산된다.
프로토콜
1. 결정 형광 분석기에 형광 제품 4-MU의 선형 범위
- 무수 에탄올 5 mL에 4- MU 11.3 mg을 용해시켜 6.4 mM의 4-MU 스톡 용액 10 ㎖를 준비한다. (V / W) 원액 10 mL로 0.9 % 염화나트륨 5 mL를 추가합니다. 9 ㎖의 1X의 분석 완충액 (33.3 mM의 2- (N- 모르 폴리 노) 에탄 술폰산 (MES) 및 4 mM의 CaCl2를, pH가 6.5)에 6.4 mM의 4-MU 1 mL로 희석 한 용액을 작업 640 μM을 준비한다.
주 : MES 13 g 및 증류수 8㎖를 1 M 염화칼슘 2 992 ㎖를 첨가하여 2 배의 분석 완충액을 준비한다. M의 NaOH (10)를 사용하여 6.5로 pH를 조정한다. 기공 크기 0.2 ㎛의 멸균 된 셀룰로오스 아세테이트 필터를 사용하여 상기 버퍼 필터. 주의! 수산화 나트륨 가성이며, 피부와 눈에 화학적 화상을 입을 수 있습니다. 그 전체 개인 보호 장비를 착용 있는지 확인하십시오. - MU-4 농도 (즉, 5 μM, 10 μM, 20 μM, 40 μM, 80 μM, 160 #의 범위 5 ㎖를 준비181; M, 및 1X 검정 완충액을 사용하여 640 μM 4-MU의 2 배 일련 희석액 내지 320 μM).
- 4-MU (즉, 5 μM, 10 μM, 20 μM, 40 μM, 80 μM, 160 μM, 320 μM 및 640 μM) 맑고로 (희석 당 두 개의 웰), 96의 각각의 일련 희석액 50 μL 분주 웰 평면 바닥 플레이트 (바탕 신호를 측정하는 역할을 공백) 나머지 웰에 1X 검정 완충액 50 μL.
주 : 반응 부피 4-MU의 최종 농도 (50 μL 4-MU + 50 μL 300 μM의 MUNANA)가 160 μM, 320 μM 2.5 μM, 5 μM, 10 μM, 20 μM, 40 μM, 80 μM이다 . - 증류수 20㎖에 MUNANA 25 mg의 재구성하여 MUNANA 2.5mM의 원액을 준비한다. 300 μM의 MUNANA 작업 용액 (한 접시에 충분한 양)을 얻었다 5.28 ㎖의 1X 검정 완충액 중 2.5 맹 무나나 0.72 mL를 섞는다. 300 μM의 MUNANA의 일하는를 포함하는 튜브를 커버즉시 사용하지 않는 g의 알루미늄 호일로 용액을 얼음에 보관. 남은 재료를 폐기하십시오.
참고 : 2.5 밀리미터 MUNANA 주식 솔루션 1 달 동안 -20 ° C에서 저장 될 수있는 한 동결 / 해동 사이클 내에서 사용되어야합니다. 4-MU와 MUNANA 솔루션은 광 감응성과 장시간 노광으로부터 보호되어야한다. - 부드럽게 섞어 탭 각 웰에 300 μM의 MUNANA의 50 μL를 추가하고, 30 분 동안 37 ℃에서 배양한다. 증발을 방지하기 위해 판 실러와 함께 접시를 커버.
주의 :이 단계는 NA 억제 분석에서의 형광 배경을 설명한다. - 0.824 M의 NaOH 2.225 ㎖ (하나의 판에 충분한 양)을 무수 에탄올 11 mL를 혼합하여 정지 용액을 준비한다.
- 반응을 중지하고 부드럽게 섞어 활용할 각 웰에 스톱 솔루션의 100 μL를 추가합니다.
- PE로서, 여기 파장 355 ㎚, 설정의 460 nm의 발광 파장을 갖는 형광 설정을 사용하여 플레이트를 판독제조업체의 지침을 r에.
- 어떠한 4-MU를 포함하지 않는 모든 웰에서 형광 신호를 사용하여, 평균 배경 신호를 계산한다. MU-4를 함유하는 각각의 웰로부터 배경이 평균 신호를 뺀 각 MU-4 농도의 평균 신호 (RFU)를 계산한다. 도 1a에 도시 된 바와 같이, MU-4 농도 (μM)의 RFU에 대하여 표준 곡선을 플롯; 곡선의 근접 선형 부분은도 1b에 도시된다.
- 선형 범위 및 최적 목표 신호를 결정하기 위해 MU-4 농도 (μM) 대 RFU의 플롯을 시각화; 선형 범위는 어디 플롯 4-MU의 농도 증가에 비례하여 형광 신호가 증가함에 따라, 최적의 목표 신호는 선형 범위 내의 임의의 4-MU 농도된다.
주 : 선형 범위 및 최적의 목표 신호는 형광 특정한다. 예를 들어, 멜버른 WHOCCRRI에서 형광은 2의 선형 범위를 갖는다0.5-40 μM 4-MU와 1,500 ~ RFU에 대응 ~ 30 μM 4-MU의 최적 목표 신호.
2. 바이러스의 NA 활동 결정
참고 : 인플루엔자 바이러스는 Madin-다비 개 신장 (MDCK) 세포 또는 발육 계란 8에서 충분한 역가을 배양한다.
- 0.1 %를 함유하는 컬럼에 희석 한 배양 된 인플루엔자 바이러스의 웰 당 120 μL 및 1X 검정 완충액 60 μL 분주 NP-40, 96 웰, U-바닥 판 (11)의 남은 열로.
- 직렬로 플레이트를 통해 바이러스의 두 배 희석을 수행하는 (즉, 2 열의 컬럼 1 내지 60 μL를 전송하는 등, 열 (11)까지) 만 1X 검정 완충액을 함유하는 블랭크로서 컬럼 (12)을두고, 멀티 채널 피펫을 사용.
- 맑은 96 웰 편평 바닥 플레이트에 웰 (희석 바이러스 블랭크)로부터 각각 50 μL를 옮긴다.
참고 : C에 필요하지 않습니다물질은 제 1 열로 통해 컬럼 (12)로부터 전송되는 경우 hange 피펫 팁. - 웰 당 (단계 1.4에 따라 제조 됨) 300 μM MUNANA 50 μL를 첨가하고 부드럽게 혼합 할 수있는 플레이트를 탭. 1 시간 동안 37 ℃에서 플레이트를 인큐베이션. 증발을 방지하기 위해 판 실러와 함께 접시를 커버.
- 반응을 종결하고 부드럽게 혼합 판은 탭하여 웰 당 (단계 1.6에 따라 제조 됨)을 정지 용액 100 μL를 추가한다.
- 형광 분석기를 사용하여 판을 읽어보십시오.
- 여기 파장 355 ㎚, 설정의 460 nm의 발광 파장 설정을 사용한다.
- 컬럼 (12)에서의 형광 판독 값에 기초하여, 평균 배경 신호를 결정하고, 각 웰의 평균 배경 신호를 감산. 바이러스 희석에 대한 RFU의 그래프를 그린다.
주 : WHOCCRRI 멜버른 100 μM의 MUNANA의 배경 값은 50과 120 사이 RFU 일반적이지만, 이들은 형광의 BEI 따라 다르고NG 사용. - 각 바이러스 (그림 2)에 대한 곡선의 선형 부분의 중간 지점을 결정하는 바이러스 희석에 대한 RFU의 줄거리를 볼 수 있습니다. 기준점으로서 (1 단계에서 결정됨) 최적 목표 신호를 사용한다.
주 :이 제 1 항에서 결정된 형광의 4-MU 선형 범위와 일치해야 바이러스의 적정 농도는 (3)에서 사용되는 제공한다.
3. NA 억제 분석을 사용하여 NA 억제제에 바이러스 감수성을 평가
- 300 μM의 농도 NA 억제제의 마스터 재고를 준비한다.
- 2 × 50 ㎖의 분석 완충액 (66.6 mM의 MES의 8 mM의 CaCl2를, pH가 6.5) 나미 비르 5.0 ㎎을 용해시켜 300 μM 나미 비르 (분자량 MW = 332.32 g / 몰)을 준비한다.
- 배 검정 완충액 50ml에 5.8 ㎎을 용해 (MW = 386.44 g / 몰 D 타르트 레이트) 300 μM 오셀 카르복시산을 준비한다.
- 준비300 μM peramivir 삼수화물 (MW = 382.45 g / mol)의 2 배 검정 완충액 50 ml에 5.7 mg의 용해.
- 배 검정 완충액 50ml에 5.2 mg을 용해시켜 300 μM laninamivir (MW = 346.34 g / 몰)을 준비한다.
주 : NA 억제제 마스터 주식 12 개월 동안 -20 ℃에서 저장 될 수있다. 정확한 무게와 볼륨 재구성에 사용되는 보장하기 위해 NA 억제제의 MW를 확인합니다. 오셀 카르복시산은 전구 약물 오셀 타미 비르 포스페이트의 활성 화합물이다. 따라서, 단지 오셀 카르복시산은 NA 억제 분석에 사용한다.
- 마스터 주식에서 0.03 nM 내지 0.3 nM의 3 nM 내지 30 nM 내지 300 nM 내지 3,000 nM의 농도에서 50 mL의 원심 분리 튜브 내의 NA 억제제의 10 배 희석액의 주식을 작동 준비하고 배 분석 30,000 nM 내지 버퍼 (66.6 mM의 MES의 8 mM의 CaCl2를, pH가 6.5); 이 여러 분석에서 사용할 수 있습니다.
비고 : 반응에 있습니다 volum NA 억제제의 최종 농도E (바이러스 희석액 300 μM의 MUNANA의 + 50 μL NA의 억제제 + 50 μL의 50 μL)을 각각 0.01 nM 내지 0.1 nM 내지 1 nM 내지 10 nM 내지 100 nM 내지 1,000 nM의, 및 10000 나노 미터이다. 최종 농도는 스톱 솔루션의 100 μL를 포함하지 않습니다. 2-8 ° C에서 모든 NA 억제제의 희석을 저장합니다. 유통 기한은 마스터 주식과 동일합니다. - 96 딥 - 웰 블록, 0.1 % NP-40 계면 활성제를 함유하는 1X 검정 완충액에 희석 바이러스를 준비한다. 네 NA 억제제 테스트 바이러스 당 2ml의 총 부피를 사용하여 섹션 (2)로부터 유도되는 NA 활성 분석 결과에 기초하여 바이러스를 희석하여 사용한다.
참고 : 96 깊은 우물 블록에 바이러스 당 두 개의 우물 (물론 당 1 mL로) 준비합니다. VIRUS 1, 2 및 3에 대한 바이러스 희석액의 예는 표 1에 나타내었다. - 8 깊은 웰에 저장한다 (단계 3.2에 따라 제조 됨) NA 억제제의 필요한 양을 분배. 여기에서, 레인 징 희석액 50 μL NA 저해제 분배이 0 ㎚ (2 × 시험 B로부터uffer 만) 맑은 96 웰 편평 바닥 플레이트에서 H로 행 A의 nM 내지 30,000이다.
주 : 플레이트 레이아웃이도 3에 도시되어있다. - 부드럽게 혼합하고 45 분 동안 실온에서 배양 접시를 탭에만 열 (12)에 열 1-11 및 1X 검정 완충액의 웰 당 50 μL로 희석하여 웰 당 시험 바이러스의 50 μL를 추가한다. 증발을 방지하기 위해 판 실러와 함께 접시를 커버.
- 웰 당 (단계 1.4에 따라 제조 됨) 300 μM MUNANA 50 μL를 첨가하고 부드럽게 혼합 할 수있는 플레이트를 탭. 1 시간 동안 37 ℃에서 플레이트를 인큐베이션. 증발을 방지하기 위해 판 실러와 함께 접시를 커버.
- 믹싱 플레이트를 부드럽게 눌러 웰 각각 (단계 1.6에 따라 제조 됨)을 정지 용액 100 μL를 추가한다.
- 형광 분석기를 사용하여 판을 읽어보십시오.
- 전술 한 바와 같이, 여기 파장 355 ㎚, 460 나노 미터의 방출 파장을 사용한다.
4. 계산IC 50 값
주 : JASPR 1.2가 IC (50) 값의 계산을 가능 곡선 피팅 소프트웨어이다. 소프트웨어는 CDC, 애틀랜타, 미국에서 인플루엔자 부문에 의해 개발되었다. 소프트웨어는 방정식을 활용 : V = V 맥스 × (1 - ([I]는 [I]는)) / (K i가 +), V 최대 대사의 최대 레이트이다은 [I]을, V는 억제제의 농도이다 반응이 억제되고, 및 K의 난 억제 곡선에 대한 IC (50)이다.
- 복사 및 12 열 플레이트 포맷 (96 웰)에 스프레드 시트로 형광에 의해 출력 된 원시 데이터를 붙여, 전지 A1부터 시작.
참고 : 각 후속 판에서 원시 데이터는 하나의 빈 행에 의해 비틀 거렸다해야합니다. 각각의 바이러스는 네 NA 억제제에 대해 테스트 된 경우 (각 판 사이의 빈 행으로) 네 세트의 원시 데이터를 붙여. - 피팅 소프트웨어 및 CL을 엽니 다'실험'탭에서 ICK. "대안이 약물 불소 (11) 샘플 '을 선택합니다.
- "옵션"탭을 클릭하고 체크 "그래프를 생성합니다."
- "옵션"을 다시 클릭하고 "새 키"탭을 클릭합니다. 원시 데이터 스프레드 시트 파일과 같은 폴더에있는 "inhibition_key".csv 파일을 저장합니다.
- inhibition_key 파일에서 ID 아래의 모든 샘플 이름을 나열합니다. 각 샘플의 이름은 고유해야합니다.
- 네 NA 억제제 테스트 한 경우, 오셀 타미 비르 다음 두 행의 추가 공간을 삽입하여 "Peramivir"에서 입력 "을 Laninamivir." inhibition_key 파일에 변경 사항을 저장합니다.
- 은 "jaspr의 V 1.2 - 억제 곡선 피팅"창으로 돌아가서으로 "실험 파일"과 inhibition_key와 같은 원시 데이터 파일 선택 "키 파일을." 분석을 실행합니다. .CSV과 PDF 파일 (* .pdf)의 결과를 저장합니다.
주 : 소프트웨어가 자동으로 억제 곡선을 그릴 것이다 (RFU 전압 강하NST NA 억제제 농도),도 4에 도시 된 바와 같이. 프로그램은 또한 개별 NA 억제제 (도 4)에 대해 각각의 바이러스에 대한 IC 50 값을 계산한다. 또한 JASPR의 IC 50 값은 스프레드 시트 형식의 신호 대 배경 (S / B)의 비율을 나타낸다. 배경 값은 사용 된 형광에 따라 실험실 실험실에서 다를 수있다. 멜버른 WHOCCRRI에서, 배경은 50 내지 120 RFU 100 μM의 범위 MUNANA 값. 10 미만의 비율은 특히 매우 낮은 NA의 활성을 갖는 돌연변이 바이러스가 여전히 허용되지만 신뢰성 IC 50 값, ≥10의 S / B의 비율이 바람직하다. - 이 IC 50 값은 소프트웨어에 의해 생성 된 곡선 형상을 검사한다. 모든 데이터 포인트에 떨어지거나 곡선에 근접한다 그렇지 않은 경우 NA 억제 분석을 반복합니다.
참고 : 비정상적으로 높은 IC (50) 값을 표시 바이러스의 경우, 분석은 반복해야한다에드는 결과를 확인합니다.
결과
인플루엔자 바이러스 감수성 9의 감시에 WHO 워킹 그룹에서 표준화 된보고 지침을 사용하여, NA 억제제에 인플루엔자 바이러스의 감수성이 용어 정상 억제 (NI), 감소 억제 (RI), 매우 감소 억제를 사용하여보고 (HRI) . NI 바이러스는 50의 값으로 10 배 이상의 인플루엔자 바이러스 (또는 인플루엔자 B 바이러스 5 배 이하)에 대한 IC (50) 중간의 기준과 비교하여 그와 IC이다. RI 바이러스 10 및 인플루엔자 A 바이러스 (또는 5- 인플루엔자 B, 50 배)에 대한 IC 50 중앙값 기준 상술 100 배 사이의 IC50 값을 갖는 것들이다. HRI 바이러스는 100 배 50 개의 값 A 형 인플루엔자 바이러스 (또는 인플루엔자 B 바이러스는 50 배 이상) IC 50 중앙값 기준으로 상기 IC를 그이고; 표 2 참조.
IC 중앙값 기준 A (H1N1) pdm09, A (H3N2) 및 B 야마가타 / B 빅토리아 바이러스 50 개 값의 IC 50 값의 작은 변화를 반영하기 위해 계산 멜버른 WHOCCRRI에서 매년 업데이트 개구 억제제 인플루엔자 균주를 순환 (표 3). 인플루엔자 A (H1N1)의 중앙값이 IC 50 값 pdm09 바이러스는 네 NA 억제제 걸쳐 거의 동일하지만, 중간 나미 비르와 laninamivir IC는 A (H3N2) 바이러스 50 개 값 오셀에 비해 높은 4 배 2-에 있고 peramivir IC 50 개 값 (표 3). 인플루엔자 B 바이러스에 대한 중앙값 오셀 IC 50 값은 일반적으로 5 행 나미 비르, peramivir 및 laninamivir IC 50 값 (표 3)보다 10 배이다.
개구 억제 분석은 유전자 associ 변경에 대한 정보를 제공하지 않는 표현형 분석이다RI 또는 HRI와 ated에. 따라서 유전자 분석은 RI 또는 HRI와 바이러스의 식별 다음을 수행하는 것이 중요합니다. 멜버른 WHOCCRRI에서 변형의 NA 유전자는 생거 시퀀싱 및 파이로 시퀀싱을 이용하여 분석한다. RI 및 HRI 변종 바이러스의 NA 유전자에서 발견 될 수있는 아미노산 치환의 대표적인 목록은 표 4에 제시되어있다. NAI의 감수성을 변경할 수 있습니다 아미노산 치환의보다 자세한 목록은 또한 WHO 웹 사이트 (10)에서 사용할 수 있습니다.
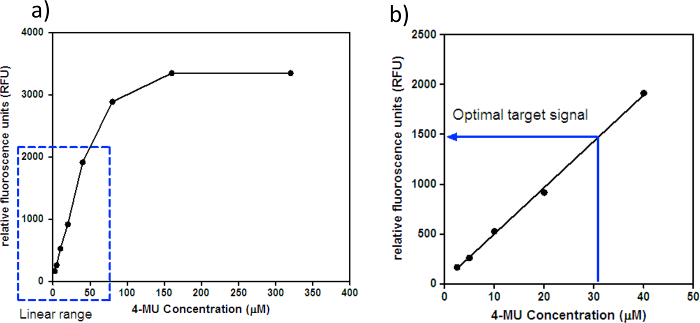
도 1 : 4-MU 농도 대 RFU. MU-4 농도 (μM) 대 RFU의 (a) 표준 곡선. 점선 박스는 형광 4-MU의 선형 범위를 도시한다. 선형 범위 위에 형광 신호가 포화하므로, 임의의 수있다형광 몰의 변화는 형광에 의해 검출되지 않을 수있다. (b)의 식별을위한도 1A의 표준 곡선의 선형 근접 부 "최적 목표 신호." 멜버른 WHOCCRRI에서 형광은 2.5-40 μM 4-MU의 선형 범위 ~ 1,500 RFU에 대응 ~ 30 μM 4-MU의 최적 목표 신호를 갖는다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
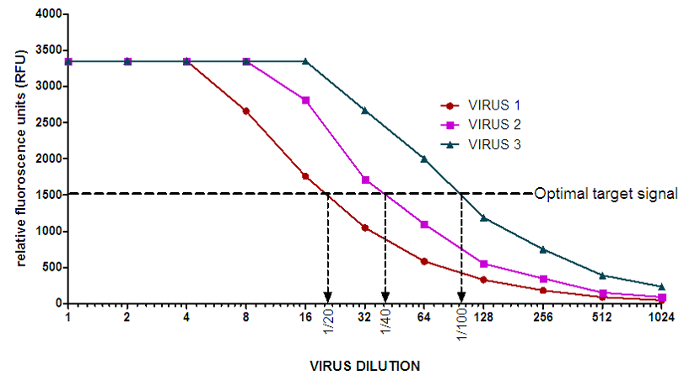
도 2 : 인플루엔자 바이러스 NA 활성 곡선의 예. 50.61 RFU 평균 배경 값은 NA 활성 곡선에서 모든 희석 점에서 제외되었다. 화살표는 각 바이러스에 대한 NA 억제 분석에 사용할 수있는 적절한 바이러스 희석을 나타낸다. 쉽게 준비에 대한바이러스 희석 aration, 하나는 바이러스 3 대신 1/96 희석에 대한 1/100 희석을 수행하도록 선택할 수 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
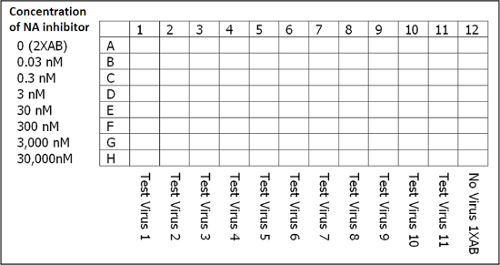
도 3 : NA 억제 분석의 셋업 플레이트 레이아웃. 각 접시에는 바이러스 만 1X 검정 완충액 (AB), NA 억제제 MUNANA을 포함하지 않는 음성 대조군으로 작용하는 마지막 열을 포함하고, 용액을 멈춘다. 주 : JASPR는 IC 50 값을 계산에 사용되는 평균 신호 빈을 결정하는 각각의 판의 열 (12)로부터 판독을 사용한다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
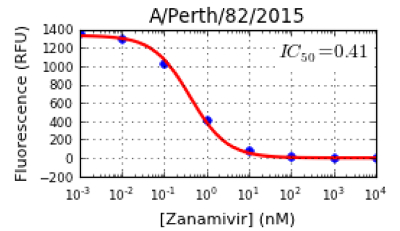
도 4 :는 A (H1N1) pdm09 바이러스 A / 퍼스 / 2,015분의 82의 억제 곡선과 IC 50 값의 예. JASPR 소프트웨어는 곡선 내의 모든 포인트 착용감, NA 억제제의 농도 증가 (㎚) 대 형광 (RFU)로 억제 곡선을 나타낸다. NA 억제제의 농도가 NA 바이러스 활성을 50 % 감소시키기 위해 억제 곡선에 기초하여, IC 50 값이 결정된다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
| 바이러스 | 바이러스 희석이 필요합니다 | 1X 검정 완충액 용적 (μL) | 계면 활성제 A-NP-40 (10 %) (mL) 중 | 바이러스 양 (mL) 중 |
| 1 | 1/20 | (940) | (10) | (50) |
| 이 | 1/40 | 965 | (10) | (25) |
| 삼 | 1/100 | 890 | (10) | (10) |
표 1 : NA 억제 분석에 VIRUS 1,2 바이러스 희석액을 제조하고, (3).
| 바이러스 종류 / 하위 / 계보 | 일반 억제 | 감소 억제 | 매우 감소 된 억제 |
| (NI) | (RI) | (HRI) | |
| A (H1N1) pdm09 | <10 배 | 10 ~ 100 배 | > 100 배 |
| A (H3N2) | 및# 60 10 배 | 10 ~ 100 배 | > 100 배 |
| B 야마가타와 B 빅토리아 | <5 배 | 5 ~ 50 배 | > 50 배 |
표 2 : WHO 바이러스 워킹 그룹은 NA 억제제에 인플루엔자 바이러스 감수성의 분류에 대한 지침을 권장합니다.
| 바이러스 종류 / 하위 / 계보 | 엔 | 자 나미 비르 | 오셀 타미 비르 | Peramivir | Laninamivir |
| 중간 값 (범위) IC 50 nm의 | 중간 값 (범위) IC 50 nm의 | 중간 값 (범위) IC 50 nm의 | 중간 값 (범위) IC 50 nm의 | ||
| A (H1N1) pdm09 | 1,326 | 0.42 (0.1-3.43) | 0.36 (0.01-3.48) | 0.19 (0.07-1.60) | 0.55 (0.05-2.29) |
| A (H3N2) | 1,654 | 0.9 (0.11-4.0) | 0.38 (0.01-3.65) | 0.33 (0.12-3.06) | 1.38 (0.01-9.38) |
| B 야마가타와 B 빅토리아 | 1,115 | 2.2 (1.24-10.72) | 15.12 (2.39-70.75) | 1.36 (0.57-6.67) | 2.89 (1.62-9.15) |
표 3 : 정상적인 억제 메디안 IC (50)와 IC (50)의 범위는 2015 (NI) 바이러스는 WHO CCRRI 멜버른 도출.
| 아미노산 치환 | 종류 / 하위 / 계보 | IC 50 배 변화 CO중간 IC 50 값을 참조하는 mpared. | |||
| 자 나미 비르 | 오셀 타미 비르 | Peramivir | Laninamivir | ||
| H275Y | A (H1N1) pdm09 | 1 | 557 (HRI) | 123 (HRI) | 이 |
| E119V | A (H3N2) | 1 | 63 (RI) | 1 | 1 |
| H134Y | B 빅토리아 | 1 | 4 | 76 (HRI) | 이 |
| N151T | B 빅토리아 | 4 | 4 | 42 (HRI) | 1 |
| G104E | B 빅토리아 | 1,220 (HRI) | 87 (HRI) | 17,724 (HRI) | 701 (HRI) |
| E105K | B 빅토리아 | 삼 | 5 (RI) | 59 (HRI) | 이 |
| I222T | B 빅토리아 | 이 | 7 (RI) | 8 (RI) | 삼 |
| H273Y | B 야마가타 | 1 | 230 (HRI) | 377 (HRI) | 이 |
| D197N | B 야마가타 | 4 | 7 (RI) | 32 (RI) | 삼 |
표 4 : 감소 된 억제 (RI) 또는 NA 억제제 매우 감소 억제 (HRI)에 연결된 아미노산 치환의 대표적인 목록.
| 문제 | 가능한 원인 (들) | 솔루션 (들) |
| 없음 또는 낮은 NA 활동 | 어떤 바이러스가 존재하거나 낮은 바이러스 수율 없었다. | 임상 표본 세포주에서 배양 (즉 Madin-다비 개 신장 세포) 또는 발육 계란에해야개구 억제 분석에 사용하기위한 더 높은 바이러스 부하. |
| 일부 돌연변이 바이러스 높은 바이러스 부하에도 불구하고 매우 낮은 NA 활동이있다. | 테스트를 위해 깔끔한 바이러스 농도를 사용합니다. 낮은 pH의 분석 완충액 (예를 들면 pH를 5.3)을 사용할 수있다. 데이터를 비교 그러나주의를 기울여야합니다. | |
| NO 또는 NA 억제 분석에서 활성이 낮은 NA | 어떤 바이러스는 추가되지 않았다. | 바이러스를 다시 희석. 바이러스를 확인하는 직접 1X 검정 완충액에 첨가 하였다. |
| 잘못된 바이러스 희석 사용 하였다. | 개구의 활성 분석을 반복한다. | |
| 부족 배양 시간. | 배양 시간을 확인하는 것이옵니다. | |
| 데이터 요소는 IC (50) 곡선 벗어나는 | 높은 농도의 NA 억제제의 교차 오염. | 팁은 NA의 inhibi과 접촉하지 있는지 확인토 96 웰 플레이트에 희석 된 바이러스를 분배 할 때. |
| 8 디프 웰 저장조를 사용한 경우, 폐기하고 새로운 8 디프 웰 저장조로 억제제 농도 NA를 재 디스펜스. | ||
| 개구 억제제 또는 MUNANA 희석 바이러스의 양은 각 웰에 첨가하여 균일하게되지 않았다. | 교정 된 멀티 채널 피펫 분석을 반복한다. 각각의 시약의 동일 부피의 각 웰에 분배 확인. | |
| 비정상적으로 높은 IC 50 값 | 바이러스의 너무 높은 농도가 추가되었습니다. | 개구의 활성 분석 및 NA 억제 분석을 반복한다. |
| 테스트 샘플은 인플루엔자 A 및 인플루엔자 B의 혼합물을 포함 | 바이러스 혼합물의 존재를 식별하기 위해 실시간 PCR을 수행합니다. | |
| 샘플에서 박테리아 오염 | 항생제의 존재와 무균 상태에서 배양 바이러스. | |
| 높은 배경 형광 신호 | MUNANA 기판은 시간이 지남에 따라 저하 될 수 있습니다. | MUNANA의 subtrate의 새로운 배치를 사용합니다. |
| 이웃하는 웰에서 형광 검출. | 블랙 96 웰 평면 바닥 플레이트를 사용하여 |
표 5 : NA 억제 분석에서 잠재적 문제를 해결.
토론
NA 억제제 인플루엔자 바이러스 감수성의 글로벌 모니터링은 현재의 형광 또는 화학 발광 NA 억제 분석 (11), (12)을 사용하여 실험실들에 의해 수행되고있다. 형광 분석은 더 일반적으로 화학 발광 분석보다 사용된다. 두 분석은 견고하고 재현하지만, 형광 계 분석에서 얻은 IC 50 값은 13 어려운 두 분석으로부터의 데이터의 직접적인 비교를 상기 발광 기반 분석법보다 종종 높다. 심지어 동일한 프로토콜을 사용하여, 한 실험에서 생성 된 데이터가 서로 다를 수있다. 때문에 실험실 사이의 이러한 변화의, 보건기구 (WHO) 워킹 그룹은 인플루엔자 바이러스 감수성의 감시에 실험실 간 비교에 도움이되는 가이드 라인을 만들었다. 오히려,이 가이드 라인을 사용하여 IC (50)의 절대 값을 비교보다중간 각 특정 실험실 테스트에서 NI 인플루엔자 바이러스의 IC (50)에 IC (50) 배의 차이에 기초하여 사행 비교. 다섯 개 협력 센터에서 데이터를 비교하는 능력은 글로벌 인플루엔자 바이러스 감수성 데이터 2, 3, 4의 연간 간행물 가져왔다. 공공 영역에서 인플루엔자 감수성 많은 양의 데이터의 가용성은 연구자가 자신의 실험실에서 생성 된 그와 그 연구에서 IC (50 개)의 데이터를 비교할 수 있습니다.
유사한 개념을 채택 기타 NA 억제 분석도 시판되고있다. 즉시 사용 가능한 시약을 포함하는이 상업 키트 (NA는 포함되지 억제제) 똑같이 재현 할 수 있습니다. 시약의 대부분에서 자체 제작 될 수 있기 때문에, 사내 NA 억제 분석은 상업용 키트보다 실질적으로 저렴더 많은 양의 이전 분석의 주요 비용을 만든 MUNANA 기판은 이제 경쟁력있는 가격으로 다양한 소스에서 구입하실 수 있습니다. 약물 당 하나 개의 인플루엔자 분리 테스트의 비용은 약 $ 1 (USD)이다. 멜버른 WHOCCRRI에서 개선 분석의 액체 처리 구성 요소에 대한 로봇 플랫폼의 혼입 후 실내 NA 억제 분석에 이루어졌다. 외에도 바이러스 희석의 수동 준비에서, 절차의 대부분은 액체 처리 로봇을 사용하여 수행됩니다. 이 수동 조작을 최소화 할뿐만 아니라 하루에 실행할 수있는 분석의 수를 증가 않을뿐만 아니라.
개구 억제 분석은 매우 견고하지만, 추가적인주의 완료 할 중요한 단계의 수있다. 우선, 억제 곡선과 IC 50 값을 이동할 수 NA 억제제 농도 어떠한 불규칙; 따라서 세심한주의를해야한다개구 억제제 농도를 준비 할 때 지불. 둘째로, 정확한 피펫 정확한 배양 기간 분석법 일관된 결과를 유지하는 데 매우 중요하다; 이는 교정 피펫 및 타이머를 사용함으로써 달성 될 수있다. 모든 분석에서 제어 바이러스의 포함은 또한 분석에서 분석 및 장기간에 걸쳐 분석 성능의 모니터링을 가능하게한다. 계절 인플루엔자 바이러스의 NA 효소 활성은 pH가 6.5에서 최적이기 때문에 셋째, 분석 완충액의 pH는 정확한 것이 중요하다. 몇몇 보고서 월 낮은 pH 조건에의 사용 등 R292K 돌연변이 14, 15를 포함하는 A (H7N9) 변종 인플루엔자 변이체의 동정을 향상 것을 발견 하였다. 그러나, 분석 완충액의 pH에 대한 수정은 IC 50 값을 이동하며, 이는 실험실에서 실험실 데이터 사이의 비교를 복잡하게 할 수있다. 기타 수정 및 페이지가 될 수있는 문제 해결erformed 표 5에 나열되어 있습니다.
NA 억제제는 현재 인플루엔자 바이러스 순환에 대한 효과적인 승인 바이러스제의 유일한 클래스입니다. 다른 바이러스 클래스 임상 사용을 위해 제공 될 때까지, 인플루엔자 바이러스 순환의 바이러스 감수성 감시 혼자 NA 억제제에 초점을 맞 춥니 다. 단순성 때문에 결과의 재현성은 NA 억제 분석의 사용은 계속 NA 억제제 인플루엔자 바이러스 감수성을 평가.
공개
저자가 공개하는 게 없다.
감사의 말
인플루엔자에 참조 및 연구 협력 센터 멜버른 WHO는 건강의 호주 정부 부서에 의해 지원됩니다.
자료
| Name | Company | Catalog Number | Comments |
| Influenza A and B viruses | Cultured in MDCK cells or 9 day old embryonated specific pathogen free (SPF) eggs | ||
| Madin-Darby Canine Kidney (MDCK) cells | ATCC | PTA-6500 | |
| 2-(4-methylumbelliferyl)-a-D-N-acetylneuraminic acid (MUNANA) | Biosynth AG | M-5507 | |
| 2-(4-methylumbelliferyl)-a-D-N-acetylneuraminic acid (MUNANA) | Sigma | M8639 | |
| 4-Methylumbelliferone (4-MU) | Sigma | M1381-25G | |
| 2-[N-morpholino]ethanesulphonic acid (MES hydrate) (free acid) | Sigma | M8250-250G | |
| Calcium Chloride (Ca Cl2) | APS AJAX Finechem | 127-500G | |
| Surfactant-Amps-NP-40 (10% solution) | Thermo Fisher Scientific | PIE28324 | |
| Sodium Hydroxide (NaOH) | APS AJAX Finechem | 482-2.5KG | |
| Absolute Ethanol | APS AJAX Finechem | 214-2.5L GL | |
| 96-well clear flat-bottom plates | NUNC | 456537 | |
| 96-well U-bottom plates | Greiner Bio-one | 4650101 | |
| 8 channel deep well block | Pacific Laboratory Products | RES-MW8-HP | |
| 96-well deep plates, 2.0 mL square wells | Pacific Laboratory Products | P-2ML-SQ-C | |
| Plate sealers | Thermo Fisher Scientific | 236366 | |
| Bottle-top vacuum filter system (cellulose membrane (nitrate), pore size 0.2 μm, membrane area 33.2 cm2, filter capacity 500 mL) | Sigma-Aldrich | CLS430758-12EA | |
| Single-channel pipettes (1 µL - 1,000 µL) | Variety of suppliers (eg. Eppendorf, Sartorius) | ||
| Multi-channel pipettes | Variety of suppliers (eg. Eppendorf, Sartorius) | 8 or 12 channel electronic and manual pipette (5 - 1250 µL volume) | |
| Pipette tips (1 µL - 1,250 µL) | Variety of suppliers (eg. Eppendorf, Sartorius) | ||
| Disposable pipettes (10 mL and 25 mL) | Greiner Bio-one | P7740-200EA and P7865-200EA | |
| Pipette controller | Eppendorf | 4430000018 | |
| Centrifuge tubes 50 mL | BD Bioscience | 352070 | |
| Racked tubes | Scientific Specialties, Inc. | 1750-00 | |
| Fluorometer with excitation wavelength setting of 355 nm and an emission wavelength setting of 460 nm | TermoFisher Scientific | ASCENT FL 374 | |
| Ascent software | TermoFisher Scientific | 5185410CD | |
| Incubator set at 37 °C | Lab Supply | Biocell 1000 | |
| Zanamivir | GlaxoSmithKline | Request directly from the company | |
| Oseltamivir carboxylate | Roche | ||
| Peramivir (BCX-1812) | BioCryst | ||
| Laninamivir (R-125489) | Daiichi-Sankyo | ||
| JASPR v1.2 | Influenza Division at the CDC Atlanta, USA | freely available upon request (fluantiviral@cdc.gov) |
참고문헌
- Moscona, A. Neuraminidase inhibitors for influenza. N.Engl.J.Med. 353 (13), 1363-1373 (2005).
- Hurt, A. C., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 132, 178-185 (2016).
- Meijer, A., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 110, 31-41 (2014).
- Takashita, E., et al. Global update on the susceptibility of human influenza viruses to neuraminidase inhibitors. Antiviral Res. 117, 27-38 (2015).
- Lackenby, A., et al. Emergence of resistance to oseltamivir among influenza A(H1N1) viruses in Europe. Euro Surveill. 13 (5), (2008).
- Hurt, A. C., et al. Community transmission of oseltamivir-resistant A(H1N1)pdm09 influenza. N Engl J Med. 365 (26), 2541-2542 (2011).
- Takashita, E., et al. Characterization of a large cluster of influenza A(H1N1)pdm09 viruses cross-resistant to oseltamivir and peramivir during the 2013-2014 influenza season in Japan. Antimicrob Agents Chemother. 59 (5), 2607-2617 (2015).
- Eisfeld, A. J., Neumann, G., Kawaoka, Y. Influenza A virus isolation, culture and identification. Nat Protoc. 9 (11), 2663-2681 (2014).
- . Meetings of the WHO working group on surveillance of influenza antiviral susceptibility - Geneva, November 2011 and June 2012. Wkly Epidemiol Rec. 87 (39), 369-374 (2012).
- Okomo-Adhiambo, M., Hurt, A. C., Gubareva, L. V. The chemiluminescent neuraminidase inhibition assay: a functional method for detection of influenza virus resistance to the neuraminidase inhibitors. Methods Mol Biol. 865, 95-113 (2012).
- Hurt, A. C., Okomo-Adhiambo, M., Gubareva, L. V. The fluorescence neuraminidase inhibition assay: a functional method for detection of influenza virus resistance to the neuraminidase inhibitors. Methods Mol Biol. 865, 115-125 (2012).
- Analysis of IC50 data. isirv Antiviral Group (isirv-AVG) Available from: https://isirv.org/site/index.php/methodology/analysis-of-ic50-data (2016)
- Sleeman, K., et al. R292K substitution and drug susceptibility of influenza A(H7N9) viruses. Emerg Infect Dis. 19 (9), 1521-1524 (2013).
- Gubareva, L. V., Robinson, M. J., Bethell, R. C., Webster, R. G. Catalytic and framework mutations in the neuraminidase active site of influenza viruses that are resistant to 4-guanidino-Neu5Ac2en. J Virol. 71 (5), 3385-3390 (1997).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유