JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
칸디다 알비칸스(Candida albicans)에 대한 펩타이드의 항진균 활성 정량화
요약
이 프로토콜은 칸 디다 알비칸스에 대한 펩타이드 및 소분자 항진균제와 같은 기타 화합물의 항진균 활성에 대한 정량적 데이터를 얻는 방법을 설명합니다. 성장 억제를 정량화하기 위해 집락 형성 단위를 세는 대신 광학 밀도를 사용하면 시간과 자원을 절약할 수 있습니다.
초록
칸디다 알비칸스(Candida albicans)에 대한 항진균성 감수성 검사를 수행하는 전통적인 방법은 시간이 많이 걸리고 정량적 결과가 부족합니다. 예를 들어, 일반적인 접근법은 한천 플레이트에 다양한 농도의 항진균 분자로 처리된 세포를 도금한 다음 콜로니를 계수하여 분자 농도와 성장 억제 사이의 관계를 결정하는 데 의존합니다. 이 방법은 식민지를 세는 데 많은 판과 상당한 시간이 필요합니다. 또 다른 일반적인 접근법은 성장을 억제하는 데 필요한 최소 농도를 확인하기 위해 항진균제로 처리된 배양물을 육안으로 검사하여 플레이트와 콜로니 계수를 제거합니다. 그러나 육안 검사는 정성적 결과만 생성하며 하위 억제 농도에서의 성장에 대한 정보는 손실됩니다. 이 프로토콜은 항진균 펩타이드에 대한 C. albicans의 감수성을 측정하는 방법을 설명합니다. 배양의 광학 밀도 측정에 의존함으로써 이 방법은 다양한 펩타이드 농도에서 배양 성장에 대한 정량적 결과를 얻는 데 필요한 시간과 재료를 줄입니다. 펩타이드를 사용한 곰팡이의 배양은 적절한 완충액을 사용하여 96웰 플레이트에서 수행되며, 대조군은 성장 억제 없음 및 완전한 성장 억제를 나타냅니다. 펩티드와 함께 배양한 후, 생성된 세포 현탁액을 희석하여 펩티드 활성을 감소시킨 다음 밤새 성장시킵니다. 하룻밤 성장 후, 각 웰의 광학 밀도를 측정하고 양성 및 음성 대조군과 비교하여 각 펩티드 농도에서 결과적인 성장 억제를 계산합니다. 이 분석을 사용한 결과는 한천 플레이트에 배양물을 도금하는 전통적인 방법을 사용한 결과와 비슷하지만 이 프로토콜은 플라스틱 폐기물과 집락 계수에 소요되는 시간을 줄입니다. 이 프로토콜의 적용은 항진균 펩타이드에 초점을 맞추었지만 이 방법은 항진균 활성이 알려지거나 의심되는 다른 분자를 테스트하는 데에도 적용할 수 있습니다.
서문
칸디다 알비칸스(Candida albicans)는 구강, 피부, 위장관 및 질을 포함한 수많은 위치에 서식하는 인간 미생물총의 일원입니다1. 인간 면역결핍 바이러스(human immunodeficiency virus, HIV) 및 면역억제 치료와 같은 질병으로 인해 면역이 저하된 환자의 경우, C. albicans의 집락화는 국소 또는 전신 칸디다증을 유발할 수 있다 2,3. 암포테리신 B, 아졸 또는 에키노칸딘과 같은 현재 이용가능한 소분자 항진균 치료제의 사용은 용해도 및 독성 문제와 치료제에 대한 감염의 저항성에 의해 복잡해질 수 있다 4,5. 현재 항진균제의 한계로 인해 연구자들은 C. albicans에 대한 활성을 가진 새로운 항진균 분자를 지속적으로 찾고 있습니다.
항균 펩티드(AMP)는 현재의 소분자 항진균제6,7,8에 대한 잠재적인 대안이며, 소분자 약물9에 비해 내성 발달에 덜 민감한 것으로 제안된다. AMP는 다양한 펩타이드 세트이지만 종종 양이온성이며 광범위한 활성 스펙트럼을 가지고 있습니다10,11,12. C. albicans에 대한 활성을 가진 AMP에는 Histatin 및 cecropin 계열 13,14,15의 잘 알려진 펩타이드와 ToAP2, NDBP-5.7 및 히스타틴 5 변이체 K11R-K17R 16,17과 같은 최근에 설명된 펩타이드가 포함됩니다. 칸디다 감염을 치료할 수 있는 잠재력으로 인해 C. albicans를 표적으로 하는 새로운 AMP를 식별하고 설계하는 것은 많은 연구 그룹에서 중요한 목표입니다.
C. albicans를 표적으로 하는 효과적인 AMP(및 기타 항진균제)를 개발하는 과정의 일환으로, 체외 검사는 일반적으로 유망한 펩타이드를 식별하는 데 사용됩니다. C. albicans에 대한 항진균 활성을 테스트하는 방법은 일반적으로 96웰 플레이트에서 AMP(완충액 또는 배지)의 연속 희석액으로 세포를 배양하는 것을 포함합니다. 배양 후 항진균 활성을 평가하기 위해 몇 가지 방법을 사용할 수 있습니다. 임상검사표준협회(Clinical Laboratory Standards Institute)에서 기술한 기술은 웰의 탁도를 시각적으로 평가하여 완전한 성장 억제(아졸 및 에키노칸딘과 같은 선택된 항진균제의 경우 최소 50% 억제)를 측정하며, MIC 이하 농도에서 성장을 정량화하지 않는다18 . 일반적으로 사용되는 또 다른 접근법은 한천 플레이트에 웰의 내용물을 도금하고 플레이트를 배양한 다음 플레이트의 집락 형성 단위(CFU) 수를 계산하여 AMP로 배양한 후 생존력을 정량화하는 것입니다. 이 방법은 히스타틴 5계 펩티드, LL-37 및 인간 락토페린 19,20,21을 포함하는 다수의 펩티드를 평가하기 위해 사용되어 왔다. 이 기술은 상대적으로 많은 양의 한천과 많은 수의 플레이트가 필요하며 플레이트의 CFU를 지루하게 계산해야합니다. 플라스틱 폐기물을 줄이고 CFU 계산을 피하면서 더 많은 정량적 데이터를 얻기 위해 웰의 내용물을 사용하여 다른 96웰 플레이트에 새로운 배지를 접종할 수 있습니다. 새로 접종된 플레이트를 인큐베이션한 후, 흡광도 플레이트 판독기 상에서 600 nm(OD600)에서의 광학 밀도를 측정함으로써 성장을 정량화할 수 있다. 이 방법은 히스타틴 5 및 그의 분해 단편 및 세포 침투 펩티드 17,22,23,24,25의 항진균 활성을 결정하는 데 사용되었습니다.
이 프로토콜은 펩타이드의 항진균 활성을 테스트하는 방법을 설명하고 OD600 방법을 사용하여 펩타이드로 인한 C. albicans 의 생존력 감소를 정량화합니다.
프로토콜
이 프로토콜(PN 274)에서 C. albicans 를 사용한 작업에 대해 메릴랜드 대학교 칼리지 파크, 기관 생물안전 위원회(IBC)로부터 승인을 받았습니다. C. albicans 균주 SC5314 ( 재료 표 참조)를 본 연구에 사용하였다; 그러나, 임의의 다른 균주가 또한 사용될 수 있다.
1. 완충액, 멸균수 및 배양액의 제조
- pH 7.4에서 멸균 된 0.1M 인산 나트륨 완충액 (NaPB) 26 을 준비하고 멸균 수로 2mM 및 1mM로 희석합니다. 2 mM NaPB 및 1 mM NaPB 각각을 100 mL 제조하는 것은 이 프로토콜의 대부분의 적용에 충분할 것이다.
- 멸균 액체 효모-펩톤-포도당(YPD, 재료 표 참조) 배지(10g/L 효모 추출물, 20g/L 포도당, 20g/L 펩톤)를 준비합니다. 100mL의 YPD를 준비하는 것은 이 프로토콜의 대부분의 응용 분야에 충분합니다.
- 멸균 된 초순수를 준비하십시오. 100mL의 물을 준비하는 것은 이 프로토콜의 대부분의 응용 분야에 충분합니다.
참고: 완충액, 매체 및 물은 오토클레이브되는 용기 내의 부피에 기초하여 적절한 시간 동안 액체 사이클 상에서 121°C에서 오토클레이빙에 의해 멸균된다27. 예를 들어, 500mL가 들어 있는 병의 경우 노출 시간은 40분이어야 합니다.
2. C. albicans의 접종, 배양 및 계대배양
주의: 학술 연구 기관에서 약물 내성에 관계없이 생물 안전성 수준(BSL) 2 유기체로, American Type Culture Collection(ATCC)에서 균주28의 약물 내성에 따라 BSL1 또는 BSL2 유기체로 분류하는 C. albicans를 사용하기 위한 모든 기관 및 정부 규정을 따르십시오.
참고: 항진균 활성 테스트를 시작하기 전날에 이 단계(2.1-2.2단계)의 접종 및 배양 부분을 수행합니다. 가능하면 생물 안전 캐비닛에서 세포(및 세포와 함께 배양될 용액)로 모든 프로토콜 단계를 수행합니다.
- 원하는 C. albicans 균주를 배양 튜브의 YPD 배지 10mL에 접종합니다.
참고: 배양액은 냉동실 스톡 또는 한천 플레이트에서 접종할 수 있지만 비교할 모든 데이터에 대해 일관된 소스를 사용해야 합니다. - 회전식 셰이커에서 30°C 및 230rpm에서 하룻밤(~12-16시간) 배양물을 성장시킵니다.
- 하룻밤 배양 C. albicans, 그리고 ~1.0-1.2의 OD600 으로 자랍니다.
- UV 분광광도계를 사용하여 하룻밤 배양의OD600 을 측정한다( 재료 표 참조).
- 하룻밤 배양의 OD600에 기초하여, 하룻밤 배양을 사용하여 10 mL의 YPD 중 0.1의OD600에서 계대배양물을 접종한다.
- OD600 이 ~1.0-1.2에 도달할 때까지 회전 셰이커에서 230rpm의 회전 셰이커에서 4-6°C에서 계대 배양을 성장시킵니다. 계대배양이 성장하는 동안 3단계(펩타이드 용액 준비)를 완료하고; 계대배양은 단계 4의 분석에 사용하기 위해 희석될 것이다.
3. 96-웰 플레이트에서 펩타이드 용액의 제조
참고: 이 단계는 펩타이드 원액이 보관 중에 안정적인 경우 미리 수행될 수 있습니다. 전형적으로, 펩티드 용액은 사용까지 -20°C에서 저장된다. 다음 단계로 진행하기 전에 실온 수조에서 해동할 수 있습니다.
- 분석에서 테스트할 각 펩타이드의 최고 농도를 결정합니다. 이것은 선택된 펩티드에 따라 달라질 것이다. 대표 결과 섹션에 제시된 데이터에 대해 히스타틴 5 및 조작된 유사체22 를 테스트했으며 테스트된 최고 농도는 50μM였습니다.
참고: 테스트할 최고 농도는 문헌에 보고된 데이터를 사용하거나 광범위한 펩타이드 농도에 대해 예비 실험을 수행하여 결정됩니다. 가능한 경우, 테스트된 최고 농도에서 생존율이 완전히 감소하는 고원과 테스트된 최저 농도에서 생존력이 감소하지 않는 고원을 관찰하기 위해 가장 높은 농도를 선택하여 전체 범위의 펩타이드 활성을 정량화할 수 있어야 합니다. - 각 펩타이드를 원하는 최고 농도의 두 배로 멸균수에 용해시킵니다. 대표 결과 섹션에 제시된 데이터의 경우, 히스타틴 5 및 조작된 유사체의 100μM 용액 150μL를 멸균수에서 준비했습니다.
참고: 펩타이드가 물에 용해되지 않는 경우 이 단계 전에 다른 용매에 가용화해야 할 수 있습니다. 디메틸 설폭사이드(DMSO)는 일반적으로 작동 농도로 희석하기 전에 펩타이드를 고농도로 가용화하는 데 사용됩니다. DMSO의 최종 농도가 1%(v/v) 이하인지확인하십시오 29 대체 용매가 세포의 성장에 영향을 미치지 않는지 확인하십시오. 또한 3.4-3.5 단계의 모든 웰에서 용매 농도가 일정하게 유지되는지 확인하십시오. - 원하는 펩타이드 스톡 용액 40μL를 96웰 둥근 바닥 배양 플레이트의 각 행의 첫 번째 웰(컬럼 1)에 추가합니다( 재료 표 참조). 이 플레이트는 플레이트 1입니다(그림 1).
참고: 각 플레이트에는 펩타이드 테스트에 사용되는 8개의 행이 있습니다. 이러한 행은 서로 다른 펩타이드 또는 동일한 펩타이드의 복제에 사용할 수 있습니다. 각 행에 단일 펩타이드만 포함합니다. - 20μL의 멸균 초순수를 펩타이드가 포함된 행의 컬럼 2에서 컬럼 12에 추가합니다(그림 1).
참고: 3.2단계에서 순수 이외의 용매로 펩타이드 스톡을 제조한 경우 이 단계의 멸균수를 첫 번째 컬럼에 추가된 펩타이드 스톡에 존재하는 용매로 교체해야 합니다. 예를 들어, 펩타이드가 DMSO에 가용화되고 펩타이드 스톡이 물에 1%(v/v) DMSO를 포함하는 경우 1% DMSO를 포함하는 물을 컬럼 2 내지 컬럼 12에 첨가해야 합니다. - 플레이트를 가로질러 펩타이드 스톡 용액을 컬럼 10까지 연속적으로 희석합니다(그림 1).
참고: 아래에 설명된 대로 플레이트에서 연속 희석을 수행하는 대신 미세 원심분리기 튜브에서 희석을 수행하고 96웰 플레이트로 옮길 수도 있습니다.- 컬럼 1에서 20 μL를 제거하고 컬럼 2로 옮기고 위아래로 피펫팅하여 혼합합니다. 컬럼 2에는 이제 컬럼 1 농도의 1:2 희석으로 40μL의 펩타이드 용액이 포함되어 있습니다.
- 컬럼 2에서 20μL를 제거하고 컬럼 3으로 옮기고 위아래로 피펫팅하여 혼합하면 컬럼 3에 컬럼 1 농도의 1:4 희석으로 40μL의 펩타이드 용액이 포함됩니다.
- 컬럼 10에 컬럼 1 농도의 1:512 희석으로 40μL의 펩타이드 용액이 포함될 때까지 이 과정을 반복합니다.
- 컬럼 10에서 20μL의 펩타이드 용액을 제거하고 폐기합니다. 이제 각 컬럼에는 20μL의 펩타이드 용액(컬럼 1-10) 또는 물(컬럼 11 및 컬럼 12)이 포함됩니다.
참고: 컬럼 11의 웰은 멸균 대조군 역할을 하고 컬럼 12의 웰은 펩타이드를 포함하지 않는 대조군 역할을 합니다.
4. C. albicans 하위 문화의 희석
참고: 계대배양이 ~1.0-1.2의 OD600 에 도달한 후 이 단계를 시작합니다(2.3.3단계).
- 계대배양물을 15mL 원심분리 튜브로 옮기고, 실온에서 3분 동안 3,900 x g 에서 원심분리하여 세포를 펠렛화하였다. 피펫팅 또는 디캔팅으로 상층액을 제거합니다.
- 펠릿을 2mM NaPB 1mL(단계 1.1)로 재현탁하고 현탁액을 1.7mL 원심분리기 튜브로 옮깁니다.
- 세포를 펠렛화하고(단계 4.1에서와 같이), 상청액을 버리고, 펠렛을 다시 1 mL의 2 mM NaPB에 재현탁시킨다.
- 단계 4.3을 추가로 2회 반복하여 세척된 세포를 2 mM NaPB 1 mL에 남겨둔다.
- 세척된 현탁액의 세포 밀도를 결정하고 5 x 105 cells/mL의 세포 밀도를 얻는 데 필요한 희석 계수를 계산합니다. 이러한 농도는 궁극적으로 1 x 104 세포를 96-웰 플레이트의 각 웰에 첨가하는 것으로 이어질 것이다.
참고: 현탁액의 세포 밀도는 혈구계 또는 자동 세포 계수기를 포함한 여러 방법을 사용하여 결정할 수 있습니다. 관련 조건 하에서 성장한 관심 균주에 대한 세포 밀도 대OD600의 표준 곡선을 본 연구에 사용하였다. 이 곡선은 다양한OD600 값을 갖는 현탁액의 세포 밀도를 결정하기 위해 혈구계(재료 표 참조)를 사용하여 제조하였다. - 세포 현탁액을 2mM NaPB에서 5 x 105 cells/mL로 희석합니다. 이 희석된 현탁액 10mL를 준비하는 것만으로도 이 연구를 완료하기에 충분할 것입니다.
5. 펩타이드 용액을 사용한 C. albicans 의 배양 및 생존력 정량화를 위한 세포 준비
- 희석된 C. albicans 현탁액(4.6단계)을 각 행의 열 1-10 및 열 12에 20μL를 추가합니다(그림 1).
참고: 첫 번째 열의 최종 펩타이드 농도는 이제 펩타이드 스톡 농도의 절반입니다. 본 연구의 경우, 이 시점에서 최종 펩티드 농도는 50 μM이었다. 각 웰의 최종 세포 현탁액에는 2.5 x 105 cells/mL가 포함됩니다. 컬럼 1-10은 다양한 펩타이드 농도에서 항진균 활성을 평가하기 위한 실험 웰 역할을 하고, 컬럼 12는 펩타이드가 없는 성장에 대한 대조군 역할을 합니다. - 20μL의 2mM NaPB를 컬럼 11에 추가합니다. 모든 웰은 이제 1mM NaPB의 최종 농도를 갖습니다. 컬럼 11은 무균 제어 역할을 합니다.
- 플레이트 1(세포 및 펩티드 둘 다 함유)을 커버하고, 이를 30°C에서 30분 동안 인큐베이션한다.
참고: 30분의 배양 시간은 많은 펩티드 17,21,22,30에 대해 충분하지만, 항진균 활성을 발휘하기 위해 더 긴 시간을 필요로 할 수 있는 펩티드를 설명하기 위해 원하는 경우 배양 시간을 60분으로 증가시킬 수 있다 25,31,32. - 생존율을 정량화하는 데 사용할 새로운 96-웰 배양 플레이트(플레이트 2)를 준비합니다(그림 2).
참고: 배양 플레이트는 플레이트 1의 배양 중에 준비해야 합니다.- 플레이트의 모든 웰에 100 μL의 YPD (단계 1.2)를 추가하십시오.
- 100 μL의 2 mM NaPB (단계 1.1)를 플레이트의 모든 웰에 첨가한다.
- 플레이트 1(세포 및 펩타이드 포함)의 샘플을 희석하고 플레이트 2(배지 및 완충액 포함)로 옮깁니다.
- 배양 30분 후 배양기에서 플레이트 1을 회수합니다.
- 각 웰에 총 부피 320μL에 대해 1mM NaPB 280μL(단계 1.1)를 추가하여 플레이트 1의 각 웰을 희석합니다(그림 2).
- 세포와 펩타이드가 포함된 모든 웰을 위아래로 피펫팅하여 혼합하여 모든 세포가 재현탁되고 웰 바닥에 침전된 세포가 보이지 않도록 합니다.
- 플레이트 1의 각 웰에서 플레이트 2의 해당 웰로 8μL를 옮깁니다. 이 부피는 플레이트 1의 각 웰에서 플레이트 2로 약 250개의 세포를 전달합니다(그림 2).
- 플레이트 2를 덮고 30°C에서 17시간 동안 350rpm으로 마이크로타이터 플레이트 쉐이커( 재료 표 참조) 상에서 인큐베이션합니다.
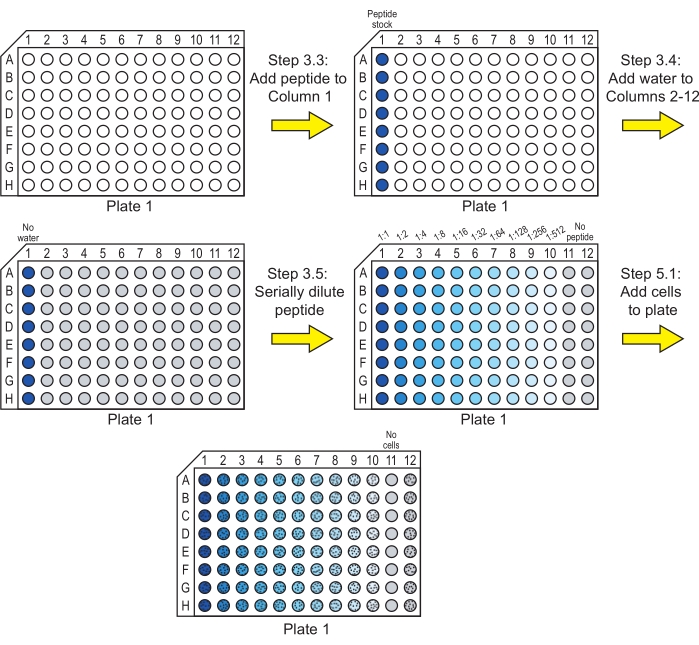
그림 1: 세포와 함께 펩타이드 연속 희석액의 인큐베이션을 위한 플레이트 1의 준비. 펩티드의 연속 희석은 물에서 이루어지며, C. albicans 세포는 플레이트 1에 첨가된다. 파란색은 펩타이드가 웰에 존재함을 나타내고 회색은 물이 있고 펩타이드가 없는 웰을 나타냅니다. 세포를 포함하는 웰은 검은 점들의 패턴으로 표시됩니다. 이러한 단계 후, 플레이트는 펩타이드가 항진균 활성을 발휘할 수 있도록 배양됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 2: 펩타이드에 의한 생존율 감소를 정량화하기 위한 플레이트 2의 제조. YPD 배지 및 NaPB를 플레이트 2에 첨가한다. 플레이트 1의 내용물을 희석한 후, 각 웰로부터의 분취량을 플레이트 1에서 플레이트 2로 옮긴다. 플레이트 2는 이어서OD600을 측정하여 정량화를 위해 임의의 생존 세포가 성장할 수 있도록 인큐베이션한다. 플레이트 2의 경우 YPD 및 NaPB만 포함하는 웰이 주황색으로 표시됩니다. YPD 및 NaPB와 혼합된 플레이트 1로부터의 분취량을 함유하는 웰은 녹색으로 표시된다. 플레이트 1의 색상에 대한 설명은 그림 1의 범례를 참조하십시오. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
6. 항진균 활성의 결정
- 플레이트600 의 각 웰에 대한 OD 2 판독값을 얻습니다.
- 배양 17시간 후 인큐베이터에서 플레이트 2를 제거합니다.
- 플레이트 2의 모든 웰을 위아래로 피펫팅하여 혼합하여 모든 세포가 재현탁되고 웰 바닥에 침전된 세포가 보이지 않도록 합니다.
알림: 기포는 OD600 판독값을 방해할 수 있으므로 이 단계에서 기포를 생성하지 마십시오. 기포가 형성되면 종종 마른 피펫 팁으로 터뜨리거나 두 개의 피펫 팁을 사용하여 우물에서 들어 올려 제거할 수 있습니다. - 600 nm의 파장에서 흡광도 플레이트 리더 ( 재료 표 참조)를 사용하여 각 웰에 대한 OD600 을 얻습니다.
- 성장 억제(백분율)를 계산하고 이를 플로팅하여 펩타이드가 C. albicans의 성장에 미치는 영향을 결정합니다.
- 각 웰에 대해 다음 방정식 17,22,23을 사용하여 대조군과 비교하여 생존율 감소를 백분율로 계산합니다.
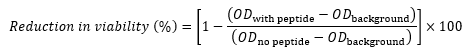
여기서 펩티드를 갖는 OD는 주어진 농도의 펩티드를 함유하는 웰의 OD600이고, OD배경은 같은 행에 있는 컬럼 11의 OD600이고,
OD는 동일한 행에 있는 컬럼 12의OD600 이다(대조군은 세포 및 펩타이드를 포함하지 않음). - 예를 들어, 다음 표현식을 사용하여 행 B의 OD600 값에서 Well B5의 생존율 감소를 계산합니다.
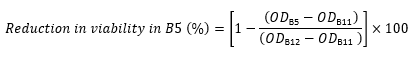
- 각 웰에 대해 다음 방정식 17,22,23을 사용하여 대조군과 비교하여 생존율 감소를 백분율로 계산합니다.
- 생존력의 감소를 펩티드 농도의 함수로 표시합니다.
결과
항진균 펩타이드로 인한 성장 감소를 정량화하기 위해 OD600 측정을 사용하면 도금 샘플 및 CFU 계수에 비해 상당한 시간을 절약할 수 있습니다. 이 프로토콜에 설명된 방법은 서로 다른 3일에 단계를 완료해야 합니다. 첫날에는 완충액과 배지(멸균 시간 제외)를 준비하고 하룻밤 배양을 위해 C. albicans 의 시작 배양을 접종하는 데 약 1시간이 필요합니다. 둘째 날에, 단계는 17시간 인큐?...
토론
이 프로토콜은 진균 병원체 C. albicans에 대한 AMP의 항진균 활성에 대한 정량적 데이터를 얻기 위한 효율적인 접근 방식을 설명합니다. 펩타이드 및 기타 항진균제를 검사하는 일반적인 대안 접근법 중 하나는 CLSI(Clinical Laboratory Standards Institute)의 표준 M2718에 설명된 브로스 미세 희석이지만 이 표준은 정량적 결과 대신 정성적 시각적 결과를 얻는 데 중점을 둡니다. 또 다른 ...
공개
저자는 경쟁하는 재정적 이익이 없다고 선언합니다.
감사의 말
이 연구는 국립 보건원 (R03DE029270, T32AI089621B), 국립 과학 재단 (CBET 1511718), 교육부 (GAANN-P200A180093) 및 메릴랜드 대학교 크로스 캠퍼스 종자 보조금의 지원을 받았습니다.
자료
| Name | Company | Catalog Number | Comments |
| 96-well plates (round bottom) | VWR | 10062-902 | |
| Absorbance microplate reader | N/A | N/A | Any available microplate reader is sufficient |
| C. albicans strain SC5314 | ATCC | MYA-2876 | Other C. albicans may also be used |
| Hemocytometer | N/A | N/A | Can be used to make a standard curve relating cell number to OD600 |
| Microplate shaker | VWR | 2620-926 | |
| Peptide(s) | N/A | N/A | Peptides can be commercially synthesized by any reliable vendor; a purity of ≥95% and trifluoroacetic acid salt removal to hydrochloride salt are recommended |
| Reagent reservoirs for multichannel pipettors | VWR | 18900-320 | Simplifies pipetting into multiwell plates with multichannel pipettor |
| Sodium phosphate, dibasic | Fisher Scientific | BP332-500 | For making NaPB |
| Sodium phosphate, monobasic | Fisher Scientific | BP329-500 | For making NaPB |
| UV spectrophotometer | N/A | N/A | Any available UV spectrophotometer is sufficient |
| YPD medium powder | BD Life Sciences | 242820 | May also be made from yeast extract, peptone, and dextrose |
참고문헌
- Gulati, M., Nobile, C. J. Candida albicans biofilms: Development, regulation, and molecular mechanisms. Microbes and Infection. 18 (5), 310-321 (2016).
- Arya, N. R., Rafiq, N. B. Candidiasis. StatPearls. , (2021).
- de Oliveira Santos, G. C., et al. Candida infections and therapeutic strategies: Mechanisms of action for traditional and alternative agents. Frontiers in Microbiology. 9, 1351 (2018).
- Espinel-Ingroff, A. Mechanisms of resistance to antifungal agents: Yeasts and filamentous fungi. Revista Iberoamericana de Micología. 25 (2), 101-106 (2008).
- Wang, X., et al. Delivery strategies of amphotericin B for invasive fungal infections. Acta Pharmaceutica Sinica B. 11 (8), 2585-2604 (2021).
- Struyfs, C., Cammue, B. P. A., Thevissen, K. Membrane-interacting antifungal peptides. Frontiers in Cell and Developmental Biology. 9, 649875 (2021).
- Huan, Y., Kong, Q., Mou, H., Yi, H. Antimicrobial peptides: Classification, design, application and research progress in multiple fields. Frontiers in Microbiology. 11, 582779 (2020).
- Sarkar, T., Chetia, M., Chatterjee, S. Antimicrobial peptides and proteins: From nature's reservoir to the laboratory and beyond. Frontiers in Chemistry. 9, 691532 (2021).
- Mahlapuu, M., Bjorn, C., Ekblom, J. Antimicrobial peptides as therapeutic agents: Opportunities and challenges. Critical Reviews in Biotechnology. 40 (7), 978-992 (2020).
- Lei, J., et al. The antimicrobial peptides and their potential clinical applications. American Journal of Translational Research. 11 (7), 3919-3931 (2019).
- Mercer, D. K., O'Neil, D. A. Innate inspiration: Antifungal peptides and other immunotherapeutics from the host immune response. Frontiers in Immunology. 11, 2177 (2020).
- Bin Hafeez, A., Jiang, X., Bergen, P. J., Zhu, Y. Antimicrobial peptides: An update on classifications and databases. International Journal of Molecular Sciences. 22 (21), 11691 (2021).
- Xu, T., Levitz, S. M., Diamond, R. D., Oppenheim, F. G. Anticandidal activity of major human salivary histatins. Infection and Immunity. 59 (8), 2549-2554 (1991).
- Helmerhorst, E. J., et al. Amphotericin B- and fluconazole-resistant Candida spp., Aspergillus fumigatus, and other newly emerging pathogenic fungi are susceptible to basic antifungal peptides. Antimicrobial Agents and Chemotherapy. 43 (3), 702-704 (1999).
- Andra, J., Berninghausen, O., Leippe, M. Cecropins, antibacterial peptides from insects and mammals, are potently fungicidal against Candida albicans. Medical Microbiology and Immunology. 189, 169-173 (2001).
- do Nascimento Dias, J., et al. Mechanisms of action of antimicrobial peptides ToAP2 and NDBP-5.7 against Candida albicans planktonic and biofilm cells. Scientific Reports. 10, 10327 (2020).
- Ikonomova, S. P., et al. Effects of histatin 5 modifications on antifungal activity and kinetics of proteolysis. Protein Science. 29, 480-493 (2020).
- Clinical Laboratory Standards Institute. . M27-A3. Reference method for broth dilution antifungal susceptibility testing of yeasts; Approved standard - Third edition. , (2008).
- Lupetti, A., et al. Candidacidal activities of human lactoferrin peptides derived from the N terminus. Antimicrobial Agents and Chemotherapy. 44 (12), 3257-3263 (2000).
- Han, J., Jyoti, M. A., Song, H. Y., Jang, W. S. Antifungal activity and action mechanism of histatin 5-halocidin hybrid peptides against Candida ssp. PLoS One. 11 (2), 0150196 (2016).
- den Hertog, A. L., et al. Candidacidal effects of two antimicrobial peptides: histatin 5 causes small membrane defects, but LL-37 causes massive disruption of the cell membrane. Biochemical Journal. 388, 689-695 (2005).
- Ikonomova, S. P., Moghaddam-Taaheri, P., Jabra-Rizk, M. A., Wang, Y., Karlsson, A. J. Engineering improved variants of the antifungal peptide histatin 5 with reduced susceptibility to Candida albicans secreted aspartic proteases and enhanced antimicrobial potency. The FEBS Journal. 285 (1), 146-159 (2018).
- Moghaddam-Taaheri, P., Leissa, J. A., Eppler, H. B., Jewell, C. M., Karlsson, A. J. Histatin 5 variant reduces Candida albicans biofilm viability and inhibits biofilm formation. Fungal Genetics and Biology. 149, 103529 (2021).
- Gong, Z., Doolin, M. T., Adhikari, S., Stroka, K. M., Karlsson, A. J. Role of charge and hydrophobicity in translocation of cell-penetrating peptides into Candida albicans cells. AIChE Journal. 65 (12), 16768 (2019).
- Gong, Z., Karlsson, A. J. Translocation of cell-penetrating peptides into Candida fungal pathogens. Protein Science. 26 (9), 1714-1725 (2017).
- Green, M. R., Sambrook, J. . Molecular Cloning: A Laboratory Manual. Fourth edition. 3, (2012).
- Consolidated Sterilizer Systems. Laboratory and Research Autoclaves Available from: https://consteril.com/wp-content/uploads/2020/12/CSS-Product-Brochure.pdf (2022)
- Rodriguez-Tudela, J. L., Cuenca-Estrella, M., Diaz-Guerra, T. M., Mellado, E. Standardization of antifungal susceptibility variables for a semiautomated methodology. Journal of Clinical Microbiology. 39 (7), 2513-2517 (2001).
- Mbuayama, K. R., Taute, H., Strmstedt, A. A., Bester, M. J., Gaspar, A. R. M. Antifungal activity and mode of action of synthetic peptides derived from the tick OsDef2 defensin. Journal of Peptide Science. 28 (5), 3383 (2022).
- Rossignol, T., Kelly, B., Dobson, C., d'Enfert, C. Endocytosis-mediated vacuolar accumulation of the human ApoE apolipoprotein-derived ApoEdpL-W antimicrobial peptide contributes to its antifungal activity in Candida albicans. Antimicrobial Agents and Chemotherapy. 55 (10), 4670-4681 (2011).
- Helmerhorst, E. J., Reijnders, I. M., van't Hof, W., Veerman, E. C., Nieuw Amerongen, A. V. A critical comparison of the hemolytic and fungicidal activities of cationic antimicrobial peptides. FEBS Letters. 449 (2-3), 105-110 (1999).
- Kerenga, B. K., et al. Salt-tolerant antifungal and antibacterial activities of the corn defensin ZmD32. Frontiers in Microbiology. 10, 795 (2019).
- Lee, I. H., Cho, Y., Lehrer, R. I. Effects of pH and salinity on the antimicrobial properties of clavanins. Infection and Immunity. 65 (7), 2898-2903 (1997).
- Li, X. S., Reddy, M. S., Baev, D., Edgerton, M. Candida albicans Ssa1/2p is the cell envelope binding protein for human salivary histatin 5. Journal of Biological Chemistry. 278 (31), 28553-28561 (2003).
- Rothstein, D. M., et al. Anticandida activity is retained in P-113, a 12-amino-acid fragment of histatin 5. Antimicrobial Agents and Chemotherapy. 45 (5), 1367-1373 (2001).
- Sanders, E. R. Aseptic laboratory techniques: Volume transfers with serological pipettes and micropipettors. Journal of Visualized Experiments. (63), e2754 (2012).
- Mansoury, M., Hamed, M., Karmustaji, R., Al Hannan, F., Safrany, S. T. The edge effect: A global problem. The trouble with culturing cells in 96-well plates. Biochemistry and Biophysics Report. 26, 100987 (2021).
- Goughenour, K. D., Balada-Llasat, J. M., Rappleye, C. A. Quantitative microplate-based growth assay for determination of antifungal susceptibility of Histoplasma capsulatum yeasts. Journal of Clinical Microbiology. 53 (10), 3286-3295 (2015).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유