É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Método de precipitação química para a síntese do Nb2O5 modificado catalisadores de níquel em massa com alta área de superfície específica
Neste Artigo
Resumo
É apresentado um protocolo para a síntese de Ni esponjoso e dobra-como1-xNbxO nanopartículas por precipitação química.
Resumo
Vamos demonstrar um método para a síntese de catalisadores de1-xO de Nb Nixcom nanoestruturas esponjoso e dobra-like. Variando a razão de Nb:Ni, uma série de NixNb1-xO nanopartículas com diferentes composições atômicas (x = 0,03, 0,08, 0,15 e 0,20) foram preparadas por precipitação química. Estes catalisadores de1-xO NixNb são caracterizadas por difração de raios x, espectroscopia de fotoelétron de raios x e microscopia eletrônica. O estudo revelou o esponjoso e dobra-como aparência de Ni0.97Nb0,03O e Ni0.92Nb0,08O na superfície NiO e a maior área de superfície de catalisadores de1-xO estes NixNb, comparado com o volume NiO. Área de superfície máxima de 173 m2/g pode ser obtida para a catalisadores O Ni0.92Nb0,08. Além disso, o hydroconversion catalítica de compostos derivados de lignina usando os sintetizado Ni0.92Nb0,08O catalisadores foram investigados.
Introdução
A preparação de nanocompósitos tem recebido atenção crescente devido à sua aplicação crucial no campo vários. Para preparar a nanopartículas de óxido de Ni-Nb-O misturado,1,2,3,4,5,6 diferentes métodos têm sido desenvolvidos como método de misturando seco,7, método de evaporação de 8 ,9,10,11,12,13 método gel sol, método de decomposição térmica de14 ,15 e autocombustão. 16 em um método de evaporação típica9, soluções aquosas contendo a quantidade adequada de metais precursores, níquel nitrato hexa-hidratado e amônio oxalato de nióbio foram aquecidos a 70 ° C. Após a remoção do solvente e mais secagem e calcinação, obteve-se o óxido misto. Estes catalisadores de óxido apresentam excelente atividade catalítica e seletividade em direção a desidrogenação oxidativa (DH) do etano, que está relacionada com o rearranjo eletrônico e estrutural induzido pela incorporação de cátions de nióbio na estrutura NiO . 11 a inserção de Nb drasticamente diminui a espécie eletrofílica oxigênio, que é responsável para as reações de oxidação de etano12. Como resultado, as extensões deste método tem sido feitas na preparação de diferentes tipos de óxidos mistos de Ni-Me-O, onde Me = Li, Mg, Al, Ga, Ti e Ta. 13 é encontrado que a variação de dopantes metais poderia alterar os radicais de oxigênio eletrofílica e unselective de NiO, assim sistematicamente sintonizar a ova atividade e seletividade para etano. No entanto, geralmente a área de superfície destes óxidos é relativamente pequeno (< 100m/2g), devido à segregação de fase estendida e a formação de grandes cristalitos de Nb2O5 e assim prejudicado seus usos em outros catalítica aplicações.
Seco, método, também conhecido como o estado sólido método de moagem, de mistura é outro método comumente usado para preparar os catalisadores de óxido misto. Desde que os materiais catalíticos são obtidos de uma forma livre de solvente, este método oferece uma alternativa promissora de verde e sustentável para a preparação de óxido misto. A maior área de superfície obtida por esse método é de 172 m2/g para Ni80Nb20 a temperatura de calcinação de 250 ° C. 8 no entanto, esse método de estado sólido não é confiável como reagentes não são misturados bem na escala atômica. Portanto, para um melhor controle de homogeneidade química e distribuição de tamanho de partículas específico e morfologia, outros métodos adequados para preparar Ni-Nb-O misturado óxido de nanopartículas ainda estão a ser procuradas. 7
Entre várias estratégias no desenvolvimento de nanopartículas, precipitação química serve como um dos métodos promissores para desenvolver o nanocatalysts, uma vez que permite a completa precipitação dos íons metálicos. Também, nanopartículas de áreas de superfície mais elevadas são comumente preparadas usando esse método. Para melhorar as propriedades catalíticas de nanopartículas de Ni-Nb-O, nós relatamos aqui o protocolo para a síntese de uma série de catalisadores de óxido Ni-Nb-O misturado com elevada área superficial pelo método de precipitação química. Temos demonstrado que a relação molar Nb:Ni é um fator crucial na determinação da atividade catalítica dos óxidos para a hydrodeoxygenation de compostos orgânicos derivados de lignina. Com alta Nb:Ni ratio acima de 0,087, formaram-se espécies6 O de2de NiNb de inativos. Ni0.92Nb0,08O, o que tinha a maior área de superfície (173 m2/g), apresenta estruturas de dobra, como nanosheets e mostrou a melhor atividade e seletividade para o hydrodeoxygenation de anisol a cicloexano.
Access restricted. Please log in or start a trial to view this content.
Protocolo
Atenção: Para a manipulação adequada de métodos, propriedades e toxicidade das substâncias químicas descritas neste documento, consulte as fichas de dados de segurança relevantes (MSDS). Alguns dos produtos químicos utilizados são tóxicos e cancerígenos e especiais cuidados devem ser tomados. Nanomateriais potencialmente podem representar riscos para a segurança e efeitos na saúde. Contato de pele e inalação deve ser evitado. Precaução deve ser exercida, como realizar a síntese do catalisador em emanações hood e catalisador de avaliação de desempenho com reatores de autoclave. Equipamentos de proteção individual é obrigatório.
1. preparação de Ni0.97Nb0,03catalisadores O onde Nb:(Ni+Nb) rácios molares igual a 0,03
- Aliam 0,161 g de hidrato de oxalato de nióbio (V) 2,821 g de nitrato de níquel em 100 mL de água desionizada num balão de 250 mL-de-pescoço-três de fundo redondo equipado com um bar de agitação.
- Agite a solução a 50 rpm e 70 ° C para dissolver os compostos até o desaparecimento do precipitado, utilizando um agitador magnético aquecimento.
- Elevar a temperatura de 80 ° C, a uma taxa de 2 ° C/min rapidamente.
- Adicione uma solução básica mista [aquoso de hidróxido de amônio (50 mL, 1,0 M) e hidróxido de sódio (50 mL, 0,2 M)] na mistura de reação gota a gota até que o pH da solução de Ni/Nb atinge 9.0.
- Agitando a mistura de reação, elevar a temperatura de 120 ° C, em 2 ° C/min.
- Agite a mistura de reação durante a noite a 50 rpm a 120 ° C até o completo desaparecimento da cor verde da solução.
- Realizar análise de espectrometria (ICP-OES) de emissão óptica-plasma indutivo para a solução avaliar a concentração dos restantes Ni2 + e Nb5 + íons na solução e assegurar a completa precipitação do níquel restante nitrato.
- Recolha o sólido por filtração utilizando balão de Büchner. Lave o sólido adicionando água 2L água deionizada repetidamente dentro de 20 min para remover o cátion at+ residual.
- Recolha o sólido em um vidro de relógio. Seca o sólido a 110 ° C, durante 12 h em forno seco.
- Calcine aquecendo os sólidos em ar sintético (20 mL/min O2 e 80 mL/min N.2) a 450 ° C por 5h em uma fornalha cilíndrica. Verifique todos os produtos vidreiros por defeito antes da utilização, alta temperatura de reação.
- Após a calcinação, obter 1 g de Ni0.97catalisador de0,03O Nb. Usar equipamento de protecção adequado como óculos de segurança, luvas, jaleco e vaporizar o capô para realizar a reação de nanocrystal devido a potenciais riscos de segurança e efeitos na saúde a nanomateriais.
2. preparação do Ni0.92Nb0,08O catalisadores onde Nb:(Ni+Nb) rácios molares igual a 0,08
- Este procedimento é semelhante de 1, exceto para as duas primeiras etapas:
- Dissolva 0,43 g de hidrato de oxalato de nióbio (V) em 100 mL de água desionizada.
- Separadamente, dissolva 2,675 g de nitrato de níquel em 100 mL de água desionizada.
3. preparação de Ni0,85Nb0.15catalisadores O onde Nb:(Ni+Nb) rácios molares igual a 0,15
- O procedimento é semelhante de 1, exceto para as duas primeiras etapas:
- Dissolva 0,807 g de hidrato de oxalato de nióbio (V) em 100 mL de água desionizada.
- Separadamente, dissolva 2,472 g de nitrato de níquel em 100 mL de água desionizada.
4. preparação de Ni0,80Nb0.20catalisadores O onde Nb:(Ni+Nb) rácios molares igual a 0,20
- O procedimento é semelhante de 1, exceto para as duas primeiras etapas:
- Dissolva 1,076 g de hidrato de oxalato de nióbio (V) em 100 mL de água desionizada.
- Separadamente, dissolva 2,326 g de nitrato de níquel em 100 mL de água desionizada.
5. preparação do Nb2O5 , usando o método de precipitação química
- Calcine ácido nióbico (Nb2O5·nH2O) em ar sintético para 5h a 450 ° C para obter puro Nb2partículas de5 O.
Nota: Confirme a conclusão da reação usando análise de difração (XRD) de pó de raio-x, onde Nb2O5·nH2O é amorfa e Nb2O5 é cristalina. De acordo com a análise, a calcinação de 5h a 450 ° C foi suficiente para completar a reação.
6. síntese de lignina de β-O-4 modelo composto, 2-(2-methoxyphenoxy)-1-phenylethan-1-one
- Dissolva bromoacetophenone (9,0 g, 45 mmol) e 2-metoxifenol (6,6 g, 53 mmol) em 200 mL de dimetilformamida (DMF) em um Erlenmeyer de 500 mL, com um agitador magnético. Use capa das emanações e de equipamentos de proteção apropriada para realizar a reação utilizando reagentes e produtos químicos corrosivos e cancerígenos.
- Misturar a solução DMF acima com hidróxido de potássio (3,0 g, 53 mmol) e agitar a mistura durante a noite a 50 rpm em temperatura ambiente usando Agitadores magnéticos.
- Extrair o produto com a solução de mistura de 200 mL de H2O e 600 mL de éter dietílico (1:3, v/v) usando funil de separação. Obter a camada superior de éter dietílico da solução.
- Adicione MgSO4 (10 g) para absorver a umidade da solução de éter dietílico. Filtre o MgSO4 para obter a solução de éter dietílico usando papel de filtro e funil.
- Após a remoção da solução de éter dietílico sob pressão reduzida em 0,08 MPa utilizando evaporador rotativo, dissolva o resíduo em 5 mL de etanol.
- Lentamente, evapore o solvente etanol para recrystallize o produto em uma proveta de 10 mL. Obter o produto (11,5 g), como pó amarelado e o rendimento do produto é de 90%, com base em bromoacetophenone. No 1análise NMR H, 1H NMR (DMSO): δ (s, 3 H, OCH3), de 3,78 5.54 (s, H 2, CH.2), ppm 6,82-8,01 (m, 9h, aromáticos). 17
7. Hydrodeoxygenation de lignina-derivado de éter aromático
Nota: O éter aromático escolhido derivados de lignina é anisole neste experimento e o catalisador é Ni0.92Nb0.08O. Utilize o equipamento de proteção adequado e coifa para realizar a reação utilizando reagentes cancerígenos.
- Equipe um reator autoclave de aço inoxidável de 50 mL com um aquecedor e um agitador magnético.
- Reduzir o Ni0.92catalisador de0,08O Nb (1g) obtido a partir do passo 2 no reator autoclave na atmosfera de2 H a 400 ° C por 2 h e em seguida passivate o catalisador sob argônio (50 mL/min) durante a noite.
- Dissolva o anisol (1,1712 g, 8% em peso) em n-decano (20 mL) com o uso de n-dodecane (0,2928 g, 2% em peso) como um padrão interno para análise quantitativa cromatografia gasosa (GC).
- Introduza os catalisadores reduzidas (0,1 g) em reator autoclave rapidamente para evitar o tempo de exposição longo, com ar (< 5 mins).
- Selo do reator autoclave, purga com H2 repetidamente (3 vezes, a 3 MPa pressão) para eliminar o ar e em seguida a mistura de reação à pressão da atmosfera.
- Defina a velocidade de agita a 700 rpm.
- Após o aquecimento à temperatura desejada em 160-210 ° C a 2 ° C/min, pressurizar o reator autoclave a 3 MPa e definir o ponto zero-tempo (t = 0).
Nota: A faixa de temperatura de 160-210 ° C é adequada neste relatório. - Posteriormente, arrefecer a mistura à temperatura ambiente de 10 ° C/min imediatamente e analisar os produtos venoso usando cromatografia em fase gasosa com detector de massa seletiva. 17
- Determine a conversão do modelo de lignina, composto de acordo com a seguinte equação:

- Determine a seletividade do produto de acordo com a seguinte equação:
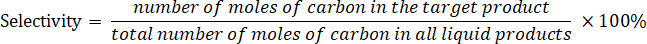
Access restricted. Please log in or start a trial to view this content.
Resultados
Padrões de difração de raios x (XRD) (Figura 1 e Figura 2), aposta áreas de superfície, redução de temperatura-programado de hidrogênio com hidrogênio (H2- TPR), microscopia eletrônica (SEM) equipado com um raio-x-energia dispersiva (EDX ), analisador de espectroscopia de fotoelétron de raios x (XPS) foram coletados para as nanopartículas NiO, Ni-Nb-O e Nb2O5 óxidos1...
Access restricted. Please log in or start a trial to view this content.
Discussão
Um dos métodos comuns para preparar as nanopartículas de óxido de nióbio em massa de níquel-dopado é método de evaporação rotativa. 9 recorrendo a diferentes condições de temperatura e pressão durante o processo de evaporação rotativa, a precipitação do comércio de partículas Ni-Nb-O com a remoção lenta do solvente. Em contraste com o método de evaporação rotativa, o método de precipitação química relatado neste estudo tem recebido atenção crescente para preparar as na...
Access restricted. Please log in or start a trial to view this content.
Divulgações
Nós não temos nada para divulgar.
Agradecimentos
Reconhecemos, com gratidão, o apoio financeiro fornecido pelo nacional chave de pesquisa & desenvolvimento de programa do Ministério da ciência e tecnologia da China (2016YFB0600305), Fundação Nacional de ciências naturais da China (n. 21573031 e 21373038), programa para excelentes talentos na cidade de Dalian (2016RD09) e educação tecnológica e maior Instituto de Hong Kong (THEi SG1617105 e THEi SG1617127).
Access restricted. Please log in or start a trial to view this content.
Materiais
| Name | Company | Catalog Number | Comments |
| Niobium(V) oxalate hydrate, 98% | Alfa | L04481902 | |
| Nickel nitrate hexahydrate, 99% | Aladdin | N108891 | |
| Sodium hydroxide, 98% | Aladdin | S111501 | |
| Ammonium hydroxide, 23-25% | Aladdin | A112077 | |
| Anisole, 99% | Sinopharm | 81001728 | |
| Diphenyl ether, 98% | Aladdin | D110644 | |
| Phenol, 98% | Sinopharm | 100153008 | |
| 2-Methoxyphenol, 98% | Sinopharm | 30114526 | |
| Vanillin, 99.5% | Sinopharm | 69024316 | |
| Potassium hydroxide, AR | Aladdin | P112284 | |
| N,N-Dimethylformamide, 99.5% | Sinopharm | 40016462 | |
| 2-Bromoacetophenone,98% | Aladdin | B103328 | |
| Diethyl ether,99.5% | Sinopharm | 10009318 | |
| Decane,98% | Aladdin | D105231 | |
| Dodecane,99% | Aladdin | D119697 | |
| Niobic acid | CBMM | 1313968 | |
| Heating and Drying Oven | DHG Series (shanghai jinghong laboratory instrument co. ltd) | ||
| Autoclave Reactor | CJF-0.05—0.1L (Dalian Tongda Equipment Technology Development Co., Ltd) | ||
| Tube furnace | SK2-1-10/12 (Luoyang Huaxulier Electric Stove Co., Ltd) | ||
| Heating magnetic stirrer | DF-101 (Yu Hua Instrument Co. Ltd.) | ||
| Rotary evaporator | RE-3000A (Shanghai Yarong Biochemical Instrument Factory) | ||
| Synthetic air | |||
| Hydrogen gas | |||
| Argon gas |
Referências
- Zhou, Y., Yang, M., Sun, K., Tang, Z., Kotov, N. A. Similar topological origin of chiral centers in organic and nanoscale inorganic structures: effect of stabilizer chirality on optical isomerism and growth of CdTe nanocrystals. J. Am. Chem. Soc. 132 (17), 6006-6013 (2010).
- Zhou, Y., et al. Optical Coupling Between Chiral Biomolecules and Semiconductor Nanoparticles: Size-Dependent Circular Dichroism Absorption. Angew. Chem. Int. Ed. 50, 11456-11459 (2011).
- Li, Z., et al. Reversible plasmonic circular dichroism of Au nanorod and DNA assemblies. J. Am. Chem. Soc. 134 (7), 3322-3325 (2012).
- Zhu, Z., et al. Manipulation of collective optical activity in one-dimensional plasmonic assembly. ACS Nano. 6 (3), 2326-2332 (2012).
- Liu, W., et al. Gold nanorod@chiral mesoporous silica core-shell nanoparticles with unique optical properties. J. Am. Chem. Soc. 135 (26), 9659-9664 (2013).
- Han, B., Zhu, Z., Li, Z., Zhang, W., Tang, Z. Conformation Modulated Optical Activity Enhancement in Chiral Cysteine and Au Nanorod Assemblies. J. Am. Chem. Soc. 136, 16104-16107 (2014).
- Rao, C. N. R., Gopalakrishnan, J. New Directions in Solid State Chemistry. , Cambridge University Press. (1989).
- Zhu, H., Rosenfeld, D. C., Anjum, D. H., Caps, V., Basset, J. -M. Green Synthesis of Ni-Nb Oxide Catalysts for Low-Temperature Oxidative Dehydrogenation of Ethane. ChemSusChem. 8, 1254-1263 (2015).
- Heracleous, E., Lemonidou, A. A. Ni-Nb-O Mixed Oxides as Highly Active and Selective Catalysts for Ethene Production via Ethane Oxidative Dehydrogenation. Part I: Characterization and Catalytic Performance. J. Cat. 237, 162-174 (2006).
- Savova, B., Loridant, S., Filkova, D., Millet, J. M. M. Ni-Nb-O Catalysts for Ethane Oxidative Dehygenation. Appl. Catal. A. 390 (1-2), 148-157 (2010).
- Heracleous, E., Delimitis, A., Nalbandian, L., Lemonidou, A. A. HRTEM Characterization of the Nanostructural Features formed in Highly Active Ni-Nb-O Catalysts for Ethane ODH. Appl. Catal. A. 325 (2), 220-226 (2007).
- Skoufa, Z., Heracleous, E., Lemonidou, A. A. Unraveling the Contribution of Structural Phases in Ni-Nb-O mixed oxides in Ethane Oxidative Dehydrogenation. Catal. Today. 192 (1), 169-176 (2012).
- Heracleous, E., Lemonidou, A. A. Ni-Me-O Mixed Metal Oxides for the Effective Oxidative Dehydrogenation of Ethane to Ethylene - Effect of Promoting Metal Me. J. Cat. 270, 67-75 (2010).
- Zhu, H., et al. Nb Effect in the Nickel Oxide-Catalyzed Low-Temperature Oxidative Dehydrogenation of Ethane. J. Cat. 285, 292-303 (2012).
- Sadovskaya, E. M., et al. Mixed Spinel-type Ni-Co-Mn Oxides: Synthesis, Structure and Catalytic Properties. Catal. Sustain. Energy. 3, 25-31 (2016).
- Alvarez, J., et al. Ni-Nb-Based Mixed Oxides Precursors for the Dry Reforming of Methane. Top. Catal. 54, 170-178 (2011).
- Jin, S., Guan, W., Tsang, C. -W., Yan, D. Y. S., Chan, C. -Y., Liang, C. Enhanced hydroconversion of lignin-derived oxygen-containing compounds over bulk nickel catalysts though Nb2O5 modification. Catal. Lett. 147, 2215-2224 (2017).
- Taghavinezhad, P., Haghighi, M., Alizadeh, R. CO2/O2-oxidative dehydrogenation of ethane to ethylene over highly dispersed vanadium oxide on MgO-promoted sulfated-zirconia nanocatalyst: Effect of sulfation on catalytic properties and performance. Korean J. Chem. Eng. 34 (5), 1346-1357 (2017).
- Muralidharan, G., Subramanian, L., Nallamuthu, S. K., Santhanam, V., Kumar, S. Effect of Reagent Addition Rate and Temperature on Synthesis of Gold Nanoparticles in Microemulsion Route. Ind. Eng. Chem. Res. 50 (14), 8786-8791 (2011).
- Sosa, Y. D., Rabelero, M., Treviño, M. E., Saade, H., López, R. G. High-Yield Synthesis of Silver Nanoparticles by Precipitation in a High-Aqueous Phase Content Reverse Microemulsion. J. Nanomater. , 1-6 (2010).
- Morterra, C., Cerrato, G., Pinna, F. Infrared spectroscopic study of surface species and of CO adsorption: a probe for the surface characterization of sulfated zirconia catalysts. Spectrochim. Acta. A Molecul. Biomolecul. Spectrosc. 55, 95-107 (1998).
- Yang, F., Wang, Q., Yan, J., Fang, J., Zhao, J., Shen, W. Preparation of High Pore Volume Pseudoboehmite Doped with Transition Metal Ions through Direct Precipitation Method. Ind. Eng. Chem. Res. 51 (47), 15386-15392 (2012).
- Saleh, R., Djaja, N. F. Transition-metal-doped ZnO nanoparticles: Synthesis, characterization and photocatalytic activity under UV light. Spectrochim. Acta. A Molecul. Biomolecul. Spectrosc. 130, 581-590 (2014).
- Ertis, I. F., Boz, I. Synthesis and Characterization of Metal-Doped (Ni, Co, Ce, Sb) CdS Catalysts and Their Use in Methylene Blue Degradation under Visible Light Irradiation. Modern Research in Catalysis. 6, 1-14 (2017).
- Jin, S., et al. Cleavage of Lignin-Derived 4-O-5 Aryl Ethers over Nickel Nanoparticles Supported on Niobic Acid-Activated Carbon Composites. Ind. Eng. Chem. Res. 54 (8), 2302-2310 (2015).
- Rojas, E., Delgado, J. J., Guerrero-Pérez, M. O., Bañares, M. A. Performance of NiO and Ni-Nb- O Active Phases during the Ethane Ammoxidation into Acetonitrile. Catal. Sci. Technol. 3 (12), 3173-3182 (2013).
- Lee, S. -H., et al. Raman Spectroscopic Studies of Ni-W Oxide Thin Films. Solid State Ionics. 140 (1), 135-139 (2001).
- Mondal, A., Mukherjee, D., Adhikary, B., Ahmed, M. A. Cobalt nanoparticles as recyclable catalyst for aerobic oxidation of alcohols in liquid phase. J. Nanopart. Res. 18 (5), 1-12 (2016).
- Wang, K., Yang, L., Zhao, W., Cao, L., Sun, Z., Zhang, F. A facile synthesis of copper nanoparticles supported on an ordered mesoporous polymer as an efficient and stable catalyst for solvent-free sonogashira coupling Reactions. Green Chem. 19, 1949-1957 (2017).
- Song, Y., et al. High-Selectivity Electrochemical Conversion of CO2 to Ethanol using a Copper Nanoparticle/N-Doped Graphene Electrode. Chemistry Select. 1, 6055-6061 (2016).
Access restricted. Please log in or start a trial to view this content.
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados