È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Modificare il metodo di precipitazione chimica per la sintesi di Nb2O5 catalizzatori di nichel Bulk con elevata superficie specifica
In questo articolo
Riepilogo
Un protocollo per la sintesi di spugnoso e piega-come Ni1-xNbxO nanoparticelle di precipitazione chimica è presentato.
Abstract
Dimostriamo un metodo per la sintesi di NixNb1-xO catalizzatori con nanostrutture spugnoso e piega-like. Variando il rapporto di Nb:Ni, una serie di NixNb1-xO nanoparticelle di varia composizione atomiche (x = 0,03, 0,08 e 0,15 0,20) sono state preparate da precipitazione chimica. Questi catalizzatori di1-xO NbxNi sono caratterizzati da diffrazione di raggi x, spettroscopia fotoelettronica a raggi x e microscopia elettronica. Lo studio ha rivelato l'aspetto spugnoso e piega-come di Ni0,97Nb0.03O e Ni0.92Nb0,08O sulla superficie NiO e la più grande superficie di questi catalizzatori di1-xO NixNb, confrontato con la maggior parte NiO. Superficie massima di 173 m2/g può essere ottenuta per catalizzatori O di Ni0.92Nb0,08. Inoltre, sono stati studiati gli idrotrattamento catalitico di lignina derivata composti utilizzando i sintetizzato Ni0.92Nb0,08O catalizzatori.
Introduzione
La preparazione dei nanocompositi ha ricevuto l'attenzione aumentante dovuto la loro applicazione cruciale in vari campi. Per preparare nanoparticelle di ossido di Ni-Nb-O miscelato,1,2,3,4,5,6 diversi metodi sono stati sviluppati come metodo di miscelazione a secco,7, metodo di evaporazione di 8 ,9,10,11,12,13 sol gel metodo, metodo di decomposizione termica di14 ,15 e auto-combustione. 16 in un tipico evaporazione metodo9, soluzioni acquose contenenti la giusta quantità di precursori metallo, nichel nitrato esaidrato e ammonio ossalato di niobio sono stati riscaldati a 70 ° C. Dopo la rimozione del solvente e ulteriore essiccazione e calcinazione, l'ossido misto è stata ottenuta. Questi catalizzatori di ossido mostrano eccellente attività catalitica e selettività verso la deidrogenazione ossidativa (ODH) di etano, imparentato con il riarrangiamento di elettronico e strutturale indotto dall'incorporazione di cationi di niobio nel reticolo NiO . 11 l'inserimento di Nb diminuisce drasticamente le specie elettrofile dell'ossigeno, che è responsabile per le reazioni di ossidazione di etano12. Di conseguenza, le estensioni di questo metodo sono state fatte sulla preparazione di diversi tipi di ossidi misti di Ni-Me-O, dove mi = Li, Mg, Al, Ga, Ti e Ta. 13 si trova che la variazione di droganti metallo potrebbe alterare i radicali dell'ossigeno non selettiva ed elettrofila di NiO, così sistematicamente sintonizzare l'ODH attività e selettività nei confronti di etano. Tuttavia, generalmente la superficie di questi ossidi è relativamente piccolo (< 100 m2/g), a causa della segregazione di fase estesa e la formazione di grandi cristalliti Nb2O5 e così ostacolato loro usi in altri catalitica applicazioni.
Secco di miscelazione metodo, noto anche come il metodo di rettifica a stato solido, è un altro metodo comunemente usato per preparare i catalizzatori di ossidi misti. Poiché i materiali catalitici sono ottenuti in modo privo di solventi, questo metodo fornisce una promettente alternativa verde e sostenibile per la preparazione di ossidi misti. La più alta superficie ottenuta con tale metodo è 172 m2/g per Ni80Nb20 temperatura calcinazione di 250 ° C. 8 tuttavia, questo metodo a stato solido non è affidabile come reagenti non sono ben miscelati su scala atomica. Di conseguenza, per un migliore controllo di omogeneità chimica e distribuzione granulometrica specifici e morfologia, altri metodi adatti per preparare Ni-Nb-O mescolato ossido nanoparticelle ancora stanno cercande. 7
Tra le varie strategie nello sviluppo delle nanoparticelle, precipitazione chimica serve come uno dei metodi promettenti per sviluppare la nanocatalisi, in quanto permette la completa precipitazione degli ioni del metallo. Inoltre, le nanoparticelle di aree di superficie superiore comunemente sono preparate utilizzando questo metodo. Per migliorare le proprietà catalitiche di Ni-Nb-O nanoparticelle, qui segnaliamo il protocollo per la sintesi di una serie di catalizzatori di ossido Ni-Nb-O mescolato con elevata superficie di metodo di precipitazione chimica. Abbiamo dimostrato che il rapporto molare di Nb:Ni è un fattore cruciale nel determinare l'attività catalitica degli ossidi verso il hydrodeoxygenation di composti organici derivati da lignina. Con rapporto di alta Nb:Ni sopra 0,087, inattivi specie NiNb2O6 sono stati formati. NI0.92Nb0,08O, che ha avuto la più grande area di superficie (173 m2/g), esposizioni nanosheets piega-come strutture e ha mostrato la migliore attività e selettività verso il hydrodeoxygenation di anisolo a cicloesano.
Access restricted. Please log in or start a trial to view this content.
Protocollo
Attenzione: Per la corretta manipolazione metodi, proprietà e tossicità dei prodotti chimici descritti in questa carta, fare riferimento alle schede di dati di sicurezza materiale (MSDS). Alcune delle sostanze chimiche utilizzate sono tossici e cancerogene e speciali cure devono essere prese. Nanomateriali potenzialmente possono rappresentare rischi per la sicurezza e gli effetti sulla salute. Inalazione e contatto dovrebbe essere evitato. Precauzione di sicurezza deve essere esercitato, ad esempio eseguendo la sintesi catalizzatore nella valutazione fume hood e catalizzatore delle prestazioni con reattori di autoclave. Dispositivi di protezione individuale devono essere indossati.
1. preparazione del Ni0,97Nb0.03catalizzatori O dove i rapporti molari Nb:(Ni+Nb) pari a 0,03
- 0,161 g di idrato di ossalato di niobio (V) si combinano con 2,821 g di nitrato di nichel in 100 mL di acqua deionizzata in un pallone da 250 mL a collo tre fondo tondo dotata di una barra per l'agitazione.
- Mescolare la soluzione a 50 rpm e 70 ° C per sciogliere i composti fino alla scomparsa del precipitato con un riscaldamento agitatore magnetico.
- Aumentare la temperatura rapidamente a 80 ° C a una velocità di 2 ° C/min.
- Aggiungere goccia a goccia una soluzione mista di base [acquosa di idrossido di ammonio (50 mL, 1.0 M) e idrossido di sodio (50 mL, 0,2 M)] nella miscela di reazione fino a quando il pH della soluzione Ni/Nb raggiunge 9.0.
- Agitando la miscela di reazione, alzare la temperatura fino a 120 ° C a 2 ° C/min.
- Mescolare la miscela di reazione durante la notte a 50 giri/min a 120 ° C fino alla completa scomparsa del colore verde della soluzione.
- Eseguire emissione ottica al plasma accoppiato induttivamente (ICP-OES) spettrometria per la soluzione valutare la concentrazione di Ni rimanenti2 + e Nb5 + ioni nella soluzione e garantire la completa precipitazione di nichel rimanenti nitrato.
- Raccogliere il solido mediante filtrazione utilizzando beuta Büchner. Lavare il solido aggiungendo acqua 2L deionizzata ripetutamente entro 20 min per rimuovere il residuo catione Na+ .
- Raccogliere il solido in un vetro da orologio. Asciugare il solido a 110 ° C per 12 h in forno secco.
- Calcine riscaldando i solidi in aria sintetica (20 mL/min O2 e 80 mL/min N2) a 450 ° C per 5 h in forno tubolare. Controllare tutta la cristalleria per difetto prima dell'uso l'alta temperatura di reazione.
- Dopo la calcinazione, ottenere 1 g di Ni0,97catalizzatore0,03O Nb. Utilizzare adeguati dispositivi di protezione come occhiali di sicurezza, guanti, camice da laboratorio e cappa aspirante per eseguire la reazione di nanocristallo a causa di potenziali rischi per la sicurezza e la salute dei nanomateriali.
2. preparazione del Ni0.92Nb0,08O catalizzatori dove rapporti molari Nb:(Ni+Nb) pari a 0,08.
- Questa procedura è simile a quella di 1 tranne che per i primi due passaggi:
- Sciogliere 0,43 g di idrato di ossalato di niobio (V) in 100 mL di acqua deionizzata.
- Separatamente, sciogliere 2,675 g di nitrato di nichel in 100 mL di acqua deionizzata.
3. preparazione di Ni0,85Nb0.15catalizzatori O dove i rapporti molari Nb:(Ni+Nb) pari a 0,15
- La procedura è simile a quella di 1 tranne che per i primi due passaggi:
- Sciogliere 0,807 g di idrato di ossalato di niobio (V) in 100 mL di acqua deionizzata.
- Separatamente, sciogliere 2,472 g di nitrato di nichel in 100 mL di acqua deionizzata.
4. preparazione di Ni0.80Nb0,20O catalizzatori dove rapporti molari Nb:(Ni+Nb) pari a 0.20
- La procedura è simile a quella di 1 tranne che per i primi due passaggi:
- Sciogliere 1,076 g di idrato di ossalato di niobio (V) in 100 mL di acqua deionizzata.
- Separatamente, sciogliere 2,326 g di nitrato di nichel in 100 mL di acqua deionizzata.
5. preparazione di Nb2O5 utilizzando il metodo di precipitazione chimica
- Calcine acido niobic (Nb2O5·nH2O) in aria sintetica per 5h a 450 ° C per ottenere puro Nb2O5 particelle.
Nota: Confermare il completamento della reazione usando analisi di diffrazione (XRD) di polvere dei raggi x, dove Nb2O5·nH2O è amorfa e Nb2O5 è cristallina. Secondo l'analisi, la calcinazione per 5h a 450 ° C è stato sufficiente per completare la reazione.
6. sintesi di lignina β-O-4 modello composto, 2-(2-methoxyphenoxy)-1-phenylethan-1-one
- Sciogliere bromoacetophenone (9,0 g, 45 mmol) e 2-metossifenolo (6,6 g, 53 mmol) in 200 mL di dimetilformammide (DMF) in una beuta da 500 mL con un agitatore magnetico. Utilizzare appropriato cappuccio protettivo dei fumi e di apparecchiature per eseguire la reazione utilizzando reagenti e prodotti chimici corrosivi e cancerogeni.
- Miscelare la soluzione DMF sopra con idrossido di potassio (3,0 g, 53 mmol) e mescolare il composto durante la notte a 50 giri/min a temperatura ambiente utilizzando agitatori magnetici.
- Estrarre il prodotto con la soluzione di miscela di 200 mL di H2O e 600 mL di etere etilico (1:3, v/v) usando l'imbuto separatore. Ottenere lo strato di etere etilico superiore della soluzione.
- Aggiungere MgSO4 (10 g) per assorbire l'umidità della soluzione di etere etilico. Filtrare il MgSO4 per ottenere la soluzione di etere etilico utilizzando carta da filtro e imbuto.
- Dopo la rimozione della soluzione di etere etilico sotto pressione ridotta a 0,08 MPa mediante evaporatore rotante, disciogliere il residuo in 5 mL di etanolo.
- Evaporare il solvente di etanolo per ricristallizzare il prodotto in un becher da 10 mL. Ottenere il prodotto (11,5 g) come polvere giallastra e la resa del prodotto è basato su bromoacetophenone il 90%. Da 1analisi H NMR, 1H NMR (DMSO): δ 3.78 (s, 3 H, OCH3), 5,54 (s, 2 H, CH2), ppm 6,82-8.01 (m, H 9, aromatico). 17
7. Hydrodeoxygenation di lignina-derivati aromatici Ether
Nota: L'etere di aromatica selezionata lignina-derivato è anisolo in questo esperimento e il catalizzatore è Ni0.92Nb0,08adeguati dispositivi di protezione O. uso e cappa per eseguire la reazione utilizzando reagenti cancerogeni.
- Equipaggiare un reattore autoclave di acciaio inox da 50 mL con una stufa e un agitatore magnetico.
- Ridurre il Ni0.92catalizzatore di0,08O Nb (1 g) ottenuto dal passaggio 2 nel reattore autoclave in atmosfera di2 H a 400 ° C per 2 h e quindi passivare il catalizzatore sotto Argon (50 mL/min) durante la notte.
- Sciogliere anisolo (g 1,1712, 8% in peso) in n-decano (20 mL) con l'uso di n-dodecano (0,2928 g, 2% in peso) come standard interno per l'analisi quantitativa gas cromatografia (GC).
- Introdurre i catalizzatori ridotti (0,1 g) nel reattore autoclave rapidamente per evitare il tempo di esposizione lungo con aria (< 5 minuti).
- Sigillare il reattore autoclave, purge con H2 più volte (3 volte, a 3 MPa pressione) per eliminare aria e quindi la miscela di reazione alla pressione dell'atmosfera.
- Impostare la velocità di agitazione a 700 rpm.
- Dopo il riscaldamento alla temperatura desiderata a 160-210 ° C a 2 ° C/min, pressurizzare il reattore autoclave a 3 MPa e impostare il punto di zero-tempo (t = 0).
Nota: La gamma di temperatura di 160-210 ° C è opportuno in questo rapporto. - Successivamente, raffreddare immediatamente la miscela a temperatura ambiente compresa tra 10 ° C/min e analizzare i prodotti deossigenati mediante gascromatografia con rivelatore di massa selettivo. 17
- Determinare la conversione del modello di lignina composto secondo la seguente equazione:

- Determinare la selettività di prodotto secondo la seguente equazione:
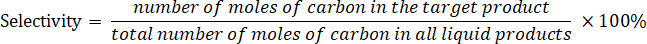
Access restricted. Please log in or start a trial to view this content.
Risultati
Modelli di diffrazione di raggi x (XRD) (Figura 1 e Figura 2), scommessa aree superficiali, temperatura programmata riduzione dell'idrogeno con l'idrogeno (H2- TPR), microscopia elettronica (SEM) equipaggiato con un energia-dispersiva dei raggi x (EDX ) analizzatore, spettroscopia fotoelettronica a raggi x (XPS) sono stati raccolti per le nanoparticelle NiO, Ni-Nb-O e Nb2O5 ossidi
Access restricted. Please log in or start a trial to view this content.
Discussione
Uno dei metodi comuni per preparare le nanoparticelle di ossido di niobio nichel-drogato alla rinfusa è metodo di evaporazione rotante. 9 impiegando varie condizioni di pressione e temperatura durante il processo di evaporazione rotativa, la precipitazione del commercio di particelle Ni-Nb-O con la lenta rimozione del solvente. In contrasto con il metodo di evaporazione rotativa, il metodo di precipitazione chimica riferito in questo studio ha ricevuto crescente attenzione per preparare le nanopa...
Access restricted. Please log in or start a trial to view this content.
Divulgazioni
Non abbiamo nulla di divulgare.
Riconoscimenti
Noi riconosciamo con gratitudine il sostegno finanziario fornito dal National Key Research & Development Program di Ministero della scienza e della tecnologia della Cina (2016YFB0600305), Fondazione nazionale di scienze naturali della Cina (nn. 21573031 e 21373038), programma per talenti eccellenti nella città di Dalian (2016RD09) e Istituto tecnologico e alta formazione di Hong Kong (THEi SG1617105 e THEi SG1617127).
Access restricted. Please log in or start a trial to view this content.
Materiali
| Name | Company | Catalog Number | Comments |
| Niobium(V) oxalate hydrate, 98% | Alfa | L04481902 | |
| Nickel nitrate hexahydrate, 99% | Aladdin | N108891 | |
| Sodium hydroxide, 98% | Aladdin | S111501 | |
| Ammonium hydroxide, 23-25% | Aladdin | A112077 | |
| Anisole, 99% | Sinopharm | 81001728 | |
| Diphenyl ether, 98% | Aladdin | D110644 | |
| Phenol, 98% | Sinopharm | 100153008 | |
| 2-Methoxyphenol, 98% | Sinopharm | 30114526 | |
| Vanillin, 99.5% | Sinopharm | 69024316 | |
| Potassium hydroxide, AR | Aladdin | P112284 | |
| N,N-Dimethylformamide, 99.5% | Sinopharm | 40016462 | |
| 2-Bromoacetophenone,98% | Aladdin | B103328 | |
| Diethyl ether,99.5% | Sinopharm | 10009318 | |
| Decane,98% | Aladdin | D105231 | |
| Dodecane,99% | Aladdin | D119697 | |
| Niobic acid | CBMM | 1313968 | |
| Heating and Drying Oven | DHG Series (shanghai jinghong laboratory instrument co. ltd) | ||
| Autoclave Reactor | CJF-0.05—0.1L (Dalian Tongda Equipment Technology Development Co., Ltd) | ||
| Tube furnace | SK2-1-10/12 (Luoyang Huaxulier Electric Stove Co., Ltd) | ||
| Heating magnetic stirrer | DF-101 (Yu Hua Instrument Co. Ltd.) | ||
| Rotary evaporator | RE-3000A (Shanghai Yarong Biochemical Instrument Factory) | ||
| Synthetic air | |||
| Hydrogen gas | |||
| Argon gas |
Riferimenti
- Zhou, Y., Yang, M., Sun, K., Tang, Z., Kotov, N. A. Similar topological origin of chiral centers in organic and nanoscale inorganic structures: effect of stabilizer chirality on optical isomerism and growth of CdTe nanocrystals. J. Am. Chem. Soc. 132 (17), 6006-6013 (2010).
- Zhou, Y., et al. Optical Coupling Between Chiral Biomolecules and Semiconductor Nanoparticles: Size-Dependent Circular Dichroism Absorption. Angew. Chem. Int. Ed. 50, 11456-11459 (2011).
- Li, Z., et al. Reversible plasmonic circular dichroism of Au nanorod and DNA assemblies. J. Am. Chem. Soc. 134 (7), 3322-3325 (2012).
- Zhu, Z., et al. Manipulation of collective optical activity in one-dimensional plasmonic assembly. ACS Nano. 6 (3), 2326-2332 (2012).
- Liu, W., et al. Gold nanorod@chiral mesoporous silica core-shell nanoparticles with unique optical properties. J. Am. Chem. Soc. 135 (26), 9659-9664 (2013).
- Han, B., Zhu, Z., Li, Z., Zhang, W., Tang, Z. Conformation Modulated Optical Activity Enhancement in Chiral Cysteine and Au Nanorod Assemblies. J. Am. Chem. Soc. 136, 16104-16107 (2014).
- Rao, C. N. R., Gopalakrishnan, J. New Directions in Solid State Chemistry. , Cambridge University Press. (1989).
- Zhu, H., Rosenfeld, D. C., Anjum, D. H., Caps, V., Basset, J. -M. Green Synthesis of Ni-Nb Oxide Catalysts for Low-Temperature Oxidative Dehydrogenation of Ethane. ChemSusChem. 8, 1254-1263 (2015).
- Heracleous, E., Lemonidou, A. A. Ni-Nb-O Mixed Oxides as Highly Active and Selective Catalysts for Ethene Production via Ethane Oxidative Dehydrogenation. Part I: Characterization and Catalytic Performance. J. Cat. 237, 162-174 (2006).
- Savova, B., Loridant, S., Filkova, D., Millet, J. M. M. Ni-Nb-O Catalysts for Ethane Oxidative Dehygenation. Appl. Catal. A. 390 (1-2), 148-157 (2010).
- Heracleous, E., Delimitis, A., Nalbandian, L., Lemonidou, A. A. HRTEM Characterization of the Nanostructural Features formed in Highly Active Ni-Nb-O Catalysts for Ethane ODH. Appl. Catal. A. 325 (2), 220-226 (2007).
- Skoufa, Z., Heracleous, E., Lemonidou, A. A. Unraveling the Contribution of Structural Phases in Ni-Nb-O mixed oxides in Ethane Oxidative Dehydrogenation. Catal. Today. 192 (1), 169-176 (2012).
- Heracleous, E., Lemonidou, A. A. Ni-Me-O Mixed Metal Oxides for the Effective Oxidative Dehydrogenation of Ethane to Ethylene - Effect of Promoting Metal Me. J. Cat. 270, 67-75 (2010).
- Zhu, H., et al. Nb Effect in the Nickel Oxide-Catalyzed Low-Temperature Oxidative Dehydrogenation of Ethane. J. Cat. 285, 292-303 (2012).
- Sadovskaya, E. M., et al. Mixed Spinel-type Ni-Co-Mn Oxides: Synthesis, Structure and Catalytic Properties. Catal. Sustain. Energy. 3, 25-31 (2016).
- Alvarez, J., et al. Ni-Nb-Based Mixed Oxides Precursors for the Dry Reforming of Methane. Top. Catal. 54, 170-178 (2011).
- Jin, S., Guan, W., Tsang, C. -W., Yan, D. Y. S., Chan, C. -Y., Liang, C. Enhanced hydroconversion of lignin-derived oxygen-containing compounds over bulk nickel catalysts though Nb2O5 modification. Catal. Lett. 147, 2215-2224 (2017).
- Taghavinezhad, P., Haghighi, M., Alizadeh, R. CO2/O2-oxidative dehydrogenation of ethane to ethylene over highly dispersed vanadium oxide on MgO-promoted sulfated-zirconia nanocatalyst: Effect of sulfation on catalytic properties and performance. Korean J. Chem. Eng. 34 (5), 1346-1357 (2017).
- Muralidharan, G., Subramanian, L., Nallamuthu, S. K., Santhanam, V., Kumar, S. Effect of Reagent Addition Rate and Temperature on Synthesis of Gold Nanoparticles in Microemulsion Route. Ind. Eng. Chem. Res. 50 (14), 8786-8791 (2011).
- Sosa, Y. D., Rabelero, M., Treviño, M. E., Saade, H., López, R. G. High-Yield Synthesis of Silver Nanoparticles by Precipitation in a High-Aqueous Phase Content Reverse Microemulsion. J. Nanomater. , 1-6 (2010).
- Morterra, C., Cerrato, G., Pinna, F. Infrared spectroscopic study of surface species and of CO adsorption: a probe for the surface characterization of sulfated zirconia catalysts. Spectrochim. Acta. A Molecul. Biomolecul. Spectrosc. 55, 95-107 (1998).
- Yang, F., Wang, Q., Yan, J., Fang, J., Zhao, J., Shen, W. Preparation of High Pore Volume Pseudoboehmite Doped with Transition Metal Ions through Direct Precipitation Method. Ind. Eng. Chem. Res. 51 (47), 15386-15392 (2012).
- Saleh, R., Djaja, N. F. Transition-metal-doped ZnO nanoparticles: Synthesis, characterization and photocatalytic activity under UV light. Spectrochim. Acta. A Molecul. Biomolecul. Spectrosc. 130, 581-590 (2014).
- Ertis, I. F., Boz, I. Synthesis and Characterization of Metal-Doped (Ni, Co, Ce, Sb) CdS Catalysts and Their Use in Methylene Blue Degradation under Visible Light Irradiation. Modern Research in Catalysis. 6, 1-14 (2017).
- Jin, S., et al. Cleavage of Lignin-Derived 4-O-5 Aryl Ethers over Nickel Nanoparticles Supported on Niobic Acid-Activated Carbon Composites. Ind. Eng. Chem. Res. 54 (8), 2302-2310 (2015).
- Rojas, E., Delgado, J. J., Guerrero-Pérez, M. O., Bañares, M. A. Performance of NiO and Ni-Nb- O Active Phases during the Ethane Ammoxidation into Acetonitrile. Catal. Sci. Technol. 3 (12), 3173-3182 (2013).
- Lee, S. -H., et al. Raman Spectroscopic Studies of Ni-W Oxide Thin Films. Solid State Ionics. 140 (1), 135-139 (2001).
- Mondal, A., Mukherjee, D., Adhikary, B., Ahmed, M. A. Cobalt nanoparticles as recyclable catalyst for aerobic oxidation of alcohols in liquid phase. J. Nanopart. Res. 18 (5), 1-12 (2016).
- Wang, K., Yang, L., Zhao, W., Cao, L., Sun, Z., Zhang, F. A facile synthesis of copper nanoparticles supported on an ordered mesoporous polymer as an efficient and stable catalyst for solvent-free sonogashira coupling Reactions. Green Chem. 19, 1949-1957 (2017).
- Song, Y., et al. High-Selectivity Electrochemical Conversion of CO2 to Ethanol using a Copper Nanoparticle/N-Doped Graphene Electrode. Chemistry Select. 1, 6055-6061 (2016).
Access restricted. Please log in or start a trial to view this content.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon