Method Article
Injeção viral esteretaxica e implantação de lente de índice de gradiente para imagem de cálcio no cérebro profundo em vivo
Neste Artigo
Erratum Notice
Resumo
Miniscópio em imagem de cálcio vivo é uma técnica poderosa para estudar dinâmica neuronal e microcircuitos em camundongos que se comportam livremente. Este protocolo descreve a realização de cirurgias cerebrais para obter uma boa imagem in vivo de cálcio usando um miniscópio.
Resumo
Um microscópio de fluorescência em miniatura (miniscópio) é uma ferramenta potente para imagens in vivo de cálcio de animais que se comportam livremente. Oferece várias vantagens em relação aos sistemas convencionais de imagem de cálcio multifótons: (1) compacto; (2) levemente ponderado; (3) acessível; e (4) permite gravar de animais que se comportam livremente. Este protocolo descreve cirurgias cerebrais para imagens de cálcio no cérebro profundo usando um sistema de gravação de miniscópio desenvolvido sob medida. O procedimento de preparação consiste em três etapas, incluindo (1) injetar estereotipicamente o vírus na região cerebral desejada de um cérebro de camundongo para rotular um subgrupo específico de neurônios com sensor de cálcio geneticamente codificado; (2) implantação de lente de gradiente-índice (GRIN) que possa retransmitir imagem de cálcio da região cerebral profunda para o sistema de miniscópio; e (3) afixar o suporte do miniscópio sobre o crânio do mouse onde o miniscópio pode ser anexado mais tarde. Para realizar imagens in vivo de cálcio, o miniscópio é preso ao suporte, e imagens neuronais de cálcio são coletadas juntamente com gravações de comportamento simultâneas. O presente protocolo cirúrgico é compatível com qualquer sistema comercial ou personalizado de imagem de fótons e dois fótons para imagens de cálcio profundo no cérebro vivo.
Introdução
A sinalização intracelular Ca2+ é um regulador essencial do crescimento celular, proliferação, diferenciação, migração, transcrição genética, secreção e apoptose1. Nos neurônios, a sinalização Ca2+ é precisamente controlada, uma vez que seu padrão espátula-temporal está relacionado a funções cruciais como excitabilidade de membrana, liberação de neurotransmissores e plasticidade sináptica2.
A imagem in vivo de cálcio é uma técnica poderosa que pode ser utilizada para decodificar a representação do circuito neural elementar aos comportamentos normais dos animais, identificar atividades neuronais aberrantes em modelos animais de distúrbios cerebrais e desvendar potenciais alvos terapêuticos que podem normalizar esses circuitos alterados. Os dois sistemas de imagem de cálcio in vivo são microscopia de fluorescência de fluorescência a laser de dois fótons 3,4,5,6 e microendoscopia miniaturizada montada na cabeça (miniscópio)7,8,9,10,11,12,13 . A microscopia convencional de dois fótons oferece vantagens de comando, como melhor resolução, menor ruído e fotobleaching mais baixo; no entanto, os animais experimentais são necessários para serem fixados na cabeça, limitando os estudos comportamentais que podem ser realizadosem 3,4,5,6. Em contrapartida, o sistema de miniscópio montado na cabeça é pequeno e portátil, tornando possível estudar uma grande variedade de testes de comportamento usando animais de comportamento livre 7,8,9,10,11,12,13.
Existem dois indicadores principais de Ca2+, indicadores químicos 5,14 e indicadores de cálcio geneticamente codificados (GECIs)15,16. A imagem ca2+ foi facilitada usando GECIs altamente sensíveis entregues com vetores virais que permitem rotulagem específica de neurônios no circuito alvo. O esforço contínuo para aumentar a sensibilidade, longevidade e capacidade de rotular até mesmo os compartimentos subcelulares torna os GECIs ideais para vários estudos de imagem de cálcio in vivo 17,18,19.
A dispersão da luz no tecido cerebral durante a imagem limita a penetração óptica em profundidade, mesmo com a microscopia de dois fótons. No entanto, a lente do Índice de Gradiente (GRIN) supera essa questão, pois a lente GRIN pode ser diretamente incorporada nos tecidos biológicos e retransmitir imagens da região cerebral profunda para o objetivo do microscópio. Ao contrário da lente convencional feita de material opticamente homogêneo e requer uma superfície em forma complicada para focar e criar imagens, o desempenho da lente GRIN é baseado em uma mudança gradual de índice de refração dentro do material da lente que alcança o foco com uma superfíciede plano 20. A lente GRIN pode ser fabricada até 0,2 mm de diâmetro. Portanto, uma lente GRIN miniaturizada pode ser implantada no cérebro profundo sem causar muito dano.
Neste artigo, é apresentado um protocolo de cirurgia completo para o cérebro profundo in vivo de imagem de cálcio. Para o propósito da demonstração, descrevemos as cirurgias cerebrais especificamente visando o córtex pré-frontal medial (mPFC) do cérebro do camundongo e a gravação de imagens in vivo de cálcio através de um sistema de miniscópio personalizado desenvolvido pelo grupo do Dr. Lin no National Institute on Drug Abuse (NIDA/IRP)7,12. O procedimento experimental envolve duas grandes cirurgias cerebrais. A primeira cirurgia é injetar estereotipicamente um vetor viral expressando GCaMP6f (um GECI) no mPFC. A segunda cirurgia é implantar a lente GRIN na mesma região cerebral. Após a recuperação dessas cirurgias cerebrais, o procedimento subsequente é fixar o suporte de miniscópio (base) no crânio do rato usando cimento dental. In vivo A imagem ca2+ pode ser realizada a qualquer momento após a montagem do miniscópio em sua base. O protocolo de cirurgia para injeção viral e implantação de lentes GRIN é compatível com qualquer sistema comercial ou personalizado de imagem de fótons e dois fótons para o cérebro profundo em imagens de cálcio vivo.
Protocolo
O protocolo experimental segue as diretrizes de cuidados com animais da Universidade de Wyoming. O camundongo utilizado neste estudo é C57BL/6J masculino de 6 meses de idade. O procedimento pode ser usado para atingir quaisquer regiões cerebrais profundas para imagens in vivo de cálcio. Aqui, para demonstração, a área cerebral alvo é o mPFC do camundongo (anterior e posterior (A/P): 1,94 mm, medial e lateral (M/L): 0,5 mm, dorsal e ventral (D/V): 1,8 mm). Este protocolo é modificado com base no protocolo21 publicado anteriormente.
1. Injeção estereotaxica do vírus no mPFC (Figura 1)
- Preparação para a cirurgia
- Esterilize todos os instrumentos cirúrgicos usando uma autoclave e coloque-os sobre uma superfície estéril.
- Prepare uma seringa de 10 μL, escorraçando-a com soro fisiológico e preenchimento com 5 μL de soro fisiológico. Fixar a seringa a uma microbomba (ver Tabela de Materiais).
- Ligue a almofada de aquecimento e mantenha a temperatura a 35 °C.
- Coloque o mouse na câmara de indução (5" x 10" x 4", comprimento x largura x altura) com 5% de isoflurane e 1 L/min de fluxo de oxigênio. Observe cuidadosamente e conte a taxa respiratória do rato. Tire o mouse assim que sua taxa respiratória diminuir para 1 respiração/s.
NOTA: A taxa de respiração do camundongo pode ser facilmente monitorada observando o movimento do músculo traseiro para baixo e para cima durante cada inalação. - Deixe que o rato se instale em uma área de bancada separada da área cirúrgica. Com um cortador de barbear, raspe o cabelo da cabeça do rato até a primeira vértebra cervical.
- Fixar o mouse no estágio estereotaxic (ver Tabela de Materiais) e fixar sua posição com barras de ouvido e clipe de nariz. Mantenha o fluxo de isoflurane para o estágio estereotaxico a 1,5% isoflurane e 0,5 L/min de fluxo de oxigênio.
- Aplique a pomada oftalmológica lubrificante em ambos os olhos com um cotonete limpo para evitar o ressecamento dos olhos durante a cirurgia. Avalie os reflexos do pedal no mouse para confirmar que o rato está totalmente anestesiado antes de iniciar a cirurgia.
- Desinfete a área sem pelos com 7,5% de solução de povidona-iodo (ver Tabela de Materiais) e 70% de etanol três vezes cada usando cotonetes estéreis.
- Injete um pequeno volume (50 μL) de 2% de lidocaína sob a pele da área sem pelos.
- Faça uma incisão de 2 cm através da pele ao longo da linha média usando um bisturi para expor a lambda e bregma do crânio.
- Remova a fáscia do crânio com a ajuda de cotonetes de algodão seco e fórceps pontiagudos.
- Após a bregma e lambda serem visíveis, use a ponta de uma rebarba de broca dentária (0,5 mm de diâmetro) para medir as coordenadas Z de bregma e lambda (ver Tabela de Materiais). Ajuste a altura do suporte do nariz até que a bregma e a lambda se deitem na mesma posição Z.
- Localize a rebarba de 0,5 mm de broca dentária em posição de A/P: 1,94 mm, M/L: 0,5 mm do bregma. Perfurar o crânio.
NOTA: Aqui, para demonstração, a região cerebral alvo é o mPFC do rato. Este protocolo pode ser usado para atingir qualquer outra região cerebral profunda. Por exemplo, se a área cerebral alvo for o Núcleo Accumbens (NAc), a posição correspondente deve ser A/P: 0,9 mm, M/L: 1,2 mm. - Remova a dura usando uma ponta de agulha de 30 G e limpe todos os pedaços de detritos ósseos usando fórceps afiados angulares de 45°.
NOTA: O sangramento é comum, pois pequenos vasos sanguíneos podem se romper durante a etapa de limpeza. Use cotonetes estéreis para parar de sangrar e aplique soro fisiológico para lavar a área. Aplique soro fisiológico na área do crânio exposto para mantê-lo úmido. - Carregue o vírus na seringa microliter usando o painel de controle da microbomba. Retire 500 nL de bolha de ar seguido por 800 nL do vírus a uma taxa de fluxo de 50 nL/s.
NOTA: Para efeito de demonstração, aqui, um sorotipo de vírus associado ao adeno 1 (AAV1) expressando GCaMP6f (um GECI), AAV1-CamKII-GCamp6f, é injetado no mPFC (ver Tabela de Materiais). O título do vírus é 2.8 x 1013 GC/mL. É 1:2 diluído em soro fisiológico antes da injeção. - Coloque a ponta da agulha na parte superior da bregma para apenas tocar a bregma e anotar a coordenada Z de bregma. Mova a agulha acima do orifício perfurado e injete 100 nL do vírus para garantir que a agulha não esteja entupida.
- Mova-se lentamente para baixo da agulha para o tecido cerebral para a coordenada Z alvo de D/V: 1,75 mm e, em seguida, mova-a ligeiramente para a coordenada Z de D/V: 1,65 mm.
NOTA: Isto é para criar um pequeno bolso para que a solução viral seja infundida. Se a região cerebral alvo for o NAc, a coordenada Z alvo correspondente de D/V deve ser de 4,2 mm e, em seguida, mover-se ligeiramente até 4,1 mm. - Use o painel de controle para definir a microbomba para injetar 500 nL do vírus na vazão de 50 nL/min. Aperte o botão RUN no painel de controle para injetar o vírus.
NOTA: A injeção levará cerca de 10 minutos. Depois que a injeção acabar, espere por mais 5-10 minutos antes de tirar a agulha do cérebro. Aplique salina frequentemente para manter a área exposta do crânio úmida durante o período de injeção. - Mova a agulha para cima e para fora do cérebro. Injete 500 nL de volume duas vezes na vazão de 50 nL/s.
NOTA: Esta etapa confirma que um volume adequado do vírus foi administrado no cérebro. Durante as primeiras 500 nL injeções, o vírus é liberado, seguido por bolhas de ar. Durante a segunda injeção de 500 nL, as bolhas de ar aparecem primeiro, seguidas por soro fisiológico. A seringa está pronta para carregar o vírus para o próximo rato. Uma vez feita a cirurgia, a seringa microlitera e a agulha são completamente limpas com acetona seguida de soro fisiológico. - Alinhe as bordas da pele e feche cuidadosamente a incisão com uma sutura (tamanho 4.0). Aplique pomada antibiótica na área costurada para prevenir infecções.
- Remova o mouse do estágio estereotaxico e devolva-o à gaiola. Coloque a gaiola em uma incubadora de 33 °C até que o mouse esteja ambulatorial.
NOTA: Geralmente leva de 10 a 15 minutos para um rato acordar da anestesia isoflurane antes de começar a se mover. - Depois que o camundongo começar a se mover, administre anti-inflamatórios não esteroides por 3 dias pós-cirúrgicos (ver Tabela de Materiais). Deixe o rato se recuperar da cirurgia por 14 dias antes de buscar a implantação das lentes GRIN.
2. Implantação de lentes GRIN no mPFC (Figura 1)
- Preparação para a cirurgia
- Prepare o fluido cerebrospinal artificial (ACSF) contendo 124 mM de NaCl, 2,5 mM de KCl, 1,25 mM de NaH2PO4, 1,2 mM de MgCl2, 25 mM de glicose, 26 mM de NaHCO3 e 2,4 mM de CaCl2.
- Esterilize todos os instrumentos cirúrgicos usando uma autoclave e coloque-os sobre uma superfície estéril.
- Ligue a almofada de aquecimento e mantenha a temperatura a 35 °C.
- Derreta 1% Agarose e mantenha-o em banho-maria a 42 °C até usar.
NOTA: A agarose derretida pode ser mantida no banho de água por algumas horas. - Desinfetar uma lente GRIN (1 mm de diâmetro, 4,38 mm de comprimento, Figura 2A) em 70% de etanol por 15 min, transfira-a para um tubo cheio de soro fisiológico para enxaguar corretamente antes de implantar.
NOTA: As lentes GRIN (ver Tabela de Materiais) são produzidas via prata e troca de íons de lítio em copos especiais, tornando-as não tóxicas e amigáveis aosneurônios 6,7. No entanto, muitas lentes GRIN comercialmente disponíveis podem lixiviar resíduos tóxicos, causando neurodegeneração, tornando-os inadequados para implantação no cérebro vivo para estudos de imagem in vivo de longo prazo. Estas lentes GRIN podem exigir revestimento com agentes biocompatíveis como parileno-C para evitar efeitos colaterais tóxicos nos neurônios vizinhos22.
- Pesar o rato e anestesia-lo por uma injeção intraperitoneal de mistura cetamina/xylazina (ver Tabela de Materiais) (Cetamina:100 mg/kg; Xylazine: 15 mg/kg).
NOTA: Um rato pesando 30 g requer 300 μL de mistura de cetamina/xylazina (Cetamina 100 mg/mL e 1,5 mg/mL) para a dose inicial e 150 μL de Cetamina (10 mg/mL) para doses adicionais durante a cirurgia. Para manter o camundongo anestesiado durante todo o processo cirúrgico, doses adicionais de Cetamina (50 mg/kg) precisam ser administradas pelo menos uma vez por hora. O estágio de anestesia do camundongo precisa ser monitorado com frequência, avaliando os reflexos dos pedais. - Raspe o cabelo da área cirúrgica com uma máquina de barbear e limpe o cabelo usando uma toalha de papel molhada.
- Coloque o mouse no estágio estereotaxico e fixe sua posição apertando o grampo do nariz e as barras de ouvido. Aplique pomada oftalmica lubrificante em ambos os olhos com um cotonete estéril. Confirme se o mouse está totalmente anestesiado avaliando os reflexos do pedal.
- Desinfete a área sem pelos com 7,5% de solução de povidona-iodo e 70% de etanol três vezes cada usando cotonetes de algodão estéreis. Administre 2 mg/kg de Dexamethasona intramuscularmente na coxa para diminuir o risco de inchaço e inflamação relacionados à cirurgia.
- Injete 50 μL de 2% de lidocaína sob a pele da área cirúrgica.
- Use uma tesoura fina para extirer uma área de pele triangular de 1,5 cm (altura) x 1,0 cm (base), do lado anterior entre os olhos para o lado posterior atrás da lambda.
- Remova o tecido periosteum do crânio usando fórceps finos, micro-lâminas e cotonetes de algodão.
NOTA: O crânio deve ser completamente limpo e seco antes de prosseguir com o próximo passo. - Aplique cianoacrilato (ver Tabela de Materiais) nas bordas da pele e conecte a pele ao crânio. Espere 5 min até o cianoacrilato see.
- Com a ajuda de uma ponta de rebarba de broca de 0,5 mm, alinhe o bregma e a lambda no mesmo plano horizontal ajustando a altura do clipe do nariz.
- Localize uma rebarba de broca dentária (1,2 mm de diâmetro) em posição de A/P: 1,94 mm, M/L: 0,8 mm do bregma. Perfurar o crânio. Remova a dura usando uma ponta de agulha de 30 G e limpe todos os pedaços de detritos ósseos usando fórceps afiados angulares de 45°.
NOTA: Estes detritos ósseos podem bloquear a etapa de aspiração subsequente se não forem completamente removidos. - Conecte uma agulha de ponta cega polida manualmente de 27 G (Figura 2B) ao suporte da agulha acoplado a um braço robótico inclinado com um ângulo de 10° (Figura 2C). Conecte a outra extremidade do suporte de agulha ao sistema de vácuo da casa.
NOTA: O braço robótico (ver Tabela de Materiais) é desenvolvido pelo grupo do Dr. Lin no NIDA/IRP e é controlado por um software de acesso aberto e desenvolvido sob medida, AutoStereota (https://github.com/liang-bo/AutoStereota)23 - Localize a ponta da agulha para tocar apenas o bregma. Defina a coordenada Z de bregma para 0 clicando no botão Bregma no AutoStereota.
- Defina o valor da entrada X para 0,8, valor de Entrada Y para 1,94, valor de entrada Z para 1.0 e clique no botão Encontrar para mover a agulha para a parte superior do orifício perfurado no crânio.
- Ajuste a posição da agulha para o centro da área de tecido cerebral exposta via AutoStereota.
NOTA: Para mover a agulha em direções laterais ou medianas, digite o valor passo e clique nos botões Lateral ou Medial no AutoStereota. Da mesma forma, para mover a agulha nas direções anterior ou posterior e dorsal ou ventral, clique nos botões Rostral ou Caudal e Dorsal ou Ventral , respectivamente. - Ligue o vácuo e comece a enxaguar a área do cérebro exposta com ACSF através de um sistema de tubulação controlado pela gravidade (ver Tabela de Materiais) conectado a uma agulha de 30 G com uma ponta dobrada. ACSF é continuamente borbulhado com uma mistura de gás de 95% O2 e 5% DE CO2 e filtrado através de um filtro de 0,2 μm.
NOTA: A vazão ACSF é de ~ 1,5 mL/min. A pressão de saída da mistura de gás é mantida em ~3 psi. - Aspirar tecido cerebral camada por camada com a ajuda do software AutoStereota (Figura 3).
NOTA: A aspiração do tecido cerebral é completada em 4 rodadas para que seja gerado um bolso de coluna (1,8 mm de profundidade e 1 mm de diâmetro).- Na sessão "zStep", clique e verifique a primeira e segunda linhas. Defina os valores da primeira linha para 0,2 e 1. Defina os valores para a segunda linha para 0,15 e 4 (Figura 3A).
- Na sessão "Mode", defina o medidor de agulha 27 e o 1.2, defina Dims 0.9. Todos os outros valores utilizam valores padrão (Figura 3A).
- Clique seqüentemente nos botões Definir, Manter Zero e Iniciar para iniciar a aspiração.
NOTA: Esta é a1ª rodada de aspiração. Os valores de entrada indicam que a profundidade da aspiração é de 0,2 mm (da coordenada Z de 0) durante a primeira etapa com 1 camada; durante a segunda etapa, a profundidade de aspiração é de 0,15 mm, continuamente repetida para 4 camadas. A resolução de aspiração é de 1,2, e o diâmetro é de 0,9 mm. Durante a aspiração, a localização instantânea da ponta da agulha pode ser monitorada através do painel gráfico de faixa. Após completar esta rodada de aspiração, é gerado um bolso de coluna com 0,8 mm de profundidade e 1 mm de diâmetro. A ponta da agulha estará de volta ao centro com a coordenada Z de 0. - Na sessão "zStep", clique e verifique a primeira e segunda linhas. Defina os valores para a primeira linha para 1 e 1. Defina os valores para a segunda linha para 0,15 e 4 (Figura 3B).
- Na sessão "Mode", mantenha todos os valores iguais à rodada anterior (Figura 3B).
- Clique seqüentemente nos botões Definir, Manter Zero e Iniciar para iniciar a aspiração.
NOTA: Esta é a2ª rodada de aspiração. Os valores de entrada indicam que a profundidade da aspiração é de 1 mm (da coordenada Z de 0) durante a primeira etapa com 1 camada; durante a segunda etapa, a profundidade de aspiração é de 0,15 mm, continuamente repetida para 4 camadas. Após completar esta rodada de aspiração, o bolso da coluna com 1,6 mm de profundidade e 1 mm de diâmetro é gerado. - Na sessão "zStep", clique e verifique apenas a primeira linha. Defina os valores da primeira linha para 1,8 e 1 (Figura 3C).
- Na sessão "Mode", defina o medidor de agulha 27 e o 2.2. Todos os outros valores permanecem os mesmos da rodada anterior (Figura 3C).
- Clique seqüentemente nos botões Definir, Manter Zero e Iniciar para iniciar a aspiração.
NOTA: Esta é a3ª rodada de aspiração. Os valores de entrada indicam que a profundidade da aspiração é de 1,8 mm (da coordenada Z de 0) com 1 camada. A resolução de aspiração é 2.2. Após completar esta rodada de aspiração, o bolso da coluna com 1,8 mm de profundidade e 1 mm de diâmetro é gerado. - Na sessão "zStep", clique e verifique apenas a primeira linha. Defina os valores da primeira linha para 1,6 e 1 (Figura 3D).
- Na sessão "Mode", defina o medidor de agulha 27 e o 2.2, defina Dims 0.6 (Figura 3D).
- Clique seqüentemente nos botões Definir, Manter Zero e Iniciar , para iniciar a aspiração.
NOTA: Esta é a4ª rodada de aspiração. O objetivo deste passo é limpar o sangue acumulado no bolso. O sangramento é comum à medida que pequenos vasos sanguíneos se rompem durante o processo de aspiração. Para limpar completamente o sangue, pare a irrigação de ACSF por 5 minutos e, em seguida, ligue a irrigação novamente. Repita a4ª rodada de aspiração várias vezes até que o bolso esteja livre de sangue. Este protocolo pode ser usado para atingir quaisquer outras regiões cerebrais profundas. Por exemplo, se a área cerebral alvo for o NAc, a coordenada Z correspondente final de D/V deve ser de 4,4 mm.
- Pare o vácuo e a irrigação do ACSF. Leve a agulha para +2 mm Z-coordinate e 0,5 mm anterior para o centro. Coloque a lente GRIN estéril de 1mm no bolso.
- Mantenha a ponta da agulha em contato com a lente GRIN exposta para garantir que a lente GRIN seja fixada no ângulo de 10°. Pressione suavemente a superfície superior da lente GRIN com papel de tecido mole estéril para garantir que a superfície inferior da lente GRIN esteja em contato com o tecido cerebral.
- Aplique a Agarose derretida na abertura entre a lente GRIN e o tecido cerebral com a ajuda de uma espátula. Depois que Agarose formar um gel, remova o excesso de Agarose usando uma micro-lâmina.
- Limpe bem o crânio com soro fisiológico e cotonetes. Deixe o crânio secar antes da aplicação subsequente de cimento dental (ver Tabela de Materiais).
- Retire bem a mistura do congelador de -20 °C. Misture o pó de cimento dentário e o líquido catalisador e aplique uma camada de cimento de resina adesiva auto-cura no crânio; primeiro, cerque a lente GRIN e, em seguida, cubra todo o crânio exposto.
- Espere 5 min e deixe-o endurecer completamente. Remova a agulha de aspiração cuidadosamente.
- Em um poço de plástico limpo, misture o pó de cimento dental, o carvão preto com o líquido, e aplique uma fina camada da mistura em cima da 1ª camada de cimento dental. Espere 5 minutos para deixá-lo endurecer.
- Proteja a lente GRIN exposta cobrindo-a com uma tampa personalizada feita de um tubo PCR (Figura 2D). Aplique cianoacrilato para fixar a tampa ao cimento dentário.
- Injete 1 mL de soro fisiológico pré-armado subcutâneamente no mouse seguido por 0,1 mg/kg de Buprenorfina. Coloque o rato de volta em sua gaiola. Coloque a gaiola em uma incubadora de 33 °C e monitore o mouse até que ele esteja ambulatorial. Geralmente leva de 20 a 40 minutos para um rato acordar da anestesia antes de começar a se mover.
- Administre anti-inflamatórios não esteroides e monitore o rato por pelo menos 3 dias pós-cirúrgicos. Deixe o rato se recuperar da cirurgia por 30 dias.
3. Afixação do suporte de miniscópio (base) ao crânio do mouse (Figura 1)
- Anestesiar o camundongo em uma câmara de indução com 5% de isoflurane e 1 L/min de fluxo de oxigênio até que sua taxa respiratória diminua para 1 respiração/s.
- Coloque o mouse no estágio estereotaxico e fixe sua posição com barras de ouvido e clipes de nariz. Manter um fluxo contínuo de isoflurane (1,5%) e oxigênio (0,5 L/min).
- Aplique pomada oftalmica em seus olhos para mantê-los úmidos. Ligue a almofada de aquecimento e mantenha a temperatura a 35 °C. Confirme se o mouse está totalmente anestesiado avaliando os reflexos do pedal.
- Remova a tampa que cobre a lente GRIN suavemente usando fórceps pontiagudas. Perfurar os resíduos secos de cianoacrilato do cimento dentário completamente usando um microdrill (ver Tabela de Materiais).
- Corte o cabelo ao redor da área de cimento dental com uma tesoura pequena. Limpe os detritos com a ajuda de um espanador de ar comprimido. Use um cotonete mergulhado em acetona para limpar a superfície superior da lente GRIN.
- Prepare o miniscópio com seu suporte (base).
- Coloque uma porca de hex #00-90 (ver Tabela de Materiais) na ranhura presente na base e aplique cianoacrilato para fixá-lo lá (Figura 2E).
- Aplique uma fita de politetrafluoroetileno (PTFE) firmemente ao redor da rosca do miniscópio e corte a fita extra (Figura 2F).
- Aperte o miniscópio até a base e use o parafuso de bloqueio para fixar o miniscópio à base (Figura 2G).
- Conecte o miniscópio ao seu cabo e ligue o software de acesso aberto e desenvolvido sob medida, NeuView (ver Tabela de Materiais).
NOTA: O software NeuView é desenvolvido sob medida para miniscópio em imagens de cálcio vivo do grupo do Dr. Lin no NIDA/IRP 7,12. É de acesso aberto (https://github.com/giovannibarbera/miniscope_v1.0). - Em NeuView, clique em Hardware, verifique LED1 e clique no botão Transmitir para ver as imagens ao vivo (Figura 4A). Para interromper a transmissão ao vivo, clique no botão Parar .
- Desira o miniscópio em um braço de retenção de miniscópio personalizado (Figura 2H) cuja posição XYZ pode ser manipulada usando controladores motorizados (Figura 2I).
- Localize o miniscópio logo acima da lente GRIN exposta e torne-o paralelo à superfície da lente. Abaixe lentamente o miniscópio em direção à lente GRIN e ajuste sua posição Z até que o melhor plano de foco seja encontrado.
NOTA: O melhor plano focal é determinado comparando várias posições Z possíveis e selecionando o plano focal com uma visualização clara da maioria dos corpos celulares. - Aplique a primeira camada de cimento dental ao redor da base do miniscópio cuidadosamente sem alterar a posição do miniscópio. Depois que o cimento for endurecido, remova suavemente o braço de retenção de forma que o miniscópio possa ficar por conta própria na cabeça do mouse.
NOTA: O cimento dental tende a encolher após o endurecimento, e arrastará o miniscópio para longe do plano de foco original. Normalmente, a posição do miniscópio Z é ligeiramente elevada acima do plano focal original antes de aplicar cimento dental para compensar a mudança potencial. - Aplique uma segunda camada de cimento dental ao redor da base para preencher todas as lacunas e garantir que não haja vazamento de luz led das lacunas. Deixe o cimento dentário endurecer.
- Remova o mouse do estágio estereotaxico. Solte o parafuso de bloqueio e desprende o miniscópio da base. Coloque uma tampa de proteção impressa em 3D na base para proteger a lente GRIN exposta e aperte o parafuso de bloqueio na base (Figura 2J).
- Coloque o rato de volta em sua gaiola.
NOTA: Geralmente leva de 10 a 15 minutos para um rato acordar da anestesia isoflurane antes de começar a se mover.
4. Montagem de miniscópios e imagem in vivo Ca2+ (Figura 1)
- Monte o miniscópio até sua base
- Anestesiar o rato brevemente na câmara de indução (5% de isoflurane e 1 L/min de fluxo de oxigênio). Coloque o mouse em uma superfície de banco limpa.
- Solte o parafuso de bloqueio com uma pequena chave de fenda, remova a tampa protetora e limpe a superfície da lente GRIN com um cotonete encharcado de acetona.
- Enrole uma fita PTFE firmemente ao redor da linha do miniscópio e fixe o miniscópio à sua base na cabeça do mouse.
- Conecte o miniscópio ao cabo (Figura 2K), ligue o Software NeuView.
- Em NeuView, clique em Hardware, verifique LED1 e clique no botão Transmitir para ver as imagens ao vivo (Figura 4A).
- Identifique o melhor plano focal ajustando a posição do miniscópio em relação à base, apertando ligeiramente ou afrouxando com a ajuda de fórceps contundentes.
NOTA: O melhor plano focal é determinado comparando vários locais possíveis e selecionando aquele com uma visualização clara da maioria dos corpos celulares. - Aperte o parafuso de travamento e coloque o mouse de volta em sua gaiola.
- No NeuView, ajuste a potência da luz LED para o nível ideal. Clique em Capturar e, em seguida, acione os botões para iniciar a gravação e aperte Stop após 150 quadros.
NOTA: A menor potência possível determina o nível ideal da potência LED para alcançar uma imagem brilhante o suficiente. O objetivo de gravar um vídeo curto é facilitar a identificação do mesmo plano focal no futuro para imagens repetitivas. - Desconecte o cabo do miniscópio. Deixe o mouse se recuperar por pelo menos 30 minutos antes de iniciar o experimento.
NOTA: Para proteger o miniscópio, normalmente, a garrafa de água e o alimentador de alimentos de arame são removidos durante este curto período de tempo. Se o mouse precisar ficar em sua gaiola doméstica por mais tempo, é recomendável fornecer gel diet comercialmente disponível (ver Tabela de Materiais) na gaiola doméstica.
- Aquisição de dados para imagem in vivo de cálcio
NOTA: A imagem in vivo de cálcio pode ser conduzida simultaneamente juntamente com quaisquer testes de comportamento que o pesquisador desejar. Para efeito de demonstração, o exemplo aqui é a imagem in vivo Ca2+ durante um teste de campo aberto. Para atingir esse objetivo, são necessários dois computadores. Um computador é equipado com software comercial (ver Tabela de Materiais) para controlar uma câmera para gravar o comportamento do mouse automaticamente. O outro computador é equipado com o NeuView para controlar o miniscópio e gravar as imagens ca2+ .- Ligue o software da câmera de comportamento (ver Tabela de Materiais) para visualizar a arena de comportamento do mouse através de uma função Livestream. Ajuste manualmente o foco da câmera superior (Figura 2L).
- Selecione Trigger/Strobe e verifique "Ativar/desativar o gatilho" (Figura 4B). Clique em Gravar botão, use Procurar para selecionar o local onde as gravações de comportamento serão salvas, selecione o formato de imagem desejado.
NOTA: A função "Trigger Control" é habilitada para permitir que a gravação de comportamento seja acionada pelo software NeuView para que os quadros de comportamento e os quadros de imagem de cálcio correspondentes sejam acoplados temporalmente. A gravação de comportamento pode ser salva em qualquer formato desejado. A gravação de comportamento é geralmente salva no formato JPEG na pasta designada. - Aproxime o mouse da arena e conecte o miniscópio ao cabo ligado ao Sistema de Aquisição de Dados (Figura 2L) (ver Tabela de Materiais). O rato é então colocado no centro da arena.
- Com a função Livestream do software NeuView, ajuste a potência LED para otimizar o brilho da imagem de cálcio.
NOTA: Para a imagem de cálcio, a taxa de quadro de gravação é de 10 quadros/s por padrão. - Em NeuView, desmarque LED1, clique em Capturar e, em seguida, acione os botões para iniciar a gravação e aperte Stop após 100 quadros.
NOTA: Isto é para gravar imagens de fundo para cerca de 100 quadros com luz LED desligada. - No software da câmera de comportamento, clique em Iniciar gravação (Figura 4C). Em NeuView, verifique LED1, clique em Capturar e, em seguida, acione os botões para iniciar a gravação. Aperte Stop após 3000 quadros.
NOTA: Isto é para registrar imagens e comportamentos de cálcio simultaneamente. O teste de campo aberto tem 15 minutos de duração, tipicamente dividido em três sessões de gravação cada uma de 5 minutos. Isto é para evitar que o miniscópio superaqueça devido ao uso contínuo. - Salve tanto as gravações de imagem de cálcio quanto de comportamento nas pastas designadas. Repita a gravação para mais duas sessões enquanto grava o plano de fundo antes de cada sessão e salve todas as gravações na pasta designada.
- Desprender miniscópio de sua base.
- Após a gravação ser concluída, desconecte o cabo do miniscópio.
- Anestesiar o rato brevemente na câmara de indução (5% isoflurane e 1L/min de fluxo de oxigênio). Coloque o mouse em uma superfície limpa e quente.
- Desaparafusar o parafuso de bloqueio na base e desprender o miniscópio da base. Coloque de volta a tampa protetora sobre a base e aperte o parafuso de bloqueio. Coloque o rato de volta em sua gaiola.
Resultados
A Figura 1 mostra o procedimento experimental esquemático, incluindo injeção viral, implantação de lentes GRIN, afixação da base do miniscópio no crânio do rato e imagem de cálcio in vivo através de um miniscópio. Todo o procedimento leva ~2 meses. A Figura 2 mostra os principais componentes descritos no protocolo para miniscópio de imagem de cálcio in vivo. A Figura 3 exibe as interfaces do software AutoStereota durante a implantação da lente GRIN. A Figura 4 exibe as interfaces do NeuView e o software de gravação de comportamento durante a imagem in vivo de cálcio.
O resultado da imagem in vivo de cálcio depende do sucesso tanto das cirurgias de injeção viral quanto de implantação de lentes GRIN. A Figura 5 mostra uma série de desfechos (ou seja, mal sucedidos, subótimos e bons) a partir de gravações in vivo de imagem de cálcio. Em casos mal sucedidos, a imagem de cálcio pode parecer escura ou brilhante, mas geralmente revela nenhum ou muito poucos neurônios ativos. Normalmente não buscamos experimentos in vivo de registro de cálcio se houver menos de cinco neurônios ativos. Uma boa imagem in vivo de cálcio normalmente revela várias centenas de neurônios ativos. Se uma gravação contém menos de cem neurônios ativos, consideramos uma gravação subótima.
Tanto em gravações subótimas quanto em boas gravações in vivo , foram realizados experimentos de imagem de cálcio, e a análise subsequente de dados foi realizada. O filme 1 mostra um representante in vivo gravação de imagem de cálcio do mouse mPFC. Vídeos de comportamento e dados de imagem de cálcio geralmente são processados separadamente. Vídeos de comportamento do mouse podem ser pontuados manualmente. Os arquivos de imagem de cálcio são processados usando a caixa de ferramentas de processamento de imagem de cálcio CaImAn24. A Figura 6 mostra um mapa celular representativo e vários traços de cálcio de uma boa gravação de imagem de cálcio in vivo .
Após a conclusão da imagem in vivo de cálcio, o passo final é confirmar se a injeção viral e a implantação das lentes GRIN ocorreram na região cerebral desejada. Para isso, o camundongo foi perfundido com soro fisiológico tamponado de fosfato (PBS), seguido por 4% de paraformaldeído (PFA). O cérebro do camundongo foi colhido, pós-fixado em 4% pfa por 12 h, e armazenado em PBS a 4 °C. O cérebro do rato foi então seccionado em fatias de 50 μm de espessura com um vibratome. As fatias cerebrais foram manchadas com DAPI e observadas sob o microscópio (não descrito no protocolo)12. Figura 7 é uma fatia cerebral do rato ~1,94 mm anterior a bregma de um rato experimental, mostrando a faixa onde a lente GRIN foi implantada. A região de fluorescência verde abaixo e ao redor da pista de lentes GRIN indica a expressão de GCaMP6f na região mPFC.
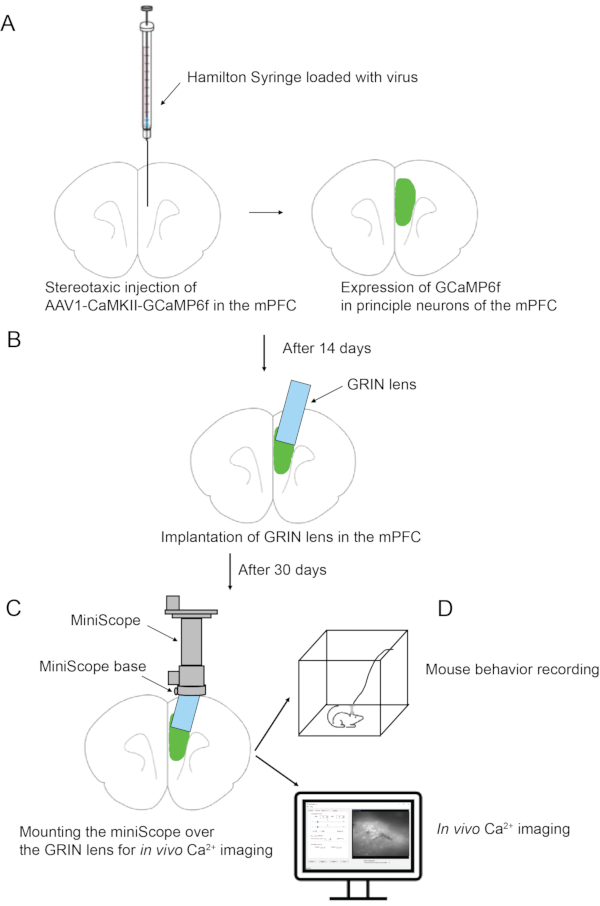
Figura 1: Visão geral esquemática do procedimento experimental. (A) Injeção estereóxica do vírus no mPFC. (B) Implantação de lentes GRIN no mPFC. (C) Base de miniscópio afixação no crânio do mouse. (D) Montagem de miniscópio e imagem de cálcio in vivo . Clique aqui para ver uma versão maior desta figura.

Figura 2: Principais componentes necessários para a imagem in vivo de cálcio. (A) Uma lente GRIN com 1 mm de diâmetro e 4,38 mm de comprimento. (B) Uma agulha de extremidade cega polida manualmente de 27 G usada para aspiração de tecido cerebral. (C) O braço robótico acoplado ao suporte de agulha. (D) Uma tampa personalizada de um tubo PCR para proteger a lente GRIN exposta até a afixação da base de miniscópio no crânio do mouse. (E) O porta-miniscópio (base) com uma porca de hex. (F) Um miniscópio cuja parte da rosca é embrulhada com a fita PTFE. (G) Um miniscópio preso à sua base com um parafuso de travamento. (H) O miniscópio segurando o braço. (I) Um controlador motorizado 3D personalizado usado para facilitar o movimento do miniscópio nas posições XYZ. (J) Uma tampa protetora presa na base para proteger a lente GRIN exposta enquanto o mouse não está realizando imagens in vivo de cálcio. (K) O miniscópio conectado ao cabo. (L) O Sistema de Aquisição de Dados para imagens in vivo Ca2 +. Clique aqui para ver uma versão maior desta figura.
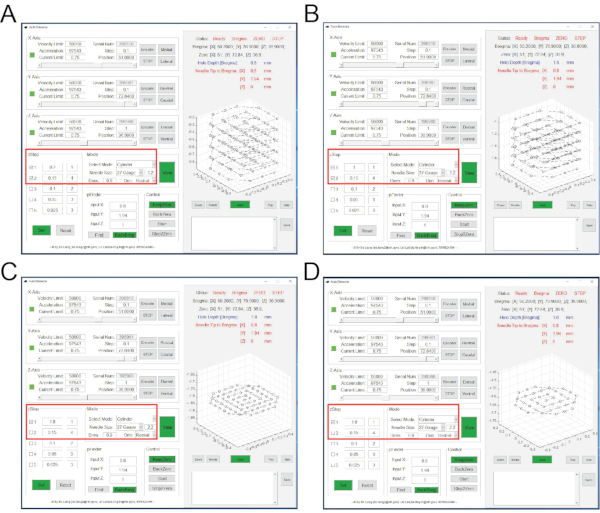
Figura 3: Interfaces do software AutoStereota durante aspiração de tecido cerebral camada por camada. (A) A interface correspondente às etapas 2.17.1 a 2.17.3. (B) A interface correspondente às etapas 2.17.4 a 2.17.6. (C) A interface correspondente às etapas 2.17.7 a 2.17.9. (D) A interface correspondente às etapas 2.17.10 a 2.17.12. As caixas vermelhas destacam os valores de entrada. Clique aqui para ver uma versão maior desta figura.
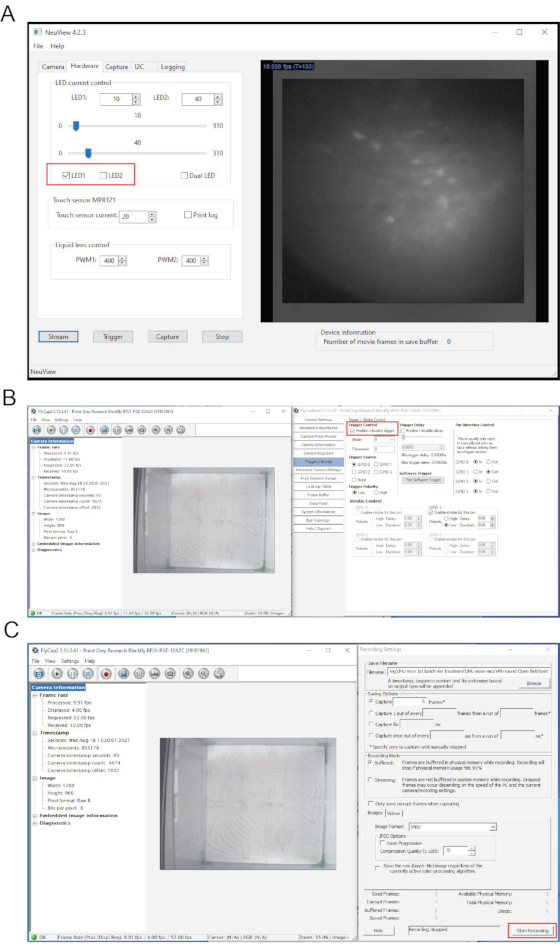
Figura 4: Interfaces do software NeuView e o software de gravação de comportamento durante a imagem in vivo de cálcio. (A) A interface do NeuView. (B,C) As interfaces do software de gravação de comportamento. Caixas vermelhas destacam botões que precisam ser clicados. Clique aqui para ver uma versão maior desta figura.
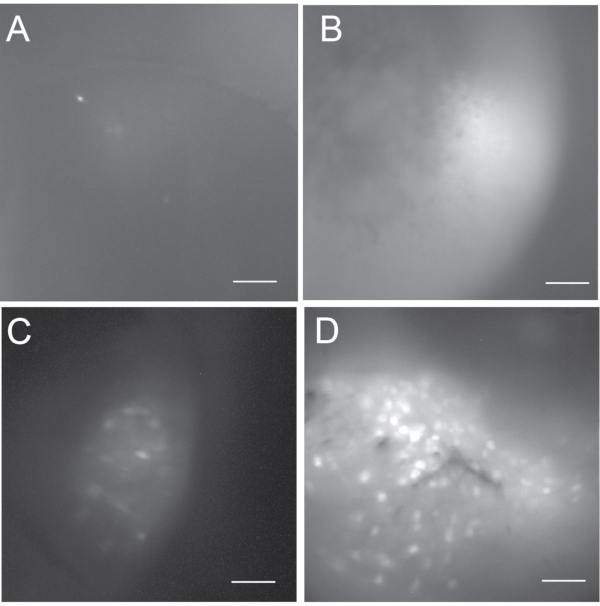
Figura 5: Mapas máximos de células de fluorescência de projeção para mostrar a gama de possíveis desfechos. (A,B) Imagens in vivo de cálcio não sucedidas que não são aceitáveis para análise de dados subsequentes. (A) é escuro e contém menos de 5 neurônios ativos. (B) é brilhante, mas não tem neurônios ativos. (C) O mapa celular de uma imagem subótima in vivo de cálcio que contém alguns neurônios ativos. (D) O mapa celular de uma boa imagem in vivo de cálcio que inclui várias centenas de neurônios ativos. Barra de escala: 100 μm. Clique aqui para ver uma versão maior desta figura.
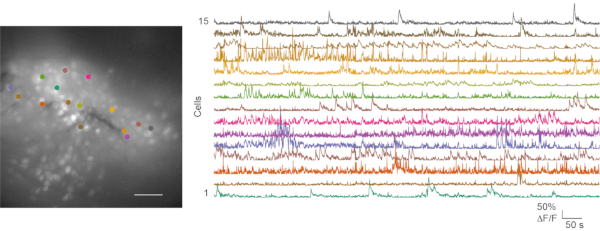
Figura 6: Mapa celular representativo e transitórios de cálcio de uma imagem de cálcio in vivo bem sucedida. O painel esquerdo é o mapa máximo da célula de fluorescência de projeção a partir de uma gravação de imagem de cálcio in vivo no mPFC durante um teste de campo aberto. A gravação dura 5 minutos. O painel direito mostra transitórios de cálcio de 15 regiões de interesse (combinadas com cores). Barra de escala: 100 μm. Clique aqui para ver uma versão maior desta figura.
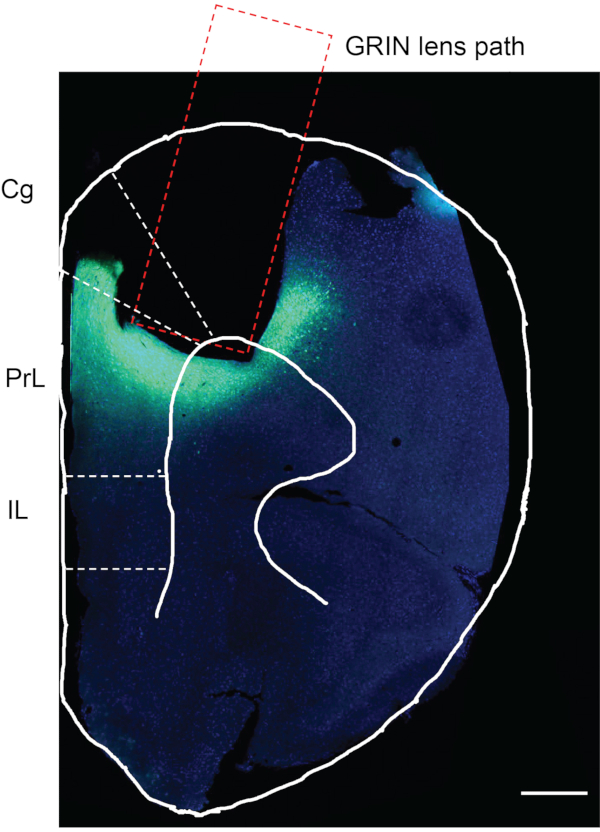
Figura 7: Avaliação pós-morte de um rato experimental. A avaliação pós-morte para expressão GCaMP6f e implantação de lentes GRIN no mPFC de um rato experimental. A área retangular indica o caminho para implantação da lente GRIN. A área verde sob a região implantada pela lente GRIN confirma que o GCaMP6f foi expresso, e a lente GRIN foi implantada precisamente na região cerebral desejada. Cg, córtex cingulado; PrL, córtex pré-limíbico; IL, córtex infralimíbido. Barra de escala: 400 μm. Clique aqui para ver uma versão maior desta figura.
Tabela 1: Comparações do sistema de miniscópio personalizado no NIDA com outros sistemas de miniscópio 7,8,9,10,11,13,25,26. Clique aqui para baixar esta Tabela.
Filme 1: Uma gravação de imagem de cálcio in vivo do mPFC do mouse durante um teste de campo aberto. Para fins de demonstração, este vídeo mostra apenas 1 min de gravação. A taxa de quadros de gravação original é de 10 quadros/s. O vídeo é 6 vezes mais rápido que a gravação original. Clique aqui para baixar este Filme.
Discussão
Uma questão central na neurociência é entender como a dinâmica neural e os circuitos codificam e armazenam informações, e como eles são alterados em doenças cerebrais. Usando um miniscópio in vivo Ca2+ sistema de imagem, a atividade neural individual de várias centenas de neurônios dentro de um microcircuito local pode ser monitorada simultaneamente a partir de um animal que se comporta livremente. Aqui, um protocolo de cirurgia detalhado para injeção viral e implantação de lentes GRIN é descrito para preparar roedores para um cérebro profundo em imagens in vivo Ca2+ através de um sistema de gravação de miniscópio desenvolvido sob medida. A Tabela 1 mostra as comparações do nosso sistema de miniscópio com outros sistemas de miniscópios disponíveis comercialmente e personalizados 7,8,9,10,11,13,25,26. Vale ressaltar que a implantação da lente GRIN usando o protocolo cirúrgico atual é compatível com qualquer sistema comercial ou personalizado de imagem de fóton único e de dois fótons para um cérebro profundo em imagens de cálcio vivo.
Da injeção viral à aquisição de dados de miniscópio em imagem de cálcio vivo , todo o procedimento experimental leva pelo menos 2 meses para ser concluído. É um processo complicado e intensivo em mão-de-obra. O sucesso final do experimento depende de múltiplos fatores, incluindo escolha adequada de GECIs, injeção de vírus com precisão na área cerebral alvo, expressão viral suficiente na população neural desejada, implantação de lente GRIN precisamente no local desejado, recuperação adequada de cirurgias, bem como, se a inflamação grave ocorre após a cirurgia, e se o comportamento do animal é severamente afetado por cirurgias, e assim por diante.
Duas etapas críticas incluem injeção estereotaxica de vírus e implantação de lentes GRIN. Para efeito de demonstração, a microinjeção estereotaxa foi realizada no mPFC do mouse, com a codificação GCaMP6f (AAV1) do vírus adeno sob o controle do promotor CaMKII que rotula seletivamente neurônios piramifecionais no mPFC. O GCaMP6f foi escolhido por ser um dos indicadores de cálcio mais rápidos e sensíveis com um tempo de meia decomposição de 71 ms15. Além disso, a expressão viral AAV de GCaMP6f é de longa duração (ou seja, vários meses), tornando-a ideal para a realização de imagens repetitivas in vivo Ca2+ durante um longo período para estudos longitudinais em modelos de camundongos de doenças neurodegenerativas27. O protocolo de cirurgia atual pode ser adaptado para atingir diferentes populações celulares em qualquer outra região cerebral. Várias ferramentas virais disponíveis permitem rotulagem seletiva de populações neurais específicas na região cerebral desejada na idade desejada. Além disso, os pesquisadores podem aproveitar o sistema de recombinação Cre-LoxP e vários modelos de camundongos transgênicos disponíveis para realizar modificações genéticas e estudar o resultado dos circuitos comportamentais e neurais28,29.
Uma característica única do protocolo apresentado é que a aspiração automatizada do tecido cerebral camada por camada foi realizada antes da implantação da lente GRIN (1 mm de diâmetro). Isso é conseguido através de uma agulha de 27 G conectada a um sistema de vácuo, controlado por um braço robótico personalizado e software23. Com base em nossa experiência, este método gera uma superfície uniforme para a lente GRIN entrar em contato e causa menos danos ao tecido vizinho do que a aspiração manual do tecido23. Por essa razão, este procedimento traz uma vantagem óbvia para as lentes GRIN com um diâmetro relativamente maior (por exemplo, 1 mm). No entanto, a aspiração tecidual pode não ser necessária para implantar uma lente GRIN com diâmetro menor (0,5 mm ou 0,25 mm). Em vez disso, pode ser diretamente plantado ao longo da pista principal feita com uma agulha de 30 G21.
Além das duas etapas críticas discutidas acima, muitos outros fatores devem ser cuidadosamente considerados para uma operação bem sucedida. (1) Todos os instrumentos que entram em contato com o cérebro devem ser esterilizados para prevenir infecções. (2) Todas as etapas da cirurgia precisam ser realizadas para minimizar os danos ao cérebro para evitar inflamações adicionais e formação excessiva de tecido cicatricial. (3) As doses de anestesia dadas inicialmente e mantidas durante a cirurgia, especialmente as administradas intraperitonealmente, precisam ser cuidadosamente consideradas. As doses de anestesia podem ser modificadas de acordo com diferentes cepas de camundongos, pois algumas podem ser mais suscetíveis. (4) A condição do camundongo precisa ser constantemente monitorada durante a cirurgia. Por fim, (5) os camundongos precisam ser monitorados regularmente após a cirurgia, pois muitas complicações podem ocorrer após a cirurgia.
Embora um pedaço de tecido cerebral seja removido unilateralmente durante a etapa de implantação das lentes GRIN, não observamos nenhum déficit de comportamento óbvio 7,12. O peso do miniscópio é de cerca de 2 gramas e o cabo é projetado sob medida para torná-lo leve e para garantir que o mouse possa carregá-lo facilmente. O miniscópio e o cabo só são ligados ao animal antes da imagem in vivo e separados após a imagem. Todo o processo de imagem geralmente não leva mais do que 30 minutos. Portanto, essas instrumentações não impedem que o mouse se comporte livremente. As etapas de instalação e desinstalação do miniscópio precisam de uma breve anestesia (menos de 2 minutos) com isoflurano para fins de contenção animal. Normalmente deixamos o rato se recuperar da breve exposição de isoflurane por 30 minutos antes de realizar imagens in vivo. Realizamos miniscópios de imagem de cálcio vivo uma vez por semana durante algumas semanas sem notar qualquer impacto na saúde do camundongo e no comportamento social do rato12.
Uma das principais limitações do sistema de gravação de miniscópios atuais é a necessidade de conectar o microscópio a um cabo para aquisição de dados. A presença do cabo às vezes restringe o desempenho da tarefa do mouse e limita a gravação de um animal por vez. Recentemente, um miniscópio sem fio foi desenvolvido25,26. Isso ampliará o desempenho da tarefa e permitirá imagens simultâneas in vivo de vários animais em um grupo. Além disso, desenvolver GECIs mais sensíveis com comprimentos de onda espectralmente separáveis combinados com um miniscópio de dupla cor oferecerá possibilidades mais interessantes para a pesquisa em neurociência.
Divulgações
Os autores não relatam interesses financeiros concorrentes.
Agradecimentos
Este trabalho é apoiado por subvenções do Instituto Nacional de Saúde (NIH) 5P20GM121310, R61NS115161 e UG3NS115608.
Materiais
| Name | Company | Catalog Number | Comments |
| 0.6mm and 1.2mm drill burrs | KF technology | 8000037800 | For craniotomy |
| 27-G and 30-G needle | BD PrecisionGlide Needle | REF 305109 and REF305106 | For both surgeries |
| 45 angled forceps | Fine Science tools | 11251-35 | For surgeries |
| 7.5% povidone-iodine solution (Betadine) | Purdue Products L.P. | NDC 67618-151-17 | Surface disinfectant |
| Acetone | Sigma-Aldrich | 179124-1L | GRIN lens cleaner |
| Agarose | Sigma-Aldrich | A9539-25G | For GRIN lens implantation |
| Antibiotic ointment | HeliDerm Technology | 81073087 | For virus injection |
| Anti-inflamatory drug (Ibuprofen) | Johnson & Johnson Consumer Inc | 30043308 | Acts as pain killer after surgeries |
| AutoStereota | NIDA/IRP | github.com/liang-bo/autostereota | For GRIN lens implantation |
| Behavior Recoding Software (Point Grey FlyCap2) | Point Grey | Point Grey Research Blackfly BFLY-PGE-12A2C | For recording behavior |
| Brass hex nut | McMASTER-CARR | 92736A112 | For GRIN lens implantation |
| Buprenorphine | Par Pharmaceuticals | NDC 4202317905 | For GRIN lens implantation |
| Calcium chloride | Sigma | 10043-52-4 | For preparing aCSF |
| Commutator | NIDA/IRP | Custom-designed | Component of image acquisition system |
| Compressed Oxygen and Caxbondioxide tank | Rocky Mountain Air Solutions | BI-OX-CD5C-K | For GRIN lens implantation |
| Compressed Oxygen tank | Rocky Mountain Air Solutions | OX-M-K | For virus injection |
| Cordless Microdrill | KF technology | 8000037800 | For craniotomy |
| Cyanoacrylate | Henkel Coorporation | # 1811182 | For GRIN lens implantation |
| Data acquisition controller | NIDA/IRP | Custom-designed | Component of image acquisition system |
| Data transmission cable | NIDA/IRP | Custom-designed | Component of image acquisition system |
| Dental cement set | C&B Metabond and Catalyst | A00253revA306 and A00168revB306 | For GRIN lens implantation |
| Dental cement set | Duralay | 2249D | For GRIN lens implantation |
| Dexamethasone | VETone | NDC 1398503702 | For GRIN lens implantation |
| Dextrose | Sigma | 50-99-7 | For preparing aCSF |
| Diet gel | Clear H20 | 72-06-5022 | Diet Supplement for mouse |
| GRIN lens | GRINTECH | NEM-100-25-10-860-S | For GRIN lens implantation |
| Heating Pad | Physitemp Instruments LLC. | #10023 | To keep the mouse body warm during surgeries |
| Isoflurane | VETone | V1 502017 | Anesthesia |
| Ketamine | VETone | V1 501072 | For GRIN lens implantation |
| Lidocaine | WEST-WARD | NDC 0143-9575-01 | Local anesthesia |
| Magnesium chloride hexahydrate | Sigma | 7791-18-6 | For preparing aCSF |
| Microliter syringe (Hamilton) | Hamilton | 7653-01 | For virus injection |
| MicroSyringe Pump Controller | World Precision Instrument | #178647 | For virus injection |
| Miniscope | NIDA/IRP | Custom-designed | For imaging |
| Miniscope base | Protolabs | Custom-designed | For mounting the base |
| Miniscope holding arm | NIDA/IRP | Custom-designed | For mounting the base |
| Miniscope protection cap | Protolabs | Custom-designed | For protecting the miniscope |
| Motorized controller | Thorlabs | KMTS50E | For mounting the base |
| NeuView | NIDA/IRP | https://github.com/giovannibarbera/miniscope_v1.0 | For in vivo imaging |
| Ophthalmic ointment | Puralube Vet Ointment | NDC 17033-211-38 | Ophthalmic |
| PCR tube | Thermo Scientific | AB-0622 | For GRIN lens implantation |
| Pinch Clamp | World Precision Instrument | 14040 | For clamping the tubing |
| Polytetrafluoroethylene (PTFE) tape | TegaSeal PTFE Tape | A-A-58092 | For fastening miniScope to the base |
| Potassium chloride | Sigma | 7447-40-7 | For preparing aCSF |
| Robotic arm | NIDA/IRP | Custom-designed | For GRIN lens implantation |
| Saline | Hospira | RL 7302 | For both surgeries |
| Set screw | DECORAH LLC. | 3BT-P9005-00-0025 | For screwing the brass hex nut in miniscope base |
| Silicone Rubber tubing, 0.062”ID, 1/8”OD | McMaster | 2124T3 | For irrigation of aCSF |
| Sodium bicarbonate | Sigma | 144-55-8 | For preparing aCSF |
| Sodium chloride | Sigma | 7647-14-5 | For preparing aCSF |
| Sodium phosphate monobasic | Sigma | 7558-80-7 | For preparing aCSF |
| Stereotaxic stage | KOPF | Model 962 Dual Ultra Precise Small Animal Stereotaxic | For both surgeries |
| Sterile cotton swab | Puritan | REF 806-WC | For both surgeries |
| Surgical tools | Fine Science tools | 11251-35 | For surgeries |
| Suture | Sofsilk | REF SS683 | For virus injection |
| Syringe filter (0.22 µm) | Millex | SLGVR33RS | For filtering aCSF during GRIN lens implantation |
| Viral suspension (AAV1-CamKII-GCamp6f) | Addgene | 100834-AAV1 | For virus injection |
| Titre: 2.8 X 10^13 GC/ml | |||
| Xylazine | VETone | V1 510650 | For GRIN lens implantation |
Referências
- Clapham, D. E. Calcium signaling. Cell. 131 (6), 1047-1058 (2007).
- Brini, M., Cali, T., Ottolini, D., Carafoli, E. Neuronal calcium signaling: function and dysfunction. Cellular and Molecular Life Sciences. 71 (15), 2787-2814 (2014).
- Chen, T. W., Li, N., Daie, K., Svoboda, K. A Map of Anticipatory Activity in Mouse Motor Cortex. Neuron. 94 (4), 866-879 (2017).
- Denk, W., Strickler, J. H., Webb, W. W. Two-photon laser scanning fluorescence microscopy. Science. 248 (4951), 73-76 (1990).
- Komiyama, T., et al. Learning-related fine-scale specificity imaged in motor cortex circuits of behaving mice. Nature. 464 (7292), 1182-1186 (2010).
- Peters, A. J., Lee, J., Hedrick, N. G., O'Neil, K., Komiyama, T. Reorganization of corticospinal output during motor learning. Nature Neuroscience. 20 (8), 1133-1141 (2017).
- Barbera, G., et al. Spatially compact neural clusters in the dorsal striatum encode locomotion relevant information. Neuron. 92 (1), 202-213 (2016).
- Cai, D. J., et al. A shared neural ensemble links distinct contextual memories encoded close in time. Nature. 534 (7605), 115-118 (2016).
- de Groot, A., et al. NINscope, a versatile miniscope for multi-region circuit investigations. Elife. 9, 49987(2020).
- Ghosh, K. K., et al. Miniaturized integration of a fluorescence microscope. Nature Methods. 8 (10), 871-878 (2011).
- Jacob, A. D., et al. A compact head-mounted endoscope for in vivo calcium imaging in freely behaving mice. Current Protocols in Neuroscience. 84 (1), 51(2018).
- Liang, B., et al. Distinct and Dynamic ON and OFF neural ensembles in the prefrontal cortex code social exploration. Neuron. 100 (3), 700-714 (2018).
- Liberti, W. A., et al. Unstable neurons underlie a stable learned behavior. Nature Neuroscience. 19 (12), 1665-1671 (2016).
- Stosiek, C., Garaschuk, O., Holthoff, K., Konnerth, A. In vivo two-photon calcium imaging of neuronal networks. Proceedings of the National Academy of Sciences of the United States of America. 100 (12), 7319-7324 (2003).
- Chen, T. W., et al. Ultrasensitive fluorescent proteins for imaging neuronal activity. Nature. 499 (7458), 295-300 (2013).
- Miyawaki, A., et al. Fluorescent indicators for Ca2+ based on green fluorescent proteins and calmodulin. Nature. 388 (6645), 882-887 (1997).
- Bassett, J. J., Monteith, G. R. Genetically encoded calcium indicators as probes to assess the role of calcium channels in disease and for high-throughput drug discovery. Advances in Pharmacology. 79, 141-171 (2017).
- Lin, M. Z., Schnitzer, M. J. Genetically encoded indicators of neuronal activity. Nature Neuroscience. 19 (9), 1142-1153 (2016).
- Tian, L., Akerboom, J., Schreiter, E. R., Looger, L. L. Neural activity imaging with genetically encoded calcium indicators. Progress in Brain Research. 196, 79-94 (2012).
- Moore, D. T. Gradient-index optics: A review. Applied Optics. 19 (7), 1035-1038 (1980).
- Zhang, L., et al. Miniscope GRIN Lens System for Calcium Imaging of Neuronal Activity from Deep Brain Structures in Behaving Animals. Current Protocols in Neuroscience. 86 (1), 56(2019).
- Yang, Y., et al. A two-step GRIN lens coating for in vivo brain imaging. Neuroscience Bulletin. 35 (3), 419-424 (2019).
- Liang, B., Zhang, L., Moffitt, C., Li, Y., Lin, D. T. An open-source automated surgical instrument for microendoscope implantation. Journal of Neuroscience Methods. 311, 83-88 (2019).
- Giovannucci, A., et al. CaImAn an open source tool for scalable calcium imaging data analysis. Elife. 8, 38173(2019).
- Barbera, G., Liang, B., Zhang, L., Li, Y., Lin, D. T. A wireless miniScope for deep brain imaging in freely moving mice. Journal of Neuroscience Methods. 323, 56-60 (2019).
- Shuman, T., et al. Breakdown of spatial coding and interneuron synchronization in epileptic mice. Nature Neuroscience. 23 (2), 229-238 (2020).
- Werner, C. T., Williams, C. J., Fermelia, M. R., Lin, D. T., Li, Y. Circuit mechanisms of neurodegenerative diseases: A new frontier with miniature fluorescence microscopy. Frontiers in Neuroscience. 13, 1174(2019).
- Brault, V., Besson, V., Magnol, L., Duchon, A., Herault, Y. Cre/loxP-mediated chromosome engineering of the mouse genome. Handbook of Experimental Pharmacology. (178), 29-48 (2007).
- McLellan, M. A., Rosenthal, N. A., Pinto, A. R. Cre-loxP-mediated recombination: General principles and experimental considerations. Current Protocols in Mouse Biology. 7 (1), 1-12 (2017).
Erratum
Formal Correction: Erratum: Stereotaxic Viral Injection and Gradient-Index Lens Implantation for Deep Brain In Vivo Calcium Imaging
Posted by JoVE Editors on 5/05/2022. Citeable Link.
An erratum was issued for: Stereotaxic Viral Injection and Gradient-Index Lens Implantation for Deep Brain In Vivo Calcium Imaging. The Discussion was updated.
The following paragraph was added to the end of the Discussion:
Although a chunk of brain tissue is removed unilaterally during the GRIN lens implantation step, we did not observe any obvious behavior deficits7,12. The weight of the miniscope is around 2 grams and the cable is custom-designed to make it light and to ensure that the mouse can easily carry it. The miniscope and cable are only attached to the animal prior to in vivo imaging and detached after imaging. The entire imaging process usually takes no longer than 30 minutes. Therefore, these instrumentations do not prevent the mouse from freely behaving. The miniscope installation and deinstallation steps need a brief anesthesia (less than 2 minutes) with isoflurane for the purpose of animal restraining. We typically let the mouse recover from the brief exposure of isoflurane for 30 minutes before performing in vivo imaging. We have performed miniscope in vivo calcium imaging once per week for a few weeks without noticing any impact on mouse health and mouse social behavior12.
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados