Method Article
Gravação e Análise da Dinâmica Multimodal de Conjuntos Neuronais em Larga Escala em Microeletrodos de Alta Densidade Integrados CMOS
Neste Artigo
Resumo
Aqui, empregamos HD-MEA para nos aprofundarmos na dinâmica computacional de conjuntos neuronais de grande escala, particularmente em hipocampo, circuitos de bulbos olfativos e redes neuronais humanas. A captura da atividade espaço-temporal, combinada com ferramentas computacionais, fornece insights sobre a complexidade do conjunto neuronal. O método melhora a compreensão das funções cerebrais, potencialmente identificando biomarcadores e tratamentos para distúrbios neurológicos.
Resumo
Redes neuronais em larga escala e seus complexos microcircuitos distribuídos são essenciais para gerar percepção, cognição e comportamento que emergem de padrões de atividade neuronal espaço-temporal. Esses padrões dinâmicos que emergem de grupos funcionais de conjuntos neuronais interconectados facilitam cálculos precisos para processar e codificar informações neurais em multiescala, impulsionando assim funções cerebrais superiores. Para investigar os princípios computacionais da dinâmica neural subjacentes a essa complexidade e investigar o impacto multiescala dos processos biológicos na saúde e na doença, gravações simultâneas em larga escala tornaram-se instrumentais. Aqui, um arranjo de microeletrodos de alta densidade (HD-MEA) é empregado para estudar duas modalidades de dinâmica neural - circuitos de bulbo hipocampal e olfatório de fatias cerebrais de camundongos ex-vivo e redes neuronais de culturas de células in vitro de células-tronco pluripotentes induzidas por humanos (iPSCs). A plataforma HD-MEA, com 4096 microeletrodos, permite gravações não invasivas, multi-site e sem rótulos de padrões de disparo extracelular de milhares de conjuntos neuronais simultaneamente em alta resolução espaço-temporal. Esta abordagem permite a caracterização de várias características eletrofisiológicas de toda a rede, incluindo padrões de atividade de spiking de uma ou várias unidades e oscilações de potencial de campo local. Para examinar esses dados neurais multidimensionais, desenvolvemos várias ferramentas computacionais incorporando algoritmos de aprendizado de máquina, detecção e classificação automática de eventos, teoria dos grafos e outras análises avançadas. Ao complementar esses pipelines computacionais com esta plataforma, fornecemos uma metodologia para estudar a dinâmica grande, multiescala e multimodal de montagens de células a redes. Isso pode potencialmente avançar nossa compreensão de funções cerebrais complexas e processos cognitivos na saúde e na doença. O compromisso com a ciência aberta e insights sobre a dinâmica neural computacional em larga escala pode melhorar a modelagem inspirada no cérebro, a computação neuromórfica e os algoritmos de aprendizagem neural. Além disso, a compreensão dos mecanismos subjacentes de computação neural em larga escala prejudicada e sua dinâmica de microcircuitos interconectados poderia levar à identificação de biomarcadores específicos, abrindo caminho para ferramentas diagnósticas mais precisas e terapias-alvo para distúrbios neurológicos.
Introdução
Conjuntos neuronais, frequentemente denominados conjuntos celulares, são fundamentais na codificação neural, facilitando cálculos intrincados para o processamento de informações neurais em multiescala 1,2,3. Esses conjuntos sustentam a formação de redes neuronais expansivas e seus microcircuitos matizados4. Tais redes e seus padrões oscilatórios conduzem funções cerebrais avançadas, incluindo percepção e cognição. Embora uma extensa pesquisa tenha explorado tipos neuronais específicos e vias sinápticas, uma compreensão mais profunda de como os neurônios formam colaborativamente conjuntos celulares e influenciam o processamento de informações espaço-temporais através de circuitos e redes permanece indefinida5.
Cortes cerebrais agudos ex-vivo são ferramentas eletrofisiológicas fundamentais para o estudo de circuitos neurais intactos, oferecendo um ambiente controlado para sondar padrões de atividade oscilatória da função neural, transmissão sináptica e conectividade, com implicações em testes farmacológicos e modelagem de doenças 6,7,8. Este protocolo de estudo destaca dois circuitos cerebrais fundamentais - o hipocampo-cortical (HC), envolvido nos processos de aprendizagem ememória9,10, e o bulbo olfatório (OB), responsável pela discriminação de odores11,12,13. Nessas duas regiões, novos neurônios funcionais são continuamente gerados pela neurogênese adulta ao longo da vida em cérebros de mamíferos14. Ambos os circuitos demonstram padrões dinâmicos multidimensionais de atividade neural e plasticidade inerente que participam da religação da rede neural existente e facilitam estratégias alternativas de processamento de informações quando necessário15,16.
Modelos de fatias cerebrais agudas e ex-vivo são indispensáveis para aprofundar a funcionalidade cerebral e entender os mecanismos da doença no nível do microcircuito. No entanto, culturas de células in vitro derivadas de redes neuronais de células-tronco pluripotentes induzidas por humanos (iPSCs) oferecem uma avenida promissora de pesquisa translacional, conectando perfeitamente achados de experimentos em animais a potenciais tratamentos clínicos humanos17,18. Esses ensaios in vitro centrados no ser humano servem como uma plataforma confiável para avaliar a toxicidade farmacológica, permitindo a triagem precisa de drogas e promovendo pesquisas sobre estratégias terapêuticas inovadoras baseadas em células19,20. Reconhecendo o papel fundamental do modelo neuronal iPSC, dedicamos o terceiro módulo deste estudo de protocolo para investigar minuciosamente as características funcionais de suas redes derivadas e ajustar os protocolos de cultura celular associados.
Esses módulos neurais eletrogênicos têm sido comumente estudados usando técnicas como imagens de cálcio (Ca2+), gravações de patch-clamp e arranjos de microeletrodos de baixa densidade (LD-MEA). Embora a imagem por Ca2+ ofereça mapeamento de atividade de célula única, é um método baseado em marcação de células dificultado por sua baixa resolução temporal e desafios em gravações de longo prazo. Os DL-MEAs carecem de precisão espacial, enquanto o patch-clamp, por ser uma técnica invasiva de sítio único e trabalhosa, frequentemente apresenta baixa taxa de sucesso 21,22,23. Para enfrentar esses desafios e sondar efetivamente a atividade em toda a rede, registros neurais simultâneos em larga escala têm emergido como uma abordagem fundamental para a compreensão dos princípios computacionais da dinâmica neural subjacente à complexidade cerebral e suas implicações na saúde e na doença24,25.
Neste protocolo JoVE, demonstramos um método de registro neural em larga escala baseado no MEA de alta densidade (HD-MEA) para capturar a atividade neuronal espaço-temporal em várias modalidades cerebrais, incluindo circuitos do bulbo hipocampal e olfatório de cortes agudos de cérebro de camundongo ex-vivo (Figuras 1A-C) e redes neuronais humanas derivadas de iPSC in vitro (Figuras 1D-E), previamente relatadas por nosso grupo e outros colegas26,27,28,29,30,31,32,33,34,35. O HD-MEA, construído sobre a tecnologia CMOS (complementary-metal-oxide-semiconductor), possui circuitos e amplificação no chip, permitindo gravações de submilissegundos em um array de 7 mm2 tamanho36. Essa abordagem não-invasiva captura padrões de disparo extracelular multissítio, livres de marcação, de milhares de conjuntos neuronais simultaneamente usando 4096 microeletrodos em alta resolução espaço-temporal, revelando a intrincada dinâmica dos potenciais de campo local (LFPs) e da atividade de spiking multiunidades (MUA)26,29.
Dada a vastidão dos dados gerados por essa metodologia, um quadro analítico sofisticado é essencial, mas impõe desafios37. Desenvolvemos ferramentas computacionais que englobam detecção automática de eventos, classificação, teoria dos grafos, aprendizado de máquina e outras técnicas avançadas (Figura 1F)26,29,38,39. Integrando o HD-MEA com essas ferramentas analíticas, uma abordagem holística é concebida para investigar a intrincada dinâmica de conjuntos de células individuais para redes neurais mais amplas em diversas modalidades neurais. Essa abordagem combinada aprofunda nossa compreensão da dinâmica computacional em funções cerebrais normais e oferece insights sobre anomalias presentes em condições patológicas28. Além disso, os insights dessa abordagem podem impulsionar avanços na modelagem inspirada no cérebro, computação neuromórfica e algoritmos de aprendizagem neural. Em última análise, este método é promissor em descobrir os principais mecanismos por trás de interrupções de redes neurais, potencialmente identificar biomarcadores e orientar a criação de ferramentas de diagnóstico precisas e tratamentos direcionados para condições neurológicas.
Protocolo
Todos os experimentos foram realizados de acordo com as regulamentações europeias e nacionais aplicáveis (Tierschutzgesetz) e foram aprovados pela autoridade local (Landesdirektion Sachsen; 25-5131/476/14).
1. Fatias cerebrais ex-vivo de circuitos hipocampal-corticais e bulbos olfativos em HD-MEA
- Preparação de soluções experimentais de corte e gravação (Figura 2A)
- No dia experimental, preparar 0,5 L de solução cortante com alto teor de sacarose e 1 L de solução de registro de líquido cefalorraquidiano artificial (aCSF) (Tabela 1A,B).
- Adicione todos os produtos químicos sólidos a um balão volumétrico seco e, em seguida, encha parte do caminho com água bidestilada (dd).
- Adicione MgCl2 e CaCl2 a partir de soluções estoque de 1 M e, em seguida, preencha o restante com água dd. Comece a mexer constantemente com um agitador magnético até que os sólidos visíveis tenham dissolvido ~5 min.
- Use um osmômetro de ponto de congelamento para validar a osmolaridade entre 350-360 mOsm para a solução de corte com alto teor de sacarose e 315-325 mOsm para a solução de registro de aCSF.
- Use um medidor de pH para validar o pH entre 7,3-7,4 para a solução de corte com alto teor de sacarose e 7,25-7,35 para a solução de registro de aCSF. Comece a borbulhar continuamente com 95% de O2 e 5% de CO2.
- Coloque a solução de corte com alto teor de sacarose no gelo por pelo menos 30 minutos antes do corte e comece a borbulhar continuamente com 95% de O2 e 5% de CO2.
- Após 10 min de carbogenação, encher um copo de 50 mL com 30 mL de solução de corte e armazená-lo no congelador (-20 °C) por 20-30 min ou até congelar parcialmente.
NOTA: Todas as soluções devem ser preparadas frescas para cada experimento. A água dd utilizada aqui é água ultrapura autoclavada armazenada à temperatura ambiente (TR). A quantidade de solução preparada deve ser adaptada à pergunta específica do estudo.
- No dia experimental, preparar 0,5 L de solução cortante com alto teor de sacarose e 1 L de solução de registro de líquido cefalorraquidiano artificial (aCSF) (Tabela 1A,B).
- Preparação das áreas de trabalho de fatias cerebrais (Figura 2A)
- Traga o animal para a sala experimental.
OBS: Neste protocolo, foram utilizados camundongos fêmeas C57BL/J6 com idade entre 8 e 16 semanas, conforme previamente descrito 26,29,32. O animal deve ser autorizado a aclimatar-se durante, pelo menos, 30 minutos após o transporte. Transferências de longa distância (ou seja, inter-instituto) devem ser evitadas no mesmo dia do experimento. A idade, o sexo e a cepa do animal devem ser determinados com base na pergunta específica do estudo. - Enquanto o animal está se aclimatando e a solução com alto teor de sacarose está esfriando, coloque as ferramentas necessárias em cada espaço de trabalho designado (consulte a Tabela de Materiais).
- Prepare o espaço de trabalho de recuperação e manutenção de fatias cerebrais. Encha a câmara de recuperação de fatias com solução de registo carbogenada, aCSF e coloque a câmara em banho-maria, regulada a 32 °C. Manter a carbogenação contínua durante todo o experimento.
- Prepare o espaço de trabalho de preparação de fatias cerebrais. Configure o vibratomo - coloque a lâmina no suporte da lâmina do vibratomo e calibre o vibratome para as configurações corretas (velocidade de deslocamento da lâmina: 0,20 mm/s, amplitude de altura: 95 μm, ângulo da lâmina: 45°). Encha a bandeja de gelo vibratome com gelo e a bandeja tampão com uma solução de corte com alto teor de sacarose e comece a carbogenar a solução na bandeja tampão.
- Prepare o espaço de trabalho de preparação do cérebro. Encha a placa de Petri de vidro de 150 mm com gelo e coloque uma placa de cultura de plástico de 90 mm com papel de filtro dentro. Encha o prato de cultura plástica com uma solução de corte com alto teor de sacarose e comece a carbogenar. Adicione uma gota de super cola à placa de amostra refrigerada e prenda o molde de agarose.
NOTA: O molde de agarose é preparado pelo menos no dia anterior com 3% de agarose em água em um molde de cérebro de camundongo personalizado. - Por fim, prepare o espaço de trabalho de extração cerebral. Cubra a folha de alumínio com papel higiênico, recupere um copo de 50 mL contendo solução de corte com alto teor de sacarose e adicione isoflurano à câmara de anestesia.
NOTA: A anestesia será adicionada à câmara de anestesia ~1 min antes da colocação do animal. Um copo de 50 mL com 30 mL de solução de corte com alto teor de sacarose será removido do freezer de -20 °C ~2 min antes da decapitação.
- Traga o animal para a sala experimental.
- Extração e fatiamento do cérebro de camundongos
OBS: Todo esse procedimento deve ser realizado o mais rápido possível para evitar a falta de oxigenação do cérebro. A remoção do cérebro deve levar apenas 1-2 minutos da decapitação para a imersão na lama da solução de corte com alto teor de sacarose.- Anestesiar o animal com a dosagem adequada de isoflurano (câmara de anestesia 0,5 mL/1 L). Determinar a profundidade da anestesia através de uma pinça na pata; Confirme a ausência de reflexo de retirada da pata antes de prosseguir.
- Transfira o animal para o papel higiênico no espaço de trabalho de extração cerebral e decapite-o com tesoura cirúrgica.
- Insira a tesoura de íris no tronco cerebral e mantenha a tesoura inferior nivelada com a calvária. Cortar ao longo da sutura sagital até atingir a sutura coronal. Coloque a tesoura de íris nas cavidades oculares e corte a sutura metópica. Use pinças curvas para mover os lados da calvária para baixo, expondo todo o cérebro.
NOTA: Tenha cuidado com a tesoura de íris e pinça para não perfurar o cérebro enquanto corta as suturas. - Deslize o cérebro com a borda romba da pinça curva para o copo de 50 mL com 30 mL de solução de corte com alto teor de sacarose. Deixe agir por 1 min.
- Transfira o cérebro para o prato de cultura de plástico de 90 mm com solução de corte carbogenada resfriada no espaço de trabalho de preparação cerebral. Orientar o cérebro para o posicionamento no molde de agarose.
- Adicione um pequeno ponto de super cola à extremidade rostral do molde de agarose. Coloque o cérebro no molde com a espátula. Certifique-se de que o cérebro é colocado com o lado dorsal para baixo para corte horizontal.
OBS: A localização da cola no molde mudará dependendo da região de interesse (ROI). Para fatias hipocampal-corticais (HC) e bulbo olfatório (OB), certifique-se de que o OB esteja estabilizado e os lados do cérebro permaneçam livres de cola. O excesso de cola afetará a qualidade do corte e causará rasgos durante o corte do vibratom. - Mova a placa da amostra para a bandeja tampão, mova a lâmina para a posição com o ângulo correto e aumente a altura da bandeja tampão para aproximar a lâmina o mais possível do cérebro.
- Cortar a uma velocidade de 0,20 mm/s intervalos de 300 μm de tecidos HC e OB e, em seguida, coletá-los após cada rodada de corte com uma pipeta de vidro Pasteur.
- Deixe as fatias na câmara de recuperação cheia de aCSF em banho-maria a 32 °C por 45 min, seguido de 1 h no TR. Certifique-se de que as fatias não se sobreponham e estejam totalmente expostas à solução carbogenada.
NOTA: Certifique-se de manter a carbogenação contínua de todas as soluções e quaisquer câmaras mencionadas que contenham a solução. Um regulador de pressão pode ser usado para sustentar uma carbogenação consistente.
2. Rede neuronal humana in-vitro baseada em iPSC em HD-MEA
NOTA: Todos os neurônios iPSC usados neste estudo são obtidos comercialmente (ver Tabela de Materiais). Essas células humanas se diferenciaram de linhagens celulares estáveis de iPS que eram derivadas de sangue periférico humano ou fibroblastos.
- Revestimento de chips HD-MEA para culturas de células iPSC humanas in vitro (Figura 2B)
- Coloque o chip HD-MEA na plataforma de gravação de aquisição, encha o reservatório com PBS e teste o chip antes do revestimento. Inicie o software Brainwave. Selecione Arquivo > Nova Sessão de Gravação. Defina os parâmetros de gravação para ter uma Frequência de Gravação de 50 Hz e uma Frequência de Amostragem de 18 kHz/eletrodo. Altere o Deslocamento do Amplificador para calibrar o chip. Consulte a Tabela 2 para obter dicas de solução de problemas.
NOTA: A frequência de gravação e os parâmetros de frequência de amostragem dependerão do tipo de dados e dos requisitos individuais do sistema. - Esterilizar e pré-condicionar HD-MEAs.
- Sob o capô, limpe o cavaco e o anel de vidro com o tecido umedecido com etanol 96% (EtOH), em seguida, coloque cada dispositivo em uma placa de Petri estéril de 100 mm x 20 mm e encha o reservatório MEA com EtOH 70% por 20 min.
- Aspirar o EtOH e lavar o reservatório com água dd filtrada estéril 3 vezes. Adicionar 1 ml de meio de pré-condicionamento e incubar durante a noite a 37 °C e 5% CO2.
NOTA: O meio de pré-condicionamento precisa ser uma solução à base de sal para tornar a superfície HD-MEA mais hidrofílica. Isso pode incluir meios completos de BrainPhys (BP) previamente preparados (não >3 meses de idade) (Tabelas 1C).
- Revestir HD-MEAs. No dia seguinte, aspirar o meio de pré-condicionamento. Adicionar 1 mL de poli-dl-ornitina (PDLO) 0,1 mg/mL para revestir toda a área ativa. Incubar a 37 °C durante a noite numa incubadora.
- Prepare e aqueça a mídia para RT. Os protocolos aqui exploram neurônios iPSC humanos funcionais de duas fontes comerciais; Assim, os componentes da mídia variam para cada fornecedor. Um protocolo está descrito em (Tabelas 1C, D) .
- Aspirar PDLO, lavar 3 vezes com dd-água e deixar os cavacos secar sob o capô por 10 min.
- Encha uma placa de Petri de 35 mm x 10 mm com água DD filtrada estéril e coloque-a ao lado do cavaco para manter a umidade adequada e evitar a evaporação das células semeadas nas próximas etapas.
- Coloque o chip HD-MEA na plataforma de gravação de aquisição, encha o reservatório com PBS e teste o chip antes do revestimento. Inicie o software Brainwave. Selecione Arquivo > Nova Sessão de Gravação. Defina os parâmetros de gravação para ter uma Frequência de Gravação de 50 Hz e uma Frequência de Amostragem de 18 kHz/eletrodo. Altere o Deslocamento do Amplificador para calibrar o chip. Consulte a Tabela 2 para obter dicas de solução de problemas.
- Plating e manutenção de neurônios iPSC humanos em HD-MEAs (Figura 2B)
- Descongelar e diluir as células para as células desejadas por concentração de microlitro (ou seja, 1000 células/μL para obter 50.000 células de densidade em uma queda de 50 μL no HD-MEA) (Tabela 1C).
- Pipetar a suspensão celular na superfície da área ativa do cavaco usando meio pontilhado de alta laminina (Tabela 1D).
- Incubar a 37 °C com 5% de CO2 durante 45-60 min.
- Encher suavemente 2 mL de meio no reservatório HD-MEA (Tabela 1C).
- Realizar 100% de troca de mídia no dia 1 (DIV1) pós-semeadura usando mídia RT (Tabela 1C). Mude 50% da mídia a cada 3-4 dias. Manter HD-MEAs incubados a 37 °C com 5% de CO2 durante todo o experimento.
NOTA: Pipetar suavemente para evitar o deslocamento das células. Verifique a cor da mídia para verificar se há alguma contaminação. O intervalo e a quantidade de mudança de mídia podem ser determinados por perguntas de estudo individuais ou necessidades/especificações da célula. - Opcional: Verificar o progresso do crescimento da cultura celular entre DIV4-DIV8 em microscópio de contraste de interferência diferencial (DIC) vertical após limpeza do estágio com EtOH >70%.
3. Registros neurais em larga escala ex-vivo e in vitro com HD-MEAs
- Preparação do espaço de trabalho de gravação de fatias cerebrais (Figura 2A)
- Enquanto as fatias cerebrais estão se recuperando, coloque as ferramentas necessárias em cada espaço de trabalho designado (consulte Tabela de Materiais).
NOTA: A configuração principal do sistema deve ser otimizada e testada bem antes do dia experimental da fatia cerebral. O sistema de perfusão (linhas de entrada, linhas de saída da bomba, tubulação e aterramento) precisa ser testado com PBS ou aCSF e um HD-MEA na plataforma de gravação para garantir um sinal limpo, aumento da relação sinal-ruído e ausência de ruído de perfusão. - Revestir o chip HD-MEA com 0,1 mg/mL de PDLO para melhorar o acoplamento tecido-chip e incubar a 37 °C por 20 min.
- Durante a incubação do chip, preencha o sistema de perfusão baseado em gravidade e as linhas com registro de aCSF. Garantir a carbogenação contínua do sistema de perfusão. Definir um caudal de 4,5 ml/min e uma temperatura de 37 °C.
- Coloque o chip HD-MEA na plataforma de gravação de aquisição, encha o reservatório com aCSF, teste o sistema de perfusão e solucione qualquer ruído restante do sistema.
- Inicie o software Brainwave. Selecione Arquivo > Nova Sessão de Gravação. Defina os parâmetros de gravação para ter uma Frequência de Gravação de 1 Hz e uma Frequência de Amostragem de 14 kHz/eletrodo. Altere o Deslocamento do Amplificador para calibrar o chip. Consulte a Tabela 2 para obter dicas de solução de problemas.
NOTA: A frequência de gravação e os parâmetros de frequência de amostragem dependerão do tipo de dados e dos requisitos individuais do sistema.
- Inicie o software Brainwave. Selecione Arquivo > Nova Sessão de Gravação. Defina os parâmetros de gravação para ter uma Frequência de Gravação de 1 Hz e uma Frequência de Amostragem de 14 kHz/eletrodo. Altere o Deslocamento do Amplificador para calibrar o chip. Consulte a Tabela 2 para obter dicas de solução de problemas.
- Verifique se a área de gravação está escura através de um sistema de iluminação da sala ou de uma gaiola sombreada na mesa óptica.
- Alinhar o estereomicroscópio com o reservatório do chip HD-MEA e a área ativa para aquisição da imagem.
- Coloque a âncora no reservatório do cavaco para equilibrar.
OBS: A âncora é uma harpa de platina feita sob medida com o mínimo de fios para promover a oxigenação; no entanto, alguns comerciais estão disponíveis. - Adicionar compostos farmacológicos aos tubos de perfusão apropriados.
NOTA: Neste protocolo, foram obtidos registros espontâneos e 100 μM de 4-aminopiridina (4-AP) induzidos farmacologicamente, conforme descrito anteriormente. Os compostos farmacológicos podem ser adaptados à questão específica do estudo. - No espaço de trabalho de preparação de fatias cerebrais, coloque um novo prato de cultura de plástico de 90 mm em uma placa de Petri de vidro de 150 mm. Adicione aCSF e comece a carbogenar.
- Enquanto as fatias cerebrais estão se recuperando, coloque as ferramentas necessárias em cada espaço de trabalho designado (consulte Tabela de Materiais).
- Gravações em todo o circuito de fatias de HC e OB usando HD-MEAs
NOTA: O acoplamento de corte deve ser realizado o mais rápido possível para evitar a falta de oxigenação ao corte. O acoplamento deve levar apenas ~1 min desde a colocação inicial do corte microdissecado na área ativa do chip até a inicialização final do sistema de perfusão.- Retire a fatia da câmara de recuperação de fatias cerebrais com uma pipeta de vidro e coloque-a em uma placa de cultura plástica de 90 mm com carbogenação contínua. Usando uma ferramenta de microdissecção, isole o HC ou OB do tecido de corte cerebral circundante.
- Mova os cortes agudos isolados de HC ou OB com uma pipeta de vidro para o reservatório HD-MEA. Alinhe suavemente a fatia na área ativa do MEA com um pincel fino. Suck todas as soluções do chip HD-MEA bem com um sistema de aspiração.
- Coloque a âncora suavemente em cima da fatia usando pinças.
OBS: A âncora deve ser colocada sem movimento de corte para evitar a perda do acoplamento. - Adicione delicadamente a solução ao reservatório do cavaco e inicie o sistema de perfusão.
NOTA: Garanta o fluxo laminar da entrada de perfusão e da saída da bomba para obter os parâmetros de gravação ideais. - Certifique-se de que a área de gravação esteja adequadamente esmaecida através do sistema de iluminação da sala ou com uma gaiola sombreada em uma configuração de mesa óptica.
- Deixe a fatia se aclimatar por 10 minutos antes de iniciar as gravações ou a modulação farmacológica adicional.
- Inicie o software Brainwave. Selecione Arquivo > Nova Sessão de Gravação. Defina os parâmetros de gravação para ter uma Frequência de Gravação de 1 Hz e uma Frequência de Amostragem de 14 kHz/eletrodo. Altere o Deslocamento do Amplificador para calibrar o chip.
NOTA: Conforme indicado anteriormente na seção 3.1.4.1, ao executar testes do sistema, certifique-se de aplicar esses mesmos parâmetros de gravação. - Pressione Record para iniciar a aquisição com as condições experimentais predefinidas.
- Imediatamente após a gravação final, capture imagens leves da fatia cerebral aguda. Mova a fatia de volta para a câmara de recuperação de fatia, remova qualquer material orgânico acoplado ao cavaco com um pincel e continue com a próxima fatia. Limpe os HD-MEAs conforme descrito na secção 3.4.
- Preparação do espaço de trabalho de gravação iPSC humano e gravações em toda a rede em HD-MEA (Figura 2B)
NOTA: Alterar a mídia no dia anterior à gravação ou imediatamente após a gravação iPSC humana (Tabela 1C). Nos estudos que utilizaram os neurônios funcionais, a mídia foi trocada a cada 4 dias, e em 4, 8, 16 e 24 meios DIV são trocados imediatamente após os registros iPSC.- Garanta um ambiente de trabalho estéril limpando a plataforma de aquisição HD-MEA com >70% EtOH.
- Coloque delicadamente uma tampa à base de polidimetilsiloxano (PDMS) com referência no anel HD-MEA sob o capô. Mova o chip HD-MEA para o espaço de trabalho de gravação iPSC e conecte o chip HD-MEA à plataforma de aquisição.
- Certifique-se de que a área de gravação está adequadamente esmaecida através de um sistema de iluminação da sala ou de uma gaiola sombreada em uma mesa óptica.
- Permita que o chip HD-MEA se equilibre por 10 minutos antes de iniciar as gravações ou a modulação farmacológica adicional.
- Inicie o software Brainwave. Selecione Arquivo > Nova Sessão de Gravação. Defina os parâmetros de gravação para ter uma Frequência de Gravação de 50 Hz e uma Frequência de Amostragem de 18 kHz/eletrodo. Altere o Deslocamento do Amplificador para calibrar o chip.
NOTA: Conforme indicado anteriormente na secção 2.1.1, ao efectuar um ensaio do sistema antes do revestimento e chapeamento, certifique-se de que aplica estes mesmos parâmetros de registo. - Registrar a atividade de disparo espontâneo ou as respostas farmacologicamente induzidas da rede iPSC humana em cada dia do plano experimental (ou seja, 4, 8, 16, 24 DIVs).
NOTA: Não deixe o chip permanecer fora da incubadora por >30 min para manter a temperatura e a umidade estáveis e evitar qualquer choque de temperatura nas células. - Incubar HD-MEAs a 37 °C com 5% de CO2 ao longo do experimento.
- Após a conclusão do experimento, corrija a rede neuronal em chips e core para obter imagens ópticas adicionais ou limpe os HD-MEAs diretamente, conforme descrito na etapa 3.4.
- Limpeza de chips HD-MEA
- Após o experimento, descartar a solução de acordo com o descarte adequado dos resíduos e enxaguar com água-dd.
- Adicione o detergente de sua preferência, limpe a área ativa e todo o reservatório com uma ponta Q e descarte o detergente. Reabasteça com detergente, incube por 20 minutos e, em seguida, descarte detergente.
- Enxágue abundantemente com água de grau laboratorial. Em seguida, enxágue 3-4 vezes com dd-água.
- Use a pressão do ar para secar completamente o chip HD-MEA.
4. Análise de registros neurais em larga escala de HD-MEAs
NOTA: Enquanto a etapa 4.1 é específica do software Brainwave, a etapa 4.2 pode ser modificada com base no tipo de dispositivo HD-MEA disponível comercialmente de cada usuário.
- Pré-processamento de dados brutos e detecção de eventos
- Abra um arquivo de dados brutos gravados (.brw) no software Brainwave. Selecione Análise > Detecção de LFP ou Detecção de pico.
NOTA: A detecção LFP emprega filtragem IIR com um filtro Butterworth de4ª ordem de passagem baixa (1-100 Hz). Os algoritmos de limiar rígido incluem um limiar alto de 150 μV, um limiar baixo de -150 μV, uma janela de energia entre 70-120 ms, um período refratário de 10 ms e uma duração máxima do evento de 1 s. Single e MUA Spike Detection emprega filtragem IIR com um filtro Butterworth de4ª ordem de passagem alta (300-3500 Hz). Um algoritmo de TEPT é aplicado com um fator de desvio padrão de 8, um período de pico de vida de 2 ms e um período refratário de 1 ms. - Para gravações de circuitos HC e OB, adicione a opção Espaço de Trabalho Avançado no arquivo de eventos detectado (.bxr) para importar a imagem de luz estrutural capturada do estereomicroscópio. Ao examinar circuitos de HC em larga escala, crie camadas estruturais contendo o giro denteado (DG), hilo, Cornu Ammonis 1 (CA1), Cornu Ammonis 3 (CA3), córtex entorrinal (EC) e córtex perirhinal (PC). Ao examinar circuitos OB em larga escala, crie camadas estruturais contendo a camada nervosa olfatória (ONL), camada glomerular (GL), camada plexiforme externa (EPL), camada de células mitrais (MCL) e camada de células granulares (GCL). Considere o EPL e o MCL como a camada de projeção (PL), incluindo o córtex olfatório (OCx).
- Abra um arquivo de dados brutos gravados (.brw) no software Brainwave. Selecione Análise > Detecção de LFP ou Detecção de pico.
- Processamento de dados com um pipeline computacional Python personalizado
- Denoising
- Leia o arquivo .bxr usando um script Python personalizado 26,29,32 e um pacote python h5py 3.6.0.
- Extraia trens spike referentes às gravações de rede iPSC e trens de eventos LFP referentes às gravações do circuito de fatias cerebrais HC e OB.
- Caracterize eventos com um número total de eletrodos ativos inferior a 0,1% ou 10% da média de eletrodos ativos por evento médio ou eventos detectados fora de uma faixa de taxa de disparo estatisticamente razoável como eventos aleatórios e remova-os. Além disso, aplique valores de limite de amplitude e duração do evento.
NOTA: Para a faixa de taxa de disparo, 0,1-15 picos/s e 0,1-60 eventos LFP/min são considerados. Estes são exemplos de valores de limite de taxa usados para os conjuntos de dados analisados. Os limiares de taxa, amplitude e duração dependerão de dados individuais. - Salve os dados de trem de eventos resultantes com as informações espaço-temporais que acompanham no formato de arquivo .npy.
- Rastergramas
- Leia os arquivos .npy e .bxr de eventos filtrados e gere um gráfico raster usando a função de pyplot Matplotlib (https://matplotlib.org/3.5.3/api/_as_gen/matplotlib.pyplot.html).
- Além disso, para gravações de fatias cerebrais com especificidade de camada, classifique e agrupe os IDs dos eletrodos com base nas camadas produzidas na etapa 4.1.2.
- Atividade média de disparo
- Processe os dados da série temporal a partir do arquivo .bxr, calculando a taxa média de disparo de cada eletrodo (número de eventos/tempo de registro).
- Construa uma matriz de dados onde as linhas e colunas representam as coordenadas dos eletrodos na matriz HD-MEA 64 x 64, onde cada valor de matriz significa a taxa média de disparo.
- Utilize uma biblioteca de plotagem, como o imshow de Matplotlib ou as funções de mapa de calor de Seaborn em Python.
- Utilize o mapa colorido "quente" aqui, criando um mapa de calor informativo que encapsula visualmente a distribuição espacial das taxas médias de disparo em toda a matriz de eletrodos.
- Traços representativos da forma de onda
- Leia dados de séries temporais do arquivo .brw e gere um rastreamento de forma de onda usando a função de pyplot Matplotlib. (https://matplotlib.org/3.5.3/api/_as_gen/matplotlib.pyplot.html).
- ID do eletrodo desejado de entrada, compartimento de tempo e banda de frequência para um traçado representativo da forma de onda. As bandas de frequência definidas nessas análises incluem oscilações LFP de baixa frequência (1-100 Hz) com bandpass filtrado δ, θ, β e γ bandas de frequência; ondulações de ondas agudas (SWR) (140-220 Hz); e alta frequência única e MUA (300-3500 Hz). As bandas de frequência δ, θ, β e γ são 1-4 Hz, 5-12 Hz, 13-35 Hz e 35-100 Hz, respectivamente.
- Densidade espectral de potência
- Leia os dados das séries temporais do arquivo .brw e calcule os periodogramas para discernir as frequências dominantes subjacentes à atividade oscilatória dentro de cada série temporal.
- Construir espectrogramas pseudocoloridos da dinâmica freqüência-tempo.
NOTA: Os espectros são calculados usando o método de Welch utilizando a Transformada Rápida de Fourier de LFPs registrados para estimar a densidade de potência espectral41. - Insira o ID desejado do eletrodo, o compartimento de tempo e a banda de frequência para um mapa de densidade espectral. As bandas de frequências definidas nestas análises incluem as descritas no passo 4.2.4.
- Conectividade funcional
- Para gravações de circuitos de fatia cerebral, siga as etapas 4.2.6.2-4.2.6.4.
- Leia os dados das séries temporais do arquivo .brw e calcule a covariância cruzada entre pares de eletrodos ativos na matriz 64 x 64 empregando o coeficiente de correlação de Pearson (PCC)42.
- Ajuste um modelo vetorial autorregressivo à série temporal usando causalidade multivariada de Granger para quantificar a influência de uma série temporal sobre outra.
- Aplicar função de transferência direcionada (DTF) para avaliar o fluxo de informações direcionais dentro dos links correlacionados.
NOTA: A conectividade funcional na rede multicamadas é estabelecida definindo um limite de valor de correlação com base naqueles acima da média e dois desvios padrão de todos os valores de covariância cruzada 43,44. - Para gravação iPSC, siga as etapas 4.2.6.6-4.2.6.8.
- Leia os dados de spiketrains do arquivo .bxr e calcule uma matriz 64x64 dos coeficientes de correlação PCC entre todas as combinações de trens spike binned usando funções spike_train_correlation (https://elephant.readthedocs.io/en/v0.7.0/reference/spike_train_correlation.html).
Observação : conectividade funcional na rede multicamadas é estabelecida definindo um limite de valor de correlação com base naqueles sobre a média e dois desvios padrão de todos os valores de covariância cruzada. - Além disso, implemente filtros espaço-temporais (STF) e limiares de latência dependentes da distância (DdLT) na matriz de conectividade para eliminar possíveis conexões pareadas que excedam a velocidade máxima de propagação (fixada em 400 mm/s)45.
- Extrair picos negativos de matrizes de correlação cruzada resultantes com operações de filtragem e limiar para identificar as conexões inibitórias usando o algoritmo de histograma de correlação cruzada (FNCCH) filtrado e normalizado45.
- Transforme cada matriz de conectividade em um arquivo de gráfico dinâmico (.gexf).
- Mapas de conectividade de rede
- Laboratório de dados abertos no programa Gephi versão 9.2 (https://gephi.org) para o gráfico dinâmico para plotar compartimentos de tempo específicos.
- Aplique Layout Geográfico na janela de layout para mapeamento espacial.
- Coloque restrições de parâmetro em Intervalo de Graus e Peso da Borda para comparação.
- Atribua cor do nó, tamanho da borda e tamanho do grau para melhor visualização.
- Denoising
Resultados
Mapeamento espaço-temporal multimodelo e extração de características oscilatórias de disparo
Para quantificar eventos LFP e spike em toda a rede que emergiram de conjuntos neuronais dinâmicos, investigamos padrões de disparo síncronos em larga escala em circuitos HC e OB e redes iPSC humanas. Os circuitos de corte cerebral gravados da etapa 3.2 e as redes iPSC gravadas da etapa 3.3 foram analisados de acordo com as etapas 4.1-4.2 do protocolo. Primeiro, a detecção e denoização de eventos foram realizadas para todos os conjuntos de dados registrados e resolvidas regionalmente de acordo com as especificações do circuito. Em seguida, foram plotados mapeamentos espaciais topográficos pseudocoloridos dos padrões médios de disparo de espículas e LFP em larga escala, rastergramas de eventos detectados e traços representativos de 5-s de formas de onda filtradas (Figuras 3 A-I). O mapeamento topográfico pseudocolorido dos padrões de LFP em larga escala e da taxa de disparo da espícula foi sobreposto às respectivas imagens ópticas capturadas ao microscópio de HC (Figura 3A), OB (Figura 3B) e rede neuronal humana iPSC (Figura 3C). Isso permite a investigação de padrões e respostas oscilatórias individuais e baseadas em rede. Os rastergramas HC e OB contêm contagens de eventos LFP detectadas ordenadas nas camadas DG, Hilus, CA3, CA1, EC e PC do circuito HC e nas camadas ONL, OCx, GL, PL e GCL da rede OB em um compartimento de tempo de 60 s (Figuras 3D,E). O rastergram iPSC humano exibe eventos de pico detectados síncronos da rede cultivada interconectada em um compartimento de tempo de 20 s (Figura 3G). Em seguida, traços de eventos representativos de 5s de locais de gravação HD-MEA em grande escala mostram uma faixa de frequências oscilatórias registradas nos circuitos HC (ou seja, eletrodo selecionado em CA3) (Figura 3G) e OB (ou seja, eletrodo selecionado em GL) (Figura 3H) e atividade de spike bursting multiunidade na rede iPSC humana a partir de quatro eletrodos ativos selecionados no array (Figura 3I). Esses sinais exemplares mostram assinaturas de biossinais, incluindo oscilações LFP de baixa frequência (1-100 Hz) com bandpass filtrado δ, θ, β e γ bandas de frequência; ondulações de ondas agudas (SWR) (140-220 Hz); e alta frequência única e MUA (300-3500 Hz). Finalmente, a análise de densidade espectral de potência (PSD) foi empregada para quantificar simultaneamente a magnitude de potência de uma banda oscilatória específica no circuito HC e OB interligado registrado a partir de HD-MEA (Figuras 3J,K).
Conectoma funcional multimodal em toda a rede
Para inferir a conectividade em larga escala de redes neurais multicamadas a partir de padrões de disparo simultâneo de conjuntos neuronais simultaneamente ativos, a covariância cruzada entre pares de eletrodos ativos em eventos detectados foi calculada de acordo com o passo 4.2.6 do protocolo. Aqui, o coeficiente de correlação foi classificado com base em camadas no circuito HC e OB ou não classificado na rede iPSC e, em seguida, armazenado em uma matriz simétrica. Conectomas funcionais dos circuitos HC e OB foram gerados pela aplicação de causalidade multivariada de Granger e função de transferência dirigida (DTF) para quantificar a influência de uma série temporal sobre outra e avaliar o fluxo direcional de informação dentro dos links correlacionados nas distintas redes. O mapeamento do conectoma de HC (Figura 4A) e OB (Figura 4B) e a visualização da rede foram realizados utilizando o programa Gephi versão 9.2 (https://gephi.org). Restrições de parâmetros semelhantes foram colocadas nos elos funcionais para comparar os circuitos de corte cerebral HC e OB e ilustraram 100 s da conectividade funcional dos eventos LFP detectados. Os nós são dimensionados de acordo com a força do grau com a cor do nó indicando a cor da camada e do link identificando as conexões intra e intercamadas. Conectomas funcionais de redes iPSC humanas foram gerados pela aplicação de filtros espaço-temporais (STF) e limiares de latência dependentes da distância (DdLT) para melhorar a seleção de links significativos e refinar a identificação de conexões significativas aplicando análise de histograma de correlação cruzada filtrada e normalizada (FNCCH). Mapeamento do conectoma de redes iPSC humanas em toda a visualização do chip HD-MEA (Figura 4C) realizado usando Gephi. A cor do nó indica entrada excitatória ou inibitória, e a cor do link identifica as conexões.
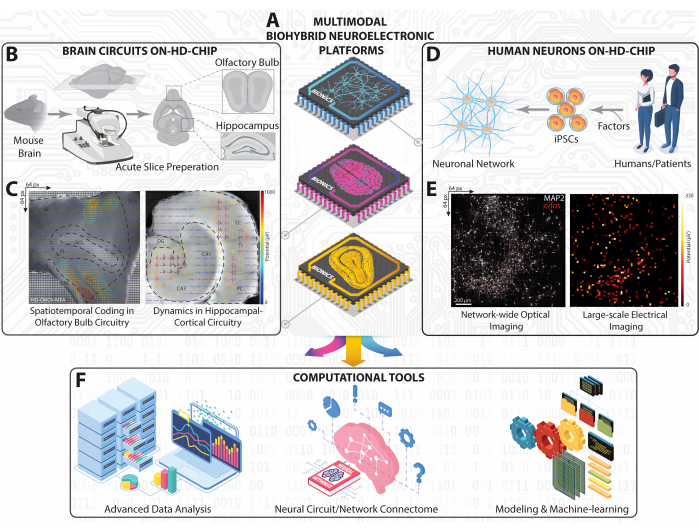
Figura 1: Visão geral da plataforma experimental e computacional em HD-MEA em larga escala. (A) Representação esquemática isométrica de nossas plataformas neuroeletrônicas biohíbridas multimodais realizadas com HD-MEA baseado em CMOS para capturar a dinâmica neural de HC, OB e circuitos e redes neuronais iPSC humanas. (B) Fluxo de trabalho esquemático para fatiamento cerebral de camundongos e sua paisagem de trabalho para obtenção de fatias de HC e OB. (C) Representações topográficas dos padrões de disparo em larga escala registrados simultaneamente a partir de todos os cortes HC e OB sobrepostos com as formas de onda extracelulares extraídas às imagens ópticas de corte. (D) Representação esquemática da rede neuronal iPSC obtida de humanos. (E) Micrografias de fluorescência mostrando c-fos celular e MAP-2 somático/dendrítico de toda a rede neuronal humana no chip HD-MEA (esquerda) combinados com todo o mapa de atividade de disparo médio (direita). (F) Estrutura computacional incluindo análise avançada de dados, mapeamento de conectividade e ferramentas de aprendizado de máquina de IA para analisar dados neurais multidimensionais obtidos de gravações em grande escala em HD-MEAs. Clique aqui para ver uma versão maior desta figura.

Figura 2: Layouts para espaços de trabalho de preparação e registro de cultura iPSC humana ex-vivo e in-vitro . (A) Fluxo de trabalho esquemático ilustrando a configuração para a preparação de fatias de HC e OB, apresentando as ferramentas e equipamentos necessários em cada espaço de trabalho. (B) Representação esquemática para a preparação da cultura humana iPSC, incluindo as ferramentas e dispositivos necessários. Uma lista completa de materiais está incluída nas etapas 1.2.2, 2.1, 2.2, 3.1.1, 3.3 e na Tabela de Materiais. Clique aqui para ver uma versão maior desta figura.
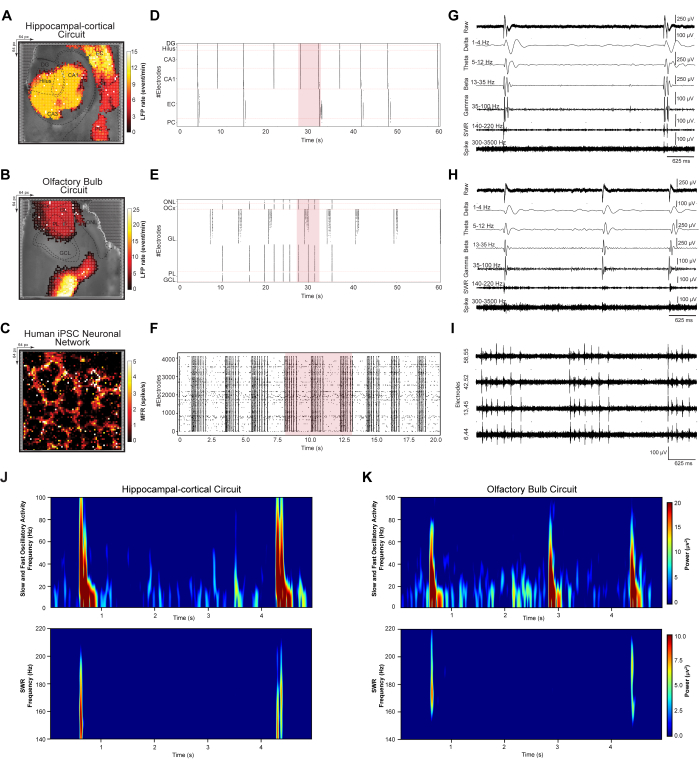
Figura 3: Mapeamento e extração de padrões espaço-temporais da dinâmica de redes. (A-C) Mapas espaciais médios de LFP e spike rate, computados em registros de cinco minutos, sobrepostos à imagem luminosa do microscópio. (D-F) Gráficos raster mostrando eventos LFP detectados e denoizados em uma subamostra de dados de 60 segundos e picos em uma subamostra de dados de 20 segundos. (G-I) Extração representativa de traços de forma de onda de um segmento de 5 segundos da subamostra de dados do gráfico raster (destacado em vermelho no gráfico raster), exibido como bandas oscilatórias LFP brutas (1-100 Hz); δ (1-4 Hz), θ (5-12 Hz), β (13-35 Hz) e γ (35-100 Hz) bandas de frequência; SWR (140-220 Hz); e pico de MUA e único de alta frequência (300-3500 Hz). (J,K) Mapas de densidade espectral de potência de LFPs oscilatórios rápidos e lentos (1-100 Hz) e SWR (140-220 Hz). Clique aqui para ver uma versão maior desta figura.
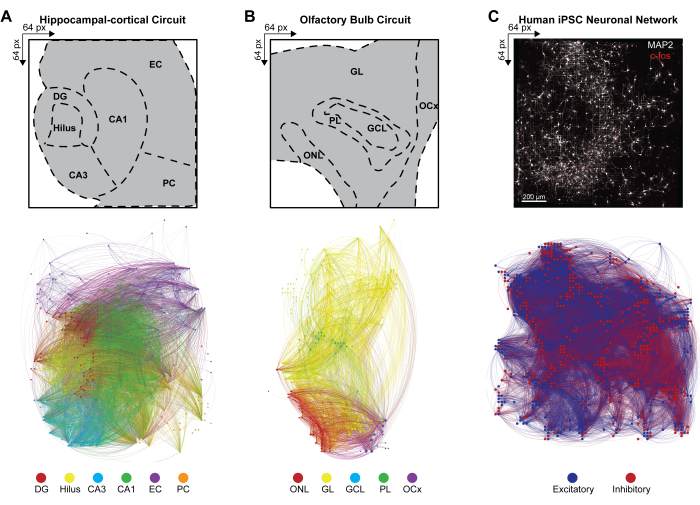
Figura 4: Organização de conectomas funcionais multimodais em rede. (A-C) Mapas Gephi ilustrando a conectividade funcional nodal, onde os nós correspondem a uma das legendas de barra de cores de exemplo (abaixo), enquanto os links (ou bordas) são sombreados para corresponder aos nós de conexão. Legendas de exemplo para (A) HC, (B) OB e (C) camadas iPSC são exibidas em uma matriz 64 x 64. As camadas HC e OB são plotadas em um compartimento de tempo de 100 s para reduzir efetivamente o número de nós visíveis e links para fins de visualização. Clique aqui para ver uma versão maior desta figura.
Tabela 1: Soluções para preparação de fatias cerebrais e meios para culturas neuronais iPSC. (A) Solução de corte com alto teor de sacarose para preparação de fatias cerebrais ex-vivo. (B) solução de gravação de aCSF para preparação e gravação de fatias cerebrais ex-vivo. (C-D) Protocolo de mídia iPSC neuronal humano, onde (C) é a mídia completa BrainPhys usada para descongelamento celular, revestimento de chip HD-MEA e manutenção HD-MEA cultivada, e (D) a mídia pontilhada usada para revestimento celular HD-MEA. Clique aqui para baixar esta tabela.
Tabela 2: Solução de problemas comuns de aquisição de gravação HD-MEA. Uma lista de problemas comuns, suas causas potenciais e soluções de solução de problemas relacionadas a chips HD-MEA, plataforma de gravação, ruído do sistema e software. Clique aqui para baixar esta tabela.
Discussão
A intrincada dinâmica da atividade neuronal espaço-temporal, emergindo de conjuntos neuronais interconectados, tem sido um assunto de intriga na neurociência. Metodologias tradicionais, como patch-clamp, MEA padrão e imagens de Ca2+, forneceram insights valiosos sobre a complexidade cerebral. No entanto, eles muitas vezes falham em capturar a dinâmica computacional abrangente em toda a rede 21,22,23. O protocolo técnico da plataforma HD-MEA, conforme detalhado neste estudo JoVE, representa um salto significativo, oferecendo uma visão panorâmica da dinâmica neural em diversas modalidades, desde montagens celulares até redes expansivas (i.e., fatias cerebrais agudas ex-vivo de camundongos e redes iPSC humanas in vitro)26,29,30,32.
Cortes cerebrais agudos ex-vivo de camundongos têm sido uma ferramenta fundamental na pesquisa neuronal, facilitando investigações moleculares e em nível de circuito 6,7. No entanto, o desafio de manter a viabilidade tecidual tem sido um gargalo persistente. O protocolo delineado neste estudo introduz modificações críticas para otimizar a qualidade e longevidade dessas fatias para explorar seus benefícios na plataforma HD-MEA. Esse protocolo ressalta a importância de: - i) Uniformidade de corte, para a qual o uso de vibratomo é preferido em relação a um picador de tecido devido à sua precisão e minimização do dano tecidual, apesar do trade-off de tempos de corte mais longos. ii) Garantir a carbogenação constante durante todo o processo, desde a extração até o registro, para manter a viabilidade do tecido. iii) Regular a temperatura e permitir um tempo adequado de recuperação antes do registro. iv) Utilizar um bloco ou molde de agarose para estabilizar o cérebro, evitar rasgos e minimizar o contato com a cola. v) Manter as taxas de fluxo ideais de aCSF carbogenadas dentro do reservatório HD-MEA para garantir a saúde do corte, evitando problemas como desacoplamento, ruído e deriva (Tabela 2).
Tanto para fatias cerebrais de camundongos quanto para preparações iPSC humanas, o aumento do acoplamento eletrodo-tecido é fundamental 30,46,47. Nosso protocolo ressalta a importância da utilização da molécula promotora de adesão Poly-dl-ornitina (PDLO). Essa molécula não só aumenta a área de superfície para detecção de sinais elétricos, mas também aumenta a condutividade elétrica46. Ao fazer isso, promove a adesão celular, o crescimento e o desenvolvimento de propriedades funcionais da rede. Tal otimização desempenha um papel fundamental no aumento da eficácia da plataforma HD-MEA. Isso, por sua vez, garante análises precisas e consistentes de conectomas ex-vivo e in vitro em microescala e suas sequências de disparo espaço-temporal. Notavelmente, PDLO demonstrou superar outros substratos como polietilenoimina (PEI) e poli-l-ornitina (PLO) na promoção de atividade de disparo espontâneo e responsividade a estímulos elétricos em culturas neuronais. Além disso, o PDLO tem sido usado para funcionalização de superfície no HD-MEA e demonstrou melhorar a interface de acoplamento eletrodo-corte e aumentar a relação sinal-ruído em ambos os cortes de OB e HC26,29. A adição de uma âncora de platina personalizada aumenta ainda mais o acoplamento da interface eletrodo-fatia, levando a gravações com uma relação sinal-ruído mais alta.
A utilização de HD-MEA para fatias cerebrais de camundongos ex-vivo e redes iPSC humanas in vitro introduz um método hábil em explorar dinâmicas extensas, multiescalares e multimodais. Essa abordagem inovadora, no entanto, traz desafios consideráveis, especialmente no gerenciamento de dados 48,49,50,51. Uma única gravação HD-MEA adquirida a 18 kHz/frequência de amostragem do eletrodo gera impressionantes 155 MB/s de dados. O volume de dados aumenta rapidamente ao considerar várias fatias, diversas condições farmacológicas ou períodos de registro prolongados. Esse influxo de informações exige infraestruturas de armazenamento robustas e ferramentas computacionais avançadas para um processamento simplificado. A capacidade da plataforma HD-MEA de coletar simultaneamente dados de milhares de conjuntos neuronais é um benefício e um obstáculo. Ele fornece insights supremos sobre a dinâmica computacional das funções cerebrais, mas também requer uma estrutura analítica refinada. Neste protocolo JoVE, fornecemos exemplos de estratégias computacionais, incluindo detecção de eventos em larga escala, classificação, teoria de grafos, análise de frequência e aprendizado de máquina. Esses métodos ressaltam os esforços intensivos feitos para enfrentar os desafios da análise de dados neurais complexos. No entanto, ainda há espaço considerável para o desenvolvimento de ferramentas computacionais mais avançadas para analisar esses conjuntos de dados neurais multidimensionais. Armado com as ferramentas e metodologias apropriadas, o potencial da plataforma HD-MEA é ampliado, oferecendo insights profundos sobre os meandros das funções cerebrais em condições saudáveis e patológicas.
Em essência, a plataforma HD-MEA, quando integrada com os protocolos detalhados e ferramentas computacionais discutidas, oferece uma abordagem transformadora para entender o intrincado funcionamento do cérebro. Ao capturar dinâmicas em larga escala, multiescala e multimodais, ele fornece insights inestimáveis sobre processos como aprendizagem, memória e processamento de informações. Além disso, sua aplicação em redes iPSC humanas in vitro tem o potencial de revolucionar a triagem de drogas e a medicina personalizada. No entanto, embora essa plataforma represente um avanço significativo na pesquisa em neurociência, é crucial reconhecer e abordar os desafios técnicos inerentes. Com o refinamento contínuo e a integração de ferramentas computacionais avançadas, a plataforma HD-MEA está pronta para inaugurar uma nova era de ferramentas de diagnóstico precisas, a identificação de biomarcadores específicos e terapias-alvo para distúrbios neurológicos.
Divulgações
Os autores declaram não ter interesses concorrentes ou financeiros.
Agradecimentos
Este estudo foi financiado por fundos institucionais (DZNE), pela Associação Helmholtz dentro do Fundo de Validação Helmholtz (HVF-0102) e pela Dresden International Graduate School for Biomedicine and Bioengineering (DIGS-BB). Também gostaríamos de agradecer à plataforma para testes comportamentais em animais da DZNE-Dresden (Alexander Garthe, Anne Karasinsky, Sandra Günther e Jens Bergmann) por seu apoio. Gostaríamos de reconhecer que uma parte da Figura 1 foi criada usando a plataforma BioRender.com.
Materiais
| Name | Company | Catalog Number | Comments |
| 150 mm Glass Petri Dish | generic | generic | Brain Preparation Workspace, Brain Slice Recording Workspace |
| 0.22 μm Sterile Filter Unit | Assorted | Assorted | Assorted |
| 90 mm Plastic Culture Dish | TPP | 93100 | Brain Preparation Workspace, Brain Slice Recording Workspace |
| Agarose | Roth | 6351.5 | Brain Preparation Workspace |
| Agarose Mold | CUSTOM | CUSTOM | Brain Preparation Workspace; Custom designed 3D Printer Design, available upon request |
| Aluminum Foil | generic | generic | Brain Extraction Workspace |
| Anesthesia chamber | generic | generic | Brain Extraction Workspace; Assorted Beaker, Bedding etc |
| Ascorbic Acid | Sigma Aldrich | A4544-25G | Solution Preparation Workspace |
| Assorted Beakers | generic | generic | Solution Preparation Workspace; 50 mL |
| Assorted Luers | Cole Parmer | 45511-00 | Brain Slice Recording Workspace |
| Assorted Volumetric flasks | generic | generic | Solution Preparation Workspace; 500 mL, 1 L |
| B27 Supplement | Life Technologies | 17504-044 | BrainXell Commercial Supplier Protocol |
| BDNF | Peprotech | 450-02 | BrainXell Commercial Supplier Protocol |
| Biological Safety Cabinet with UV Lamp | Assorted | Assorted | HD-MEA Coating, Plating, Mainainance Workspace |
| BrainPhys Neuronal Medium | STEMCELL Technologies | 05790 | CDI, and BrainXell Commerical Supplier Protocol |
| Brainwave Software | 3Brain AG | Version 4 | Brain Slice and Human iPSC Recording Workspace |
| BrainXell Glutamatergic Neuron Assay | BrainXell | BX-0300 | BrainXell Commercial Supplier Protocol |
| CaCl2 | Sigma Aldrich | 21115-100ML | Solution Preparation Workspace |
| Carbogen | generic | generic | All Workspaces; 95%/5% O2 and CO2 mixture |
| Cell Culture Incubator | Assorted | Assorted | Assorted |
| CMOS-based HD-MEA chip | 3Brain AG | CUSTOM | Brain Slice and Human iPSC Recording Workspace |
| Conical Tubes, 50 mL, Falcon (Centrifuge Tubes) | STEMCELL Technologies | 38010 | CDI Commerical Supplier Protocol |
| Crocodile Clip Grounding Cables | JWQIDI | B06WGZG17W | Brain Slice Recording Workspace |
| Curved Forceps | FST | 11052-10 | Brain Extraction Workspace |
| DMEM/F12 Medium | Life Technologies | 11330-032 | BrainXell Commercial Supplier Protocol |
| Dulbecco’s Phosphate Buffered Saline without Ca2+ and Mg2+ (D-PBS) | STEMCELL Technologies | 37350 | CDI Commerical Supplier Protocol |
| Filter Paper | Macherey-Nagel | 531 011 | Brain Preparation Workspace |
| Fine Brush | Leonhardy | 773 | Brain Slice Preparation Workspace, Brain Slice Recording Workspace |
| Forceps | VITLAB | 67895 | Brain Slice Recording Workspace |
| GDNF | Peprotech | 450-10 | BrainXell Commercial Supplier Protocol |
| Geltrex | Life Technologies | A1413201 | BrainXell Commercial Supplier Protocol |
| Glass pasteur pipette | Roth | 4518 | Brain Slice Preparation Workspace, Brain Slice Recording Workspace |
| Glucose | Sigma Aldrich | G7021-1KG | Solution Preparation Workspace |
| GlutaMAX | Life Technologies | 35050-061 | BrainXell Commercial Supplier Protocol |
| Gravity-based Perfusion System | ALA | VC3-8xG | Brain Slice Recording Workspace |
| HD-MEA Recording platform | 3Brain AG | CUSTOM | Brain Slice and Human iPSC Recording Workspace |
| Heater | Warner Instruments | TC-324C | Brain Slice Recording Workspace |
| Hemocytometer or Automated Cell Counter | Assorted | Assorted | HD-MEA Coating, Plating, Mainainance Workspace |
| Hypo Needles | Warner Instruments | 641489 | Brain Slice Recording Workspace |
| iCell GlutaNeurons Kit, 01279 | CDI | R1061 | CDI Commerical Supplier Protocol |
| Iris Scissors | Vantage | V95-304 | Brain Extraction Workspace |
| Isoflurane | Baxter | HDG9623 | Brain Extraction Workspace |
| KCl | Sigma Aldrich | P5405-250G | Solution Preparation Workspace |
| Laminin | Sigma-Aldrich | L2020 | CDI Commerical Supplier Protocol |
| Liquid Nitrogen Storage Unit | Assorted | Assorted | HD-MEA Coating, Plating, Mainainance Workspace |
| Magnetic Stirrer | generic | generic | Solution Preparation Workspace |
| Metal Screws | Thorlabs | HW-KIT2/M | Brain Slice Recording Workspace |
| MgCl2 | Sigma Aldrich | M1028-100ML | Solution Preparation Workspace |
| MgSO4 | Sigma Aldrich | 63138-250G | Solution Preparation Workspace |
| Microdissection Tool Holder | Braun | 4606108V | Brain Slice Preparation Workspace, Brain Slice Recording Workspace |
| Microdissection Tool Needle | Braun | 9186166 | Brain Slice Preparation Workspace, Brain Slice Recording Workspace |
| Modular Stereomicroscope | Leica | CUSTOM | Brain Slice Recording Workspace; custom specifications and modifications |
| N2 Supplement | Life Technologies | 17502-048 | CDI, and BrainXell Commercial Supplier Protocol |
| NaCl | Sigma Aldrich | S3014-1KG | Solution Preparation Workspace |
| NaH2PO4 | Sigma Aldrich | S0751-100G | Solution Preparation Workspace |
| NaHCO3 | Sigma Aldrich | S5761-500G | Solution Preparation Workspace |
| Neurobasal Medium | Life Technologies | 21103-049 | BrainXell Commercial Supplier Protocol |
| Optical Cage System | Thorlabs | Assorted | Brain Slice Recording Workspace |
| Optical Table w/Breadboard | Thorlabs | SDA7590 | Brain Slice Recording Workspace |
| PDLO | Sigma Aldrich | P0671 | HD-MEA Coating, Brain Slice Recording Workspace |
| Penicillin-streptomycin, 100x | Thermo Fisher Scientific | 15140-122 | CDI Commerical Supplier Protocol |
| Pipette tips | TipONE | S1120-8810 | Brain Slice Recording Workspace |
| Pipettors | Assorted | Assorted | Assorted |
| Platinum Anchor | CUSTOM | CUSTOM | Brain Slice Recording Workspace |
| Polyethylene Tubing | Assorted | Assorted | Brain Slice Recording Workspace |
| Pump | MasterFlex | 78018-22 | Brain Slice Recording Workspace |
| Razor Blade | Apollo | 10179960 | Brain Preparation Workspace |
| Reference Electrode Cell Culture Cap | CUSTOM | CUSTOM | Human iPSC Recording Workspace; Custom designed 3D Printer Design, available upon request |
| Rubber Pipette Bulb | Duran Wheaton Kimble | 292000205 | Brain Slice Preparation Workspace, Brain Slice Recording Workspace |
| Serological Pipettes, 1 mL, 2 mL, 5 mL, 10 mL, 25 mL | Assorted | Assorted | Assorted |
| Slice Recovery Chamber | CUSTOM | CUSTOM | Brain Slice Recovery Workspace; Custom designed 3D Printer Design, available upon request |
| Spatula | ISOLAB | 047.06.150 | Brain Preparation Workspace |
| Sucrose | Sigma Aldrich | 84100-1KG | Solution Preparation Workspace |
| Super Glue | UHU | 358221 | Brain Slice Preparation Workspace |
| Surgical Scissors | Peters Instruments | BC 344 | Brain Extraction Workspace |
| Tabletop Centrifuge | Assorted | Assorted | Assorted |
| TGF-β1 | Peprotech | 100-21C | BrainXell Commercial Supplier Protocol |
| Tissue Paper | generic | generic | Brain Extraction Workspace |
| Trypan Blue | STEMCELL Technologies | 07050 | CDI Commerical Supplier Protocol |
| Upright Microscope | Olympus | CUSTOM | Imaging Workspace; Custom specifications and modifications |
| Vacusip | Integra | 159010 | Brain Slice Recording Workspace |
| Vibratome | Leica | VT1200s | Brain Slice Preparation Workspace; Includes: Specimen plate, buffer tray, ice tray, specimen plate holding tool, vibratome blade adjusting tool |
| Vibratome Blade | Personna | N/A | Brain Slice Preparation Workspace |
| Water Bath | Lauda | L000595 | Brain Slice Recovery Workspace |
Referências
- Hebb, D. O. . The Organization of Behavior; A Neuropsychological Theory. , (1949).
- Cossart, R., Garel, S. Step by step: cells with multiple functions in cortical circuit assembly. Nat Rev Neurosci. 23, 395-410 (2022).
- Carrillo-Reid, L., Yuste, R. Playing the piano with the cortex: role of neuronal ensembles and pattern completion in perception and behavior. Curr Opin Neurobiol. 64, 89-95 (2020).
- Buzsáki, G. Large-scale recording of neuronal ensembles. Nat Neurosci. 7, 446-451 (2004).
- Buzsáki, G. Neural Syntax: Cell assemblies, synapsembles, and readers. Neuron. 68 (3), 362-385 (2010).
- Huang, Y., Williams, J. C., Johnson, S. M. Brain slice on a chip: opportunities and challenges of applying microfluidic technology to intact tissues. Lab Chip. 12 (12), 2103-2117 (2012).
- Cho, S., Wood, A., Bowlby, M. Brain slices as models for neurodegenerative disease and screening platforms to identify novel therapeutics. Curr Neuropharmacol. 5 (1), 19-33 (2007).
- Bliss, T. V. P., Collingridge, G. L. A synaptic model of memory: long-term potentiation in the hippocampus. Nature. 361, 31-39 (1993).
- Anderson, P., Morris, R., Amaral, D., Bliss, T., O'Keefe, L. . The Hippocampus Book. , (2006).
- Lisman, J., et al. Viewpoints: how the hippocampus contributes to memory, navigation and cognition. Nat Neurosci. 20, 1434-1447 (2017).
- Mori, K., Nagao, H., Yoshihara, Y. The olfactory bulb: Coding and processing of odor molecule information. Science. 286 (5440), 711-715 (1999).
- Buck, L., Axel, R. A novel multigene family may encode odorant receptors: A molecular basis for odor recognition. Cell. 65 (1), 175-187 (1991).
- Bushdid, C., Magnasco, M. O., Vosshall, L. B., Keller, A. Humans can discriminate more than 1 trillion olfactory stimuli. Science. 343 (6177), 1370-1372 (2014).
- Kempermann, G. Why new neurons? Possible functions for adult hippocampal neurogenesis. J Neurosci. 23 (3), 635-638 (2003).
- Aimone, J. B., Wiles, J., Gage, F. H. Computational influence of adult neurogenesis on memory encoding. Neuron. 61 (2), 187-202 (2009).
- Nithianantharajah, J., Hannan, A. J. Enriched environments, experience-dependent plasticity and disorders of the nervous system. Nat Rev Neurosci. 7, 697-709 (2006).
- Takahashi, K., et al. Induction of pluripotent stem cells from adult human fibroblasts by defined factors. Cell. 131 (5), 861-872 (2007).
- Espuny-Camacho, I., et al. Pyramidal neurons derived from human pluripotent stem cells integrate efficiently into mouse brain circuits in vivo. Neuron. 77 (3), 440-456 (2013).
- Rajamohan, D., et al. Current status of drug screening and disease modelling in human pluripotent stem cells. Bioessays. 35 (3), 281-298 (2013).
- Heilker, R., Traub, S., Reinhardt, P., Schöler, H. R., Sterneckert, J. iPS cell derived neuronal cells for drug discovery. Trends Pharmacol Sci. 35 (10), 510-519 (2014).
- Zhao, S. R., Mondéjar-Parreño, G., Li, D., Shen, M., Wu, J. C. Technical applications of microelectrode array and patch clamp recordings on human induced pluripotent stem cell-derived cardiomyocytes. J Vis Exp. (186), e64265 (2022).
- Hamill, O. P., McBride, D. W. Induced membrane hypo/hyper-mechanosensitivity: A limitation of patch-clamp recording. Annu Rev Physiol. 59, 621-631 (1997).
- Manz, K. M., Siemann, J. K., McMahon, D. G., Grueter, B. A. Patch-clamp and multi-electrode array electrophysiological analysis in acute mouse brain slices. STAR Protoc. 2 (2), 100442 (2021).
- Lee, C. H., Park, Y. K., Lee, K. Recent strategies for neural dynamics observation at a larger scale and wider scope. Biosens Bioelectron. 240, 115638 (2023).
- Urai, A. E., Doiron, B., Leifer, A. M., Churchland, A. K. Large-scale neural recordings call for new insights to link brain and behavior. Nat Neurosci. 25 (1), 11-19 (2022).
- Hu, X., Khanzada, S., Klütsch, D., Calegari, F., Amin, H. Implementation of biohybrid olfactory bulb on a high-density CMOS-chip to reveal large-scale spatiotemporal circuit information. Biosens Bioelectron. 198, 113834 (2022).
- Amin, H., Marinaro, F., Tonelli, D. D. P., Berdondini, L. Developmental excitatory-to-inhibitory GABA-polarity switch is disrupted in 22q11.2 deletion syndrome: A potential target for clinical therapeutics. Sci Rep. 7 (1), 15752 (2017).
- Amin, H., Nieus, T., Lonardoni, D., Maccione, A., Berdondini, L. High-resolution bioelectrical imaging of Aβ-induced network dysfunction on CMOS-MEAs for neurotoxicity and rescue studies. Sci Rep. 7 (1), 2460 (2017).
- Emery, B. A., Hu, X., Khanzada, S., Kempermann, G., Amin, H. High-resolution CMOS-based biosensor for assessing hippocampal circuit dynamics in experience-dependent plasticity. Biosens Bioelectron. 237, 115471 (2023).
- Amin, H., et al. Electrical responses and spontaneous activity of human iPS-derived neuronal networks characterized for 3-month culture with 4096-electrode arrays. Front Neurosci. 10, 121 (2016).
- Lonardoni, D., et al. Recurrently connected and localized neuronal communities initiate coordinated spontaneous activity in neuronal networks. PLoS Comput Biol. 13 (7), e1005672 (2017).
- Emery, B. A., et al. Large-scale multimodal recordings on a high-density neurochip: Olfactory bulb and hippocampal networks. 2022 44th Annual International Conference of the IEEE Engineering in Medicine & Biology Society (EMBC). , 3111-3114 (2022).
- Rossi, L., Emery, B. A., Khanzada, S., Hu, X., Amin, H. Pharmacologically and electrically-induced network-wide activation of olfactory bulb with large-scale biosensor. 2023 IEEE BioSensors Conference (BioSensors). , 1-4 (2023).
- Emery, B. A., et al. Recording network-based synaptic transmission and LTP in the hippocampal network on a large-scale biosensor. 2023 IEEE BioSensors Conference (BioSensors). , 1-4 (2023).
- Hierlemann, A., Frey, U., Hafizovic, S., Heer, F. Growing cells atop microelectronic chips: Interfacing electrogenic cells in vitro with CMOS-based microelectrode arrays). Proceedings of the IEEE. 99 (2), 252-284 (2011).
- Berdondini, L., et al. Active pixel sensor array for high spatio-temporal resolution electrophysiological recordings from single cell to large scale neuronal networks. Lab Chip. 9, 2644-2651 (2009).
- Siegle, J. H., Hale, G. J., Newman, J. P., Voigts, J. Neural ensemble communities: open-source approaches to hardware for large-scale electrophysiology. Curr Opin Neurobiol. 32, 53-59 (2015).
- Amin, H., Maccione, A., Zordan, S., Nieus, T., Berdondini, L. High-density MEAs reveal lognormal firing patterns in neuronal networks for short and long term recordings. 2015 7th International IEEE/EMBS Conference on Neural Engineering (NER). , 1000-1003 (2015).
- Altuntac, E., et al. Bottom-up neurogenic-inspired computational model. 2023 IEEE BioSensors Conference (BioSensors). , 1-4 (2023).
- Maccione, A., et al. A novel algorithm for precise identification of spikes in extracellularly recorded neuronal signals. J Neurosci Methods. 177 (1), 241-249 (2009).
- Welch, P. D. The use of fast Fourier transform for the estimation of power spectra: A method based on time averaging over short, modified periodograms. IEEE Transactions on Audio and Electroacoustics. 15 (2), 70-73 (1967).
- Eggermont, J. J., Munguia, R., Pienkowski, M., Shaw, G. Comparison of LFP-based and spike-based spectro-temporal receptive fields and cross-correlation in cat primary auditory cortex. PLoS One. 6 (5), e20046 (2011).
- Damos, P. Using multivariate cross correlations, Granger causality and graphical models to quantify spatiotemporal synchronization and causality between pest populations. BMC Ecol. 16, 33 (2016).
- Kaminski, M. J., Blinowska, K. J. A new method of the description of the information flow in the brain structures. Biol Cybern. 65, 203-210 (1991).
- Pastore, V. P., Massobrio, P., Godjoski, A., Martinoia, S. Identification of excitatory-inhibitory links and network topology in large-scale neuronal assemblies from multi-electrode recordings. PLoS Comput Biol. 14 (8), e1006381 (2018).
- Amin, H., Dipalo, M., De Angelis, F., Berdondini, L. Biofunctionalized 3D nanopillar arrays fostering cell guidance and promoting synapse stability and neuronal activity in networks. ACS Appl Mater Interfaces. 10 (17), 15207-15215 (2018).
- Woeppel, K., Yang, Q., Cui, X. T. Recent advances in neural electrode-tissue interfaces. Curr Opin Biomed Eng. 4, 21-31 (2017).
- Steinmetz, N. A., Koch, C., Harris, K. D., Carandini, M. Challenges and opportunities for large-scale electrophysiology with Neuropixels probes. Curr Opin Neurobiol. 50, 92-100 (2018).
- Siegle, J. H., Hale, G. J., Newman, J. P., Voigts, J. Neural ensemble communities: open-source approaches to hardware for large-scale electrophysiology. Curr Opin Neurobiol. 32, 53-59 (2015).
- Freeman, J. Open source tools for large-scale neuroscience. Curr Opin Neurobiol. 32, 156-163 (2015).
- Stevenson, I. H., Kording, K. P. How advances in neural recording affect data analysis. Nat Neurosci. 14 (2), 139-142 (2011).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados