Method Article
Очистка и аналитика моноклонального антитела от китайских яичников хомяка с помощью автоматизированной системы микробиореактора
В этой статье
Резюме
Описан подробный протокол очистки и последующего анализа моноклональных антител из собранной жидкости клеточной культуры (HCCF) автоматизированных микробиореакторов. Также представлена аналитика для определения критических атрибутов качества (КЗА) и максимизации ограниченного объема выборки для извлечения жизненно важной информации.
Аннотация
Моноклональные антитела (mAbs) являются одним из самых популярных и хорошо охарактеризованных биологических продуктов, производимых сегодня. Чаще всего производится с использованием китайских хомяков яичников (CHO) клетки, культура и условия процесса должны быть оптимизированы, чтобы максимизировать антитела титры и достичь целевых профилей качества. Как правило, эта оптимизация использует автоматизированные микромасштабные биореакторы (15 мл) для параллельного скрининга нескольких условий процесса. Критерии оптимизации включают производительность культуры и критические атрибуты качества (КЗА) моноклонального продукта антител (mAb), которые могут повлиять на его эффективность и безопасность. Показатели производительности культуры включают рост клеток и потребление питательных веществ, в то время как C'As включают n-гликозилации mAb и агрегирования профилей, варианты заряда, и молекулярный вес. Этот подробный протокол описывает, как очистить и впоследствии проанализировать образцы HCCF, производимые автоматизированной системой микробиореактора, чтобы получить ценные показатели производительности и выходы. Во-первых, автоматизированный метод быстрой белковой жидкости хроматографии (FPLC) используется для очищения mAb от собранных образцов клеточной культуры. После концентрации гликановые профили анализируются масс-спектрометрией с помощью определенной платформы (см. таблицу материалов). Молекулярные веса антител и профили агрегации определяются с помощью микрографа-версия хроматографии-многократное рассеяние углового света (SEC-MALS), в то время как варианты заряда анализируются с помощью электрофораса зоны капилляров микрочипа (mC'E). В дополнение к метрикам производительности культуры, захваченным в процессе биореактора (т.е. жизнеспособность культуры, количество клеток и общие метаболиты, включая глутамин, глюкозу, лактат и аммиак), анализируются расходные средства массовой информации для определения ограничивающих питательных веществ улучшить стратегии кормления и общий дизайн процесса. Поэтому также описан подробный протокол абсолютной количественной оценки аминокислот жидкой хроматографической масс-спектрометрией (LC-MS) отработанных носителей. Методы, используемые в этом протоколе, используют высокопроизводительные платформы, совместимые для большого количества малообъемных образцов.
Введение
Белковые терапии используются для лечения растущего разнообразия заболеваний, включая осложнения трансплантации тканей, аутоиммунные расстройства и рак1. С 2004 года Управление по контролю за продуктами и лекарствами США (USFDA) задокументировало увеличение доли биологических заявок на лицензии (BLAs) всех утверждений, регулируемых Центром по оценке и исследованиям лекарственных средств (CDER), при этом на БЛО приходится более 25% в 2014 и 2015 годах2.
Учитывая этот расширяющийся рынок, биофармацевтические производители сталкиваются с проблемой быстрого доставки большего количества продукции с последовательным качеством. Усилия по увеличению урожайности продукции были сосредоточены на CHO клеточной инженерии и скрининга производственной линии, хотя наиболее значительные улучшения связаны с достижениями в области медиа / питания стратегии оптимизации и клеточной культуры экологического контроля1, 3 , 4 , 5 в процессе производства.
Так как mAbs производятся в биологической системе, может быть присущая изменчивость белка. Состав антител может быть изменен пост-переводически, такие как гликозилирование или влияние деградации или ферментативных реакций. Эти структурные изменения могут спровоцировать опасные иммунные реакции или изменить связывание антител, которые, в свою очередь, могут уменьшить или устранить предполагаемую терапевтическую функцию5. Таким образом, критические атрибуты качества (КЗА) моноклональных антител - N-гликанский профиль, распределение вариантов заряда и процент антител в мономерной форме - регулярно контролируются и контролируются в рамках подхода «Качество по дизайну» (кбД) во время производственныепроцессы 1,6. В регулируемой производственной среде терапевтические белки должны соответствовать критериямпринятия лицензии в качестве утвержденного коммерческого лекарственного продукта 7. Методы, представленные в этом вопросе, как правило, являются частью процесса характеристики качества для антитела7,8, и любой ученый белка будет знаком с их использованием.
В предыдущей работе9, применение и эксплуатация микробиореакторов для высокой пропускной мощности скрининга клеточной культуры условия хроноув биообработки была описана. Очищенный продукт, полученный из различных медиа-условий подвергается N-гликананализа анализа с использованием LC-MS. Гликозилирование моделей терапевтических белков могут быть обнаружены и охарактеризованы с помощью методов LC-MS10,11, и наличие различных видов гликанов было связано с параметрами биопроцесса, такими как стратегия корма, рН и температура12. Влияние различных условий мультимедиа на качество продукции, о чем свидетельствует процент полученного IgG в мономерной форме, также оценивается с помощью хроматографии отчуждения размера- Многоугловое рассеяние света (SEC-MALS)13,14 , 15. Профиль варианта заряда представляет ряд модификаций16, которые могут повлиять на функцию продукта. Микрокапиллярная зона электрофорексис (mC'E) является методом, который предлагает значительно более быстрое время анализа по сравнению с традиционной катионной обмен (CEX) хроматографии и капиллярной изоэлектрической фокусировки (cIEF) методы, используемые для анализа варианта заряда17 ,18. Отработанные биореакторные носители были проанализированы для отслеживания потребления аминокислот во время производства белка, поскольку это относится к изменениям в определяющих атрибутах антитела19,20,21,22 , 23.
Белковая аналитика позволяет нам определить критические параметры процесса (CPP) на основе взаимосвязи между входными данными процесса и изменениями в C'As. Во время разработки биопроцесса, выявление и измерение КТГ фундаментально демонстрирует контроль процесса и гарантирует, что продукт не изменился, что имеет важное значение в строго регулируемых производственных средах. В этой работе представлены аналитические методы измерения некоторых биохимических характеристик белка, наиболее уместного для продукта СЗА (профиль N-гликанов, варианты заряда и однородность размера).
протокол
1. Очищение антител
ПРИМЕЧАНИЕ: Буфер равновесия для внутренних антител составляет 25 мМ Трис, 100 мМ NaCl, рН 7.5. Используемый буфер элюции составляет 0,1 м уксусной кислоты. Буферы и мислины (Белок А) зависят от очищенных антител. Объем колонны эквивалентен высоте кровати министы. Объем используемой мобильной фазы определяется с точки зрения объема столбцов.
- Инициализация системы очистки
- Откройте программное обеспечение, подключенное к системе очистки. Используя инструкции ручной работы, уравновешивать столбец с буфером равновесия при скорости потока 2 мл/мин в течение 40 мин. Остановите ручной запуск после равновесия.
- В сборщике фракций поместите 15 мл конических трубок для сбора очищенных антител и конических труб 50 мл для сбора протекателей во время высокой промывки соли. Убедитесь, что сборщик фракции сбросить в начальное положение, открыв и закрыв фракционный коллектор перед началом запуска. Сборщик фракций поддерживается при 7 градусах Цельсия.
ПРИМЕЧАНИЕ: Сборщик фракции может быть сброса вручную под вкладкой Fraction Collector в настройках,как для 15 мл, так и для 50 мл труб.
- Инъекция образца
ПРИМЕЧАНИЕ: Собранная жидкость культуры клеток, используемая в следующих процедурах, была получена изклеток китайского хомяка яичников, культивированных в автоматизированных микро-биореакторах 9.- Добавьте 0,22 мкм фильтрованную жидкость культуры клеток урожая к пустому шприцу 12 мл, конец сопла которого ограничен.
- Держа шприц с насадкой лицом вниз, вставьте шприц поршень до небольшой части поршень дюйма Убедившись, что жидкость не течет, поверните шприц с насадкой вверх и снимите крышку.
- Тем не менее проведение шприц с соплом вверх, нажмите цилиндр, чтобы рассеять любой воздух, пока жидкость клеточной культуры находится на кончике сопла. Вставьте сопло шприца в порт ручного впрыска на системе очистки и закрутите, чтобы затянуть.
- Нажмите вниз на поршень, пока весь образец вводится и виден в прилагается 10 мл большой объем образца цикла.
- Откройте файл сохраненного метода. Сохранить файл результата в требуемом месте и указать имя файла при запросе. Хит запустить после образца был введен в большой цикл образца объема.
- Запуск метода очистки
- Выберите сохраненный метод и нажмите на кнопку запуска, когда вызвано инструментом программного обеспечения (шаг 1.2.5).
ПРИМЕЧАНИЕ: Система настроена для выполнения следующих шагов. Пользователю не нужно ничего делать во время работы инструмента. - Равновесие столбца с тремя громкостями столбцов (CVs) буфера равновесия при скорости потока 2 мл/мин. Как только столбец будет уравновезен, система, используя большой цикл образца объема, введет образец в столбец со скоростью потока 1 мл/мин.
- Падение УФ-сигнала на 280 нм указывает на то, что образец завершен. Вымойте столбец с буфером равновесия на скорости потока 2 мл/мин, пока уф-сигнал не упадет ниже 25 мАС.
- Используйте четыре резюме 25 мМ Tris с 1 M NaCl при рН 7,5 для выполнения вторичной высокой промывки соли при скорости потока 2 мл/мин. Коллектор фракции системы соберет любой протеин/ДНК который приходит с колонки во время мытья соли в пробках 50 mL.
- Нанесите пять резюме буфера elution со скоростью потока 1 мл/мин, чтобы снять антитела с столбца. Соберите eluate в 15 мл труб на основе УФ-сигнала; когда сигнал UV 280 превышает 35 мАС, начинается сбор; сбор заканчивается, когда сигнал опускается ниже 50 мАС; это называется пиковой резки.
ПРИМЕЧАНИЕ: Пик резки обеспечивает нормализацию elution профилей и, чтобы избежать elution пик хвост, который может содержать белковые агрегаты24. - Вымойте столбец с помощью трех резюме буфера равновесия. Пробег заканчивается после шага стирки.
- После elution немедленно нейтрализовать очищенный белок, используя 1 M Tris базы до рН в размере 5,5 евро. Измерьте концентрацию белка с помощью микротома УФ-Вис спектрофотометра на 280 нм и 260 нм и храните при 4 градусах Цельсия.
- Концентрируйте очищенные антитела с помощью центробежных единиц (шаг 2). Затем подвергните очищенное антитело гликан-анализу с помощью LC-MS и после анализа профиля агрегации с помощью SEC-MALS (шаги 3 и 4).
ПРИМЕЧАНИЕ: Очищенные антитела не должны быть заморожены без дальнейшего буферного обмена, так как частые циклы замораживания-оттепели могут вызвать агрегацию и осадки.
- Выберите сохраненный метод и нажмите на кнопку запуска, когда вызвано инструментом программного обеспечения (шаг 1.2.5).
2. Концентрация очищенных антител
ПРИМЕЧАНИЕ: Буфер Tris-ацетата 0.1 M уксусной кислоты нейтрализован с 1 M Tris Base до рН в 5,5 евро.
- Вставьте 100 kDa фильтры в центрифуговых труб.
- Вымойте фильтры с 500 л двойной дистиллированной воды. Центрифуга в течение 10 мин при температуре в комнате 14 000 х г (RT). Повторите этот шаг дважды. Откажитесь от фильтрата.
- Перенесите промытые фильтры в свежие центрифуги и добавьте 500 зл и тока образца к каждому фильтру. Центрифуга в течение 10 мин при 14000 х г.
- Перевернуть фильтр в свежую спиновой трубку. Центрифуга в течение 2 мин при 1000 х г для сбора концентрированного образца.
- Определить концентрации образцов с помощью уф-вис-спектрофотометра. Пустой спектрофотометр с помощью раствора буфера Tris-ацетата. Используйте коэффициент вымирания белка 1,37 мл (мгзсм)-1 при 280 Нм для раствора IgG 1% (% м/в).
- Используйте концентрированный образец для подготовки рабочего раствора 12,5 л 2 мг/мл для гликанового анализа и 30 л рабочего раствора для SEC-MALS.
ПРИМЕЧАНИЕ: Протокол можно приложить здесь. Образцы должны быть охлаждены при 4 градусах Цельсия. При концентрации 2 мг/мл эти образцы должны быть стабильными в течение по крайней мере трех месяцев при 4 градусах Цельсия, в то время как более высокие концентрации могут выпасть.
3. Анализ N-гликанов с использованием масс-спектроскопии
- N-Гликан маркировки и изоляции
- Начните с концентрации антител 2 мг/мл в соответствующем буфере, таком как нейтральный фосфат натрия, цитрат или буфер HEPES. Подготовьте нетронутый стандарт mAb (например, NIST mAb) на уровне 2 мг/мл для обработки вместе с экспериментальными образцами, чтобы служить положительным контролем.
ПРИМЕЧАНИЕ: Антитела должны быть в окончательном буфере, не содержащем SDS и менее 0,1 мМ нуклеофилов (таких как Tris, DTT, глицин или гистидин). SDS в буфере выборки должны быть удалены. Если нуклеофилы находятся в буфере, то разбавьте их вниз или выполнить буферный обмен, так как они будут мешать комплекту. Общий протокол снабжен набором гликанов. - Разбавить 7,5 л антител с 15,3 л воды LC-MS-класса в 1 мл труб, обеспеченных комплектом, а затем денатурировать с помощью 6 qL 5% раствора фермент-дружественных и MS-дружественных сурфактант при 90 кв КС в течение 3 мин.
- Охладите образцы в течение 3 мин до комнатной температуры (RT). Затем добавьте 1,2 злиц PNGase F и инкубировать в течение 5 мин при 50 градусах Цельсия.
- После охлаждения 3 мин на RT, этикетка расщепляется N-гликанов, добавив 12 л. флуоресцентного пометки реагента, растворенного в ангирусном диметилформамидина (DMF) и ждать 5 мин. Разбавить помечены N-гликан смеси с 358 л ацетонитрила (ACN).
- Поместите гидрофильные взаимодействия хроматографии (HILIC) пластины в вакууме многообразия с оболями и отходов лоток. Используйте многоканальный пипетку для большого количества образцов.
- Состояние скважин с 200 л воды, где вакуум регулируется так жидкость будет принимать 15-30 с пройти через hilIC мизины. Равновесие с 200 зл и 85% ACN до загрузки ACN-разбавленной маркировкой гликановой смеси (400 л), применяя вакуум после того, как каждая новая жидкость добавляется в скважины. Вымойте с помощью 600 л л 1% для мковой кислоты (ФА)/90% ACN дважды.
- Замените лоток для отходов на 600 трубк для сбора. Выделите помеченные N-гликаны с буфером elution SPE (3 elutions по 30 Л каждый) в трубки для сбора. Разбавить объединенные эмулямы с 310 Зл из разбавитель образца DMF/ACN. Pipette образцы в авто пробоотборник флаконы, чтобы быть готовым к флуоресценции (FLR)-MS анализа.
ПРИМЕЧАНИЕ: Эти образцы стабильны при хранении при -80 градусов по Цельсию в течение не менее 1 месяца. Храните пластину HILIC в оригинальной упаковке, заклеенный лентой и внутри дезикатора для использования в будущем.
- Начните с концентрации антител 2 мг/мл в соответствующем буфере, таком как нейтральный фосфат натрия, цитрат или буфер HEPES. Подготовьте нетронутый стандарт mAb (например, NIST mAb) на уровне 2 мг/мл для обработки вместе с экспериментальными образцами, чтобы служить положительным контролем.
- LC-MS анализ помеченных N-гликанов
- Проанализируйте маркированные образцы N-гликановой элуции на системе Ultra Performance Liquid Chromatography (UPLC) в сочетании с детектором флуоресценции и масс-спектротером для четырехборья (З-ТоФ). Используйте столбец, одобренный для хроматографического разделения помеченных гликанов и тепла до 60 градусов по Цельсию во время разделения.
ПРИМЕЧАНИЕ: Столбец должен быть промыт с 60% ацетонитрила и 40% H2O перед использованием: 50 резюме до первого использования или 20 резюме, если столбец был использован ранее.- Используйте 50 мМ аммония formate (AmF) (сделано с мобильным концентратом фазы) и 100% LC-MS-класса ACN для мобильных фаз. AmF чувствителен к изменениям рН и может быть пригоден к удобоввввв в течение 1 месяца после смешивания. Установите начальную скорость потока до 0,4 мл/мин, при этом градиент LC обеспечивает увеличение AmF во время фазы выдвижения.
- Установите детектор FLR для измерения на EX 265/EM 425 нм с частотой отбора проб 2 Гц. Установите режим положительной ионной чувствительности MS1, с массой 100-2000 далтонов (Da), время сканирования 0,25 секунды и приобретение данных континуума. Используйте лейцин энкефалин (2 нг/Л в 50% ACN/0.1% FA) для внутренней массовой ссылки, в режиме "Не применяйте коррекцию".
ПРИМЕЧАНИЕ: Внутренняя коррекция ссылки массы будет применена позже при обработке данных. - Повторно приостановить dextran лестницы последовательно в 22,5 зл h2O, 25 Зл Л DMF и 52,5 Л ACN. Приготовьте 10 аликвот для хранения при температуре -80 градусов по Цельсию, так как лестница не стабильна более чем на 24 ч при более высоких температурах (комнатная температура, 4 градуса по Цельсию). Dextran лестница деградирует после более чем одного цикла замораживания оттепели.
- Поместите образцы в авто сэмплер установлен до 10 градусов по Цельсию. Загрузите флакон dextran лестницы вместе с образцами, так как информация о времени хранения лестницы будет использоваться для заданий, в то время как массовая информация, используемая для проверки идентификационных данных. Используйте 10 инъекций для образцов и 7,5 инъекций для лестницы. Инъекционные образцы в тройном. Запустите загруженный метод.
- Проанализируйте маркированные образцы N-гликановой элуции на системе Ultra Performance Liquid Chromatography (UPLC) в сочетании с детектором флуоресценции и масс-спектротером для четырехборья (З-ТоФ). Используйте столбец, одобренный для хроматографического разделения помеченных гликанов и тепла до 60 градусов по Цельсию во время разделения.
- N-Гликан идентификации для данных LC-MS
- Выполняйте обработку данных с помощью программы, оптимизированной для гидрофильной взаимодействия хроматографии флуоресценции масс-спектрометрии (HILIC-FLR-MS) данных.
- Применить внутренние коррекции ссылки массы в рамках программы. Обозначьте инъекции dextran лестницы как "Стандарт" в примере информации. В методе анализаустановите время удержания соединения разделения на те из соединений лестницы, которые были обнаружены во время бега.
- Чтобы обеспечить возврат area % для идентифицированных гликанов, измените метод анализа: Под вкладкой Обработка, нажмите Параметры количественной оценки - Калибрит и установите "Тип соответствия кривой калибровки" на "Относительный ответ (%)"
4. Анализ агрегации антител с использованием SEC-MALS
- Подготовка образцов
- Перенесите 3,5 мг/мл (шаг 2) разбавленного белка на флакон со стеклянной вставкой 150 л. Используйте гель загрузки наконечник пипетка в нижний колокол вставки, чтобы избежать введения пузырьков.
- Крышка флакон с септой крышкой и немедленно проанализировать. Храните при 4-c при анализе позже.
- Конфигурация и уравновесие SEC-MALS
ПРИМЕЧАНИЕ: Анализ агрегации на SEC-MALS, настроенной с помощью сверхвысокой жидкой хроматографии (UHPLC) с детектором MALS и детектором рефракционных индексов, управляемым программным обеспечением MALS.- Настроили файл метода в программном обеспечении UHPLC для управления системой UHPLC, установив скорость потока до 0,4 мл/мин с мобильной фазой 1x фосфатного буферного соления (PBS) (разбавленного от 10x), объем впрыска до 5 л, температура колонки до 25 градусов по Цельсию , и детектор диод Array (DAD) для мониторинга 280 нм. Установите время выполнения до 20 мин. Выравнь систему, по крайней мере 4 ч до любого анализа образца.
- Интерфейс между UHPLC и multi Angle Light Scattering - Refractive Index (MALS-RI) требует использования аналогового вывода на DAD. Установите затухание DAD до 1000 mAU в файле метода DAD и настройке AU/UV до 1 (УФ-инструмент;Каналы;Канал 1).
- Включите лампу DAD за 30 минут до начала анализа и установите длину волны до 280 нм. В то же время, очистить Рефракционный индекс (RI) эталонной ячейки в течение 15 минут или до тех пор, пока базовый установится, а затем закрыть справочную ячейку.
- Настроили последовательность программного обеспечения SEC-MALS, установив время сбора до 12 мин, объем впрыска до 5 л, dn/dc до 0,185 мл/г, коэффициент вымирания A280, если ранее экспериментально определено или до 1,37 мл .)-1, и концентрация Образец. Нажмите Run и ждать "ожидание вводить" диалог появится на экране.
ПРИМЕЧАНИЕ: Коэффициент вымирания A280 специфичен для белка, интересуемого, и должен определяться экспериментально. - Назначьте список образцов в программном обеспечении UHPLC в том же порядке, что и в программном обеспечении MALS-RI, и отправьте его.
ПРИМЕЧАНИЕ: Важно запустить проверку пригодности системы до и после запуска. Бойвин сыворотки альбумин обычно используется для проверки пика расширения, знак того, что колонка SEC, возможно, потребуется очистка или замена. Та же стандартная инъекция BSA может быть использована для определения выравнивания сигналов, расширения пика и нормализации детекторов.
-
Агрегированный анализ с программным обеспечением MALS
- Нажмите на вкладку отмеченные Процедуры. Указать минимальный уровень требуемого уровня? ни один из них, как правило, является достаточным.
- Убедитесь, что базовые линии были нарисованы правильно и при необходимости корректируются для КАНАЛов LS1, LS2, LS3, RI и УФ-излучения. Установите пиковую область интереса.
- Просмотрите распределение молекулярной массы, чтобы подтвердить, что так называемые пики содержат частицы аналогичного размера.
5. Анализ варианта заряда
- Подготовка и маркировка образцов
- Начните с 80 л антитела 3,5 мг/мл. Обезсоль образец с помощью 0,5 мл десолютирующей колонны (7k MWCO). Подготовьте колонку, сначала отсвативсив нижнюю пробку, затем ослабив верхнюю пробку и поместив ее в микроцентрифугу мощностью 1,7 мл. Центрифуги опреснительной колонки в течение 1 мин при 1500 х г.
ПРИМЕЧАНИЕ: Отметьте внешний вид колонны точкой, чтобы она была помещена в исходную ориентацию для следующих шагов. - Перенесите колонку в новую микроцентрифужную трубку. Добавьте 80 л разбавленного белка в верхнюю часть столбца. Выровнять столбец с исходной ориентацией. Центрифуга в течение 2 мин при 1500 х г. Удалите образец из центрифуги, отбросьте опреснительную колонку и хорошо перемешайте образец.
ПРИМЕЧАНИЕ: Дезалостирование требуется только в том случае, если матрица образца содержит первичные амины, эксциенты, которые будут возмущать образец электрофорез, или другие несовместимые вещества. - Разбавить образец до конечной концентрации 2 мг/мл в объеме 25 л и добавить 5 зл и l буфера маркировки (см. Таблица материалов: Набор реагента chargeVariant) в 96-хорошей пластине. Подготовка маркировки реагента путем разбавления необходимого количества маркировки реагента (см. Таблица материалов: Заряд Вариант реагента Kit) 1:30 в диметилформамид. Инкубировать образец в течение 10 минут при комнатной температуре вдали от света.
ПРИМЕЧАНИЕ: Важно, чтобы оттаять, а затем немедленно использовать этот реагент и использовать его в течение 10 минут смешивания с DMF. - После инкубации добавьте 60 л реагента и хорошо перемешайте путем трубачания. Накройте тарелку уплотнением и центрифуги яму на 1000 х г в течение 1 мин.
- Начните с 80 л антитела 3,5 мг/мл. Обезсоль образец с помощью 0,5 мл десолютирующей колонны (7k MWCO). Подготовьте колонку, сначала отсвативсив нижнюю пробку, затем ослабив верхнюю пробку и поместив ее в микроцентрифугу мощностью 1,7 мл. Центрифуги опреснительной колонки в течение 1 мин при 1500 х г.
- Подготовка чипа варианта заряда
- Подготовьте чип Charge Variant, удалив раствор для хранения и стирку колодцев 1, 3, 4, 7, 8 и 10 с водой. Затем замените воду с pH 7.2 работает буфер (см. Таблица материалов: Заряд Вариант реагента Kit).
- Добавьте 750 кЛ рН 7.2 бегущего буфера к буферной трубке и поместите буферную трубку в указанное место на верхнем левом углу лотка образца. Теперь снимите уплотнение пластины с 96-хорошей пластины, нажмите Разгрузить плиту на пользовательском интерфейсе инструмента, и вставьте пластину в лоток образца GXII.
ПРИМЕЧАНИЕ: для этого анализа использовались буферы pH 7.2. pH 5.6-7.2 буферы могут быть использованы в зависимости от белка pI. При использовании более низких буферов pH может потребоваться большевремени времени выполнения образца. - Нажмите кнопку «Разгрузить чип» на пользовательском интерфейсе. Убедитесь, что электроды свободны от каких-либо частиц, а если нет, очистить с ворсом свободной тампоном. При вставке чипа убедитесь, что окно в центре чипа свободно частиц или пятен. При необходимости, очистить с ворсом мягкой тканью.
ПРИМЕЧАНИЕ: При работе с капиллярными электрофорасными чипами, удалите буфер вакуумным аспиризацией, а затем немедленное добавление следующего раствора для предотвращения высыхания скважин. Чтобы свести к минимуму введение пузырьков, наниденьте технику обратного трубача. При обработке чипа помните о хрупком капилляре, простирающихся от нижней части чипа, убедившись, что он не высохнет и не прорвется через грубую обработку. - Закройте крышку к чип-камере и выберите анализ HT Protein Charge Variant. Нажмите кнопку "Запуск". Следуйте подсказкам, чтобы выбрать образец скважин, тип пластины, время асссы (68, 90 или 100 с) и имя файла. Нажмите Кнопка Начало в конце запросов.
- Чип очистки требует промывки каждого колодца 2x с водой, а затем добавление хранения буфера (см. Таблица материалов: Заряд Вариант реагента Kit). Оказавшись в буфере хранения, замените чип в инструменте и, по промединиваемому, выберите анализ заряда белка HT. На главном экране выберите Wash на пользовательском интерфейсе. После завершения, удалить чип, протрите электроды с водой и без ворса тампон, и хранить чип на 4 градусов по Цельсию.
- Анализ варианта заряда
- Откройте программное обеспечение для анализа приборов. Импорт перспективе, перейдя к Файла)gt;Импорт данных файл... и нажав на нужный файл .gxd. Только название будет перенесено на программное обеспечение, так что переименование скважин выгодно (Инструменты Выберите файлы, которые будут экспортироваться, удерживая сдвиг при выборе файлов. Нажмите Файл»gt;Экспорт... и выберите поле Raw Data, а затем поле формата A.
- Откройте вкладку Browse Projects в программном обеспечении для анализа. Нажмите на базу данных и импортные данные... Файлы CDF.
- После импорта перейдите на вкладку «Инъекции», выберите файлы для анализа, нажмите правой кнопкой мыши и перейдите к Process... В окне, которое всплывает, выберите флажок рядом с process и выберите радиополе "Использование заданного метода обработки" и желаемого метода обработки из выпадающей коробки. В выпадающем поле сразу ниже с надписью "Как:" выберите калибровку и количественный. После обработки перейдите на вкладку «Результаты» и проверьте интеграцию хроматограмм.
ПРИМЕЧАНИЕ: Метод обработки должен быть проверен для каждого метода. В качестве отправной точки параметры, используемые для текущего метода обработки, включены в дополнительный файл.
ПРИМЕЧАНИЕ: Экспорт данных может осуществляться в форме отчета или экспортироваться только пиковая количественная оценка. Это может быть сделано в то же время, как обработка или из окна результатов.
6. Анализ аминокислот
- Настройка стандартной кривой для абсолютной количественной оценки аминокислот по LC-MS
- Подготовка расширенной аминокислоты (EAA) смесь путем растворения 59,45 мг Asn, 59,00 мг Hyp, 65,77 мг Глн, и 91,95 мг Trp в 25 мл 0,1 N HCl. Окончательная концентрация каждой аминокислоты в смеси EAA составляет 18 нмоль/Л.
- Подготовьте раствор запаса внутреннего стандарта (ISTD), растворив 58,58 мг Нва и 44,54 мг Сар в 50 мл HCl.
- Подготовка полного аминокислоты стандартов путем объединения аминокислоты бульон решение, содержащее Ала, Asp, Arg, Cys, Glu, Gly, Его, Ile, Leu, Met, Phe, Pro, Ser, Thr, Trp, Tyr, Val на 1 нмоль / Л каждый с EAA смесь для окончательного аминокислоты концентрации 900 , 225, 90, 22,5, и 9 моль / Л. Добавьте подготовленный запас ISTD к аминокислотным стандартам для конечной концентрации либо 90 пмоль/Л, либо 900 моль/Л для создания "низких" и "высоких" внутренних стандартов для использования в качестве позитивного контроля для метода.
- Поместите концентрации аминокислот в пробных флаконах в автосэмпере UPLC. Создание кривой калибровки (от 9 до 900 моль/Л) в программном обеспечении прибора на основе стандартных концентраций аминокислот с использованием следующих инструкций.
- Используйте режим ионизации электроспрея (ESI) в режиме положительной чувствительности в сочетании с UPLC для анализа нетронутых аминокислот. Для хроматографического разделения используйте нормальный фазовый столбец, изготовленный для разделения аминокислот. Подготовьте следующие буферы с реагентами класса масс-спектрометрии: ацетонитрил - 0,1% для метакислоты и B - 100 мМ аммония formate. Установите скорость потока LC до 0,6 м/мин, а столбик и температуру колонки - до 40 градусов по Цельсию.
- Используйте следующие 15-минутные условия градиента для разъединения аминокислот: 14% B (0-3 мин), 14-100% B (3-10 мин), 100% B (10-13 мин), 100-8% B (13-14 мин), 8% B (14-15 мин).
- Используйте колонки "Тип образца" и "Conc A" в программе приобретения MS для создания кривой калибровки для будущего анализа сырого биореактора в программе количественной оценки. Чтобы эти столбцы отображались в программе приобретения, используйте команду Customize Display при нажатии правого нажима на верхнем меню.
- Тип образца для стандартов аминокислот будет "Стандартный", в то время как образцы носителей будут "Аналит". Заполните столбец "Conc A" с числовыми концентрациями стандартов в требуемых единицах (экс: пмоль/Зл).
- Выполнить подготовленные аминокислоты стандартных концентраций по крайней мере в два раза. Проверить, что прибор UPLC и масс-спектрометр работают должным образом, проверяя пики ISTD.
- Для создания метода количественной оценки (файл «Edit Method» — «Метод отодвигать» в приложении к количественной оценке). Определите все аминокислоты, представляющие интерес в применении квантитарии, такие как значение соединения, значение м/з и ожидаемое время удержания. Измените параметры интеграции метода здесь.
- Используйте созданный метод аминокислот на стандартных образцах для создания кривой калибровки. Эта кривая может быть экспортирована в файл q.cdb для использования в образцах мультимедиа с помощью команды Экспорта и Калибрации...
- В приложении к количественной оценке сохраните желаемый макет в файле q.qlt, чтобы применить сярпричку к будущим наборам данных с помощью «Сохранить Layout As...». Имя (имя инъекций), область и Conc являются наиболее важными выходными столбиками.
- Аминокислотный анализ сырого биореакторного носителя от LC-MS
- Centrifuge сырой биореактор средств на 1,962 х г в течение 5 минут и пройти через 0,22 мкм фильтра.
- Последующие с перхлорной кислоты очистки для удаления белка и твердых частиц: смешать фильтрованные биореакторы с 0,4 N HClO4 в соотношении 1:1 и центрифуги на 14700 х г в течение 5 минут на RT. Соберите уточненных средств массовой информации в автосэмпемер флаконы.
ПРИМЕЧАНИЕ: Отрегулируйте объем инъекций по мере необходимости, чтобы концентрации аминокислот попали в диапазон калибровки. В зависимости от прибора, объем инъекций может быть скорректирован между 0,1 л и 10 Зл. - Запуск образцов мультимедиа в трипликате по LC-MS. Используйте "Процесс образцы" в рамках программы количественной оценки вместе с методом (.mdb) и калибровки файла (.cdb). Метод и кривая калибровки будут автоматически применены к пробам сырой мультимедиа в приложении кколичественности после завершения всех инъекций.
- Для экспорта данных для анализа в другой программе(например, в электронной таблице) используйте команду «Печать» и создайте файл q.xps или q.pdf.
Результаты
Собранная клеточная культура жидкости из автоматизированного микромасштабного биореактора очищается с помощью быстрой белковой жидкой хроматографии (FPLC), как видно на рисунке 1, а критические качества очищенных белков (КЗА) характеризовались различными аналитические методы. Это ключевое преимущество автоматизированной системы микробиореакторов; различия в СЗА могут быть быстро оценены по широкому кругу условий. N-гликанов данные из CHO производства mAbs, которые обрабатываются масс-спектрометрии должны выглядеть как хроматограммы показано на рисунке 2. На рисунке изображено сравнение двух хроматограмм, показывающих, что пик маннозы 5 (M5) из одного образца значительно ниже. Если вместо пиков наблюдается только шумная базовая линия, это может означать, что установка хроматографии неисправна или что процедура не является успешной. С помощью элементов управления можно упростить устранение неполадок. Во-первых, оценить пики FLR с dextran лестницы; эти пики указывают на то, что хроматографическая система работает правильно. Затем сравните экспериментально полученные пики с пиками, полученными из обработанного стандарта mAb. Если пики стандарта видны, но пики образца не определены, то образцы mAb были обработаны неправильно. Это может быть связано с присутствием SDS или нуклеофилила в буфере, мешающим N-гликанской маркировке и очистке.
SEC-MALS может быть использован для оценки еще двух КЗА: профиля агрегации и молекулярного веса антител. Представительная хроматограмма SEC-MALS сравнима с той, которая показана на рисунке 3. Распределение молекулярной массы и абсолютный молекулярный вес были определены с помощью необходимого программного обеспечения с коэффициентом вымирания 1,37 мл (мг/см)-1 и dn/dc 0,185 мл/г. Поскольку пиковое вызов и настройка базового значения в программном обеспечении выполняются вручную, результаты могут незначительно отличаться от пользователя к пользователю. Абсолютный молекулярный вес мономерного IgG1 с рисунка 3 составляет 1,504 х 105 Да 0,38% (синий) и комплекс высшего порядка 7,799 х 10Da и 3,0% (красный). Polydispersity агрегатов гораздо больше, чем у мономера, о чем свидетельствует распределение массы красного моляра Пика 1(рисунок 3). Небольшое количество выборки и важность агрегации в качестве КЗА делают этот метод весьма ценным дополнительным аналитическим инструментом для автоматизированной системы микробиореактора.
Результатом мЗЗе является электроферограмма, например, на рисунке 4, который показывает профиль варианта заряда для моноклонального антитела. Профиль является уникальной подписью для исследуемого белка и очень чувствителен к действующему рН. Также виден пик свободного красителя слева от профиля варианта заряда. При установлении операционного рН оператору есть определенное усмотрение, чтобы сбалансировать разрешение и сигнал; кроме того, оператор должен обеспечить хорошее отделение от пика свободного красителя, который мигрирует на 30 с. Образец может быть опреснена после маркировки, чтобы удалить этот пик, хотя это приводит к значительной потере сигнала. Как только рабочая рН установлена, профили образца можно сравнить. Хотя в целом последовательно, изменения в эффективности маркировки или различия в excipients может привести к незначительным различиям в миграции образца и заряда вариант профиля делает электроферограммы трудно непосредственно сравнить. Вместо этого метод сравнения обычно основывается на процентах основных, основных и кислых видов. В этом случае относительные различия, как малые, как 1-2% могут быть определены с помощью mCE.
Потребление аминокислот можно контролировать, чтобы определить, является ли истощение причиной изменений в Ца. Хроматограмма считывания из масс-спектрометра могут быть использованы для оценки успешного создания кривой калибровки для абсолютной количественной оценки аминокислот в сырых биореакторных медиа-пробах. На рисунке 5 изображены два общих ионных хроматограммы (TIC) и один извлеченный ионный хроматограмма (XIC) в качестве репрезентативного результата в ходе этого процесса. На рисунке 5Aпоказанный ТИК изображает фоновый сигнал из буферной системы, когда был введен только заготовка воды. Рисунок 5 B изображает репрезентативную ТИК аминокислотного стандарта, где, по сравнению с пустой водой, можно наблюдать небольшие пики, соответствующие отдельным аминокислотным видам (например, лизин на 7,96 минут). Для интеграции пика и облегчения количественной оценки пиковой области (и, следовательно, концентрации) используется XIC, где отображается только сигнал из определенного "хромограммного массового окна". В зависимости от чувствительности прибора и качества хроматографического разделения оптимальное массовое окно должно определяться пользователем. В этом примере(Рисунок 5C),XIC из лизин (м /z 147.1144) с массовым окном 10 промилле показано, где лизин в аминокислоты стандарта elutes от столбца на 8,03 минут.
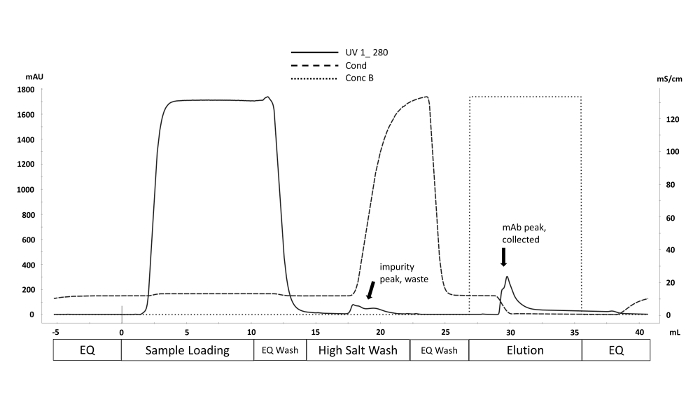
Рисунок 1 . Представительная хроматограмма схемы очистки с использованием метода быстрой протеиновидной хроматографии (FPLC). Фазы метода очистки, соответствующие объему (мЛ), маркируются по всей оси x. УФ-абсорбция на уровне 280 нм (mAU y-axis, твердая линия) контролируется на протяжении всего цикла очистки. Неспецифически связанные примеси вытесняются повышением проводимости (mS/cm y-axis, пунктирная линия) во время высокосолевой вымойки. Антитела вытесняется из столбца Protein A с введением элютионного буфера (Conc B, пунктирная линия), когда рН уменьшается до 4 (не показано). Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
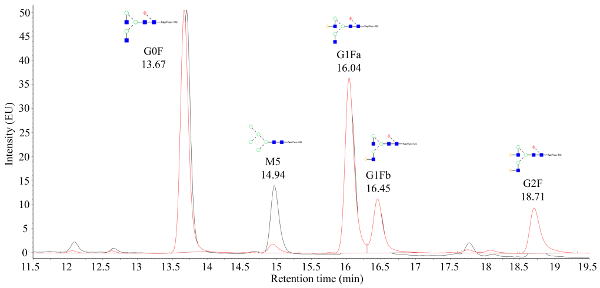
Рисунок 2. Представитель флуоресценции хроматограмма, полученная из помеченных гликанов, которые являются массовыми проверками. X-оси время удержания (минуты), в то время как y-оси интенсивности сигнала. Пик в 14.94 мин представляет собой гликан Mannose 5 (M5), где между двумя накладными образцами наблюдается большая разница между силой сигнала M5. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
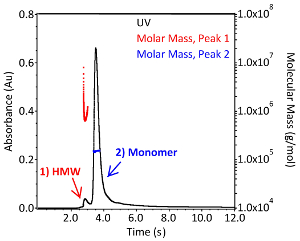
Рисунок 3. Молекулярное распределение веса моноклональных антител IgG1. Хроматограмма нетронутого моноклонального антитела IgG1, разделенная по размеру исключения хроматографии в 1x PBS (pH7.4). Абсорбция контролируется на уровне 280 нм (черная; левая ось) и для расчета абсолютного молекулярного веса каждого пика (красный и синий; правая ось) использовались детекторы рассеяния и рефракционных индексов. Виды с высоким молекулярным весом обозначены пиком с надписью "HMW". Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.

Рисунок 4 . Профиль варианта заряда моноклонального антитела IgG1. Эта электроферограмма генерируется на платформе mC'E. Пик свободного красителя мигрирует на 30 с и хорошо отделен от IgG1. Для количественной оценки пики были разделены на основные, основные и кислые виды с использованием программного обеспечения для анализа данных приборов. Красная линия определяет интегрированные пиковые области. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
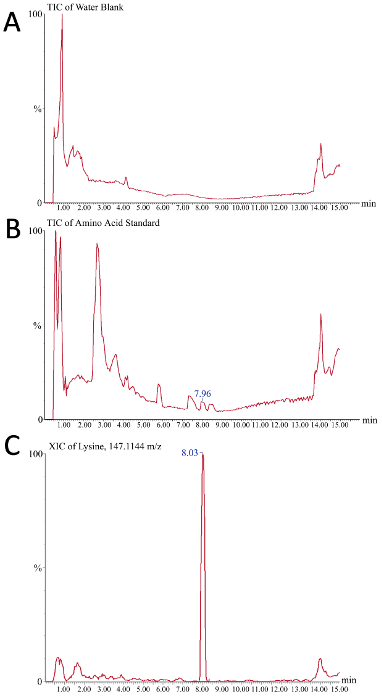
Рисунок 5. Репрезентативные результаты ионных хроматограмм для анализа аминокислот на основе масс-спектрометрии сырых биореакторных носителей. X-ось времени (минут), в то время как y-оси интенсивности сигнала (A) пустой воды служит в качестве отрицательного контроля и показывает фоновый сигнал наблюдается в течение жидкой хроматографии градиента (B) 225 пмоль / L аминокислоты стандарт используется здесь в качестве положительного контроля, так как отдельные пики, наблюдаемые в этой общей хроматограмме иона, представляют различные аминокислоты стандартной смеси, разрешаемой хроматографически (C) Представитель извлеченный ионный хроматограмма для m /z 147.1144, который является лизин. Пик 7,96 мин в B соответствует пику 8,03 в C лизин. Пожалуйста, нажмите здесь, чтобы просмотреть большую версию этой цифры.
Обсуждение
HCCF содержит мусор и крупные частицы, которые могут засорять и уничтожать дорогостоящие приборы, поэтому перед дальнейшей обработкой ниже по течению необходимо прояснение культуры. Центрифугация, как правило, первый подход к отдельным клеткам и другим нерастворимым частицам от белков с последующей фильтрацией. Этот отфильтрованный HCCF затем подвергается быстрой протеиновидной жидкой хроматографии (FPLC) для очистки. Очистка HCCF от автоматизированных микробиореакторов для получения продукта является важным шагом в обработке ниже по течению. Здесь для получения моноклональных антител от HCCF используется система fPLC с колонкой белка А. Аналитика для процессов восходящего потока может дать полезную информацию о поведении клеток и руководство дизайн биопроцесса, помогая получить последовательный и надежный качественный продукт. Аналитика также позволяет нам связывать критические атрибуты качества (КЗА) с процессами вверх и вниз по течению. Здесь представлены четыре анализы, которые обычно используются в характеристике моноклональных антител. Эти методы являются надежными, надежными и легко развертываемыми для анализа процессов и продуктов из различных источников, которые лишь частично очищены и могут по-прежнему содержать остаточные уровни ДНК и HCP.
При очистке образцов для аналитики необходимо найти важный баланс между созданием образца, достаточно чистого для анализа, сохраняя при этом изменчивость, присутствующую в биореакторе. Двумя наиболее распространенными загрязняющими веществами, влияющими на продукт, являются ДНК и HCP, которые могут быть проверены путем измерения абсорбции соотношения на уровне 260/280 нм и через SDS-PAGE или ЗСЕ-СДС. Представленные здесь анализы не чувствительны к низким уровням содержания ДНК. Чистота продукта является чистым, как это определено в соответствии с «CE-SDS».
Анализ варианта заряда с системой микрокапиллярного электрофорасиса обеспечивает высокопроизводительный метод для определения вариантов заряда, с чипами и реагентами, которые относительно просты в реализации. Характер техники и химия реагента маркировки чувствительны к excipients и другим главным образом amines, таким образом требуя шаг опреснения для большинств матриц образца. По опыту, низкие уровни ДНК комигрируют со свободным красителями от реакции маркировки и не влияют на качество результатов. В то время как вариативность основной, основной и кислой пиковой количественной оценки, как правило, является йт-1, более высокие уровни ДНК и других загрязняющих веществ могут увеличить изменчивость анализа. Чрезвычайно важно быть в соответствии с маркировкой белка и обеспечить оперативное использование DMF после удаления из бутылки и смешивания с красителя. В качестве контроля маркировки рекомендуется использовать стандарты лизин и/или гистидина. С течением времени и в зависимости от качества образца, чипы могут фол или потерять покрытие на микрофлюидных каналов, что приводит к большему шуму, наличие призрак пиков, и больше выборки к образцу изменения. Для выявления этого явления с регулярными интервалами одновременно анализировались пробелы и стандарт пригодности системы (т.е. NISTmAb). При возникновении проблем с чипами чипы можно промыть раствором для хранения или заменить.
Методы, используемые для гликанового анализа терапевтических гликопротеинов, в первую очередь включают в себя жидкую хроматографию (LC) и/или масс-спектрометрию (MS), при этом анализ микроаррей лектин набирает популярность в качестве третьего варианта25. Метод, описанный в настоящем документе, использует как LC, так и MS, который имеет преимущества и недостатки. Масс-спектрометрические методы имеют преимущество массовой проверки проанализированных гликанов, что невозможно с помощью LC-методов с использованием флуоресцентного обнаружения выход или лектин microarrays. Этот метод использует обнаружение LC и флуоресценции для присвоения гликанов идентификационных данных, используя сравнение времени удержания к стандарту dextran лестницы. Мониторинг флуоресценции позволяет повысить чувствительность и количественную оценку в связи с легкостью его обнаружения, где MS только не может быть в состоянии количественно низкого изобилия видов из-за низкой эффективности ионизации олигосахаридов. Массовая информация от MS используется для подтверждения гликановых идентификационных данных, но программное обеспечение для обработки не использует массовую информацию в качестве основного критерия назначения. Таким образом, без воспроизводимой хроматографии и легко разрешимых пиков, этот метод может пострадать в отношении гликанских заданий. К счастью, массовая информация может помочь с гликанзан назначений даже в ситуациях, когда хроматография является subpar, таких как сдвиги во времени удержания, которые препятствуют воспроизводимых назначений гликанов. Если этот метод используется без MS, хроматография должна быть на самом высоком уровне, так как массовая информация не может быть использована для коррекции для дрейфа времени проживания.
Метод анализа аминокислот, описанный здесь, использует LC-MS для быстрой количественной оценки недоивтатных аминокислот в сырых средствах культуры клеток. Альтернативные методы анализа аминокислот требуют аминокислотных агентов производнозации, чтобы уф-обнаружить26. Метод LC-MS предлагает важные преимущества перед методом LC-UV: он позволяет идентифицировать на основе времени удержания и ионной массы, в отличие от метода LC-UV, который ограничен отсутствием массовой характеристики. Кроме того, метод LC-MS предлагает преимущества времени и воспроизводимости, так как метод LC-UV требует длительной реакции производной, которая может придать изменчивости образца27. Тем не менее, инъекция сырой среды культуры клеток в методе LC-MS может вызвать пагубное воздействие на сигнал MS из-за ионного скиммера загрязнения. Калибровка лестницы вводится часто в качестве проверки пригодности системы, и выборка порядка рандомизированы для предотвращения предвзятости в данных.
Процесс культуры клеток для производства антител с использованием микробиореакторов ранее описано 9. В этом исследовании четко определены подробные протоколы для методов характеристик моноклональных антител, которые максимизируют данные, полученные из ограниченных объемов выборки. Ограниченное количество собранной жидкости клеточной культуры иногда может ограничить полученную информацию о продукте, и выбор правильных аналитических процедур для получения данных о качестве продукции имеет важное значение. Аналитика важна для объединения параметров процесса восходящего потока с изменениями в качестве продукции. Здесь предусмотрено руководство для пользователей для характеристики mAbs при работе с микробиореакторами.
Раскрытие информации
Эта публикация отражает мнения автора и не должна быть истолкована как представляющая взгляды или политику FDA.
Благодарности
Авторы хотели бы поблагодарить Скотта Лютза за аналитическую поддержку, оказанную им. Частичное внутреннее финансирование и поддержка этой работы обеспечивается Программой критического пути CDER (CA #1-13). Этот проект частично поддерживается назначением на стажировку/программу участия в исследованиях в Управлении биотехнологических продуктов, Управление по контролю за продуктами и лекарствами США, находящемся в ведении Института науки и образования Оук-Ридж, через межведомственное соглашение между Министерством энергетики США и FDA.
Материалы
| Name | Company | Catalog Number | Comments |
| CHO DG44 Cell Line | Invitrogen | A1100001 | |
| Akta Avant 25 | General Electric Life Sciences | 28930842 | |
| Pro Sep vA Ultra Chromatography Resin | Millipore Sigma | 115115830 | Purification Stationary Phase |
| Omnifit 10cm Column | Diba Fluid Intelligence | 006EZ-06-10-AA | Housing for Stationary Phase |
| Tris Base | Fisher Scientific | BP154-1 | |
| Superloop 10 mL | GE Healthcare | 18-1113-81 | |
| µDawn Multi Angle Light Scattering Detector | Wyatt | WUDAWN-01 | |
| 0.22 µm Millex GV Filter Unit PVDF Membrane | Merck Millipore | SLGV033RB | |
| 10X Phosphate Buffered Saline | Corning | 46-013-CM | |
| 12 mL Syringe | Covidien | 8881512878 | |
| 1290 Infinity Binary Pump | Agilent Technologies | G4220A | |
| 1290 Infinity DAD | Agilent Technologies | G4212A | |
| 1290 Infinity Sampler | Agilent Technologies | G4226A | |
| 1290 Infinity Thermostat | Agilent Technologies | G1330B | |
| 1290 Infinity Thermostatted Column Compartment | Agilent Technologies | G1316C | |
| 15 mL Falcon tube | Corning Inc. | 352097 | |
| 150 uL Glass Inserts with Polymer Feet | Agilent Technologies | 5183-2088 | |
| 50 mL Falcon tube | Corning Inc. | 352070 | |
| 96-Well Plate | Bio-Rad | 127737 | |
| Acetic Acid | Sigma-Aldrich | 695072 | |
| Acetonitrile | Fisher Chemical | BPA996-4 | |
| ACQUITY I-Class UPLC BSM | Waters Corporation | 18601504612 | |
| ACQUITY I-Class UPLC Sample Manager | Waters Corporation | 186015000 | |
| ACQUITY UPLC FLR Detector | Waters Corporation | 176015029 | |
| Amicon Ultra-4 100 kDa centrifugal filters | Merck Millipore | UFC810096 | |
| Amino Acid Standard, 1 nmol/µL | Agilent Technologies | 5061-3330 | |
| Amino Acid Supplement | Agilent Technologies | 5062-2478 | |
| Ammonium Formate Solution - Glycan Analysis | Waters Corporation | 186007081 | |
| Blue Screw Caps with Septa | Agilent Technologies | 5182-0717 | |
| CD OptiCHO AGT Medium | Thermo Fisher Scientific | A1122205 | |
| Centrifuge Tubes | Eppendorf | 22363352 | |
| Charge Variant Chip | Perkin Elmer | 760435 | |
| Charge Variant Reagent Kit | Perkin Elmer | CLS760670 | |
| Chromatography Water (MS Grade) | Fisher Chemical | W6-4 | |
| Dimethylformamide | Thermo Scientific | 20673 | |
| Extraction Plate Manifold for Oasis 96-Well Plates | Waters Corporation | 186001831 | |
| Formic Acid | Fisher Chemical | A117-50 | |
| GlycoWorks RapiFlour-MS N-Glycan Starter Kit - 24 Sample | Waters Corporation | 176003712 | |
| GXII Buffer Tubes | E&K Scientific | 697075- NC | |
| GXII Detection Window Cleaning Cloth | VWR | 21912-046 | |
| GXII HT Touch | Perkin Elmer | CLS138160 | |
| GXII Ladder Tubes | Genemate | C-3258-1 | |
| GXII Lint-Free Swab | ITW Texwipe | TX758B | |
| Hydrochloric Acid | Fisher Scientific | A144-500 | |
| Intact mAb Mass Check Standard | Waters Corporation | 186006552 | |
| Intrada Amino Acid Column 150 x 2 mm | Imtakt | WAA25 | |
| NanoDrop One Microvolume UV-Vis Spectrophotometer | Thermo Fisher Scientific | 840274100 | |
| Optilab UT-rEX Differential Refractive Index Detector | Wyatt | WTREX-11 | |
| Perchloric acid | Aldrich Chemistry | 311421 | |
| Pipet Tips with Microcapillary for Loading Gels | Labcon | 1034-960-008 | |
| Polypropylene 96-Well Microplate, F-bottom, Chimney-style, Black | Greiner Bio-One | 655209 | |
| RapiFlour-MS Dextran Calibration Ladder | Waters Corporation | 186007982 | |
| Screw Top Clear Vial 2mL | Agilent Technologies | 5182-0715 | |
| Sodium Chloride | Fisher Scientific | S271-1 | |
| Sodium Iodide | Sigma Aldrich | 383112 | |
| TSKgel UP-SW3000 4.6mm ID x 30 cm L | Tosoh Biosciences | 003449 | |
| UNIFI Scientific Information System | Waters Corporation | 667005138 | |
| Vacuum Manifold Shims | Waters Corporation | 186007986 | |
| Vacuum Pump | Waters Corporation | 725000604 | |
| Xevo G2 Q-ToF | Waters Corporation | 186005597 | |
| Zeba Spin Desalting Column, 0.5 mL | Thermo Scientific | 89883 |
Ссылки
- . . Pharmaceutical cGMPs for the 21st Century: A Risk-Based Approach. , (2004).
- New Molecular Entity (NME) Drug and New Biologic Approvals. FDA Available from: https://www.dfa.gov/Drugs/DevelopmentApprovalProcess/HowDrugsareDevelopedandApproved/DrugandBiologicAprrovalReports/NDAandBLAApprovalReports/ucm373420.htm (2015)
- Foltz, I. N., Karow, M., Wasserman, S. M. Evolution and Emergence of Therapeutic Monoclonal Antibodies. Circulation. 127, 2222-2230 (2013).
- Kondragunta, B., Drew, J. L., Brorson, K. A., Moreira, A. R., Rao, G. Advances in clone selection using high-throughput bioreactors. Biotechnology Progress. 26 (4), 1095-1103 (2010).
- Hmiel, L., Brorson, K., Boyne, M. Post-translational structural modifications of immunoglobulin G and their effect on biological activity. Analytical & Bioanalytical Chemistry. 407 (1), 79-94 (2015).
- Rathore, A. S. Roadmap for implementation of quality by design (QbD) for biotechnology products. Trends in Biotechnology. 27 (9), 546-553 (2009).
- . International Council for Harminisation of Techinical Requirements for Pharmaceuticals for Human Use. ICH. , (1999).
- Berkowitz, S. A., Engen, J. R., Mazzeo, J. R., Jones, G. B. Analytical tools for characterizing biopharmaceuticals and the implications for biosimilars. Nature Reviews Drug Discovery. 11 (7), 527-540 (2012).
- Velugula-Yellela, S. R., et al. Use of high-throughput automated microbioreactor system for production of model IgG1 in CHO cells. Journal of Visualized Experiments. , (2018).
- Largy, E., Cantais, F., Van Vyncht, G., Beck, A., Delobel, A. Orthogonal liquid chromatography-mass spectrometry methods for the comprehensive characterization of therapeutic glycoproteins, from released glycans to intact protein level. Journal of Chromatography A. 1498, 128-146 (2017).
- Yang, J. -. M., et al. Investigation of the correlation between charge and glycosylation of IgG1 variants by liquid chromatography-mass spectrometry. Analytical Biochemistry. 448, 82-91 (2014).
- Agarabi, C. D., et al. Bioreactor Process Parameter Screening Utilizing a Plackett-Burman Design for a Model Monoclonal Antibody. Journal of Pharmaceutical Sciences. 104 (6), 1919-1928 (2015).
- Wen, J., Arakawa, T., Philo, J. S. Size-Exclusion Chromatography with On-Line Light-Scattering, Absorbance, and Refractive Index Detectors for Studying Proteins and Their Interactions. Analytical Biochemistry. 240 (2), 155-166 (1996).
- Veurink, M., Stella, C., Tabatabay, C., Pournaras, C. J., Gurny, R. Association of ranibizumab (Lucentis) or bevacizumab (Avastin) with dexamethasone and triamcinolone acetonide: An in vitro stability assessment. European Journal of Pharmaceutics and Biopharmaceutics. 78 (2), 271-277 (2011).
- Li, Y., Weiss, W. F., Roberts, C. J. Characterization of high-molecular-weight nonnative aggregates and aggregation kinetics by size exclusion chromatography with inline multi-angle laser light scattering. Journal of Pharmaceutical Sciences. 98 (11), 3997-4016 (2009).
- Espinosa-de la Garza, C. E., et al. Analysis of recombinant monoclonal antibodies by capillary zone electrophoresis. Electrophoresis. 34 (8), 1133-1140 (2013).
- Han, H., Livingston, E., Chen, X. High throughput profiling of charge heterogeneity in antibodies by microchip electrophoresis. Analytical Chemistry. 83 (21), 8184-8191 (2011).
- Wheeler, T. D., et al. Microchip zone electrophoresis for high-throughput analysis of monoclonal antibody charge variants. Analytical Chemistry. 86 (11), 5416-5424 (2014).
- Carrillo-Cocom, L., et al. Amino acid consumption in naive and recombinant CHO cell cultures: producers of a monoclonal antibody. Cytotechnology. 67 (5), 809-820 (2015).
- Chen, P., Harcum, S. W. Effects of amino acid additions on ammonium stressed CHO cells. Journal of Biotechnology. 117 (3), 277-286 (2005).
- Xing, Z., et al. Optimizing amino acid composition of CHO cell culture media for a fusion protein production. Process Biochemistry. 46 (7), 1423-1429 (2011).
- Fan, Y., et al. Amino acid and glucose metabolism in fed-batch CHO cell culture affects antibody production and glycosylation. Biotechnology and Bioengineering. 112 (3), 521-535 (2015).
- Read, E. K., et al. Fermentanomics informed amino acid supplementation of an antibody producing mammalian cell culture. Biotechnology Progress. 29 (3), 745-753 (2013).
- Mazzer, A. R., Perraud, X., Halley, J., O'Hara, J., Bracewell, D. G. Protein A chromatography increases monoclonal antibody aggregation rate during subsequent low pH virus inactivation hold. Journal of Chromatography. A. 1415, 83-90 (2015).
- Zhang, L., Luo, S., Zhang, B. Glycan analysis of therapeutic glycoproteins. MAbs. 8 (2), 205-215 (2016).
- Wahl, O., Holzgrabe, U. Amino acid analysis for pharmacopoeial purposes. Talanta. 154, 150-163 (2016).
- Le, A., Ng, A., Kwan, T., Cusmano-Ozog, K., Cowan, T. M. A rapid, sensitive method for quantitative analysis of underivatized amino acids by liquid chromatography-tandem mass spectrometry (LC-MS/MS). Journal of Chromatography B. 944, 166-174 (2014).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены