Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Объединенные ГЕНЕТИЧЕСКИе экраны на основе CRISPR в клетках млекопитающих
В этой статье
Резюме
Технология CRISPR-Cas9 обеспечивает эффективный метод точного редактирования генома млекопитающих в любом типе клеток и представляет собой новое средство для выполнения генетических экранов генома. Здесь представлен подробный протокол, в котором обсуждаются шаги, необходимые для успешного выполнения объединенных экранов CRISPR-Cas9, в масштабах всего генома.
Аннотация
Редактирование генома с помощью системы CRISPR-Cas значительно повысило способность точно редактировать геномы различных организмов. В контексте клеток млекопитающих, эта технология представляет собой новое средство для выполнения генома всей генетические экраны для функциональных исследований геномики. Библиотеки направляющих РНК (sgRNA), ориентированные на все открытые кадры чтения, позволяют легкому поколению тысяч генетических возмущений в одном пуле клеток, которые могут быть проверены на конкретные фенотипы для вовлечения функции гена и клеточных процессов в беспристрастной и систематической образом. Экраны CRISPR-Cas предоставляют исследователям простой, эффективный и недорогой метод раскрытия генетических чертежей клеточных фенотипов. Кроме того, дифференциальный анализ экранов, выполняемых в различных клеточных линиях и из различных типов рака, может определить гены, которые имеют контекстуально важное значение в опухолевых клетках, выявляя потенциальные цели для конкретных противоопухолевых методов лечения. Выполнение геномных экранов в клетках человека может быть сложной задачей, так как это предполагает обработку десятков миллионов клеток и требует анализа больших наборов данных. Детали этих экранов, такие как характеристика клеточной линии, соображения библиотеки CRISPR и понимание ограничений и возможностей технологии CRISPR в ходе анализа, часто упускаются из виду. Приведен ный подробный протокол для успешного выполнения объединенных экранов на основе CRISPR-Cas9 в масштабах всего генома.
Введение
CRISPR-Cas, сокращение от кластерных регулярно межпространственных коротких палиндромных повторов и связанных с CRISPR нуклеаза, состоит из одного белка nuclease (например, Cas9) в комплексе с синтетической направляющей РНК (sgRNA). Этот комплекс рибонуклеопротеинов нацелен на фермент Cas9, чтобы вызвать двухцепочечные разрывы ДНК при специфическом геномном локусе1. Двухцепочечные перерывы могут быть отремонтированы с помощью гомологии направленного ремонта (HDR) или, чаще всего, через негомологическую конечную присоединение (NHEJ), механизм ремонта, подверженный ошибкам, который приводит к вставке и/или удалению (INDELS), которые часто нарушают функцию гена 1. Эффективность и простота CRISPR позволяет ранее недостижимый уровень геномного таргетинга, что намного превосходит предыдущие технологии редактирования генома, т.е. цинковый палец nucleases (ЗНФ) или транскрипции активатор-как эффектор nucleases ( TALENS), оба из которых страдают от повышенной сложности конструкции, более низкой эффективности трансфекции, и ограничения в мультиплексном редактированиигенов 2.
Основное исследовательское применение однонаправного редактирования генома на основе РНК позволило ученым эффективно и недорого изучить функции отдельных генов и топологию генетических сетей взаимодействия. Способность выполнять функциональные экраны генома была значительно расширена с помощью системы CRISPR-Cas, особенно по сравнению с более ранними генетическими технологиями возмущения, такими как РНК-интерференция (РНК) и мутагенез генной ловушки. В частности, RNAi страдает от высоких вне цели эффекты и неполный нокдаун, в результате чего более низкая чувствительность и специфичность по сравнению с CRISPR3,4,5, в то время как методы генной ловушки являются возможными только в гаплоидных ячейки для экранов потери функций, ограничивающих область клеточных моделей, которые могут быть допрошены6. Способность CRISPR генерировать полный выбив из генов обеспечивает более биологически надежную систему для допроса мутантных фенотипов, с низким уровнем шума, минимальными эффектами вне цели и последовательной активностью реагентов5. CRISPR-Cas9 sgRNA библиотеки, которые ориентированы на весь геном человека в настоящее время широко доступны, что позволяет одновременное поколение тысяч генов нокаутов в одном эксперименте3,7,8,9 .
Мы разработали уникальные библиотеки scgRNA по всей геному CRISPR-Cas9, называемые библиотеками Toronto Knock-out (TKO) (доступны через Addgene), которые компактны и оптимизированы последовательность для облегчения функционального геномики высокого разрешения экранов. Последняя библиотека, TKOv3, ориентирована на 18 000 человеческих генов кодирования белка с 71 090 направляющих, оптимизированных для редактирования эффективности с использованием эмпирических данных10. Кроме того, TKOv3 доступен в качестве однокомпонентной библиотеки (LCV2:::TKOv3, Addgene ID #90294), выражающей Cas9 и sgRNA на одном векторе, облегчая необходимость создания стабильных клеток Cas9- Expressing, что позволяет нокаутировать геном по широкому кругу типы клеток млекопитающих. TKOv3 также доступен в векторе без Cas9 (pLCKO2::TKOv3, Addgene ID 125517) и может быть использован в ячейках, которые выражают Cas911.
Геном всей CRISPR-Cas9 редактируемых клеток населения может подвергаться различным условиям роста, с обилием sgRNAs с течением времени количественно следующего поколения секвенирования, обеспечивая считывание для оценки отсева или обогащения клеток с прослеживаемыми генетическими Возмущений. Библиотеки выбивания CRISPR могут быть использованы для определения генов, которые, после возмущения, вызывают дефекты клеточного фитнеса, умеренную чувствительность к лекарственным препаратам (например, чувствительные или устойчивые гены), регулировать экспрессию белка (например, репортер) или необходимы для определенного функции пути и клеточного состояния12,13,14. Например, дифференциальные фитнес-экраны в линии раковых клеток могут выявить как истощение, так и уменьшение онкогенов и обогащения или увеличение генов супрессоров опухолей3,14,15. Аналогичным образом, использование промежуточных доз терапевтических препаратов может выявить как лекарственной устойчивости и сенсибилизации генов16,17.
Приведенный здесь подробный протокол скрининга для генома масштаба CRISPR-Cas9 потери функции скрининга с использованием Торонто Knock-out библиотек (TKOv1 или v3) в клетках млекопитающих от библиотеки поколения, скрининг производительности для анализа данных. Хотя этот протокол был оптимизирован для скрининга с использованием библиотек Toronto Knock-out, он может быть применен и масштабируемым для всех объединенных библиотек CRISPR sgRNA.
Access restricted. Please log in or start a trial to view this content.
протокол
Эксперименты, изложенные ниже, должны следовать руководящим принципам Управления по охране окружающей среды и безопасности Института.
1. Бассейн CRISPR sgRNA лентивирусной библиотеки плазмид усиления
- Разбавить готовый CRISPR sgRNA плазмид ной ДНК библиотеки до 50 нг / Л в TE (например, TKOv3).
- Электропорат библиотеки с помощью электрокомпетентных клеток. Настроили в общей сложности четыре реакции электропорации, как описано ниже.
- Добавьте 2 л из 50 нг/Л Библиотеки ТКО к 25 л оттаятых электрокомпетентных клеток к предварительно охлажденным кюветам (1,0 мм) на льду.
- Электропорат с использованием оптимальных настроек, предложенных протоколом производителя. В пределах 10 с импульса, добавить 975 л восстановления medium (или SOC среды) в cuvette.
- Перенесите электропорированные клетки в культурную трубку и добавьте 1 мл восстановительного среднего. Инкубировать трубки в трясущемся инкубаторе при 250 об/мин при 1 ч при 37 градусах Цельсия.
- Навязайте разбавленную пластину для титрировать библиотеку и оценить эффективность преобразования.
- Бассейн все 8 мл восстановленных клеток и хорошо перемешать. Передача 10 зл и цельсия объединенных клеток в 990 л восстановительного среднего для 800-кратного разбавления и хорошо перемешайте.
- Плита 20 л разбавления на предварительно разогретой 10 см Lb и карбенициллин (100 мкг/л) агарплита пластины. Это приводит к 40000-кратному разбавлению трансформаторов, которые будут использоваться для расчета эффективности преобразования.
- Плита 400 л восстановленных клеток на каждой пластине в общей сложности 20 предварительно разогретых 15 см LB и карбенициллин агар пластин. Инкубировать тарелки для 14-16 ч при 30 градусах Цельсия.
ПРИМЕЧАНИЕ: Рост при такой более низкой температуре сводит к минимуму рекомбинацию между длинными терминальными повторами (LTR)18. - Чтобы рассчитать эффективность преобразования, подсчитайте количество колоний на 40 000-кратной раз разбавленной пластине (шаг 1.3.2). Умножьте количество колоний, подсчитанных на 40 000, чтобы получить общее количество колоний на всех плитах. Продолжить, если общее число колоний представляет собой охват библиотеки эквивалентно минимум 200x колоний на sgRNA (наиболее оптимальным является 500-1000x).
- Например, минимальный номер колонии для библиотеки TKOv3 (71 090 сГРН) составляет 1,4 х 107,что эквивалентно 200-x колониям на сгРН. Если представительство колонии недостаточно, увеличьте количество электропораций в шаге 1.2 в зависимости от количества колоний на разбавленной пластине для достижения минимального охвата библиотеки.
- Урожай колоний, как описано ниже
- К каждой 15 см пластины, добавить 7 мл LB и carbenicillin (100 мкг / л) среды, а затем соскребать колонии с помощью распределителя клеток. С помощью 10 мл пипетки перенесите выцарапанные клетки в стерильную 1 л конической колбы или бутылку.
- Еще раз промыть тарелку с 5 мл LB и карбенициллин среды и передать раствор в бутылку.
- Повторите для всех пластин, чтобы бассейн клетки из 20 пластин в стерильную бутылку.
- Смешайте собранные клетки с перемешивание бар для 1 ч при комнатной температуре (RT), чтобы разбить ячейки сгустки. Передача клеток в предварительно взвешенные центрифуги бутылки и центрифуги на 7000 х г гранулы бактерий, а затем отказаться от средств массовой информации.
- Взвесьте мокрые клетки гранулы и вычесть вес бутылки центрифуги, чтобы определить окончательный вес мокрой гранулы. Очистите плазмидную ДНК с помощью макси- или мега-шкалы плазмидной очистки комплекта в зависимости от количества бактериальных гранул каждый столбец может обрабатывать.
2. Крупномасштабная библиотека CRISPR sgRNA производства лентивирусного
ПРИМЕЧАНИЕ: Все действия в этом разделе протокола выполняются в BSL2 "объекта в классе II, Тип A2 биобезопасности кабинета.
- Рассчитайте количество 15 см пластин, необходимых для производства вируса на основе оценки, что 18 мл вируса, как правило, собирают из одной 15 см пластины.
- Подготовка клеток для трансфекции путем посева HEK-293T упаковочных клеток в низко-антибионовых средах роста (DMEM 10% FBS и опционально: 0.1x перо/strep) на 8 x 106 клеток на 15 см пластины в 20 мл носителей. Инкубировать клетки на ночь при 37 градусах Цельсия, 5% CO2. Убедитесь, что покрывало клетки 70%-80% конфлюент и равномерно распределены в момент трансфекции.
- На следующий день приготовьте три трансфекционные плазмиды смеси, изложенные в таблице 1 для 15 см пластин. Рассчитайте количество плазмиды, необходимое для одного трансфекции и сделать смесь плазмиды для количества пластин, а также один для транс-инфекции.
- Подготовьте липидный трансфекционный реагент для каждого трансфекционного реагента, как описано в таблице 2. Aliquot уменьшил осечек сыворотки в отдельные 1,5 мл микроцентрифуговых труб для числа пластин, которые будут трансфицироваться. Добавить трансфекционный реагент, аккуратно перемешать и инкубировать в течение 5 мин на RT.
- После 5 мин инкубации, добавить количество ДНК, необходимое для одного трансфекции в трансфекционный реагент для 3:1 отношение трансфекционного реагента к мкг ДНК комплекса. Смешайте осторожно и инкубировать в течение 30 минут на RT.
ПРИМЕЧАНИЕ: Последующие трансфекции могут быть подготовлены в наборах из пяти или менее, с интервалом 5 минут, чтобы оптимизировать время и избежать чрезмерной инкубации. - После 30 минут инкубации тщательно перенесите каждую смесь трансфекции на каждую тарелку упаковочных ячеек. Добавить всю смесь с помощью 1 мл пипетка отзыв dropwise в круговой, зигзагообразное движение, не нарушая монослой клетки. Инкубировать клетки при 37 градусах по Цельсию на 18 ч при 5% CO2.
- Подготовка вирусных носителей урожая: 500 мл Среднего DMEM 32 мл акций BSA (20 г/100 мл, растворенного в DMEM, фильтра стерилизованного с фильтром 0,22 мкм) 5 мл 100x пера/стрептококка.
- После 18 ч, удалить средства массовой информации (использовать надлежащее обращение с лентивирусными отходами, такими как инкубация в 1% гипохлорит натрия в течение 30 минут до удаления). Аккуратно замените 18 мл вирусных носителей урожая на каждую тарелку. Инкубировать клетки при 37 градусах по Цельсию на 18 ч при 5% CO2.
- После 24 ч, проверить упаковочные клетки для ненормальных и сросшиеся морфологии, как признак хорошего производства вируса. Затем собираем лентивирус, собирая все супернатанты и передаваясь в стерильную коническую центрифугу трубки.
- Спин сми, содержащие вирус на 300 х г в течение 5 мин и гранулы упаковочных клеток. Aliquot супернатант в стерильную трубку полипропилена, не нарушая гранулы.
- Храните вирус при 4 градусах По Цельсия в течение коротких периодов (менее 1 недели) или сразу при -80 градусов по Цельсию для длительного хранения. Крупномасштабный вирус Aliquot подготавживает к одноразовым объемам использования для длительного хранения, чтобы избежать замораживания/оттаивания.
3. Характеристика клеточной линии для скрининга
- Выберите нужную линию ячейки.
- Измерьте и запишите приблизительное время удвоения клеток.
- Определите оптимальную плотность клеточного покрытия для культивирования клеток каждые 3-4 клетки, удвоение в сосуде культуры тканей по выбору (например, 15 см пластин культуры тканей).
- Определите концентрацию пуромицина для использования в желаемой клеточной линии для выбора библиотек ТКО, содержащих маркер сопротивления пуромицину следующим образом:
- Семенные клетки в 12 хорошо пластины при плотности, необходимой для достижения слияния после 72 ч, а затем инкубировать на ночь (37 градусов по Цельсию, 5% CO2).
- На следующий день переоденьте на носитель, содержащий диапазон разбавления концентраций пуромицина от 0 мкг/мл до 10 мкг/мл, с шагом 0,5 мкг/мл. Инкубировать клетки на 48 ч.
- После 48 ч измерьте жизнеспособность клеток путем подсчета клеток или окрашивания alamarBlue.
- Определите самую низкую концентрацию, которая убивает 100% клеток в 48 ч. Используйте эту концентрацию, чтобы выбрать для библиотеки CRISPR передаваемые популяции клеток в шагах 4.6 и 5.2.6.
ПРИМЕЧАНИЕ: Для клеточных линий с более длительным удвоением времени можно переносить более длительные инкубации с пуромицином. В таких ситуациях определите кривую убийства для инкубационного времени, необходимого для удвоения ячейки в йт;3. Свести к минимуму время отбора, чтобы избежать отсева основных генов до начала скрининга.
- Проверьте клетки на чувствительность к бромистому гексадиметрину (до 8 мкг/мл) путем выполнения кривой реакции дозы в том же методе, который используется для измерения чувствительности пуромицина (шаг 3.2). Если токсичность наблюдается с йlt;8 мкг/мл бромистого гексадиметрина, не используйте.
4. Функциональная титрование объединенной лентивирусной библиотеки CRISPR для определения МВД
- Оттепель свежий аликвот объединенной библиотеки CRISPR sgRNA лентивирус (например, LCV2::TKOv3) и держать на льду.
- Разработай серию объемов вирусов для тестирования между диапазоном 0-2 мл (т.е. 0 мл, 0,25 мл, 0,5 мл, 1 мл и 2 мл).
- Урожай целевых клеток и семенных клеток в 15 см пластин при плотности, необходимой для достижения слияния в 72 ч.
- Для каждого объема вируса, который будет протестирован, подготовить дубликаты пластин. Добавьте клетки, вирус, бромистый гексадиметрин (8 мкг/мл) и носители до окончательного объема 20 мл. Тщательно перемешайте тарелки, посидите на уровне инкубатора и инкубировать 24 ч (37 градусов по Цельсию, 5% CO2).
- После 24 ч удалите вирус, содержащий носители мультимедиа, и утилизируйте (используйте меры предосторожности биобезопасности для обработки лецивирусных отходов). Дополнительно, осторожно промыть тарелку с теплой PBS для удаления посторонних вирусов.
- Для каждого состояния вируса, заменить 20 мл средств, содержащих пуромицин с помощью концентрации определяется убить клетки в разделе 3, на одну пластину репликации. К другой пластине добавьте 20 мл свежих носителей без пуромицицина. Инкубировать 48 ч (37 градусов по Цельсию, 5% CO2).
- После 48 ч, убедитесь, что все неинфицированные клетки (состояние вируса 0 мл), обработанные пуромицином мертвы. Урожай все пластины индивидуально и разогнать клетки путем повторного нежного пипеттинг.
- Подсчитайте клетки всех пластин и вычислите МВД для каждого объема вируса, сравнивая количество клеток с выбором пуромицина с количеством клеток без пуромицина (т.е. пуромицин).
- График результаты, чтобы определить объем вируса, что приводит к 30%-40% выживаемости клеток с puromycin выбор по сравнению без пуромицина. Используйте этот объем вируса для достижения МВД 0,3-0,4 во время экрана в тех же условиях культуры тканей.
5. Первичная инфекция экрана, выбор и пропуск клеток
- Выберите покрытие библиотеки CRISPR sgRNA, которая будет поддерживаться по всему экрану (рекомендуемое минимум в 200 раз).
- Основываясь на библиотечном охвате, определите количество клеток, необходимых для поддержания этого охвата на сгРНК, и количество клеток, необходимых для инфицирования в МВД 0,3 (Таблица 3).
- Определите количество пластин, необходимых для настройки инфекции(Таблица 4).
- Заражение клеток библиотекой CRISPR
- Урожай клетки и семена необходимого номера ячейки для каждой тарелки 15 см.
- Добавьте бромистый гексадимитрин (8 мкг/мл) во все пластины.
- Добавьте вирус в объеме, необходимом для МВД 0,3, к скринингу и контрольные 2 пластины. Для Control 1 не добавляйте вирус и заменяйте этот том носителями.
- Тщательно перемешайте тарелки, наклонив. Поместите тарелки в инкубатор, убедившись, что они являются ровными.
ПРИМЕЧАНИЕ: Пакет инфекций может быть сделано путем объединения мастер сочетание вируса, средств массовой информации и гексадетрина бромистого бромида в клетки в подвеске перед покрытием. - Удалить средства массовой информации и заменить свежими средствами, содержащими пуромицин в концентрации определяется в шаге 3.2.4 для скрининга и контролировать 1 пластины 24 ч после вирусной инфекции. Добавить свежие носители без пуромицина в контроль 2 пластины. Инкубировать клетки для 48 ч (37 градусов по Цельсию, 5% CO2).
- 48 ч после puromycin кроме того, убедитесь, что все неинфицированные клетки мертвы (контроль 1) для подтверждения активности пуромицина, а затем урожай инфицированных клеток.
- Сбор инфицированных клеток населения и клеточной просажещения
- Урожай пуромицин-выбранных клеток из всех скрининговых пластин в один стерильный контейнер. Соберите ячейки с каждой контрольной пластины отдельно. Разгоняйте клетки нежным повторным пипеттингом.
- Подсчитайте клетки из объединенных скрининговых ячеек, контролируйте 1 и контролируйте 2 отдельно и вычисляйте количество ячеек на 1 мл.
- Рассчитайте МВД и сложите охват, достигнутый следующим образом:
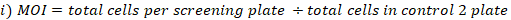
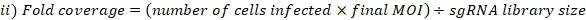
- Соберите три реплики клеточных гранул из объединенных клеток в выбранной библиотеке покрытия для экстракции геномной ДНК. Центрифуги клетки на 500 х г в течение 5 мин. Вымойте с PBS. Пометьте трубки и заморозить сухой клеточных гранул на -80 градусов по Цельсию (это T0 эталонных образцов).
- Разделите пул инфицированных клеток на три группы репликации (например, реплицировать A, реплицировать B, реплицировать C), сохраняя при этом охват библиотеки в каждой репликации. Семенные клетки при той же плотности посева, как обычно, используются при их расширении. Используйте одинаковое количество клеток для каждой репликационной пластины и такое же общее количество клеток между репликациями.
- Продолжайте проход клеток и собрать три реплики клеточных гранул из каждой репликации объединенных инфицированных клеток, как указано выше, каждые 3-8 дней в зависимости от клеточной линии, до 15-20 клеточных удвоений. При каждом проходе собирают клетки из всех пластин в каждой группе репликации друг с другом (т.е. все клетки из репликационных пластин смешиваются вместе, все клетки из повторяют пластин Ы смешиваются вместе и т.д.).
- Этикетка каждого гранулы с временем (T) и репликации обозначения. Это соответствует количеству дней после T0, которые собираютгра (например, T3'A, T3'B, T3'C и т.д.).
- Для отрицательного отбора наркотиков экраны, позволяют клеткам восстановить, по крайней мере один проход после T0 до лечения. На T3 или T6, разделить клетки от каждой группы репликации (A, B, C) в медикаментозное лечение и контроль населения, используя ту же плотность посева используется в шаге 5.3.5.
- Отдельно объединить количество клеток, необходимых для библиотечного покрытия для каждого репликации в группе лечения наркомании. Добавить препарат в промежуточных концентрациях (IC20-IC50). Семя клетки и инкубировать (37 градусов по Цельсию, 5% CO2) до следующего прохода.
- Отдельно объедините количество ячеек, необходимых для покрытия библиотеки для каждого репликации в группе управления транспортным средством. Добавьте управление транспортным средством, используя тот же объем, что и препарат (0,5% v/v). Семя клетки и инкубировать (37 градусов по Цельсию, 5% CO2) до следующего прохода.
- Продолжайте проход клеток и собирать клетки гранулы для геномной ДНК каждые 3 дня, как описано в шаге 5.3.5, в то время как освежающий препарат или транспортное средство на каждом проходе.
- Для положительных экранов отбора или лекарственной устойчивости разделите каждую группу репликации в зависимости от количества ячеек, необходимых для покрытия библиотеки. Добавьте концентрацию ic90 наркотиков к каждой репликации. В IC90, большинство клеток будут убиты. Разрешить устойчивых популяций расти и собирать клеточные гранулы (1-2 х 107 клеток) для экстракции геномной ДНК.
6. Подготовка и секвенирование образца CRISPR
- Геномная очистка ДНК
- Инкубировать замороженные клеточные гранулы в течение 5-10 минут на RT для оттаивания.
- Добавьте 1,4 мл PBS в 50 мл центрифуги трубки, содержащей клеточные гранулы. Вихрь на 20 с, чтобы повторно приостановить клетки и отдохнуть в течение 1 мин. При необходимости, пипетка 15x с P1000, чтобы разбить оставшиеся ячейки скопления. При переносе клеток из трубки 15 мл или 1,5 мл, resuspend клетки с 1 мл PBS, а затем передать клетки в 50 мл трубки и промыть оригинальную трубку с 400 Л Л PBS.
- Добавьте 5 мл раствора ядра лизиса в новьостановимые клетки. Используя пипетку 10 мл, смешайте образец, повысив вверх и вниз в 5 раз.
- Добавьте 32 кЛ RNase A (20 мг/мл; для получения конечной концентрации 100 мкг/мл) к ядерному лизату и смешайте образец, инвертируя трубку 5x. Инкубировать смесь при 37 градусов по Цельсию в течение 15 минут и дать пробе остыть в течение 10 минут на RT.
- Добавьте 1,67 мл раствора протеинового осадка в лизат и вихрь энергично в течение 20 с. Небольшие белковые комки могут быть видны после смешивания.
- Центрифуга при 4500 х г в течение 10 мин на RT.
- Используя пипетку 10 мл, перенесите супернатант в 50-мл центрифугную трубку, содержащую 5 мл изопропанола. Аккуратно перемешайте раствор 10x путем инверсии до тех пор, пока ДНК не будет замечена.
ПРИМЕЧАНИЕ: ДНК можно наблюдать как белые, нити, как нити, которые образуют видимую массу. - Центрифуга при 4500 х г в течение 5 мин на RT, чтобы гранулы ДНК.
- Используя 10 мл пипетки, тщательно удалить супернатант и избежать вытеснения ДНК гранулы. Добавьте 5 мл 70% этанола на RT в ДНК. Аккуратно поверните трубку, чтобы промыть гранулы ДНК и стороны центрифуги трубки.
- Центрифуга при 4500 х г в течение 5 мин на RT.
- Используя 10 мл пипетки, тщательно удалить 70% этанола и избежать выбивания ДНК гранулы. Воздушно-сухая геномная ДНК в течение 10 мин на RT.
- Добавьте 400 зЛ раствора TE в трубку и дайте ДНК раствориться, инкубируя при 65 градусах По Цельсию в течение 1 ч. Смешайте ДНК, аккуратно щелкая трубкой каждые 15 минут. Если ДНК не растворяется полностью, инкубировать трубку при 65 градусах По Цельсию в течение дополнительного 1 ч, нежно щелкая трубку каждые 15 минут, и оставьте ее на 4 градуса Цельсия на ночь.
- Центрифуга при 4500 х г в течение 1 мин на РТ и передача геномной ДНК в 1,5 мл низкосвязной трубки.
- Количественно и измерить чистоту геномной ДНК как на спектрофотометре (для общего содержания нуклеиновой кислоты) и на фторометре (для двухцепочечного содержания ДНК).
- Дополнительно, осадок геномной ДНК, если Есть проблемы с вниз по течению PcR усиления sgRNA следующим образом.
- Передача 400 мл геномной ДНК в микроцентрифугную трубку 1,5 мл.
- Добавьте 18 л из 5 M NaCl (окончательная концентрация 0,2 М) и 900 л 95% этанола.
- Перевернуть трубку 10x до тщательного смешивания, затем центрифугу при 16000 х г в течение 10 минут на RT.
- Тщательно удалите супернатант и избежать вытеснения гранул ДНК. Вымойте гранулы ДНК с 500 зл 70% этанола. Аккуратно поверните трубку, чтобы вымыть гранулы ДНК.
- Центрифуга при 16 000 х г в течение 5 мин на RT.
- Тщательно удалите супернатант и избежать выбивания гранул ДНК. Воздушно-сухая геномная ДНК в течение 10 мин на RT.
- Добавьте 300 зЛ TE, чтобы растворить ДНК, как описано в шагах 6.1.12.
- Количественно и измерить чистоту геномной ДНК, как описано в шаге 6.1.14.
- Подготовка библиотеки покечня CRISPR
- Назначь ПЦР 1, как указано в таблице 5, используя в общей сложности 100 мкг геномной ДНК. Добавьте 3,5 мкг геномной ДНК на реакцию 50 л и установите идентичные реакции 50 л для достижения желаемого покрытия. В таблице 6 приведены примеры грунтовых последовательностей для усиления библиотек секвеи LCV2::TKOv3. В таблице 7 приведены примеры грунтовых последовательностей для усиления библиотек секвенирования pLCKO2::TKOv3.
- Усилируйте реакцию ПЦР 1 в термоцикле, используя программу, изложенную в таблице 8.
- Проверьте усиление ПЦР 1, запустив 2 ЗЛ продукта ПЦР на 1% агарозного геля. ПЦР 1 дает продукт 600 bp.
- Объедините все отдельные реакции 50 л для каждого образца геномной ДНК и смешайте путем вихря.
- Назначь одну реакцию ПЦР 2 (50 кВ) для каждого образца, изложенного в таблице 9, используя в качестве шаблона 5 КЛ объединенного продукта ПЦР 1. Используйте уникальные комбинации индексных праймеров для каждого отдельного образца, чтобы объединить образцы библиотеки последовательности.
- Усилируйте реакцию ПЦР 2 в термоцикле, используя программу, изложенную в таблице 10.
- Очистите оборудование геля агарозы для очистки усиленных продуктов с 0,1 N HCl в течение 10 минут до литья геля. Подготовьте 2% агарозный гель, содержащий днк-пятно для очистки пЦР 2 усиленных продуктов.
- Запустите продукт PCR 2 на 2% агарозный гель при низком напряжении (1,0-1,5 ч перспективе). ПЦР 2 дает продукт 200 bp.
- Визуализируйте продукты ПЦР на синем световом трансиллиносторе. Выакцион 200 bp полосы и очистить ДНК от ломтика геля агарозы с помощью комплекта извлечения геля. Количественно и измерить чистоту библиотеки секвенирования как на спектрофотометре, так и на флюорометре.
ПРИМЕЧАНИЕ: Типичная концентрация библиотеки секвенирования геля колеблется от 5-10 нг/Л и общей урожайностью 150-300 нг.
- Секвенирование высокой пропускной способности
- Последовательность библиотек CRISPR по секвенсорам следующего поколения.
- Последовательность ссылки T0 образцов на более высокой глубине чтения 400-500-кратного покрытия библиотеки. Последовательность экспериментальных образцов временных точек для отсева экранов с минимальной глубиной чтения в 200 раз. Для сильных положительных экранов отбора для идентификации обогащенных сгРН достаточно минимальной глубины чтения в 50 раз.
ПРИМЕЧАНИЕ: Очень важно секвенировать образец T0, чтобы определить представление библиотеки для конкретного экрана и служить в качестве эталона для определения изменений сгиба sgRNA с течением времени.
7. Анализ данных
- Выровнять последовательность с помощью таких программ, как Bowtie, чтобы сопоставить последовательность считывается в справочную библиотеку, используя следующие параметры: -v2 (позволяет два несоответствия) и -m1 (отбрасывание любого чтения, которое отображено до более чем одной последовательности в библиотеке).
- Нормализовать количество уникально отображеных считывателей для каждого sgRNA для данного образца до 10 миллионов считывает на образец следующим образом:
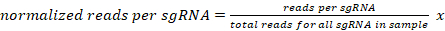 107
107
- Рассчитайте изменение складок журнала каждого sgRNA для каждого репликации в каждую точку времени (Tn) по сравнению с образцом T0 (Tn/T0). Добавьте псевдо-счет в 0,5 считывает все считываемые счета, чтобы предотвратить разрывы от нулей. Исключите sgRNA с йlt;30 сырые читает в образце T0 от расчета складных изменений и вниз по течению анализа.
- Анализ изменения раза с Байесовского анализа генов Essentiality (BAGEL) алгоритм ат-л;https://github.com/hart-lab/bagel Дополнительная таблица S1) или Наркотики »lt;https://github.com/hart-lab/drug»gt; для экранов наркотиков20.
- Рассчитайте точность и напомните для оценки производительности экрана с помощью баллов BF. Используйте важный набор из шага 7.4 в качестве истинного положительного списка для функции точного отзыва и кривой библиотеки Scikit-learn для Python, наряду с приведенным выше подмножеством баллов BF. Кроме того, выполните то же самое с помощью пакета PRROC в R.
- Рассчитайте среднее изменение складок всех направляющих для каждого гена. Создание плотных участков для основных и несущественных генов (см. шаг 7.4) в R или эквивалентном программном обеспечении. В R, если x.ess является вектором, содержащим значения изменения складок журнала основных генов и x.nonEss содержат несущественные гены, график с использованием следующей команды:
плотность (плотность ( x.ess ), xlab'"средний logFC", col"red", lwd-2 )
линии (плотность (x.nonEss), коле "синий", lwd-2 )
ПРИМЕЧАНИЕ: Для Python версии детали и пакеты используются, см scikit-узнать v0.19.1: (опубликовано Pedregosa и др.21).
Access restricted. Please log in or start a trial to view this content.
Результаты
Обзор рабочего процесса скрининга по масштабу генома CRISPR
Рисунок 1 иллюстрирует обзор объединенного потока скрининга CRISPR, начиная с заражения целевых клеток с помощью лентивирусной библиотеки CRISPR при низком ?...
Access restricted. Please log in or start a trial to view this content.
Обсуждение
Благодаря простоте использования и высокой гибкости, технология CRISPR была широко принята в качестве инструмента выбора для точного редактирования генома. Объединенный скрининг CRISPR предоставляет метод для допроса тысяч генетических возмущений в одном эксперименте. В объединенных экр?...
Access restricted. Please log in or start a trial to view this content.
Раскрытие информации
Авторы не заявляют о каких-либо конкурирующих финансовых интересах.
Благодарности
Эта работа была поддержана Геномканады, Исследовательским фондом Онтарио и Канадскими институтами исследований в области здравоохранения (MOP-142375, PJT-148802).
Access restricted. Please log in or start a trial to view this content.
Материалы
| Name | Company | Catalog Number | Comments |
| 0.22 micron filter | |||
| 30°C plate incubator | |||
| 37°C shaking incubator | |||
| 37°C, 5% CO2 incubator | |||
| 5 M NaCl | Promega | V4221 | |
| 50X TAE buffer | BioShop | TAE222.4 | |
| 6 N Hydrochloric acid solution | BioShop | HCL666.500 | |
| 95% Ethanol | |||
| Alamar blue | ThermoFisher Scientific | DAL1025 | |
| Blue-light transilluminator | ThermoFisher Scientific | G6600 | |
| Bovine Serum Albumin,Heat Shock Isolation, Fraction V. Min. 98%, Biotechnology grade | Bioshop | ALB001.250 | |
| Dulbecco's Modification of Eagles Medium | Life Technologies | 11995-065 | Cel culture media |
| Electroporation cuvettes | BTX | 45-0134 | |
| Electroporator | BTX | 45-0651 | |
| Endura electrocompetent cells | Lucigen | 90293 | |
| Fetal Bovine Serum | GIBCO | 12483-020 | |
| HEK293T packaging cells | ATCC | CRL-3216 | recommend passage number <15 |
| Hexadimethrine Bromide (Polybrene) | Sigma | H9268 | Cationic polymer to enhance transduction efficiency |
| Hexadimethrine Bromide (Polybrene) | |||
| LB agar plates with carbenicillin | |||
| LB medium with carbenicillin | |||
| Low molecular weight DNA ladder | New England Biolabs | N3233S | |
| Nanodrop spectrophotometer | ThermoFisher Scientific | ND-ONE-W | |
| NEBNext Ultra II Q5 Master Mix | New England Biolabs | M0544L | |
| Opti-MEM | Life Technologies | 31985-070 | Reduced serum media |
| Plasmid maxi purification kit | Qiagen | 12963 | |
| pMD2.G (envelope plasmid) | Addgene | Plasmid #12259 | lentiviral system |
| psPAX2 (packaging plasmid) | Addgene | Plasmid #12260 | lentiviral system |
| Puromycin | Wisent | 400-160-UG | |
| QIAquick gel extraction kit | Qiagen | 28704 | |
| Qubit dsDNA BR assay | ThermoFisher Scientific | Q32853 | |
| Qubit fluorometer | ThermoFisher Scientific | Q33226 | |
| RNAse A | Invitrogen | 12091021 | |
| S.O.C recovery medium | Invitrogen | 15544034 | |
| SYRB Safe DNA gel stain | ThermoFisher Scientific | S33102 | |
| Toronto KnockOut CRIPSR library (TKOv3) - Cas9 included | Addgene | Addgene ID #90203 | Genome-wide CRISPR library , includes Cas9, 71,090 sgRNA |
| Toronto KnockOut CRIPSR library (TKOv3) - non-cas9 | Addgene | Addgene ID #125517 | Genome-wide CRISPR library, non-Cas9, 71,090 sgRNA |
| Tris-EDTA (TE) solution, pH8.0 | |||
| UltraPure agarose | ThermoFisher Scientific | 16500500 | |
| Wizard genomic DNA purification kit | Promega | A1120 | |
| X-tremeGENE 9 DNA transfection reagent | Roche | 06 365 809 001 | Lipid based transfection reagent |
Ссылки
- Jiang, F., Doudna, J. A. CRISPR-Cas9 Structures and Mechanisms. Annual Review of Biophysics. 46, 505-529 (2017).
- Baliou, S., et al. CRISPR therapeutic tools for complex genetic disorders and cancer (Review). International Journal of Oncology. 53 (2), 443-468 (2018).
- Hart, T., et al. High-Resolution CRISPR Screens Reveal Fitness Genes and Genotype-Specific Cancer Liabilities. Cell. 163 (6), 1515-1526 (2015).
- Morgens, D. W., Deans, R. M., Li, A., Bassik, M. C. Systematic comparison of CRISPR/Cas9 and RNAi screens for essential genes. Nature Biotechnology. 34 (6), 634-636 (2016).
- Evers, B., et al. CRISPR knock-out screening outperforms shRNA and CRISPRi in identifying essential genes. Nature Biotechnology. 34 (6), 631-633 (2016).
- Miles, L. A., Garippa, R. J., Poirier, J. T. Design, execution, and analysis of pooled in vitro CRISPR/Cas9 screens. The FEBS Journal. 283 (17), 3170-3180 (2016).
- Wang, T., Wei, J. J., Sabatini, D. M., Lander, E. S. Genetic screens in human cells using the CRISPR-Cas9 system. Science. 343 (6166), 80-84 (2014).
- Wang, T., et al. Identification and characterization of essential genes in the human genome. Science. 350 (6264), 1096-1101 (2015).
- Sanson, K. R., et al. Optimized libraries for CRISPR-Cas9 genetic screens with multiple modalities. Nature Communications. 9 (1), 5416(2018).
- Hart, T., et al. Evaluation and Design of Genome-Wide CRISPR/SpCas9 Knock-out Screens. G3: Genes|Genomes|Genetics. 7 (8), 2719-2727 (2017).
- Mair, B., Tomic, J., et al. Essential gene profiles for human pluripotent stem cells identify uncharacterized genes and substrate dependencies. Cell Reports. 27 (2), 599-615 (2019).
- Shalem, O., et al. Genome-scale CRISPR-Cas9 knock-out screening in human cells. Science. 343 (6166), 84-87 (2014).
- Sharma, S., Petsalaki, E. Application of CRISPR-Cas9 Based Genome-Wide Screening Approaches to Study Cellular Signalling Mechanisms. International Journal of Molecular Sciences. 19 (4), (2018).
- Steinhart, Z., et al. Genome-wide CRISPR screens reveal a Wnt-FZD5 signaling circuit as a druggable vulnerability of RNF43-mutant pancreatic tumors. Nature Medicine. 23 (1), 60-68 (2017).
- Wang, T., et al. Gene Essentiality Profiling Reveals Gene Networks and Synthetic Lethal Interactions with Oncogenic Ras. Cell. 168 (5), 890-903 (2017).
- Zimmermann, M., et al. CRISPR screens identify genomic ribonucleotides as a source of PARP-trapping lesions. Nature. 559 (7713), 285-289 (2018).
- Deans, R. M., et al. Parallel shRNA and CRISPR-Cas9 screens enable antiviral drug target identification. Nature Chemical Biology. 12 (5), 361-366 (2016).
- Trinh, T. J. J., Bloom, F., Hirsch, V. STBL2: an Escherichia coli strain for the stable propagation of retroviral clones and direct repeat sequences. Focus. 16, 78-80 (1994).
- Hart, T., Moffat, J. BAGEL: a computational framework for identifying essential genes from pooled library screens. BMC Bioinformatics. 17, 164(2016).
- Wang, G. Z. M., et al. Identifying drug-gene interactions from CRISPR knock-out screens with drugZ. bioRxiv. , Available from: https://doi.org/10.1101/232736 (2017).
- Pedregosa, F. V., G,, et al. Scikit-learn: Machine Learning in Python. Journal of Machine Learning Research. 12, 2825-2830 (2011).
- Ketela, T., et al. A comprehensive platform for highly multiplexed mammalian functional genetic screens. BMC Genomics. 12, 213(2011).
- Doench, J. G. Am I ready for CRISPR? A user's guide to genetic screens. Nature Review Genetics. 19 (2), 67-80 (2018).
- Hartenian, E., Doench, J. G. Genetic screens and functional genomics using CRISPR/Cas9 technology. FEBS Journal. 282 (8), 1383-1393 (2015).
- Li, W., et al. MAGeCK enables robust identification of essential genes from genome-scale CRISPR/Cas9 knock-out screens. Genome Biology. 15 (12), 554(2014).
- Sheel, A., Xue, W. Genomic Amplifications Cause False Positives in CRISPR Screens. Cancer Discovery. 6 (8), 824-826 (2016).
- Meyers, R. M., et al. Computational correction of copy number effect improves specificity of CRISPR-Cas9 essentiality screens in cancer cells. Nature Genetics. 49 (12), 1779-1784 (2017).
- Henser-Brownhill, T., Monserrat, J., Scaffidi, P. Generation of an arrayed CRISPR-Cas9 library targeting epigenetic regulators: from high-content screens to in vivo assays. Epigenetics. 12 (12), 1065-1075 (2017).
Access restricted. Please log in or start a trial to view this content.
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены