Для просмотра этого контента требуется подписка на Jove Войдите в систему или начните бесплатную пробную версию.
Method Article
Имплантация и оценка меланомы в сосудистой оболочке мыши с помощью оптической когерентной томографии
* Эти авторы внесли равный вклад
В этой статье
Резюме
Настоящий протокол описывает имплантацию и оценку меланомы в сосудистой оболочке мыши с использованием оптической когерентной томографии.
Аннотация
Создание экспериментальных моделей меланомы хориоидеи является сложной задачей с точки зрения способности индуцировать опухоли в правильной локализации. Кроме того, трудности в наблюдении за меланомой задней хориоидеи in vivo ограничивают локализацию опухоли и оценку роста в режиме реального времени. Описанный здесь подход оптимизирует методы определения меланомы хориоидеи у мышей с помощью многоступенчатой процедуры субхориоидальной инъекции клеток B16LS9. Чтобы обеспечить точность при введении в небольшие размеры сосудистой оболочки мыши, вся процедура выполняется под микроскопом. Сначала конъюнктивальная перитомия формируется в дорсально-височной области глаза. Затем путем введения иглы через обнаженную склеру создается тракт в подхориоидальное пространство. Затем следует введение тупой иглы в тракт и инъекция клеток меланомы в сосудистую оболочку. Сразу после инъекции используется неинвазивная оптическая когерентная томография (ОКТ) для определения местоположения и прогрессирования опухоли. Отслойка сетчатки оценивается как предиктор локализации и размера опухоли. Представленный метод позволяет воспроизвести индукцию меланомы, локализованной в сосудистой оболочке у мышей, и визуализировать оценку роста опухоли в реальном времени. Таким образом, он является ценным инструментом для изучения внутриглазных опухолей.
Введение
Увеальная меланома (УМ) является наиболее частым внутриглазным первичным злокачественным новообразованием у взрослых. Приблизительно 90% меланом глаза происходят из меланоцитов в сосудистой оболочке увеального тракта1. UM является основной причиной заболеваемости и смертности, поскольку, по оценкам, около 50% пациентов развивают метастатическое заболевание, причем печень является основным местом метастазирования2. Раннее лечение первичных поражений может снизить вероятность метастазов, однако никакое эффективное лечение не предотвращает образование метастазов3.
Стандартное лечение увеальной меланомы включает лучевую терапию, которая связана с потерей зрения из-за оптической нейропатии, ретинопатии, синдрома сухого глаза и катаракты. Хирургическая резекция обычно откладывается до тех пор, пока рост поражения не будет распознан и охарактеризован. Однако такая задержка может привести к развитию метастатического заболевания4. В некоторых случаях требуется бесполезная энуклеация. Конечно, эта радикальная процедура ставит под угрозу зрение и приводит к резкому ухудшению эстетики.
Было предпринято много усилий, посвященных разработке экспериментальных моделей для изучения увеальной меланомы. Доклинические модели на животных, которые позволяют точно оценить это злокачественное новообразование, являются ключевыми для изучения новых диагностических и терапевтических стратегий увеальной меланомы. Экспериментальные модели меланомы глаза на животных в основном основаны на инокуляции опухолевых клеток у мышей, крыс и кроликов 5,6. Мышиные модели экономически эффективны и широко используются для исследований меланомы из-за их быстрой скорости размножения и высокого сходства генома с людьми. Клеточная линия меланомы кожи мышей B16 обычно используется для инокуляции мышей C57BL6 и индуцирования сингенных опухолей. При использовании этой модели для индукции увеальной меланомы опухолевидные глаза обычно необходимо энуклеировать через 7-14 дней после инокуляции. Кроме того, B16 является высокоинвазивной моделью. Иммунно-привилегированная природа глаза поддерживает метастазирование, и метастазы обычно могут быть обнаружены через 3-4 недели после инокуляции опухолевых клеток. Субкультуры исходной линии B16 проявляют отчетливые метастатические свойства6. Например, линия меланомы Квинса имеет высокий показатель метастазов 7,8. Клеточная линия B16LS9 имеет морфологию дендритных клеток и была получена из метастазов в печень мышей C57BL / 6, которым была введена родительская линия кожной меланомы B16F19. Было показано, что при введении в задний отдел глаза эти клетки образуют внутриглазные опухоли, которые гистологически напоминают увеальную меланому человека и образуют специфические для печени метастазы у C57BL / 6, но не у Balb / C, мышей10,11,12. Генетически клетки характеризуются более высокой экспрессией протоонкогена c-met, который действует как клеточный рецептор для фактора роста гепатоцитов13. Напротив, B16F10,10-й пассаж родительского B16, в первую очередь метастазирует в легкие при инокуляциивнутриглазно 14. И B16F10, и B16LS9 пигментированы12.
Несколько ключевых проблем ограничивают успех моделей увеальной меланомы у мышей. Во-первых, рефлюкс опухолевых клеток может привести к экстраокулярной или субконъюнктивальной меланоме. Во-вторых, рост опухоли после внутриглазной инокуляции клеток меланомы часто сильно варьируется, что создает трудности в оценке лечения и прогресса. Другой серьезной трудностью является ограниченная способность следить за ростом опухоли in vivo. В то время как биолюминесцентная визуализация, такая как опухоли, экспрессирующие люциферазу, обычно используется для мониторинга роста опухолиглаза 15,16, она не может предоставить информацию о внутриглазном расположении опухоли. Поэтому оценка опухоли обычно проводится после энуклеации глаза10,17. Это значительно ограничивает способность характеризовать прогрессирование опухоли и широкий ответ на лечение. Еще одним серьезным препятствием в изучении увеальной меланомы является трудность мониторинга поражений у пигментированных мышей. Новые подходы, которые преодолевают эти трудности, необходимы для содействия исследованию увеальной меланомы на животных моделях.
Оптическая когерентная томография (ОКТ) предоставляет отличительные возможности для получения изображений вглубь различных участков глаза с высоким разрешением, что не имеет аналогов в других методологиях, включая ультразвук18,19. ОКТ-визуализация использовалась на животных моделях для изучения различных глазных заболеваний20. Недавно ОКТ-визуализация была продемонстрирована как неинвазивное средство оценки внутриглазного роста опухоли21. Описанный здесь протокол изображает имплантацию клеток меланомы в сосудистую оболочку мыши и использование ОКТ для прогнозирования локализации и размера внутриглазной опухоли во время инокуляции клеток.
Access restricted. Please log in or start a trial to view this content.
протокол
Эксперименты в протоколе были одобрены Израильским национальным советом по экспериментам на животных и соответствуют Заявлению ARVO об использовании животных в офтальмологических исследованиях и исследованиях зрения. Самки мышей C57BL / 6 в возрасте 8-10 недель были использованы для настоящего исследования и подвергались воздействию 12/12-часовых циклов света-темноты. Животные были получены из коммерческого источника (см. Таблицу материалов).
1. Клеточная культура
- Культивирование клеток B16LS9 в среде RPMI 1640 с добавлением 10% эмбриональной бычьей сыворотки, 2 мМ L-глутамина, 1 мМ пирувата натрия, 25 мМ HEPES, 1% смеси незаменимых витаминов, 200 ЕД/мл пенициллина и 200 мг/мл стрептомицина (см. Таблицу материалов), в увлажненном инкубаторе с температурой 37 °C с 5%CO2.
- Собирают клетки для инъекций при слиянии 70%-80%.
2. Подготовка животных
- Приготовьте обезболивающую смесь кетамина (75 мг/кг массы тела) и медетомидина (0,5 мг/кг массы тела). Обезболивают мышей, вводя анестезирующую смесь внутрибрюшинно за одну инъекцию.
- Нанесите местный офтальмологический анестетик оксибупрокаин (0,4%) на оба глаза.
- Расширьте зрачки мышей, местно применяя тропикамид (0,5%).
3. Создание перитомии конъюнктивы и склерального тракта в подхориоидальное пространство
- Нанесите 1,4% гидроксиэтилцеллюлозу (см. Таблицу материалов) в качестве смазки на оба глаза, чтобы избежать высыхания. Нанесите 0,5% тропикамида на правый глаз.
- Наблюдайте за прооперированным глазом мыши под операционным микроскопом (см. Таблицу материалов). Держите веки открытыми стерильными внутриглазными щипцами.
- С помощью внутриглазных щипцов возьмитесь за верхневисочную лимбальную конъюнктиву и потяните в сторону инфрананазального положения22. Закрепите это положение, удерживая его на протяжении всей процедуры (рис. 1А).
- Используя кончик иглы 30 G, сделайте небольшую (1-2 мм) перитомию конъюнктивы в дорсально-височной области, примерно на 1-2 мм кзади от лимба.
ПРИМЕЧАНИЕ: Использование более тонких игл может предотвратить чрезмерную пункцию и повысить точность определения местоположения опухоли. - Удалите излишки капсулы Тенона из отверстия перитомии.
ПРИМЕЧАНИЕ: Капсула Тенона представляет собой слой плотной соединительной ткани, которая окружает глазнойшар 22. - В этом месте вставьте кончик иглы, чтобы проникнуть через склеру. Сделайте иссечение, чтобы создать тракт в субхориоидальном пространстве до тех пор, пока коричневый цвет сосудистой оболочки не появится через обнаженное белое вещество склеры (рис. 1B).
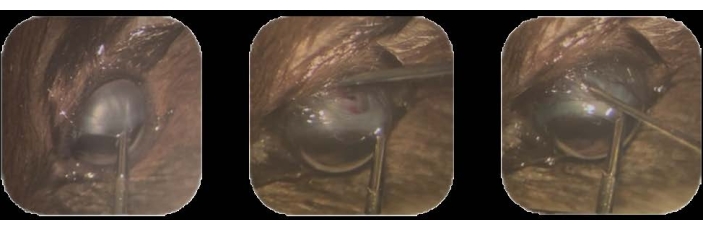
Рисунок 1: Инокуляция опухолевых клеток . (A) Верхневисочная лимбальная конъюнктива удерживается с помощью внутриглазных щипцов и подтягивается к инфраносальному положению. (B) Наконечник иглы 30 G вводится для проникновения через склеру, и делается иссечение для создания дорожки в подхориоидальном пространстве. (C) Шприц, наполненный клетками и оснащенный иглой 32 G, вставляется в дорожку, и клетки вводятся. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
4. Инокуляция клеток меланомы
- Ресуспендирование 70 000 клеток B16LS9 в 2 мкл PBS. Эта сумма рассчитана на один глаз.
- Загрузите клетки в стерильный стеклянный шприц Гамильтона объемом 10 мкл (см. Таблицу материалов), установленный с помощью тупой иглы 32 G, скрученной под углом 45°.
- Вставьте загруженную иглу шприца примерно на 2 мм в дорожку, созданную на шаге 3.
- Вводят 2 мкл клеточной суспензии.
- Удерживайте иглу на месте после инъекции в течение 2-3 с, пока вся жидкость не очистится.
- Извлеките иглу, осторожно и медленно вытащив ее, чтобы избежать утечки из дорожки (рис. 1C).
ПРИМЕЧАНИЯ: Регулировка скорости и силы инъекции может повлиять на характер развития опухоли. Предлагается, чтобы эти параметры были откалиброваны людьми, экспериментирующими, чтобы определить правильную приложенную силу и скорость. Всего в предварительных экспериментах было определено 70 000 клеток. Однако, поскольку могут быть различия в типах или партиях клеточных культур или между штаммами мышей, калибровка этого числа необходима.
5. Оценка места инъекции
- Наблюдайте за инъецированным глазом с помощью ОКТ-сканирования сразу после инокуляции клеток меланомы, чтобы определить появление отслойки сетчатки (RD), повреждения сетчатки и / или клеток в стекловидном теле23.
ПРИМЕЧАНИЯ: При необходимости повторно нанесите тропикамид, оксибупрокаин и этилцеллюлозу. - На основе ОКТ-сканирования из шага 5.1 классифицируйте шаблоны21 RD в соответствии с: (1) локальным сайтом RD-one RD; (2) утечка в материал клеток стекловидного тела в стекловидном теле; (3) расширенные RD-множественные сайты RD.
- Прогнозировать локализацию опухоли на основе: (1) локальных РД-ожидаемых опухолей хориоидеи; (2) утечка в ожидаемые опухоли стекловидного тела в стекловидном теле; (3) расширенные РД-ожидаемые вариабельные и дисперсные опухоли (рис. 2).
ПРИМЕЧАНИЕ: Ожидается, что только у мышей с локальным RD (около 50%) разовьются опухоли, ограниченные сосудистой оболочкой.
6. Прогнозирование размера опухоли на основе высоты RD
- Измерьте высоту локального RD в ОКТ-сканировании с помощью программного обеспечения для сегментации/анализа ОКТ (см. Таблицу материалов) и классифицируйте по следующим группам: малый = <300 мкм; средний = 300-400 мкм; большой = >400 мкм.
- Оцените объем, который, как ожидается, опухоли достигнут в течение 5 дней после инъекции в соответствии со следующими критериями:
Небольшая высота RD обычно наблюдается при опухолях небольшого размера (объем опухоли колеблется от 0,0059 мм3 до 0,07 мм3 со средним объемом 0,027 ± 0,005мм3).
Средняя высота РД обнаруживается как при малых, так и при средних опухолях (объем опухоли колеблется от 0,015 мм3 до 0,15 мм3 со средним объемом 0,056 ± 0,016мм3).
Большая высота РД связана с широким диапазоном объемов опухоли до 0,36мм3.
ПРИМЕЧАНИЕ: Диапазон ожидаемых размеров опухоли был получен из предыдущих результатов и разделен на три группы малых, средних и крупных опухолей.
7. Послеоперационные процедуры
- Применяют офтальмологический офлоксацин 0,3% местно.
- Отмените анестезию, введя атипамезола гидрохлорид (3 мг / кг) подкожно.
- Подкожно вводят бупренорфин (0,05 мг/кг массы тела) два раза в день в течение 3 дней, чтобы уменьшить боль и страдания животных.
- Через 5 дней после инъекции клеток меланомы оцените размер опухоли, выполнив следующие действия.
- Обезболивайте мышей, как описано в шаге 2.1. Применяют тропикамид (0,5%).
- Исследуйте глаза с помощью продольного и сагиттального ОКТ-сканирования и используйте программное обеспечение для сегментации/анализа ОКТ для измерения объема и локализации опухоли.
- Рассчитайте объем опухоли по формуле24: V = a*b*c*6/π (a, b и c = длина, ширина и высота соответственно).
- Исследуйте размер опухоли каждые 2-3 дня, как описано в шагах 7.4.1-7.4.3.
ПРИМЕЧАНИЕ: Процедура должна быть оптимизирована при использовании разных штаммов мышей или клеточных линий.
Access restricted. Please log in or start a trial to view this content.
Результаты
Глаза исследовали с помощью ОКТ сразу после инъекции клеток B16LS9. После инъекции наблюдалась локальная отслойка сетчатки. У мышей наблюдалось три паттерна РД: очаговая (рис. 2, верхняя панель), утечка в стекловидное тело (рис. 2, средняя панель) и расширенная РД (рис
Access restricted. Please log in or start a trial to view this content.
Обсуждение
Увеальная меланома является разрушительным заболеванием, для которого крайне необходимы новые терапевтические подходы. Однако исследования увеальной меланомы и потенциальных методов лечения ограничены техническими проблемами моделей увеальной меланомына животных ...
Access restricted. Please log in or start a trial to view this content.
Раскрытие информации
Маркович А.Л.: Steba Biotech (), Йеда Вейцман (), АйЙон Медикал (К,), Мор Исум (). c) = консультант; (P) = Патент. У всех остальных авторов нет конкурирующих интересов.
Благодарности
Это исследование было частично поддержано грантом 1304/20 от Израильского научного фонда (ISF), Израиль, для Арье Марковича. Благодарим Шахар Иш-Шалом и Ади Йосиповича из отделения патологии Медицинского центра Каплан, Реховот, Израиль, за гистологический анализ.
Access restricted. Please log in or start a trial to view this content.
Материалы
| Name | Company | Catalog Number | Comments |
| 10 μL glass syringe (Hamilton Co., Bonaduz, Switzerland) | Hamilton | 721711 | |
| 30 G needles | BD Microbalance | 2025-01 | |
| Atipamezole hydrochloride | Orion Phrma | ||
| B16LS9 cells | from Hans Grossniklaus USA | ||
| Buprenorphine | richter pharma | 102047 | |
| C57BL/6 female mice | Envigo | ||
| Essential vitamin mixture | satorius | 01-025-1A | |
| Fetal bovine serum | rhenium | 10270106 | |
| HEPES | satorius | 03-025-1B | |
| Hydroxyethylcellulose 1.4% eye drops | Fisher Pharmaceutical | 390862 | |
| InSight OCT segmentation software | Phoenix Micron, Inc | ||
| Ketamine | bremer pharma GMBH (medimarket) | 17889 | |
| L-glutamine | satorius | 03-020-1B | |
| Medetomidine | zoetis (vetmarket) | 102532 | |
| Ofloxacin 0.3% eye drops | allergan | E92170 | |
| Optical coherence tomography | Phoenix Micron, Inc | ||
| Oxybuprocaine 0.4% | Fisher Pharmaceutical | 393050 | |
| Penicillin-streptomycin-amphoteracin | satorius | 03-033-1B | |
| Phosphate buffered saline (PBS) | satorius | 02-023-1a | |
| RPMI cell media | satorius | 01-104-1A | |
| Sodium pyruvate | satorius | 03-042-1B | |
| Surgical microscope | Zeiss | OPMI-6 CFC | |
| Tropicamide 0.5% | Fisher Pharmaceutical | 390723 |
Ссылки
- Jager, M. J., et al. Uveal melanoma. Nature Reviews Disease Primers. 6 (1), 1-25 (2020).
- Bustamante, P., Piquet, L., Landreville, S., Burnier, J. V. Uveal melanoma pathobiology: Metastasis to the liver. Seminars in Cancer Biology. 71, Academic Press. 65-85 (2021).
- Damato, B. Ocular treatment of choroidal melanoma in relation to the prevention of metastatic death-A personal view. Progress in Retinal and Eye Research. 66, 187-199 (2018).
- Jouhi, S., et al. The small fatal choroidal melanoma study. A survey by the European Ophthalmic Oncology Group. American Journal of Ophthalmology. 202, 100-108 (2019).
- Cao, J., Jager, M. J. Animal eye models for uveal melanoma. Ocular Oncology and Pathology. 1 (3), 141-150 (2015).
- Uner, O. E., Gandrakota, N., Azarcon, C. P., Grossniklaus, H. E. Animal models of uveal melanoma. Annals of Eye Science. 7, 21-30 (2022).
- Yang, H., Dithmar, S., Grossniklaus, H. E. Interferon alpha 2b decreases hepatic micrometastasis in a murine model of ocular melanoma by activation of intrinsic hepatic natural killer cells. Investigative Ophthalmology & Visual Science. 45 (7), 2056-2064 (2004).
- Yang, H., Grossniklaus, H. E. Combined immunologic and anti-angiogenic therapy reduces hepatic micrometastases in a murine ocular melanoma model. Current Eye Research. 31 (6), 557-562 (2006).
- Rusciano, D., Lorenzoni, P., Burger, M. M. Murine models of liver metastasis. Invasion & Metastasis. 14 (1-6), 349-361 (1994).
- Diaz, C. E., Rusciano, D., Dithmar, S., Grossniklaus, H. E. B16LS9 melanoma cells spread to the liver from the murine ocular posterior compartment (PC). Current Eye Research. 18 (2), 125-129 (1999).
- Rusciano, D., Lorenzoni, P., Burger, M. M. Murine models of liver metastasis. Invasion & Metastasis. 14 (1-6), 349-361 (1994).
- Ashur-Fabian, O., et al. Tetrac delayed the onset of ocular melanoma in an orthotopic mouse model. Frontiers in Endocrinology. 12, 632335(2019).
- Elia, G., et al. Mechanisms regulating c-met overexpression in liver-metastatic B16-LS9 melanoma cells. Journal of Cellular Biochemistry. 81 (3), 477-487 (2001).
- Harning, R., Szalay, Z. Ocular metastasis of in vivo and in vitro derived syngeneic murine melanoma. Investigative Ophthalmology & Visual Science. 28 (9), 1599-1604 (1987).
- Ezra-Elia, R., et al. Can an in vivo imaging system be used to determine localization and biodistribution of AAV5-mediated gene expression following subretinal and intravitreal delivery in mice. Experimental Eye Research. 176, 227-234 (2018).
- Notting, I. C., et al. Whole-body bioluminescent imaging of human uveal melanoma in a new mouse model of local tumor growth and metastasis. Investigative Ophthalmology & Visual Science. 46 (5), 1581-1587 (2005).
- Yang, H., et al. In-vivo xenograft murine human uveal melanoma model develops hepatic micrometastases. Melanoma Research. 18 (2), 95-103 (2008).
- Murthy, R. K., Haji, S., Sambhav, K., Grover, S., Chalam, K. V. Clinical applications of spectral domain optical coherence tomography in retinal diseases. Biomedical Journal. 39 (2), 107-120 (2016).
- Drexler, W., et al. Ultrahigh-resolution ophthalmic optical coherence tomography. Nature Medicine. 7 (4), 502-507 (2001).
- Ochakovski, G. A., Fischer, M. D. Phenotyping of mouse models with OCT. Methods in Molecular Biology. 1834, 285-291 (2019).
- Zaks, O., et al. In-vivo imaging for assessing tumor growth in mouse models of ocular melanoma. Experimental Eye Research. 204, 108431(2021).
- Brar, V. S. American Academy of Ophthalmology 2022-2023 BCSC. 2. Fundamentals and principles of ophthalmology. , (2022).
- Duker, J. S., Waheed, N. K., Goldman, D. Handbook of Retinal OCT: Optical Coherence Tomography, 2nd Edition. , Elsevier Health Sciences. (2021).
- Tomayko, M. M., Reynolds, C. P. Determination of subcutaneous tumor size in athymic (nude) mice. Cancer Chemotherapy and Pharmacology. 24 (3), 148-154 (1989).
- Richards, J. R., Yoo, J. H., Shin, D., Odelberg, S. J. Mouse models of uveal melanoma: Strengths, weaknesses, and future directions. Pigment Cell & Melanoma Research. 33 (2), 264(2020).
- Chen, R., et al. Photoacoustic molecular imaging-escorted adipose photodynamic-browning synergy for fighting obesity with virus-like complexes. Nature Nanotechnology. 16 (4), 455-465 (2021).
- Yu, Q., et al. Label-free visualization of early cancer hepatic micrometastasis and intraoperative image-guided surgery by photoacoustic imaging. Journal of Nuclear Medicine. 61 (7), 1079-1085 (2020).
Access restricted. Please log in or start a trial to view this content.
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены