Method Article
Протокол построения модели раны крысы при сахарном диабете 1 типа
* Эти авторы внесли равный вклад
В этой статье
Резюме
Индуцированная стрептозотоцином модель диабетической раны у самцов крыс SD в настоящее время является наиболее широко используемой моделью для изучения заживления ран при сахарном диабете I типа. В этом протоколе описываются методы, используемые для построения этой модели. Он также представляет и решает потенциальные проблемы и исследует прогрессирование и ангиогенные характеристики диабетических ран.
Аннотация
Однократная инъекция стрептозотоцина в высокой дозе с последующим иссечением кожи на всю толщину спины крыс является распространенным методом построения животных моделей диабетических ран 1 типа. Однако неправильные манипуляции могут привести к нестабильности модели и высокой смертности у крыс. К сожалению, существует несколько существующих руководств по моделированию диабетических ран 1 типа, и им не хватает деталей и не представлены конкретные эталонные стратегии. Таким образом, в этом протоколе подробно описывается полная процедура построения модели диабетической раны 1 типа и анализируются прогрессирование и ангиогенные характеристики диабетических ран. Моделирование диабетической раны 1 типа включает в себя следующие этапы: подготовка инъекции стрептозотоцина, индукция сахарного диабета 1 типа и построение модели раны. Площадь раны измеряли на 7-й и 14-й день после ранения, а кожные ткани крыс извлекали для гистопатологического и иммунофлюоресцентного анализа. Результаты показали, что сахарный диабет 1 типа, вызванный стрептозотоцином 55 мг / кг, был связан с более низкой смертностью и высокой вероятностью успеха. Уровень глюкозы в крови был относительно стабильным после 5 недель индукции. Скорость заживления диабетических ран была значительно ниже, чем у нормальных ран на 7-й и 14-й день (p < 0,05), но оба могли достигать более 90% на 14-й день. По сравнению с нормальной группой, закрытие эпидермального слоя диабетических ран на 14-е сутки было неполным и имело замедленную реэпителизацию и достоверно более низкий ангиогенез (p < 0,01). Модель диабетической раны 1 типа, построенная на основе этого протокола, имеет характеристики хронического заживления ран, включая плохое закрытие, отсроченную реэпителизацию и снижение ангиогенеза по сравнению с нормальными ранами крыс.
Введение
Сахарный диабет 1 типа (СД1) – хроническое заболевание обмена веществ, характеризующееся гипергликемией и разрушением β-клеток поджелудочной железы1. Рана СД1 является хронической незаживающей раной и наиболее частым и разрушительным осложнением сахарного диабета у человека 2,3. Животные модели являются наиболее подходящими прототипами для изучения патологических изменений во время заживления ран, а также безопасности и эффективности потенциальных терапевтических агентов4. По сравнению с другими типами, самцы крыс Sprague-Dawley (SD) более чувствительны к стрептозотоцину (STZ) и демонстрируют более низкий уровень смертности, что делает их популярными в исследованиях диабетических ран 5,6.
Описаны многочисленные методы построения моделей ран СД1. Что касается модели СД1, исследования в основном были сосредоточены на влиянии метода инъекций STZ на успешность индукции диабета 7,8. Однако процесс моделирования страдает от непоследовательного выполнения этого же шага. В одном исследовании крысы голодали в течение 18 часов перед инъекцией STZ; крысы с уровнем глюкозы в крови выше 16,67 ммоль / л через 1 неделю после инъекции STZ были признаны диабетиками, и диабетическая рана была введена через 3 недели9. И наоборот, в соответствующем исследовании Zhu et al. голодали крысам в течение 12 часов перед инъекцией STZ; крысы с уровнем глюкозы в крови выше 16,7 ммоль/л через 72 ч после инъекции считались диабетиками, и диабетическая рана вводилась через 4 недели10. В целом, существуют несоответствия в протоколах инъекций STZ, критериях диагностики диабета и времени введения в рану.
С точки зрения моделирования раны, в большинстве исследований иссекается вся толщина дорсальной кожи для построения ран СД1 после успешной индукции диабета11,12,13. Хотя эта модель подвержена кожной контрактуре у крыс, она является наиболее часто используемой моделью в исследованиях заживления ран, поскольку она менее трудоемка и дешева14,15. Тем не менее, методические исследования этого метода иссечения на всю толщину отсутствуют. Кроме того, в существующих исследованиях нет единых стандартов относительно размера и расположения раны12,16. Размер и расположение раны могут косвенно влиять на согласованность плана эксперимента и научную обоснованность результатов. Поэтому существует острая необходимость в стандартном протоколе индукции СД1 и моделирования ран в качестве справочного материала для исследователей. Целью данного исследования является визуализация конкретного протокола моделирования ран СД1, который может быть использован в качестве эталона для исследований ран СД1.
протокол
Протокол был проведен в соответствии с Хельсинкской декларацией, и все эксперименты на животных были одобрены Управляющим комитетом Университета традиционной китайской медицины Чэнду (запись No 2021-13).
1. Подготовка инъекции стрептозотоцина
- Выберите 15 самцов SD крыс, не содержащих патогенов (SPF), в возрасте 8 недель и весом 220 г ± 20 г. Используя простой метод рандомизации, разделите крыс на группу диабетиков (n = 10) и нормальную группу (n = 5).
- Измерьте начальный вес крыс и определите дозировку STZ путем введения 55 мг / кг.
ПРИМЕЧАНИЕ: Основываясь на предварительных экспериментах, 55 мг / кг является оптимальной дозой STZ. - Точно взвесьте порошок STZ и поместите его в светонепроницаемый контейнер.
- Добавьте соответствующее количество 0,1 моль/л буфера цитрата натрия (рН 4,5) для растворения STZ до концентрации 1%.
ПРИМЕЧАНИЕ: Перед использованием буфер цитрата натрия необходимо предварительно охладить в течение 2 часов в холодильнике с температурой 4 °C. Приготовление раствора СТЗ должно обеспечивать стерильность. - Встряхните в течение 30 с с помощью лекарственного осциллятора. Поместите в ящик для льда и отложите в сторону.
ПРИМЕЧАНИЕ: Инъекцию следует использовать в течение 15 минут.
2. Индукция модели T1DM
- Перед инъекцией STZ разговите крыс в течение 18 часов и обеспечьте свободный доступ к воде.
- Проводят внутрибрюшинную инъекцию 1% раствора СТЗ.
- Возьмите крысу и обнажьте кожу живота и место инъекции (пересечение линии, соединяющей корни двух бедер и среднюю линию живота).
- Дважды продезинфицируйте место инъекции ватным тампоном, смоченным в 75% спирте (один раз по часовой стрелке и один раз против часовой стрелки). Поместите голову крысы ниже брюшка.
- Введите иглу параллельно средней линии живота под углом 45°, а после прокалывания кожи уменьшите угол иглы до 30°, а затем введите иглу на 2-3 мм. Осторожно потяните за игольчатую пробку, следя за тем, чтобы в шприц не всасывалась кровь или жидкость. Введите раствор СТЗ, вытащите иглу и остановите кровотечение ватным тампоном.
ПРИМЕЧАНИЕ: Если желтая жидкость втягивается обратно в шприц, игла могла проникнуть в мочевой пузырь, а если втягивается темно-зеленая жидкость, игла могла проникнуть в толстую кишку или слепую кишку. В любом случае иглу следует немедленно извлечь. Животное должно быть оценено ветеринарным персоналом.
- Измерьте случайный (не натощак или натощак) уровень глюкозы в крови в 09:00 утра на 3-й день и 7-й день после индукции STZ.
ПРИМЕЧАНИЕ: Время для случайного измерения уровня глюкозы в крови фиксировано. В этом протоколе он зафиксирован в 09:00 утра. Однако это не единственное используемое время. Кровь, собранная из каудальной вены с помощью пункции иглой, менее восприимчива к тканевой жидкости, чем кровь, взятая из отрубленного хвоста, поэтому значения глюкозы в крови более точны.- Обездвижите крысу с помощью фиксатора крысы (рис. 1).
- Найдите расположение каудальной вены. Дважды продезинфицируйте хвост крысы, используя ватный тампон, смоченный в 75% спирте.
- Проколите каудальную вену, чтобы вызвать кровотечение, и измерьте уровень глюкозы в крови с помощью глюкометра. Остановите кровотечение ватным тампоном.
ПРИМЕЧАНИЕ: Уровень глюкозы выше 16,7 ммоль/л на 7-й день после инъекции STZ считается СД1.
- Еженедельно взвешивайте крыс и измеряйте уровень глюкозы в крови и другие параметры, включая диету, потребление воды и диурез.
- Кормите животных нормально в течение 8 недель после индукции STZ.
3. Построение модели раны
- Побрейте крыс электробритвой за 1 день до моделирования раны. Выбритая область 5 см х 5 см на спинной стороне крысы, как правило, идеальна.
- Протрите бритый участок теплым ватным тампоном с физиологическим раствором, дайте ему высохнуть, а затем нанесите крем для депиляции на 5 минут. Очистите область марлей и смойте остатки крема для депиляции теплым физиологическим раствором.
- Взвесьте крыс и рассчитайте необходимую дозу нембутала на основе стандарта 35 мг / кг. Растворите нембутал с помощью обычного физиологического раствора до концентрации 3%. Для этой процедуры можно использовать другие общие анестетики, такие как кетамин / ксилазин или изофлуран. Пожалуйста, работайте с институциональными комитетами по уходу за животными и их использованию, чтобы убедиться, что лучше.
ПРИМЕЧАНИЕ: Для обеспечения эффективности раствор должен быть свежеприготовленным, а порошок и раствор нембутала должны быть защищены от света. - Голодают крысам в течение 12 ч до анестезии. Вводят анестезию внутрибрюшинно. Используйте тетрациклиновую глазную мазь или общую смазку для глаз, чтобы предотвратить сухость глаз после введения анестезии.
ПРИМЕЧАНИЕ: Анестезия считалась умеренной, когда мышцы крысы были относительно расслаблены, движения глаз исчезли, дыхание было регулярным, а реакция на болевые раздражители была небольшой. - Дважды продезинфицируйте кожу спины, используя ватные тампоны, смоченные йодом (один раз по часовой стрелке и один раз против часовой стрелки) и 75% спиртом (альтернативные раунды).
- После высыхания срежьте кожу круговым биопсийным пуансоном диаметром 20 мм.
- Наложите палатку на кожу стерильными щипцами, а затем с помощью стерильных хирургических ножниц удалите кожу на всю толщину вдоль следов порезов. Остановите кровотечение с помощью обычного солевого ватного тампона.
ПРИМЕЧАНИЕ: Верхняя граница раны должна быть на 5-10 мм ниже нижней границы лопатки и на 5-10 мм справа/слева от позвоночника крысы (рис. 2). Раны симметричны вдоль позвоночника, когда строятся две раны. - Используйте вазелиновую марлю, чтобы покрыть раны, и оберните их марлей и дышащей повязкой, удерживаемой на месте резиновой лентой. Вводите карпрофен подкожно (5 мг / кг) один раз в день для облегчения послеоперационной боли. Меняйте повязку на рану один раз в день (использование карпрофена для обезболивания).
ПРИМЕЧАНИЕ: Наблюдайте за движением и дыханием крысы на предмет любых отклонений после наложения повязки и убедитесь, что дышащая повязка достаточно плотная. - Поместите линейку под рану и фотографируйте рану цифровой камерой до 14-го дня. Усыпьте крыс на 14-й день в соответствии с рекомендациями по уходу за животными и их использованию. Разрежьте рану кожной тканью на расстоянии 5 мм от края раны. Разделите образец ткани на две части, промойте их PBS для удаления видимых пятен крови, а затем зафиксируйте 4% раствором параформальдегида.
4. Расчет площади раны с помощью программного обеспечения ImageJ
- Нажмите кнопку « Файл » после открытия программного обеспечения, а затем раскройте и нажмите « Открыть », чтобы открыть раневые изображения.
- Выберите инструмент «Прямые » и нарисуйте прямую линию длиной 1 см вдоль линейки на рисунках раны.
- Нажмите на команду « Установить масштаб » в меню « Анализ » и установите для параметра «Известное расстояние » значение 1.
- Выберите инструмент « Выделение от руки » и нарисуйте контур раны на рисунке.
- Нажмите на команду « Измерить » в меню « Анализ» и прочтите значение «Площадь » после того, как появится результат.
5. Окрашивание гематоксилином и эозином (H&E)
- Извлеките кожную ткань из фиксатора, разрежьте ее на тонкие срезы скальпелем в вытяжном шкафу и поместите в кассету для обезвоживания.
- Поместите кассету для обезвоживания в дегидратационную машину и обезвоживайте ткани в следующие этапы: 75% спирт в течение 4 часов; 85% спирт в течение 2 ч; 90% спирт в течение 2 ч; 95% спирт в течение 1 ч; безводный этанол I и II по 30 мин каждый; спиртобензол в течение 5-10 мин; ксилол I и II по 5-10 мин; и воск I, II и III по 1 часу.
- Встройте салфетки в воск. Охладите при температуре −20° на морозильном столе и аккуратно поправьте восковой блок.
- Разрежьте восковые блоки в продольном направлении с помощью парафиновой секционной машины на участки толщиной 3 мкм.
- Последовательно замочите срез в ксилоле I и II на 20 мин каждый, безводном этаноле I и II на 5 мин каждый, водопроводной воде на 5 мин.
- Залить ткани гематоксилином в течение 3-5 мин, дифференцировать 0,5% водный раствор соляной кислоты, 0,5% водный раствор аммиака обратно до синего цвета и промыть водой.
- Обезвоживайте участки тканей 85% и 95% спиртом. Залить ткани раствором для окрашивания эозином на 5 минут.
ПРИМЕЧАНИЕ: Обычно окрашивание эозином занимает от 30 до 2 минут, и время может быть скорректировано в соответствии с результатами окрашивания и требованиями. - Последовательно обезвоживают срезы следующими растворами: безводный этанол I, безводный этанол II, безводный этанол III, ксилол I и ксилол II каждый в течение 5 мин. Наконец, покройте предметные стекла нейтральным бальзамом.
- Исследуйте ткани, окрашенные H&E, под микроскопом в 40, 20 и 10 раз и сделайте снимки, чтобы сохранить репрезентативные изображения каждого предметного стекла.
6. Иммунофлуоресцентное окрашивание CD31
- Замочите срезы тканей в ксилоле I и II на 15 мин каждый, безводном этаноле I и II на 5 мин каждый, 85% спирте на 5 мин и 75% спирте на 5 мин и промойте дистиллированной водой.
- Репарация антигена
- Добавьте подходящий буфер лимонной кислоты 10 мМ с pH 6,0 в емкость микроволновой печи, нагрейте его до кипения на сильном огне, а затем поместите в него предметное стекло.
- Кипятить 8 мин на среднем огне, остановиться на 8 мин, а затем снова кипятить на среднем или слабом огне в течение 7 мин.
- Дайте предметным стеклам остыть, поместите их в PBS (pH 7,4) и промойте три раза по 5 минут каждый с помощью шейкера для обесцвечивания.
- Добавьте 5% козьей сыворотки по каплям в круг и выдерживайте в течение 30 минут.
- Аккуратно стряхните укупорочный раствор (5% козью сыворотку) и добавьте антитело кролика против CD31 (разбавленное с помощью PBS в соотношении 1:200) по каплям на срезы. Поместите срезы во влажный ящик и инкубируйте в течение ночи при температуре 4 ° C.
- Промойте предметные стекла три раза PBS (pH 7,4) на шейкере для обесцвечивания в течение 5 минут каждый. Слегка встряхните срезы, чтобы высушить их, а затем покройте их круговой каплей козьего антикроличьего IgG с маркировкой FITC. Инкубировать при комнатной температуре в течение 50 минут в темноте.
- Промойте предметные стекла три раза PBS (pH 7,4) на шейкере для обесцвечивания в течение 5 минут каждый. Высушите срезы на воздухе легким встряхиванием и добавьте окрашивающий раствор DAPI. Выдержите срезы в темноте в течение 10 минут при комнатной температуре.
- После высыхания срезов нарисуйте круги вокруг ткани с помощью PepPen (чтобы предотвратить потерю антител), добавьте к кругам гасящий автофлуоресценцию агент (0,3% Sudan Black B) в течение 5 мин, а затем промойте их под проточной водой в течение 10 мин.
- Промойте предметные стекла три раза PBS (pH 7,4) на шейкере для обесцвечивания в течение 5 минут каждый. Слегка встряхните секции и загерметизируйте их монтажной средой с защитой от выцветания.
- Наблюдайте и фотографируйте срезы под флуоресцентным микроскопом в 40, 20 и 10 раз.
ПРИМЕЧАНИЕ: Длина волны возбуждения DAPI UV составляет 330-380 нм, а длина волны излучения составляет 420 нм (синий свет). Длина волны возбуждения FITC составляет 465-495 нм, а длина волны излучения - 515-555 нм (зеленый свет).
7. Статистический анализ
- Собирайте и анализируйте данные с помощью SPSS.
- Сообщайте данные как среднее ± стандартное отклонение.
- Используйте независимый выборочный t-критерий для анализа различий между диабетической и нормальной группами.
- Установите статистическую значимость на уровне **p < 0,01 и *p < 0,05.
Результаты
В общей сложности 10 крыс SD получили одну внутрибрюшинную инъекцию STZ для индукции модели СД1. Одна крыса умерла преждевременно (10%), но диабет был индуцирован у всех крыс (100%). После 3 дней инъекции STZ уровень глюкозы в крови всех крыс был выше 16,7 ммоль / л, а уровень глюкозы в крови стабилизировался через 5 недель после индукции (рис. 3A). Вес группы диабетиков постепенно увеличивался после инъекции STZ, но уменьшался на 3-й неделе, а затем снова медленно увеличивался с 4-й недели (рис. 3B). Напротив, вес крыс в нормальной группе неуклонно увеличивался, и их средний вес через 3 дня после индукции диабета был выше, чем в группе диабетиков (рис. 3B). У всех крыс с диабетом наблюдались типичные симптомы жажды, полиурии и потери веса, аналогичные выводам Hao et al.17.
На 7-й и 14-й день после ранения макроскопический анализ показал, что реэпителизация была более выражена у крыс в нормальной группе, чем в группе диабетиков (рис. 4А). Количественные результаты показали, что скорость заживления ран была достоверно ниже в группе диабетиков, чем в группе с нормальным уровнем на 7-й и 14-й день (p < 0,01). Однако на 14-й день скорость заживления ран также может быть выше 90% в группе диабетиков (p < 0,05, рис. 4B). Это говорит о том, что модель раны СД1 характеризуется плохим закрытием, но не в такой степени, как хроническое незаживание, наблюдаемое при диабетических ранах человека.
Окрашивание H&E на 14-й день заживления раны выявило неполный эпидермис раны, медленную пролиферацию кератиноцитов и задержку реэпителизации в группе диабетиков по сравнению с нормальной группой. Диабетические раны показали частичную потерю волосяных фолликулов и сальных желез. Также было меньше видимых капилляров (рис. 5).
Диабет вызывает дисфункцию эндотелиальных клеток, гликозилирование белков внеклеточного матрикса и сосудистую денервацию18. Эти осложнения приводят к более низкому, чем обычно, ангиогенезу ран при диабетических ранах18. Ангиогенез необходим для заживления ран, а раневой ангиогенез часто анализируется с помощью иммуноокрашивания CD31 (рис. 6A)19,20. Исходя из средней оптической плотности (AOD) экспрессии CD31, ангиогенез в месте раны был достоверно выше в норме, чем в группе диабетиков (p < 0,01, рис. 6B).
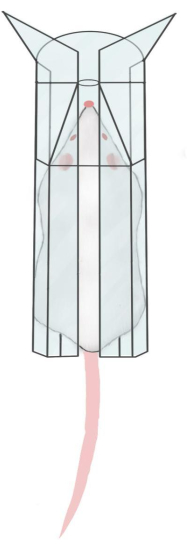
Рисунок 1: Изображение крыс, обездвиженных фиксаторами. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
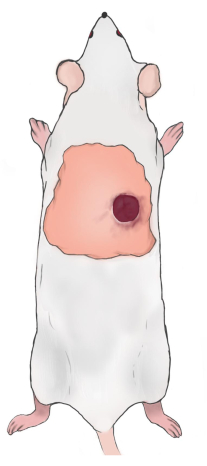
Рисунок 2: Схема расположения раны крысы. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
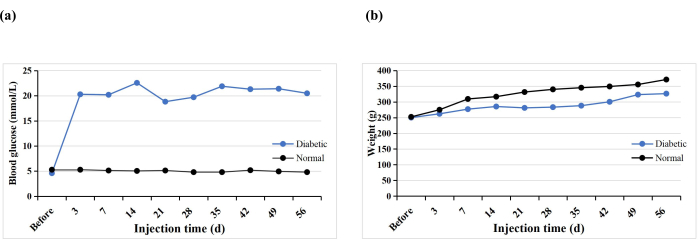
Рисунок 3: Уровни глюкозы в крови и вес экспериментальных крыс. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
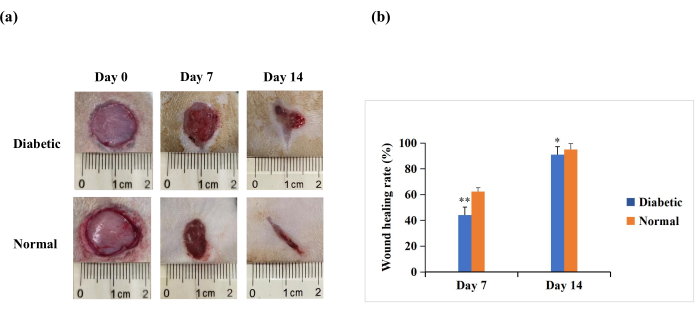
Рисунок 4: Кожные раны на всю толщину (диаметром 20 мм) на спине экспериментальных крыс. (A) Макроскопический вид ран на 0-й, 7-й и 14-й день. Изображения морфологии ран на 0-й, 7-й и 14-й дни были получены с помощью цифровой камеры. (B) Площадь раны была измерена с помощью программного обеспечения ImageJ и использовалась для расчета скорости заживления раны. Скорость заживления раны (%) рассчитывали следующим образом: (начальная площадь раны − площадь раны в указанный момент времени)/начальная площадь раны × 100. Значения представлены как средние ± SD (n = 14). Статистическая значимость была установлена на уровне ** p < 0,01 и * p < 0,05. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
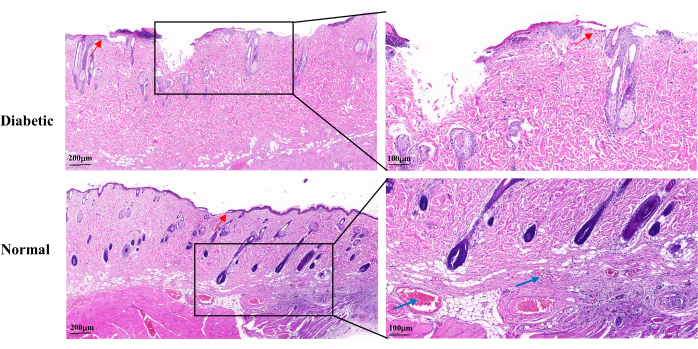
Рисунок 5: Репрезентативные гистопатологические изображения H&E на 14-й день после заживления раны. Синими стрелками обозначены капилляры. Красные стрелки показывают пролиферацию кератиноцитов. Левая шкала: один стержень = 200 мкм; Правая шкала: одна полоса = 100 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
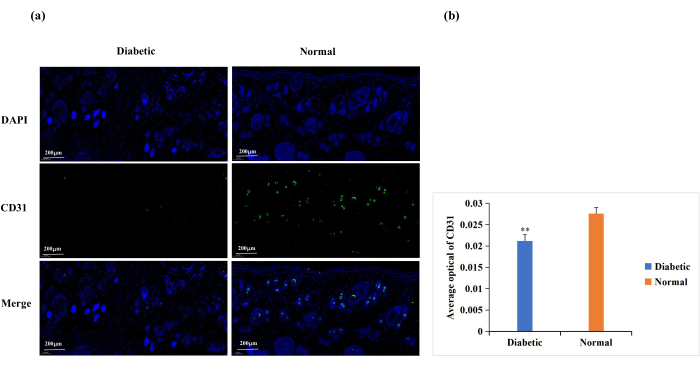
Рисунок 6: Иммунофлуоресцентный анализ окрашивания на экспрессию CD31. Уровни CD31 использовались для определения состояния ангиогенеза. (A) Репрезентативные изображения иммунофлуоресцентного окрашивания CD31 в диабетической и нормальной группах. Интегральное значение оптической плотности (IOD) и площадь пикселя (AREA) для каждого образца кожи были рассчитаны с помощью программного обеспечения Image-Pro Plus 6.0. Также было получено среднее значение оптической плотности (AOD) (AOD = IOD/AREA). Значение AOD было прямо пропорционально положительной экспрессии CD31. (B) Количественное сравнение положительной экспрессии CD31 в диабетической и нормальной группах. Данные представлены в виде среднего ± SD. ** p < 0,01. Масштаб: один стержень = 200 мкм. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Обсуждение
Этот протокол разъясняет спорные операции при моделировании раны СД1. В этой работе были рассмотрены вопросы, связанные с протоколами инъекций STZ, критериями успеха индукции СД1, временем стабилизации уровня глюкозы в крови, а также расположением и размером раны. Кроме того, уточнены патологические характеристики и измеримые параметры для оценки заживления ран СД1.
Крысы голодали в течение 18 ч перед инъекцией STZ, чтобы избежать конкурентного связывания глюкозы или ее аналогов с β-клетками, что могло повлиять на эффективность STZ. Наиболее часто используемым методом индукции СД1 является однократная высокая доза STZ, которая увеличивает уровень глюкозы в крови за счет повреждения островков и снижения секреции инсулина21. Предэкспериментальные испытания показали, что оптимальная доза STZ для высокой частоты успеха и низкого уровня смертности составила 55 мг / кг, что ниже оптимальных доз, о которых сообщалось в предыдущих исследованиях22,23,24. В этом протоколе СД1 индуцировали с помощью однократной внутрибрюшинной инъекции 55 мг/кг STZ.
Уровень глюкозы в крови был выше 16,7 ммоль / л через 3 дня после инъекции STZ. Тем не менее, уровень глюкозы в крови выше 16,7 ммоль / л на 7-й день после инъекции STZ является рекомендуемым критерием для успешного моделирования СД1, поскольку степень повреждения островков варьируется у крыс, и соответствующее продление времени диагностики может снизить ложноотрицательную частоту. Кроме того, колебания уровня глюкозы в крови стабилизировались через 5 недель после инъекции STZ, и крысы постепенно набирали вес в течение этого периода, что согласуется с предыдущими результатами25,26. Это указывает на то, что уровень глюкозы в крови в модели СД1 должен быть стабилизирован в течение не менее 6 недель, а увеличение массы крысы через 6 недель снижает показатели смертности при моделировании раны. Следовательно, по этому протоколу проводилось моделирование раны через 8 недель после инъекции STZ.
Частота закрытия раны на 7-й и 14-й день после ранения была значительно ниже у диабетиков, чем в группе с нормальной раной, что указывает на медленное заживление. Более того, реэпителизация раны и ангиогенез были значительно ниже у диабетиков, чем в нормальной группе. Это свидетельствует о том, что модель раны СД1 демонстрирует более медленное заживление ран и замедленную реэпителизацию, чем у нормальных крыс, что может быть связано с патологическими изменениями сниженного раневого ангиогенеза. Однако на 14-й день скорость заживления ран СД1 также была выше 90%, что отличается от хронической незаживляющей характеристики диабетических ран человека. Это может быть связано с тем, что физиологические механизмы заживления ран у грызунов отличаются от таковых у людей27. Следовательно, наилучший диаметр раны составляет не менее 20 мм, что достаточно много, чтобы дать время оценить эффективность вмешательства в исследовании диабетической раны. Расположение раны должно избегать лопатки и позвоночника, так как непрерывное движение в этих двух местах может нарушить заживление раны.
В заключение следует отметить, что построение модели раны СД1 с использованием метода данного протокола является эффективным. Протокол воспроизводит некоторые характеристики хронических диабетических ран, такие как более медленное заживление ран, отсроченная реэпителизация и снижение ангиогенеза по сравнению с обычными ранами крыс. Однако неизвестно, может ли модель воспроизвести другие хронические фенотипы диабетических ран. Кроме того, этот протокол описывает наиболее фундаментальный и широко используемый метод, который не учитывает проблему сокращения кожи у крыс. Будущие исследования могут включать использование раневых шин в этот протокол или изучать дополнительные модели хронических диабетических ран, что станет серьезной проблемой для исследователей в будущем.
Раскрытие информации
Все авторы заявляют, что данная рукопись не имеет конфликта интересов.
Благодарности
Это исследование было финансово поддержано Национальным фондом естественных наук Китая (82104877).
Материалы
| Name | Company | Catalog Number | Comments |
| Antifade mounting medium | Southern Biotechnology Associates, Inc. | 0100-01 | |
| AutoFluo Quencher | Servicebio Technology co., Ltd. | G1221 | |
| Automatic slide stainer | Thermo Fisher Scientific Inc. | Varistain™ Gemini ES | |
| CD31 | Servicebio Technology co., Ltd. | GB11063-2 | |
| Citrate antigen retrieval solution | Servicebio Technology co., Ltd. | G1201 | |
| Cover glass | Citotest Labware Manufacturing Co., Ltd. | 10212432C | |
| DAPI | Servicebio Technology co., Ltd. | G1012 | |
| Decolorization shaker | Scilogex | S1010E | |
| Depilatory cream | Guangzhou Ruixin Biotechnology Co., Ltd. | — | |
| Dimethyl benzene | Chengdu Kelong Chemical Co., Ltd. | 64-17-5 | |
| Drug oscillator | Shenzhen Jiashi Technology Co., Ltd. | VM-370 | |
| Electric razor | Shanghai Flyco Electrical Appliance Co., Ltd. | FC5908 | |
| Embedding machine | Wuhan Junjie Electronics Co., Ltd. | JB-P5 | |
| Ethanol absolute | Chengdu Kelong Chemical Co., Ltd. | 1330-20-7 | |
| Fitc-labeled goat anti-rabbit IgG | Servicebio Technology co., Ltd. | GB22303 | |
| Goat serum | Thermo Fisher Scientific Inc. | 16210064 | |
| Hematoxylin and eosin staining solution | Beijing Regan Biotechnology Co., Ltd. | DH0020 | |
| Image J software | National Institutes of Health | — | |
| Microwave oven | Midea Group Co., Ltd. | M1-L213B | |
| Mini centrifuge | Scilogex | D1008 | |
| Neutral balsam | Sinopharm Chemical Reagent Co., Ltd | 10004160 | |
| PBS buffer | Biosharp | G4202 | |
| Portable blood glucose meter | Sinocare Inc. | GA-3 | |
| Rapid tissue processor | Thermo Fisher Scientific Inc. | STP420 ES | |
| Rat fixator | Globalebio (Beijing) Technology co., Ltd | GEGD-Q10G1 | |
| Slicing machine | Thermo Fisher Scientific Inc. | HM325 | |
| Slides glass | Citotest Labware Manufacturing Co., Ltd. | 80312-3181 | |
| sodium citrate buffer | Beijing Solarbio Science & Technology Co., Ltd. | c1013 | |
| Streptozotocin | Sigma | 57654595 |
Ссылки
- Zimmet, P., Alberti, K. G., Shaw, J. Global and societal implications of the diabetes epidemic. Nature. 414 (6865), 782-787 (2001).
- Grennan, D. Diabetic foot ulcers. Journal of the American Medical Association. 321 (1), 114 (2019).
- Eming, S. A., Martin, P., Tomic-Canic, M. Wound repair and regeneration: Mechanisms, signaling, and translation. Science Translational Medicine. 6 (265), 265sr6 (2014).
- Patel, S., Srivastava, S., Singh, M. R., Singh, D. Mechanistic insight into diabetic wounds: Pathogenesis, molecular targets and treatment strategies to pace wound healing. Biomedicine & Pharmacotherapy. 112, 108615 (2019).
- Deeds, M. C., et al. Single dose streptozotocin-induced diabetes: Considerations for study design in islet transplantation models. Laboratory Animals. 45 (3), 131-140 (2011).
- Chao, P. C., et al. Investigation of insulin resistance in the popularly used four rat models of type-2 diabetes. Biomedicine & Pharmacotherapy. 101, 155-161 (2018).
- Furman, B. L. Streptozotocin-induced diabetic models in mice and rats. Current Protocols. 1 (4), e78 (2021).
- Wu, J., Yan, L. J. Streptozotocin-induced type 1 diabetes in rodents as a model for studying mitochondrial mechanisms of diabetic β cell glucotoxicity. Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy. 8, 181-188 (2015).
- Yang, J., Chen, Z., Pan, D., Li, H., Shen, J. Umbilical cord-derived mesenchymal stem cell-derived exosomes combined pluronic F127 hydrogel promote chronic diabetic wound healing and complete skin regeneration. International Journal of Nanomedicine. 15, 5911-5926 (2020).
- Zhu, Y., Wang, Y., Jia, Y., Xu, J., Chai, Y. Roxadustat promotes angiogenesis through HIF-1α/VEGF/VEGFR2 signaling and accelerates cutaneous wound healing in diabetic rats. Wound Repair and Regeneration. 27 (4), 324-334 (2019).
- Shao, Z., et al. Wound microenvironment self-adaptive hydrogel with efficient angiogenesis for promoting diabetic wound healing. Bioactive Materials. 20, 561-573 (2022).
- Asfour, H. Z., et al. Enhanced healing efficacy of an optimized gabapentin-melittin nanoconjugate gel-loaded formulation in excised wounds of diabetic rats. Drug Delivery. 29 (1), 1892-1902 (2022).
- Wei, L., et al. Mesenchymal stem cells promote wound healing and effects on expression of matrix metalloproteinases-8 and 9 in the wound tissue of diabetic rats. Stem Cells and Development. 32 (1-2), 25-31 (2022).
- Pastar, I., et al. . Preclinical models for wound-healing studies. In Skin Tissue Models., edited by. , 223-253 (2018).
- Yang, R. H., et al. Epidermal stem cells (ESCs) accelerate diabetic wound healing via the Notch signalling pathway. Bioscience Reports. 36 (4), e00364 (2016).
- Suliman Maashi, M., Felemban, S. G., Almasmoum, H. A., Jarahian, M. Nicaraven-loaded electrospun wound dressings promote diabetic wound healing via proangiogenic and immunomodulatory functions: A preclinical investigation. Drug Delivery and Translational Research. 13 (1), 222-236 (2023).
- Hao, M., Ding, C., Sun, S., Peng, X., Liu, W. Chitosan/sodium alginate/velvet antler blood peptides hydrogel promotes diabetic wound healing via regulating angiogenesis, inflammatory response and skin flora. Journal of Inflammation Research. 15, 4921-4938 (2022).
- Kolluru, G. K., Bir, S. C., Kevil, C. G. Endothelial dysfunction and diabetes: Effects on angiogenesis, vascular remodeling, and wound healing. International Journal of Vascular Medicine. 2012, 918267 (2012).
- Okonkwo, U. A., DiPietro, L. A. Diabetes and wound angiogenesis. International Journal of Molecular Sciences. 18 (7), 1419 (2017).
- Yi, C., et al. Targeted inhibition of endothelial calpain delays wound healing by reducing inflammation and angiogenesis. Cell Death & Disease. 11 (7), 533 (2020).
- Goodson 3rd, W. H., Hung, T. K. Studies of wound healing in experimental diabetes mellitus. Journal of Surgical Research. 22 (3), 221-227 (1977).
- Luippold, G., Klein, T., Mark, M., Empagliflozin Grempler, R. a novel potent and selective SGLT-2 inhibitor, improves glycaemic control alone and in combination with insulin in streptozotocin-induced diabetic rats, a model of type 1 diabetes mellitus. Diabetes, Obesity & Metabolism. 14 (7), 601-607 (2012).
- Sayed, N., et al. Effect of dapagliflozin alone and in combination with insulin in a rat model of type 1 diabetes. The Journal of Veterinary Medical Science. 82 (4), 467-474 (2020).
- Han, Y., et al. Human umbilical cord mesenchymal stem cells implantation accelerates cutaneous wound healing in diabetic rats via the Wnt signaling pathway. European Journal of Medical Research. 24 (1), 10 (2019).
- Ansell, D. M., Marsh, C., Walker, L., Hardman, M. J., Holden, K. Evaluating STZ-induced impaired wound healing in rats. Journal of Investigative Dermatology. 138 (4), 994-997 (2018).
- Liu, Y., et al. Human umbilical cord-derived mesenchymal stem cells not only ameliorate blood glucose but also protect vascular endothelium from diabetic damage through a paracrine mechanism mediated by MAPK/ERK signaling. Stem Cell Research & Therapy. 13 (1), 258 (2022).
- Zindle, J. K., Wolinsky, E., Bogie, K. M. A review of animal models from 2015 to 2020 for preclinical chronic wounds relevant to human health. Journal of Tissue Viability. 30 (3), 291-300 (2021).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены