Method Article
Virüs mutasyon Frekans RNA Virüsler ve Karakterizasyonu Fidelity Varyantlar izolasyonu
Bu Makalede
Özet
Bu makale, RNA virüsleri ve doku kültürü aslına Değişiklikleri onaylamak için mutasyon sıklığı verileri kullanmak RNA polimeraz sadakat varyantları izole ve karakterize etmek için gerekli adımları açıklamaktadır.
Özet
RNA virüsleri RNA bağımlı RNA polimeraz genomların çoğaltmak için kullanın. Bu enzimlerin özünde yüksek hata oranı virüs adaptasyon ve evrim kolaylaştıran aşırı nüfus çeşitliliğinin nesil için büyük bir katkıda bulunuyor. Giderek artan kanıtlar, içsel bir hata oranları ve RNA virüsleri ortaya çıkan mutasyon frekansları, viral polimeraz ince amino asit değişiklikleri modüle olabileceğini göstermektedir. Biyokimyasal testleri dahil kantitatif ölçmek sadakat izin veren bazı viral RNA polimeraz için mevcut olmasına rağmen, biz burada sadakat değiştirerek mutasyonları tespit biyokimyasal yaklaşımlar kadar doğru olduğunu kanıtlamıştır RNA virüslerinin mutasyon frekansları ölçmek için basit bir yöntem tarif. Bu yaklaşım, en biyoloji laboratuarları yapılabilir geleneksel virolojik ve sıralama teknikleri kullanır. Bir dizi farklı virüsler ile tecrübemize dayanarak, sadakat varyantları tecrit ve istatistiksel olarak anlamlı veri üreten olasılığını artırmak için optimize edilmesi gereken önemli adımları belirledik. Sadakat değiştiren mutasyonlar izolasyonu ve karakterizasyonu polimeraz yapısı ve fonksiyonu 1-3 yeni anlayışlar sağlayabilir. Ayrıca, bu sadakat varyantları virüs adaptasyon ve evrim mekanizmaları 4-7 karakterize faydalı bir araç olabilir.
Protokol
1. Minimal hücreleri için toksik, mutajen konsantrasyonlarının aralığı belirlemek
Bu alıştırmanın amacı, mutajen konsantrasyonlarının aralığı fazla hücre toksisite olmadan bir enfeksiyon sırasında kullanılan ne olabilir belirlemektir. Esasen, virüs enfeksiyonu için gerekli koşulları çoğaltmak isteyecektir. En çok virüsler, enfeksiyonlar 2 ile 7 gün arasında sürebilir. Her gün numune hücreleri için yeterli bir tabak hazırlayın. Yapışmaz hücrelerin kullanılması halinde, bu doğrultuda protokolü değiştirin.
- Denemeden önce, tohum 7 gün x 10 5 HeLa hücrelerinde / iyi bir alt konfluent (% 75) tek tabaka elde bir deney gün 6 plaka. Plakasının her bir iyi, bir dizi 6 konsantrasyonlarının izin mutajen farklı bir konsantrasyon ile ele alınacaktır.
- Deney günü, mutajen dilüsyonları doku kültürü ortamı hazırlayın. HeLa hücreleri için, baz analogları için 0 ila 1000 mcM aralığı (ribavirin, 5-fluorourasil, 5-azacytidine), 0 - 50 mM MgCl 2 ve MnCl 2 için 0 ile 5 mM kullanın.
- Kuyulardan orta aspire ve 2 ml mutajen desteği orta ve inkübatör dönmek ile değiştirin.
- Her 24 saatte bir, hücre hücre canlılığı kontrol etmek için bir tabak kullanın. Bu boyama mavi tripan veya ticarileştirilmiş floresan / lüminesans testlerin (örneğin Promega CellTiter-Glo ® Luminesans Hücre Canlılık Testi) kullanılarak yapılabilir.
- Trypan mavisiyle boyama boyama için bir plaka (mutajen farklı konsantrasyonları ile tedavi) ve santrifüj yoluyla hafifçe pelet hücreler hücreleri ayırın.
- PBS içinde supernatant ve tekrar süspansiyon hücreleri (serum boyama ile müdahale) atın.
- Oda sıcaklığında 2 dakika boyunca inkübe% 0.4 tripan mavi, 1 hacim 1 hacim hücre süspansiyon PBS içinde karıştırın.
- Bir hemasitometre, uygulanabilir (boyasız) ve cansız (lekeli mavi) hücreleri sayar. Mutajen tedavi edilmezse kontrolü de dahil olmak üzere her bir konsantrasyon için geçerli hücrelerinin yüzdesini hesaplayın. Biz bu koşulları sonucu enfeksiyon sonlanma noktası% 50 daha az hücre ölümü (maksimum titreleri ulaşıldığında) mutajen direnç izolasyonu için ideal olduğunu bulabilirsiniz.
2. Orta (yaklaşık 0.5-2 log azalma) virüs titreleri azaltır optimal toksik olmayan mutajen konsantrasyon belirleyin
Bu egzersiz, nüfusun aşırı mutagenizing olmadan, güçlü bir seçici baskı mutajen konsantrasyonu belirlemek için hizmet vermektedir. RNA mutajenler için, biz bu virüs titresi 10,5-2 günlükleri azalmalara karşılık geldiğini bulabilirsiniz. Bu konsantrasyonlarda, her genomunun en az bir veya iki pozisyonda mutasyona uğramış. Mutajen direnci mutasyon, daha sonra geçit üzerinden seçilecektir nesil yardımcı olabilir. Çok sayıda mutasyonlar tanıtıldı (çok yüksek mutajen konsantrasyonlarda), direnç mutasyonu taşıyan mutantlar kendilerini onların izolasyon engelleyen ölümcül mutagenized olacaktır.
- 1. adımı kullanarak aynı koşullar hücreleri ile Tohum plakalar
- Deney günü, mutajen dilüsyonları doku kültürü ortamı hazırlayın. Yukarıda belirlenen konsantrasyonları aynı aralıkta kullanın, ancak konsantrasyonları hariç% 50'den fazla hücre ölümü ile sonuçlandı. Mutajen her bir konsantrasyon ile, enfeksiyon önce hücreleri tedavi öncesi için izin, iki kez (ortalama 4 ml) iyi karşılamak için yeterli orta hazırlayın.
- 2 saat boyunca mutajen desteği ortamda inkübe mutajen, orta ve ön işlemden hücreleri aspire. Çoğu hücre tipleri için, bu mutajen alımı için yeterli zaman.
- Orta çıkarın ve minimum hacim düşük enfeksiyon çokluğu İçişleri Bakanlığı (0.1 veya 0.01) (6 kuyucuğu için 200 ul) virüsü ile enfekte. Virüs hücreleri enfekte izin vermek için 15-60 dakika inkübe edin. Inokulum hücre tek tabaka kapsar emin olmak için düzenli aralıklarla plaka Rock.
- Inoküle virüs aspire edin ve mümkün olduğu kadar çok inokulum kaldırmak için 2 ml PBS ile iki kez yıkayın.
- 3-6 çoğaltma döngüleri eşdeğer her iyi ve inkübe hücreleri mutajen uygun konsantrasyonları orta ekleyin.
- Hasat her kuyudan virüs ve virüs titresi antiviral etkisini belirlemek. Bu standart plak tahlil veya seyreltme sınırlayıcı (TCID 50) tarafından yapılabilir. Not: teknikleri ile virüs Kantitasyonu mutajenik etkileri tespit edilemez çünkü tedbir ancak RNA sentezi uygun olmayabilir. Ölümcül mutasyonlar içeren Mutagenized genomların hala örneğin QRT-PCR ile tespit edilebilir, ancak virüs canlılığı deneyleri gözlenen olmazdı.
- Hesaplanan titreleri, aynı zamanda hücreleri (ideal olarak,% 50 daha az toksisite) yüksek derecede toksik değildir 10,5-2 günlükler virüs titreleri azaltır mutajen konsantrasyonu (tedavi edilmemiş kontrol enfeksiyona kıyasla) tanımlamak.
3. İzolasyon ve tanımladıbahsedilmekte, mutajen dirençli varyantları
Yukarıda tanımlanan optimum mutajen konsantrasyon büyük nüfus büyüklüğü geçişleri gerçekleştirmek ve geçit serisi genelinde virüs titreleri kontrol. Kontrol olarak, herhangi bir mutajen olmadan büyüme orta geçit virüs. Başka bir denetime arızalı müdahale parçacıklar (DI) potansiyelinin ortaya çıkması izlemek için olduğu gibi, her geçiş adım (unpassaged kontrol) mutajen yokluğu taze enfeksiyonların gerçekleştirin.
- Gününde enfeksiyon, tohum 25 cm önce 1,5 x 10 6 HeLa hücrelerinde (diğer şişesi boyutları kullanılabilir) 2 adet matara, ertesi gün alt-konfluent mono tabakaları elde etmek için .
- Enfeksiyon gün, 2 saat boyunca her mutajen 2. bölümünde belirlenen optimal konsantrasyonu içeren orta hücreleri ön işlemden.
- Orta çıkarın ve en az bir İçişleri Bakanlığı 1 veya virüs çalışılan arızalı müdahale (DI) parçacık oluşumu sonucu olmadığı İçişleri Bakanlığı en büyük hacmi ile hücreleri enfekte.
- 30-60 dakika sonra enfeksiyon, inokulum aspirat ve PBS ile iki kez yıkayın, daha sonra uygun konsantrasyonlarda mutajen ile desteklenmiş taze orta ekleyin.
- Bu koşullarda maksimum virüs titresi karşılık gelen bölüm 1 ve 2 belirlenen süre için inkübe edin. Döl virüs Hasat.
- Titresi her geçit virüs ve 3 Yukarıdaki adımları tekrarlayın.
- Ilk birkaç geçişleri sırasında, mutajen tedavi örnekleri virüs titreleri orijinal virüs titresi ve kontrolü (tedavi edilmemiş ve unpassaged) virüs titreleri göre, buna göre damla gerekir. Mutajen, virüs titreleri örnekleri tedavi edilmezse kontrolü ile aynı seviyelere geri tırmanmaya geçişli, nüfusun büyük bir ihtimalle mutajen dayanıklı varyant içerir. 5 ve 15 pasajlar arasında sadakat varyantları en izole olmasına rağmen 20 veya 30 geçişleri için gerekli olabilir.
- Belirli bir geçiş serisi için virüs titreleri tedavi edilmezse kontrolü titreleri olarak aynı büyüklüğe ulaştıklarında, aynı pasajda sayıda tedavi edilmezse kontrolü de dahil olmak üzere tüm örneklerinden RNA ayıklayın. RNA ekstraksiyon kitleri veya Trizol çıkarma kullanılabilir.
- RT-PCR ilgi virüs polimeraz veya replikaz genler yükseltmek primerler kullanarak gerçekleştirin. İkinci adımda ise, tüm genom (en az kodlama bölgeleri) direnç fenotipleri de başka bir virüs genleri için harita olup olmadığını incelemek için sıralı olmalıdır. Bu ribavirin, virüs ve hücre fonksiyonu diğer yönlerini etkiler gibi baz analog mutajenler için özellikle önemlidir. Bu durumda varyant bu diğer antiviral faaliyetleri biri dayanıklı olabilir ve bir vefa varyant olmayacaktır.
- Mutajen dayanıklı nüfus konsensüs sırasını elde etmek için PCR saflaştırma kiti ve sırası ile RT-PCR ürünleri arındırın. (Tartışma) sıralama hata için arka plan denetimleri ekleyin.
- Bir referans olarak kullanarak, bir dizi hizalama yazılım ve virüs konsensüs dizisi dizileri aynı hizaya getirin. Virüs titreleri normal seviyelere ulaşan geçit mutajen tedavi nüfus görünen herhangi özel bir önem verilerek yeni bir nokta mutasyonları, tanımlayın. Bu mutasyon önceki pasajlar bulunan ve aynı geçiş sayısı (hücre kültürü geçit uyum gösteren) tedavi edilmezse kontrolleri mevcut değil ise, o zaman bu mutasyon mutajen direnci için, en azından kısmen, muhtemelen sorumludur. Baz olarak adlandırılan dizisi (sırası metin versiyonu) ve yalnız hizalama yazılım güvenmeyin. Hizalama yazılım tarafından kaçırılmış olabilir azınlık doruklarına kromatogramlar kontrol edin. Toplam nüfusun% 20-30 oranında temsil eden bir mutant hala bir pik olarak göstermek, ancak standart dizi analizi bir 'N' olarak tanımlanan çok küçük olacak.
4. Bir mutasyon tespit edildikten sonra, izole veya varyant ve çeşitli RNA mutajenler direnç fenotipi onaylamak
Daha sonra, belirlenen mutasyon sunulması varyant direnç fenotipi bağlantı onaylamak için izole edilmiştir. Bu sadakat değişen şüphelenilen mutasyon (yani, başka genom ek mutasyonlar sunmuyorlar) genetik temiz bir arka planda incelenmiştir esastır. En iyi durum, bulaşıcı bir cDNA klonu, bir hisse senedi, genetik temiz bir arka plan üzerinde site directed mutagenesis mutajen dayanıklı varyant nesil izin verecek var. Bu durumda, 4. bölümde gerekli değildir. Ancak, bir cDNA klonu mevcut değilse, izolasyon aşağıda açıklanan plak arıtma, virüs tarafından yapılması olabilir. Bir tur fazla plak arınma, temiz, genetik bir arka plan üzerinde varyant izole etmek için gerekli olabilir.
- Mutajen dirençli mutant plak yöntemi ile izolasyonu.
- Tespit mutant izole etmek için, standart bir plak tahlil agaroz (ağırlık / hacim son 0,5 -% 1) 6-kuyucuğu kaplaması altında gerçekleştirin. Dil için stok titreleri dayalı virüs seri dilüsyonları, hazırlayın10 ve 50 iyi ayrılmış plaklar arasında üretecek utions.
- Plaklar açıkça görülebilir virüs bağlı olarak 2 ile 5 gün sonrası enfeksiyon, (genellikle), plakalar plakların yerini işaretlemek ve filtre ucu ile P200 pipet kullanarak agaroz bindirme yoluyla ucu hafifçe atılmak için dikkatli yerinden ve bindirme konumunu vardiya (bireysel plakların çapraz kontaminasyon sonucu).
- Kaplamanın ucu dikkatlice kaldırın ve orta ve vorteks 250 ul içeren bir eppendorf ucu bulunan agaroz fiş aktarımı. Ucu kaldırılır agaroz içermiyorsa Merak etmeyin, pek çok RNA virüsleri için, pek çok RNA virüsleri için ortalama bir plak 10 5 virüsleri içerir ve yeterli miktarda plak yüzeyine ucu dokunarak kolayca transfer edilecektir.
- Mutajen tedavi başına 10 plaklar Pick up. Mutasyon tespit sıralama kromatogramlar bağlı, istenilen mutasyon içeren nüfusun ne oranda yaklaşık olarak tahmin. Amacı, mutasyon ile üç ya da dört plaklar izole etmektir. Bu mutantların bazıları da daha sonra sıralama tarafından tespit edilecek ek istenmeyen mutasyonlar taşıyacaktır.
- (Ama virüs daha büyük bir stok yapmak için örnek yarısı kaydetmek) bu örneklerden RNA ayıklayın ve tüm genom diziliminin izin RT-PCR gerçekleştirmek. Bu nedenle, herhangi bir ek mutasyonlar olmadan istenilen mutasyon içeren izole belirlemek için bir zaman virüsler saflaştırılmış dizisi 3 ya da 4 plak, ortalama olarak, RNA virüsleri fikir birliği sırasına göre iki mutasyon farklılıklar içerecektir.
- Tespit T75 balon hücreleri, örneğin 8x10 6 HeLa hücrelerinde daha büyük bir balon bulaştırmak için yukarıda elde edilen plak arıtılmış örnek kullanarak, tüm alt çalışmaları için bu virüsün daha büyük bir stok yapmak ..
- Tespit mutasyon öngördüğü mutajen duyarlılık / direnç onaylayın.
- Ya tam bir mutajen konsantrasyonlarının aralığı ya da direnç mutasyonu oluşturulduğu konsantrasyonu kullanarak bölüm 2 deneyleri tekrarlama, izole veya yeni oluşturulan klon, benzer koşullarda hazırlanan ve vahşi bir tür denetim virüsü kullanma.
- Birkaç farklı RNA mutajenik koşulları kullanın (ribavirin, 5-fluorourasil, 5-azacytidine, Mg 2 arttı +, Mn 2 +). Polimeraz varyantı mutajen, birden fazla tür dayanıklı ise, o zaman bu varyant yüksek sadakat olduğunu olasılığı daha yüksektir. Alternatif olarak, bu bileşiklerin bazı mekanizmaları 8 numara üzerinden RNA virüsleri etkileyen bir direnç mutasyon, özellikle bu yana, tek bir mutajenik durum için özel olduğunu mümkündür .
5. Çoğaltma oranlarını kontrol edin
Yılından bu yana sadakat değiştiren mutasyonlar en sık polimeraz harita, aynı polimeraz mutasyonu çoğaltma kinetiği önemli ölçüde değiştirecek ve bu mutasyon frekansları farklılıkları daha iyi bir karşılaştırma altında bir performans izin verecektir çoğaltma benzerlikleri ve farklılıkları belirlemek için önemlidir. Virüs üretim ve RNA sentezi inceler başka inceler - Bunu yapmak için, en az iki tamamlayıcı yaklaşımlar ile çoğaltma incelemek.
- Bir adım virüs büyüme kinetiği
- Gün önce deney, tohum 6-kuyucuğu gerektiği şekilde test edilecek nokta başına bir plaka. Her mutant ve vahşi tip virüs için üç nüsha kuyu kullanmayı düşünün.
- Deney günü, orta kaldırmak ve her hücrede aynı anda enfekte olduğundan emin olmak için 10, bir İçişleri Bakanlığı kuyuların her virüs bulaştırmak. 37 az 30-60 dakika inkübe ° C
- Kaya levhalar her 10 dakikada bir hücre tek tabaka kurumasını önlemek için. Virüs çıkarın ve 2 ml PBS ile iki kez yıkayın. , Mümkün olduğu inokulum kadar çok kaldırmak için önemlidir. Besi ile değiştirin.
- Bir tabak zaman = 0, hasat virüs bulaştıktan sonra. Inkübatör plakalarını dönün ve düzenli aralıklarla tek bir çoğaltma döngüsü (7h 3h örneğin, 5 saat, 9 saat, 12 saat, 24 saat) yayılan virüsler hasat.
- Titresi her zaman noktası (örneğin plak testi TCID50, FFU tahlil) hasat virüs, ve grafik titresi zamana büyüme eğrileri.
- RNA sentezi Kinetiği
RNA sentezi kinetiği yaklaşımlar aşağıda belirtilen kullanarak izlenebilir. Mümkünse, bir adım büyüme kinetiği belirlemek için kullanılan aynı örnekleri RNA düzeylerini ölçmek için kullanılmalıdır.- Mah-PCR. Bu prosedür birkaç genom kopya> 10 10 testinin hassasiyetine bağlı olarak, geniş bir yelpazede üzerinde çoğaltma yüksek kantitatif tedbirler verir . Tasarım astar ve son derece korunmuş bir genomik bölgenin küçük bir parçası (<200 bp) kapsamaktadır probları.
- Northern blot analizi. Mah-PCR daha az kantitatif rağmen, bu tekniğin, tam uzunlukta genomların ve çoğaltma sonuçları anlamlı zincir sonlanması polimeraz mutasyon sonucu olarak ortaya çıkar görsel onay izin verir.
- Bir muhabir gen ifadesi. Bir muhabir gen (örneğin lusiferaz) ifade eden bir cDNA klonu varsa, o zaman bu replikatif kapasitesini incelemek için bir vekil olarak kullanılır olabilir. Ancak, rekombinant virüs bu virüs üzerinde etkili seçici baskılar, bu virüsler eklenen muhabiri geni silmek için bir eğilim var, özellikle de, aynı olmayabilir çünkü diğer uygulamalar (mutasyon sıklığı belirlenmesi gibi) kullanılabilir olmamalıdır.
6. Ölçü mutasyon frekansları
Bu tespit polimeraz mutasyon mutajen değiştirir çoğaltma sadakat direnç göstermesini sağlayan doğrulayan önemli bir adım. Burada ölçülen mutasyon frekansları mutasyon oranları olduğunu not etmek önemlidir. Oranları, çoğaltma kinetiği çok dikkatli ölçümü (sentezlenen RNA miktarını ve çoğaltma döngüsü uzunluğu) belirlemek için, ancak mutasyon frekansları Ölçüm in çarpanlarına olmalıdır sürece geçişi tarih ve çoğaltma kinetiği izlenir, çoğaltma tekrarlanabilir, kantitatif önlemleri sağlar. sadakat. Mutasyon frekansları canlı virüs ya da nüfus (plak klonlar veya sınırlayıcı seyreltme) veya toplam virüs nüfus (virüs hisse senedi veya süpernatant) tespit edilebilir. Mutasyon frekansları belirlemek için, daha sonraki bir geçiş (örneğin geçit 2 veya sonrası) virüs stokları hazırlamak. Virüs nüfusunun yakın bir mutasyon seçim dengeleri genetik çeşitliliğini genişletmek için zaman geçtiğinden çok önemlidir.
- Canlı virüs nüfusun Mutasyon frekansları
Bu yaklaşım, daha zahmetli olsa da, çoğaltma yeterlik tutar ortalama genom üzerinde kaç mutasyonlar hakkında bilgi verir. Yüksek fitness varyantlar için bir önyargı oluşacağını, ancak dikkat edilmelidir ve alt fitness, canlı varyantları kolayca plak, örneğin, tespit olmayabilir yok yani. Gibi, aynı zamanda eşanlamlı daha iyi önlemler (dS) ve pozitif seçim nüfus üzerinde etkili olup olmadığını araştırmak için kullanılabilir olmayan eşanlamlı (DN) nükleotid değiştirmelerin izin verir. Ancak, daha az mutasyonlar sayısal olacağından, daha büyük bir sayı dizilerinin istatistiksel analizi için gerekli olacak. Bu teknik, yukarıda açıklandığı gibi, plak arıtma veya sınırlayıcı seyreltme ya da bireysel virüs izolasyonu dayanmaktadır. Bir başlangıç noktası olarak, biz vahşi tip virüs ve mutajen dayanıklı varyant 48 bireysel "klonlar" izolasyonu önerilir. Bu şekilde izole Her klonal nüfus kurucusu genom sunulan ne olursa olsun mutasyonu taşıması bekleniyor. RNA miktar izole plak mevcut veya seyreltme sınırlayıcı RT-PCR ile amplifikasyonu için genellikle yeterli olur. Gerekirse, en az bir hücre sayısı (örneğin 24 plaka biçimi) hakkında kısa bir amplifikasyon (az bir çoğaltma döngüsü) daha fazla RNA elde etmek için kullanılır, ancak, en az amplifikasyon yeni mutasyonların birikmesi yapılmalıdır. Karşılaştırılan her klon ve nüfus çoğaltma döngüleri aynı sayıda geçmesi gerektiğini unutmayın.- Plak arıtma veya sınırlayıcı seyreltme tarafından 24 - 48 virüs klonlar izole edin.
- Izole klonal nüfus RNA Özü
- RT-PCR, her numune için 3KB örtbas bir parça yükseltmek. Yapısal olmayan genlerin daha fazla korunmuş bölgelere oranla daha uygun mutasyon tolere etme eğilimindedir yapısal protein bölge, karşılamak için en iyisidir.
- PCR ürünleri, sekans arındırmak ve mutasyon analizi (bölüm 7) gerçekleştirmek.
- Toplam virüs nüfusun Mutasyon frekansları
Bu ikinci yöntem bir avantaj olmasına rağmen formsuz çeşitleri bile, mutasyonlar spektrumunun daha geniş bir resim izin sıralama dahil olacak. Ancak, canlı virüs popülasyonları (örneğin DN / DS değerleri) ve en alakalı mutasyonların belirlenmesi varsayıyorum filogenetik analizler için ideal olmayabilir beri ölümcül değişiklikleri bütünüyle tespit edilemeyen (RNA yapısı, stop kodon, dramatik amino asit değişiklikleri değiştirilmiş) ve analiz saklanır. Bununla birlikte, bu teknik in vitro biyokimyasal tahlil eksikliği olduğu zaman sadakat değişiklik onaylamak için en istatistiksel olarak anlamlı veriler elde etmek için araştırmacı izin verir. Bu teknik, düşük-fitness veya plaklar üretmek değil ölümcül mutasyonlar genomların dahil olmak üzere toplam virion RNA, RT-PCR dayanmaktadır. Bu yöntem ile elde edilen mutasyon frekansları plak veya seyreltme klonlama sınırlayıcı tarafından daha 10 kat daha yüksek olabilir.- Toplam virion nüfus RNA Özü
- RT-PCR kuvvetlendiricilerify genomik kodlama dizisi, mutasyonlar tahammül ve genetik varyans (örneğin yapısal proteinleri) bilinen bir parçası 800 1200 nükleotid bölge. Büyük parçaları, TopoTA klonlama vektörleri içine kolayca eklemek ve transformants yetersiz sayıda üretecek. Küçük parçaları bile daha iyi olmasına rağmen, genom dizisi kapsama istatistiksel anlamlılık elde etmek için çok az olabilir. En az 800 baz puan (bp) bir parçası, iki primer dizisi kapsama izin verir ve iyi dizisi kapsama alanı maksimum düzeye çıkarmak ve sıralama maliyetleri en aza indirmek arasında bir uzlaşmadır. Biz 800 nükleotid bir bölgeyi kapsayan 70 ile 100 dizileri tekrarlanabilir laboratuvarda inceledik varyantları değişen sadakat teyit bulabilirsiniz. Eşit verimliliği ile diğer vektör / klonlama yöntemleri kullanılabilir unutmayın.
- RT-PCR ürünü, ticari bir kit veya standart DNA ekstraksiyonu / yağış kullanarak arındırın.
- Kullandığınız RT-PCR enzimler çıkıntılar vermezse, 1 mcM ATP ve Taq polimeraz ekleyerek 10 dakikalık bir uzatma gerçekleştirmek
- TopoTA klon aşağıdaki üreticinin talimatlarına
- Her virüs nüfus incelenecektir için, mavi / beyaz tarama XGal kaplı plakalar üzerinde olumlu bir ekleme sahip olarak tanımlanan 96 koloniler seçin. Başlangıçta, mavi / beyaz tarama agaroz jel veya tek koloni PCR plazmid boyutu tarama ile teyit etmek, klonlanmış her biri farklı genom bölgesi için ekler varlığı test edin. Parçanın boyut ve yukarıdaki koşullara kullanarak,% 90 pozitif elde
- 96 iyi bakteri kültürü plakalar LB orta 1 ml sıvı suyu gecede her koloninin büyütün
- Ertesi gün, 96-well formatında minipreps hazırlar.
- Sıra her klonlanmış segmentinin maksimum kapsama alanı elde etmek için yeterli primerler (örneğin RT-PCR için kullanılan astar, ya da TopoTA M13 primerler) plakası. Mutasyon analizi (bölüm 7) gerçekleştirin.
7. Sekans analizi
Her nüfus ve uygun bir uyum yazılımı için bir referans veya fikir birliği dizisi dizisi analizleri kullanarak gerçekleştirin. Biz Lasergene veya kolayca fikir birliğine göre SNP tespit Sequencher tavsiye ediyoruz.
- Uygun yazılım kullanarak (örneğin Lasergene veya Sequencher) dizileri hizalayın.
- Kalitesiz dizileri (kötü tabanı arama, çok sayıda 'N veya uzunluğu çok kısa) atın. Tüm sıraları ile kaplıdır nükleotid aralığı belirleyin. Genomun farklı bölgelerinde daha fazla veya daha az mutasyonlar tahammül yılından bu yana, karşılaştırma nedenlerden dolayı aynı bölgede tam analiz için tutulan her sıralı klon için kapalı olması gereklidir. Böylece, birkaç dizisi reaksiyonlar klon başına ve bir sıra belirli bir klonu başarısız olup olmadığını analiz klon (tüm dizileri) atın.
- Belirlenmesi ve referans suşu farklı SNP saymak.
- (Bölge sıralı klonlar x uzunluk sayısı) sıralı nükleotidler toplam sayısına göre belirlenen SNP toplam sayısına bölünmesi ile mutasyon sıklığı hesaplayın. 10K nt sıralı başına ortalama mutasyonlar nükleotid ortalama olarak bırakarak daha kullanıcı dostu bir numara vermektedir olarak bu sayı sunmak. Örneğin, Tablo 1, 55 vahşi tip nüfus için mutations/121, 978 toplam nükleotidler X 10.000 = 10.000 nükleotidler başına 4.51 mutasyonlar sıralı.
- Aynı SNP klonları çok sayıda belirirse, bu tekrarlanan mutasyonlar veya dışarıda iki değer sunuyoruz. Genel olarak, homojen bir üst (plak arıtma veya bulaşıcı bir klon) üretilen ve sadece bir kaç kez hücre kültürü geçişli bir virüs nüfus için, pozitif seleksiyon, aynı SNP birikimi ve mutasyonun neden etkileri yeterince sarf değil frekans değerleri bu şekilde daha iyi, olumlu ya da temizleyici seçim minimal etkisi ile polimeraz hata sıklığını yansıtacak ölçülür.
- Mutasyon dağılımının belirlenmesi. Her nüfus klon sayısı bir sırada listesini Varolan 0, 1, 2, 3, vb olun .. bölgedeki mutasyonlar sıralı.
- Ikili mesafe karşılaştırma viral nüfus çeşitliliği hesaplayın. Itibaren temizlenmiş ve manüel olarak düzeltildiğinde dizileri referans bölge de dahil olmak üzere bir hizalama hazırlar. ClustalW / X (: çeşitli hizalama programları vardır http://www.clustal.org/ ), kas ( http://www.drive5.com/muscle/ Mac kullanıcıları için), EbioX ( http://www. ebioinformatics.org / ebiox / ) vb tüm dizileri emin olun, gerekirse bitki aynı uzunlukta olduğundan emin olun. Dizilerin başlangıç arka analizi kolaylaştırmak için bir kodlama kodon olması tavsiye edilir. Fasta biçimi, kolayca kullanılabilir çoğu yazılım tarafından okunan tüm hizalanmalar tutmak öneririz.
- ikili mesafe analizi gerçekleştirmek için, aynı nüfusa ait dizileri arasında mümkün olan tüm ikili karşılaştırmalar hesaplamak. Karşılaştırmalar bulundu Ortalama mutasyonlar sonra nüfus heterojenite göstermek için hesaplanabilir.
- Eşanlamlı (dS) ve nüfus içinde (DN) olmayan eş anlamlı değerler kolayca elde edilebilir. Biz MEGA yazılım (http://www.megasoftware.net/) faydalı ve bu tür bir analiz için kullanıcı dostu bulmak.
- Mümkün olan sadece onlar olmasa da seçim yönde elde etmek için iki ihtimal vermek. 1) dN ve dS arasındaki oran alın. 1'den daha yüksek değerler olumlu bir seçim anlamına gelir. 1'den daha düşük değerler arındırıcı seçim anlamına gelir. 2) Datamonkey web sunucusu ( http://www.datamonkey.org/ kullanın ). Fasta formatında hizalanmalar SLAC modülü ile yükleyin ve bunları analiz. Bu DN / DS bir tahmin verecektir.
- Istatistiksel analizler gerçekleştirin. Veri ve sıra sayısı miktarına bağlı olarak, çeşitli testler kullanılabilir. Bazı çalışmalar, tüm klonlar 9 birleştirilir konsensüs nükleotidlerin toplam sayısı karşısında mutasyonların toplam sayısı ki kare testleri yararlanmıştır . Diğer çalışmalar, Fisher exact testleri mutasyonlar olmadan dizilerinin sayısı karşısında mutasyonlar sunan 10 dizilerinin sayısı üzerinden hesaplanan var. Yeterince mutasyon veri üretilmesi ise, biz her RNA sıralı mutasyonların sayısı her virüs nüfus sayısı klonlar rütbe, Bunu yapmak için, Mann Whitney U olarak sıralanır sum testi yapılması önerilir. Nüfus mutasyon dağılımı farklılıklar için Mann Whitney sonra test edecek. Bu nedenle, birden fazla mutasyonları ile klonlar bulma olasılığını artırmak için, en az 800 baz çiftinden sıralama önermektedir. Bu test, sağlam, ancak daha büyük örneklem büyüklüğü gerektirir. Öte yandan, karşılaştırılan iki popülasyon için aynı örneklem büyüklüğü gerektirmez (örneğin, Tablo 1 örnekleri n 1 = 148 ve n 2 = 84).
8. Temsilcisi sonuçları:
Hücre canlılığı ve virüs canlılığı mutajen konsantrasyonu doza bağımlı etkisi Bu örnekte, 100 mcM AZC virüs geçişi, hedeflenen 10,5-2 günlük virüs titresi azalmış bulundu. Şekil 1'de gösterildiği gibi, ama HeLa hücre canlılığı virüs enfeksiyonu için gerekli olan 2 gün boyunca olumsuz etkiledi. Seri virüs geçişi için 100 mcM AZC konsantrasyon seçim liderliğindeki Bu pilot deneyi, mutajen direnci için seçin. Şekil 2 mutajen direnç fenotipi ortaya çıkması ardından titresi ilk azalma göstermektedir. Mutajen ilk birkaç geçişleri sırasında, ölümcül mutasyonlar birikir olarak, virüs titreleri önemli bir düşüş meydana gelir. Yavaş yavaş, mutajen dayanıklı varyant bir ortaya çıkması tedavi edilmemiş kontrol farklı virüs titreleri bir dönüş ile çakışmaktadır ortaya çıkar. Bu aşamada, virüs nüfusun büyük bir yüzdesini direnci mutasyon sunuyor. Bu virüs nüfus Sıralama amino asit değişikliği (ler) sorumludur ortaya koymaktadır. Bir kez tanımlanır ve izole veya yeni oluşturulan, mutajen dirençli virüs farklı RNA mutagenler vahşi tip (farklı yapısı baz analogları, örneğin) daha az hassas olabilir. Şekil 3, daha yüksek titreleri bir RNA mutajen dirençli Coxsackie virüsü B3 gösterir ribavirin, 5-fluorourasil ve 5-azacytidine ve yüksek MgCl 2 ve MnCl 2 varlığı vahşi tip. RNA mutagenler geniş direnci artan çoğaltma aslına güçlü bir göstergesi. Mutasyon frekanslarının karşılaştırılması yardımcı olacak sadakat varyant çoğaltma kinetiği doğrulanıyor vahşi tip virüse benzer. Şekil 4 vahşi tip göre yüksek sadakat varyantın bir adım büyüme kinetiği göstermektedir. Çoğaltma oranları ve nihai titreleri benzer değilse, o adımları çoğaltma aynı sayıda mermi geçiren virüs nüfus, benzer büyüklükte karşılaştırmak için alınan olmalıdır. RNA sentezi oranı ve çoğaltma sadakat arasındaki bağlantıyı, özellikle de in vivo olarak karakterize değildir. Şekil 4'te gösterildiği gibi, bu mutlak bir kural olmasa da yavaş bir çoğaltma oranı, bir azalma mutasyon frekansı (yüksek sadakat) neden olabilir. Yukarıdaki parametreler kurulan ile sadakat varyant ve vahşi tip popülasyonları mutasyon frekansları değişmiş çoğaltma aslına genetik onay almak için karşılaştırılabilir. Nokta mutasyonları tespit Şekil 5, vahşi bir türü ve yüksek sadakat varyant bir dizi hizalama gösterir. 10.000 nükleotidler, Şekil 6 sıralı ortalama mutasyonlar sayılır, klon başına mutasyon (Tablo 1) sayısına göre sıralanır ve nüfus başına ortalama mutasyon sıklığı olarak gösterilir.

Şekil 1. RNA mutajen direnci seçmek için en uygun koşulların belirlenmesi: ılımlı bir (virüs titresi 1-2 günlük düşüş) HeLa hücrelerinde yüksek hücre canlılığı saklama belirtilen konsantrasyonlarda ribavirin ile tedavi edilen ve bir İçişleri Bakanlığı vahşi tip Coxsackie virüsü B3 ile enfekte olmuş 0.01. 48 saat post enfeksiyon, döl virüsü hasat ve TCID 50 titreleri belirlendi. Tripan mavi boyama tarafından belirlenen 48 saatte tedavi hayatta kalan hücrelerin yüzdesi, x-ekseni altında gösterilir. Sonuçlar 100 konsantrasyonları ve 200 mcM hücre canlılığı etkilemeden, 1-2 günlük virüs titreleri azalttığını göstermektedir.
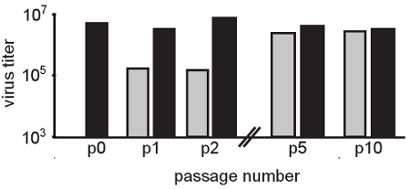
Şekil 2. RNA mutagenler orta yoğunlukta varlığı Seri geçiş mutajen dirençli toplumlar için seçer bu rakam, 50 mcM ribavirin (gri bar) varlığı Chikungunya virüsü HeLa hücrelerinde geçişli. Kontrol pasajlar ribavirin yokluğu (siyah çubuklar) yapıldı. Her metreyi bulan geçitten sonra, virüs döl BHK hücreleri üzerinde klasik plak yöntemi ile belirlendi. Mutajenik etkisi ilk geçişleri sırasında açıktır (p0 başlayan nüfus ile karşılaştırıldığında p1 ve p2) tarafından 2 günlük tedavi virüs titreleri bırak. Yavaş yavaş, titreleri normal (işlenmemiş) düzeyleri dönmek. Dirençli varyantları seçilmiştir düşündüren, tedavi edilmezse ile karşılaştırıldığında geçit 5 mutajen tedavi popülasyonları anlamlı bir fark görülmektedir. Gerçekten de, nüfusun konsensus sıralama ribavirin tedavisi gören virüs nüfus benzersiz mutasyonları tespit.
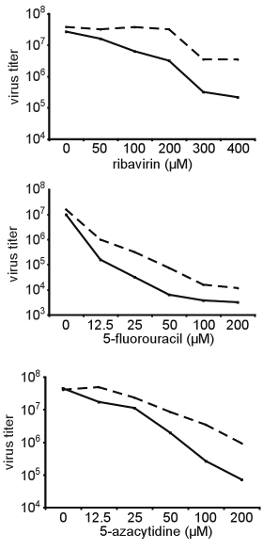
Şekil 3. Farklı bir yapıya mutajenler RNA geniş direnç Onay Burada gösterilen, başlangıçta, 3. bölümde de tarif ekran izole Coxsackie virüsü B3 yüksek sadakat A372V varyant bulaşıcı bir klon üretilen ve farklı konsantrasyonları bağıl duyarlılık test farklı RNA mutagenler (ribavirin, 5-fluorourasil, 5-azacytidine). HeLa hücrelerinde belirtilen konsantrasyonlarda ribavirin ile tedavi edilen ve 0.01 bir İçişleri Bakanlığı vahşi tip Coxsackie virüsü B3 ile enfekte edildi. 48 saat post enfeksiyon, döl virüsü hasat ve TCID 50 titreleri belirlendi. Vahşi tip (düz çizgiler) ve mutajen konsantrasyonunun bir fonksiyonu olarak A372V varyant (kesik çizgiler) titreleri burada gösterilir. A372V sürekli test edilen tüm koşullar altında vahşi tip daha yüksek titreleri.
Şekil 4. Çoğaltma oranları ve sadakat varyantları virüs üretiminin bir adım büyüme kinetiği belirlemek için, HeLa hücreleri (düz çizgi) ya da vahşi tip, yüksek sadakat varyant A372V (uzun tire) veya çoğaltma eksik varyant Cx64 (kısa ile İçişleri Bakanlığı = 10 enfekte olmuş Coxsackie virüsü B3 tire). Zaman noktalarında virüs döl hücreleri ve donma-çözülme süpernatantlar hasat ve TCID 50 oranında titre, belirtilir. A372V sadakat artış gözlemlenebilir bir çoğaltma kusur doku kültürü ile örtüşmemektedir. Varyant Cx64 çoğaltma kinetiği önemli bir gecikme sunuyor ve vahşi tip virüs göre 1000 kat daha düşük olan maksimum titreleri ulaşır.
Şekil 5. Her virüs nüfus TopoTA klonlanmış dizileri Hizalama Bölüm 7, klonlanmış RT-PCR ürünü elde edilen her dizisi açıklanan yaklaşımı kullanarak tahminen toplam virüs nüfus içinde bir tek, eşsiz bir genom kaynaklanan ve böylece benzersiz mutasyonlar taşıyacak . Bu rakam, düşük kaliteli dizileri ve SNP görselleştirme temiz takip, tipik bir uyum gösterir. Toplam nüfus içinde SNP (bu rakam 10) sayılır ve her klon görünen SNP sayısı belirtilmiştir. 8 diğer klonlar, benzersiz, tek bir mutasyon ise Örneğin, bir bar altı çizili klon, 2 benzersiz mutasyonlar içerir. Bu veriler Tablo 1 derlemek için kullanılır. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayınız .
Şekil 6. Grafik gösterimi, virüsün popülasyonlarının mutasyon frekanslarının daha kolay yorumlanması için, sırası ve istatistiksel analizler elde edilen sayısal veri ya grafik veya histogramı (burada görüldüğü gibi) olarak temsil edilebilir . A372V virüs daha az vahşi tip mutasyonların üretir ve anlamlı olarak daha düşük bir mutasyon frekansı (* p <0.01) sunar. Titreleri için vahşi tip, pres göre 1000 kat daha çoğaltır Cx64 varyant,çoğaltma hız ve sadakat mutlaka bağlantılı değildir belirten aynı mutasyon sıklığı (NS, anlamlı değil) veliler. Aynı Chikungunya virüsü (CHIKV) popülasyonuyla virüs stoku konusunda benzer bir mutasyon frekansları verir, ya da 10 5 kat seyreltme, RNA ekstraksiyonu için kullanılır .
Istatistiksel analiz için Mutasyon dağıtım özeti.
Not: Her klon, aynı genomik bölge (ve sırası uzunluğu) kapalı olması gereklidir. Bu durumda, ortalama 859 nükleotidler klon. Bu istatistiksel analizler için kritik öneme sahiptir. Öte yandan, rank sum testi istatistiksel analiz için kullanılan örnek boyutları aynı olması gerekmez, araştırmacı örneklem büyüklüğü farklı nüfus karşılaştırmak için ücretsizdir. Bu nedenle, vahşi tip 142 klonları A372V 84 klonları ile mukayese edilebilir.
| N mutasyonlar # klonlar | vahşi tip | A372V |
| 7 mutasyonlar | 0 | 0 |
| 6 mutasyonlar | 0 | 0 |
| 5 mutasyonlar | 0 | 0 |
| 4 mutasyonlar | 0 | 0 |
| 3 mutasyonu | 1 | 0 |
| 2 mutasyonlar | 6 | 2 |
| 1 mutasyonlar | 40 | 14 |
| 0 mutasyonlar | 95 | 68 |
| Toplam mutasyonlar | 55 | 18 |
| Toplam klonlar sıralı | 142 | 84 |
| Toplam nükleotidler sıralı | 121.978 | 72.156 |
| Mutations/10 4 nt | 4,51 | 2,49 |
Tablo 1. Istatistiksel analiz için Mutasyon dağıtım özeti Not: Her klon, aynı genomik bölge (ve sırası uzunluğu) kapalı olması gereklidir. Bu durumda, ortalama 859 nükleotidler klon. Bu istatistiksel analizler için kritik öneme sahiptir. Öte yandan, rank sum testi istatistiksel analiz için kullanılan örnek boyutları aynı olması gerekmez, araştırmacı örneklem büyüklüğü farklı nüfus karşılaştırmak için ücretsizdir. Bu nedenle, vahşi tip 142 klonları A372V 84 klonları ile mukayese edilebilir.
Tartışmalar
Hücre hattı seçimi. RNA mutajenler olarak baz analogları etkinliği farklı hücre tipleri tarafından 11 bağıl alımı ile ilişkilidir. Normal virüs geçişi için kullanılan hücre hattı alımı ya da çok hassas (yüksek hücre toksisite) mutajen dirençli bulunduğu kanıtlanırsa, bu gereksinimleri karşılar ve hala viral replikasyon için izin veren başka bir hücre hattı kullanmak için gerekli olabilir. Mutajen direnç varyantı izole sonra, karakterizasyonu kalan orijinal, tercih edilen bir hücre hattı yapılabilir. Deneyimlerimize göre, HeLa hücrelerinde kolaylıkla mutajen kadar sürebilir; BHK hücreleri mutajen alımı refrakter 10 kat daha yüksek konsantrasyonlarda ve Vero hücreleri gerektirir.
Mutajen fazla bir tür kullanılır mutajen. Seçimi mutajen tedavi, başarı olasılığını sadakat varyantları izole etmeye çalışan artar. Yanlışlıkla çoğaltma sırasında genomların dahil farklı yapısı, Temel analog mutajenler mutasyonların sonraki çoğaltma döngüsü içinde belirli bir alt grubunda ağırlıklı olarak sonuçlara sebep: ribavirin tedavisi GtoA ve CtoU geçiş mutasyonlar 12 yanadır; 5-azacytidine benzer bir önyargı vardır, CtoG ve GtoC transversions 13 Ayrıca; 5-fluorourasil tercihen Atog ve UtoC geçişler (14) neden olur. Alternatif olarak, daha yüksek konsantrasyonlarda Mg 2 + veya Mn 2 + 12 yukarıda açıklanan önyargısız RNA virüsleri genel mutasyon sıklığını artırmak için orta takviye olabilir. Virüs kodon dizileri bağlı olarak, ve bir vefa varyant üretmek için gerekli kodon değişiklikleri, bu şartlar bazı diğerleri üzerinde bu varyantın ortaya çıkması tercih edecektir. Kodon yerinde gerekli Atog geçiş ağırlıklı olarak bu ribavirin tarafından oluşturulan mutasyonlar denk çünkü yüksek sadakat poliovirus G64S ve Coxsackie virüsü A372V için, ribavirin tedavisi en kolay varyantları için seçilir.
İçişleri Bakanlığı vs nüfus büyüklüğü viroloji, doku kültürü enfeksiyon için protokoller, arızalı müdahale parçacıklar (düşük İçişleri Bakanlığı) (yüksek İçişleri Bakanlığı) birikmesi veya virüsler arasında rekombinasyon teşvik etmek, enfeksiyon (İçişleri Bakanlığı) çokluğu özellikle dikkat örnek. Pasajlanması seri üzerinde ortaya çıkması olayları seçmek için, virüs nüfus büyüklüğü dikkate almak da önemlidir. Dirençli mutant başlangıçta düşük frekans var, her geçişte ortaya çıkan bu değişik kaybetmemek için bir sonraki (10 5 -10 6 virüsler, gibi) bir geçit gibi büyük bir nüfus büyüklüğü mümkün olduğunca aktarmak en iyisidir. Ölçekleme kadar iyi veya balonun büyüklüğü (enfekte olan hücreleri sayısı), İçişleri Bakanlığı olarak bu endişe ise artışını en aza indirmek için yardımcı olabilir. Öte yandan, deneyler, mutajen bir virüs duyarlılığı test olduğu için, düşük İçişleri Bakanlığı enfeksiyonu ile daha yüksek bir fitness genomların Deneyde ortaya çıkan çoğaltma döngülerinin sayısını artırmak ve mutagenized genomların kurtarma önlemek için yapılır ko-enfekte olan hücreleri tamamlama. Çoğaltma ilk turda döl genomları üzerinde oluşturulan mutasyonlar hemen tespit edilemez çünkü bu önemlidir. Bu mutagenized RNA'lar çoğu hala virion içine paketlenmiş olacak. Bu enfeksiyon sonraki turda iptal çoğaltma döngüsü bu genomlarındaki ölümcül mutasyonlar sonucu, ve virüs titresi azalma olacağını. Bu ölümcül mutagenez önemli bir etkisi gözlenen mutasyonların birikimi birkaç tur için önce izin için gerekli olabilir. Son olarak, mutajen varlığı geçiş serisi üzerinde virüs titreleri nesli kadar düşmesi devam ederse, daha sonra araştırmacı, mutajen (çok düşük konsantrasyonda başlayarak) giderek artan miktarlarda virüs Pasajlanması denemelisiniz.
İzolasyon ve RNA mutajen dayanıklı nüfus RNA mutajen dirençli klon nesil. RNA mutajenler her genom birden fazla rastlantısal mutasyonlar tanıtmak, ancak direnç için seçim direnci mutasyon sadece zenginleştirmek (ve düzeltmek için konsensüs dizisi) . Bu mutasyon belirlemek için, sırası mutajen dayanıklı nüfus (nüfusun uzlaşma) ve bireysel virüsler değil. Bu nedenle, mutajen tarafından oluşturulan tek, rastlantısal mutasyonlar sırayla tespit değildir, sadece seçimi aşağıdaki fikir birliği değişiklikler sonucu bulundu mutasyonlar. Deneyimlerimiz bize, sadece bir ya da iki Böyle bir fikir birliğine dizisi değişiklikleri belirlemek. Mutajen dayanıklı nüfus elde edilir ve direnci mutasyon tespit edildikten sonra, bu varyant daha saf bir stok oluşturmak için gereklidir. Yukarıda, bir plaket arıtma prosedürü nitelendirdi. Alternatif olarak, faiz virüs kolayca tanımlanabilir plaklar vermezse, istediğiniz şekli purif olabilirseyreltme sınırlayarak IED. Bu yaklaşım, aslında bir virüs stokunun% 50 daha az kuyu enfekte olduğu gibi seyreltilmiş 96-kuyu biçiminde TCID 50 . Bu seyreltme yukarıdaki gibi aynı yaklaşımı kullanarak, 10 özel türevleri kadar tecrit ve dizileri teyit alınır. Belirtildiği gibi, en iyi durumlarda, bulaşıcı bir virüs suşu cDNA klonu kullanılabilir. Varyant izolasyonu böylece gerekli olmayacaktır. Deneyimlerimize göre, sadakat varyantları tek bir amino asit değiştirmelerin sonucudur ve böylece Quikchange (Agilent) gibi basit, ticarileştirilmiş mutagenez kitleri kullanılarak oluşturulabilir. İkinci seçenek yakından ilgili bir zorlanma cDNA klonu kullanmak. Ancak, ilgili suşu kullanıldığı takdirde, biz yakından ilişkili iki virüsler aynı netlikte değiştiren mutasyon mutlaka aynı etkiye sahip olmayacaktır, çünkü bu yaklaşım ve virüs izolasyonu (örneğin plak arıtma) hem kullanarak öneririz.
Sadakat ve RNA mutajen dirençli varyantları çoğaltma Seçim vahşi tip meslektaşları 4,12,15 benzer büyüme özellikleri ile hem daha yüksek ve daha düşük bir sadakat varyantları izolasyonu sonuçlandı . Şu anda, polimeraz aktivitesi oranları ve sadakat arasındaki bağlantı tam olarak anlaşılmış değildir. Düşük sadakat türevleri, daha hızlı işleme 1-3,12 eğiliminde iken, in vitro saflaştırılmış RNA polimeraz kullanarak biyokimyasal çalışmalar, yüksek sadakat varyantları yavaş işleme oranlarına sahip olduğunu göstermiştir . Doku kültürü, bu farklılıklar, hız sınırlayıcı adım, bu kaynakların kullanılabilirliğini ziyade içsel polimeraz aktivitesi kinetiği düşündürmektedir, genellikle belli değildir. Sadakat varyant vahşi tip önemli ölçüde farklı değildir kinetiği çoğaltır, daha sonra kendi mutasyon frekanslarının bir karşılaştırma doğrudan yapılabilir. Çoğaltma kinetiği çok önemli bir değişiklik varsa, daha sonra veri çoğaltma döngüleri aynı sayıda geçirmiş virüsler karşılaştırarak örneğin kinetik farklılıklar hesaba normalize edilmelidir. Bizim tecrübelerimize göre bir adım büyüme kinetiği yabani türü ve yüksek sadakat varyantları arasında anlamlı bir fark gözlendi rağmen, (içinde yüksek sadakat türevleri sürekli vahşi tip göre (1 günlüğüne içinde) yüksek titrede gözlenen ama onlar biraz daha az RNA yapmak aynı büyüklük sırası), ayrıca ürettikleri genomların daha az mutasyonlar içeren ve daha bulaşıcı, böylece olduğunu düşündürmektedir.
Örnek hazırlama ve sıralama bu protokoller tüm adımlar için, biyolojik ilgili mutasyonlar ayırt edilemez yılından bu yana yüksek sadakat, redaksiyon enzimleri ek mutasyonlar tanıtarak sınırlamak için PCR ve RT-PCR için kullanılan zorunludur. Karşılaştırılan virüs popülasyonları yeterli başlangıç materyal olduğundan emin olmak için de önemlidir (geçit geçmişi, doku kültür ortamı, sıcaklık, RNA ekstraksiyon yöntemi, RT-PCR protokolleri, vb) aynı şartlarda hazırlanmış olması kritik RT-PCR ile güçlü bir grup oluşturulur böyle RNA ekstraksiyonu aldı. 1 / 100 dilüsyon RNA örnek bir örnek yeterli sayıda temsil yanlılığı önlemek için (aynı genomunun tekrar tekrar yükseltme) RNA molekülleri içerdiğini belirten saptanabilir RT-PCR bant vermelidir. Mutasyon sıklığı bir dağıtım olduğundan, bir benzer değerlere nüfus büyüklüğü ne olursa olsun söz konusu önyargı meydana değildir sağlanan elde edilebilir olacağı beklenebilir. Şekil 6'da görüldüğü gibi, bir virüs stokunun 10 5 kat seyreltme ebeveyn stok önemli ölçüde farklı bir mutasyon sıklığı verir.
TopoTA klonlama için en uygun koşulları bulununcaya kadar, sıralama önce koloni PCR ile mavi / beyaz tarama sonra ekler varlığını doğrulamak. Mutasyon gürültü (RT-PCR ve sıralama tarafından tanıtılan mutasyonların) için bir kontrol olarak (in vitro transkripsiyonu RNA virüs genomuna ait bir plazmid taşıyan aynı viral dizisi ve / veya klon ve sırası RT-PCR ürünleri PCR ürünü klonu in vitro transkripsiyon enzimler farklı farkında) farklı hata oranlarına sahip ve gerçek arka plan hata yordamı yararlı bilgi vermeyebilir. Bazı virüs dizileri, bakteri için zehirli olabilir, bu yüzden bu mutasyon sıklığı viral genom dizilimini bölgeye karar vermeden önce doğrulamak için önemlidir. TopoTA elde dizileri analiz, her klon sadece bir ekleme / sıralama içermesi gerektiğini unutmayın. Karışık bir nüfus düşündüren bir çift tepe görülürse, bu iki komşu bakteri kolonilerinin olduğunu mümkündür. Mutasyon son derece olası bakteri kültürü plazmid amplifikasyon sırasında olduğunu, bakteri çoğaltma düşük mutasyon frekansları verilen rağmen, aynı zamanda mümkündür. Plak ppopülasyonları urified, bir çift tepe yeni bir mutasyon satın almak ya da plak gelişimi sırasında bir mutasyon dönüyor üst üste plaklar ya da bir virüs temsil edebilir. Tutarlı olun ve saymak veya bu mutasyonlar saymak karar.
Son olarak, burada kullanılan mutasyon frekanslar göreli değerleri olduğunu unutmayın. Onlar sadece, aynı koşul altında yetiştirilen virüs popülasyonları karşılaştırarak geçerli ve aynı bölge üzerinde sıralı! Bunlar mutasyon oranı, ya da bir bütün olarak genom mutasyon sıklığı mutlak değer olarak alınmamalıdır. Ancak, şartlar kontrol edilir, onlar mutasyon dağıtım ve frekans farklılıkları tekrarlanabilir, kantitatif karşılaştırmalar izin veren.
Açıklamalar
Teşekkürler
Bu çalışma, Paris Şehir, hiçbir Fransız Ulusal hibe ANR-09-JCJC-0118-1 ve ERC Starting Grant RNAvirusPopDivNVax Proje Tıp ve Sağlık Araştırma hibe fon tarafından desteklenmiştir. 242.719.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Reaktifin Adı | Şirket | Katalog numarası | Yorumlar |
|---|---|---|---|
| Ribavirin | Sigma | R9644-10mg | |
| 5-fluorourasil | Sigma | F6627-1G | |
| 5-azacytidine | Sigma | A2385-100mg | |
| MgCl 2 | Sigma | M1028 = On Olunca-100ML | |
| MnCl 2 | Sigma | M1787 | |
| Tripan mavi | Sigma | T8154-20ml | |
| TopoTA klonlama kiti | Invitrogen | 10351021 | |
| Quikchange mutasyon kiti | Agilent | 200516 | CDNA bulaşıcı bir klon varsa |
| 96-iyi miniprep kiti | Macherey'nin-NAGEL | 740625 | |
| Lasergene, Sequencher | DNAstar, Gen Kodları Corporation'ın | www.dnastar.com www.genecodes.com | Veya diğer hizalama yazılımı |
Referanslar
- Arias, A. Determinants of RNA-dependent RNA polymerase (in)fidelity revealed by kinetic analysis of the polymerase encoded by a foot-and-mouth disease virus mutant with reduced sensitivity to ribavirin. J Virol. 82, 12346-12355 (2008).
- Arnold, J. J., Vignuzzi, M., Stone, J. K., Andino, R., Cameron, C. E. Remote site control of an active site fidelity checkpoint in a viral RNA-dependent RNA polymerase. J Biol Chem. 280, 25706-25716 (2005).
- Korneeva, V. S., Cameron, C. E. Structure-function relationships of the viral RNA-dependent RNA polymerase: fidelity, replication speed, and initiation mechanism determined by a residue in the ribose-binding pocket. J Biol Chem. 282, 16135-16145 (2007).
- Pfeiffer, J. K., Kirkegaard, K. A single mutation in poliovirus RNA-dependent RNA polymerase confers resistance to mutagenic nucleotide analogs via increased fidelity. Proc Natl Acad Sci U S A. 100, 7289-7294 (2003).
- Pfeiffer, J. K., Kirkegaard, K. Increased fidelity reduces poliovirus fitness and virulence under selective pressure in mice. PLoS Pathog. 1, e11-e11 (2005).
- Vignuzzi, M., Stone, J. K., Arnold, J. J., Cameron, C. E., Andino, R. Quasispecies diversity determines pathogenesis through cooperative interactions in a viral population. Nature. 439, 344-348 (2006).
- Vignuzzi, M., Wendt, E., Andino, R. Engineering attenuated virus vaccines by controlling replication fidelity. Nat Med. 14, 154-161 (2008).
- Crotty, S., Cameron, C., Andino, R. Ribavirin's antiviral mechanism of action: lethal mutagenesis. J Mol Med. 80, 86-95 (2002).
- Coffey, L. L., Vignuzzi, M. Host alternation of chikungunya virus increases fitness while restricting population diversity and adaptability to novel selective pressures. J Virol. 85, 1025-1035 (2011).
- Ciota, A. T. Role of the mutant spectrum in adaptation and replication of West Nile virus. J Gen Virol. 88, 865-874 (2007).
- Ibarra, K. D., Pfeiffer, J. K. Reduced ribavirin antiviral efficacy via nucleoside transporter-mediated drug resistance. J Virol. 83, 4538-4547 (2009).
- Levi, L. I. Fidelity variants of RNA dependent RNA polymerases uncover an indirect, mutagenic activity of amiloride compounds. PLoS Pathog. 6, e1001163-e1001163 (2010).
- Sierra, S., Dávila, M., Lowenstein, P. R., Domingo, E. Response of foot-and-mouth disease virus to increased mutagenesis: influence of viral load and fitness in loss of infectivity. J Virol. 74, 8316-8323 (2000).
- Ruiz-Jarabo, C. M., Ly, C., Domingo, E., de la Torre, J. C. Lethal mutagenesis of the prototypic arenavirus lymphocytic choriomeningitis virus (LCMV). Virology. 308, 37-47 (2003).
- Sierra, M. Foot-and-mouth disease virus mutant with decreased sensitivity to ribavirin: implications for error catastrophe. J Virol. 81, 2012-2024 (2007).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır