Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Domateste Tohum Geliştirme Çalışması için Verimli Bir Takas Protokolü (Solanum lycopersicum L.)
Bu Makalede
Özet
Domates tohumu, bitki üremesi sırasında genetik ve gelişim biyolojisini incelemek için önemli bir modeldir. Bu protokol, daha ince embriyonik yapıyı gözlemlemek için farklı gelişim aşamalarında domates tohumlarının temizlenmesi için yararlıdır.
Özet
Domates (Solanum lycopersicum L.) dünya çapında en büyük nakit mahsullerinden biridir. Domates tohumu, bitki üremesi sırasında genetik ve gelişim biyolojisini incelemek için önemli bir modeldir. Bir domates tohumu içindeki daha ince embriyonik yapının görselleştirilmesi genellikle tohum kabuğu müsilajı, çok hücreli katmanlı bütünlük ve zahmetli gömme bölümleme ile çözülmesi gereken kalın duvarlı bir endosperm tarafından engellenir. Daha basit bir alternatif, kimyasal maddeler kullanarak tohumu neredeyse şeffaf hale getiren doku temizleme teknikleri kullanmaktır. Geleneksel temizleme prosedürleri, daha ince bir tohum kabuğuna sahip daha küçük tohumlara derinlemesine bilgi vermesine rağmen, domates tohumlarının temizlenmesi, özellikle geç gelişim aşamalarında, teknik olarak zor olmaya devam etmektedir.
Burada, embriyonik morfolojinin neredeyse tamamlandığı çiçeklenmeden 3 ila 23 gün sonra domates tohumu gelişimini gözlemlemek için hızlı ve emek tasarrufu sağlayan bir temizleme protokolü sunulmaktadır. Bu yöntem, Arabidopsis'te yaygın olarak kullanılan kloral hidrat bazlı temizleme çözeltisini, Formalin-Aseto-Alkol (FAA) fiksasyonunun ihmal edilmesi, tohumların sodyum hipoklorit muamelesinin eklenmesi, yumuşatılmış tohum kabuğu müsilajının çıkarılması ve yıkama ve vakum işlemi dahil olmak üzere diğer modifikasyonlarla birleştirir. Bu yöntem, domates tohumlarının farklı gelişim aşamalarında verimli bir şekilde temizlenmesi için uygulanabilir ve mutant tohumların gelişim sürecinin iyi mekansal çözünürlükle tam olarak izlenmesinde yararlıdır. Bu temizleme protokolü, Solanaceae'deki ticari olarak önemli diğer türlerin derin görüntülenmesine de uygulanabilir.
Giriş
Domates (S. lycopersicum L.), 2020 yılında 5,1 milyon hektardan 186,8 milyon ton etli meyve üretimi ile dünyadaki en önemli sebze mahsullerinden biridir1. Patlıcan, biber, patates ve tütün gibi ticari açıdan önemli birçok ürün de dahil olmak üzere yaklaşık 2.716 tür2 ile büyük Solanaceae familyasına aittir. Ekili domates, genom boyutu yaklaşık 900 Mb3 olan bir diploid türüdür (2n = 2x = 24). Uzun süredir, yabani Solanum spp'den arzu edilen özellikleri seçerek domates evcilleştirme ve ıslahına yönelik büyük çaba sarf edilmiştir. Domates Genetiği Kaynak Merkezi'nde listelenen 5.000'den fazla domates katılımı vardır ve dünya çapında 80.000'den fazla germplazma domates depolanmaktadır4. Domates bitkisi serada çok yıllıktır ve tohumlarla yayılır. Olgun bir domates tohumu üç ana bölmeden oluşur: tam yetişkin bir embriyo, artık hücresel tip endosperm ve sert bir tohum kabuğu 5,6 (Şekil 1A). Çift döllenmeden sonra, hücresel tip endosperm gelişimi, zigotların gelişiminden önce gelir. Çiçeklenmeden (DAF) ~ 5-6 gün sonra, endosperm altı ila sekiz çekirdek7'den oluştuğunda iki hücreli proembriyo ilk önce gözlenir. Solanum pimpinellifolium'da, embriyo 20 DAF'tan sonra son boyutuna yaklaşır ve tohumlar 32 DAF8'den sonra çimlenme için uygundur. Embriyo geliştikçe, endosperm yavaş yavaş emilir ve tohumda sadece az miktarda endosperm kalır. Kalıntı endosperm, radikül ucunu çevreleyen mikropylar endosperm ve tohumun geri kalanında lateral endosperm 9,10'dan oluşur. Dış tohum kabuğu, bütünlüğün kalınlaşmış ve odunlaşmış dış epidermisinden gelişir ve bütünleşme kalıntılarının ölü katmanlarıyla, embriyoyu ve endospermi korumak için sert bir kabuk oluştururlar5.
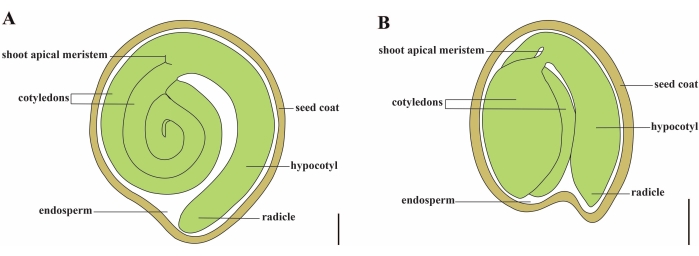
Resim 1: Solanum lycopersicum ve Arabidopsis thaliana'da olgun bir tohumun şematik gösterimi . (A) Olgun bir domates tohumunun uzunlamasına anatomisi. (B) Olgun bir Arabidopsis tohumunun uzunlamasına anatomisi. Olgun bir domates tohumu, bir Arabidopsis tohumundan yaklaşık 70 kat daha büyüktür. Ölçek çubukları = (A) 400 μm, (B) 100 μm. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
Yüksek kaliteli domates tohumlarının üretimi, embriyo, endosperm ve maternal tohum bileşenleri arasındaki koordinasyona bağlıdır11. Tohum gelişimindeki anahtar genlerin ve ağların diseksiyonu, mutant tohumların derin ve tam hatlı bir fenotipik kaydını gerektirir. Yarı ince kesit ve parafin kesit gibi geleneksel gömme-kesit teknikleri, embriyonun yerel ve daha ince yapılarını gözlemlemek için domates tohumlarına yaygın olarak uygulanır12,13,14,15. Bununla birlikte, tohum gelişimini ince kesitlerden analiz etmek genellikle zahmetlidir ve z ekseni uzamsal çözünürlüğünden yoksundur. Buna karşılık, doku temizleme, ortaya çıkması en muhtemel embriyo defektlerinin gelişim aşamasını belirlemek için hızlı ve etkili bir yöntemdir16. Temizleme yöntemi, kırılma indisini bir veya daha fazla biyokimyasal ajanla homojenleştirerek iç dokunun opaklığını azaltır16. Tüm doku temizleme, bir bitki doku yapısının bütünlüğünü bozmadan gözlemlenmesine izin verir ve temizleme teknolojisi ile üç boyutlu görüntülemenin kombinasyonu, bir bitki organının morfolojisi ve gelişimsel durumu hakkında bilgi edinmek için ideal bir çözüm haline gelmiştir17,18. Yıllar geçtikçe, Arabidopsis thaliana, Hordeum vulgare ve Beta vulgaris19,20,21,22,23 dahil olmak üzere çeşitli bitki türlerinde tohum temizleme teknikleri kullanılmıştır. Bunlar arasında, bütün monte edilmiş ovül temizleme teknolojisi, küçük boyutu, tohum kabuğu hücresinin 4-5 katmanı ve nükleer tip endosperm24,25 nedeniyle Arabidopsis'in tohum gelişimini incelemek için etkili bir yaklaşım olmuştur. Hoyer çözeltisi26'nın ortaya çıkması gibi farklı temizleme karışımlarının sürekli güncellenmesiyle, arpa ovülünün iç yapıları, endospermi tohumların büyük kısmını oluşturmasına rağmen, yüksek derecede netlikle görüntülenmiştir. Şeker pancarının embriyogenezi, vakum işlemi ile birlikte temizlenerek ve hidroklorik asit19 ile yumuşatılarak gözlemlenebilir. Bununla birlikte, yukarıda belirtilen türlerin aksine, domates tohumlarındaki protokollerin temizlenmesiyle embriyolojik gözlemler bildirilmemiştir. Bu, domateslerin embriyonik ve tohum gelişiminin ayrıntılı bir şekilde araştırılmasını önler.
Kloral hidrat, daldırılmış dokuların ve hücrelerin farklı optik düzlemlerde görüntülenmesini sağlayan ve hücreleri veya doku bileşenlerini büyük ölçüde koruyan bir temizleme çözeltisi olarak yaygın olarak kullanılır27,28,29. Kloral hidrat bazlı temizleme protokolü, Arabidopsis21,28'in embriyosunu ve endospermini gözlemlemek için tohumların tamamen temizlenmesi için başarıyla kullanılmıştır. Bununla birlikte, bu temizleme çözeltisi, Arabidopsis tohumlarından daha geçirimsiz olan domates tohumlarının temizlenmesinde etkili değildir. Fiziksel engeller şunları içerir: (1) domates bütünlüğünün 3 ila 15 DAF 30,31'de yaklaşık 20 hücre katmanı vardır, (2) domates endospermi nükleer tip 32 değil, hücresel tiptedir ve (3) domates tohumları 33,34 boyutunda yaklaşık70 kat daha büyüktür ve (4) temizleme reaktiflerinin penetrasyonunu engelleyen ve embriyo hücrelerinin görselleştirilmesini etkileyen büyük miktarlarda tohum kabuğu müsilajı üretir.
Bu nedenle, bu rapor, domates tohumlarının farklı aşamalarda tamamen monte edilmesi için optimize edilmiş bir kloral hidrat bazlı temizleme yöntemi sunar ve bu da embriyo gelişim sürecinin derin görüntülenmesini sağlar (Şekil 2).
Access restricted. Please log in or start a trial to view this content.
Protokol
1. Çözeltilerin hazırlanması
- 50 mL'lik bir santrifüj tüpüne 2,5 mL% 37 formaldehit, 2,5 mL buzul asetik asit ve 45 mL% 70 etanol ekleyerek FAA fiksatif hazırlayın. Vorteks yapın ve 4 °C'de saklayın. Kullanmadan hemen önce FAA fiksatif hazırlayın.
DİKKAT: %37 formaldehit aşındırıcıdır ve maruz kalırsa veya solunduğunda potansiyel olarak kanserojendir. Fiksatif, uygun kişisel koruyucu ekipman giyerken bir duman başlığında yapılmalıdır. - Kalay folyo ile sarılmış 100 mL'lik bir cam şişeye 5 mL% 100 gliserol, 40 g kloral hidrat ve 10 mL damıtılmış su ekleyerek temizleme çözeltisi hazırlayın. Oda sıcaklığında gece boyunca manyetik bir karıştırıcı kullanarak çözün. Hazırlanan çözelti 4 °C'de 6 aya kadar saklanabilir.
DİKKAT: Kloral hidrat kanserojendir ve keskin bir kokusu vardır. Deneyi bir duman başlığında yapın ve uygun kişisel koruyucu ekipman giyin. Kloral hidratın havada arındırılması kolaydır ve büyük miktarlarda depolanmamalıdır. Temizleme çözeltisi ışığa maruz kaldığında ayrışabilir ve ışıktan uzak tutulmalıdır. - 50 mL'lik bir santrifüj tüpüne 10 mL% 6 sodyum hipoklorit, 40 mL damıtılmış su ve 50 μL Ara-20 ekleyerek dezenfektan çözeltisini hazırlayın. Vorteks yapın ve oda sıcaklığında saklayın. Dezenfektan çözeltisini kullanımdan hemen önce taze olarak hazırlayın.
NOT: Uzun süre yerleştirilen sodyum hipokloritin etkili klor içeriği azalabilir ve gerçek duruma göre% 6 sodyum hipoklorit içeriği arttırılabilir.
2. Tohum toplama
- Domates tohumlarını (S. lycopersicum L. cv. Micro-Tom, bakınız Malzeme Tablosu) 8 cm × 8 cm × 1:1 çiçek besin toprağı ve substrat (v/v) karışımı ile dolu 8 cm kare havzalara ekin (bkz. Malzeme Tablosu) ve 24 ± 2 °C (gündüz) ve 18 ± 2 °C (gece) 16/8 saat aydınlık / karanlık periyotlu bir büyüme odasında yetişin, % 60 -% 70 bağıl nem ve 4.000 Lux ışık yoğunluğu. Yaklaşık 6 hafta sonra, bitkiler çiçeklenme aşamasına girdi.
- Bağımsız çiçeklerin çiçeklenme tarihini antezde etiketleyin (yaprakların açılma açısı 90 ° 'dir) ve çiçeklenmeden sonraki günü (DAF) kaydedin.
- Meyveleri 3 ila 23 DAF domates bitkisinden toplayın ve hemen buza koyun. Meyveleri (tohumlar veya embriyolar) 3 ila 23 DAF arasında erken (3-10 DAF), orta (11-16 DAF) ve geç (17-23 DAF) meyvelere (tohumlar veya embriyolar) bölün.
NOT: Bir seferde çok fazla meyve toplamayın ve daha fazla işlem için her meyvedeki tohumların 1 saat içinde soyulduğundan emin olun. - Erken meyveler için, meyveyi kırın ve bir slayta koyun ve stereomikroskop altında hassas forseps ile taze tohumları dikkatlice toplayın (bkz. Orta ve geç meyveler için, meyveyi kırın ve hassas forseps kullanarak doğrudan taze tohumlar toplayın.
3. Tohumların kloral hidrat bazlı temizlenmesi
NOT: Bu çalışmada geleneksel35 ve optimize edilmiş protokoller, tohum temizleme verimlilikleri açısından karşılaştırılmıştır.
- Geleneksel bir protokol kullanarak temizleme
- Taze tohumları (adım 2.4'te elde edilen) hemen 1.5 mL FAA fiksatif içeren 2 mL'lik bir santrifüj tüpüne yerleştirin ve oda sıcaklığında 4 saat boyunca yörüngesel bir çalkalayıcı (5 rpm, Malzeme Tablosuna bakınız) üzerinde inkübe edin.
- Bu tohumları, yörüngesel bir çalkalayıcıda (5 rpm) her biri 1 saat boyunca% 70,% 95 ve% 100 etanol (v / v) etanol serisinde kurutun.
- Tohumları slayta 3-5 damla temizleme çözeltisine (~ 100 μL) yerleştirin ve numuneyi bir örtü ile yavaşça örtün. Orta ve geç tohumlar için slaytı tek bir içbükey slaytla değiştirin (bkz. Malzeme Tablosu).
- Bu slaytları veya tek içbükey slaytları, tohum materyalinin gelişim aşamalarına bağlı olarak 30 dakika (3 DAF), 2 saat (6 DAF), 1 gün (9 DAF), 3 gün (12 DAF) veya 7 gün (14 ila 22 DAF) oda sıcaklığında tutun (malzemeler ne kadar genç olursa, temizleme hızı o kadar hızlı olur).
- Örnekleri, 10x, 20x ve 40x büyütmede bir dijital kamera ( Malzeme Tablosu'na bakınız) ile donatılmış bir diferansiyel girişim kontrastı (DIC) mikroskobu ile gözlemleyin. İletilen ışık parlaklığını, DIC kaydırıcısını ve kondenser diyaframını her örnek için gerçek zamanlı olarak ayarlayın ve optimize edin ve görüntüler yakalayın.
- Optimize edilmiş protokolü kullanarak temizleme
- Taze tohumları (adım 2.4'te elde edilen) doğrudan 1.5 mL dezenfektan çözeltisi (adım 1.3) içeren 2 mL'lik bir santrifüj tüpüne yerleştirin.
NOT: 2 mL santrifüj tüpünde toplanan tohum sayısı, tohumların gelişim aşamasına göre değişmektedir. Ayrıntılar Tablo 1'de listelenmiştir. - Numuneleri, en içteki tohum kabuğu taslağı açıkça görülene kadar oda sıcaklığında 3 ila 50 dakika boyunca bir orbital çalkalayıcı (30 rpm) üzerinde inkübe edin. Dezenfektan çözeltisini atın.
NOT: Gerekli kuluçka süresi, tohum gelişim aşamasına bağlıdır (tohumlar ne kadar geç olursa, kuluçka süresi o kadar uzun olacaktır). Ayrıntılar Tablo 1'de listelenmiştir. - Orta ve geç tohumlar için, tohumları bir slayta aktarın ve tohum müsilajını forseps ve stereomikroskop altında 1x ila 4x büyütmede diseksiyon iğnesi ile çıkarın. Forseps kullanarak tohumları orijinal santrifüj tüpüne geri aktarın.
NOT: Bu adım erken tohumlar için gerekli değildir. - Tohumları 5x, her seferinde 10 s olmak üzere 1,5 mL deiyonize su ile yıkayın. Deiyonize suyu atın.
- Tohumların hacmine 2 × bir temizleme çözeltisi ekleyin, ardından bir vakum pompası ile 0 ila 50 dakika vakumlu işlem (Tablo 1) ekleyin (bkz. Aralıklı vakum işlemi, her vakum işlemi ile 10 dakikalık aralıklarla 10 dakika aralıklı olarak gerçekleştirilir.
- Tohumların hacmine 2 × taze bir temizleme çözeltisi ile değiştirin. Tohumları içeren 2 mL santrifüj tüpünü oda sıcaklığında tutun ve temizlemeyi kolaylaştırmak için 30 dakika ila 7 gün boyunca ışıktan koruyun (Tablo 1). Kuluçka sırasında, geç embriyolar için, temizleme çözeltisini günlük olarak taze çözelti ile değiştirin ve tohumları 10 dakika boyunca vakum işlemine tabi tutun.
- Temizlenmiş tohumları slaytlarda veya tek içbükey slaytlarda hazırlayın ve 10x, 20x ve 40x büyütmede bir dijital kamera ile donatılmış DIC mikroskobu ile gözlemleyin. İletilen ışık parlaklığını, DIC kaydırıcısını ve kondenser diyaframını her örnek için gerçek zamanlı olarak ayarlayın ve optimize edin ve görüntüler yakalayın.
- Taze tohumları (adım 2.4'te elde edilen) doğrudan 1.5 mL dezenfektan çözeltisi (adım 1.3) içeren 2 mL'lik bir santrifüj tüpüne yerleştirin.
Access restricted. Please log in or start a trial to view this content.
Sonuçlar
Domates tohumları Arabidopsis'te olduğu gibi geleneksel bir yöntem kullanılarak temizlendiğinde, yoğun endosperm hücreleri erken domates embriyolarının 3 DAF ve 6 DAF'ta görselleştirilmesini engelledi (Şekil 3A, B). Embriyonun toplam hacmi arttıkça, küresel bir embriyo 9 DAF'ta zar zor ayırt edilebildi (Şekil 3C). Bununla birlikte, tohum büyüklüğü artmaya devam ettikçe, geçirgenliği azaldı ve 12 DAF'ta bulanık...
Access restricted. Please log in or start a trial to view this content.
Tartışmalar
Mekanik kesitleme ile karşılaştırıldığında, temizleme teknolojisi, bitki dokularının veya organlarının bütünlüğünü koruduğu için üç boyutlu görüntüleme için daha avantajlıdır16. Geleneksel temizleme protokolleri, kimyasal çözeltilerin daha kolay nüfuz etmesi nedeniyle genellikle küçük numunelerle sınırlıdır. Domates tohumu, doku temizliği için sorunlu bir örnektir, çünkü boyut olarak bir Arabidopsis tohumundan yaklaşık 70 kat daha büyüktür ...
Access restricted. Please log in or start a trial to view this content.
Açıklamalar
Yazarların açıklayacağı bir çıkar çatışması yoktur.
Teşekkürler
Yazarlar, sırasıyla diferansiyel girişim kontrast mikroskobu ve geleneksel temizleme yöntemi hakkındaki yararlı önerileri için Dr. Jie Le ve Dr. Xiufen Song'a minnettardır. Bu araştırma, Çin Ulusal Doğa Bilimleri Vakfı (31870299) ve Çin Bilimler Akademisi Gençlik İnovasyon Teşvik Derneği tarafından finanse edildi. Şekil 2, BioRender.com ile oluşturulmuştur.
Access restricted. Please log in or start a trial to view this content.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 1,000 µL pipette | GILSON | FA10006M | |
| 1,000 µL pipette tips | Corning | T-1000-B | |
| 2 ml centrifuge tube | Axygen | MCT-200-C | |
| 37% formaldehyde | DAMAO | 685-2013 | |
| 5,000 µL pipette | Eppendorf | 3120000275 | |
| 5,000 µL pipette tips | biosharp | BS-5000-TL | |
| 50 ml centrifuge tube | Corning | 430829 | |
| Absolute Ethanol | BOYUAN | 678-2002 | |
| Bottle glass | Fisher | FB800-100 | |
| Chloral Hydrate | Meryer | M13315-100G | |
| Coverslip | Leica | 384200 | |
| DIC microscope | Zeiss | Axio Imager A1 | 10x, 20x and 40x magnification |
| Disinfectant | QIKELONGAN | 17-9185 | |
| Dissecting needle | Bioroyee | 17-9140 | |
| Flower nutrient soil | FANGJIE | ||
| Forceps | HAIOU | 4-94 | |
| Glacial Acetic Acid | BOYUAN | 676-2007 | |
| Glycerol | Solarbio | G8190 | |
| Magnetic stirrer | IKA | RET basic | |
| Micro-Tom | Tomato Genetics Resource Center | LA3911 | |
| Orbital shaker | QILINBEIER | QB-206 | |
| Seeding substrate | PINDSTRUP | LV713/018-LV252 | Screening:0-10 mm |
| Single concave slide | HUABODEYI | HBDY1895 | |
| Slide | Leica | 3800381 | |
| Stereomicroscope | Leica | S8 APO | 1x to 4x magnification |
| Tin foil | ZAOWUFANG | 613 | |
| Tween 20 | Sigma | P1379 | |
| Vacuum pump | SHIDING | SHB-III | |
| Vortex meter | Silogex | MX-S |
Referanslar
- FAOSTAT. , Available from: https://www.fao.org/faostat/en/#data/QCL (2022).
- Olmstead, R. G., Bohs, L. A summary of molecular systematic research in Solanaceae: 1982-2006. Acta Horticulturae. 745, 255-268 (2007).
- Consortium, T. G. The tomato genome sequence provides insights into fleshy fruit evolution. Nature. 485 (7400), 635-641 (2012).
- Ebert, A. W., Chou, Y. Y. The tomato collection maintained by AVRDC - The World Vegetable Center: composition, germplasm dissemination and use in breeding. Acta Horticulturae. 1101, 169-176 (2015).
- Hilhorst, H., Groot, S., Bino, R. J. The tomato seed as a model system to study seed development and germination. Acta Botanica Neerlandica. 47, 169-183 (1998).
- Chaban, I. A., Gulevich, A. A., Kononenko, N. V., Khaliluev, M. R., Baranova, E. N. Morphological and structural details of tomato seed coat formation: A different functional role of the inner and outer epidermises in unitegmic ovule. Plants-Basel. 11 (9), 1101(2022).
- Iwahori, S. High temperature injuries in tomato. V. Fertilization and development of embryo with special reference to the abnormalities caused by high temperature. Journal of The Japanese Society for Horticultural Science. 35 (4), 379-386 (1966).
- Xiao, H., et al. Integration of tomato reproductive developmental landmarks and expression profiles, and the effect of SUN. on fruit shape. BMC Plant Biology. 9 (1), 49(2009).
- Karssen, C. M., Haigh, A. M., Toorn, P., Weges, R. Physiological mechanisms involved in seed priming. Recent advances in the development and germination of seeds. NATO ASI Series. Taylorson, R. B. 187, Springer. Boston, MA. (1989).
- Nonogaki, H. Seed dormancy and germination-emerging mechanisms and new hypotheses. Frontiers in Plant Science. 5, 233(2014).
- Doll, N. M., Ingram, G. C. Embryo-endosperm interactions. Annual Review of Plant Biology. 73, 293-321 (2022).
- Serrani, J. C., Fos, M., Atarés, A., García-Martínez, J. L. Effect of gibberellin and auxin on parthenocarpic fruit growth induction in the cv micro-tom of tomato. Journal of Plant Growth Regulation. 26 (3), 211-221 (2007).
- Yang, C., et al. A regulatory gene induces trichome formation and embryo lethality in tomato. Proceedings of the National Academy of Sciences USA. 108 (29), 11836-11841 (2011).
- Goetz, S., et al. Role of cis-12-oxo-phytodienoic acid in tomato embryo development. Plant Physiology. 158 (4), 1715-1727 (2012).
- Ko, H. Y., Ho, L. H., Neuhaus, H. E., Guo, W. J. Transporter SlSWEET15 unloads sucrose from phloem and seed coat for fruit and seed development in tomato. Plant Physiology. 187 (4), 2230-2245 (2021).
- Richardson, D. S., Lichtman, J. W. Clarifying tissue clearing. Cell. 162 (2), 246-257 (2015).
- Kurihara, D., Mizuta, Y., Sato, Y., Higashiyama, T. ClearSee: A rapid optical clearing reagent for whole-plant fluorescence imaging. Development. 142 (23), 4168-4179 (2015).
- Vieites-Prado, A., Renier, N. Tissue clearing and 3D imaging in developmental biology. Development. 148 (18), (2021).
- Kwiatkowska, M., Kadłuczka, D., Wędzony, M., Dedicova, B., Grzebelus, E. Refinement of a clearing protocol to study crassinucellate ovules of the sugar beet (Beta vulgaris L., Amaranthaceae). Plant Methods. 15, 71(2019).
- Ponitka, A., Ślusarkiewicz-Jarzina, A. Cleared-ovule technique used for rapid access to early embryo development in Secale cereale × Zea mays crosses. Acta Biologica Cracoviensia. Series Botanica. 46, 133-137 (2014).
- Ceccato, L., et al. Maternal control of PIN1 is required for female gametophyte development in Arabidopsis. PLoS One. 8 (6), 66148(2013).
- Wilkinson, L. G., Tucker, M. R. An optimised clearing protocol for the quantitative assessment of sub-epidermal ovule tissues within whole cereal pistils. Plant Methods. 13, 67(2017).
- Hedhly, A., Vogler, H., Eichenberger, C., Grossniklaus, U. Whole-mount clearing and staining of Arabidopsis flower organs and Siliques. Journal of Visualized Experiments. (134), e56441(2018).
- Creff, A., Brocard, L., Ingram, G. A mechanically sensitive cell layer regulates the physical properties of the Arabidopsis seed coat. Nature Communications. 6, 6382(2015).
- Yang, T., et al. The B3 domain-containing transcription factor ZmABI19 coordinates expression of key factors required for maize seed development and grain filling. Plant Cell. 33 (1), 104-128 (2021).
- Anderson, L. E. Hoyer's solution as a rapid permanent mounting medium for bryophytes. Bryologist. 57 (3), 242-244 (1954).
- Herr, J. M. A new clearing-squash technique for the study of ovule development in angiosperms. American Journal of Botany. 58 (8), 785-790 (1971).
- Yadegari, R., et al. Cell differentiation and morphogenesis are uncoupled in Arabidopsis raspberry embryos. The Plant Cell. 6 (12), 1713-1729 (1995).
- Grini, P. E., Jurgens, G., Hulskamp, M. Embryo and endosperm development is disrupted in the female gametophytic capulet mutants of Arabidopsis. Genetics. 162 (4), 1911-1925 (2002).
- Kataoka, K., Uemachi, A., Yazawa, S. Fruit growth and pseudoembryo development affected by uniconazole, an inhibitor of gibberellin biosynthesis, in pat-2 and auxin-Induced parthenocarpic tomato fruits. Scientia Horticulturae. 98 (1), 9-16 (2003).
- de Jong, M., Wolters-Arts, M., Feron, R., Mariani, C., Vriezen, W. H. The Solanum lycopersicum auxin response factor 7 (SlARF7) regulates auxin signaling during tomato fruit set and development. Plant Journal. 57 (1), 160-170 (2009).
- Roth, M., Florez-Rueda, A. M., Paris, M., Stadler, T. Wild tomato endosperm transcriptomes reveal common roles of genomic imprinting in both nuclear and cellular endosperm. Plant Journal. 95 (6), 1084-1101 (2018).
- Orsi, C. H., Tanksley, S. D. Natural variation in an ABC transporter gene associated with seed size evolution in tomato species. PLoS Genetics. 5 (1), 1000347(2009).
- Herridge, R. P., Day, R. C., Baldwin, S., Macknight, R. C. Rapid analysis of seed size in Arabidopsis for mutant and QTL discovery. Plant Methods. 7 (1), 3(2011).
- Xu, T. T., Ren, S. C., Song, X. F., Liu, C. M. CLE19 expressed in the embryo regulates both cotyledon establishment and endosperm development in Arabidopsis. Journal of Experimental Botany. 66 (17), 5217-5227 (2015).
- Ghadiri Alamdari, N., Salmasi, S., Almasi, H. Tomato seed mucilage as a new source of biodegradable film-forming material: effect of glycerol and cellulose nanofibers on the characteristics of resultant films. Food and Bioprocess Technology. 14 (12), 2380-2400 (2021).
- Gardner, R. O. An overview of botanical clearing technique. Stain Technology. 50 (2), 99-105 (1975).
- Beresniewicz, M. M., Taylor, A. G., Goffinet, M. C., Terhune, B. T. Characterization and location of a semipermeable layer in seed coats of leek and onion (Liliaceae), tomato and pepper (Solanaceae). Seed Science and Technology. 23 (1), 123-134 (1995).
- Stebbins, G. L. A bleaching and clearing method for plant tissues. Science. 87 (2245), 21-22 (1938).
- Debenham, E. M. A modified technique for the microscopic examination of the xylem of whole plants or plant organs. Annals of Botany. 3 (2), 369-373 (1939).
- Morley, T. Accelerated clearing of plant leaves by NaOH in association with oxygen. Stain Technology. 43 (6), 315-319 (1968).
Access restricted. Please log in or start a trial to view this content.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır