Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Akıllı Yüksek Verimli Antimikrobiyal Duyarlılık Testi / Faj Tarama Sistemi ve Lar Antimikrobiyal Direnç İndeksinin Uygulanması
Bu Makalede
Özet
Burada akıllı, yüksek verimli antimikrobiyal duyarlılık testi/faj tarama sisteminin prensibini, yapısını ve talimatını tanıtıyoruz. Uygulaması, örnek olarak Çin'in Shandong kentindeki kümes hayvanlarından izole edilen Salmonella kullanılarak gösterilmiştir. Lar indeksi hesaplanır ve antimikrobiyal direncin değerlendirilmesindeki önemi kapsamlı bir şekilde tartışılır.
Özet
Dirençli bakteriler için antimikrobiyal duyarlılık testi (AST) ve faj yüksek verimli taramanın verimliliğini artırmak ve tespit maliyetini azaltmak için, 96 noktalı matris aşılayıcı, görüntü elde etme dönüştürücü ve ilgili yazılımı içeren akıllı bir yüksek verimli AST / faj tarama sistemi, AST kriterlerine ve Klinik ve Laboratuvar Standartları Enstitüsü (CLSI) tarafından formüle edilen direnç kırılma noktalarına ( R ) göre geliştirilmiştir. Çin'in Shandong kentindeki kümes hayvanlarından izole edilen 1.500 Salmonella suşunun 10 antimikrobiyal ajana karşı minimum inhibitör konsantrasyon (MIC) dağılımlarının (R / 8 ila 8R) AST ve istatistikleri, akıllı yüksek verimli AST / faj tarama sistemi tarafından gerçekleştirildi. "Daha az antibiyoz, daha az direnç ve az antibiyoza kadar rezidüel" anlamına gelen Lar indeksi, her bir MK'nin ağırlıklı ortalamasının hesaplanması ve R'ye bölünmesi ile elde edildi. Bu yaklaşım, yüksek dirençli suşların antimikrobiyal direnç (AMR) derecesini karakterize etmek için direnç prevalansının kullanılmasına kıyasla doğruluğu artırır. Yüksek AMR'li Salmonella suşları için, litik fajlar bu sistem tarafından faj kütüphanesinden verimli bir şekilde tarandı ve lizis spektrumu hesaplandı ve analiz edildi. Sonuçlar, akıllı yüksek verimli AST / faj tarama sisteminin çalıştırılabilir, doğru, yüksek verimli, ucuz ve bakımı kolay olduğunu gösterdi. Shandong veteriner antimikrobiyal direnç izleme sistemi ile birlikte sistem, AMR ile ilgili bilimsel araştırma ve klinik tespit için uygundu.
Giriş
Antimikrobiyal ajanlar bakteriyel enfeksiyon hastalıklarını önlemek için yaygın olarak kullanıldığından, antimikrobiyal direnç (AMR) küresel bir halk sağlığı sorunu haline gelmiştir1. AMR ile mücadele, epidemiyolojik patojenlerin AMR'sini izlemek ve hassas antimikrobiyal ajanların ve litik bakteriyofajların sinerjik tedavisinin mevcut ana görevidir2.
İn vitro antimikrobiyal duyarlılık testi (AST), tedaviyi izlemek ve AMR seviyesini tespit etmek için temel dayanaktır. Antimikrobiyal farmakolojinin önemli bir parçasıdır ve klinik ilaç tedavisinin kritik temelidir. Amerika Birleşik Devletleri Klinik ve Laboratuvar Standartları Enstitüsü (CLSI) ve Avrupa Antimikrobiyal Duyarlılık Testi Komitesi (EUCAST), AST ile ilgili uluslararası kriterleri formüle etmiş ve revize etmiş ve AST yöntemlerini ve kesme noktalarını hassas (S), dirençli (R) veya orta (I) olarak belirli bir "organizma-antimikrobiyal ajan" kombinasyonunun MIC'sini belirlemek için sürekli olarak değiştirilmiş ve tamamlamıştır.3, 4.
1980'lerden 1990'lara kadar, otomatik mikro et suyu seyreltme cihazları hızla geliştirildi ve Alfred 60AST, VITEK System, PHOENIXTM ve Cobasbact 5,6,7 gibi örneklerle klinik uygulamaya uygulandı. Bununla birlikte, bu aletler pahalıydı, yüksek maliyetli sarf malzemeleri gerektiriyordu ve tespit aralıkları klinik hasta ilaçları için tasarlandı 5,6,7. Bu nedenlerden dolayı, veteriner klinik muayenesi ve büyük miktarlarda yüksek dirençli suşların tespiti için uygun değildirler. Bu çalışmada, 96 noktalı matris inokülatörü (Şekil 1), görüntü elde etme dönüştürücüsü (Şekil 2) ve ilgili yazılım8'i içeren akıllı, yüksek verimli bir AST / faj tarama sistemi, bir grup bakteri suşu için birden fazla antimikrobiyal ajana karşı aynı anda agar seyreltme yöntemi ile AST'yi yürütmek üzere geliştirilmiştir. Ayrıca sistem, fajların antimikrobiyal dirençli bakterilere karşı lizis paternlerini tespit etmek ve analiz etmek için de kullanıldı9 ve litik fajlar faj kütüphanesinden verimli bir şekilde seçildi. Bu sistemin verimli, uygun fiyatlı ve kullanımı kolay olduğu bulundu.
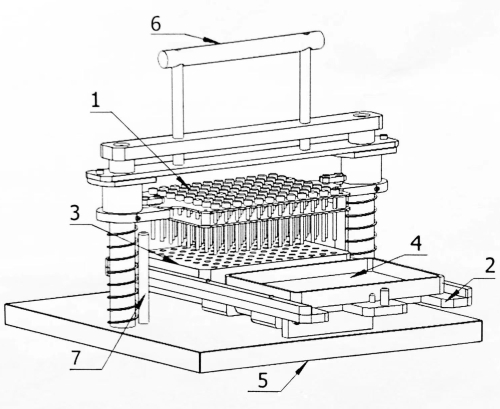
Şekil 1: 96 noktalı matris aşılayıcının yapısal diyagramı. 1: Aşılama pim plakası; 2: Mobil operatör; 3: Tohum bloğu; 4: İnkübe plakası; 5: Taban; 6: Çalıştırma kolu; 7: Limit pimi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
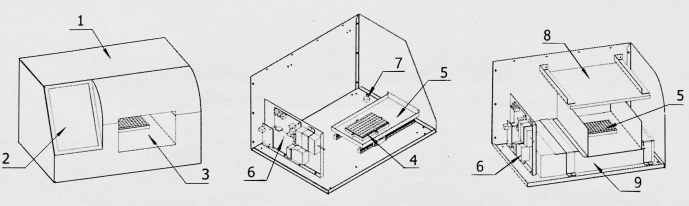
Şekil 2: Görüntü elde etme dönüştürücüsünün yapısal diyagramı. 1: Kabuk; 2: Görüntü ekranı; 3: Görüntü alma odası; 4: Algılama panosu tabanı; 5: Depo içinde ve dışında algılama panosu; 6: Kontrol panosu; 7: Görüntü alma dönüştürme cihazı; 8: Işık kaynağı; 9: Görüntü tarayıcı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Protokol
Bu çalışmada kullanılan Salmonella suşları, Çin'deki Shandong Tarım Bilimleri Akademisi, Hayvan Bilimleri ve Veterinerlik Enstitüsü Biyogüvenlik Komitesi'nden onay alındıktan sonra Çin'in Shandong kentindeki kümes hayvanlarından toplanmıştır.
1. Akıllı yüksek verimli AST sisteminin uygulanması8
- Aşı hazırlama
- Kalite kontrol organizması Escherichia coli ve 93 Salmonella suşu, Mueller-Hinton agar (MHA) plakalarında AST için test edilecek 37 ° C'de 16-18 saat boyunca inkübe edin3.
- Her bir suşun aşısını, CLSI standardı3'tebelirtilen yönteme göre 0,5 McFarland bulanıklık standardına uyacak şekilde hazırlayın ve ardından 10 kez seyreltin.
- Negatif kontrol olarak 96 oyuklu plakanın yatay 1. kuyucuğuna (A1) 200 μL steril normal salin, pozitif kontrol olarak yatay 2. ve 3. kuyucuklara (A2ve A3) iki kalite kontrol organizması süspansiyonu yerleştirin ve kalite kontrol sırasıyla. Test edilen her boyanın 200 μL seyreltilmiş aşı süspansiyonlarını 96 oyuklu tohum bloğundaki karşılık gelen 93 oyuğa ekleyin.
- Antimikrobiyal agar plağının hazırlanması
- Lar indeksinin hesaplama aralığına göre test edilen farklı antibakteriyel ajanların konsantrasyon aralıklarını ayarlayın (0.125R ila 8R). Konsantrasyonlar, kalite kontrol aralığından veya 0.0625R'den (daha düşük aralığa tabi) 8R'ye kadar değişir.
NOT: Lar indeksi hesaplanmazsa, antibiyotik konsantrasyonları aralığı AST ihtiyaçlarına göre ayarlanabilir. - CLSI standardı3'te belirtilen agar seyreltme yöntemine dayalı olarak uygun bir stok konsantrasyonu ile başlayarak antibiyotik çözeltisi için bir log2 ikiye katlama seyreltme şeması yürütün.
- 18 mL Mueller-Hinton agar ortamı içeren 50 mL cam şişeleri sterilize edin. 45-50 °C'ye soğutulmuş 18 mL erimiş ortama antimikrobiyal çözeltinin uygun dilüsyonlarından 2 mL ekleyin, iyice karıştırın ve biyogüvenlik kabinindeki plakalara dökün.
- Agarın oda sıcaklığında (RT) katılaşmasına izin verin, inkübe edilmiş plakaların kapağının altında bir boşluk bırakın ve aşılamadan önce agar yüzeyini kurutmak için üfleyin.
- İnkübe edilmiş plakaların arka tarafındaki antimikrobiyal ajan türlerini ve konsantrasyonlarını etiketleyin. Her bir antimikrobiyal ajanın çoklu inkübe edilmiş plakalarını, log2-iki katına çıkan seyreltme sırasına göre bir yığın halinde düzenleyin.
- Her bir antimikrobiyal ajan için kontrol olarak iki ilaçsız agar plakası hazırlayın.
- Lar indeksinin hesaplama aralığına göre test edilen farklı antibakteriyel ajanların konsantrasyon aralıklarını ayarlayın (0.125R ila 8R). Konsantrasyonlar, kalite kontrol aralığından veya 0.0625R'den (daha düşük aralığa tabi) 8R'ye kadar değişir.
- 96 noktalı matris aşılayıcı için aşılama adımları
- Otoklavlanmış aşılama pimi plakasını biyogüvenlik kabinindeki 96 noktalı matris aşılayıcının desteğine takın.
- Hazırlanan tohum bloğunu, test edilmiş suşlar ve agar inkübe edilmiş bir plaka ile birlikte, iki plaka için aynı konumlandırma açısına sahip mobil taşıyıcıya yerleştirin.
- Mobil taşıyıcıyı, tohum bloğu doğrudan aşılama pimi plakasının altında olacak şekilde itin.
- Çalıştırma koluna basın, aşılama pimi plakasını aşağı doğru hareket ettirin ve 96 pimi tohum bloğunun 96 kuyusundaki aşıya yönlendirin.
- Çalıştırma kolunu kontrollü olarak serbest bırakın, ardından yayın etkisi altında aşılama pimi plakasını sıfırlayın.
- Her bir aşıyı iyice karıştırmak ve daldırmak için çalıştırma koluna 2-3 kez basın. Taşıyıcı plakayı, inkübe edilmiş plaka doğrudan aşılama pimi plakasının altında olacak şekilde itin ve hareket ettirin.
- Çalıştırma koluna basın, aşılama pimi plakasını aşağı doğru hareket ettirin ve aşılama pimlerinin inkübe edilmiş plakanın yüzeyine tam olarak temas etmesini sağlamak için 1-2 saniye durun.
- Çalıştırma kolunu serbest bırakın. Bu bir aşılamayı tamamlar. Başka bir inkübe plakasını değiştirin ve bir grup antimikrobiyal agar plakası bitene kadar döngüye devam edin.
- Başka bir aşılama pimi plakasını ve tohum bloğunu değiştirin ve başka bir test edilmiş suş grubunu aşılayın. Tüm aşılamalar tamamlanana kadar döngü yapın.
NOT: Kontaminasyon veya antimikrobiyal ajan taşınmadığından emin olmak için önce bir kontrol agar plakasını (antimikrobiyal ajan yok), ardından plakayı düşükten yükseğe ilaç konsantrasyonu sırasına göre ve en son ikinci bir kontrol agar plakasını aşılayın. Aşılama hacmi, yaklaşık 2 μL'lik her bir pimin doğal birikiminin hacmine dayanır.
- Antimikrobiyal agar plakalarının inkübe edilmesi
- Aşılanmış antimikrobiyal agar plakalarını, aşılama noktalarındaki nem agar tarafından emilene kadar RT'de inkübe edin.
- Plakaları ters çevirin ve inhibe edilmemiş bakterilerin koloniler oluşturmasını sağlamak için test edilen suşlar için 37 ° C'de 16-20 saat inkübe edin.
- Görüntü elde etme ve veri istatistikleri
- Programı açmak için 96 noktalı matris AST görüntü toplama sistemine çift tıklayın.
- Görev çubuğundaki Test Bilgileri'ne tıklayın. Yeni bir test görevi oluşturmak için Yeni'ye tıklayın ve kod, isim, kaynak, bakteri, suş sayısı, antibiyotikler ve gradyan dahil olmak üzere bilgileri istemlere göre doldurun.
- Oluşturulan yeni görevi seçmek için Veri Toplama > Fotoğraf > Test öğesine tıklayın. Antibiyotiğin adını seçmek için Antibiyotikler'e tıklayın ve bu antibiyotiğin başlangıç konsantrasyonunu seçmek için Gradyan'a tıklayın.
- Görüntü alma dönüştürücüsüne bağlanmak için Bağlan'a tıklayın.
- Karşılık gelen inkübasyon plakalarını, oryantasyon için sağ ön tarafta eksik açı olacak şekilde algılama plakası tabanına yerleştirin ve görüntü alma dönüştürücüsüne itin.
- Görüntüleri elde etmek için Koleksiyon'a tıklayın. Antibiyotik gradyanı otomatik olarak bir sonraki gradyana atlayacaktır. Bir sonraki plakayı sırayla yerleştirin ve bu antibiyotik için plakalar toplanana kadar Koleksiyon'a tıklamaya devam edin.
- Antibiyotikler'e tıklayın ve bir sonraki inkübe plaka setini seçin. Başlangıç gradyanını seçmek ve bir sonraki görüntü toplama turuna geçmek için Gradyan'a tıklayın.
- Tüm koleksiyonları tamamladıktan sonra Gönder'e tıklayın. Program, görüntülerdeki her aşılama noktasında biçimlendirilmiş beyaz piksel sayısını otomatik olarak tanıyacak, koloni oluşumu olup olmadığını belirleyecek ve görüntüleri MIC değerlerine dönüştürecektir.
- Test edilen antibiyotiklere karşı suşların tüm MIC sonuçlarını elde etmek için Sorgu'ya tıklayın.
NOT: Akıllı yüksek verimli AST sistemi, büyük bakteri suşlarının MIC'lerini belirlemek için uygundur. Hazırlık, aşılama, inkübasyon ve sonuç okuma dahil olmak üzere test süreci 3 gün sürer. Antibiyotik türleri ve MIC tespit aralıkları ilgili ihtiyaçlara göre ayarlanabilir ve ana sarf malzemeleri yeniden kullanılabilir.
- Lar indeksinin hesaplanması
- Lar indeksini aşağıdaki formülle doğru bir şekilde belirleyin: , burada:
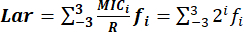
MICi: minimum inhibitör konsantrasyon.
MIC-3'ten MIC3'e kadar olan MIC dağılım aralığı, R merkezli seri iki katlı konsantrasyonları temsil eder: 0.125R, 0.25R, 0.5R, R, 2R, 4R ve 8R. 2i'dir ve i aralığı -3 ila 3'tür.
2i'dir ve i aralığı -3 ila 3'tür.
R: CLSI tarafından standardize edilmiş antimikrobiyal ajanlara karşı bakterilerin direncinin kırılma noktaları.
f: MIC frekans dağılımı.
NOT: Genel Lar indeksi, tüm Lar indekslerinin aritmetik ortalamasıdır. Lar dizini hesaplandıktan sonra, son değeri ondalık virgülden sonra iki anlamlı basamağa yuvarlayın.
- Lar indeksini aşağıdaki formülle doğru bir şekilde belirleyin: , burada:
2. Akıllı yüksek verimli faj tarama sistemi9
- Faj tohum bloğunun ve bakteri içeren çift katmanlı inkübe plakaların hazırlanması.
- Farklı fajlar yapmak için çift katmanlı agar yöntemi10 veya sıvı kültür yöntemi11'i kullanın. 1 x 104-5 pfu / mL'lik bir titre ile uygun bir paralel konsantrasyona seyreltin ve 96 oyuklu tohum bloğuna 200 μL faj aşısı ekleyin.
- Test edilecek bakteri içeren çift katmanlı plakalar yapın (10 μL bakteri [agar 12 g / L] ve 6 mL üst yarı agar ortamı [6 g / L] ile 100 g / L [0.5 McFarland]).
- Test edilecek her suş için çift katmanlı bir inkübasyon plakası yapın. Çift katlı plakanın kapağının altında bir boşluk bırakın ve biyogüvenlik kabinindeki agar yüzeyini kurutmak için üfleyin.
- Tarama testi
- Hazırlanan faj tohum bloğunu ve çift katmanlı plakayı 96 noktalı matris inokülatörün mobil taşıyıcısına yerleştirin ve tüm faj inokullarını yarı agar yüzeyine aktarın. Test edilen tüm suşlar tamamlanana kadar döngülere devam edin.
- Aşılanmış çift katmanlı plakaların, aşı noktalarındaki nem yarı agar tarafından tamamen emilene kadar RT'de kalmasına izin verin.
- Plakaları ters çevirin ve berrak litik lekelerin oluşmasını sağlamak için test edilen suşlar için uygun koşullar altında 4-6 saat inkübe edin.
- Verileri analiz etme
- Görüntü alma dönüştürücüsü ile her bir çift katmanlı plakanın deneysel sonucunun görüntüsünü elde edin ve kaydedin (adım 1.5.4-1.5.6).
- Elde edilen görüntülere dayalı olarak farklı noktaların sayılarını ve morfolojilerini bir elektronik tabloya kaydedin ve farklı faj türlerinin ilgili oranlarını hesaplayın.
Sonuçlar
Akıllı yüksek verimli AST sisteminin protokolünü takiben, uygulaması örnek olarak Çin'in Shandong kentindeki kümes hayvanlarından elde edilen Salmonella ile gösterilmiştir.
Görüntü elde etme dönüştürücüsü tarafından belirlenen 2 ila 256 μg/mL konsantrasyonlarda ampisilin (32 μg/mL R) içeren agar plakalarında Salmonella suşlarının büyümesi Şekil 3'te gösterilmektedir. Yatay 1. kuyu A1 negatif kontroldü...
Tartışmalar
Agar seyreltme yöntemi iyi kurulmuş ve yaygın olarak kullanılmaktadır. Yüksek verimli AST sisteminin prensibi, agar seyreltme yöntemiydi. Protokoldeki kritik adımlardan biri, arka arkaya birden çok kez gerçekleştirilen 96 aşının tek seferde doğru yüksek verimli transferiydi. Bu kritik adımı tamamlamak için, 96 noktalı matris aşılayıcının pimleri tek tip ve çok pürüzsüzdü. Her bir pimin doğal birikimi yaklaşık 2 μL'lik bir hacimdi ve agar ortamının yüzeyinde küçük damlacıklar halin...
Açıklamalar
Yuqing Liu ve ark. 96 noktalı matris aşılayıcı ve görüntü elde etme dönüştürücüsü ve uygulamaları için Çin patentleri başvurusunda bulundu (Patent numarası ZL 201610942866.3 ve Patent numarası ZL 201910968255.X).
Teşekkürler
Bu çalışma Ulusal Anahtar Araştırma ve Geliştirme Projesi (2019YFA0904003) tarafından desteklenmiştir; Shandong Eyaletinde Modern Tarımsal Endüstriyel Sistem (SDAIT-011-09); Uluslararası İşbirliği Platformu Optimizasyon Projesi (CXGC2023G15); Tarım Bilimleri Akademisi Shandong, Çin'in tarım bilimi ve teknoloji inovasyon projesinin başlıca İnovasyon görevleri (CXGC2023G03).
Malzemeler
| Name | Company | Catalog Number | Comments |
| 96 well culture plate | Beijing lanjieke Technology Co., Ltd | 11510 | |
| 96-dot matrix AST image acquisition system | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright | |
| 96-dot matrix inoculator | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | N/A | Patented product |
| Agar | Qingdao hi tech Industrial Park Haibo Biotechnology Co., Ltd | HB8274-1 | |
| Amikacin | Shanghai McLean Biochemical Technology Co., Ltd | A857053 | |
| Amoxicillin | Shanghai McLean Biochemical Technology Co., Ltd | A822839 | |
| Ampicillin | Shanghai McLean Biochemical Technology Co., Ltd | A830931 | |
| Analytical balance | Sartorius | BSA224S | |
| Automated calculation software for Lar index of AMR | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright | |
| Bacteria Salmonella strains | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | N/A | Animal origin |
| Bacterial resistance Lar index certification management system V1.0 | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright | |
| Ceftiofur | Shanghai McLean Biochemical Technology Co., Ltd | C873619 | |
| Ciprofloxacin | Shanghai McLean Biochemical Technology Co., Ltd | C824343 | |
| Clavulanic acid | Shanghai McLean Biochemical Technology Co., Ltd | C824181 | |
| Clean worktable | Suzhou purification equipment Co., Ltd | SW-CJ-2D | |
| Colistin sulfate | Shanghai McLean Biochemical Technology Co., Ltd | C805491 | |
| Culture plate | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | N/A | Patented product |
| Doxycycline | Shanghai McLean Biochemical Technology Co., Ltd | D832390 | |
| Enrofloxacin | Shanghai McLean Biochemical Technology Co., Ltd | E809130 | |
| Filter 0.22 μm | Millipore | SLGP033RB | |
| Florfenicol | Shanghai McLean Biochemical Technology Co., Ltd | F809685 | |
| Gentamicin | Shanghai McLean Biochemical Technology Co., Ltd | G810322 | |
| Glass bottle 50 mL | Xuzhou Qianxing Glass Technology Co., Ltd | QX-7 | |
| High-throughput resistance detection system V1.0 | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright | |
| Image acquisition converter | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | N/A | Patented product |
| Meropenem | Shanghai McLean Biochemical Technology Co., Ltd | M861173 | |
| Mueller-Hinton agar | Qingdao hi tech Industrial Park Haibo Biotechnology Co., Ltd | HB6232 | |
| Petri dish 60 mm x 15 mm | Qingdao Jindian biochemical equipment Co., Ltd | 16021-1 | |
| Petri dish 90 mm x 15 mm | Qingdao Jindian biochemical equipment Co., Ltd | 16001-1 | |
| Salmonella phages | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | N/A | |
| Shaker incubator | Shanghai Minquan Instrument Co., Ltd | MQD-S2R | |
| Turbidimeter | Shanghai XingBai Biotechnology Co., Ltd | F-TC2015 | |
| Varms base type library system V1.0 | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright | |
| Vertical high-pressure steam sterilizer | Shanghai Shen'an medical instrument factory | LDZX-75L | |
| Veterinary pathogen resistance testing management system | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright | |
| Veterinary resistance cloud monitoring and phage control platform V1.0 | Institute of Animal Science and Veterinary Medicine, Shandong Academy of Agricultural Sciences | In-house software copyright |
Referanslar
- Ramanan, L., et al. Antimicrobial resistance-the need for global solutions. The Lancet Infectious Diseases. 13 (12), 1057-1098 (2013).
- Xiaonan, Z., Qing, Z., Thomas, S. P., Yuqing, L., Martha, R. J. C. inPhocus: Perspectives of the application of bacteriophages in poultry and aquaculture industries based on Varms in China. PHAGE: Therapy, Applications, and Research. 2 (2), 69-74 (2021).
- CLSI. . Performance Standards for Antimicrobial Disk Susceptibility Tests. CLSI document M100. , (2022).
- Yuqing, L., et al. . Antimicrobial Sensitivity Testing Standard of EUCAST. , (2017).
- Barnini, S., et al. A new rapid method for direct antimicrobial susceptibility testing of bacteria from positive blood cultures. BMC Microbiology. 16 (1), 185-192 (2016).
- Höring, S., Massarani, A. S., Löffler, B., Rödel, J. Rapid antimicrobial susceptibility testing in blood culture diagnostics performed by direct inoculation using the VITEK®-2 and BD PhoenixTM platforms. European Journal of Clinical Microbiology & Infectious Diseases. 38 (3), 471-478 (2019).
- Dupuis, G. Evaluation of the Cobasbact automated antimicrobial susceptibility testing system. European Journal of Clinical Microbiology & Infectious Diseases. 4 (2), 119-122 (1985).
- Liu, Y., et al. A system of bacterial antimicrobial resistance detection and its operation method. China Patent. , (2019).
- Liu, Y. A high throughput test plate for screening bacteriophage of zoonotic pathogens and its application. China Patent. , (2022).
- Adams, M. H. . Bacteriophages. , (1959).
- Nair, A., Ghugare, G. S., Khairnar, K. An appraisal of bacteriophage isolation techniques from environment. Microbial Ecology. 83 (3), 519-535 (2022).
- . . Shandong veterinary antibiotic resistance system. , (2023).
- Ming, H., et al. Comparison of the results of 96-dot agar dilution method and broth microdilution method. Chinese Journal of Antibiotics. 43 (6), 729-733 (2018).
- Laxminarayan, R., Klugman, K. P. Communicating trends in resistance using a drug resistance index. BMJ Open. 1 (2), e000135 (2011).
- Chen, Y., et al. Assessing antibiotic therapy effectiveness against the major bacterial pathogens in a hospital using an integrated index. Future Microbiology. 12, 853-866 (2017).
- Ciccolini, M., Spoorenberg, V., Geerlings, S. E., Prins, J. M., Grundmann, H. Using an index-based approach to assess the population-level appropriateness of empirical antibiotic therapy. Journal of Antimicrobial Chemotherapy. 70 (1), 286-293 (2015).
- Yanbo, L., et al. Preliminary application of inoculation system for high-throughput drug susceptibility test. China Poultry. 42 (6), 52-57 (2020).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır