Method Article
تحليل مجسم الفيديو لنقص الأكسجين الرئوي من الشرايين داخل الرئة باستخدام مورين الدقة قطع شرائح الرئة
In This Article
Summary
التهاب الأوعية الدموية الرئوية نقص الأكاكس (HPV) هو ظاهرة فسيولوجية هامة يتم من خلالها مطابقة تغلغل الرئة نقص الأكسيجة في السن الهوائية للتهوية. الجزء الوعائي الرئيسي المساهم في فيروس الورم الحليمي البشري هو الشريان داخل الأسينار. هنا، نقوم بوصف بروتوكولنا لتحليل فيروس الورم الحليمي البشري للأوعية الرئوية المورينية التي يتراوح قطرها بين 20 و100 ميكرومتر.
Abstract
نقص الأكسياج السنخي الحاد يسبب التهاب الأوعية الدموية الرئوي (HPV) - المعروف أيضا باسم آلية فون يولر-Liljestrand - الذي يعمل على مطابقة تغلغل الرئة مع التهوية. وحتى الآن، لا تفهم الآليات الأساسية فهما كاملا. الجزء الوعائي الرئيسي المساهم في فيروس الورم الحليمي البشري هو الشريان داخل الأسينار. هذا القسم الأوعية مسؤولة عن إمدادات الدم من acinus الفردية, الذي يعرف بأنه جزء من الرئة البعيدة إلى الشعب الهوائية الطرفية. تقع الشرايين داخل الأسينار في الغالب في ذلك الجزء من الرئة الذي لا يمكن الوصول إليه بشكل انتقائي من خلال عدد من التقنيات الشائعة الاستخدام مثل قياس ضغط الشريان الرئوي في الرئتين المعزولتين أو التسجيلات القوة من شرائح الشريان الرئوي القريبة تشريح1,2. يقتصر تحليل الأوعية دون الجنبية عن طريق المسح المجهري بالليزر الكونفوجال في الوقت الحقيقي على السفن التي يصل قطرها إلى 50ميكرومترا 3.
نحن نقدم تقنية لدراسة فيروس الورم الحليمي البشري من الشرايين داخل الرئة مورين في حدود 20-100 ميكرومتر الأقطار الداخلية. وهو يستند إلى التحليل المرئي للشرايين المقطعية في شرائح الرئة المقطوعة بدقة (PCLS). تسمح هذه الطريقة بالقياس الكمي ل فاسوريانيتي للشرايين الصغيرة داخل الأسينار ذات القطر الداخلي بين 20-40 ميكرومتر والتي تقع في gussets من الحاجز الحويصلات بجوار القنوات السنخية والشرايين الأكبر قبل الأسينار ذات الأقطار الداخلية بين 40-100 ميكرومتر والتي تعمل بجوار القصبات الهوائية والشعب الهوائية. على النقيض من التصوير في الوقت الحقيقي للأوعية دون الجنبية في الفئران المخدرة والتهوية ، يحدث التحليل المرئي المتبلور ل PCLS في ظل ظروف خالية من إجهاد القص. في نموذجنا التجريبي كلا القطاعين الشرياني يحمل فيروس الورم الحليمي البشري أحادي الطور عندما تتعرض للغاز المتوسط مع 1٪ O2 والاستجابة يتلاشى بعد 30-40 دقيقة في نقص الأكسيجة.
Introduction
في معظم الأسرة الوعائية الجهازية نقص الأكسيجة يحفز توسع الأوعية الدموية، بالمقارنة مع تضيق الأوعية الناجم عن نقص الأكسيجة في الأوعية الدموية الرئوية. تسمى هذه الاستجابة الخاصة بالرئة لتوتر الأكسجين المنخفض استئصال الأوعية الرئوية نقص الأكاكس (HPV) ، وت يبدأ في غضون ثوان ويعكس بسرعة بعد التبديل إلى التهوية ال نورموكسيك. على الرغم من أن فيروس الورم الحليمي البشري معروف منذ أكثر من 60 عاما ، إلا أن مستشعر الأكسجين الخلوي (أجهزة) وسلسلة الإشارات (السلاسل) التي تؤدي إلى استئصال الأوعية لا تزال قيد المناقشة. هناك إجماع واسع نسبيا على أن الأكسدة التي تثيرها نقص الأكسيا وتغييرات ROS ضرورية لفيروس الورم الحليمي البشري وتطور ارتفاع ضغط الدم الرئوي (تمت مراجعتها في Sylvester et al. 4 وشوماكر وآخرون. 5). تدعم البيانات الخاصة بنا دورا مركزيا للمعقد الثاني من سلسلة الجهاز التنفسي الميتوكوندريا في فيروس الورم الحليمي البشري6,7. مؤخرا، وانغ وآخرون. قدم مفهوم جديد تماما لاستشعار الأكسجين وفيروس الورم الحليمي البشري: استنادا إلى بياناتهم يقترحون أن نقص الأكسوجة السنفية تشعر به الشعيرات الدموية المجاورة مما يسبب إزالة الاستقطاب الغشائي للخلايا البطانية. يتم نشر الاستجابة عبر connexion 40 تقاطعات الفجوة من الخلايا البطانية مما يؤدي إلى انقباض خلايا العضلات الملساء من الشرايين المنبع8.
شرايين الرئة تعمل جنبا إلى جنب مع الشعب الهوائية، فرع معهم، وانخفاض مستمر في القطر، وأخيرا توريد الدم إلى نظام الشعرية الموجودة في الجدران الحويصلات. يتكون هذا الدوران الشرياني من أجزاء متميزة تشريحيا ووظيفيا. تتبع شرايين القناة القريبة ، التي تتميز بوفرة من الألياف المرنة في الجدران ، شرايين عضلية بالكامل داخل الرئة تتحكم إلى حد كبير في مقاومة الأوعية الدموية الرئوية. خطوة بخطوة، هذه الشرايين العبور إلى شرائح حيث تصبح طبقة العضلات غير مكتملة، وأخيرا الأوعية خالية من الخلايا النشطة مناعية العضلات الملساء. الشريان داخل acinar تغذية acinus الرئوي الفردية مع الدم يمثل جزء العضلات جزئيا6. وبالمثل، فإن الجهاز الشرياني الرئوي لا يمثل بنية موحدة فيما يتعلق بالاستجابة لنقص الأكز ولكن المعارض تميز التنوع الإقليمي9,10. على سبيل المثال ، في الشرايين الرئوية القريبة المعزولة عن قصور الأكسيجة الفئران يؤدي إلى استجابة ثنائية المراحل ، مما يعرض انكماشا سريعا أوليا لمدة قصيرة - بعد استرخاء غير مكتمل - يتبعه انكماش بطيء ثان ولكنه مستمر11. في شرايين المقاومة المعزولة عن بارنشيما الرئة الفئران كقسم الرابع والخامس من الشرايين الرئوية (القطر الخارجي <300 ميكرومتر)، نقص الأكسيجة يسبب انقباض أحادي الطور9. بالفعل في عام 1971 وخلص Glazier وموراي من قياسات التغيرات في تركيز خلايا الدم الحمراء الشعرية في رئات الأمراض التهوية مع خليط الغاز نقص الأكاكس أن الزيادة الناجمة عن نقص الأكسيجة في مقاومة الأوعية الدموية وقعت أساسا المنبع من الشعيرات الدموية12. في الوقت الحاضر ، يمثل المجهر داخل الرئتين السليمتين للفئران المخدرة والتهوية الميكانيكية أداة قوية لتحليل الخلايا المجهرية الرئوية13،14. إن استئصال نافذة دائرية في الجدار الصدري يتيح الوصول المجهري إلى سطح الرئة ويسمح بتحليل الأوعية الرئوية دون الجنبية التي يصل قطرها إلى 50 ميكرومتر. من خلال الجمع بين هذه التقنية مع ضخ FITC-dextran، تابوشي وآخرون. أظهرت أن الشرايين متوسطة الحجم فقط مع أقطار 30-50 ميكرومتر تظهر استجابة ملحوظة لنقص الأكxia التي استمرت على مدى فترة 60 دقيقة مع توهين طفيفة بعد 30 دقيقة. في المقابل، أظهرت الشرايين الصغيرة ذات أقطار 20-30 ميكرومتر استجابة طفيفة فقط لنقص الأكxia3. ومع ذلك، لا تسمح هذه التقنية بتحليل الشرايين التي يبلغ قطرها أكبر من 50 ميكرومترا نظرا لأن هذه الأوعية تقع عميقا جدا في أنسجة الرئة.
من أجل سد الفجوة في تحليل الشرايين الرئوية الكبيرة والصغيرة جدا (مثل الأوعية تحت الجنبية) من الرئتين مورين، اعتمدنا الطريقة التي وصفها مارتن وآخرون. لتحليل التفاعل من الشعب الهوائية15. استنادا إلى تقنية غرس هلام الآغروز ، فإنه يسهل إعداد شرائح الرئة المقطوعة بدقة (PCLS) من هذا العضو الناعم والمرن نسبيا. داخل شرايين PCLS العرضية مع القطر الداخلي بين 20-100 ميكرومتر يمكن ملاحظتها مباشرة عن طريق التنظير بالفيديو. يسمح تطبيق الأدوية أثناء حضانة الفينول الخماسي الكلور بتحليل آثارها على فيروس الورم الحليمي البشري. ومن الأهمية بمكان أن هذه التقنية يمكن أيضا أن تطبق على الماوس المعدلة وراثيا. بناء على موقعها داخل الرئة، ونحن نصنف الشرايين والأوعية قبل وداخل acinar، مع أقطار داخلية من 20-40 ميكرومتر و 40-100 ميكرومتر، على التوالي. تحت وجهة نظر وظيفية الشريان داخل acinar تزويد acinus الرئوية الفردية مع الدم والشريان قبل acinar هو أقسام الأوعية السابقة. تسجيل الصور على كاميرا رقمية يسمح للقياس الكمي اللاحقة من vasoreaction. سمة واضحة من هذا النموذج PCLS هو عدم وجود القص الإجهاد بناء على البطانة. في المقابل ، في الأوعية المشبعة فيروس الورم الحليمي البشري الحاد يؤدي إلى ارتفاع في إجهاد القص وبالتالي تحفيز الآليات الثانوية مثل NO release16. بالإضافة إلى ذلك ، فإن استخدام PCLS يسمح بقياسات فيروس الورم الحليمي البشري دون تأثيرات عصبية أو هرمونية خارج الرئة. على النقيض من نظم زراعة الخلايا ، على سبيل المثال أعدت من الخلايا العضلية الملساء الشريان الرئوي ال17، يتم الحفاظ على العمارة النسيجية لجدار السفينة تماما تقريبا.
وباختصار، يوفر هذا البروتوكول طريقة مفيدة لتحليل أجهزة استشعار الأكسجين الجزيئية المحتملة و / أو المسارات الخلوية المسؤولة عن فيروس الورم الحليمي البشري للشرايين داخل الرئة ذات الأقطار الداخلية بين 20-100 ميكرومتر في ظل ظروف خالية من إجهاد القص.
Protocol
1. إعداد مخاليط الغاز والمعدات والأدوات والحلول
يصف هذا القسم المعدات الضرورية وإعداد البروتوكول. يمكن العثور على تفاصيل إضافية ومعلومات الشركة المصنعة في الجدول المرفق.
- الحصول على أو تحضير مخاليط الغاز التالية:
- زجاجتين مع خليط غاز نورموكسيك تتألف من 21٪ O2،5.3٪ CO2،73.7٪ N2.
- زجاجة واحدة مع خليط غاز نقص الأكاسيك تتألف من 1٪ O2،5.3٪ CO2،93.7٪ N2.
- جمع المعدات التالية:
- فرن ميكروويف، لذوبان الآغاروز.
- خزانة التدفئة، لغسل agarose من أقسام الرئة (انظر أدناه). أدخل أنبوبا متصلا بزجاجة مع خليط غاز نورموكسيك في الخزانة.
- هزاز مع شفرات الحلاقة المناسبة، لقطع الرئتين إلى شرائح سميكة 200 ميكرومتر. ومن المفيد إذا تم تأثيث الهزاز مع مجموعة التبريد لتهدئة العازلة في حوض هزاز.
- غرفة تدفق من خلال التخبط شنت على المجهر المقلوب، لتحليل فيروس الورم الحليمي البشري من الشرايين غير الرئوية.
- لتسهيل تثبيت أقسام الرئة إلى أسفل الغرفة ، قم بتوصيل سلاسل النايلون بخاتم بلاتيني (ذاتي البناء). انضم إلى غرفة التشوه إلى مضخة مع التيار مع تعديل معدلات التدفق إلى 0.7 مل/دقيقة و6 مل/دقيقة على التوالي.
- تجميع المعدات بحيث يتم تخزين وسائل الإعلام خلال التجارب في حمام مائي 37 درجة مئوية وفقاعة مع الغاز نورموكسيك أو نقص الأكاسيد باستخدام 21 G × 4 3/4 cannulas. بالإضافة إلى ذلك استخدام اتصال ثان من زجاجة الغاز للسماح لخليط الغاز normoxic / hypoxic أن تغذيها في الفضاء الجوي للغرفة التغلغل. تأكد من أن جميع أنابيب هذا النظام هي الغاز ضيق.
- كاميرا CCD مثبتة على مجهر مقلوب مستقيم لتسجيل صور الشريان التي تم تحليلها.
- إعداد الصكوك التالية:
- لإعداد الرئتين: مجموعة تشريح معقمة بما في ذلك مقص خشن وزوجان من ملقط ، ومقص ناعم لفتح الصدر ، ومقص صغير لقطع ثقب في القصبة الهوائية لملء الأغروز ، وخياطة القطن (حوالي 20 سم) ربط القصبة الهوائية لمنع تدفق الآغروز.
- لملء الشعب الهوائية مع agarose: توصيل حقنة 2 مل إلى أنبوب بلاستيكي مرن من قنية iv indwelling (20 G x 1 1/4).
- لتشويش الرئتين مع العازلة: إصلاح حقنة 50 مل كخزان عازلة حوالي 40 سم فوق مكان العمل لإعداد الماوس.
- لتدفق العازلة: ربط المحقنة إلى أنبوب الذي يتم إرفاق 25 G × 1 قنية. استخدم المشبك في الأنبوب لضبط التدفق إلى حوالي قطرة واحدة في الثانية (حوالي 0.3-0.4 مل / دقيقة).
- تحضير المخازن المؤقتة والوسائط التالية:
- جعل 1000 مل HEPES-Ringer العازلة (10 MM HEPES، 136.4 mM NaCl، 5.6 MM KCl، 1 mM MgCl2• 6H2O، 2.2 mM CaCl2• 2H2O، 11 mM الجلوكوز، pH 7.4). تخزين المخزن المؤقت المعقم (حجم المسام من مرشح: 0.2 ميكرومتر) في 4 درجة مئوية.
- حوالي 30 دقيقة قبل البدء في عزل الرئتين إعداد الحلول التالية:
- حل 1.5٪ ث / الخامس agarose نقطة انصهار منخفضة في العازلة HEPES-Ringer (إجمالي حجم 10 مل) وتذوب عن طريق الطهي في فرن الميكروويف. بعد ذلك، تبريده إلى 37 درجة مئوية عن طريق التخزين في خزانة التدفئة. قبل الحرب حقنة 2 مل لملء agarose في الشعب الهوائية الرئوية.
- خذ 20 مل من العازل HEPES-Ringer، وأضف الهيبارين إلى تركيز نهائي يبلغ 250 I.U./ml، وسخن العازل إلى 37 درجة مئوية. مباشرة قبل الاستخدام إضافة نيتروسسايد الصوديوم إلى تركيز النهائي من 75 ميكرومتر. هذا هو حاجز التشوه للهروب من الدم من الأوعية الدموية الرئوية.
- وضع 200 مل HEPES-Ringer العازلة في كوب زجاجي وتخزينها على الجليد. ستكون هناك حاجة إلى هذا العازلة لتبريد الرئتين المعزولة المملوءة بالأغاروز.
- ملء حوالي 200 مل MEM تكملها مع 1٪ البنسلين / streptomycin في كوب زجاجي وتخزينها في 37 درجة مئوية في خزانة التدفئة. فقاعة المتوسطة مع خليط الغاز normoxic. وسوف تستخدم هذه لإزالة agarose من أقسام الرئة.
- زجاجات ما قبل الحرب 2 من MEM تكملها 1٪ البنسلين / streptomycin في حمام مائي إلى 37 درجة مئوية وفقاعة لهم مع خليط الغاز نورموكسيك ونقص الأكز، على التوالي، لمدة 2 ساعة على الأقل قبل البدء في القياسات videomorphometric. وسوف تكون هناك حاجة إلى ما يقرب من 250 مل من الميكرم المتعددة الأطراف لكل قياس.
- جمع المواد الإضافية التالية:
- 70٪ EtOH للتطهير.
- محلول الأسهم من الهيبارين (25.000 I.U./5 مل)، المخزنة في 4 درجة مئوية (انظر أعلاه).
- محلول المخزون من نيتروسسايد الصوديوم المانح NO (Nipruss): 10 mM في H2O، المخزنة على الجليد (انظر أعلاه).
- حل المخزون من الثرومبوكسان التناظرية U46619: 10 ميكرومتر في الإيثانول، المخزنة على الجليد.
- الغراء الفائق.
- خياطة القطن ربط القصبة الهوائية بعد ملء مع agarose.
2. الحيوانات
استخدام الفئران (على سبيل المثال من سلالة C57Bl6) من كلا الجنسين في سن 10-25 أسبوعا. يمكن أيضا تحليل فيروس الورم الحليمي البشري في سلالات خروج المغلوب وسلالات النوع البري المقابلة.
وقد أجريت جميع التجارب وفقا للمبادئ التوجيهية للمعهد الوطني للصحة لرعاية الحيوانات التجريبية واستخدامها، ووافقت عليها المجالس المؤسسية المحلية.
3. عزل الرئتين مورين وإعداد الدقة قطع شرائح الرئة (PCLS)
- قتل الماوس عن طريق خلع عنق الرحم. مباشرة بعد القتل، تعقيم سطح الجسم البطني مع 70٪ EtOH واستخدام مقص الخام لقطع الجلد على طول خط الوسط البطني من الذقن إلى الحوض.
ملاحظة: منذ أنه من المعروف أن التخدير استنشاق مثل ايزوفلوران لها تأثير على لهجة الأوعية الدموية18,19, لا تستخدم التخدير المتطايرة. - بعد فتح تجويف البطن، وضع الحلقات المعوية جانبا وقطع الأوعية البطنية الكبيرة للنزيف. بعد اختراق الحجاب الحاجز بالمقص الدقيق ، ستنهار الرئتين نتيجة لدخول الهواء إلى التجويف الجنبي. استخدم المقص لفصل الحجاب الحاجز عن فتحة الصدر السفلية. قطع الأضلاع والقعقعة أفقيا لإزالة الجزء البطني من القفص مزق.
ملاحظة: من المهم أن لا تتلف الرئتين في هذه الخطوة لأن الانتفاخ خلاف ذلك من الرئتين مع agarose سيكون من المستحيل! استخدم أدوات معقمة وأدوات زجاجية معملية فقط. - قبل البدء في تغلغل الأوعية الدموية الرئوية ، قطع ثقب صغير في البطين الأيسر للقلب لتفريغ العازلة. ملء خزان حقنة مع الحارة (37 درجة مئوية) HEPES-Ringer العازلة التي تحتوي على الهيبارين والصوديوم نيتروبروسسايد (عازلة التغلغل) وثقب الأوعية الدموية الرئوية ببطء عن طريق البطين الأيمن.
ملاحظة: التغلغل فعال عندما تغير الرئتين لونهما وتحصل على مظهر أبيض. في هذه الخطوة من المهم إضافة نيتروسسايد الصوديوم في المخزن المؤقت للتشويش؛ وهذا يمنع الشرايين ما قبل الأسينار من تمزيق من الأنسجة المحيطة بها. - إزالة الغدد اللعابية والعضلات الصغيرة والأنسجة الضامة من القصبة الهوائية. فصل القصبة الهوائية من النسيج الضام المحيطة والخيط خياطة القطن بين المريء والرغامى ربط في وقت لاحق.
- استخدام microscissor لقطع ثقب صغير في الجزء العلوي من القصبة الهوائية بين اثنين من الغضاريف القصبة الهوائية المجاورة. الآن إدراج أنبوب من البلاستيك مرنة من قنية iv indwelling عبر ثقب صغير في القصبة الهوائية وإصلاحه بعناية مع القطن الخياطة. ملء ببطء الشعب الهوائية مع الحارة (37 درجة مئوية) نقطة انصهار منخفضة agarose. مراقبة الرئتين: في البداية تبدأ الرئة اليمنى في التوسع تليها الرئة اليسرى. يتم إكمال التعبئة عندما يتم تضخيم كلتا الرئتين إلى حجم مماثل للحالة في الجسم الحي (حوالي 1.2-2.0 مل اعتمادا على الجنس والعمر والوزن).
ملاحظة: إذا توسعت رئة واحدة فقط، فقد يكون الأنبوب البلاستيكي قد تم إدخاله عميقا جدا بحيث يصل إلى الشعب الهوائية. في هذه الحالة، يجب أن يتم سحبها قليلا. نضع في اعتبارنا أن الآغاروز سوف تصلب عندما يبرد تدريجيا. - عندما تمتلئ الرئتين، في وقت واحد سحب الأنابيب البلاستيكية وligate القصبة الهوائية مع القطن الخياطة لمنع تدفق من agarose. في وقت لاحق، وقطع القصبة الهوائية فوق الرباط وفصل الرئتين والقلب على كتلة من الصدر.
ملاحظة: للمبتدئين، قد يكون من المفيد أن تطلب من زميل الدعم في خطوة الربط. - نقل حزمة الجهاز إلى الجليد الباردة HEPES-Ringer العازلة لترسيخ agarose. يحدث هذا في غضون بضع دقائق.
- فصل فصوص الرئة الفردية وإصلاح فص واحد مع superglue على حامل عينة من الهزاز.
ملاحظة: من المفيد أن تلصق قطعة من فلين الشمبانيا على حاملها والتي تعمل كحرف أثناء قطع أنسجة الرئة المرنة. اعتمادا على فص الرئة المستخدمة وعلى اتجاهه على حامل العينة، قد يكون PCLS التي تم الحصول عليها أكثر ملاءمة لتحليل الأوعية الصغيرة أو الكبيرة. في الغالب نستخدم الفص الأيسر والفص القحفي الأيمن لإعداد PCLS. للحصول على الشرايين الصغيرة المقطعة داخل الأسينار ، قم بلصق الفص الأيمن القحفي مع المقبض إلى الحامل وشريحة من المحيط. للحصول على شرايين مقطعة قبل الأسينار، قم بمحاذاة هيلوم الفص الأيمن مع فلين الشمبانيا. - استخدم هزازا مجهزا بشفرة حلاقة جديدة لقطع فص الرئة إلى شرائح سمكها 200 ميكرومتر (السرعة: 12 = 1.2 مم /ثانية؛ التردد: 100؛ السعة: 1.0). جمع PCLS في حوض هزاز مليئة 4 درجة مئوية الباردة HEPES-Ringer العازلة.
ملاحظة: ينصح بتبريد HEPES-Ringer ولكن غير ضروري. - لإزالة agarose، نقل أقسام الجهاز في كوب زجاجي مليئة حوالي 200 مل 37 درجة مئوية MEM الحارة. وضع الكأس في خزانة التدفئة التي أنبوب انضم إلى زجاجة مع خليط الغاز normoxic يتم إدراجها. فقاعة MEM مع الغاز normoxic بحيث أقسام الرئة تتحرك ببطء في المتوسط. بعد حوالي 2 ساعة ، سيتم إزالة "لويحات الآغاروز" التي تملأ المجال الجوي من أنسجة الرئة. ويمكن التعرف على ذلك من خلال حقيقة أن الأقسام لم تعد تسبح في الجزء العلوي من الوسط ولكنها تستقر في الجزء السفلي من الكأس.
4. تحليل فيديومورمومتري من الشرايين Intrapulmonary من PCLS
- للتحليل المرئي المتبلور للشرايين داخل الرئة، قم بنقل PCLS واحد إلى غرفة التدفق من خلال التخبط الفائق المليئة ب 1.2 مل من MEM الغازية normoxic. إصلاح PCLS في الجزء السفلي من الغرفة مع سلاسل النايلون متصلة حلقة البلاتين (القطر الخارجي / الداخلي: 14/10 ملم).
- مسح PCLS مجهريا للشرايين المقطعية ذات الأقطار الداخلية بين 20-100 ميكرومتر.
ملاحظة: تصطف تجويف الشرايين بواسطة خلايا البطانية المسطحة. يمكن تحديد خلايا العضلات الملساء المحيطة في صورة تباين المرحلة على أنها "حلقة داكنة" تحيط بالتشحيم (انظر صور تباين المرحلة في الشكل 2). في المقابل ، يمكن تحديد الشعب الهوائية من خلال ظهارة العمود الزائفة في البداية التي تعبر في الطريق إلى السطح الجنبي إلى ظهارة عمود بسيطة تليها ظهارة صغيرة بسيطة.- قياس القطر الداخلي في بداية كل تجربة.
ملاحظة: في الأوعية المقطوعة بشكل غير مباشر قليلا ، يمكن تحديد القطر الداخلي الحقيقي للبنية الأنبوبية بزاوية 90 درجة إلى أطول محور لللمن. شرايين كبيرة قبل الأسينار ذات أقطار داخلية >40 ميكرومتر تعمل بجوار القصبات الهوائية والشعب الهوائية. وتقع الشرايين الصغيرة داخل acinar مع القطر الداخلي <40 ميكرومتر في gussets من الحاجز السنفي بجوار الحويصلات والقنوات الحويصلات6.
- قياس القطر الداخلي في بداية كل تجربة.
- التصميم التجريبي:
- ابدأ كل تجربة ب "مرحلة تكيف" يتم فيها تغلغل الغرفة مع وسيط غاز نورموكسيك (معدل التدفق: 0.7 مل/دقيقة؛ 10 دقائق). بعد ذلك، اختبر صلاحية الوعاء: تحليل انقباض الشريان بإضافة 12 ميكرولتر من 10 ميكرومتر U46619 (التركيز النهائي 0.1 ميكرومتر؛ 10 دقائق؛ بدون تدفق).
ملاحظة: بالنسبة لهذا العمل، يتم تعريف السفينة بأنها قابلة للحياة عندما يتم تقليل المساحة الإنارة بنسبة 30٪ على الأقل (لطريقة القياس انظر أدناه). - بعد غسل الدواء مع normoxic الغاز المتوسط (معدل التدفق: 6 مل / دقيقة؛ 10 دقيقة) توسيع الشريان عن طريق تطبيق 3 ميكرولتر من 10 mM Nipruss (التركيز النهائي 25 ميكرومتر؛ 10 دقيقة؛ لا تدفق).
- مرة أخرى، إزالة الدواء عن طريق غسل 10 دقيقة مع نورموكسيك الغاز المتوسط (معدل التدفق: 6 مل / دقيقة) تليها 10 دقيقة في تدفق 0.7 مل / دقيقة.
- حث احتقان الأوعية الرئوية نقص الأكاكس عن طريق حضانة PCLS مع وسيطة الغاز نقص الأكاكس (معدل التدفق: 0.7 مل / دقيقة؛ 40 دقيقة). بواسطة نظام أنبوب إضافي، تغذية خليط الغاز hypoxic في الفضاء الجوي للغرفة التغلغل.
- إزالة المتوسطة hypoxic عن طريق غسل 20 دقيقة مع وسيطة الغاز normoxic (معدل التدفق: 6 مل / دقيقة).
- في نهاية كل تجربة، أضف 1.2 ميكرولتر من 10 ميكرومتر U46619 (التركيز النهائي 0.01 ميكرومتر؛ 20 دقيقة؛ لا تدفق) إلى غرفة التشوه للحث على استئصال الأوعية.
ملاحظة: تسمح هذه الخطوة الأخيرة بتحديد ما إذا كان التغيير في الاستجابة نقص الأوكسي (على سبيل المثال الناجم عن التطبيق المتزامن لعقار في مرحلة نقص الأكسيد أو الملاحظ في PCLS المعد من سلالة فأرة خروج المغلوب) محددا للانقباض الناجم عن نقص الأكسيجة أو ما إذا كان يعكس تأثيرا عاما على الانقباض. ويتوافق تركيز 0.01 ميكرومتر مع قيمة EC50 ل U46619 التي قدرت في قياسات انكماش التركيز السابقة (غير المنشورة). - استخدام PCLS آخر لإجراء تجارب التحكم مع normoxic بدلا من MEM الغاز hypoxic وخليط الغاز normoxic في الفضاء الجوي للغرفة perfusion.
- ابدأ كل تجربة ب "مرحلة تكيف" يتم فيها تغلغل الغرفة مع وسيط غاز نورموكسيك (معدل التدفق: 0.7 مل/دقيقة؛ 10 دقائق). بعد ذلك، اختبر صلاحية الوعاء: تحليل انقباض الشريان بإضافة 12 ميكرولتر من 10 ميكرومتر U46619 (التركيز النهائي 0.1 ميكرومتر؛ 10 دقائق؛ بدون تدفق).
5. تحليل فاسوريتيتي وعرض بياني
- باستخدام برامج مناسبة التقاط الصور من الشريان المقطعة كل دقيقة خلال التجربة بأكملها.
- باستخدام برنامج مناسب تقييم التغيرات في المنطقة الإنارة من السفن عن طريق بطانة الحدود الداخلية باليد باستخدام صور ملء الشاشة.
ملاحظة: يكفي تحليل كل صورة ثانية للحصول على رسوم بيانية واضحة. ومع ذلك، عندما يتم تغيير شرط واحد في غرفة التدفق من خلال التخبط إلى آخر، وتحليل كل صورة. الصور المتبقية بمثابة احتياطية في حالة صورة واحدة لا يمكن تحليلها.
لسوء الحظ ، يجب أن تتم هذه الخطوة المستهلكة للوقت باليد وليس عن طريق البرامج المناسبة لأن خلايا الدم في بعض الأحيان متصلة بجدار الأوعية الدموية التي تتحرك أثناء القياس أو أنها ليست مقطعا عرضيا مثاليا من السفينة ولكن قسما عرضيا لا يمكن فيه إجراء توطين موثوق للحدود الداخلية إلا تحت التحكم البصري. - تحديد القيمة التي تم الحصول عليها لمنطقة تجويف السفينة في بداية التجربة على أنها 100٪ والتعبير عن تضيق الأوعية أو التمدد على أنه انخفاض نسبي أو زيادة في هذه القيمة.
- لكل تجربة رسم المنطقة الإنارة النسبية مع الزمن باستخدام البرامج المناسبة.
- لتلخيص عدة تجارب، رسم وسائل المناطق الإنارة النسبية +/- خطأ قياسي من المتوسط (SEM) مع مرور الوقت.
ملاحظة: للحصول على عرض واضح لآثار المواد المختلفة على نقص الأكسوجة - أو U46619 الناجم عن التهاب الأوعية الرئوية أو الاستجابة نقص الأكاكس لسلالات الماوس بالضربة القاضية ، يمكن حذف المرحلة الأولية من التجارب ، التي يتم فيها اختبار صلاحية السفينة ، من الرسم البياني. في هذه الحالة، يتم تعريف القيم التي تم الحصول عليها في بداية التعرض لانخفاض الأكسجين بنسبة 100٪.
6. التحليل الإحصائي
- تحليل الاختلافات بين المجموعات التجريبية مع Kruskal واليس - ومان ويتني الاختبار ، مع p≤0.05 تعتبر كبيرة ، وp≤0.01 كبيرة للغاية.
ملاحظة: للحصول على معلومات إضافية حول إعداد واستخدام العمليات من PCLS انظر أيضا20,21.
النتائج
في الشكل 1 يتم إعطاء نتائج قياس فيروس الورم الحليمي البشري من الشريان قبل الأسينار كبيرة وفي الشكل 2 من الشرايين داخل acinar الصغيرة. في صور النقيضالمرحلة (الشكلان 1A و 2A)يصبح من الواضح أنه من الممكن التمييز بين هاتين الفئتين من الشرايين استنادا إلى موقعها داخل أنسجة الرئة: الشرايين ما قبل الأسينور تعمل في حي قريب من القصبات الهوائية والشعب الهوائية (الشكل 1A) ، في حين تقع الشرايين داخل الأسينار في gussets من الحاجز السنخي وتحيط بها الحويصلة الهوائية (الشكل 2A). مع القليل من الممارسة فمن الممكن أن نرى التغييرات في المنطقة الإنارة استجابة لU46619 على صور النقيضالمرحلة (الشكلين 1A و 2A). ومع ذلك، غالبا ما يكون التهاب الأوعية الرئوية hypoxic غير واضح ويصبح واضحا إلا بعد التقييم الكامل للتغيرات في المناطق الإنارة(الشكل 1B، 1C، 2B، و، 2C). لسبب تعليمي أعطينا مثالا على الشريان قبل acinar الذي يظهر تضيق الأوعية وضوحا بشكل غير عادي. في المتوسط، يؤدي فيروس الورم الحليمي البشري إلى انخفاض بنسبة 20-30٪ في المنطقة الإنارة.
في الشكل 2 تظهر تسجيلات الشرايين الصغيرة داخل الأسينار المحتضنة بوسيطة غازية نقص الأكاكس مع أو بدون 50 ميكرومتر بيناسيديل (فتاحة غير انتقائية لقنوات البوتاسيوم الحساسة ل ATP الميتوكوندريا) ويصبح التأثير المثبط للدواء مرئيا بوضوح. الجزء الأخير من التجربة يدل على انتقائية عمل الدواء على فيروس الورم الحليمي البشري: لا يتم تغيير استئصال الأوعية الناجم عن الجلطات التناظرية U46619 بإضافة pinacidil. في الواقع ، فإن منحنى الشريان كشف pinacidil يعمل أقل بشكل واضح من الاثنين الآخرين ، ولكن مدى انخفاض المنطقة الإنارة بواسطة U46619 وحده قابل للمقارنة. في هذه الحالة كان الارتداد غير الكامل لفيروس الورم الحليمي البشري هو الذي يسبب الفرق بين المنحنيات. في هذا الرسم البياني أيضا يتم تضمين الشريان المعرضة للوسط الغاز normoxic كتحكم إضافي. في ظل هذه الحالة، لا يمكن الكشف عن أي تغييرات في المنطقة الإنارة.
في الشكل 3 تظهر بيانات السلسلة الكاملة من القياسات حول تأثير pinacidil على فيروس الورم الحليمي البشري. وللمقارنة بين المجموعتين للاختلافات الإحصائية، تم تحليل مجموعات البيانات الخاصة بالنقاط الزمنية المشار إليها باستخدام اختبار كروسكال واليس واختبار مان ويتني. تم إلغاء فيروس الورم الحليمي البشري بوضوح في وجود pinacidil في حين أن الانكماش الناجم عن U46619 لم يتغير.
وبدلا من ذلك، يمكن تحديد الاختلافات بين المجموعات بالمقارنة مع المنطقة الواقعة تحت المنحنى كما هو موضح في مولر - ريدتزكي وآخرين. 22
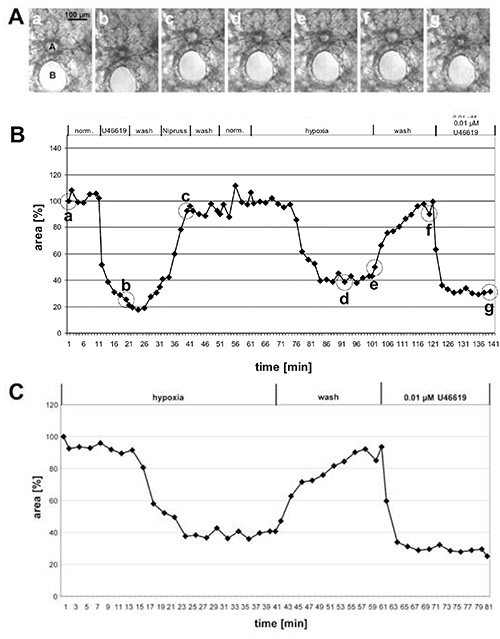
الشكل 1 - الأرقام 1- الأرقام 1 قياس فيروس الورم الحليمي البشري من الشريان قبل الأسينار كبيرة. (أ) صور التباين المرحلي من الشريان قبل acinar مقطعة (أ) الذي يمتد في حي قريب من الشعب الهوائية المقطعة(B). يتم التقاط الصور في النقاط الزمنية المشار إليها في (B) من قبل دوائر: في بداية القياس (أ)، في نهاية العلاج مع U46619 (ب)، في نهاية التعرض لNipsruss (ج)، بعد 30 أو 40 دقيقة في المتوسط الغازي نقص الأكاسيد (د، ه)، بعد الغسيل مع وسيط الغازات الترموكسية (و)، وبعد التطبيق النهائي للU46619 (ز). في الرسم البياني(B)يتم رسم تغييرات المنطقة الإنارة مع الوقت في حين يتم تعريف المنطقة الإنارة في بداية التجربة على أنها 100٪ ويتم إعطاء التمدد الوعائي / التمدد كقيم نسبية. في هذه الحالة نقص الأكسيجة يؤدي إلى انخفاض 60٪ من المنطقة الإنارة. (ج)للحصول على عرض أوضح للاستجابة نقص الأكز، لم يتم تضمين المرحلة الأولية من التجربة التي تم اختبار فاسوريتشيتيك، ولكن القيمة التي تم الحصول عليها مباشرة قبل التعرض لانخفاض الأكسجين يتم تعيين 100٪ (انظر أيضا الشكل 2). انقر هنا لعرض صورة أكبر.
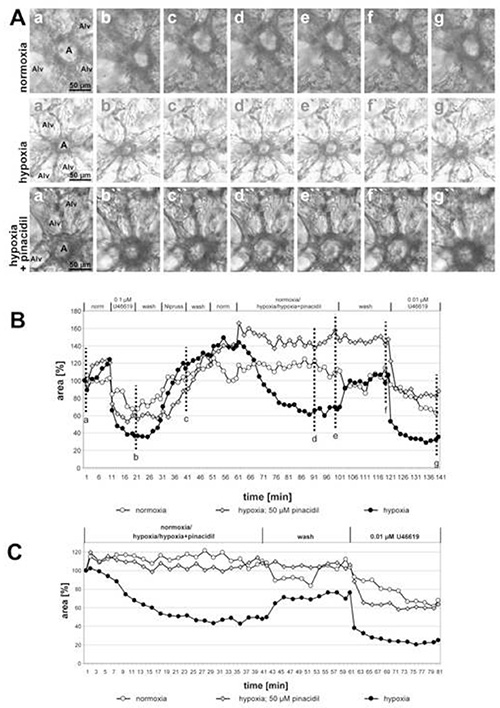
الشكل 2 - الأرقام 2- الأرقام التي تم تأثير pinacidil (فتاحة غير انتقائية من قنوات البوتاسيوم الحساسة ATP الميتوكوندريا؛ ميتوكاتب) على فيروس الورم الحليمي البشري من الشرايين الصغيرة داخل الأسينار. (أ)تقع الشرايين داخل acinar (أ) في gussets من الحاجز الحويصلات. ألف = الحويصلات. وترد تسلسل الشروط الفردية المطبقة في هذه التجارب في العنوان الرئيسي للرسم البياني(ب). يتم تنفيذ التعرض لنقص الأكسيد في وجود أو عدم وجود 50 ميكرومتر بيناسيديل. تتم حضانات التحكم مع وسيطة الغاز normoxic. يتم التقاط الصور المبينة في (A) في بداية القياس (أ، أ،أ))، في نهاية العلاج مع U46619 (ب، ب'، ب")، في نهاية التعرض ل Nipruss (c, c', c")، بعد 30 أو 40 دقيقة في وسط الغاز نقص الأكاسيد أو نورموكسيك (د، د،د"؛ ه، ه،ه")، بعد غسل مع وسيط الغاز normoxic (و، و'، و")، وبعد التطبيق النهائي لU46619 (ز، g'، g"). للحصول على عرض أوضح للاستجابة ل normoxia / نقص الأكسيجة / نقص الأكسيجة + pinacidil ، يتم تعيين القيم التي تم الحصول عليها مباشرة قبل التعرض للوسط normoxic / hypoxic الغاز بنسبة 100 ٪ (C). انقر هنا لعرض صورة أكبر.
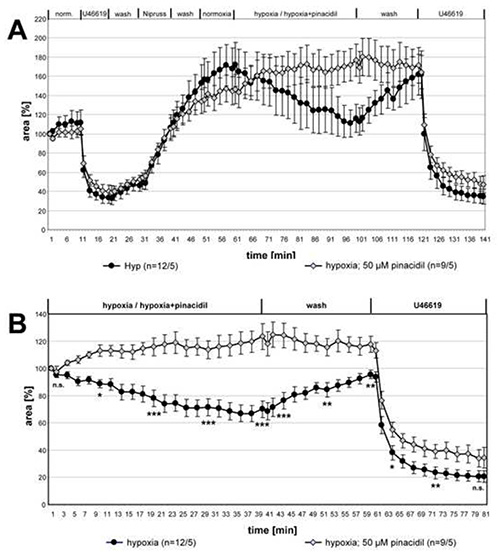
الشكل 3 - الأرقام 3- الأرقام التي يمكن أن تثبيط فيروس الورم الحليمي البشري عن طريق pinacidil. يتم تلخيص وتسجيلات الشرايين الصغيرة داخل الأسينار المعرضة لوسط غازي نقص الأكدمة مع أو بدون pinacidil 50 ميكرومتر وتقدم كوسيلة ± SEM. في (أ) يتم إعطاء التسجيلات الكاملة ، في (ب) تظهر البيانات النسبية فيما يتعلق بالقيمة في بداية الحضانة نقص الأكز. لا يمكن الكشف عن النشاط الوعائي في PCLS التي تتعرض لوسط hypoxic الغازية التي تحتوي على pinacidil. لا يتأثر استئصال الأوعية الناجم عن U46619 بالمخدرات. "n" بين قوسين يشير إلى عدد الشرايين / عدد الحيوانات التي تم صنع PCLS منها. وبعبارة أخرى، يصف الرقم الأول عدد أقسام الرئة التي تم تحليلها، ويعطي الرقم الثاني عدد الفئران التي تم إعداد هذه الأقسام منها. في الوقت المحدد نقاط يتم اختبار الاختلافات بين المجموعتين لأهمية. n.s.: ليست كبيرة، *: p≤0.05، **: p≤0.01، ***: p≤0.001. انقر هنا لعرض صورة أكبر.
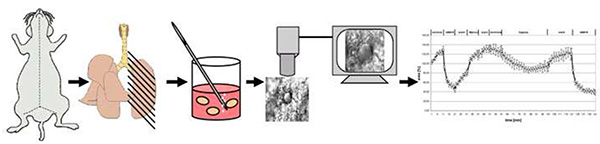
الشكل 4 - الأرقام 4- الأرقام التي تم ال نظرة عامة تخطيطية للطريقة. لفترة وجيزة، يتم قتل الفئران عن طريق خلع عنق الرحم. بعد فتح الصدر، تمتلئ الرئتين مع agarose نقطة انصهار منخفضة وبعد تهدئة خفض إلى 200 ميكرومتر قطع شرائح الرئة الدقة سميكة (PCLS). بعد إزالة agarose في 37 درجة مئوية يتم نقل PCLS واحد في غرفة التدفق من خلال التخبط الذي يتعرض للوسط normoxic أو الغاز المتوسط مع 1٪ O2. يتم تسجيل Vasoreactivity كتغيرات في المنطقة الإنارة. انقر هنا لعرض صورة أكبر.
Discussion
الرئة الماوس التهوية والمتغلغلة معزولة هو نموذج ممتاز لتحليل الاستجابة الفسيولوجية للنظام الأوعية الدموية الرئوية على التغيرات في إمدادات الأوكسجين وغيرها يسمح للقياس المستمر للضغط الشرياني الرئوي1. ومع ذلك، لا يسمح هذا النموذج بتحديد وتحليل تلك القطاعات الوعائية (القطاعات) التي تظهر أقوى استجابة لنقص الأكسيجة. هذه هي ميزة تحليلنا المرئي للمجسم PCLS الذي يسهل قياس فيروس الورم الحليمي البشري للشرايين الفردية ذات الأقطار الداخلية من 20-100 ميكرومتر. وعلى النقيض من أنظمة زراعة الخلايا، فإن جميع أنواع الخلايا موجودة في تكوينها الأصلي لمصفوفة الأنسجة. وعلاوة على ذلك، رئة واحدة كافية لإعداد العديد من PCLS، بحيث يمكن على الأقل جزئيا التجارب يمكن توحيدها باستخدام أقسام من نفس الماوس. وفقا لمفهوم 3R (الحد من وصقل واستبدال الحيوانات المختبرية في علوم الحياة) من راسل و بورش23 هذه الحقيقة يجادل أيضا لاستخدام PCLS.
ومع ذلك ، يجب على المرء أن نضع في اعتبارنا ، أن الأنسجة معطوبة عن طريق القطع مع الهزاز والإشارات الطولية على سبيل المثال عن طريق الخلايا البطانية كما افترض كوبلر وآخرون. 14 لم يعد ممكنا.
في البداية ، تم تطبيق PCLS بشكل رئيسي للدراسات الكيميائية الحيوية والصيدلانية والسمية ، ولكن في هذه الأثناء يتم استخدامها أيضا لقياس انقباض الشعب الهوائية ، ووظيفة المخاض واستجابات الأوعية الدموية (للمراجعة انظر Sanderson20 و Davies21). عقد وآخرون. وقد أجريت دراسة التي قارنت نماذج الرئة الماوس المتغلغلة والتهوية معزولة وPCLS24. ووجدوا من خلال تحليل استجابات الشعب الهوائية والأوعية الرئوية لمجموعة متنوعة من الوسطاء الداخليين أن الخصائص الهامة للرئة بأكملها تم الحفاظ عليها في PCLS.
في PCLS ، لا يتم إنشاء حالات نقص الأكز عبر الشعب الهوائية كما هو الحال في الرئة السليمة ولكن عن طريق حضانة قسم الرئة في الوسط المصاب بنقص الأكز الغازي. قمنا بتحليل ضغط الأكسجين الجزئي (pO2)من الغازات المسبقة المتوسطة مع 1٪ O2، 5.3٪ CO2، 93.7٪ N2 ومع 21٪ O2، 5.3٪ CO2، 73.7٪ N2، على التوالي ، باستخدام محلل غاز الدم. مباشرة قبل إطعامه في غرفة التشويش ، كان PO2 من MEM الغازي نقص الأكاسيد 40 مم زئبق ومتوسط 160 مم زئبق6. في الرئة سليمة يحدث فيروس الورم الحليمي البشري عندما يسقط PO2 السنفي أقل من 50 ملم زئبق25، وهو الوضع الذي يمكن أن يحاكي بوضوح عن طريق تطبيق وسيط نقص الأكز والغاز. تتطابق بياناتنا حول مدى فيروس الورم الحليمي البشري بشكل جيد مع النتائج التي تم الحصول عليها باستخدام نهج تجريبي مختلف. ياماغوتشي وآخرون. وقد طبقت الرئتين الفئران معزولة لفحص microvessels مع قطرها من 20-30 ميكرومتر عن طريق الليزر confocal في الوقت الحقيقي المسح المجهري التلألؤ مقرونة كاميرا عالية الحساسية مع صورة مكثف10. ولاحظوا انخفاضا متوسطا في القطر قدره 2.7 ميكرومتر بعد تعرض الرئتين لنقص الأكسيجة. يمكن للمرء أن يحسب أن انخفاض 20٪ من المساحة الإنارة ونحن نقيسها في نظامنا يتوافق مع حوالي 15٪ انخفاض في القطر.
في تجاربنا قمنا بتصنيف الشرايين على أنها أوعية ما قبل وداخل الأسينار ، على التوالي ، بأقطار داخلية تتراوح بين 40-100 ميكرومتر و 20-40 ميكرومتر. في البشر يحدث الانتقال من الشرايين العضلية إلى غير العضلية في نطاق قطر 70-100 ميكرومتر. في الفئران ، وخلايا العضلات الملساء موجودة وصولا الى قطر خارجي قدره 20 ميكرومتر26. لهذا السبب فإنه ليس من الممكن لتحليل الشرايين مع أقطار أقل من 20 ميكرومتر لأنها لا يمكن الاعتماد عليها يمكن تحديدها على أساس صورة النقيض المرحلة. في الطرف الآخر من المقياس ، لا يكاد تجد الأوعية التي يزيد قطرها عن 100 ميكرومتر في PCLS ويتم تجريدها عادة من الأنسجة المحيطة بها.
في الواقع ، تتم مناقشة عدد من المرشحين الجزيئية كمستشعر (أجهزة) الأكسجين الجزيئي أو كعنصر من سلسلة الإشارات الناتجة عن فيروس الورم الحليمي البشري (للمراجعة انظر Sylvester et al. 4). مرة واحدة مناسبة الفئران خروج المغلوب المتاحة يمكن استخدامها videomorphometry لتحليل vasoreactivity من الشرايين قبل وداخل acinar بالمقارنة مع الحيوانات البرية نوع. ومع ذلك، تم استخدام PCLS أيضا لقضايا أخرى: فارو وآخرون. استخدمت لهم لتوصيف تطور تمدد التمدد المعتمد على الانثيوم في الرئة بعد الولادة29 واستخدمت PCLS المعدة من الخنازير الغينية المعرضة للدخان أو الهواء يوميا لمدة 2 أسابيع لإثبات تأثير دخان السجائر على النشاط الوعائي عن طريق تحريض الخلل البطاني30.
الخطوات الهامة داخل البروتوكول
في تجاربنا صنفنا الشرايين على أنها ما قبل الأسينار (أقطار داخلية من 40-100 ميكرومتر) وداخل الأسينار (أقطار داخلية من 20-40 ميكرومتر). خاصة بالنسبة لإعداد أقسام الرئة التي ينبغي استخدامها لتحليل الأوعية الكبيرة من المهم إضافة نيتروسسايد الصوديوم إلى العازلة التغلغل. يمنع هذا الدواء تقلص الأوعية أثناء إعداد العينة وبالتالي تمزقها من الأنسجة المحيطة مما يؤدي إلى توسع الأوعية غير المكتمل. نيتروبروسايد الصوديوم في العازلة perfusion ليست مهمة جدا لإعداد قسم الرئة التي ينبغي استخدامها لتحليل الشرايين الصغيرة لأنها راسية بقوة إلى الحاجز السنفي.
يجب أن تبدأ جميع التجارب مع الحضانات التي يتم اختبار التفاعل من الشرايين. نادرا ما حصلنا على تحضيرات الرئة التي لم يكن من الممكن اكتشاف استجابة الأوعية للمتعاقدين أو المتوسعات. نحن لا نعرف السبب في ذلك: قد يكون حجم الآغاروز شغلها في الرئتين كانت كبيرة جدا أو منخفضة جدا بحيث قطع الجهاز إلى PCLS لم يكن الأمثل. بدلا من ذلك ، يمكن تخيل أن الآغروز كان يبرد بسرعة كبيرة أثناء إجراء التقطير مما أدى إلى إجهاد القص الضار. في حالة أنه في PCLS الفردية لا يوجد شريان قابل للحياة يمكن الكشف عنها، يجب التخلص من القسم واستبداله واحد آخر.
تم اتخاذ القرار بشأن صلاحية الشريان بناء على الاستجابة ل U46619. تطبيق U46619 بتركيز 0.1 ميكرومتر يحفز تضيق الأوعية الذي - بعد بعض التمارين الرياضية - مرئي مباشرة في تسلسل الصورة على الشاشة. نظرا لوجود بعض التباينات في النشاط الوعائي ، فإننا نحقق في تأثير الدواء على فيروس الورم الحليمي البشري عن طريق قياس vasoresponse في أقسام الرئة المعرضة للدواء أو للوسط وحده بدوره.
فيروس الورم الحليمي البشري من الشريان الفردي غالبا ما يكون بالكاد يمكن الكشف عنها في المجهر، وفي المتوسط يؤدي إلى الحد من المنطقة الإنارة من حوالي 20-30٪. ومع ذلك ، فإن التغيرات الصغيرة في قطر الشريان لها مدخلات متميزة على مقاومة التدفق. وفقا لمعادلة "R = 1/r4" مع R = المقاومة و r = نصف قطرها ، فإن مقاومة التدفق تتناسب عكسيا مع القوة الرابعة لنصف القطر. اسمحوا لي أن أعطي مثالا: "الشريان المثالي" الذي يعرض مقطع عرضي دائري يبلغ قطره 40 ميكرومتر (r = 20 ميكرومتر) تبلغ مساحته الإنارة حوالي 1260 ميكرومتر2. عندما يتم تخفيض المساحة الإنارة بنسبة 20٪، يمكننا حساب أن قطر السفينة ينخفض بنسبة 10.5٪ إلى 35.8 ميكرومتر (ص = 17.9 ميكرومتر). وفقا للمعادلة المذكورة أعلاه، فإن مقاومة تدفق هذه السفينة زيادة من 6.25 × 10-6 إلى 9.71 × 10-6 وهذا هو بنحو 55٪. في حالة انخفاض مساحة الإنارة بنسبة 30٪ سينخفض نصف القطر بنحو 16٪، ولكن مقاومة التدفق ستزيد بنحو 100٪. على الرغم من أن هذه الحسابات هي تبسيط مفرط حيث يفترض تدفق الدم صفح وشكل وعاء من أنبوب جامدة أنه يوحي بتأثير تغييرات طفيفة بالفعل من القطر على مقاومة التدفق.
Disclosures
ليس لدى المؤلفين ما يكشفون عنه.
Acknowledgements
هذا البحث برعاية نظام التميز العنقودي لأمراض القلب والرئة.
Materials
| Name | Company | Catalog Number | Comments |
| Vibratome "Microm HM 650 V" | Microm/Thermo Fisher Scientific, Schwerte, Germany | ||
| Microwave oven | Bosch, Frankfurt, Germany | HMT 702C | |
| Heating cabinet | Heraeus/Thermo Fisher Scientific, Schwerte, Germany | ||
| Flow-through superfusion chamber | Hugo Sachs Elektronik, March, Germany | PCLS-Bath Type: 847 SN:4017 | |
| Upright inverted microscope equipped with 4X, 10X, 20X, and 40X objectives | Leica, Wetzlar, Germany | ||
| CCD-camera | Stemmer Imaging, Puchheim, Germany | ||
| Peristaltic pump Minipuls 3 | Gilson, Limburg-Offheim, Germany | ||
| Water bath “Universal Wasserbad Isotem 205” | Thermo Fisher Scientific, Schwerte, Germany | 9452450 | |
| Gas tight tubes Tygon R3603-13 Øi: 3/32 in, Øa: 5/32 in, wall: 1/32 in | VWR, Darmstadt, Germany | ||
| Various scissors and forceps | |||
| Sewing cotton | |||
| 2 ml Syringe | Braun-Melsungen AG, Melsungen, Germany | ||
| 50 ml Syringe | Braun-Melsungen AG, Melsungen, Germany | ||
| Flexible plastic pipe of an IV indwelling cannula “IntrocanR-W” (cannula 20 G x 1 ¼ in, 1.1 x 32 mm) | Braun-Melsungen AG, Melsungen, Germany | 4254112B | For instillation of the agarose into the lung |
| Cannula 21 G x 4 ¾ in; 0.8 x 120 mm | Braun-Melsungen AG, Melsungen, Germany | 4665643 | For bubbling of the medium |
| Cannula Nr. 17, 24 G x 1, 0.55 x 25 mm | Terumo, Eschborn, Germany | NN 2425 88DSF18 | For lung perfusion |
| Normoxic gas mixture (21% O2, 5.3% CO2, 73.7% N2) | Linde, Hildesheim, Germany | ||
| Hypoxic gas mixture (1% O2, 5.3% CO2, 93.7% N2) | Linde, Hildesheim, Germany | ||
| HEPES | Sigma, Deisenhofen, Germany | H 4034 | |
| NaCl | Roth, Karlsruhe, Germany | 3957.1 | |
| KCl | Merck, Darmstadt, Germany | 1.04936.0500 | |
| MgCl2•6H2O | Merck, Darmstadt, Germany | 1.05833.0250 | |
| CaCl2•2H2O | Merck, Darmstadt, Germany | 1.02382.0500 | |
| Glucose D-(+) | Sigma, Deisenhofen, Germany | G 7021 | |
| Low melting point agarose | Bio-Rad, Munich, Germany | 161-3111 | |
| Heparin-sodium | Ratiopharm, Ulm, Germany | 5120046 | |
| Phenolred-free minimal essential medium (MEM) | Invitrogen, Darmstadt, Germany | 5120046 | |
| 70% EtOH for desinfection | Stockmeier Chemie, Dillenburg, Germany | ||
| Superglue | UHU, Bühl/Baden, Germany or from a supermarket | ||
| U46619 (a thromboxane analog) | Calbiochem/Merck, Darmstadt, Germany | 538944 | |
| Sodium nitroprusside (Nipruss) | Schwarz Pharma, Monheim, Germany | 5332804 | |
| Optimas 6.5 software | Stemmer, Puchheim, Germany | ||
| SPSS 19 | AskNet, Karlsruhe, Germany |
References
- Weissmann, N., Akkayagil, E., et al. Basic features of hypoxic pulmonary vasoconstriction in mice. Respir. Physiol. Neurobiol. 139, 191-202 (2004).
- Leach, R. M., Hill, H. M., Snetkov, V. A., Robertson, T. P., Ward, J. P. T. Divergent roles of glycolysis and the mitochondrial electron transport chain in hypoxic pulmonary vasoconstriction of the rat: identity of the hypoxic sensor. J. Physiol. 536, 211-224 (2001).
- Tabuchi, A., Mertens, M., Kuppe, H., Pries, A. R., Kuebler, W. M. Intravital microscopy of the murine pulmonary microcirculation. J. Appl. Physiol. 104 (2), 338-3346 (2008).
- Sylvester, J. T., Shimoda, L. A., Aaronson, P. I., Ward, J. P. Hypoxic pulmonary vasoconstriction. Physiol. Rev. 92 (1), 367-520 (2012).
- Schumacker, P. T. Lung cell hypoxia: role of mitochondrial reactive oxygen species signaling in triggering responses. Proc. Am. Thorac. Soc. 8 (6), 477-4784 (2011).
- Paddenberg, R., König, P., Faulhammer, P., Goldenberg, A., Pfeil, U., Kummer, W. Hypoxic vasoconstriction of partial muscular intra-acinar pulmonary arteries in murine precision cut lung slices. Respir. Res. 29 (7), 93-109 (2006).
- Paddenberg, R., et al. Mitochondrial complex II is essential for hypoxia-induced pulmonary vasoconstriction of intra- but not of pre-acinar arteries. Cardiovasc. Res. 93 (4), 702-710 (2012).
- Wang, L., Yin, J., et al. Hypoxic pulmonary vasoconstriction requires connexin 40-mediated endothelial signal conduction. J. Clin. Invest. 122 (11), 4218-4230 (2012).
- Archer, S. L., Huang, J. M., et al. Differential distribution of electrophysiologically distinct myocytes in conduit and resistance arteries determines their response to nitric oxide and. 78, 431-442 (1996).
- Yamaguchi, K., Suzuki, K., et al. Response of intra-acinar pulmonary microvessels to hypoxia, hypercapnic acidosis, and isocapnic acidosis. Circ. Res. 82, 722-728 (1998).
- Bennie, R. E., Packer, C. S., Powell, D. R., Jin, N., Rhoades, R. A. Biphasic contractile response of pulmonary artery to hypoxia. Am. J. Physiol. 261(2 Pt. 1, 156-163 (1991).
- Glazier, J. B., Murray, J. F. Sites of pulmonary vasomotor reactivity in the dog during alveolar hypoxia and serotonin and histamine infusion). J. Clin. Invest. 50 (12), 2550-2558 (1971).
- Bhattacharya, J., Staub, N. C. Direct measurement of microvascular pressures in the isolated perfused dog lung. Science. 210, 327-328 (1980).
- Kuebler, W. M. Real-time imaging assessment of pulmonary vascular responses. Proc. Am. Thorac. Soc. 8 (6), 458-4565 (2011).
- Martin, C., Uhlig, S., Ullrich, V. Videomicroscopy of methacholine-induced contraction of individual airways in precision-cut lung slices. Eur. Respir. J. 9 (12), 2479-2487 (1996).
- Grimminger, F., Spriestersbach, R., Weissmann, N., Walmrath, D., Seeger, W. Nitric oxide generation and hypoxic vasoconstriction in buffer-perfused rabbit lungs. J. Appl. Physiol. 78, 1509-1515 (1995).
- Ng, L. C., Kyle, B. D., Lennox, A. R., Shen, X. M., Hatton, W. J., Hume, J. R. Cell culture alters Ca2+ entry pathways activated by store-depletion or hypoxia in canine pulmonary arterial smooth muscle cells. Am. J. Physiol. Cell Physiol. 294 (1), 313-323 (2008).
- Fehr, D. M., Larach, D. R., Zangari, K. A., Schuler, H. G. Halothane constricts bovine pulmonary arteries by release of intracellular calcium. J. Pharmacol. Exp. Ther. 277 (2), 706-713 (1996).
- Oshima, Y., Ishibe, Y., Okazaki, N., Sato, T. Isoflurane inhibits endothelium-mediated nitric oxide relaxing pathways in the isolated perfused rabbit lung. Can. J. Anaesth. 44 (10), 1108-1114 (1997).
- Sanderson, M. J. Exploring lung physiology in health and disease with lung slices. Pulm. Pharmacol. Ther. 24 (5), 452-465 (2011).
- Davies, J. . Replacing Animal Models: A Practical Guide to Creating and Using Culture-based Biomimetic Alternatives (Google eBook. , 57-68 (2012).
- Müller-Redetzky, H. C., Kummer, W., et al. Intermedin stabilized endothelial barrier function and attenuated ventilator-induced lung injury in mice). PLoS One. 7 (5), (2012).
- Russell, W. M. S., Burch, R. L. The Principles of Humane Experimental Technique. Universities Federation for Animal Welfare. , (1959).
- Held, H. D., Martin, C., Uhlig, S. Characterization of airway and vascular responses in murine lungs. Br. J. Pharmacol. 126 (5), 1191-1199 (1999).
- Köhler, D., Schönhofer, B., Voshaar, T. Pneumologie: Ein Leitfaden für rationales Handeln in Klinik und Praxis. Thieme Verlag. , 198-19 (2009).
- Will, J. The Pulmonary Circulation. in Health and Disease. Elsevier Science, p49. , (1987).
- Faro, R., Moreno, L., Hislop, A. A., Sturton, G., Mitchell, J. A. Pulmonary endothelium dependent vasodilation emerges after birth in mice. Eur. J. Pharmacol. 567 (3), 240-244 (2007).
- Wright, J. L., Churg, A. Short-term exposure to cigarette smoke induces endothelial dysfunction in small intrapulmonary arteries: analysis using guinea pig precision cut lung slices. J. Appl. Physiol. 104, 1462-1469 (2008).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved