Method Article
تقييم توافر المعادن في أعلاف الأسماك باستخدام أساليب تكميلية موضحة مع مثال الزنك في سمك السلمون الأطلسي
In This Article
Summary
يشرح هذا المقال بالتفصيل نهجا منهجيا لتقييم توافر المعادن الدقيقة في سمك السلمون الأطلسي. وتشمل المنهجية أدوات ونماذج ذات تعقيد بيولوجي متزايد: (1) تحليل التحليل الكيميائي، (2) قابلية الذوبان في المختبر، (3) دراسات امتصاص في خطوط الخلايا، و (4) في دراسات الأسماك الحية.
Abstract
10 - يشكل تقييم مدى توافر المعادن الدقيقة الغذائية تحديا رئيسيا في التغذية المعدنية لأنواع الأسماك. تهدف هذه المقالة إلى وصف نهج منهجي يجمع بين منهجيات مختلفة لتقييم توافر الزنك (Zn) في سلمون المحيط الأطلسي(Salmo salar). وبالنظر إلى أن العديد من الأنواع الكيميائية Zn يمكن أن تكون موجودة في تغذية السلمون الأطلسي، كان من المفترض أن توافر Zn يتأثر الأنواع الكيميائية Zn الموجودة في الأعلاف. وهكذا، في هذه الدراسة، البروتوكول الأول هو حول كيفية استخراج مختلف الأنواع الكيميائية Zn من الأعلاف وتحليلها عن طريق استبعاد حجم الكروماتوغرافيا المقترنة استحثاثيا البلازما الطيفية الشامل (SEC-ICP-MS) الأسلوب. وفي وقت لاحق، تم تطوير طريقة في المختبر لتقييم قابلية الذوبان من Zn الغذائية في أعلاف السلمون الأطلسي. يصف البروتوكول الثالث طريقة دراسة تأثير تغيير تكوين الأنواع الكيميائية Zn على امتصاص Zn في نموذج ظهاري معوي للأسماك باستخدام خط خلايا الأمعاء لتراوت قوس قزح (RTgutGC). معا، تمت مقارنة النتائج من أساليب المختبر مع دراسة في الجسم الحي دراسة توافر واضح من المصادر غير العضوية والعضوية من Zn تكملها إلى أعلاف السلمون الأطلسي. وأظهرت النتائج أنه يمكن العثور على العديد من الأنواع الكيميائية ZN في الأعلاف وكفاءة مصدر Zn العضوية يعتمد كثيرا على ليغاند الأحماض الأمينية المستخدمة لchelate Zn. وكانت نتائج أساليب المختبر أقل ارتباطا بتلك النتيجة من الدراسة في الجسم الحي. ومع ذلك، قدمت بروتوكولات المختبر الموصوفة في هذه المقالة معلومات حاسمة بشأن توافر Zn وتقييمها في أعلاف الأسماك.
Introduction
كانت وجبة السمك وزيت السمك تستخدم تقليديا في تغذية السلمون الأطلسي. ومع ذلك، يتم استبدال هذه المكونات بشكل متزايد من قبل المكونات النباتية1. وقد أدى التحول المذكور أعلاه في تكوين الأعلاف إلى انخفاض توافر الغذاء وزيادة الحاجة إلى تحسين توافر المعادن في أعلاف السلمون الأطلسي، وخاصة الزنك (Zn)2. وقد يكون انخفاض التوافر نتيجة لتغير في مستوى Zn أو الأنواع الكيميائية Zn أو /وعوامل مضادة للتغذية موجودة في مصفوفة الأعلاف. وفي هذا السيناريو، ظهرت مجموعة جديدة من الإضافات التي تعتبر عموما "مصادر عضوية" مع إمكانية أن تكون مصدرا أفضل متاحة للمعادن الغذائية للأسماك. لذلك، من المهم فهم الكيمياء الأساسية وعلم وظائف الأعضاء التي تحكم توافر المعادن ومصادرها للأسماك. الزنك عنصر أساسي تتبع لجميع الكائنات الحية3. وقد وصف دور Zn كجزيء إشارة على كل من مستوى شبه الخلية وداخل الخلايا في الأسماك4. في سمك السلمون الأطلسي, وقد ارتبط نقص ZN مع تشوهات الهيكل العظمي وانخفاض نشاط مختلف المعادن زن5,6.
تصف هذه الدراسة نهجا منهجيا لفهم توافر Zn من خلال تصنيفه إلى أربع مقصورات مختلفة من التعقيد الكيميائي والبيولوجي المتنوع. ويرد وصف الأساليب المعنية في أربعة أقسام، كما يتضح في الشكل 1 : (1)تقييم الأنواع الكيميائية Zn في جزء قابل للذوبان من تغذية السلمون الأطلسي باستخدام حجم استبعاد الكروماتوغرافيا المقترنة استقرائيا البلازما الطيف الكتلي (SEC-ICP-MS) الطريقة7; (2) في الذوبان في المختبر من Zn المكملة في تغذية السلمون الأطلسي؛ (3) تقييم ZN امتصاص الأنواع الكيميائية من قبل في المختبر نموذج الأمعاء (RTgutGC)8; و (4) توافر واضح من ZN في سمك السلمون الأطلسي (Salmo salar)9. ويمكن وضع بروتوكولات مماثلة لمعادن أخرى (مثل المنغنيز والسيلينيوم والنحاس) ذات أهمية غذائية لأنواع الأسماك في تربية الأحياء المائية.
Protocol
أجريت تجربة التغذية في القسم 4 وفقا للتشريعات النرويجية (FOR-2015-06 - 18-761) والتشريعات الأوروبية (التوجيه 2010/63/EU).
1. تقييم الأنواع الكيميائية Zn في جزء قابل للذوبان من تغذية السلمون الأطلسي باستخدام طريقة SEC-ICP-MS
- المخزن المؤقت للاستخراج (100 متر م تريس-HCl، pH 8.5)
- إعداد العازلة استخراج عن طريق حل كمية مناسبة من تريس (هيدروكسي ميثيل)أمينوميثان للوصول إلى القوة الأيونية المطلوبة (100 mM) في ultrapure H2O.
- ضبط درجة الحموضة للحل إلى درجة الحموضة 8.5 مع حل HCl، ورصد تغيير درجة الحموضة مع متر درجة الحموضة.
- إعداد عينات الأعلاف
ملاحظة: تم تصميم عينة الأعلاف المستخدمة على أساس الأعلاف التجارية لسمك السلمون الأطلسي، والتي تحتوي على مصادر البروتين أساسا من المكونات النباتية (أي ما يقرب من 5٪ من بروتين السمك، و 10٪ زيت السمك، و 68٪ من البروتين النباتي و 12٪ من الزيت النباتي). تم تكميل كبريتات الزنك إلى الأعلاف.- طحن عينة الأعلاف باليد باستخدام الحشرات وقذائف الهاون.
- غربال عينة التغذية لضمان أن يتم تنفيذ الاستخراج في جزء تغذية مع حجم الجسيمات مماثلة (من 850 ميكرومتر إلى 1.12 ملم).
- المضي قدما لتنفيذ استخراج ZN.
- استخراج الزنك من عينة تغذية
- تزن ما يقرب من 0.5 غرام من الأعلاف في ثلاثة كلورات في أنابيب مخروطية 15 مل.
- إضافة المخزن المؤقت استخراج (5 مل من 100 mM تريس-HCl، pH 8.5) إلى العينات.
- استخراج العينات في الدوار (20 دورة في الدقيقة) في 4 درجة مئوية لمدة 24 ساعة.
- فصل الكسور القابلة للذوبان وغير القابلة للذوبان عن طريق الطرد المركزي لمدة 10 دقائق عند 3000 × ز.
- استخدم مرشح حقنة 0.45 ميكرومتر قابل للتصرف لتصفية الكسر القابل للذوبان.
- نقل العينات المصفاة لتنظيف الأنابيب.
- إجراء تحليل المواصفات Zn في الكسور القابلة للذوبان باستخدام SEC-ICP-MS، كما هو موضح في الخطوة 1.6.
ملاحظة: يتم وصف ملخص الإجراء لاستخراج Zn من عينة تغذية في الشكل 2.
- حل المرحلة المتنقلة (50 mM تريس-HCl + 3٪ MeOH، الرقم الحموضة 7.5)
- إعداد حل المرحلة المتنقلة حل 6.057 غرام من tris (هيدروكسي ميثيل)أمينوميثان في 1 لتر من 3٪ محلول MeOH (v/v).
- ضبط درجة الحموضة للحل إلى درجة الحموضة إلى 7.5 مع حل HCl، ورصد تغيير درجة الحموضة مع متر درجة الحموضة.
- تصفية حل المرحلة المتنقلة من خلال مرشح غشاء 0.45 ميكرومتر.
- معايرة الوزن الجزيئي لنطاق فصل عمود SEC
- معايرة نطاق الفصل عن طريق إجراء معايرة الوزن الجزيئي.
ملاحظة: في هذه الدراسة thyroglobulin (660 kDa), Zn / Cu superoxide dismutase (32 kDa), تم استخدام الميوجلوبين (17 kDa) وفيتامين B12 (1.36 kDa). - إعداد كل من المعايير مع تركيز معروف في فائقةpure H2O.
- قم بإعداد قارورة كروماتوغرافيا سائلة عالية الأداء (HPLC) بإضافة 250 ميكرولتر من المعيار إلى قارورة.
- تحميل قوارير مع المعايير لتشغيل تسلسل العينات.
- قم بتشغيل معايرة الوزن الجزيئي في بداية ونهاية التسلسل التحليلي، ورصد 127I (الثيروغلوبولين)، و66Zn (Zn/Cu superoxide dismutase)، و57في (الميوجلوبين)، و59Co (فيتامين B12).
ملاحظة: يتم إجراء معايرة الوزن الجزيئي في وقت واحد مع تحليل الطيف Zn.
- معايرة نطاق الفصل عن طريق إجراء معايرة الوزن الجزيئي.
- تحليل تحليل تحليل الزنك باستخدام SEC-ICP-MS
ملاحظة: تم تطوير تحليل المواصفات Zn من قبل طريقة SEC-ICP-MS استنادا إلى المبادئ الموصوفة في مكان آخر10،11 وتم إجراء مزيد من التحسين لتحليل تغذية السلمون الأطلسي7.- إجراء تحليل المواصفات Zn على الكسور القابلة للذوبان باستخدام حجم استبعاد الكروماتوغرافيا (SEC) عمود وHPLC مقرونة مطياف كتلة البلازما المقترنة بشكل استحثازي (ICP-MS).
- قم بإعداد قارورة HPLC بإضافة 250 ميكرولتر من الكسر القابل للذوبان إلى قارورة.
- قبل التحليل، ارتفاع جميع العينات مع 0.5 ميكرولتر من فيتامين B12. تسمح هذه الخطوة بتصحيح نوبات أوقات الاحتفاظ ، ومراقبة 59Co.
- تمييع الكسر القابل للذوبان مع المخزن المؤقت للاستخراج (100 mM Tris-HCl، درجة الحموضة 8.5) والتكيف مع حجم نهائي قدره 1 مل.
- إعداد تشغيل تسلسل العينات بترتيب عشوائي.
- ضبط ICP-MS وفقا لتعليمات الشركة المصنعة.
- اتبع إعدادات الجهاز ل HPLC و ICP-MS إجراء تحليل المواصفات Zn (انظر الجدول 1).
2. في الذوبان في المختبر من ZN المكملة في تغذية السلمون الأطلسي
ملاحظة: تم تصميم عينة الأعلاف المستخدمة على أساس الأعلاف التجارية لسمك السلمون الأطلسي، والتي تحتوي على مصادر البروتين أساسا من المكونات النباتية (أي ما يقرب من 5٪ وجبة السمك، 10٪ زيت السمك، 68٪ المكونات النباتية و 12٪ زيت نباتي).
- طحن عينات تغذية السلمون الأطلسي لمدة 10 ق في 3000 دورة في الدقيقة باستخدام مطحنة سكين وتخزينها في 4 درجة مئوية حتى مزيد من التحليل.
- وزن ~ 0.2 غرام من عينات تغذية الأرض في الخطوة 2.1 وإضافة Zn radiotracer(65زن) من نشاط محدد معروف في أنبوب عينة حجم 5 مل (مع غطاء).
تنبيه: يجب إجراء هذا الإجراء داخل مجموعة النويدات المشعة. وينبغي تدريب الشخص الذي يقوم بهذه الخطوة واعتماده للتعامل مع النظائر الراديوية. ويجب اتباع تدابير السلامة والحيطة التي تنصح بها إدارة السلامة الإشعاعية في المعهد بدقة. - ثم قم بإعداد محلول العازلة الإنارة المعوية في المياه العذبة كما هو موضح أدناه.
- لحل الملح A، تزن 11.65 غرام من NaNO3،0.55 غرام من KNO3 و 0.4 غرام من MgSO4. حل الأملاح في فائقة البور H2O والتكيف مع حجم النهائي من 60 مل.
- للمحلول الملح B، تزن 0.31 غرام من Ca (NO3)2· 4 H2O. حل الأملاح في فائقةpure H2O والتكيف مع حجم النهائي من 10 مل.
- استخدام 500 mM HEPES الأسهم الحل كمحلول الملح C.
- للمحلول الملح D, تزن 1.2 غرام من MgCl2, حل الملح في فائقةpure H2O والتكيف مع حجم النهائي من 20 مل.
- لحل الملح E، تزن 0.9 غرام من MgSO4،حل الملح في فائقة البور H2O والتكيف مع حجم النهائي من 20 مل.
- إعداد محلول بيروفاتي عن طريق حل 0.55 غرام من CH3COCOONa في 10 مل من ultrapure H2O.
- حل 0.9 غرام من الجلاكتوز (C6H12O6) في فائقة الشراء H2O.
- حل جيدا باستخدام stirrer المغناطيسي وتعقيم حلول الملح A, B, D و E عن طريق الالاستعباد التلقائي, والحل C, بيروفاتي وgalactose عن طريق الترشيح من خلال مرشح حقنة 200 ميكرومتر.
- بعد إعداد حلول المخزون المختلفة، لإعداد 100 مل من محلول العمل من المخزن المؤقت، اخلط الحلول المعدة أعلاه في النسبة التالية: 6.8 مل من محلول الملح A، 4.14 مل من B، 5 مل من C، 2.5 مل من D، 1.5 مل من E، و 1.14 مل لكل من بيروفاتي وجالاكتوز. تشكل حجم إلى 100 مل باستخدام المياه deionized.
ملاحظة: العازلة أعلاه الآن تمثل التكوين الأيوني للتجويف المعوية الموجودة في سمك السلمون في المياه العذبة.
- إعداد ستة aliquots أخرى من العازلة الموصوفة في الخطوة 2.6 وإضافة واحدة من الأحماض الأمينية التالية (السيستين، ميثيونين، الجليسين، الهستيدين، ليسين وأرجينين) للوصول إلى تركيز الضرس النهائي من 5M.
- أضف العازلة الإنارة المعوية في المياه العذبة (حجم التفاعل = 3 مل؛ درجة الحموضة 7.4) إلى عينة التغذية.
- كرر الخطوة 2.5 مع المخازن المؤقتة الموصوفة في 2.4 (في وجود الأحماض الأمينية المختلفة في تركيز 5 MM).
- أغلق الأنابيب واسمح لها بالدوران في الدوار الدوار لمدة 30 دقيقة عند 25 دورة في الدقيقة.
- فصل الكسور القابلة للذوبان وغير القابلة للذوبان عن طريق الطرد المركزي لمدة 10 دقائق عند 1157 × ز.
- استخدم جهاز صراف غاما لقياس عدد الأصوات في الدقيقة (cpm) البالغ 65زن في الكسور القابلة للذوبان وغير القابلة للذوبان.
- حساب نسبة النظائر الراديوية من Zn(65Zn) الموجودة في الكسور القابلة للذوبان وغير القابلة للذوبان.
3. تقييم امتصاص الأنواع الكيميائية Zn باستخدام نموذج الأمعاء في المختبر (RTgutGC)
- ثقافة خلايا RTgutGC
ملاحظة: يجب أن تكون جميع مواد العمل المستخدمة في هذه الخطوة عقيمة.- إحياء خلايا RTgutGC المجمدة بلطف في حمام مائي تعيين في 20 درجة مئوية.
- ماصة بلطف من الحل الذي يحتوي على الخلايا وتعليقها في 10 مل من L15 المتوسطة التي تحتوي على 10٪ مصل البقر الجنيني (FBS).
ملاحظة: يستخدم فقط 10٪ FBS لإحياء الخلايا المجمدة. للمرور اللاحق، يستخدم FBS بنسبة 5٪. يمكن أن يختلف تكوين FBS بين دفعات ، لذلك من المستحسن شراء وتخزين بقدر ما هو مطلوب من دفعة واحدة لتجنب الاختلافات بين الدفعات في تكوين المصل. - إضافة تعليق الخلية إلى 75 سم2 قارورة زراعة الخلية واحتضان في حاضنة تعيين في 19 درجة مئوية تحت الغلاف الجوي العادي.
- تحقق من الخلايا وعند التقاء (التقاء 80٪، وتقييم بصريا من خلال فحص كثافة سطح الخلية تحت المجهر)، وتقسيم الخلايا إلى قوارير جديدة (مرور لاحق) أو الحصاد لاستخدامها في التجارب.
ملاحظة: مثال على خلايا RTgutGC 1 ح و 1 أسبوع بعد البذر إلى قوارير ثقافة الخلية هو مبين في الشكل 3.
- حصاد الخلايا والتحضير لتجارب التعرض
- غسل الخلايا مرتين مع 1 مل حمض الإيثيلين أمينتتراستيك (EDTA) الحل. بعد كل غسل، سحب محلول EDTA باستخدام أنبوب شفط معقم.
- علاج الخلايا مع تريبسين (0.7 مل من تريبسين, في 0.25٪ في الفوسفات العازلة المالحة [PBS]).
- تدوير بلطف قارورة في زوايا حادة لنشر التربسين على طول سطح القارورة.
- استمر في الدوران لمدة دقيقتين، بينما تنفصل الخلايا.
- بعد تناوب بلطف لمدة 2 دقيقة، إضافة 10 مل من L15/FBS المتوسطة لتحييد التريبسين.
- decant تعليق الخلية الناتجة في أنبوب الطرد المركزي السفلي مخروطية باستخدام ماصة معقمة والطرد المركزي لمدة 3 دقائق في 130 × ز.
- تحديد كثافة الخلايا المحصودة عن طريق العد اليدوي باستخدام مقياس الدم.
- إضافة حجم المطلوبة من L15/FBS المتوسطة لتحقيق كثافة الخلية من 5 × 104 خلايا / مل.
- البذور الخلايا على لوحات 24 جيدا عن طريق pipetting 1 مل من تعليق الخلية لكل بئر لتحقيق كثافة الخلية النهائية من 5 × 104 خلايا / جيدا.
ملاحظة: يفضل استخدام ماصة متعددة الاستغناء لتقليل التباين وتقليل الوقت. - ضع الصفائح المصنفة في حاضنة تحت الغلاف الجوي العادي عند 19 درجة مئوية لمدة 48 ساعة قبل التجارب.
ملاحظة: تريبسين ليتم تخزينها في -20 درجة مئوية; حل EDTA ووسائط L15/FBS عند 4 °C. ضبط درجة حرارة جميع حلول العمل والوسائط إلى 19 درجة مئوية قبل الاستخدام مباشرة.
- إعداد وسائط التعريض الضوئي
ملاحظة: يجب أن يتم هذه الخطوة تحت غطاء الدخان تحت ظروف معقمة ومعقمة.- إعداد L15/ex عن طريق خلط 6.8 مل من محلول الملح A (الخطوة 2.3.1) و 1.14 مل من B (الخطوة 2.3.2) و 5 مل من C (الخطوة 2.3.3) و 1.14 مل لكل من البيروفاتي (الخطوة 2.3.6) والجالاكتوز (الخطوة 2.3.7). تشكل حجم إلى 100 مل باستخدام الخلايا العقيمة ثقافة الصف الماء المقطر.
- إعداد FW عن طريق خلط 6.8 مل من محلول الملح A (2.3.1) ، 4.14 مل من B (2.3.2) ، 5 مل من C (2.3.3) ، 2.5 مل من D (2.3.4) و 1.5 مل من E (2.3.5) و 1.14 مل لكل من بيروفاتي (2.3.6) وجالاكتوز (2.3.7). تشكل حجم إلى 100 مل باستخدام العقيمة، خلية ثقافة الصف الماء المقطر.
- تحديد تركيزات الأيونات في وسائط التعرض باستخدام ICP-MS كما هو موضح في مكان آخر12.
ملاحظة: يتم عرض التركيزات الأيونية التي تم تحليلها في التحضيرات الإعلامية في الجدول 2.
- الزنك (65Zn) اختبارات التدفق
- قم بزرع خلايا RTgutGC على 24 لوحة بئر (5 × 104 خلايا / جيدا) في متوسط L15/FBS الكامل.
- حضانة لمدة 48 ساعة في حاضنة مع الغلاف الجوي العادي في 19 درجة مئوية.
- ضبط جميع الاستعدادات وسائل الإعلام التجريبية إلى درجة الحموضة 7.4 باستخدام 0.5 M NaOH في وجود أو غياب L-ميثيونين (L-ميت) أو DL-ميثيونين (DL-ميت) في تركيز 2 MM.
ملاحظة: يجب إجراء تعديل رقم الحموضة للمخازن المؤقتة الموضحة في 3.4.3 حديثا قبل معالجة الخلايا في الخطوة 3.4.5. - بعد الانتهاء من فترة الحضانة، وإزالة المتوسطة من الآبار، وشطف جيدا مع برنامج تلفزيوني.
- أضف الوسائط التجريبية المعدلة حسب درجة الحموضة، واتركها تتكيف لمدة 20 دقيقة.
- تعريض خلايا RTgutGC لتركيزات اسمية من 3.07، 6.14، 12.27 و 24.55 ميكرومتر 65Zn(II) (كما ZnCl2؛ ~ 4 كيلو متر مربع / مل) في وسائل الإعلام الموصوفة في الخطوة 3.4.3.
- بعد ذلك مباشرة، احتفظ بالخلايا في الحاضنة عند 19 درجة مئوية لمدة 15 دقيقة.
- بعد انتهاء الحضانة التي تبلغ 15 دقيقة ، قم بتوبيخ الثقافة الفائقة وإزالتها من البئر.
- شطف الخلايا مع الجليد الباردة FW المتوسطة (مع 200 ميكرومتر زن، درجة الحموضة 7.4) ثم إرواء بإضافة 5 mM الإيثيلين غليكول بيس (β أمينوثيل الأثير)-N,N',N',N'tetraacetic حمض (EGTA) العازلة (درجة الحموضة 7.4) لمدة 5 دقائق, للتخلص من أي مموه 65Zn(II).
- تعريض الخلايا للاستعدادات وسائل الإعلام أعلاه في وجود أو عدم وجود 10 MM 2-Aminobicyclo [2.2.1] حمض الهيبتان-2-كاربوكسيليك (BCH)، مثبط نقل الأحماض الأمينية.
- بعد فترة التعرض 15 دقيقة، كرر الخطوتين 3.4.8 و 3.4.9.
- سيتم الالتزام بخلايا RtgutGC إلى أسفل الآبار كغرس أحادي. هضم الخلايا باستخدام 0.2٪ من كبريتات دودسيل الصوديوم الساخنة (SDS) المنظفات (100 ميكرولتر / جيد).
ملاحظة: يجب وضع محلول SDS لمدة ساعة واحدة في حمام مائي يتم ضبطه على 90 درجة مئوية قبل الاستخدام. - أسبيرات واستعادة هضم الخلية في أنبوب 1.5 مل.
- قياس النشاط الإشعاعي للخلية هضم باستخدام عداد غاما.
ملاحظة: يجب تصحيح الأعداد في الدقيقة (cpm) للاضمحلال الإشعاعي ونشاط الخلفية وتخضع لحسابات نشاط محددة وفقا للصيغ التي وصفها Glover و Hogstrand13. - لقياس تركيز البروتين في الخلايا، وتجانس الخلايا مع 500 ميكرولتر من 0.5 M NaOH.
- استخدم مجموعة اختبارات برادفورد لقياس تركيز البروتين في عينة الخلية ، مع ألبوم مصل البقر (BSA) كمعيار.
ملاحظة: بمجرد أن يتم قياس تركيز البروتين كميا، يمكن التعبير عن معدل امتصاص Zn من قبل خلايا RTgutGC كبروتين pmoles Zn min-1 ملغ-1.
4. توافر واضح من ZN الغذائية في سمك السلمون الأطلسي (Salmo salar)
ملاحظة: تم صياغة أعلاف السلمون الأطلسي على أساس الأعلاف التجارية، التي تحتوي على مصادر البروتين أساسا من المكونات النباتية (أي ما يقرب من 5٪ من بروتين السمك، 10٪ زيت السمك، 68٪ البروتين النباتي و 12٪ زيت النبات). تم استكمال اثنين من الأعلاف بمصدر غير عضوي (كبريتات زان) أو مصدر عضوي (Zn chelate of glycine) لتحقيق تركيز Zn من 150 ملغم / كجم من الأعلاف. بالإضافة إلى ذلك، تمت إضافة أكسيد Yttrium (درجة التغذية) إلى التغذية بنسبة 0.01٪ كعلامة خاملة لتمكين حساب معامل التوافر الظاهر.
- التأقلم مع سمك السلمون الأطلسي (سلالة SalmoBreed، سن 1+ سنوات، مجموعات مختلطة الجنس) في خزانات كل منها حتى يتم استخدام الأسماك للظروف التجريبية.
- تقييم تأقلم سمك السلمون الأطلسي من خلال رصد مداهم اليومي من الأعلاف.
ملاحظة: أجريت هذه التجربة في خزانات ثلاثية الدوائر، وبالتالي تم استخدام ما مجموعه ست دبابات. خلال تجربة التغذية كانت درجة حرارة الماء 11.9 ± 0.3 درجة مئوية وكان تشبع الأكسجين المذاب 101 ± 5٪. - إطعام الأسماك مع الأعلاف التجريبية لمدة 11 يوما.
- قتل الأسماك بجرعة زائدة باستخدام 6 مل من محلول مخزون الميثان ثلاثي الكينا لكل لتر من الماء.
- جمع عينة مجمعة من البراز من الأسماك من نفس الخزان في لوحة عن طريق التعري من زعنفة البطن إلى فتحة الشج.
- إزالة البراز من لوحة مع ملعقة في أنبوب مخروطي 50 مل وتخزين العينات على الفور في -20 درجة مئوية.
ملاحظة: تم الاحتفاظ بالعينات عند -20 درجة مئوية حتى إجراء مزيد من التحليل. - تجميد عينات البراز الجافة لمدة 72 ساعة في -80 درجة مئوية.
- تجانس يدويا عينة البراز في مسحوق ناعم باستخدام الحشرات وقذائف الهاون.
- تحديد تركيز Zn وYttrium في عينات الأعلاف والبراز باستخدام ICP-MS (كما هو موضح في مكان آخر9).
- تحديد معامل التوفر الظاهر (AAC, ٪) باستخدام الصيغة التالية:

النتائج
تقييم الأنواع الكيميائية Zn في جزء قابل للذوبان من تغذية السلمون الأطلسي باستخدام طريقة SEC-ICP-MS
وتوفر طريقة SEC-ICP-MS بيانات عن الأنواع الكيميائية من Zn الموجودة في الجزء القابل للذوبان من علف السلمون الأطلسي. يوضح الشكل 4 الملف اللوني ل Zn الموجود في الكسر القابل للذوبان. تم الحصول على هذا الرسم اللوني باستخدام أسلوب SEC-ICP-MS. تم العثور على خمسة Zn تحتوي على قمم في الكسور القابلة للذوبان من تغذية السلمون الأطلسي. كل ذروة لها وزن جزيئي مختلف. الذروة الأولى (~ 600 كيلودا)، الذروة الثانية والذروة الثالثة (من 32 إلى 17 كيلودا)، الذروة الرابعة (من 17 إلى 1.36 كيلودا) والذروة الخامسة (> 1.36 كيلودا). وكانت الذروة الرابعة هي الأكثر وفرة، تليها الذروة الثانية والثلاثة والخامسة وواحدة على التوالي. يمكن أن يكون لأنواع Zn الكيميائية الموجودة في الكسر القابل للذوبان مصادر مختلفة لأن الأعلاف المستخدمة تحتوي على مكونات بحرية ونباتية على حد سواء ، وشكل مكمل (أي كبريتات Zn). ويشير نطاق الوزن الجزيئي للأنواع الكيميائية Zn إلى أن هذه المركبات قد تكون ميتالوبروتينات.
في الذوبان في المختبر من Zn المكملة في تغذية السلمون الأطلسي
Solubility تكملة 65زن زيادة في وجود الأحماض الأمينية. جميع الأحماض الأمينية اختبار زيادة قابلية الذوبان من تكملة 65Zn. ميثيونين, الجليسين, السيستين, الهستيدين, وتحسين ليسين 65Zn الذوبان; تم العثور على أعلى الذوبان مع الهستيدين واللسين (الشكل 5).
تقييم امتصاص الأنواع Zn باستخدام نموذج الأمعاء في المختبر (RTgutGC)
تأثر امتصاص الزنك Apical في خلايا RTgutGC بشكل كبير بوجود L-Met أو DL-Met بتركيزات 2 mM. وعلاوة على ذلك، فإن تأثير الميثيونين على امتصاص Zn في خلايا RTgutGC تأثر سلبا بوجود BCH (مانع نظام نقل الأحماض الأمينية)، بالمقارنة مع الخلايا غير المعالجة مع BCH (الشكل 6).
توافر واضح من ZN الغذائية في سمك السلمون الأطلسي (Salmo salar)
في الأعلاف العملية لسمك السلمون الأطلسي، كان توافر ZN الظاهر هو نفسه عند المكمل بمصدر غير عضوي (كبريتات زان) أو مصدر عضوي (Zn chelate of glycine). وكانت القيم المقدرة للتوافر الظاهر ل Zn (٪, n = 3) في سمك السلمون الأطلسي 31٪ ± 12٪ عند المكمل بمصدر غير عضوي (كبريتات زان) و31٪ ± 3٪ عند استكمال مصدر عضوي (Zn chelate of glycine).
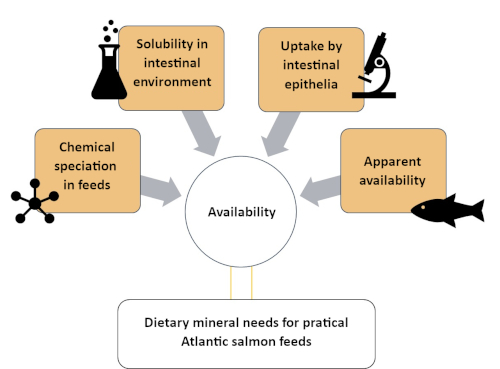
الشكل 1:ملخص للنهج المنهجي لتقييم توافر المعادن باستخدام أساليب تكميلية. وقد استخدم هذا النهج لدراسة توافر الزنك في سمك السلمون الأطلسي، بما في ذلك المواصفات Zn، الذوبان زن في بيئة الأمعاء، امتصاص الزنك من قبل الخلايا المعوية وتوافر Zn واضح. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
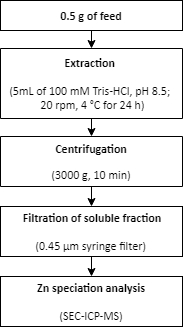
الشكل 2:ملخص للإجراءات لاستخراج ZN من عينة تغذية. يتم استخراج الزنك من عينة تغذية باستخدام ظروف استخراج خفيفة. ويتبع الاستخراج تحليل مواصفات Zn. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
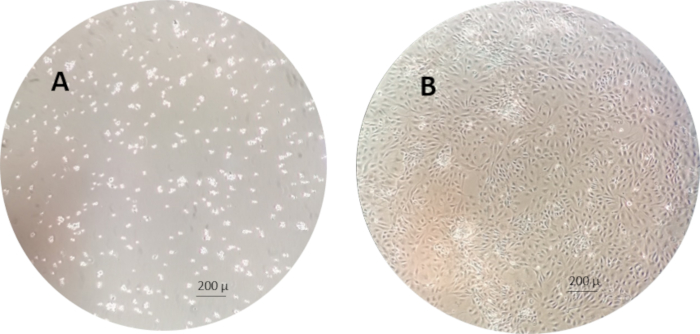
الشكل 3:مثال على خلايا RTgutGC 1 ساعة (يسار) و 1 أسبوع (يمين) بعد البذر في قوارير ثقافة الخلية. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
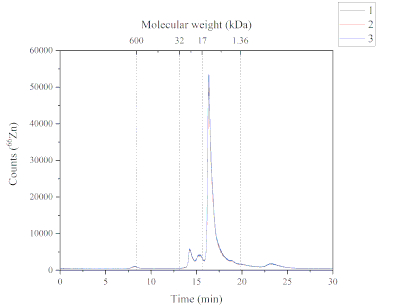
الشكل 4:رسم لوني يظهر القمم المحتوية على Zn من الكسر القابل للذوبان من علف السلمون الأطلسي وتحليله من قبل SEC-ICP-MS. وتتميز النسخ المتماثلة الثلاث بالخطوط الزرقاء والحمراء والسوداء. أجريت معايرة الوزن الجزيئي باستخدام الثيروغلوبولين (660 كيلودا، رصد 127I)، Zn/Cu superoxide dismutase (32 كيلودا، رصد 66زنا)، الميوجلوبين (17 كيلودا، رصد 57في)، فيتامين B12 (1.36 كيلودا، رصد 59كو)؛ الذروة 1 (P1): ~ 600 كيلودا، وقت الاحتفاظ (RT) 8.2 دقيقة؛ الذروة 2+3 (P2+3): من 32 إلى 17 كيلودا، RT 14.2 + 15.3 دقيقة؛ الذروة 4 (P4): من 17 إلى 1.36 كيلودا، RT 16.3 دقيقة؛ الذروة 5 (P5): > 1.36 كيلودا، Rt 23.2 دقيقة. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
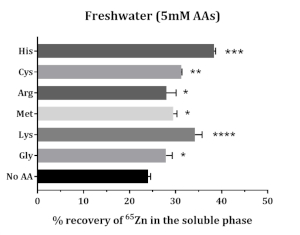
الشكل 5:تأثير الأحماض الأمينية على الذوبان في المختبر من Zn المكملة في تغذية السلمون الأطلسي. يتم تقديم البيانات على أنها متوسط ± SD (n = 3). تم تحليل البيانات من خلال ANOVA أحادية الاتجاه ، تليها اختبار المقارنة المتعددة ل Dunnet ، مقارنة متوسط كل مجموعة AA مع متوسط مجموعة التحكم (No AA). تشير العلامات النجمية إلى مستوى أهمية ANOVA (القيم P < 0.05 (*) < 0.01 (**) < 0.001 (***) و < 0.0001 (****)). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
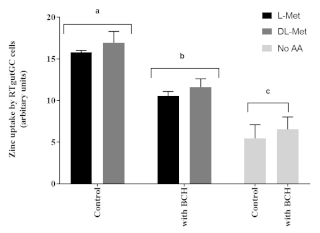
الشكل 6: تأثير ميثيونين ومثبط نقل الأحماض الأمينية (2-Aminobicyclo [2.2.1] حمض الهيبتان-2-كاربوكسيليك، BCH، 10 mM). يتم تقديم البيانات على أنها متوسط ± SD (n = 3). تم تحليل البيانات من خلال ANOVA في اتجاهين ، تليها اختبار مقارنة Tukey المتعدد مع p < مستوى 0.05 من الأهمية. وتمثل الاختلافات اللاحقة للتعيين بين المجموعات كحرف فوق القضبان؛ الحانات مع نقوش مختلفة تختلف إحصائيا (ص < 0.05). يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
| إعدادات HPLC | |
| عمود | عمود SEC (30 سم × 7.8 مم، حجم جسيم 5 ميكرومتر) + عمود حراسة (حجم جسيم 7 ميكرومتر) |
| نطاق المعايرة | 1.0 × 104 - 5.0 × 105 دا |
| مرحلة الجوال | 50 mM تريس-HCl + 3٪ MeOH (الرقم الحموضة 7.5) |
| معدل التدفق | 0.7 مل دقيقة−1 |
| حجم الحقن | 50 ميكرولتر |
| إعدادات ICP-MS | |
| قوة أمامية | 1550 واط |
| تدفق غاز البلازما | 15.0 لتر فيالدقيقة −1 |
| تدفق الغاز الناقل | 0.86 لتر دقيقة−1 |
| تدفق غاز المكياج | 0.34 لتر فيالدقيقة −1 |
| وقت الإقامة | 0.1 s لكل نظير |
| النظائر التي تم رصدها | 127 أنا، 66زن، 59كو، 57في |
الجدول 1 - الجداول نظرة عامة على إعدادات الأجهزة الخاصة ب HPLC و ICP-MS.
| التركيب الكيميائي (mM) | L15/السابقين | وسيط تجريبي (L15/FW) |
| نترات الصوديوم | 155 | 155 |
| نترات البوتاسيوم | 6.2 | 6.2 |
| كبريتات المغنيسيوم | 3.8 | 19.5 |
| نترات الكالسيوم | 1.5 | 5.4 |
| هيبس | 5 | 5 |
| كلوريد المغنيسيوم | - | 15 |
| بيروفات الصوديوم | 5.7 | 5.7 |
| غالاكتوز | 5.7 | 5.7 |
| الرقم الهيدروجيني | 7.1 | 7.4 |
| قوة أيونية | 178 | 258 |
| التكوين الأيوني (mM) | ||
| الكالسيوم، Ca2+ * | 1.6 ± 0.1 | 5.3 ± 0.2 |
| المغنيسيوم، ملغ2+ * | 3.9 ± 0.3 | 32.5 ± 0.7 |
| البوتاسيوم، ك+ * | 8.2 ± 1.2 | 8.6 ± 1.1 |
| الصوديوم، نا+ * | 160 ± 3 | 157 ± 2 |
| نترات، NO3- ** | 164 | 172.4 |
| كبريتات، SO4- ** | 3.8 | 18.7 |
| كلوريد، كل- ** | 1.5 | 31.5 |
الجدول 2 - الأرباح تم اختبار التركيب الكيميائي والأيوني للوسائط التجريبية.
Discussion
امتصاص المعوية من زن ويبدو أن تتأثر الشكل الكيميائي للأنواعزن 13. وفي هذا الصدد، أتاح استخدام البروتوكولات الموصوفة في هذه المادة دراسة الجوانب الكيميائية والبيولوجية التي تقوم عليها "توافر" Zn في سلمون المحيط الأطلسي.
وأفادت هذه الدراسة باستخدام طريقة تحليل المواصفات Zn. 10- وقدمت طريقة لجنة الأوراق المالية والبورصة - برنامج المقارنات الدولية - التصلب المتعدد بيانات نوعية تتعلق بالوزن الجزيئي للأنواع الكيميائية من الزن الموجودة في الجزء القابل للذوبان من علف السلمون الأطلسي. وقد تحقق ذلك بالمقارنة مع أوقات الاحتفاظ بمعايير معايرة الوزن الجزيئي (أي الثيروغلوبولين (660 كيلودا) وزن/كو سوبر أكسيد ديسموتاز (32 كيلودا) والميوجلوبين (17 كيلودا) وفيتامين B12 (1.36 كيلودا)) مع أوقات الاحتفاظ ب Zn التي تحتوي على قمم. وكان أحد التحديات التي وجدها تحليل مواصفات Zn هو تحديد الأنواع الكيميائية غير المعروفة من Zn بسبب عدم وجود معايير تحليلية. في لجنة الأوراق المالية والبورصة ، ويستند فصل الجزيئات على أحجامها بالنسبة للمسام في المرحلة الثابتة. من حيث المبدأ ، سوف تنتقل الجزيئات الأكبر بشكل أسرع ، وتنتقل أولا ، وستسافر الجزيئات الأصغر أبطأ ، وتنتقل لاحقاإلى 14. وبالتالي، قد تحتوي كل Zn التي تحتوي على الذروة عدة مركبات ذات وزن جزيئي مماثل15. وهذا يسهم أيضا في التحدي المتمثل في تحديد الأنواع الكيميائية غير المعروفة من نوع Zn. وعلاوة على ذلك، تم اختبار العديد من ظروف استخراج خفيفة لاستخراج ZN. وكان ZN المستخرج منخفضة (~ 10٪). تم تطبيق ظروف استخراج معتدلة للحفاظ على الأنواع الكيميائية ZN سليمة ولكن هذا قد يكون للخطر كفاءة استخراج7.
في اختبار الذوبان في المختبر، الذوبان من Zn المكمل (كما النظير الراديو 65ZnCl2)أشارت إلى أن الأحماض الأمينية، وخاصة الهستيدين والليوزين، وزيادة قابلية الذوبان من ZN (الشكل 5). ويستند استخدام عينات الأعلاف مباشرة لاتقياسات الذوبان في المختبر تحت ظروف الجهاز الهضمي محاكاة على معرفة أن التغيير في الطيف زن هو الأسهق تعتمد16. ومع ذلك، قد تؤدي الظروف الحمضية في بداية الجهاز الهضمي إلى بعض التغيير في التكهنات التي قد تكون لا رجعة فيها (على سبيل المثال، ZnO-> ZnCl2، في وجود HCl في ظل ظروف حمضية في المعدة). ومع ذلك ، فإن مصدر Zn المستخدم هنا هو ZnSO4 وتم تحسين قابلية الذوبان من خلال الأحماض الأمينية في الوسط. وكان السؤال التالي الذي يتعين الإجابة عليه هو، هل يمكن ترجمة زيادة الذوبان إلى توافر؟ تم استخدام خط الخلايا المعوية RTgutGC لدراسة هذا السؤال. في سياق التغذية المعدنية في الحيوانات ، من الصعب تعريف مصطلح "التوافر" ويمكن تنظيمه بشكل تفاضلي في الخلايا (في المختبر) مقارنة بالحيوان (في الجسم الحي). ومن ثم، تم استخدام مصطلح "امتصاص" عندما يتعلق الأمر بتقييم المختبر باستخدام خط الخلايا المعوية. وقدم خط الخلية معلومات مفيدة عن آليات امتصاص Zn في ظهارة الأمعاء التي هي جزء من العملية التنظيمية المعقدة التي تحكم توافر المعادن في الحيوانات. وقد اكتسبت خلايا RTgutGC قدرة أفضل على امتصاص الزنى في وجود حمض أميني (أي الميثيونين؛ الشكل 6). ومع ذلك، فإن التوافر الواضح في الجسم الحي لم يختلف بشكل كبير بين مصادر Zn غير العضوية والعضوية في سمك السلمون الأطلسي. في دراسة توافر في الجسم الحي, تم إجراء مقارنة مصدر Zn في مستويات Zn الغذائية تتجاوز بكثير متطلبات Zn المعروفة من سمك السلمون الأطلسي17, مجموع تركيز ZN من 150 ملغم / كغ تغذية. يتم تصور الاختلافات في التوافر بشكل أفضل عندما تقع المستويات الغذائية التي تم اختبارها في النطاق الديناميكي الخطي قبل أن يصل الحيوان إلى التشبع. في الوقت الحاضر في دراسة الجسم الحي، فمن الممكن أن سمك السلمون الأطلسي كانت مشبعة بشكل جيد إلى الفرق الملحوظ في امتصاص زن بين المصادر المستخدمة.
وباختصار، وفرت الطريقة الأولى معلومات نوعية عن مختلف أنواع الزنا الكيميائية الموجودة في الجزء القابل للذوبان من علف السلمون الأطلسي؛ الطريقة الثانية, في الذوبان في المختبر من ZN تكملة تم تحسين في وجود ligands الأحماض الأمينية; وأكد الأسلوب الثالث أن تحسين الذوبان عن طريق الأحماض الأمينية يمكن أن يحسن امتصاص في ظهارة الأمعاء; وعلى العكس من ذلك، فشلت الطريقة الرابعة في العثور على اختلافات في توافر Zn من المصدر غير العضوي أو العضوي إلى سمك السلمون الأطلسي. وختاما، على الرغم من عدم اتساقها مع النتائج في الجسم الحي، فإن البروتوكولات في المختبر لم توفر رؤى مثيرة للاهتمام في فهم المكونات المختلفة لتوافر Zn.
Disclosures
وليس لدى صاحبي البلاغ ما يكشفان عنه.
Acknowledgements
وقد تم تنفيذ هذا العمل في إطار مشروع APREMIA (توافر المعادن ومتطلباتها في سلمون المحيط الأطلسي، المنحة رقم 244490) الممولة من قبل مجلس البحوث النرويجي.
Materials
| Name | Company | Catalog Number | Comments |
| 0.45 µm syringe filter | Sartorius | ||
| 0.45 μm membrane filter | Pall | ||
| 10 % fetal bovine serum | Eurobio | ||
| 1282 Compugamma Laboratory Gamma Counter | LKB Wallac | ||
| 24 well plates (Falcon, TPP microplates) | Thermo Fisher Scientific | 10048760 | |
| 2-aminobicyclo(2.2.1)heptane-2-carboxylic acid | Sigma Aldrich | A7902 | |
| 75 cm2 cell culture flasks (Falcon, TPP tissue culture flasks) | TPP Techno Plastic Products AG | 90075 | |
| L-Arginine | Sigma Aldrich | A5006 | |
| Bradford assay kit | Bio-Rad | 5000001 | |
| Centrifuge | Eppendorf Centrifuge 5702 | ||
| L-Cysteine | Sigma Aldrich | 30089 | |
| DL-methionine | Alfa Aesar | 59-51-8 | |
| D-methionine | Sigma Aldrich | M9375 | |
| Experimental fish feeds | Skretting | ||
| Glycine | Sigma Aldrich | 410225 | |
| Guard column, TSKgel SWxl Type (7 μm particle size) | Tosoh | ||
| L-Histidine | Sigma Aldrich | 53319 | |
| HPLC coupled with a 7500ce ICP-MS | Agilent Technologies | ||
| Hydrochloric acid | Emsure ACS, ISO, 37% w/w, Merck | 1.00317 | |
| Knife mill | GM 300, Retsch Gmbh | ||
| L-15 medium | Invitrogen/Gibco | 21083027 | |
| L-methionine | Sigma Aldrich | M9625 | |
| L-Lysine | Sigma Aldrich | 23128 | |
| Methanol | LiChrosolv, HPLC grade, Merck | 1.06035 | |
| Milli-Q water (18.2 MΩ cm) | EMD Millipore Corporation | ||
| Myoglobin | Sigma Aldrich | M1882 | |
| NexION 350D ICP-MS | Perkin Elmer | ||
| Pasteur pipette | VWR | ||
| pH meter | inoLab | ||
| Phosphate-buffered saline (PBS) | Sigma Aldrich | 806552 | |
| RTgutGC cells | Obtained in kind from Professor Dr. Kristin Schirmer, Dept. of Environmental Toxicology, Eawag, Swiss Federal Institute of Aquatic Science and Technology, Switzerland | ||
| SEC column, TSKgel G3000SWxl | Tosoh | ||
| Sieve stainless steel (850?μm - 1.12?mm) | Retsch | ||
| Sodium dodecyl sulphate (SDS) | Sigma Aldrich | 436143 | |
| Superoxide dismutase | Sigma Aldrich | S7571 | |
| Thyroglobulin | Sigma Aldrich | T1001 | |
| Tricaine methanesulphonate | PharmaQ | ||
| Tris(hydroxymethyl)aminomethane | Sigma Aldrich | 252859 | |
| Trypsin in 0.25% in phosphate-buffer saline | Biowest | L0910 | |
| Versene EDTA solution | Invitrogen/Gibco | 15040-033 | |
| Vitamin B12 | Sigma Aldrich | V2876 | |
| Zinc chelate of glycine | Phytobiotics | ||
| Zinc sulphate | Vilomix |
References
- Ytrestoyl, T., Aas, T. S., Asgard, T. Utilisation of feed resources in production of Atlantic salmon (Salmo salar) in Norway. Aquaculture. 448, 365-374 (2015).
- Prabhu, P. A. J., et al. Evaluating dietary supply of microminerals as a premix in a complete plant ingredient-based diet to juvenile rainbow trout (Oncorhynchus mykiss). Aquaculture Nutrition. 24 (1), 539-547 (2018).
- Maret, W. Zinc biochemistry: from a single zinc enzyme to a key element of life. Advances in nutrition. 4 (1), 82-91 (2013).
- Hogstrand, C., Wood, C. M., Farrell, A. P., Brauner, C. J. . Fish Physiology. 31, 135-200 (2011).
- Baeverfjord, G., et al. Mineral nutrition and bone health in salmonids. Reviews in Aquaculture. , (2018).
- Maage, A., Julshamn, K. Assessment of zinc status in juvenile Atlantic salmon (Salmo salar) by measurement of whole body and tissue levels of zinc. Aquaculture. 117 (1), 179-191 (1993).
- Silva, M. S., Sele, V., Sloth, J. J., Araujo, P., Amlund, H. Speciation of zinc in fish feed by size exclusion chromatography coupled to inductively coupled plasma mass spectrometry – Using fractional factorial design for method optimization and mild extraction conditions. Journal of Chromatography B. , (2018).
- Prabhu, A. J., et al. Zinc uptake in fish intestinal epithelial model RTgutGC: Impact of media ion composition and methionine chelation. Journal of Trace Elements in Medicine and Biology. 50, 377-383 (2018).
- Silva, M. S., et al. Apparent availability of zinc, selenium and manganese as inorganic metal salts or organic forms in plant-based diets for Atlantic salmon (Salmo salar). Aquaculture. 503, 562-570 (2019).
- Persson, D. P., Hansen, T. H., Laursen, K. H., Schjoerring, J. K., Husted, S. Simultaneous iron, zinc, sulfur and phosphorus speciation analysis of barley grain tissues using SEC-ICP-MS and IP-ICP-MS. Metallomics. 1 (5), 418-426 (2009).
- Lothian, A., Roberts, B. R. Standards for Quantitative Metalloproteomic Analysis Using Size Exclusion ICP-MS. Journal of Visualized Experiments. (110), (2016).
- Minghetti, M., Schirmer, K. Effect of media composition on bioavailability and toxicity of silver and silver nanoparticles in fish intestinal cells (RTgutGC). Nanotoxicology. 10 (10), 1526-1534 (2016).
- Glover, C. N., Hogstrand, C. Amino acid modulation of in vivo intestinal zinc absorption in freshwater rainbow trout. Journal of Experimental Biology. 205 (1), 151-158 (2002).
- Ekman, R., Ekman, R. . Mass spectrometry: Instrumentation, interpretation, and applications. Wiley Series on Mass Spectrometry. , 105-115 (2009).
- Hong, P., Koza, S., Bouvier, E. S. P. A Review Size-Exclusion Chromatography for the Analysis of Protein Biotherapeutics and Their Aggregates. Journal of Liquid Chromatography & Related Technologies. 35 (20), 2923-2950 (2012).
- Krezel, A., Maret, W. The biological inorganic chemistry of zinc ions. Archives of Biochemistry and Biophysics. 611, 3-19 (2016).
- National Research Council. . Nutrient Requirements of Fish and Shrimp. , (2011).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved