Method Article
Évaluation de la disponibilité des minéraux dans les aliments pour poissons à l’aide de méthodes complémentaires démontrées par l’exemple du zinc dans le saumon de l’Atlantique
Dans cet article
Résumé
Cet article explique en détail une approche systématique pour évaluer la disponibilité des microminéraux chez le saumon de l’Atlantique. La méthodologie comprend des outils et des modèles de complexité biologique croissante : (1) analyse de spéciation chimique, (2) solubilité in vitro, (3) études d’absorption dans des lignées cellulaires et (4) études in vivo sur les poissons.
Résumé
L’évaluation de la disponibilité des micro-minéraux alimentaires est un défi majeur dans la nutrition minérale des espèces de poissons. Le présent article vise à décrire une approche systématique combinant différentes méthodologies pour évaluer la disponibilité du zinc (Zn) chez le saumon atlantique (Salmo salar). Considérant que plusieurs espèces chimiques de Zn peuvent être présentes dans un aliment pour saumon de l’Atlantique, il a été émis l’hypothèse que la disponibilité du Zn est influencée par les espèces chimiques de Zn présentes dans l’aliment. Ainsi, dans cette étude, le premier protocole consiste à extraire les différentes espèces chimiques de Zn de l’aliment et à les analyser par une méthode de chromatographie d’exclusion de taille par spectroscopie de masse à plasma à couplage inductif (SEC-ICP-MS). Par la suite, une méthode in vitro a été mise au point pour évaluer la solubilité du Zn alimentaire dans les aliments pour saumons de l’Atlantique. Le troisième protocole décrit la méthode permettant d’étudier l’impact de la modification de la composition chimique des espèces chimiques de Zn sur l’absorption de Zn dans un modèle épithélial intestinal de poisson utilisant une lignée cellulaire intestinale de truite arc-en-ciel (RTgutGC). Ensemble, les résultats des méthodes in vitro ont été comparés à une étude in vivo examinant la disponibilité apparente de sources inorganiques et organiques de Zn supplémentées aux aliments pour saumons de l’Atlantique. Les résultats ont montré que plusieurs espèces chimiques de Zn peuvent être trouvées dans les aliments pour animaux et que l’efficacité d’une source organique de Zn dépend beaucoup du ligand d’acide aminé utilisé pour chélater le Zn. Les résultats des méthodes in vitro avaient moins de corrélation avec ce résultat de l’étude in vivo. Néanmoins, les protocoles in vitro décrits dans cet article ont fourni des informations cruciales concernant la disponibilité du Zn et son évaluation dans les aliments pour poissons.
Introduction
La farine et l’huile de poisson étaient traditionnellement utilisées dans l’alimentation du saumon de l’Atlantique. Cependant, ces ingrédients sont de plus en plus remplacés par des ingrédients d’origine végétale1. Le changement susmentionné dans la composition des aliments pour animaux a entraîné une faible disponibilité alimentaire et un besoin accru d’améliorer la disponibilité des minéraux dans les aliments pour saumons de l’Atlantique, en particulier le zinc (Zn)2. La disponibilité réduite pourrait être le résultat d’une modification du niveau de Zn, des espèces chimiques de Zn et/ou des facteurs antinutrionnels présents dans la matrice alimentaire. Dans ce scénario, une nouvelle gamme d’additifs considérés de manière générique comme des « sources organiques » a émergé avec le potentiel d’être une meilleure source disponible de minéraux alimentaires pour les poissons. Par conséquent, il est important de comprendre la chimie et la physiologie fondamentales régissant la disponibilité des minéraux et de leurs sources pour les poissons. Le zinc est un oligo-élément essentiel pour tous les organismes vivants3. Le rôle du Zn en tant que molécule de signalisation a été décrit à la fois au niveau paracellulaire et intracellulaire chez lespoissons 4. Chez le saumon atlantique, le déficit en Zn a été associé à des anomalies squelettiques et à une activité réduite de diverses métalloenzymesZn 5,6.
Cette étude décrit une approche systématique pour comprendre la disponibilité du Zn en le catégorisant en quatre compartiments différents de complexité chimique et biologique variée. Les méthodes impliquées sont décrites en quatre sections, comme on peut le voir à la figure 1: (1) évaluation des espèces chimiques Zn dans la fraction soluble d’un aliment pour saumon de l’Atlantique à l’aide d’une méthode de chromatographie de masse à plasma à couplage inductif d’exclusion de taille (SEC-ICP-MS)7; 2) solubilité in vitro du Zn supplémenté dans les aliments pour saumons de l’Atlantique; (3) évaluation de l’absorption des espèces chimiques Zn par modèle intestinal in vitro (RTgutGC)8; et (4) disponibilité apparente de Zn dans le saumon de l’Atlantique (Salmo salar)9. Des protocoles similaires peuvent être élaborés pour d’autres minéraux (p. ex. manganèse, sélénium, cuivre) pouvant présenter un intérêt nutritionnel pour les espèces de poissons aquacoles.
Protocole
L’essai d’alimentation de la rubrique 4 a été réalisé conformément à la législation norvégienne (FOR-2015-06 - 18-761) et européenne (directive 2010/63/UE).
1. Évaluation des espèces chimiques de Zn dans la fraction soluble d’un aliment pour saumon de l’Atlantique à l’aide d’une méthode SEC-ICP-MS
- Tampon d’extraction (100 mM Tris-HCl, pH 8,5)
- Préparer le tampon d’extraction en dissolvant une quantité appropriée de tris(hydroxyméthyl)aminométhane pour atteindre la force ionique souhaitée (100 mM) dansH2Oultrapur.
- Ajuster le pH de la solution à pH 8,5 avec la solution HCl, en surveillant le changement de pH avec un pH-mètre.
- Préparation d’échantillons d’aliments pour animaux
REMARQUE : L’échantillon d’aliments utilisé a été formulé à partir d’aliments commerciaux pour saumon de l’Atlantique, contenant des sources de protéines provenant principalement d’ingrédients d’origine végétale (c.-à-d. environ 5 % de protéines de poisson, 10 % d’huile de poisson, 68 % de protéines végétales et 12 % d’huile végétale). Le sulfate de zinc a été complété par l’aliment.- Broyer l’échantillon d’aliments à la main à l’aide d’un pilon et d’un mortier.
- Tamiser l’échantillon d’alimentation pour s’assurer que l’extraction est effectuée dans une fraction d’alimentation de taille de particules similaire (de 850 μm à 1,12 mm).
- Procédez à l’extraction Zn.
- Extraction du zinc à partir d’un échantillon d’alimentation
- Peser environ 0,5 g d’aliment en triple exemplaire dans des tubes coniques de 15 mL.
- Ajouter le tampon d’extraction (5 mL de 100 mM Tris-HCl, pH 8,5) aux échantillons.
- Extraire les échantillons dans un rotateur (20 tr/min) à 4 °C pendant 24 h.
- Séparer les fractions solubles et non solubles par centrifugation pendant 10 min à 3000 x g.
- Utilisez un filtre à seringue jetable de 0,45 μm pour filtrer la fraction soluble.
- Transférer les échantillons filtrés dans des tubes propres.
- Effectuer l’analyse de spéciation du Zn dans les fractions solubles à l’aide de SEC-ICP-MS, comme décrit à l’étape 1.6.
REMARQUE : Un résumé de la procédure d’extraction du Zn à partir d’un échantillon d’alimentation est décrit à la figure 2.
- Solution de phase mobile (50 mM Tris-HCl + 3% MeOH, pH 7,5)
- Préparer la solution de phase mobile en dissolvant 6,057 g de tris(hydroxyméthyl)aminométhane dans 1 L de solution de MeOH à 3 % (v/v).
- Ajuster le pH de la solution à un pH de 7,5 avec la solution HCl, en surveillant le changement de pH avec un pH-mètre.
- Filtrer la solution de phase mobile à travers un filtre à membrane de 0,45 μm.
- Étalonnage en poids moléculaire de la plage de séparation des colonnes SEC
- Calibrer la plage de séparation en effectuant un étalonnage de masse moléculaire.
REMARQUE: Dans cette étude, la thyroglobuline (660 kDa), la superoxyde dismutase Zn / Cu (32 kDa), la myoglobine (17 kDa) et la vitamine B12 (1,36 kDa) ont été utilisées. - Préparer chacune des étalons avec une concentration connue en H2O ultrapur.
- Préparer un flacon de chromatographie liquide à haute performance (CLHP) en ajoutant 250 μL d’étalon à un flacon.
- Chargez les flacons avec des étalons pour la séquence des échantillons.
- Effectuer l’étalonnage du poids moléculaire au début et à la fin de la séquence analytique, en surveillant 127I (thyroglobuline), 66Zn (superoxyde dismutase Zn/Cu), 57Fe (myoglobine) et 59Co (vitamine B12).
REMARQUE: L’étalonnage du poids moléculaire est effectué simultanément avec l’analyse de spéciation Zn.
- Calibrer la plage de séparation en effectuant un étalonnage de masse moléculaire.
- Analyse de la spéciation du zinc à l’aide de SEC-ICP-MS
NOTE: L’analyse de la spéciation du Zn par la méthode SEC-ICP-MS a été développée sur la base des principes décrits ailleurs10,11 et une optimisation supplémentaire a été effectuée pour l’analyse d’un aliment pour saumon de l’Atlantique7.- Effectuer l’analyse de spéciation Zn sur les fractions solubles à l’aide d’une colonne de chromatographie d’exclusion de taille (SEC) et d’une CLHP couplée à une spectroscopie de masse à plasma à couplage inductif (ICP-MS).
- Préparer un flacon HPLC en ajoutant 250 μL de fraction soluble à un flacon.
- Avant l’analyse, augmentez tous les échantillons avec 0,5 μL de vitamine B12. Cette étape permet de corriger les temps de rétention des quarts de travail, en surveillant 59Co.
- Diluer la fraction soluble avec un tampon d’extraction (100 mM Tris-HCl, pH 8,5) et ajuster à un volume final de 1 mL.
- Préparez l’exécution séquentielle des échantillons dans un ordre aléatoire.
- Réglez l’ICP-MS selon les instructions du fabricant.
- Suivez les paramètres de l’instrument pour la CLHP et l’ICP-MS en effectuant l’analyse de spéciation Zn (voir Tableau 1).
2. Solubilité in vitro du Zn supplémenté dans les aliments pour saumons de l’Atlantique
REMARQUE : L’échantillon d’aliments utilisé a été formulé à partir d’aliments commerciaux pour le saumon de l’Atlantique, contenant des sources de protéines provenant principalement d’ingrédients d’origine végétale (c.-à-d. environ 5 % de farine de poisson, 10 % d’huile de poisson, 68 % d’ingrédients d’origine végétale et 12 % d’huile végétale).
- Broyer les échantillons d’aliments pour saumon de l’Atlantique pendant 10 s à 3000 tr/min à l’aide d’un broyeur à couteaux et conserver à 4 °C jusqu’à une analyse plus approfondie.
- Peser environ 0,2 g des échantillons d’alimentation broyés à l’étape 2.1 et ajouter le radiotraceur Zn(65Zn) d’activité spécifique connue dans un tube d’échantillon de volume de 5 mL (avec un bouchon).
ATTENTION : Cette procédure doit être effectuée à l’intérieur d’une suite de radionucléides. La personne qui effectue cette étape doit être formée et certifiée pour manipuler les radio-isotopes. Les mesures de sécurité et de précaution conseillées par l’administration de la radioprotection de l’institut doivent être strictement suivies. - Ensuite, préparez la solution tampon luminale intestinale d’eau douce comme décrit ci-dessous.
- Pour la solution saline A, peser 11,65 g de NaNO3,0,55 g de KNO3 et 0,4 g de MgSO4. Dissoudre les sels dans H2O ultrapur et ajuster à un volume final de 60 mL.
- Pour la solution saline B, peser 0,31 g de Ca(NO3)2· 4 H2O. Dissoudre les sels dans H2O ultrapur et ajuster à un volume final de 10 mL.
- Utiliser la solution mère HEPES de 500 mM comme solution saline C.
- Pour la solution saline D, peser 1,2 g deMgCl2,dissoudre le sel dans H2O ultrapur et ajuster à un volume final de 20 mL.
- Pour la solution saline E, peser 0,9 g deMgSO4,dissoudre le sel dansH2Oultrapur et ajuster à un volume final de 20 mL.
- Préparer la solution de pyruvate en dissolvant 0,55 g de CH3COCOONa dans 10 mL de H2Oultrapur.
- Dissoudre 0,9 g de galactose(C6H12O6)dans H2O ultrapur.
- Bien dissoudre à l’aide d’un agitateur magnétique et stériliser les solutions salines A, B, D et E par autoclavage, et la solution C, le pyruvate et le galactose par filtration à travers un filtre à seringue de 200 μm.
- Après préparation des différentes solutions types, pour préparer 100 mL de solution de travail du tampon, mélanger les solutions préparées ci-dessus dans la proportion suivante: 6,8 mL de solution saline A, 4,14 mL de B, 5 mL de C, 2,5 mL de D, 1,5 mL de E et 1,14 mL chacun de pyruvate et de galactose. Porter le volume à 100 mL en utilisant de l’eau désionisée.
REMARQUE: Le tampon ci-dessus représentera maintenant la composition ionique de la lumière intestinale trouvée dans les salmonidés d’eau douce.
- Préparer six autres aliquotes du tampon décrit à l’étape 2.6 et ajouter l’un des acides aminés suivants (cystéine, méthionine, glycine, histidine, lysine et arginine) pour atteindre une concentration molaire finale de 5 mM.
- Ajouter le tampon luminal intestinal d’eau douce (volume de réaction = 3 mL; pH 7,4) à l’échantillon d’alimentation.
- Répétez l’étape 2.5 avec les tampons décrits au point 2.4 (en présence de différents acides aminés à une concentration de 5 mM).
- Fermez les tubes et laissez-les tourner dans une essoreuse rotative pendant 30 min à 25 tr/min.
- Séparer les fractions solubles et non solubles par centrifugation pendant 10 min à 1157 x g.
- Utilisez un guichet gamma pour mesurer les comptes par minute (cpm) de 65Zn dans les fractions solubles et non solubles.
- Calculer la proportion des radio-isotopes du Zn(65Zn) présents dans les fractions solubles et non solubles.
3. Évaluation de l’absorption des espèces chimiques Zn à l’aide d’un modèle intestinal in vitro (RTgutGC)
- Culture de cellules RTgutGC
REMARQUE: Tous les matériaux de travail utilisés dans cette étape doivent être stériles.- Faire revivre doucement les cellules RTgutGC congelées au bain-marie fixé à 20 °C.
- Pipeter doucement la solution contenant les cellules et les suspendre dans 10 mL de milieu L15 contenant 10% de sérum fœtal bovin (FBS).
REMARQUE: 10% FBS n’est utilisé que pour raviver les cellules congelées. Pour le passage ultérieur, FBS est utilisé à 5%. La composition de FBS peut varier d’un lot à l’autre, il est donc conseillé d’acheter et de stocker autant que nécessaire à partir d’un seul lot pour éviter les variations inter-lots de la composition sérique. - Ajouter la suspension cellulaire à 75 cm2 flacons de culture cellulaire et incuber dans un incubateur réglé à 19 °C sous atmosphère normale.
- Vérifiez les cellules et, lorsqu’elles sont confluentes (confluence à 80%, évaluez visuellement en examinant la densité de la surface cellulaire au microscope), divisez les cellules en nouvelles fioles (passage ultérieur) ou récoltez-les pour les utiliser dans des expériences.
REMARQUE: Un exemple des cellules RTgutGC 1 h et 1 semaine après l’ensemencement dans les flacons de culture cellulaire est illustré à la figure 3.
- Récolte de cellules et préparation aux expériences d’exposition
- Laver les cellules deux fois avec 1 mL de solution d’acide éthylènediaminetétraacétique (EDTA). Après chaque lavage, siphonner la solution d’EDTA à l’aide d’un tube d’aspiration stérile.
- Traiter les cellules avec de la trypsine (0,7 mL de trypsine, dans 0,25 % dans une solution saline tamponnée au phosphate [PBS]).
- Faites tourner doucement la fiole à des angles aigus pour répandre la trypsine tout le long de la surface de la fiole.
- Continuez la rotation pendant 2 min, pendant que les cellules se détachent.
- Après avoir tourné doucement pendant 2 min, ajouter 10 mL de milieu L15/FBS pour neutraliser la trypsine.
- Décanter la suspension cellulaire résultante dans un tube de centrifugeuse à fond conique à l’aide d’une pipette stérile et d’une centrifugeuse pendant 3 min à 130 x g.
- Déterminer la densité des cellules récoltées par comptage manuel à l’aide d’un hémocytomètre.
- Ajouter le volume requis de milieu L15/FBS pour atteindre une densité cellulaire de 5 x 104 cellules/mL.
- Ensemencez les cellules sur des plaques de 24 puits en pipetant 1 mL de suspension cellulaire par puits pour atteindre la densité cellulaire finale de 5 x 104 cellules/puits.
REMARQUE: Utilisez de préférence des pipettes multi-distributions pour minimiser les variations et réduire le temps. - Placer les plaques ensemencées dans un incubateur sous atmosphère normale à 19 °C pendant 48 h avant les expériences.
REMARQUE: Trypsine à stocker à -20 °C; Solution EDTA et support L15/FBS à 4 °C. Réglez la température de toutes les solutions de travail et de tous les supports à 19 °C juste avant utilisation.
- Préparation des milieux d’exposition
REMARQUE: Cette étape doit être effectuée sous la hotte dans des conditions aseptiques et stériles.- Préparer L15/ex en mélangeant 6,8 mL de solution saline A (étape 2.3.1), 1,14 mL de B (étape 2.3.2), 5 mL de C (étape 2.3.3) et 1,14 mL chacun de pyruvate (étape 2.3.6) et de galactose (étape 2.3.7). Porter le volume à 100 mL à l’aide d’eau distillée stérile de qualité culture cellulaire.
- Préparer FW en mélangeant 6,8 mL de solution saline A (2.3.1), 4,14 mL de B (2.3.2), 5 mL de C (2.3.3), 2,5 mL de D (2.3.4), 1,5 mL de E (2.3.5) et 1,14 mL de pyruvate (2.3.6) et de galactose (2.3.7). Porter le volume à 100 mL à l’aide d’eau distillée stérile de qualité culture cellulaire.
- Quantifier les concentrations d’ions dans les milieux d’exposition à l’aide de l’ICP-MS comme décritailleurs 12.
NOTE : Les concentrations ioniques analysées dans les milieux préparés sont présentées dans le tableau 2.
- Dosages d’afflux de zinc(65Zn)
- Ensemencez les cellules RTgutGC sur des plaques de 24 puits (5 x10 4 cellules/puits) dans un milieu L15/FBS complet.
- Incuber pendant 48 h dans un incubateur à atmosphère normale à 19 °C.
- Ajuster toutes les préparations expérimentales au pH 7,4 en utilisant 0,5 M de NaOH en présence ou en l’absence de L-méthionine (L-Met) ou de DL-méthionine (DL-Met) à une concentration de 2 mM.
REMARQUE: L’ajustement du pH des tampons décrit au point 3.4.3 doit être effectué récemment avant le traitement des cellules à l’étape 3.4.5. - Une fois la période d’incubation terminée, retirez le milieu des puits et rincez abondamment avec du PBS.
- Ajouter le milieu expérimental FW ajusté au pH et laisser s’acclimater pendant 20 min.
- Exposer les cellules RTgutGC à des concentrations nominales de 3,07, 6,14, 12,27 et 24,55 μM 65Zn(II) (sous forme de ZnCl2; ~4 kBq/mL) dans le milieu décrit à l’étape 3.4.3.
- Immédiatement après, maintenez les cellules dans l’incubateur à 19 °C pendant 15 min.
- Une fois l’incubation de 15 minutes terminée, aspirez le surnageant de culture et retirez-le du puits.
- Rincez les cellules avec un milieu FW glacé (avec 200 μM Zn, pH 7,4), puis éteignez-les en ajoutant le tampon d’acide tétraacétique (pH 7,4) de 5 mM d’éthylène glycol-bis(β-aminoéthylique)-N,N,N',N'-tétraacétique (EGTA) pendant 5 min, pour se débarrasser de tout 65Zn(II) adsorbé.
- Exposer les cellules aux préparations de milieux ci-dessus en présence ou en l’absence de 10 mM d’acide 2-aminobicyclo [2.2.1] heptane-2-carboxylique (BCH), un inhibiteur du transport des acides aminés.
- Après la période d’exposition de 15 min, répétez les étapes 3.4.8 et 3.4.9.
- Les cellules RtgutGC seront collées au fond des puits en monocouche. Digérez les cellules à l’aide d’un détergent à 0,2 % de dodécylsulfate de sodium chaud (FDS) (100 μL/puits).
REMARQUE: La solution SDS doit être placée pendant 1 h dans un bain-marie réglé à 90 ° C avant utilisation. - Aspirer et récupérer le digestat cellulaire dans un tube de 1,5 mL.
- Mesurer la radioactivité des digestes cellulaires à l’aide d’un compteur gamma.
REMARQUE: Les comptes par minute (cpm) doivent être corrigés pour la désintégration radioactive, l’activité de fond et sont soumis à des calculs d’activité spécifiques selon les formules décrites par Glover et Hogstrand13. - Pour quantifier la concentration protéique des cellules, homogénéiser les cellules avec 500 μL de 0,5 M NaOH.
- Utilisez un kit de dosage Bradford pour mesurer la concentration en protéines dans l’échantillon cellulaire, avec l’albumine sérique bovine (BSA) comme norme.
REMARQUE: Une fois la concentration en protéines quantifiée, le taux d’absorption de Zn par les cellules RTgutGC peut être exprimé en pmoles Zn min-1 mg-1 protéine.
4. Disponibilité apparente de Zn alimentaire dans le saumon de l’Atlantique (Salmo salar)
REMARQUE : Les aliments pour saumon de l’Atlantique ont été formulés à partir d’aliments commerciaux, contenant des sources de protéines provenant principalement d’ingrédients d’origine végétale (c.-à-d. environ 5 % de protéines de poisson, 10 % d’huile de poisson, 68 % de protéines végétales et 12 % d’huile végétale). Deux aliments ont été complétés par une source inorganique (sulfate de Zn) ou une source organique (chélate de Zn de glycine) pour atteindre une concentration de Zn de 150 mg/kg d’aliment. De plus, de l’oxyde d’yttrium (qualité d’alimentation) a été ajouté à l’aliment à 0,01 % en tant que marqueur inerte pour permettre le calcul du coefficient de disponibilité apparente.
- Acclimater le saumon de l’Atlantique (souche SalmoBreed, âge 1+ ans, groupes mixtes) dans leurs bassins respectifs jusqu’à ce que les poissons soient habitués aux conditions expérimentales.
- Évaluer l’acclimatation du saumon de l’Atlantique en surveillant sa consommation quotidienne d’aliments.
REMARQUE: Cet essai a été effectué dans des réservoirs triples, donc un total de six réservoirs ont été utilisés. Au cours de l’essai d’alimentation, la température de l’eau était de 11,9 ± 0,3 °C et la saturation en oxygène dissous était de 101 ± 5 %. - Nourrissez les poissons avec des aliments expérimentaux pendant 11 jours.
- Euthanasier le poisson par surdosage en utilisant 6 mL de solution stock de méthanesulfonate de tricaïne par litre d’eau.
- Prélever un échantillon regroupé d’excréments du poisson du même aquarium dans une assiette en les rayant de la nageoire ventrale à l’anus.
- Retirer les matières fécales de la plaque à l’aide d’une spatule dans un tube conique de 50 mL et conserver immédiatement les échantillons à -20 °C.
NOTE: Les échantillons ont été conservés à -20 °C jusqu’à une analyse plus approfondie. - Lyophilisation des échantillons de matières fécales pendant 72 h à -80 °C.
- Homogénéiser manuellement l’échantillon de matières fécales en une poudre fine à l’aide d’un pilon et d’un mortier.
- Déterminer la concentration de Zn et d’Yttrium dans les échantillons d’aliments et de matières fécales à l’aide d’un ICP-MS (tel que décrit ailleurs9).
- Déterminer le coefficient de disponibilité apparente (CAA, %) à l’aide de la formule suivante :

Résultats
Évaluation des espèces chimiques de Zn dans la fraction soluble d’un aliment pour saumon de l’Atlantique à l’aide d’une méthode SEC-ICP-MS
La méthode SEC-ICP-MS fournit des données sur les espèces chimiques Zn présentes dans la fraction soluble de l’alimentation du saumon de l’Atlantique. La figure 4 illustre le profil chromatographique du Zn présent dans la fraction soluble. Ce chromatogramme a été obtenu à l’aide de la méthode SEC-ICP-MS. Cinq pics contenant du Zn ont été trouvés dans les fractions solubles de l’alimentation du saumon de l’Atlantique. Chaque pic a un poids moléculaire différent; pic un (~ 600 kDa), pic deux et pic trois (de 32 à 17 kDa), pic quatre (de 17 à 1,36 kDa) et pic cinq (> 1,36 kDa). Le pic quatre était le plus abondant, suivi du pic deux, trois, cinq et un, respectivement. Les espèces chimiques de Zn présentes dans la fraction soluble peuvent avoir différentes sources parce que l’aliment utilisé contient à la fois des ingrédients d’origine marine et végétale, et une forme supplémentée (c.-à-d. sulfate de Zn). La gamme de poids moléculaire des espèces chimiques Zn suggère que ces composés pourraient être des métalloprotéines.
Solubilité in vitro du Zn supplémenté dans les aliments pour saumons de l’Atlantique
La solubilité du 65Zn supplémenté a augmenté en présence d’acides aminés. Tous les acides aminés testés ont augmenté la solubilité de 65Zn supplémentés. Méthionine, glycine, cystéine, histidine et lysine ont amélioré la solubilité de 65Zn; une solubilité plus élevée a été trouvée avec l’histidine et la lysine (Figure 5).
Évaluation de l’absorption des espèces de Zn à l’aide d’un modèle intestinal in vitro (RTgutGC)
L’absorption apicale de zinc dans les cellules RTgutGC a été significativement influencée par la présence de L-Met ou de DL-Met à des concentrations de 2 mM. En outre, l’impact de la méthionine sur l’absorption du Zn dans les cellules RTgutGC a été affecté négativement par la présence de BCH (un bloqueur du système de transport des acides aminés), par rapport aux cellules non traitées avec BCH (Figure 6).
Disponibilité apparente du Zn alimentaire dans le saumon de l’Atlantique (Salmo salar)
Dans les aliments pratiques pour le saumon de l’Atlantique, la disponibilité apparente de Zn était la même lorsqu’il s’agissait d’une source inorganique (sulfate de Zn) ou d’une source organique (chélate de Zn de glycine). Les valeurs estimées de la disponibilité apparente de Zn (%, n = 3) chez le saumon de l’Atlantique étaient de 31 % ± 12 % en cas de supplémentation avec une source inorganique (sulfate de Zn) et de 31 % ± 3 % en complétant une source organique (chélate de Zn de glycine).
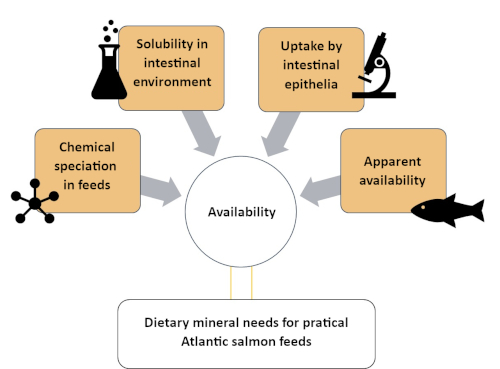
Figure 1: Résumé de l’approche systématique d’évaluation de la disponibilité des minéraux à l’aide de méthodes complémentaires. Cette approche a été utilisée pour étudier la disponibilité du zinc chez le saumon de l’Atlantique, y compris la spéciation du Zn, la solubilité du Zn dans l’environnement intestinal, l’absorption du Zn par les cellules intestinales et la disponibilité apparente du Zn. Veuillez cliquer ici pour voir une version agrandie de cette figure.
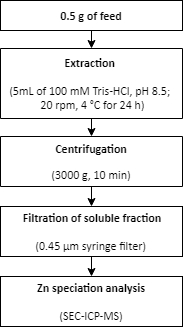
Figure 2: Résumé de la procédure d’extraction du Zn à partir d’un échantillon d’alimentation. Le zinc est extrait d’un échantillon d’alimentation en utilisant des conditions d’extraction douces. L’extraction est suivie d’une analyse de spéciation Zn. Veuillez cliquer ici pour voir une version agrandie de cette figure.
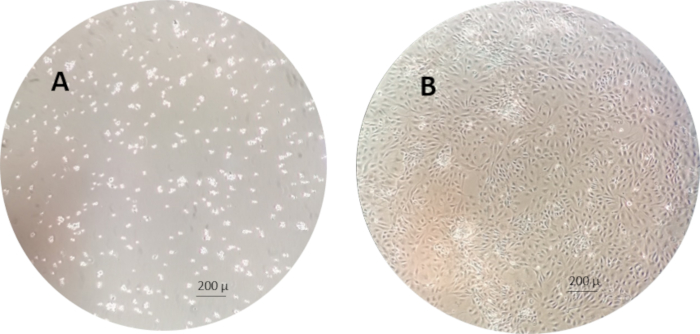
Figure 3: Exemple des cellules RTgutGC 1 h (à gauche) et 1 semaine (à droite) après l’ensemencement dans les flacons de culture cellulaire. Veuillez cliquer ici pour voir une version plus grande de cette figure.
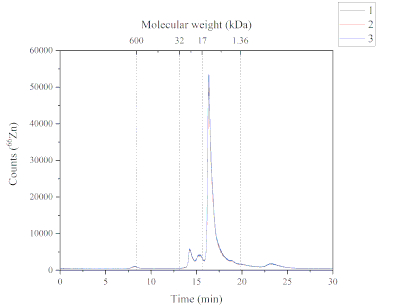
Figure 4: Chromatogramme montrant les pics contenant du Zn provenant de la fraction soluble des aliments pour saumons de l’Atlantique et analysé par SEC-ICP-MS. Les trois répliques sont caractérisées par les lignes bleues, rouges et noires. Un étalonnage du poids moléculaire a été effectué à l’aide de thyroglobuline (660 kDa, surveillance 127I), de superoxyde dismutase Zn/Cu (32 kDa, surveillance 66Zn), de myoglobine (17 kDa, surveillance 57Fe), de vitamine B12 (1,36 kDa, surveillance 59Co); Crête 1 (P1): ~600 kDa, temps de rétention (RT) 8,2 min; Pic 2+3 (P2+3) : de 32 à 17 kDa, RT 14,2 + 15,3 min ; Crête 4 (P4) : de 17 à 1,36 kDa, RT 16,3 min ; Pic 5 (P5): > 1,36 kDa, Rt 23,2 min. Veuillez cliquer ici pour voir une version plus grande de cette figure.
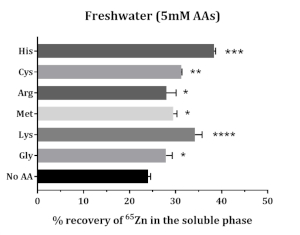
Figure 5: L’impact des acides aminés sur la solubilité in vitro du Zn supplémenté dans l’alimentation du saumon de l’Atlantique. Les données sont présentées comme moyennes ± ET (n = 3). Les données ont été analysées au moyen d’une ANOVA unidirectionnelle, suivie du test de comparaison multiple de Dunnet, comparant la moyenne de chaque groupe AA avec celle du groupe témoin (pas de AA). Les astérisques indiquent le niveau de signification de l’ANOVA (valeurs P < 0,05 (*), < 0,01 (**), < 0,001 (***) et < 0,0001 (****)). Veuillez cliquer ici pour voir une version agrandie de cette figure.
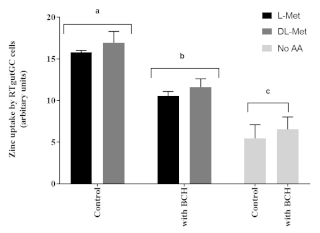
Figure 6: L’influence de la méthionine et d’un inhibiteur du transport des acides aminés (acide 2-Aminobicyclo [2.2.1] heptane-2-carboxylique, BCH, 10 mM). Les données sont présentées comme moyennes ± ET (n = 3). Les données ont été analysées par le biais d’ANOVA bidirectionnelle, suivie du test de comparaison multiple de Tukey avec p < niveau de signification de 0,05. Les différences post-hoc entre les groupes sont représentées par une lettre en exposant au-dessus des barres; les barres avec des exposants différents sont statistiquement différentes (p < 0,05). Veuillez cliquer ici pour voir une version agrandie de cette figure.
| Paramètres HPLC | |
| Colonne | Colonne SEC (30 cm x 7,8 mm, taille des particules de 5 μm) + colonne de garde (taille des particules de 7 μm) |
| Plage d’étalonnage | 1,0 × 104 - 5,0 × 105 Da |
| Phase mobile | 50 mM Tris-HCl + 3% MeOH (pH 7,5) |
| Débit | 0,7 mL min−1 |
| Volume d’injection | 50 μL |
| Paramètres ICP–MS | |
| Puissance avant | 1550 W |
| Flux de gaz plasma | 15,0 L min−1 |
| Flux de gaz porteur | 0,86 L min−1 |
| Flux de gaz d’maquillage | 0,34 L min−1 |
| Temps de séjour | 0,1 s par isotope |
| Isotopes surveillés | 127 I, 66Zn, 59Co, 57Fe |
Tableau 1. Vue d’ensemble des paramètres de l’instrument pour la CLHP et l’ICP-MS.
| Composition chimique (mM) | L15/ex | Milieu expérimental (L15/FW) |
| Nitrate de sodium | 155 | 155 |
| Nitrate de potassium | 6.2 | 6.2 |
| Sulfate de magnésium | 3.8 | 19.5 |
| Nitrate de calcium | 1.5 | 5.4 |
| HEPES | 5 | 5 |
| Chlorure de magnésium | - | 15 |
| Pyruvate de sodium | 5.7 | 5.7 |
| Galactose | 5.7 | 5.7 |
| pH | 7.1 | 7.4 |
| Force ionique | 178 | 258 |
| Composition ionique (mM) | ||
| Calcium, Ca2+ * | 1,6 ± 0,1 | 5,3 ± 0,2 |
| Magnésium, Mg2+ * | 3,9 ± 0,3 | 32,5 ± 0,7 |
| Potassium, K+ * | 8.2 ± 1.2 | 8,6 ± 1,1 |
| Sodium, Na+ * | 160 ± 3 | 157 ± 2 |
| Nitrate, NO3- ** | 164 | 172.4 |
| Sulfate, SO4- ** | 3.8 | 18.7 |
| Chlorure, Cl- ** | 1.5 | 31.5 |
Tableau 2. La composition chimique et ionique des milieux expérimentaux testés.
Discussion
L’absorption intestinale du Zn semble être influencée par la forme chimique de l’espèce Zn13. À cet égard, l’utilisation des protocoles décrits dans cet article a permis d’étudier séquentiellement les aspects chimiques et biologiques sous-jacents à la « disponibilité » du Zn chez le saumon atlantique.
Cette étude a rapporté l’utilisation d’une méthode d’analyse de spéciation Zn. La méthode SEC-ICP-MS a fourni des données qualitatives concernant le poids moléculaire des espèces chimiques Zn présentes dans la fraction soluble d’un aliment pour saumon de l’Atlantique. Ceci a été réalisé en comparant les temps de rétention des étalons d’étalonnage du poids moléculaire (c.-à-d. thyroglobuline (660 kDa), superoxyde dismutase Zn/Cu (32 kDa), myoglobine (17 kDa) et vitamine B12 (1,36 kDa)) avec les temps de rétention des pics contenant du Zn. Un défi trouvé dans l’analyse de la spéciation du Zn était l’identification de l’espèce chimique inconnue du Zn en raison de l’absence de normes analytiques. Dans la SEC, la séparation des molécules est basée sur leur taille par rapport aux pores en phase stationnaire. En principe, les molécules plus grosses voyageront plus vite, éluant d’abord, et les molécules plus petites voyageront plus lentement, éluant plus tard14. Par conséquent, chaque pic contenant du Zn peut contenir plusieurs composés de poids moléculaire similaire15. Cela contribue également au défi d’identifier les espèces chimiques inconnues de Zn. De plus, plusieurs conditions d’extraction légères ont été testées pour l’extraction du Zn. Le Zn extrait était faible (~10%). Des conditions d’extraction douces ont été appliquées pour garder intactes les espèces chimiques Zn, mais cela a pu compromettre l’efficacité de l’extraction7.
Dans le test de solubilité in vitro, la solubilité du Zn supplémenté (sous forme de radio-isotope 65ZnCl2)a indiqué que les acides aminés, en particulier l’histidine et la lysine, augmentaient la solubilité du Zn(Figure 5). L’utilisation d’échantillons d’aliments directement pour des tests de solubilité in vitro dans des conditions gastro-intestinales simulées est basée sur la connaissance que le changement dans la spéciation du Zn dépend du pH16. Cependant, les conditions acides au début du tractus gastro-intestinal peuvent entraîner un changement dans la spéciation qui pourrait être irréversible (par exemple, ZnO -> ZnCl2, en présence de HCl dans des conditions acides dans l’estomac). Néanmoins, la source de Zn utilisée ici est le ZnSO4 et dont la solubilité a été améliorée par les acides aminés dans le milieu. La question suivante à laquelle il fallait répondre était la suivante: la solubilité accrue peut-elle être traduite en disponibilité? La lignée cellulaire intestinale RTgutGC a été utilisée pour étudier cette question. Dans le contexte de la nutrition minérale chez les animaux, le terme « disponibilité » est difficile à définir et peut être régulé différemment dans les cellules (in vitro) par rapport à un animal (in vivo). Par conséquent, le terme « absorption » a été utilisé lorsqu’il s’agissait de l’évaluation in vitro à l’aide de lignées cellulaires intestinales. La lignée cellulaire a fourni des informations utiles sur les mécanismes d’absorption du Zn au niveau de l’épithélium intestinal, qui fait partie du processus de régulation complexe qui régit la disponibilité des minéraux chez les animaux. Les cellules RTgutGC ont obtenu une meilleure capacité d’absorption apicale du Zn en présence d’un acide aminé (c.-à-d. la méthionine; Figure 6). Cependant, la disponibilité apparente in vivo ne différait pas significativement entre les sources inorganiques et organiques de Zn dans le saumon de l’Atlantique. Dans l’étude de disponibilité in vivo, la comparaison de la source de Zn a été faite à des niveaux de Zn alimentaire dépassant largement les besoins connus en Zn du saumon atlantique17, concentration totale de Zn de 150 mg / kg d’aliment. Les différences de disponibilité sont mieux visualisées lorsque les niveaux alimentaires testés tombent dans la plage dynamique linéaire avant que l’animal n’atteigne la saturation. Dans la présente étude in vivo, il est possible que le saumon de l’Atlantique était bien saturé à la différence observée dans l’absorption du Zn entre les sources utilisées.
En résumé, la première méthode a fourni des informations qualitatives sur les différentes espèces chimiques de Zn trouvées dans la fraction soluble d’un aliment pour saumon de l’Atlantique; la deuxième méthode, la solubilité in vitro du Zn supplémenté a été améliorée en présence de ligands d’acides aminés; la troisième méthode a confirmé qu’une solubilité améliorée par les acides aminés peut améliorer l’absorption au niveau de l’épithélium intestinal; à l’inverse, la quatrième méthode n’a pas permis de trouver des différences dans la disponibilité du Zn d’une source inorganique ou organique au saumon de l’Atlantique. Pour conclure, bien qu’ils ne correspondent pas aux résultats in vivo, les protocoles in vitro ont fourni des informations intéressantes pour comprendre les différentes composantes de la disponibilité du Zn.
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ces travaux ont été réalisés dans le cadre du projet APREMIA (Apparent availability and requirement of minerals in Atlantic salmon, grant no. 244490) financé par le Conseil norvégien de la recherche.
matériels
| Name | Company | Catalog Number | Comments |
| 0.45 µm syringe filter | Sartorius | ||
| 0.45 μm membrane filter | Pall | ||
| 10 % fetal bovine serum | Eurobio | ||
| 1282 Compugamma Laboratory Gamma Counter | LKB Wallac | ||
| 24 well plates (Falcon, TPP microplates) | Thermo Fisher Scientific | 10048760 | |
| 2-aminobicyclo(2.2.1)heptane-2-carboxylic acid | Sigma Aldrich | A7902 | |
| 75 cm2 cell culture flasks (Falcon, TPP tissue culture flasks) | TPP Techno Plastic Products AG | 90075 | |
| L-Arginine | Sigma Aldrich | A5006 | |
| Bradford assay kit | Bio-Rad | 5000001 | |
| Centrifuge | Eppendorf Centrifuge 5702 | ||
| L-Cysteine | Sigma Aldrich | 30089 | |
| DL-methionine | Alfa Aesar | 59-51-8 | |
| D-methionine | Sigma Aldrich | M9375 | |
| Experimental fish feeds | Skretting | ||
| Glycine | Sigma Aldrich | 410225 | |
| Guard column, TSKgel SWxl Type (7 μm particle size) | Tosoh | ||
| L-Histidine | Sigma Aldrich | 53319 | |
| HPLC coupled with a 7500ce ICP-MS | Agilent Technologies | ||
| Hydrochloric acid | Emsure ACS, ISO, 37% w/w, Merck | 1.00317 | |
| Knife mill | GM 300, Retsch Gmbh | ||
| L-15 medium | Invitrogen/Gibco | 21083027 | |
| L-methionine | Sigma Aldrich | M9625 | |
| L-Lysine | Sigma Aldrich | 23128 | |
| Methanol | LiChrosolv, HPLC grade, Merck | 1.06035 | |
| Milli-Q water (18.2 MΩ cm) | EMD Millipore Corporation | ||
| Myoglobin | Sigma Aldrich | M1882 | |
| NexION 350D ICP-MS | Perkin Elmer | ||
| Pasteur pipette | VWR | ||
| pH meter | inoLab | ||
| Phosphate-buffered saline (PBS) | Sigma Aldrich | 806552 | |
| RTgutGC cells | Obtained in kind from Professor Dr. Kristin Schirmer, Dept. of Environmental Toxicology, Eawag, Swiss Federal Institute of Aquatic Science and Technology, Switzerland | ||
| SEC column, TSKgel G3000SWxl | Tosoh | ||
| Sieve stainless steel (850?μm - 1.12?mm) | Retsch | ||
| Sodium dodecyl sulphate (SDS) | Sigma Aldrich | 436143 | |
| Superoxide dismutase | Sigma Aldrich | S7571 | |
| Thyroglobulin | Sigma Aldrich | T1001 | |
| Tricaine methanesulphonate | PharmaQ | ||
| Tris(hydroxymethyl)aminomethane | Sigma Aldrich | 252859 | |
| Trypsin in 0.25% in phosphate-buffer saline | Biowest | L0910 | |
| Versene EDTA solution | Invitrogen/Gibco | 15040-033 | |
| Vitamin B12 | Sigma Aldrich | V2876 | |
| Zinc chelate of glycine | Phytobiotics | ||
| Zinc sulphate | Vilomix |
Références
- Ytrestoyl, T., Aas, T. S., Asgard, T. Utilisation of feed resources in production of Atlantic salmon (Salmo salar) in Norway. Aquaculture. 448, 365-374 (2015).
- Prabhu, P. A. J., et al. Evaluating dietary supply of microminerals as a premix in a complete plant ingredient-based diet to juvenile rainbow trout (Oncorhynchus mykiss). Aquaculture Nutrition. 24 (1), 539-547 (2018).
- Maret, W. Zinc biochemistry: from a single zinc enzyme to a key element of life. Advances in nutrition. 4 (1), 82-91 (2013).
- Hogstrand, C., Wood, C. M., Farrell, A. P., Brauner, C. J. . Fish Physiology. 31, 135-200 (2011).
- Baeverfjord, G., et al. Mineral nutrition and bone health in salmonids. Reviews in Aquaculture. , (2018).
- Maage, A., Julshamn, K. Assessment of zinc status in juvenile Atlantic salmon (Salmo salar) by measurement of whole body and tissue levels of zinc. Aquaculture. 117 (1), 179-191 (1993).
- Silva, M. S., Sele, V., Sloth, J. J., Araujo, P., Amlund, H. Speciation of zinc in fish feed by size exclusion chromatography coupled to inductively coupled plasma mass spectrometry – Using fractional factorial design for method optimization and mild extraction conditions. Journal of Chromatography B. , (2018).
- Prabhu, A. J., et al. Zinc uptake in fish intestinal epithelial model RTgutGC: Impact of media ion composition and methionine chelation. Journal of Trace Elements in Medicine and Biology. 50, 377-383 (2018).
- Silva, M. S., et al. Apparent availability of zinc, selenium and manganese as inorganic metal salts or organic forms in plant-based diets for Atlantic salmon (Salmo salar). Aquaculture. 503, 562-570 (2019).
- Persson, D. P., Hansen, T. H., Laursen, K. H., Schjoerring, J. K., Husted, S. Simultaneous iron, zinc, sulfur and phosphorus speciation analysis of barley grain tissues using SEC-ICP-MS and IP-ICP-MS. Metallomics. 1 (5), 418-426 (2009).
- Lothian, A., Roberts, B. R. Standards for Quantitative Metalloproteomic Analysis Using Size Exclusion ICP-MS. Journal of Visualized Experiments. (110), (2016).
- Minghetti, M., Schirmer, K. Effect of media composition on bioavailability and toxicity of silver and silver nanoparticles in fish intestinal cells (RTgutGC). Nanotoxicology. 10 (10), 1526-1534 (2016).
- Glover, C. N., Hogstrand, C. Amino acid modulation of in vivo intestinal zinc absorption in freshwater rainbow trout. Journal of Experimental Biology. 205 (1), 151-158 (2002).
- Ekman, R., Ekman, R. . Mass spectrometry: Instrumentation, interpretation, and applications. Wiley Series on Mass Spectrometry. , 105-115 (2009).
- Hong, P., Koza, S., Bouvier, E. S. P. A Review Size-Exclusion Chromatography for the Analysis of Protein Biotherapeutics and Their Aggregates. Journal of Liquid Chromatography & Related Technologies. 35 (20), 2923-2950 (2012).
- Krezel, A., Maret, W. The biological inorganic chemistry of zinc ions. Archives of Biochemistry and Biophysics. 611, 3-19 (2016).
- National Research Council. . Nutrient Requirements of Fish and Shrimp. , (2011).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon