Method Article
عزل الخلايا العصبية تحت المهاد المستهدفة لدراسات التنظيم الهرموني والأيضي والكهربائي
In This Article
Summary
نقدم هنا بروتوكولا لزراعة أنواع فرعية محددة من الخلايا تحت المهاد في الثقافة. يمكن اختيار الخلايا بناء على علامات الغشاء المناسبة / الفريدة واستخدامها في العديد من التطبيقات ، بما في ذلك المقايسات المناعية والفيزيولوجية الكهربية والكيميائية الحيوية.
Abstract
ينظم ما تحت المهاد عمليات التمثيل الغذائي الأساسية من خلال التحكم في وظائف متنوعة مثل تناول الطعام ودرجة حرارة الجسم وإطلاق الهرمونات. نظرا لأن وظائف منطقة ما تحت المهاد يتم التحكم فيها بواسطة مجموعات فرعية محددة من المجموعات العصبية ، فإن القدرة على عزلها توفر أداة رئيسية لدراسة آليات التمثيل الغذائي. في هذا الصدد ، يشكل التعقيد العصبي لما تحت المهاد تحديات استثنائية.
لهذه الأسباب ، تم استكشاف تقنيات جديدة ، مثل فرز الخلايا المنشطة مغناطيسيا (MACS). تصف هذه الورقة تطبيقا جديدا لفرز الخلايا المنشطة مغناطيسيا (MACS) باستخدام تقنية الميكروبيدات لعزل مجموعة الخلايا العصبية المستهدفة عن أدمغة الفئران قبل الولادة. هذه التقنية بسيطة وتضمن ثقافة الخلايا العصبية تحت المهاد الأولية النقية للغاية والقابلة للحياة مع قابلية عالية للاستنساخ. يتم فصل منطقة ما تحت المهاد بلطف ، ويتم عزل الخلايا العصبية بشكل انتقائي وفصلها عن الخلايا الدبقية ، وأخيرا ، باستخدام جسم مضاد محدد لعلامة سطح الخلية ، يتم اختيار السكان المعنيين.
بمجرد عزلها ، يمكن استخدام الخلايا العصبية المستهدفة للتحقق من خصائصها المورفولوجية والكهربائية والغدد الصماء واستجاباتها في الظروف الطبيعية أو المرضية. علاوة على ذلك ، نظرا للأدوار المتنوعة لما تحت المهاد في تنظيم التغذية والتمثيل الغذائي والإجهاد والنوم والتحفيز ، فإن إلقاء نظرة فاحصة على الخلايا العصبية المستهدفة والخاصة بالمنطقة قد يوفر نظرة ثاقبة لمهامها في هذه البيئة المعقدة.
Introduction
منطقة ما تحت المهاد هي منطقة متعددة الجوانب في الدماغ تتوسط وظائف الغدد الصماء واللاإرادية والحشوية والسلوكية ، بما في ذلك التغذية والتمثيل الغذائي والنوم ودرجة حرارة الجسم والسلوك الاجتماعي والدافع الجنسي 1،2،3،4،5. يتم تحقيق عدم التجانس الوظيفي من خلال مزيج تآزري من الآليات الكيميائية الحيوية والكهربائية: تطلق الخلايا العصبية تحت المهاد إمكانات العمل وتفرز وتطلق الهرمونات والببتيدات العصبية لتعديل مناطق الدماغ وأعضاء الجسم. أخيرا ، تترجم الخلايا العصبية تحت المهاد رسائل الاستتباب من الجسم ، وتستجيب بردود فعل طويلة الأجل وقصيرة الأجل ولوائح التغذيةالأمامية 6.
تشمل البيئة العصبية المعقدة لما تحت المهاد الخلايا العصبية الغدد الصماء المغنطيسية ، وإطلاق الأوكسيتوسين والفاسوبريسين. الخلايا العصبية ذات الخلايا الصغيرة ، التي تشارك في المقام الأول في التنظيم الهرموني الجهازي ، والإفراج على سبيل المثال ، هرمون إطلاق هرمون الثيروتروبين (TRH) ، وهرمون إفراز الكورتيكوتروبين (CRH) إلى الغدة النخامية ؛ الخلايا العصبية الإسقاط الببتيدرجي الكبيرة ، والإفراج عن orexin وهرمون تركيز الميلانين (MCH) ؛ والخلايا العصبية الببتيدرجية الصغيرة من النواة المقوسة (ARC) التي تطلق POMC (proopiomelanocortin) و AgRP (بروتين مرتبط ب agouti) ، المسمى ARCPOMC و ARCAgRP ، على التوالي. جنبا إلى جنب مع الخلايا الإفرازية ، تشارك الخلايا العصبية المثيرة والمثبطة الأخرى ، بما في ذلك الخلايا العصبية الدوبامينية ، والجلوتامينرجيك ، و GABAergic 7 ، في تشكيل دوائر داخل المهاد وخارج المهاد ، وبالتالي إنشاء شبكات منسقة واسعة النطاق من عدم التجانس الخلوي الكبير8.
كان التنوع تحت المهاد تحديا يحاول الباحثون التغلب عليه على مدار ال 50 عاما الماضية. لدراسة هذا عدم التجانس في مرحلة ما تحت المهاد النامية والناضجة والشيخوخة ، استخدم الباحثون ، من ناحية ، تسلسل الحمض النووي الريبي أحادي الخلية لاستكشاف تنظيم الخلايا العصبية ، بالإضافة إلى التوقيعات الجزيئية والنسخية. قدم هذا الجهد نظرة ثاقبة على الأدوار المتنوعة للخلايا العصبية تحت المهاد وتناول الروابط بين الهوية الخلوية ودورها المحتمل في النظام الفسيولوجي8،9،10. من ناحية أخرى ، تم التحقيق في الوظائف العصبية من خلال التلاعب البصري الوراثي والنهج السلوكية للقياس الضوئي للألياف ، مما يوفر نظرة فاحصة على بنية الدوائر. في العقدين الماضيين ، سمحت تقنية Cre-recombinase للباحثين بتحفيز أو تثبيط مجموعة مستهدفة من الخلايا العصبية وراثيا مع ملاحظة التغيرات في السلوكيات واستجابات الجسم6،11،12.
ومع ذلك ، فإن هذه الأساليب تدرس وظائف ما تحت المهاد من منظور عام دون الغوص بشكل أعمق في الآليات الخلوية المحددة أو الأساس البيولوجي لدورها في بيئة ما تحت المهاد المعقدة. لمعالجة هذا الأمر ، ركز عدد قليل جدا من الدراسات على التحقيق في الخصائص الجزيئية والكيميائية الحيوية والكهربائية باستخدام الثقافات الأولية غير المتجانسة. سعت هذه الدراسات إلى تشريح عمليات عصبية محددة في بيئة معقدة وولدت نماذج تكاملية للآليات الفسيولوجية13،14،15. ومع ذلك، فإن الثقافات غير المحددة تشكل تحديات كبيرة. على سبيل المثال ، يتم تعطيل الاتصال الفسيولوجي للخلايا العصبية والتوزيع التشريحي عن طريق طلاء الخلايا العصبية من مناطق ما تحت المهاد المختلفة التي لا تتفاعل عادة ، مما يخلق تأثيرات مربكة. بالإضافة إلى ذلك ، لكل منطقة أدوار مختلفة ومجموعات عصبية متنوعة ، مما يجعل من الصعب دراسة العمليات البيولوجية البسيطة.
لمواجهة هذه التحديات ، في العقد الماضي ، تم تنفيذ مناهج جديدة لعزل الخلايا العصبية ذات الأهمية ، مثل الفرز المناعي ، وفرز الخلايا المنشطة بالفلورسنت (FACS) ، وفرز الخلايا المنشطة مغناطيسيا (MACS). Immunopanning هي استراتيجية تستخدم لتنقية الخلايا المستهدفة باستخدام أطباق مغلفة بالأجسام المضادة لسلسلة من التحديدات غير العصبية (السلبية) والعصبية (الإيجابية). في حين أن هذه التقنية يمكن ، من حيث المبدأ ، أن تولد ثقافات خلايا نقية عالية الغلة ، إلا أنها تستخدم في الغالب في الغالب للخلايا النجمية والخلايا قليلة التغصن لأن هذه الخلايا يمكنها مقاومة ساعات من التلاعب16,17. تعد تقنية FACS أداة قوية لفرز الخلايا بناء على علامات الفلورسنت والخصائص الخلوية باستخدام قياس التدفق الخلوي18،19،20. ومع ذلك ، استخدم عدد قليل جدا من الدراسات هذه الطريقة لعزل الخلايا لزراعة الخلايا. هذه التقنية مكلفة وتتطلب موظفين ذوي مهارات عالية لاستخدامها وصيانتها ؛ بالإضافة إلى ذلك ، من الصعب الحفاظ على خلايا قابلة للحياة ومعقمة في نهاية إجراء الفرز21. بشكل عام ، يبدو أن MACS تقنية بسيطة وغير مكلفة للحصول على ثقافات نقية للغاية وقابلة للحياة من الخلايا العصبية الأولية تحت المهاد. تستخدم الطريقة حبات مغناطيسية مرتبطة بالخلايا عبر جسم مضاد. هذا يسمح بعزل الخلايا باستخدام المجال المغناطيسي للعمود.
نصف هنا طريقة تعتمد على تقنية MACS ، والتي تستخدم عادة مع الخلايا العصبية القشرية. يسمح هذا البروتوكول بعزل الخلايا العصبية تحت المهاد القابلة للحياة والنقاء للغاية من حيث المبدأ. في هذه الدراسة ، نقوم بإعداد الثقافات الأولية للخلايا العصبية التي تعبر عن مستقبلات اللبتين (LepR) ، مثل الخلايا العصبية ARCPOMC و ARCAgRP ، الموجودة فقط في نواة المقوس. تستجيب هذه الخلايا العصبية لليبتين ، وهو هرمون فقدان الشهية الذي تفرزه الأنسجة الدهنية ، بطرق كيميائية حيوية وكهربائية. لذلك ، فإن عزل هذه المجموعة من الخلايا العصبية في الثقافة يسمح بدراسة خصائصها الهرمونية والأيضية والكهربائية في المختبر.
Protocol
ملاحظة: يتم توضيح منظر عام للإجراء التجريبي بيانيا في الشكل 1 أ. تمت الموافقة على جميع التجارب التي أجريت على الفئران في هذه الدراسة من قبل لجنة رعاية واستخدام الحيوان في مؤسستنا (IACUC). استخدمنا فئران C57BL6 / J البالغة من العمر 3 أشهر ، والتي تم إيواؤها في حظيرة معتمدة من جمعية تقييم واعتماد رعاية المختبر الدولية (AAALAC) ، تحت رعاية طبيب بيطري. عاشت الفئران في أقفاص كبيرة ، مع دورة 12 ساعة من الضوء والظلام ، وتم إطعامها حسب الحاجة.
1. التحقق من الحمل والحمل
- ضع الفئران من أي خلفية ونمط وراثي مهم للتكاثر. سجل تاريخ ووزن الأنثى قبل الحمل.
- بعد 6 ساعات ، افحص الأنثى بحثا عن لوحة مع مسبار. إذا كانت اللوحة موجودة ، افصل الأنثى عن الذكر. إذا لم تكن اللوحة موجودة ، احتفظ بالأنثى في القفص حتى اليوم التالي ، ثم افصل الفئران.
- في الأيام 7 و 10 و 14 بعد الحمل ، قم بوزن الأنثى لتأكيد الحمل.
2. الوسائط ، لوحة 24 بئر ، وإعداد المواد
- في يوم عزل الخلية ، ضع أغطية زجاجية جاهزة للاستخدام ومطلية بالبولي دي ليسين (انظر جدول المواد) في لوحة مكونة من 24 بئرا على النحو التالي:
- تحت غطاء بيولوجي ، قم بتعقيم عبوة واحدة تحتوي على 15 غطاء مع 70٪ إيثانول واتركها تجف. افتح العبوة وضع أغطية الغطاء في لوحة 60 مم. هز اللوحة أفقيا لفصل أغطية الغطاء. بعد ذلك ، اقلب اللوحة لالتقاط أغطية مفردة لوضعها في آبار لوحة 24 بئرا.
- اغسل أغطية الغطاء مرة واحدة ب 1.0 مل من محلول الملح المتوازن المعقم من هانك (HBSS) لمدة 5 دقائق.
- في غضون ذلك ، قم بإعداد 20.0 مل من وسائط الطلاء على النحو التالي: إلى 18.31 مل من BME (النسر القاعدي المتوسط ، + أملاح إيرل) ، مع استكمال 1.0 مل من مصل بقري الجنين المعطل بالحرارة (FBS) ، أضف 200 ميكرولتر من بيروفات الصوديوم (من مخزون 100x) ، 200 ميكرولتر من الجلوتامين (من مخزون 200 نانومتر) ، و 100 ميكرولتر من البنسلين / الستربتومايسين (من مخزون 200x).
- استبدل HBSS في الآبار ب 1.0 مل من وسائط الطلاء وضع اللوحة في الحاضنة عند 37 درجة مئوية.
- باستخدام موقد بنسن ، قم بتلميع النار ثلاث ماصات باستور بأقطار متناقصة. أمسك الماصة بيد واحدة ، أدخل الطرف في اللهب وقم بإزالته بسرعة. كرر العملية حتى ينعم الطرف ويتم تقليل القطر إلى القطر المطلوب (يتم تقييمه بالعين).
3. إعداد الكاشف لتفكك الأنسجة العصبية ، باتباع توجيهات مجموعة التفكك العصبي
- بعد تسخين محلول الهضم 1 في درجة حرارة الغرفة ، قم بإعداد Enzyme Mix 1 عن طريق خلط 50 ميكرولتر من الإنزيم 1 مع 1.91 مل من Buffer 1 و Enzyme Mix 2 عن طريق خلط 15 ميكرولتر من الإنزيم 2 مع 30 ميكرولتر من Digestion Buffer 2. الخلطات كافية لاستخدامها في أنسجة دماغ جميع الأجنة.
- تحضير 0.5 ٪ ألبومين مصل البقر (BSA) في HBSS ، على سبيل المثال ، 0.25 غرام في 50.0 مل من HBSS.
4. استخراج الأجنة
- الأوتوكلاف ملقط دقيق مستقيم ، ملقط نقطة منحنية ، وزوج واحد من المقصات الجراحية الدقيقة وتعقيمها بالإيثانول بنسبة 70٪ قبل الاستخدام. ثم املأ أطباق بتري ب HBSS.
- القتل الرحيم سد حامل E14-E16 في غرفة CO2 وإجراء خلع عنق الرحم.
ملاحظة: يجب تنفيذ الخطوات التالية تحت غطاء المحرك في ظل ظروف معقمة: - تعقيم البطن مع 70 ٪ من الإيثانول. قطع فتح تجويف البطن من الارتفاق العاني إلى عملية الخنجري من القفص الصدري مع مقص الجراحية والملقط.
- استخراج قرن الرحم ووضعه في لوحة 100 ملم مليئة HBSS الجليد الباردة واغسلها جيدا.
- استخراج وفصل جميع الأجنة من الرحم مع ملقط غرامة. قطع رأس الأجنة بسرعة بمقص جراحي دقيق و / أو ملقط. ضع الرؤوس في طبق بتري 60 مم مملوء ب HBSS.
5. استخراج ما تحت المهاد وجمعها وتفكك الأنسجة
- ضع ملقطا رفيعا واحدا في تجويف العين لتثبيت الدماغ. باستخدام الملقط الرفيع الآخر ، قم بإزالة الجلد والجمجمة عن طريق التقشير حتى يصبح الدماغ مرئيا. يميز الدماغ عن الأنسجة الأخرى بناء على مظهره الأبيض. الجلد والجمجمة وردية وغنية بالأوعية الدموية.
- قم بإزالة الدماغ من الجمجمة باستخدام ملقط النقطة المنحنية وأخرج الدماغ من المصابيح الشمية ، وقلبه رأسا على عقب.
- الآن القشرة بطنية ، وما تحت المهاد مرئي ظهريا على السطح العلوي (الشكل 1 ب). باستخدام الملقط المنحني ، قم بإزالة طبقة السحايا والأوعية الدموية حتى يظهر الدماغ أبيض وواضح.
- باستخدام الملقط المنحني ، افصل منطقة المهاد عن بقية الدماغ.
- قطع ما تحت المهاد إلى 3-4 قطع صغيرة ومع ماصة ، ونقل القطع إلى أنبوب 15 مل.
- كرر الخطوات للأجنة الأخرى أثناء وجود الأنبوب على الجليد.
- املأ الأنبوب ب 6.0 مل من HBSS واترك الأنسجة تستقر ، وأزل المادة الطافية ، وأضف Enzyme Mix 1. امزج الأنبوب برفق وحركه لمنع الأنسجة.
- احتضان الأنبوب في حمام مائي 37 درجة مئوية لمدة 15 دقيقة وحرك الأنسجة كل 5 دقائق لإعادة تعليق المنديل.
- بعد 15 دقيقة ، أضف 30 ميكرولتر من مزيج الإنزيم 2. فصل أنسجة المخ باستخدام ماصة باستور ذات القطر الأكبر (<1 مم). ماصة صعودا وهبوطا 10x دون تشكيل فقاعات.
- احتضان لمدة 10 دقائق على 37 درجة مئوية في حمام مائي. حرك الأنبوب برفق لإعادة تعليق المنديل كل 5 دقائق.
- بعد 10 دقائق ، أضف 15 ميكرولتر المتبقية من مزيج الإنزيم 2. افصل الأنسجة 10x مع الماصتين الأخريين المصقولتين بالنار ذات القطر المتناقص ، لأعلى ولأسفل دون تشكيل فقاعات.
- إلى الأنبوب مع الأنسجة المنفصلة ، أضف على الفور 10.0 مل من HBSS-0.5٪ BSA وأجهزة الطرد المركزي عند 300 × جم لمدة 10 دقائق في درجة حرارة الغرفة.
- نضح المادة الطافية وإعادة تعليق حبيبات الخلية في 1.0 مل من HBS-0.5٪ BSA.
6. عد الخلايا
- تمييع تعليق الخلية 1: 5 باستخدام HBSS-0.5٪ BSA.
- ضع 10 ميكرولتر من معلق الخلية المخففة في غرفة عد نيوباور.
- تحت مجهر برايت فيلد ، عد فقط الخلايا الموجودة في مربعات زاوية الغرفة الأربعة. احسب المتوسط واضربه في 5 × 104.
ملاحظة: تأكد من وجود >106 خلايا للمضي قدما في عزل الخلية; رقم الخلية الأمثل هو 107.
7. الاختيار السلبي
ملاحظة: يتيح الانتقاء السلبي للمستخدمين الحصول على مزرعة عصبية أولية نقية عن طريق فصل الخلايا العصبية وغير العصبية. استخدم المحاليل المبردة مسبقا.
- أجهزة الطرد المركزي تعليق الخلية في 300 × غرام لمدة 3 دقائق (يمكن تمديد الطرد المركزي حتى 10 دقائق). قم بشفط المادة الطافية برفق وأعد تعليق الحبيبات إلى تركيز 107 خلايا في 80 ميكرولتر من HBSS-0.5٪ BSA.
- أضف 20 ميكرولتر من كوكتيل الأجسام المضادة للبيوتين للخلايا غير العصبية واحتضانها لمدة 5 دقائق عند 4 درجات مئوية.
- اغسل الخلايا لإزالة الأجسام المضادة الحرة باستخدام 2.0 مل من HBSS-0.5٪ BSA وأجهزة الطرد المركزي عند 300 × جم لمدة 3 دقائق.
- قم بشفط المادة الطافية برفق وأعد تعليق الحبيبات في 80 ميكرولتر من HBSS-0.5٪ BSA. أضف 20 ميكروبيدات مضادة للبيوتين ، واخلطها جيدا ، واحتضنها لمدة 10 دقائق عند 4 درجات مئوية.
- أضف 0.5 مل من HBSS-0.5٪ BSA لما يصل إلى 107 خلايا وانتظر حتى يصبح العمود المغناطيسي جاهزا.
8. الفصل المغناطيسي ، الاختيار السلبي
ملاحظة: الفصل المغناطيسي هو خطوة حاسمة تسمح بفصل الخلايا غير العصبية عن الخلايا العصبية. يتم تمرير العينة التي تحتوي على خلايا عصبية وغير عصبية عبر المجال المغناطيسي والخلايا غير العصبية ، المرتبطة بمركب حبة مغناطيسية من البيوتين والأجسام المضادة ، محاصرة في العمود (الشكل 1C). يتم استخلاص الخلايا العصبية الحرة من خلال العمود ويتم جمعها في أنبوب 15 mL.
- قم بإعداد الحامل (المضمن في المجموعة) باستخدام الفاصل وعمود MS كما هو موضح في الشكل 1C.
- افتح العمود وقم بإعداد الحامل فقط عندما تكون الخلايا جاهزة للفصل.
- شطف العمود مع 0.5 مل من HBSS-0.5 ٪ BSA. انتظر حتى يتوقف المحلول عن التنقيط.
- لجمع الخلايا العصبية ، ضع أنبوبا سعة 15 mL أسفل العمود ومرر 0.5 mL من معلق الخلية عبر العمود. اجمع الشطف في الأنبوب حتى يتوقف عن التنقيط. لالتقاط الخلايا العصبية المتبقية ، اغسل العمود 3 × 0.5 مل من HBSS-0.5٪ BSA.
- لجمع الخلايا غير العصبية ، قم بإزالة العمود من المغناطيس ووضعه داخل أنبوب جديد سعة 15 مل. أضف 1.0 مل من HBSS - 0.5٪ BSA إلى العمود واستخدم المكبس لجمع الخلايا غير العصبية ذات العلامات المغناطيسية.
- أجهزة الطرد المركزي الخلايا العصبية وغير العصبية في 300 × غرام لمدة 3 دقائق. قم بشفط المادة الطافية برفق وأعد تعليق الخلايا في 1.0 مل من HBSS-0.5٪ BSA. عد الخلايا كما هو موضح سابقا في القسم 6.
- إذا لزم الأمر ، قم بلوحة الخلايا غير العصبية في لوحة 24 بئرا ؛ وإلا تخلص منها.
9. الاختيار الإيجابي
ملاحظة: بمجرد الحصول على تعليق الخلايا العصبية النقية ، يتم إجراء اختيار إيجابي لعزل الخلايا المستهدفة. يمكن عزل الخلايا باستخدام جسم مضاد مقترن بالبيوتين لمولد ضد سطحي. يتم التعرف على الجسم المضاد بواسطة حبات مغناطيسية مضادة للبيوتين. من خلال تدفق تعليق الخلية عبر العمود ، يتم احتجاز الخلايا ذات الأهمية فقط في المجال المغناطيسي.
- الطرد المركزي تعليق الخلايا العصبية النقية في 300 × غرام لمدة 3 دقائق. قم بشفط المادة الطافية برفق وأعد تعليق الحبيبات في 80 ميكرولتر من HBSS-0.5٪ BSA. أضف الجسم المضاد المحدد باتباع تعليمات الشركة المصنعة واحتضانه عند 4 درجات مئوية لمدة 10 دقائق.
ملاحظة: إذا تم البحث عن الخلايا التي تعبر عن LepR ، فإننا نقترح وجود جسم مضاد حيوي من Mouse Leptin R (انظر جدول المواد) بتركيز 0.50 ميكروغرام / 106 خلايا. - اغسل الجسم المضاد الزائد ب 2.0 مل من HBSS-0.5٪ BSA وأجهزة الطرد المركزي عند 300 × جم لمدة 3 دقائق.
- قم بإزالة المادة الطافية ، وأعد تعليق الحبيبات في 80 ميكرولتر من HBSS-0.5٪ BSA ، وأضف 20 ميكرولتر من الميكروبيدات المضادة للبيوتين. احتضان على حرارة 4 درجة مئوية لمدة 10 دقائق.
- لكل 107 خلايا ، أضف 0.5 مل من HBSS-0.5٪ BSA وانتظر حتى يصبح العمود المغناطيسي جاهزا.
10. الفصل المغناطيسي ، الاختيار الإيجابي
- قم بإعداد الحامل باستخدام الفاصل وعمود MS. شطف العمود MS مع 0.5 مل من HBSS-0.5٪ BSA. انتظر حتى يتوقف التنقيط.
- ضع أنبوبا حجمه 15 مل أسفل العمود ، ومرر 0.5 mL من معلق الخلية عبر العمود ، واجمع الشطف الذي يتكون من الخلايا العصبية غير المتخصصة. لتنظيف عمود الخلايا العصبية غير المحددة المتبقية ، اغسل ب 3 × 0.5 مل من HBSS-0.5٪ BSA.
- قم بإزالة العمود من المغناطيس ، وضعه في أنبوب جديد سعة 15 مل ، وأضف 1.0 مل من HBSS-0.5٪ BSA. استخدم المكبس لطرد الخلايا المستهدفة.
- جهاز طرد مركزي كلا الأنبوبين عند 300 × جم لمدة 3 دقائق. قم بإزالة المادة الطافية برفق وأعد تعليقها في 0.5 مل من وسط الطلاء.
- عد الخلايا كما هو موضح سابقا في القسم 6.
- صفيحة كل من الخلايا المستهدفة كعنصر تحكم موجب وخلايا غير محددة كعنصر تحكم سلبي عند كثافة 120,000-200,000 خلية / مم3 في صفيحة 24 بئر المعدة مسبقا كما هو موضح في القسم 2 وتحضن عند 37 درجة مئوية في 5٪ CO 2 و 9٪ O2 و 95٪ رطوبة لمدة 12 ساعة.
11. صيانة زراعة الخلايا
- تحضير 20 مل من وسط المزرعة مع 19.2 مل من وسط الثقافة العصبية ، و 400 ميكرولتر من مكمل B27 (من مخزون 50x) ، و 200 ميكرولتر من الجلوتامين (من مخزون 200 ميكرومتر) ، و 100 ميكرولتر من البنسلين / الستربتومايسين (من مخزون 200x).
- استبدل وسائط الطلاء من 24 لوحة بئر تحتوي على خلايا عصبية أو غير عصبية.
- يغسل مع 2 × 1.0 مل من HBSS.
- أضف 1.0 مل من الوسائط الثقافية.
- قم بتحديث الوسائط كل 2/3 أيام عن طريق استبدال 0.5 مل من الوسائط القديمة ب 0.5 مل من الوسائط الجديدة.
ملاحظة: يمكن الاحتفاظ بالخلايا في المزرعة واستخدامها لمدة تصل إلى 21 يوما في المختبر (DIV21).
12. تلطيخ الخلايا العصبية المناعية
- قبل اثنتي عشرة ساعة من التلوين ، قم بإعداد محلول يتكون من 50/50 ميثانول وأسيتون وقم بتبريده عند -20 درجة مئوية طوال الليل.
- اغسل الخلايا العصبية في لوحة 24 بئرا مع 2 × 1.0 مل من 1x محلول ملحي مخزن بالفوسفات (PBS) لمدة 5 دقائق.
- استبدل محلول PBS ب 1.0 مل من محلول 50/50 واحتضانه في الثلج لمدة 20 دقيقة.
- يغسل مع 1x PBS لمدة 3 × 5 دقائق.
- منع الخلايا العصبية مع 3٪ BSA في 1x PBS لمدة 1 ساعة في درجة حرارة الغرفة.
- قم بإعداد محلول الأجسام المضادة الأساسي في 3٪ BSA في 1x PBS ، باستخدام تركيز الأجسام المضادة المذكور في توجيهات الشركة المصنعة. يتم سرد الأجسام المضادة والتركيزات المستخدمة في جدول المواد.
- استبدل محلول الحجب بمحلول الأجسام المضادة الأساسي واحتضانه عند 4 درجات مئوية طوال الليل.
- اغسل الخلايا لمدة 3 × 10 دقائق باستخدام 1x PBS.
- قم بإعداد محلول الأجسام المضادة الثانوي مع 3٪ BSA في 1x PBS ، باستخدام تركيزات الأجسام المضادة باتباع تعليمات الشركة المصنعة. يتم سرد الأجسام المضادة الثانوية المستخدمة في جدول المواد.
- احتضان الخلايا بمحلول الأجسام المضادة الثانوي في درجة حرارة الغرفة لمدة 1 ساعة.
- اغسل الخلايا لمدة 3 × 10 دقائق باستخدام 1x PBS.
- اترك الخلايا العصبية في 1x PBS أثناء إجراء التركيب. ضع قطرة صغيرة من وسط التركيب (مع أو بدون 4 '، 6-diamidino-2-phenylindole لتحديد الهوية النووية) على شريحة المجهر. استخرج غطاء زجاجي واحد يحتوي على خلايا عصبية بالملقط واضغط على جانب الغطاء على منديل ورقي لتجفيف PBS الزائد. اقلب الغطاء على وسط التثبيت ، وتأكد من أن الخلايا العصبية تواجه شرائح المجهر ؛ اضغط برفق على وسائط التركيب الزائدة وقم بإزالتها باستخدام المناديل الورقية.
- شرائح المجهر جاهزة للتحليل باستخدام حقل ساطع أو مجهر متحد البؤر.
النتائج
تصف هذه الورقة بروتوكولا لعزل الخلايا العصبية المستهدفة في منطقة ما تحت المهاد (الشكل 1). نطاق الطريقة هو دراسة خصائص عصبية محددة في سياق خاضع للرقابة ومعزول. وهكذا ، تم استخراج أجنة الفئران من السدود الحامل في E14-E16. تمت إزالة السحايا ، وتم عزل منطقة ما تحت المهاد عن بقية الدماغ. تم فصل الأنسجة بلطف مع خليطين من الإنزيمات المحضرة حديثا باستخدام مجموعة التفكك المشار إليها. أولا ، تم فصل الخلايا غير العصبية عن الخلايا العصبية الدبقية ، الخلايا الدبقية الصغيرة ، وتم جمع الخلايا العصبية في نفس تعليق الخلية الواحدة. تحقيقا لهذه الغاية ، تم تصنيف الخلايا غير العصبية باستخدام مزيج من الأجسام المضادة التي تتعرف على حواجز السطح غير العصبية. بعد الحضانة ، تم اقتران مجمع خلايا الأجسام المضادة مع الميكروبيدات المغناطيسية ثم مر لاحقا عبر عمود مغناطيسي لاحتجاز الخلايا غير العصبية.
أسفرت هذه الخطوة عن تعليقين للخلايا ، أحدهما يحتوي على خلايا غير عصبية والآخر يحتوي على خلايا عصبية. يمكن طلاء كلا التعليقين على الفور. بدلا من ذلك ، يمكن التلاعب بتعليق الخلايا العصبية لفصل مجموعة فرعية عصبية (تعليق مستهدف) عن الباقي باستخدام نفس الإستراتيجية. بناء على تجربة الاهتمام ، يمكن طلاء الخلايا العصبية من 125000 إلى 200000 خلية / مم3. يمكن استخدام الثقافات الأقل كثافة لتحليل الخلايا العصبية بدقة خلية واحدة: من التطور المحوري ، والتكوين المشبكي ، والانتقال إلى الفيزيولوجيا الكهربية. يمكن استخدام الثقافات الأكثر كثافة للتحليلات الكيميائية الحيوية ، بما في ذلك استخراج الحمض النووي والحمض النووي الريبي ، واللطخة الغربية ، واللطخة الجنوبية ، واللطخة الشمالية ، وتفاعل البوليميراز المتسلسل في الوقت الفعلي ، وتسلسل الحمض النووي الريبي.
في هذه الدراسة ، تم استهداف LepR لعزل الخلايا العصبية المشاركة في نظام الميلانوكورتين ، مثل الخلايا العصبية ARCPOMC و ARCAgRP. تم طلاء الخلايا بكثافات تتراوح من 120000 خلية / مم 3 ، للخلايا العصبية LepR + ، إلى 200000 خلية / مم3 لمجموعات الخلايا العصبية العامة. بعد 48 ساعة ، بدأت الخلايا العصبية LepR + في تكوين الخلايا العصبية (الشكل 2). في DIV4 ، أظهرت الامتدادات المحورية تقدما ، بينما بدأت العمليات التغصنية في الظهور. في DIV6 ، تم تطوير الخلايا العصبية بشكل كاف وبالتالي كانت جاهزة للتحليل. أظهرت تجارب التألق المناعي على الخلايا العصبية LepR + تعبيرا بنسبة 99٪ عن LepR (أخضر ، الشكل 3 أ). لم يلاحظ أي خلايا دبقية أو خلايا غير عصبية أخرى ، مما يؤكد نقاء الثقافة العصبية الأولية. تم تأكيد الطبيعة العصبية للخلايا من خلال تلطيخ البروتين 2 المرتبط بالأنابيب الدقيقة (MAP2) ، مع تحديد المحاور العصبية والنتوءات الشجيرية (الشكل 3B). في DIV10 ، عبرت 30٪ من خلايا LepR + عن POMC (أحمر). هذا متوقع لأن غالبية خلايا LepR + تعبر إما عن POMC أو AgRP. يوضح الشكل 3C ، D التوطين المشترك بين إشارات POMC و LepR. لاحظ أن التوطين المشترك كان بارزا عند النواة وحولها ، كما هو متوقع.
تم استخدام الثقافات العامة التي تحتوي على مجموعات عصبية غير متجانسة تحت المهاد للسيطرة. أظهر التألق المناعي اتصالا ووظائف متشابكة ، كما تم تقييمها بواسطة Synapsin-1 (أخضر) و PSD 95 (أحمر) تلطيخ مشترك (الشكل 4 أ ، ب). كان عدد الخلايا العصبية LepR + الموجودة في الثقافة العامة ~ 5٪ ، وهي نسبة تتوافق مع فكرة أن غالبية الخلايا العصبية المعبرة عن LepR قد تم اختيارها أثناء عملية الفصل المغناطيسي (خلايا LepR + التمثيلية موضحة في الشكل 4C ، D). جميع البيانات التي تم إنشاؤها أو تحليلها خلال هذه الدراسة متاحة على https://doi.org/10.5061/dryad.cnp5hqc9c.
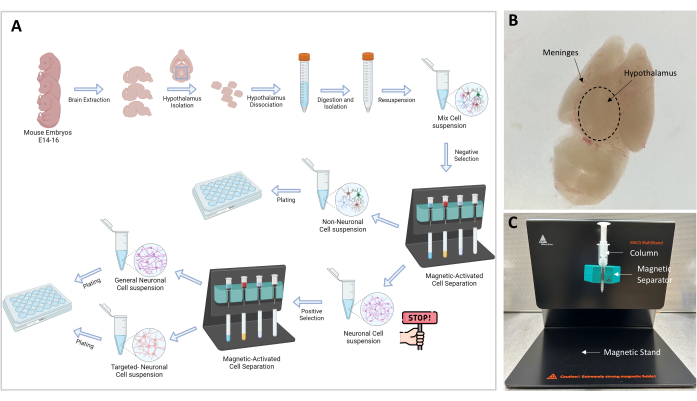
الشكل 1: مخطط التدفق التجريبي والإعداد. أ: تمثيل بياني للإجراء التجريبي. الذهاب لا تذهب: ≥106 خلايا ضرورية للمضي قدما في عزل الخلية. رقم الخلية الأمثل هو 107. ب: صورة تمثيلية لدماغ جنين E16 . يشار إلى ما تحت المهاد والسحايا. (ج) إعداد MACS المستخدم لفصل الخلايا المستهدفة وعزلها. يشار إلى الحامل المغناطيسي والفاصل المغناطيسي والعمود. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
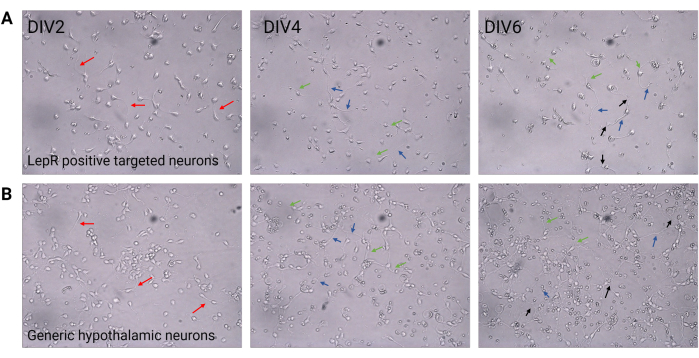
الشكل 2: الثقافة العصبية بين DIV2 و DIV6. (أ) تظهر خلايا LepR + التي تم الحصول عليها من الانتقاء الإيجابي انخفاضا في كثافة الخلايا واتصالها ، ولكن التطور الطبيعي للخلايا العصبية (الأسهم الحمراء) والمحاور العصبية (الأسهم الزرقاء) والزوائد الشجيرية (الأسهم الخضراء). تم طلاء الخلايا بكثافة 120000 خلية / مم3. شريط المقياس = 100 ميكرومتر. (ب) الخلايا العصبية تحت المهاد العامة ، المطلية بكثافة 200000 خلية / مم3 ، تظهر ميزات النمو والنمو الطبيعية والاتصال (الأسهم السوداء). شريط المقياس = 100 ميكرومتر. الاختصارات: DIV = أيام في المختبر. LepR = مستقبلات اللبتين. جميع البيانات التي تم إنشاؤها أو تحليلها لبناء هذا الرقم متاحة في https://doi.org/10.5061/dryad.cnp5hqc9c. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
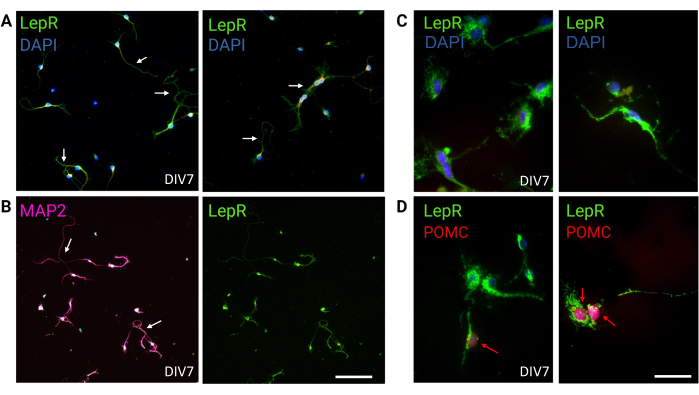
الشكل 3: يتم تلخيص الخلايا العصبية في الجسم الحي بواسطة خلايا LepR + العصبية المستزرعة. (أ) صور تمثيلية لثقافة الخلايا العصبية التي تعبر عن LepR (أخضر ؛ DAPI أزرق). تسعة وتسعون في المئة من الخلايا عبرت عن LepR. تم طلاء الخلايا العصبية بكثافة 120000 خلية / مم3 . في DIV7 ، قدمت الخلايا العصبية محاور عصبية ممدودة ، ونضج تغصني ، واتصال عصبي (أسهم). شريط المقياس = 40 ميكرومتر. (ب) استخدم التألق المناعي مع مضاد MAP2 لتأكيد الطبيعة العصبية للخلايا. يتم عرض الأشكال الخاصة بالخلايا العصبية مثل المحاور العصبية والتشعبات والنتوءات (الأسهم). شريط المقياس = 40 ميكرومتر. ج: تكبير خلايا LepR+ . LepR باللون الأخضر و DAPI باللون الأزرق. شريط المقياس = 10 ميكرومتر. (د) التلوين المشترك مع LepR (أخضر) و POMC (أحمر). ما يقرب من 30 ٪ من الخلايا العصبية LepR + كانت مناعية مشتركة ل POMC ، والتي تم اكتشافها على مستوى النواة (الأسهم الحمراء). شريط المقياس = 10 ميكرومتر. الاختصارات: DAPI = 4',6-دياميدينو-2-فينيليندول; MAP2 = البروتين المرتبط بالأنابيب الدقيقة 2 ؛ POMC = بروبيوميلانوكورتين. LepR = مستقبلات اللبتين. جميع البيانات التي تم إنشاؤها أو تحليلها لبناء هذا الرقم متاحة في https://doi.org/10.5061/dryad.cnp5hqc9c. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
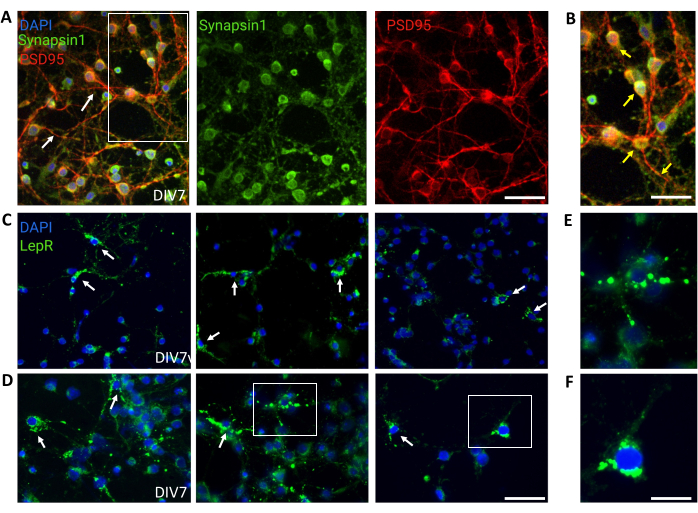
الشكل 4: تلخص الخلايا في الجسم الحي الخلايا العصبية تحت المهاد العامة المستزرعة. (أ) صور تمثيلية لثقافة عصبية عامة تحت المهاد ملطخة ب Synapsin 1 (أخضر) و PSD95 (أحمر) و DAPI (أزرق). أظهرت الخلايا العصبية اتصالا متطورا ووظائف متشابكة (أسهم). شريط المقياس = 40 ميكرومتر. (B) تكبير المربع في (A) ، مع إظهار التوطين المشترك ل Synapsin 1 (أخضر) و PSD95 (أحمر ، أسهم). شريط المقياس = 20 ميكرومتر. (ج، د) صور تمثيلية تظهر خلايا LepR + في ثقافة عامة. شكلت خلايا LepR + (الخضراء) ~ 5٪ من الإجمالي. يشار إلى خلايا LepR + التمثيلية بالأسهم. شريط المقياس = 40 ميكرومتر. (ه، و) تكبير المربعات في (C,D) تظهر مستقبلات اللبتين النقطية الخضراء المترجمة في سوما. شريط المقياس = 20 ميكرومتر. جميع البيانات التي تم إنشاؤها أو تحليلها لبناء هذا الرقم متاحة في https://doi.org/10.5061/dryad.cnp5hqc9c. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
Discussion
يعد التحقيق في الخصائص الكيميائية الحيوية والكهربائية للخلايا العصبية تحت المهاد أمرا أساسيا لفهم الأساس الجزيئي لعملية التمثيل الغذائي ، والتنظيم الحراري ، وإدارة الحالة المزاجية ، وسلوك التغذية ، والمزيد. ومع ذلك ، فإن عدم التجانس العصبي في منطقة ما تحت المهاد يجعل هذا الجهد صعبا ، وهناك حاجة إلى طرق لعزل ودراسة مجموعات فرعية محددة تحت المهاد.
تستخدم التقنيات في الجسم الحي CRE-recombinase ، وعلم البصريات ، والقياس الضوئي للألياف ، وتصوير الكالسيوم. تسمح هذه الأساليب في المقام الأول بدراسة الخصائص الكهربائية للخلايا العصبية تحت المهاد ، وهناك عدد قليل جدا من الطرق المتاحة حاليا للتحقيق في سماتها غير الكهربائية. يمكن أن توفر تقنية MACS التي تم تطويرها في هذه الدراسة تقنية قابلة لعزل مجموعات فرعية محددة من الخلايا العصبية تحت المهاد في المختبر ، وبالتالي توفير العلاجات والتحليلات المستهدفة. الثقافات العصبية أسهل في الإدارة مقارنة بالثقافات المشتركة لمجموعات عصبية مختلفة. بالإضافة إلى ذلك ، تتجنب الثقافات النقية الآثار المربكة الناجمة عن وجود الخلايا الدبقية والخلايا الدبقية الصغيرة. وبالتالي ، يمكن دراسة الخلايا العصبية من نفس المنطقة والنوع تحت المهاد استجابة لمدخلات التمثيل الغذائي والهرمونية المحددة.
في هذا البروتوكول ، اخترنا الخلايا العصبية تحت المهاد التي تعبر عن LepR. تم استزراع خلايا LepR + المعزولة للتحقيق في خصائصها الخلوية والمورفولوجية والجزيئية التي يصعب دراستها في الجسم الحي. كان نقاء الثقافات 99 ٪ ، مما يدعم دقة الطريقة. بالإضافة إلى ذلك ، كانت خلايا LepR + صحية وقابلة للحياة في DIV7 حتى DIV21.
هذه التقنية ، ومع ذلك ، لديها بعض القيود. E18 أو أقدم الثقافات العصبية النقية يصعب الحفاظ عليها. لذلك ، تقتصر نافذة الاستخراج على E14-E16. هذا يعني أن التغييرات الخلوية التي تحدث بعد E16 مفقودة. على سبيل المثال ، يزداد التعبير عن مستقبلات اللبتين في الخلايا العصبية ARC خلال فترة ما بعد الولادة المبكرة22. يجب إجراء إجراء العزل في أسرع وقت ممكن لتقليل الإجهاد الخلوي والموت وتحسين الغلة. يمكن أن يستغرق الإجراء ما يصل إلى 5 ساعات ؛ وبالتالي ، من الضروري الحفاظ على الظروف المعقمة وتقليل التلاعب إلى الحد الأدنى الضروري. يمكن أن يؤدي الاختيار الإيجابي إلى انخفاض الغلة بسبب انخفاض كميات الأنسجة المتاحة ، مما يحد من عدد التجارب التي يمكن إجراؤها باستخدام إعداد واحد. لوحظ ارتفاع موت الخلايا العصبية ، ربما بسبب انخفاض كثافة الخلايا وانخفاض الاتصال العصبي والدعم داخل الخلايا العصبية.
علاوة على ذلك ، يجب أن يرتبط الجسم المضاد الذي يستهدف المستضد محل الاهتمام بسطح الخلية لضمان الفصل الصحيح ؛ عادة ما تكون الأجسام المضادة المستخدمة في قياس التدفق الخلوي مناسبة لتقنية MACS. إذا لم يتم استخدام الجسم المضاد من قبل في طرق فصل الخلايا ، فستكون هناك حاجة إلى تجارب التحقق والمعايرة لتحديد الاستخدام والتركيز المثاليين. يتطلب استخراج الخلايا المستهدفة علامة سطح الخلية. هنا استخدمنا جسما مضادا بيوتينيلاتي ولكن من حيث المبدأ ، يمكن أيضا استخدام الأجسام المضادة المترافقة مع جزيئات أخرى ، مثل FITC (فلوريسئين إيزوثيوسيانات) و PE (مضاد فيكويريثرين المنقى). يمكن أيضا تطبيق تقنية MACS على الخلايا العصبية التي تعبر عن الفلوروفور ، مثل GFP أو بروتين Tag آخر ، مما قد يزيد من الخصوصية والعائد. إذا لم يتم استخدام الفلوروفور ، فسيكون البديل هو تأكيد التعبير عن الجزيء محل الاهتمام عن طريق التألق المناعي قبل إجراء تجارب الخلايا الحية. ستختبر الدراسات المستقبلية صحة هذه البدائل.
أحد الجوانب المهمة التي لم تعالجها هذه الدراسة يتعلق ب "إخلاص" المجموعات العصبية الفرعية. تأكدنا من أن الخلايا العصبية LepR + المستزرعة عبرت عن POMC ، وهو توقيع للخلايا العصبية الأصليةARC POMC . ومع ذلك ، سيكون من الضروري إجراء المزيد من الاختبارات لاستنتاج أن الثقافات العصبية LepR + تلخص نظيراتها الأصلية في الجسم الحي . بشكل عام ، قد يوفر بروتوكول عزل الخلايا العصبية MACS المقدم هنا طريقة صالحة وفعالة لدراسة آليات المهاد في المختبر والتي سيكون من الصعب التحقيق فيها في الجسم الحي.
Disclosures
يعلن أصحاب البلاغ أنه ليس لديهم تضارب في المصالح.
Acknowledgements
تم إنشاء الأشكال الرسومية مع BioRender.com. تم دعم هذا العمل من خلال منحة NIA (R01AG060919) ومنحة NSF (2030348) إلى FS.
Materials
| Name | Company | Catalog Number | Comments |
| Embryo extraction | |||
| 1 curved point forceps | Fine Science Tools | 11270-20 | Dumont |
| 1 fine surgical scissor | Fine Science Tools | 14058-11 | Dumont |
| 100 mm Petri dish | Corning | 430167 | |
| 2 straight fine forceps | Fine Science Tools | 11254-20 | Dumont |
| 60 mm Petri dish | Corning | 430196 | |
| 70% ethanol | Decon Laboratories, INC. | 2801 | Ethanol 190 Proof |
| Anti-Biotin MicroBeads 1mL | Miltenyi Biotec | 130-115-390 | |
| Anti-MAP2 antibody | Abcam | ab5392 | 1 : 800 |
| Bench pads | |||
| Bovine Serum Albumin | Sigma-Aldrich | A9418-50G | |
| Buffer Y | Miltenyi Biotec | 130-094-802 | |
| Buffer Z | Miltenyi Biotec | 130-094-802 | |
| Cell Culture | |||
| Anti-Biotin MicroBeads 1mL | Miltenyi Biotec | 130-115-390 | |
| Bovine Serum Albumin | Sigma-Aldrich | A9418-50G | |
| Buffer Y | Miltenyi Biotec | 130-094-802 | |
| Buffer Z | Miltenyi Biotec | 130-094-802 | |
| Enzyme A | Miltenyi Biotec | 130-094-802 | |
| Enzyme P | Miltenyi Biotec | 130-094-802 | |
| GG-12-1.5, 12 mm dia.#1.5 thick 100 pc cell culture tested German coverglasses | Neuvitro Corporation | GG-12-15 | |
| Gibco B-27 Supplement 10 mL | ThermoFisher | 17504-044 | |
| Gibco Basal Medium Eagle (BME) 500 mL | ThermoFisher | 21010046 | (+) Earle's Salts, (-) L-Glutamine |
| Gibco HBBS (1x) Hanks' Balanced Salt Solution 500 mL | ThermoFisher | 14025092 | Calcium, Magnesium, No phenol red |
| Gibco HI FBS 100 mL | ThermoFisher | 16140-063 | |
| Gibco L-Glutamine 200 mM (100x) | ThermoFisher | 25030-081 | |
| Gibco Penicilline/Streptomicine | ThermoFisher | 15140-122 | 10,000 U/mL |
| Gibco Sodium Pyruvate (100 mM) 100 mL | ThermoFisher | 11360070 | |
| MiniMACS Separator and Starting Kit | Miltenyi Biotec | 130-042-102 | |
| Mouse Leptin R Biotinylated Antibody | R&D Systems | ABAF497 | 0.25 μg/106 cells |
| MS Column | Miltenyi Biotec | 130-042-201 | |
| Neaubeaur-Improved Brightline 100 µm Chamber | Hausser Scientific | 3120 | |
| Neural Tissue Dissociation Kit - Postnatal Neurons | Miltenyi Biotec | 130-094-802 | |
| Neuronal Culture Medium 500 mL | ThermoFisher | 88283 | |
| Non-Neuronal Cell Biotin-Antibody Cocktail mouse 1 mL | Miltenyi Biotec | 130-115-389 | |
| Olympus SZ61 Zoom Stereomicroscope | Olympus Life Science | SZ61/SZ51 | |
| Pierce Primary Neuron Isolation Kit | ThermoFisher | 88280Y | |
| Staining | |||
| Anti-MAP2 antibody | Abcam | ab5392 | 1 : 800 |
| Donkey anti-Mouse IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor Plus 488 | ThermoFisher | A32766 | 1 : 500 |
| Donkey anti-Rabbit IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor Plus 488 | ThermoFisher | A32790 | 1 : 500 |
| Dulbecco's Phosphate Buffered Saline (DPBS) | Sigma Aldrich | MFCD00131855 | |
| Goat anti-Chicken IgY (H+L) Cross-Adsorbed Secondary Antibody, Alexa Fluor Plus 647 | ThemoFisher | A32933 | 1 : 500 |
| Goat anti-Rabbit IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor 594 | ThermoFisher | A11037 | 1 : 200 |
| Invitrogen Leptin Receptor Recombinant Rabbit Monoclonal Antibody (JA73-01) | ThermoFisher | MA5-32685 | 1 : 500 |
| Mouse Leptin R Biotinylated Antibody | R&D Systems | ABAF497 | 1 : 500 |
| POMC Rabbit mAb | Cell Signaling Technology | D3R1U | 1 : 500 |
| PSD95 (D74D3) XP Rabbit mAb | Cell Signaling Technology | D74D3#3409 | 1 : 500 |
| Streptavidin, Alexa Fluor 594 conjugate | ThermoFisher | S11227 | 1 : 500 |
| Synapsin 1 Monoclonal Antibody (7H10G6) | ThermoFisher | MA5-31919 | 1 : 500 |
| Vectashield Plus Antifade Mountina Medium with DAPI 10 mL | Vector Laboratories | H-2000 |
References
- Cone, R. D. Anatomy and regulation of the central melanocortin system. Nature Neuroscience. 8 (5), 571-578 (2005).
- Clarke, I. J. Hypothalamus as an endocrine organ. Comprehensive Physiology. 5 (1), 217-253 (2015).
- Mignot, E., Taheri, S., Nishino, S. Sleeping with the hypothalamus: emerging therapeutic targets for sleep disorders. Nature Neuroscience. 5 Suppl, 1071-1075 (2002).
- Baird, A. D., Wilson, S. J., Bladin, P. F., Saling, M. M., Reutens, D. C. Neurological control of human sexual behaviour: insights from lesion studies. Journal of Neurology, Neurosurgery, and Psychiatry. 78 (10), 1042-1049 (2007).
- Caria, A., Dall, O. G. Functional neuroimaging of human hypothalamus in socioemotional behavior: a systematic review. Brain Sciences. 12 (6), 707(2022).
- Andermann, M. L., Lowell, B. B. Toward a wiring diagram understanding of appetite control. Neuron. 95 (4), 757-778 (2017).
- Romanov, R. A., Alpar, A., Hokfelt, T., Harkany, T. Unified classification of molecular, network, and endocrine features of hypothalamic neurons. Annual Review of Neuroscience. 42, 1-26 (2019).
- Hajdarovic, K. H., Yu, D., Webb, A. E. Understanding the aging hypothalamus, one cell at a time. Trends in Neurosciences. 45 (12), 942-954 (2022).
- Zhang, Y. H., et al. Cascade diversification directs generation of neuronal diversity in the hypothalamus. Cell Stem Cell. 28 (8), 1483-1499 (2021).
- Chen, R., Wu, X., Jiang, L., Zhang, Y. Single-cell RNA-seq reveals hypothalamic cell diversity. Cell Reports. 18 (13), 3227-3241 (2017).
- Ma, C., et al. Neural pathways from hypothalamic orexin neurons to the ventrolateral preoptic area mediate sleep impairments induced by conditioned fear. Frontiers in Neuroscience. 17, 1122803(2023).
- Wang, F., et al. A parabrachial to hypothalamic pathway mediates defensive behavior. Elife. 12, e85450(2023).
- Cowley, M. A., et al. Leptin activates anorexigenic POMC neurons through a neural network in the arcuate nucleus. Nature. 411 (6836), 480-484 (2001).
- Parekh, R. U., et al. Hypothalamic kinin B1 receptor mediates orexin system hyperactivity in neurogenic hypertension. Scientific Reports. 11 (1), 21050(2021).
- Schmidt, C. X., Tsang, A. H., Oster, H. Generation of mouse primary hypothalamic neuronal cultures for circadian bioluminescence assays. Bio-protocol. 11 (5), e3944(2021).
- Foo, L. C. Purification of rat and mouse astrocytes by immunopanning. 2013 (5), Cold Spring Harbor Protocols. 421-432 (2013).
- Emery, B., Dugas, J. C. Purification of oligodendrocyte lineage cells from mouse cortices by immunopanning. 2013 (9), Cold Spring Harbor Protocols. 854-868 (2013).
- Zhao, H., et al. Changes of constituents and activity to apoptosis and cell cycle during fermentation of tea. International Journal of Molecular Sciences. 12 (3), 1862-1875 (2011).
- Zhang, Z. M., et al. Down-regulation of human leukocyte antigens class I on peripheral T lymphocytes and NK cells from subjects in region of high-incidence gastrointestinal tumor. Chinese Medical Journal. 124 (12), 1813-1817 (2011).
- Drake, S. S., Zaman, A., Simas, T., Fournier, A. E. Comparing RNA-sequencing datasets from astrocytes, oligodendrocytes, and microglia in multiple sclerosis identifies novel dysregulated genes relevant to inflammation and myelination. WIREs Mechanisms of Disease. 15 (2), e1594(2023).
- Mattanovich, D., Borth, N. Applications of cell sorting in biotechnology. Microbial Cell Factories. 5, 12(2006).
- Cottrell, E. C., et al. Developmental changes in hypothalamic leptin receptor: relationship with the postnatal leptin surge and energy balance neuropeptides in the postnatal rat. American Journal of Physiology. Regulatory, Integrative and Comparative Physiology. 296 (3), R631-R639 (2009).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved