Method Article
تغطية قوقعة صناعية محسنة والحفاظ على السمع في حالات فقدان السمع عالية التردد عبر التحفيز الصوتي الكهربائي باستخدام قطب كهربائي أطول
In This Article
Summary
يمكن أن يوفر التحفيز الصوتي الكهربائي (EAS) مع الأقطاب الكهربائية الأطول تغطية أوسع للقوقعة الصناعية وأنواعا مختلفة من الخرائط في حالات فقدان السمع عالي التردد. يسمح الجمع بين الجراحة الأقل توغلا والأقطاب الكهربائية المرنة للجدار الجانبي وإعطاء الستيرويد بإدخال أعمق مع صدمة جراحية قليلة أو معدومة ، مما يؤدي إلى الحفاظ على السمع بشكل جيد.
Abstract
التحفيز الكهربائي الصوتي (EAS) هو علاج واعد لتحسين القدرة على السمع لدى المرضى الذين يعانون من ضعف السمع عالي التردد (HL). في جراحات EAS ، تم تفضيل أقطاب كهربائية أقصر لتجنب وجود قطب كهربائي يغطي منطقة السمع المتبقية. ومع ذلك ، أظهرت دراساتنا السابقة أن EAS مع أقطاب كهربائية أطول (28 مم) يمكن أن تحافظ على السمع الصوتي. بالإضافة إلى ذلك ، أبلغنا أن درجات الحفاظ على السمع (HP) كانت مستقلة عن طول الأقطاب الكهربائية التي تم إدخالها ، بما يتفق مع المراجعة المنهجية. نظرا لأن معظم مرضى EAS يفقدون السمع المتبقي تدريجيا بمرور الوقت بسبب المسار الطبيعي ل HL ، في هذه الحالات ، كان توفير تغطية قوقعة صناعية أوسع باستخدام أقطاب كهربائية أطول مفيدا في مطابقة أفضل للمكان. بالإضافة إلى الاستعداد لتدهور السمع في المستقبل ، يمكن أن تقدم EAS ذات الأقطاب الكهربائية الأطول أنواعا مختلفة من استراتيجيات الخرائط. هنا ، نعرض الإجراءات السابقة والداخلية واللاحقة لجراحة EAS. أدى التقييم المناسب قبل الجراحة ، والجراحة الأقل توغلا ، والأقطاب الكهربائية المرنة للجدار الجانبي ، وإدارة الستيرويد إلى صحة جيدة بعد EAS بأقطاب كهربائية أطول.
Introduction
زراعة القوقعة الصناعية التقليدية (CI) هي علاج قياسي لتحسين القدرة على السمع لدى المرضى الذين يعانون من ضعف السمع الشديد إلى العميق (HL). بعد ذلك ، يتم استخدام التحفيز الكهربائي الصوتي (EAS) لعلاج المرضى الذين يعانون من ضعف السمع الشديد عالي التردد والسمع المتبقي منخفضالتردد 1. في مثل هؤلاء المرضى ، يعد الحفاظ على السمع الصوتي المتبقي أمرا مهما لتحقيق إدراك أفضل للكلام في الضوضاء ، وتوطين الصوت ، وتحسين جودة الصوت عند الاستماع إلى الموسيقى2. لمعالجة هذا الأمر ، تم تفضيل استخدام أقطاب كهربائية أقصر في مرضى EAS لتجنب التدخل في الوظيفة المتبقية في المنطقة الصوتية للقوقعة. ومع ذلك ، فقد وثقت دراساتنا السابقة3،4،5،6 أنه حتى في حالات EAS ، مكنت جراحة CI الأقل توغلا جنبا إلى جنب مع الأقطاب الكهربائية "الأطول" الرفيعة والمستقيمة والمرنة من الحفاظ على السمع المتبقي. بالإضافة إلى ذلك، أبلغنا أن الحفاظ على السمع لم يكن مرتبطا بطول قطب غرسة القوقعة الصناعية الذي تم إدخاله7، بما يتفق مع المراجعة المنهجية8.
في المرضى الذين خضعوا ل CI التقليدي ، أدت الأقطاب الكهربائية الأطول إلى إدراك أفضل للكلام9،10،11 حيث توفر الأقطاب الكهربائية الأطول تغطية قوقعة صناعية أوسع ومطابقة أفضل للمكان. وبالمثل ، تم الإبلاغ عن وجود علاقة بين زاوية الإدخال العميقة (AID) والسمع الأفضل12،13. في معظم مرضى EAS ، يتدهور السمع المتبقي تدريجيا بمرور الوقت14. يسمح تحديد الجين المسؤول عن HL للمرء بالتنبؤ بالسمع في المستقبل. عندما يتوقع فقدان سمعهم عبر جميع الترددات في المستقبل ، فإن EAS مع أقطاب كهربائية أطول ، وليس أقطاب كهربائية أقصر ، مثالي في توفير نسبة مئوية أعلى من تغطية القوقعةالصناعية 15. كان يعتقد أن AID الأمثل يتراوح من 630 درجة إلى 720 درجة 16،17،18 ، وهو ما يتوافق مع توزيع الخلايا العصبية العقدية الحلزونية في القوقعة البشرية. ومع ذلك ، نظرا لأن كل طول قناة قوقعة صناعية (CDL) له نطاق واسع من التباين19 ، فقد كان قياس CDL في كل حالة مطلوبا لتحقيق AID المناسب ، حتى في مرضى EAS. في الآونة الأخيرة ، سمحت البرامج المتاحة تجاريا (انظر جدول المواد) بقياس كل CDL بسهولة بناء على بيانات التصوير المقطعي المحوسب (CT) ، والتي كانت ممكنة سريريا.
يصف هذا البروتوكول ما يلي: (1) تقييم ما قبل الجراحة تضمن التحليل الجيني لتحديد مسببات قياس طول القناة القوقعية وقياس طول القوقعة الصناعية لتحديد طول القطب الأمثل ، (2) إجراء جراحي أقل توغلا عن طريق التنظير الخارجي والتنظير الداخلي ، و (3) نتائج السمع بعد الجراحة واستراتيجية رسم الخرائط في المرضى الذين يعانون من HL عالي التردد الذين خضعوا ل EAS بقطب أطول.
Protocol
تمت الموافقة على الإجراءات الموصوفة من قبل مجلس المراجعة المؤسسية لكلية الطب بجامعة شينشو (الموافقة رقم 4133). قدم المرضى موافقة خطية مستنيرة قبل المشاركة في الدراسة. الكواشف والمعدات والبرامج المستخدمة في هذه الدراسة مدرجة في جدول المواد.
1. تقييم ما قبل الجراحة
- راجع سلسلة مخططات السمع النقية في المرضى الذين يعانون من السمع المتبقي للتأكد من تطور HL في كل حالة.
- إجراء الاختبارات الجينية على عينات الدم التي تم الحصول عليها من كل من المرضى وأفراد أسرهم.
- يوصي بإجراء تسلسل الجيل التالي على لوحة من الجينات المرتبطة ب HL 6,7.
- إجراء اختبارات التصوير، مثل التصوير المقطعي المحوسب و/أو التصوير بالرنين المغناطيسي (MRI). يوصى بأن يكون سمك شريحة التصوير المقطعي المحوسب 0.6 مم أو أقل. بالنسبة للتصوير بالرنين المغناطيسي ، اعتبرت قوة 1.5 تسلا كافية.
- قم بعمل تنبؤات بشأن السمع السمعي المتبقي في المستقبل إلى أقصى حد ممكن بعد جمع سلسلة مخطط السمع6 وتحديد المسببات من خلال التصوير و / أو التحليل الجيني.
- استيراد بيانات DICOM من صور التصوير المقطعي المحوسب قبل الجراحة إلى برنامج OTOPLAN. يقيس البرنامج تلقائيا CDL في كل حالة.
- حدد الطول المناسب لمصفوفة CI لتغطية المنطقة التي يتوقع أن يتدهور فيها السمع المتبقي في المستقبل. استخدم فقط أقطاب كهربائية رفيعة ومستقيمة ومرنة.
- تطبيق بريدنيزولون عن طريق الفم بجرعة 0.5-1.0 ملغ/كغ/يوم ابتداء من يومين قبل الجراحة.
2. الإجراء الجراحي
- ضع المريض في وضع ضعيف.
- تحفيز التخدير باستخدام الفنتانيل الوريدي (1-2 ميكروغرام / كغ) ، والبروبوفول (1-2 مجم / كجم) ، والروكورونيوم (0.6 مجم / كجم). الحفاظ على التخدير باستخدام البروبوفول (3-8 مجم / كجم / ساعة) ، ورميفنتانيل (0.1-0.2 ميكروغرام / كجم / دقيقة) ، والفنتانيل (الإجمالي: 300-500 ميكروغرام) ، بدون الفيكورونيوم ، لتسهيل المراقبة العصبية العضلية.
- يجب تطبيق التسريب الوريدي بمقدار 8 ملغ من ديكساميثازون قبل إجراء الشق ب 30 دقيقة.
- قم بتدوير رأس المريض إلى 45 درجة أثناء الجراحة.
- حقن التخدير الموضعي (تحت الجلد 0.5٪ ليدوكائين مع 1: 1،00،000 أدرينالين) بعد الأذن.
- قم بإجراء شق ما بعد الأذن بطول 5-6 سم (على شكل حرف S) واستئصال الخشاء باستخدام قضبان قطع 6.0-4.0 مم حتى الوصول إلى النقطة التي يشتمل فيها الطبق على القناة الجانبية نصف الدائرية والعملية القصيرة للإنكس6.
- قم بإجراء بضع الطبلة الخلفي بين العصب الوجهي المتوقع وطبلة الأذن الحبلية باستخدام قضبان ماسية 1.5-2.0 مم.
- تخيل مكانة النافذة المستديرة وقم بإزالة الجزء المتدلي العظمي للنافذة المستديرة باستخدام مثقاب منخفض السرعة مع قضيب ماسي 1.0-1.5 مم ، مما يكشف غشاء النافذة المستدير.
- افتح غشاء النافذة المستدير بشكل كاف باستخدام معول وأدخل القطب ببطء ببطء لأكثر من 3 دقائق.
- إجراء الأشعة السينية وتصوير السمع بعد الانتهاء من إدخال القطب.
3. تقييم ما بعد الجراحة
- تطبيق ديكساميثازون عن طريق الوريد بمعدل 8 ملغ/يوم، و4 ملغ/يوم، و4 ملغ/يوم لمدة 3 أيام بعد الجراحة.
- قم بقياس العتبات السمعية غير المدعومة بعد 6 أشهر من التنشيط الأولي ، وقم بتقييم معدل HP باستخدام التصنيف المقدم من Skarzynski et al.20.
- قم بتحسين إعدادات الخريطة باستخدام أداة برمجية بناء على نتائج مخطط السمع بعد الجراحة وتفضيلات المريض.
النتائج
تم إجراء EAS على 10 مرضى (11 أذن) استوفوا المعايير السمعية ل EAS (راجع الجدول 1). وتضمنت معايير الإدراج ما يلي: مستويات السمع النقي الثنائي ≤65 ديسيبل ل 125 هرتز و 250 هرتز و 500 هرتز. ≥80 ديسيبل عند 2000 هرتز ؛ و ≥85 ديسيبل عند 4000 هرتز و 8000 هرتز. بالإضافة إلى ذلك ، كانت هناك حاجة إلى الحد الأدنى من الفائدة من المعينات السمعية التقليدية ، والتي تم تعريفها على أنها درجات أحادية المقطع في هدوء أقل من 60٪ حتى في الحالة المثلى. خضع جميع المشاركين لاختبار EAS باستخدام أقطاب كهربائية أطول (انظر جدول المواد). يوضح الشكل 1 مخططات السمع قبل الجراحة وبعد 6 أشهر بعد جراحة EAS ، مما يشير إلى أن السمع المتبقي منخفض التردد قد تم الحفاظ عليه جيدا في جميع الحالات. وفقا لنظام تصنيف الحفاظ على السمع (HP) الذي أبلغ عنه Skarzynski et al.20 ، أظهر 36.4٪ (4 من 11 حالة) صحة كاملة ، و 63.6٪ (7 من 11 حالة) أظهروا HPs جزئيا. لم تكن هناك حالات تدهور كبير في السمع.
عرض الحالة (الحالة #8)
في سن الخامسة ، أثناء فحص صحي روتيني في المدرسة الابتدائية ، تم الإبلاغ عن فتاة تبلغ من العمر 14 عاما لم تخضع لفحص السمع لحديثي الولادة للاشتباه في إصابتها بفقدان السمع (HL). بعد تشخيص إصابتها ب HL عالي التردد ، بدأت في استخدام المعينات السمعية. نظرا للتدهور الملحوظ في سمعها ، طلبت التقييم في قسمنا في سن 13 عاما.
تم تحديد المتغيرات المسببة للأمراض لجين CDH23 من خلال الاختبار الجيني6. نظرا لأنه كان من المحتمل أن يتدهور السمع المتبقي بسبب HL المرتبط ب CDH23 ، فقد تم اختيار قطب أطول لتغطية المنطقة الصوتية. خضعت لعملية جراحية EAS في الأذن اليسرى في سن 14 عاما. تم الحفاظ على السمع المتبقي بالكامل بعد 6 أشهر من الجراحة. فضلت "رسم خرائط التحفيز الكهربائي (ES) فقط" مع أقطاب كهربائية قمية نشطة تعبر منطقة السمع المتبقي في ذلك الوقت (الشكل 2). كان المريض راضيا عن التضخيم الصوتي الذي تم الحصول عليه باستخدام ES عند الترددات المنخفضة.
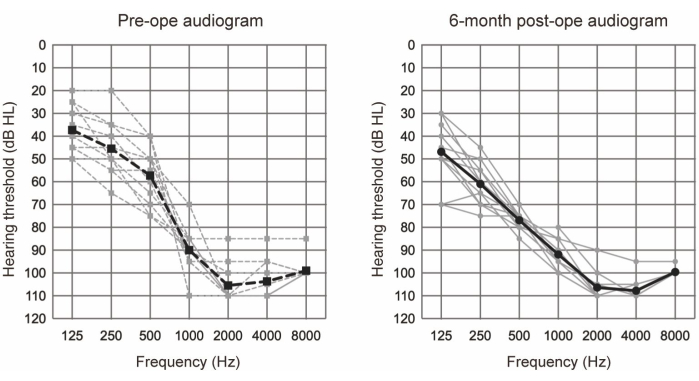
الشكل 1: متوسط عتبات السمع في التوصيل الهوائي. تشير الخطوط المتقطعة والصلبة إلى قياسات ما قبل الجراحة وما بعد الجراحة لمدة 6 أشهر ، على التوالي. يظهر الخطان الرمادي والأسود البيانات الفردية والمتوسط ، على التوالي. تم اقتباس هذا الرقم من Yoshimura et al.6. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
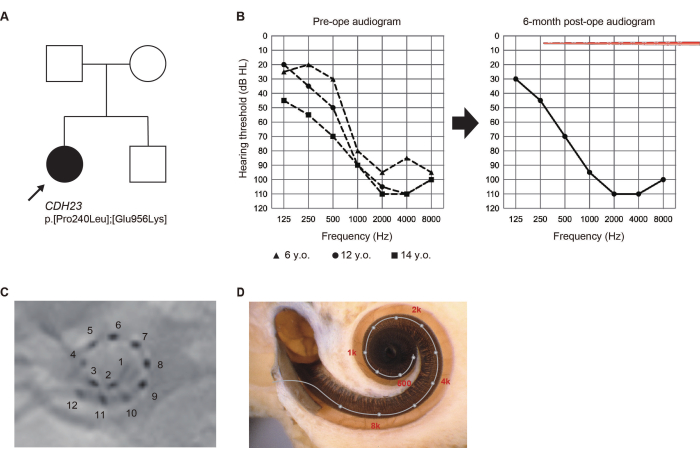
الشكل 2: النتائج السريرية للحالة # 8. (أ) نسب المريض. (ب) مخططات السمع قبل الجراحة وبعد 6 أشهر. تمثل الرسوم التوضيحية لمصفوفة الأقطاب عمق الإدخال. (ج) نتائج الأشعة السينية بعد الجراحة ، مع أرقام تتوافق مع القنوات الفردية. (د) التصوير لكل موقع قطب كهربائي والخريطة المرجعية للتونوتوب. تم اقتباس هذا الرقم من Yoshimura et al.6. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
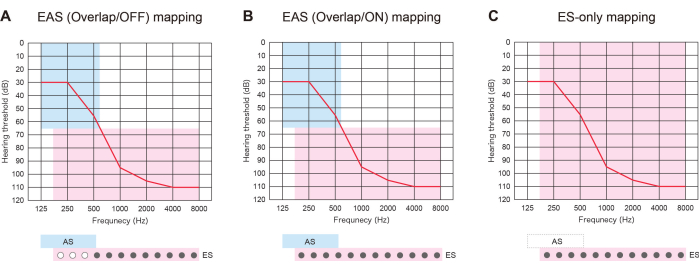
الشكل 3: ثلاثة أنواع من استراتيجية رسم الخرائط في المرضى الذين يعانون من EAS باستخدام أقطاب كهربائية أطول. (أ) خريطة EAS (التداخل / الإيقاف). تم إلغاء تنشيط بعض جهات الاتصال القمية ، بينما تم تنشيط التحفيز الصوتي (AS). (ب) خريطة EAS (التداخل/التشغيل). تم استخدام كل من التحفيز الكهربائي (ES) في الإعداد الافتراضي لزرع القوقعة الصناعية (CI) و AS. (ج) خريطة ES فقط. في إعداد ES ، تم ضبط مدى التردد من 70-8,500 هرتز. الرجاء النقر هنا لعرض نسخة أكبر من هذا الرقم.
| صبور | مزروع | مزروع | مسؤول | ما قبل العملية | 6 م بعد العملية | HP العددي | إتش بي | |
| لا. | جنس | العمر (سنوات) | جنب | الجين | LFA (ديسيبل) | LFA (ديسيبل) | مقياس (٪) | تصنيف |
| 1 | F | 12 | L | SLC26A4 | 63.3 | 70 | 70.8 | جزئي |
| 2 | F | 9 | L | SLC26A4 | 50 | 65 | 62.5 | جزئي |
| 3 | M | 50 | L | سي دي إتش 23 | 50 | 56.7 | 78.6 | كامل |
| 4 | F | 31 | L | مجهول | 45 | 61.7 | 67.7 | جزئي |
| 31 | R | 46.7 | 56.7 | 75.9 | كامل | |||
| 5 | F | 57 | R | مجهول | 38.3 | 65 | 59 | جزئي |
| 6 | F | 55 | R | مجهول | 26.7 | 55 | 68.4 | جزئي |
| 7 | M | 21 | R | لوكسد 1 | 33.3 | 66.7 | 37.2 | جزئي |
| 8 | F | 14 | R | سي دي إتش 23 | 56.7 | 48.3 | 100 | كامل |
| 9 | M | 20 | L | مجهول | 51.7 | 73.3 | 48.1 | جزئي |
| 10 | M | 64 | R | مجهول | 51.7 | 58.3 | 82.1 | كامل |
الجدول 1: ملخص خصائص الموضوع ونتائج الحفاظ على السمع. تم اقتباس هذا الجدول من Yoshimura et al.6.
Discussion
يعد تحديد مسببات HL في تقييم ما قبل الجراحة أمرا بالغ الأهمية للتنبؤ بمخطط السمع المستقبلي في كل حالة. في دراستنا السابقة ، تم تحديد المتغيرات المسببة للأمراض في CDH23 و ACTG1 و Mit1555A>G و MYO7A و MYO15A و SLC26A4 و TMPRSS3 بشكل متكرر في المرضى الذين يعانون من HL7 عالي التردد. في معظم هؤلاء المرضى ، تدهور السمع المتبقي تدريجيا (انظر حالة HL المتعلقة ب CDH23 في الشكل 2). في هذه الحالات ، تم أخذ المسار الطبيعي ل HL في الاعتبار عند اختيار قطب CI لتغطية القوقعة الصناعية الأوسع.
يتطلب تحديد طول مصفوفة القوقعة الصناعية قياس طول قناة القوقعة الصناعية (CDL). لتسهيل هذه العملية ، أثبت برنامج OTOPLAN أنه ممكنسريريا 21. في الإصدارات السابقة ، مثل OTOPLAN 3.0 ، تم قياس CDL يدويا لرسم قطر كل قوقعة وعرض وارتفاع. ومع ذلك ، مع OTOPLAN 4.0 ، أصبح القياس التلقائي ل CDL ممكنا ، مما يوفر مزيدا من الراحة للجراحين ويقلل من تباين القياس. والجدير بالذكر أن صور التصوير المقطعي المحوسب بسمك شريحة 0.6 مم أو أقل كانت مناسبة للتحليل التلقائي الذي قدمته OTOPLAN. بعد ذلك ، يجب تحديد طول مصفوفة CI لتحقيق الزاوية المثلى لعمق الإدراج (AID) في كل حالة.
لإجراء جراحة EAS أقل توغلا ، كانت هناك حاجة إلى إدارة ما قبل وأثناء وبعد الستيرويد لتقليل الالتهاب الحاد الذي يمكن أن يرفع عتبة السمع22. في المستقبل القريب ، لتقليل ليس فقط التفاعلات الحادة ولكن أيضا المزمنة بعد جراحة CI و EAS ، سيكون من المستحسن استخدام الأقطاب الكهربائية المملوءة بالديكساميثازون. بالإضافة إلى إعطاء الستيرويد, كانت الأقطاب الكهربائية الجانبية المرنة ضرورية لتقليل الصدمة التي لحقت القوقعة. أدى إدخال مثل هذه الأقطاب الكهربائية في القوقعة بعناية وببطء باستخدام نهج النافذة المستديرة إلى الحد الأدنى من التوغل. للمساعدة في ذلك ، كان إجراء الجراحة باستخدام المناظير الخارجية والمناظير مفيدا لتوليد مجال رؤية أوضح وتأكيد المكونات الدقيقة للأذن الوسطى. لمنع إحداث تكوين أنسجة عظامية ليفية واسعة النطاق في القوقعة ، يجب تجنب نهج النافذة المستديرة الممتدة وفغر القوقعة23.
كان EAS مع الأقطاب الكهربائية الأطول مفيدا ليس فقط للتحضير للتدهور المستقبلي ل HL ولكن أيضا لتقديم ثلاثة أنواع من استراتيجيات الخرائط. إذا تداخلت الأقطاب الكهربائية التي تم إدخالها مع منطقة السمع المتبقية ، فيمكن للمرضى الذين يعانون من EAS استخدام ES مع أو بدون AS: "خريطة EAS (Overlap / ON)" أو "خريطة ES فقط". بدلا من ذلك ، يمكنهم إيقاف تشغيل بعض جهات الاتصال القمية وتنشيط AS: "خريطة EAS (Overlap / OFF)". إذا تدهور السمع ، فيمكن تشغيل جميع جهات الاتصال لاحقا لتوفير مطابقة أفضل لدرجة الصوت (الشكل 3). تظهر كل هذه النتائج أن EAS مع أقطاب كهربائية أطول يسمح للمستخدمين بتحسين الخرائط لمزيد من السمع الطبيعي.
هنا ، يتضح أن التحضير قبل الجراحة والتقنيات الجراحية المتقدمة ضرورية لتقليل الصدمات الجراحية. سمح إجراء سلسلة الإجراءات المذكورة أعلاه قبل وأثناء الجراحة للمرضى بالاستفادة من EAS بأقطاب كهربائية أطول.
القيود
على الرغم من التقدم في الإجراءات الجراحية الأقل توغلا المذكورة أعلاه ، لا يزال السمع المتبقي يتدهور في عدد معين من المرضى بعد CI. ستكون المراقبة أثناء الجراحة ، مثل ميكروفونيات القوقعة الصناعية (CM) ، مجدية سريريا لقياس تلف القوقعة أثناء إدخال القطب24. ومع ذلك ، فإن كيفية تقييم EAS باستخدام أقطاب كهربائية أطول وما يجب فعله في حالة استجابات CM معينة ، مثل انخفاض السعة ، لا تزال غير واضحة حتى الآن. وهناك حاجة إلى مزيد من الدراسات في هذا المجال.
Disclosures
يعلن أصحاب البلاغ عدم وجود تضارب في المصالح.
Acknowledgements
تم تمويل هذا البحث من خلال منحة أبحاث علوم الصحة والعمل للبحث عن الأمراض النادرة والمستعصية والبحث الشامل حول صحة الإعاقة ورفاهيتهم من وزارة الصحة والعمل والرفاهية في اليابان (S.U. 20FC1048 ، 23FC10149) ومنح المعونة من الوكالة اليابانية للبحث والتطوير الطبي (AMED) (SU 19ek0109363h0002 ، 21ek0109542h003).
Materials
| Name | Company | Catalog Number | Comments |
| DEXART 3.3 mg | Fuji Pharma | 22100AMX01404 | equal to dexamethasone sodium phosphate (4 mg) |
| DEXART 6.6 mg | Fuji Pharma | 22100AMX01402 | equal to dexamethasone sodium phosphate (8 mg) |
| Fentanyl injection 0.1 mg | TERUMO | 22100AMX00009 | |
| MAESTRO 7.0 | MED-EL | 4582290238456 | fitting software for map settings |
| Midas Rex MR8 | Medtronic | 301ADBZX00046000 | high speed drill |
| OTOPLAN software | Cascination / MED-EL | REF 20125 | for measuring cochlear duct length (CDL) |
| Predonine tablets | Shionogi | 16000AMZ01740000 | |
| Propofol 1% 50 mL | Maruishi Pharmaceutical Co.,Ltd | 30100AMX00158 | |
| Remifentanil 2 mg | Daiichi-Sankyo | 22800AMX00090 | |
| Rocuronium bromide 50 mg/50 mL | Maruishi Pharmaceutical Co.,Ltd | 22800AMX00534 | |
| SONNET2 EAS | MED-EL | 4582290241807 | processor |
| Synchrony2 FLEX28 | MED-EL | 4571573943026 | cochlear implant (electrode) |
| Xylocaine 0.5% with epinephrine | Sandoz Pharma | 4KUZ13127 |
References
- Von Ilberg, C., et al. Electric-acoustic stimulation of the auditory system. New technology for severe hearing loss. ORL J Otorhinolaryngol Relat Spec. 61 (6), 334-340 (1999).
- Gstoettner, W., et al. A new electrode for residual hearing preservation in cochlear implantation: First clinical results. Acta Otolaryngol. 129 (4), 372-379 (2009).
- Moteki, H., et al. Feasibility of hearing preservation for residual hearing with longer cochlear implant electrodes. Acta Otolaryngol. 138 (12), 1080-1085 (2018).
- Usami, S., et al. Achievement of hearing preservation in the presence of an electrode covering the residual hearing region. Acta Otolaryngol. 131 (4), 405-412 (2011).
- Usami, S., et al. Hearing preservation and clinical outcome of 32 consecutive electric acoustic stimulation (EAS) surgeries. Acta Otolaryngol. 134 (7), 717-727 (2014).
- Yoshimura, H., Moteki, H., Nishio, S. Y., Usami, S. I. Electric-acoustic stimulation with longer electrodes for potential deterioration in low-frequency hearing. Acta Otolaryngol. 140 (8), 632-638 (2020).
- Yoshimura, H., et al. Genetic testing has the potential to impact hearing preservation following cochlear implantation. Acta Otolaryngol. 140 (6), 438-444 (2020).
- Van de Heyning, P. H., et al. Systematic literature review of hearing preservation rates in cochlear implantation associated with medium- and longer-length flexible lateral wall electrode arrays. Front Surg. 9, 893839 (2022).
- Buchman, C. A., et al. Influence of cochlear implant insertion depth on performance: A prospective randomized trial. Otol Neurotol. 35 (10), 1773-1779 (2014).
- Buchner, A., Illg, A., Majdani, O., Lenarz, T. Investigation of the effect of cochlear implant electrode length on speech comprehension in quiet and noise compared with the results with users of electro-acoustic-stimulation, a retrospective analysis. PLoS One. 12 (5), e0174900 (2017).
- Canfarotta, M. W., et al. Long-term influence of electrode array length on speech recognition in cochlear implant users. Laryngoscope. 131 (4), 892-897 (2021).
- Nassiri, A. M., et al. Hearing preservation outcomes using a precurved electrode array inserted with an external sheath. Otol Neurotol. 41 (1), 33-38 (2020).
- O'Connell, B. P., et al. Electrode location and angular insertion depth are predictors of audiologic outcomes in cochlear implantation. Otol Neurotol. 37 (8), 1016-1023 (2016).
- Moteki, H., et al. Long-term results of hearing preservation cochlear implant surgery in patients with residual low frequency hearing. Acta Otolaryngol. 137 (5), 516-521 (2017).
- Von Ilberg, C. A., Baumann, U., Kiefer, J., Tillein, J., Adunka, O. F. Electric-acoustic stimulation of the auditory system: A review of the first decade. Audiol Neurootol. 16, 1-30 (2011).
- Ariyasu, L., Galey, F. R., Hilsinger, R., Byl, F. M. Computer-generated three-dimensional reconstruction of the cochlea. Otolaryngol Head Neck Surg. 100 (2), 87-91 (1989).
- Danielian, A., Ishiyama, G., Lopez, I. A., Ishiyama, A. Morphometric linear and angular measurements of the human cochlea in implant patients using 3-dimensional reconstruction. Hear Res. 386, 107874 (2020).
- Kawano, A., Seldon, H. L., Clark, G. M. Computer-aided three-dimensional reconstruction in human cochlear maps: Measurement of the lengths of organ of Corti, outer wall, inner wall, and Rosenthal's canal. Ann Otol Rhinol Laryngol. 105 (9), 701-709 (1996).
- Rask-Andersen, H., et al. Human cochlea: Anatomical characteristics and their relevance for cochlear implantation. Anat Rec (Hoboken). 295 (11), 1791-1811 (2012).
- Skarzynski, H., et al. Towards a consensus on a hearing preservation classification system. Acta Otolaryngol Suppl. 564, 3-13 (2013).
- Yoshimura, H., Watanabe, K., Nishio, S. Y., Takumi, Y., Usami, S. I. Determining optimal cochlear implant electrode array with OTOPLAN. Acta Otolaryngol. 143 (9), 748-752 (2023).
- Skarzynska, M. B., et al. Preservation of hearing following cochlear implantation using different steroid therapy regimens: a prospective clinical study. Med Sci Monit. 24, 2437-2445 (2018).
- Geerardyn, A., et al. Human histology after structure preservation cochlear implantation via round window insertion. Laryngoscope. 134 (2), 945-953 (2023).
- Campbell, L., et al. Intraoperative real-time cochlear response telemetry predicts hearing preservation in cochlear implantation. Otol Neurotol. 37 (4), 332-338 (2016).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved