Method Article
כיסוי שבלול משופר ושימור שמיעה בליקוי שמיעה בתדרים גבוהים באמצעות גירוי אקוסטי חשמלי עם אלקטרודה ארוכה יותר
In This Article
Summary
גירוי אקוסטי חשמלי (EAS) עם אלקטרודות ארוכות יותר יכול להציע כיסוי שבלול רחב יותר וסוגים שונים של מפות במקרים של אובדן שמיעה בתדר גבוה. שילוב של ניתוח פחות פולשני, אלקטרודות גמישות בדופן הצידית ומתן סטרואידים מאפשר החדרה עמוקה יותר עם מעט או ללא טראומה ניתוחית, וכתוצאה מכך שימור טוב של השמיעה.
Abstract
גירוי חשמלי-אקוסטי (EAS) הוא טיפול מבטיח לשיפור יכולת השמיעה בחולים עם ליקוי שמיעה בתדרים גבוהים (HL). בניתוחי EAS העדיפו אלקטרודות קצרות יותר כדי למנוע נוכחות של אלקטרודה המכסה את אזור השמיעה השיורי. עם זאת, מחקרים קודמים שלנו הראו כי EAS עם אלקטרודות ארוכות יותר (28 מ"מ) יכול לשמר שמיעה אקוסטית. בנוסף, דיווחנו כי ציוני שימור השמיעה (HP) היו בלתי תלויים באורך האלקטרודות שהוחדרו, בהתאם לסקירה השיטתית. מכיוון שרוב מטופלי EAS מאבדים בהדרגה את שאריות השמיעה לאורך זמן עקב המהלך הטבעי של HL, במקרים אלה, מתן כיסוי שבלול רחב יותר באמצעות אלקטרודות ארוכות יותר היה מועיל להתאמה טובה יותר של גובה הצליל. בנוסף להתכוננות להידרדרות בשמיעה בעתיד, EAS עם אלקטרודות ארוכות יותר יכול להציע סוגים שונים של אסטרטגיות מפה. כאן, אנו מראים את ההליכים לפני, תוך ואחרי ניתוח EAS. הערכה טרום ניתוחית מתאימה, ניתוח פחות פולשני, אלקטרודות גמישות בדופן הצידית ומתן סטרואידים הביאו ל-HP טוב לאחר EAS עם אלקטרודות ארוכות יותר.
Introduction
השתלת שבלול קונבנציונלית (CI) היא טיפול סטנדרטי לשיפור יכולת השמיעה במטופלים עם ליקוי שמיעה חמור עד עמוק (HL). לאחר מכן, גירוי חשמלי-אקוסטי (EAS) משמש לטיפול בחולים עם ליקוי שמיעה חמור בתדרים גבוהים ושמיעה שיורית בתדר נמוך1. בחולים כאלה, שימור השמיעה האקוסטית השיורית חשוב להשגת תפיסת דיבור טובה יותר ברעש, לוקליזציה של צלילים ואיכות צליל משופרת בעת האזנה למוזיקה2. כדי להתמודד עם זה, השימוש באלקטרודות קצרות יותר בחולי EAS הועדף כדי להימנע מהפרעה לתפקוד השיורי באזור האקוסטי של השבלול. עם זאת, המחקרים הקודמים שלנו 3,4,5,6 תיעדו כי אפילו במקרים של EAS, ניתוח CI פחות פולשני בשילוב עם אלקטרודות דקות, ישרות וגמישות "ארוכות" יותר אפשרו שימור שמיעה שיורית. בנוסף, דיווחנו כי שימור השמיעה לא היה קשור לאורך אלקטרודת שתל השבלול7 שהוחדרה, בהתאם לסקירה השיטתית8.
במטופלים שעברו CI קונבנציונלי, אלקטרודות ארוכות יותר הובילו לתפיסת דיבור טובה יותר 9,10,11 מכיוון שאלקטרודות ארוכות יותר מספקות כיסוי שבלול רחב יותר והתאמה טובה יותר של גובה הצליל. באופן דומה, דווח על מתאם בין זווית עמוקה יותר של החדרה (AID) לבין שמיעה טובה יותר12,13. ברוב חולי EAS, השמיעה השיורית מידרדרת בהדרגה עם הזמן14. זיהוי הגן האחראי ל-HL מאפשר לחזות שמיעה עתידית. כאשר צפוי שהשמיעה שלהם תאבד בכל התדרים בעתיד, EAS עם אלקטרודות ארוכות יותר, לא אלקטרודות קצרות יותר, הוא אידיאלי במתן אחוז גבוה יותר של כיסוי שבלול15. חשבו שה-AID האופטימלי נע בין 630° ל-720°16,17,18, המקביל להתפלגות נוירוני גנגליון ספירליים בשבלול האנושי. עם זאת, מכיוון שלכל אורך צינור שבלול (CDL) יש מגוון רחב של וריאציות19, מדידת ה- CDL בכל מקרה נדרשה כדי להשיג את ה- AID המתאים, אפילו בחולי EAS. לאחרונה, תוכנה זמינה מסחרית (ראה טבלת חומרים) אפשרה למדוד כל CDL בקלות בהתבסס על נתוני טומוגרפיה ממוחשבת (CT), דבר שהיה אפשרי מבחינה קלינית.
פרוטוקול זה מתאר את הדברים הבאים: (1) הערכה טרום ניתוחית שכללה ניתוח גנטי לזיהוי האטיולוגיה של מדידת אורך HL ואורך צינור השבלול כדי לקבוע את אורך האלקטרודה האופטימלי, (2) הליך כירורגי פחות פולשני באמצעות אקסוסקופיה ואנדוסקופיה, ו-(3) תוצאת השמיעה לאחר הניתוח ואסטרטגיית המיפוי בחולים עם HL בתדר גבוה שעברו EAS עם אלקטרודה ארוכה יותר.
Protocol
ההליכים המתוארים אושרו על ידי מועצת הביקורת המוסדית של בית הספר לרפואה של אוניברסיטת שינשו (אישור מס '4133). המטופלים סיפקו הסכמה מדעת בכתב לפני שהשתתפו במחקר. הריאגנטים, הציוד והתוכנות ששימשו למחקר זה מפורטים בטבלת החומרים.
1. הערכה טרום ניתוחית
- סקור את סדרת האודיוגרמות של צלילים טהורים בחולים עם שמיעה שיורית כדי לוודא את התקדמות HL בכל מקרה.
- לבצע בדיקות גנטיות על דגימות דם שהתקבלו הן מהחולים והן מבני משפחתם.
- ממליץ לבצע ריצוף של הדור הבא על פאנל של גנים הקשורים ל-HL 6,7.
- ביצוע בדיקות הדמיה, כגון CT ו / או דימות תהודה מגנטית (MRI). הומלץ שעובי פרוסת ה-CT יהיה 0.6 מ"מ ומטה. עבור MRI, חוזק של 1.5 טסלה נחשב מספיק.
- בצע תחזיות לגבי שמיעה אקוסטית שיורית עתידית ככל האפשר לאחר איסוף סדרת האודיוגרמה6 וזיהוי האטיולוגיה באמצעות הדמיה ו / או ניתוח גנטי.
- ייבא נתוני DICOM מתמונות CT לפני הניתוח לתוכנת OTOPLAN. התוכנה מודדת באופן אוטומטי את CDL בכל מקרה.
- בחר את האורך המתאים של מערך CI כדי לכסות את האזור שבו השמיעה השיורית צפויה להידרדר בעתיד. השתמש רק באלקטרודות דקות, ישרות וגמישות.
- מתן פרדניזולון דרך הפה במינון של 0.5-1.0 מ"ג/ק"ג/יום החל מיומיים לפני הניתוח.
2. הליך כירורגי
- הניחו את המטופל במצב שכיבה.
- יש להשרות הרדמה באמצעות פנטניל תוך ורידי (1-2 מק"ג/ק"ג), פרופופול (1-2 מ"ג/ק"ג) ורוקורוניום (0.6 מ"ג/ק"ג). שמור על הרדמה עם פרופופול (3-8 מ"ג / ק"ג / שעה), רמיפנטניל (0.1-0.2 מיקרוגרם / ק"ג / דקה), ופנטניל (סה"כ: 300-500 מיקרוגרם), ללא vecuronium, כדי להקל על ניטור עצבי-שרירי.
- לנהל עירוי תוך ורידי של 8 מ"ג של dexamethasone 30 דקות לפני ביצוע החתך.
- סובב את ראשו של המטופל ל -45 מעלות במהלך הניתוח.
- יש להזריק הרדמה מקומית (לידוקאין תת-עורי 0.5% עם אפינפרין בקנ"מ 1:1,00,000) לאחר ההזרקה.
- יש לבצע חתך פוסטאוריקולרי של 5-6 ס"מ (בצורת S עצלה) וכריתת מסטואידקטומיה עם מוטות חיתוך 6.0-4.0 מ"מ עד להגעה לנקודה בה האנטרום כולל את התעלה החצי עגולה הצידית ואת התהליך הקצר של האינקוס6.
- בצע טימפנוטומיה אחורית בין עצב הפנים הצפוי לבין כורדה טימפאני באמצעות מוטות יהלום 1.5-2.0 מ"מ.
- דמיינו את נישת החלון העגול והסירו את הסככה הגרמית של החלון העגול באמצעות מקדחה במהירות נמוכה עם מוט יהלום 1.0-1.5 מ"מ, החושף את קרום החלון העגול.
- פתחו מספיק את קרום החלון העגול באמצעות פיק והכניסו בזהירות את האלקטרודה באיטיות במשך יותר מ-3 דקות.
- בצע צילום רנטגן ואודיוגרמות לאחר השלמת החדרת האלקטרודה.
3. הערכה לאחר הניתוח
- מתן דקסמתזון תוך ורידי במינון 8 מ"ג/יום, 4 מ"ג/יום ו-4 מ"ג/יום במשך 3 ימים לאחר הניתוח.
- מדוד ערכי סף שמיעתיים ללא סיוע 6 חודשים לאחר ההפעלה הראשונית, והערך את קצב HP באמצעות הסיווג שסופק על-ידי Skarzynski et al.20.
- מטב את הגדרות המפה באמצעות כלי תוכנה המבוסס על תוצאות האודיוגרמה שלאחר הניתוח והעדפות המטופל.
תוצאות
EAS נערך על 10 מטופלים (11 אוזניים) אשר מילאו את הקריטריונים האודיולוגיים עבור EAS (עיין בטבלה 1). קריטריוני ההכללה כללו את הדברים הבאים: רמות שמיעה דו-צדדיות בטון טהור ≤65 dBHL עבור 125 הרץ, 250 הרץ ו-500 הרץ; ≥80 dBHL ב-2,000 הרץ; ו- ≥85 dBHL ב- 4000 הרץ ו- 8000 הרץ. בנוסף, נדרשה תועלת מינימלית ממכשירי שמיעה קונבנציונליים, המוגדרים כציוני חד-הברה בשקט מתחת ל-60% גם במצב הסיוע האופטימלי. כל המשתתפים עברו EAS באמצעות אלקטרודות ארוכות יותר (ראה טבלת חומרים). איור 1 מראה את האודיוגרמות לפני הניתוח ו-6 חודשים לאחר ניתוח EAS, דבר המצביע על כך ששאריות שמיעה בתדר נמוך השתמרו היטב בכל המקרים. על פי מערכת סיווג שימור השמיעה (HP) שדווחה על ידי Skarzynski et al.20, 36.4% (4 מתוך 11 מקרים) הראו HP מלא, ו -63.6% (7 מתוך 11 מקרים) הראו HP חלקי. לא היו מקרים של הידרדרות משמעותית בשמיעה.
הצגת מקרה (מקרה #8)
בגיל 5, במהלך בדיקת בריאות שגרתית בבית הספר היסודי, נערה בת 14 שלא עברה בדיקת שמיעה ליילוד סומנה כחשודה לליקוי שמיעה (HL). לאחר שאובחנה עם HL בתדר גבוה, היא החלה להשתמש במכשירי שמיעה. לאור ההידרדרות שנצפתה בשמיעתה, היא פנתה להערכה במחלקה שלנו בגיל 13.
גרסאות פתוגניות של הגן CDH23 זוהו באמצעות בדיקות גנטיות6. מכיוון שהשמיעה השיורית הייתה צפויה להידרדר עקב HL הקשור ל - CDH23, נבחרה אלקטרודה ארוכה יותר לכסות את האזור האקוסטי. היא עברה ניתוח EAS באוזן שמאל בגיל 14. שארית השמיעה נשמרה במלואה 6 חודשים לאחר הניתוח. היא העדיפה "מיפוי של גירוי חשמלי (ES) בלבד" עם אלקטרודות אפיקליות מופעלות שחצו את אזור השמיעה השיורית באותו זמן (איור 2). המטופל היה מרוצה מההגברה האקוסטית שהתקבלה באמצעות ES בתדרים נמוכים.
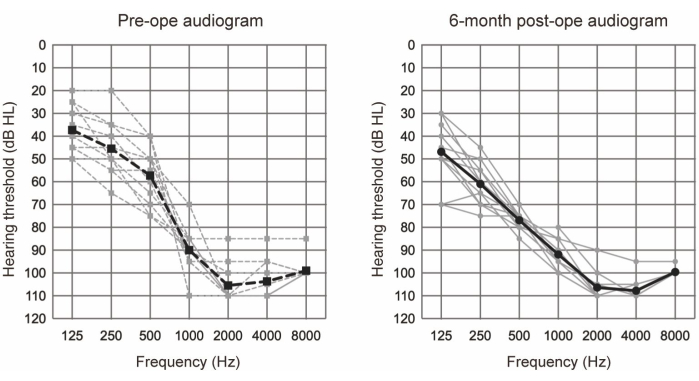
איור 1: סף שמיעה ממוצע של הולכת אוויר. הקווים המקווקווים והמוצקים מציינים מדידות לפני הניתוח ו-6 חודשים לאחר הניתוח, בהתאמה. קווים אפורים ושחורים מציגים את הנתונים הבודדים ואת הממוצע, בהתאמה. איור זה הותאם מיושימורה ואחרים 6. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
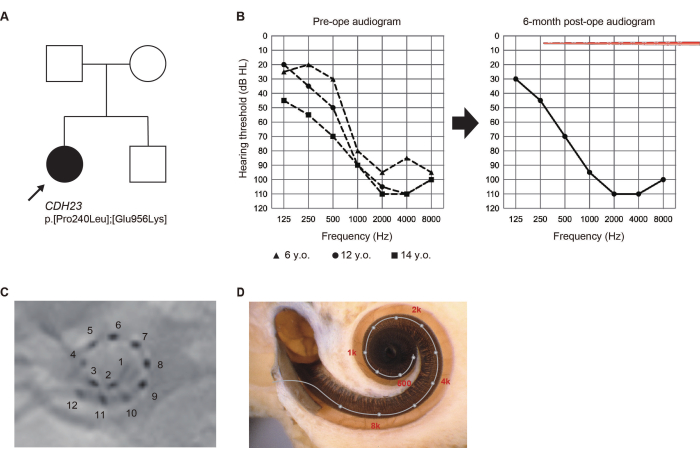
איור 2: ממצאים קליניים של מקרה #8. (A) אילן יוחסין של המטופל. (B) אודיוגרמות לפני הניתוח ו-6 חודשים לאחר הניתוח. איורים של מערך אלקטרודות מייצגים עומק החדרה. (C) ממצאי רנטגן לאחר הניתוח, עם מספרים המתאימים לערוצים בודדים. (D) הדמיה של כל מיקום אלקטרודה ומפת הייחוס לנוטופית. איור זה הותאם מיושימורה ואחרים 6. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
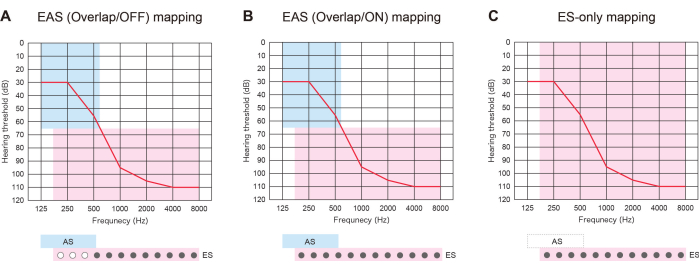
איור 3: שלושה סוגים של אסטרטגיית מיפוי במטופלים עם EAS באמצעות אלקטרודות ארוכות יותר. (A) מפת EAS (חפיפה/כיבוי). חלק מהמגעים האפיים הושבתו, בעוד שהגירוי האקוסטי (AS) הופעל. (B) מפת EAS (חפיפה/ON). נעשה שימוש הן בגירוי חשמלי (ES) בהגדרת ברירת המחדל של השתלת השבלול (CI) והן ב- AS. (C) מפת ES בלבד. בהגדרת ES, טווח התדרים נקבע בין 70-8,500 הרץ. AS הושבת. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
| מטופל | מושתל | מושתל | אחראי | טרום ניתוח | 6 דקות לאחר הניתוח | מספרי HP | HP | |
| לא. | מין | גיל (שנים) | צד | גן | LFA (dB) | LFA (dB) | קנה מידה (%) | מיון |
| 1 | F | 12 | L | SLC26A4 | 63.3 | 70 | 70.8 | חלקית |
| 2 | F | 9 | L | SLC26A4 | 50 | 65 | 62.5 | חלקית |
| 3 | M | 50 | L | CDH23 | 50 | 56.7 | 78.6 | להשלים |
| 4 | F | 31 | L | ידוע | 45 | 61.7 | 67.7 | חלקית |
| 31 | R | 46.7 | 56.7 | 75.9 | להשלים | |||
| 5 | F | 57 | R | ידוע | 38.3 | 65 | 59 | חלקית |
| 6 | F | 55 | R | ידוע | 26.7 | 55 | 68.4 | חלקית |
| 7 | M | 21 | R | LOXHD1 | 33.3 | 66.7 | 37.2 | חלקית |
| 8 | F | 14 | R | CDH23 | 56.7 | 48.3 | 100 | להשלים |
| 9 | M | 20 | L | ידוע | 51.7 | 73.3 | 48.1 | חלקית |
| 10 | M | 64 | R | ידוע | 51.7 | 58.3 | 82.1 | להשלים |
טבלה 1: סיכום מאפייני הנושא ותוצאות שימור השמיעה. טבלה זו אומצה על ידי Yoshimura et al.6.
Discussion
זיהוי האטיולוגיה של HL בהערכה טרום ניתוחית הוא חיוני לחיזוי האודיוגרמה העתידית בכל מקרה. במחקר הקודם שלנו, וריאנטים פתוגניים בגנים CDH23, ACTG1, Mit1555A>G, MYO7A, MYO15A, SLC26A4 ו-TMPRSS3 זוהו לעתים קרובות בחולים עם HL7 בתדירות גבוהה. אצל רוב החולים האלה, השמיעה השיורית התדרדרה בהדרגה (ראו מקרה HL הקשור ל-CDH23 באיור 2). במקרים אלה, המהלך הטבעי של HL נלקח בחשבון בעת בחירת אלקטרודת CI עבור כיסוי שבלול רחב יותר.
קביעת אורך מערך CI דרשה מדידת אורך תעלת השבלול (CDL). כדי להקל על תהליך זה, תוכנת OTOPLAN הוכחה כאפשרית מבחינה קלינית21. בגרסאות מוקדמות יותר, כגון OTOPLAN 3.0, ה-CDL נמדד ידנית כדי לשרטט את הקוטר, הרוחב והגובה של כל שבלול. עם זאת, עם OTOPLAN 4.0, מדידה אוטומטית של CDL התאפשרה, מה שהציע נוחות מוגברת למנתחים ומזער את השונות במדידה. יש לציין כי צילומי CT בעובי פרוסה של 0.6 מ"מ או פחות התאימו לניתוח האוטומטי שסופק על ידי OTOPLAN. לאחר מכן, יש לבחור את אורך מערך CI כדי להשיג את הזווית האופטימלית של עומק החדרה (AID) בכל מקרה.
כדי לבצע ניתוח EAS פחות פולשני, נדרשה מתן לפני, תוך ואחרי סטרואידים כדי למזער את הדלקת החריפה שעלולה להעלות את סף השמיעה22. בעתיד הקרוב, כדי למזער לא רק תגובות חריפות אלא גם כרוניות לאחר ניתוח CI ו- EAS, השימוש באלקטרודות פולטות דקסמתזון יהיה רצוי. בנוסף למתן סטרואידים, אלקטרודות גמישות בדופן הצידית היו חיוניות למזעור הטראומה לשבלול. החדרת אלקטרודות כאלה לשבלול בזהירות ובאיטיות באמצעות גישת החלון העגול הביאה לפולשניות מינימלית. כדי לסייע בכך, ביצוע ניתוח באמצעות אקסוסקופים ואנדוסקופים היה שימושי ליצירת שדה ראייה ברור יותר ולאישור המרכיבים הזעירים של האוזן התיכונה. כדי למנוע גרימת היווצרות נרחבת של רקמת פיברו-אוסאוס בשבלול, יש להימנע מהתקרבות החלון העגול המורחב ומהשבלול23.
EAS עם אלקטרודות ארוכות יותר היה שימושי לא רק כדי להתכונן להידרדרות עתידית של HL, אלא גם להציע שלושה סוגים של אסטרטגיות מפה. אם האלקטרודות שהוחדרו חופפות לאזור השמיעה השיורי, מטופלים עם EAS יכולים להשתמש ב-ES עם או בלי AS: "מפת EAS (חפיפה/ON)" או "מפת ES בלבד". לחלופין, הם יכולים לכבות חלק מאנשי הקשר האפיקליים ולהפעיל את מפת AS: "EAS (חפיפה/כיבוי)". אם השמיעה מתדרדרת, ניתן להפעיל את כל המגעים מאוחר יותר כדי לספק התאמת גובה צליל טובה יותר (איור 3). כל הממצאים הללו מראים כי EAS עם אלקטרודות ארוכות יותר מאפשר למשתמשים למטב מפות לשמיעה טבעית יותר.
כאן, הוכח כי הכנה טרום ניתוחית וטכניקות כירורגיות מתקדמות חיוניות כדי למזער את הטראומה הכירורגית. ביצוע הסדרה הנ"ל של הליכים טרום ותוך ניתוחיים איפשר לחולים להפיק תועלת מ- EAS עם אלקטרודות ארוכות יותר.
מגבלות
למרות ההתקדמות בפרוצדורות הכירורגיות הפחות פולשניות שהוזכרו לעיל, השמיעה השיורית עדיין מתדרדרת במספר מסוים של חולים לאחר CI. ניטור תוך-ניתוחי, כגון מיקרופוניקת שבלול (CM), יהיה אפשרי מבחינה קלינית למדוד נזק לשבלול במהלך החדרת אלקטרודה24. עם זאת, כיצד להעריך EAS עם אלקטרודות ארוכות יותר ומה לעשות במקרה של תגובות CM מסוימות, כגון ירידה באמפליטודה, נותר לא ברור עד כה. נדרשים מחקרים נוספים בתחום זה.
Disclosures
המחברים מצהירים כי אין ניגודי עניינים.
Acknowledgements
מחקר זה מומן על ידי מענק מחקר במדעי הבריאות והעבודה לחקר מחלות נדירות ובלתי פתירות ומחקר מקיף על בריאות ורווחה של מוגבלות ממשרד הבריאות, העבודה והרווחה של יפן (S.U. 20FC1048, 23FC10149) ומענקים בסיוע מהסוכנות היפנית למחקר ופיתוח רפואי (AMED) (S.U. 19ek0109363h0002, 21ek0109542h003).
Materials
| Name | Company | Catalog Number | Comments |
| DEXART 3.3 mg | Fuji Pharma | 22100AMX01404 | equal to dexamethasone sodium phosphate (4 mg) |
| DEXART 6.6 mg | Fuji Pharma | 22100AMX01402 | equal to dexamethasone sodium phosphate (8 mg) |
| Fentanyl injection 0.1 mg | TERUMO | 22100AMX00009 | |
| MAESTRO 7.0 | MED-EL | 4582290238456 | fitting software for map settings |
| Midas Rex MR8 | Medtronic | 301ADBZX00046000 | high speed drill |
| OTOPLAN software | Cascination / MED-EL | REF 20125 | for measuring cochlear duct length (CDL) |
| Predonine tablets | Shionogi | 16000AMZ01740000 | |
| Propofol 1% 50 mL | Maruishi Pharmaceutical Co.,Ltd | 30100AMX00158 | |
| Remifentanil 2 mg | Daiichi-Sankyo | 22800AMX00090 | |
| Rocuronium bromide 50 mg/50 mL | Maruishi Pharmaceutical Co.,Ltd | 22800AMX00534 | |
| SONNET2 EAS | MED-EL | 4582290241807 | processor |
| Synchrony2 FLEX28 | MED-EL | 4571573943026 | cochlear implant (electrode) |
| Xylocaine 0.5% with epinephrine | Sandoz Pharma | 4KUZ13127 |
References
- Von Ilberg, C., et al. Electric-acoustic stimulation of the auditory system. New technology for severe hearing loss. ORL J Otorhinolaryngol Relat Spec. 61 (6), 334-340 (1999).
- Gstoettner, W., et al. A new electrode for residual hearing preservation in cochlear implantation: First clinical results. Acta Otolaryngol. 129 (4), 372-379 (2009).
- Moteki, H., et al. Feasibility of hearing preservation for residual hearing with longer cochlear implant electrodes. Acta Otolaryngol. 138 (12), 1080-1085 (2018).
- Usami, S., et al. Achievement of hearing preservation in the presence of an electrode covering the residual hearing region. Acta Otolaryngol. 131 (4), 405-412 (2011).
- Usami, S., et al. Hearing preservation and clinical outcome of 32 consecutive electric acoustic stimulation (EAS) surgeries. Acta Otolaryngol. 134 (7), 717-727 (2014).
- Yoshimura, H., Moteki, H., Nishio, S. Y., Usami, S. I. Electric-acoustic stimulation with longer electrodes for potential deterioration in low-frequency hearing. Acta Otolaryngol. 140 (8), 632-638 (2020).
- Yoshimura, H., et al. Genetic testing has the potential to impact hearing preservation following cochlear implantation. Acta Otolaryngol. 140 (6), 438-444 (2020).
- Van de Heyning, P. H., et al. Systematic literature review of hearing preservation rates in cochlear implantation associated with medium- and longer-length flexible lateral wall electrode arrays. Front Surg. 9, 893839 (2022).
- Buchman, C. A., et al. Influence of cochlear implant insertion depth on performance: A prospective randomized trial. Otol Neurotol. 35 (10), 1773-1779 (2014).
- Buchner, A., Illg, A., Majdani, O., Lenarz, T. Investigation of the effect of cochlear implant electrode length on speech comprehension in quiet and noise compared with the results with users of electro-acoustic-stimulation, a retrospective analysis. PLoS One. 12 (5), e0174900 (2017).
- Canfarotta, M. W., et al. Long-term influence of electrode array length on speech recognition in cochlear implant users. Laryngoscope. 131 (4), 892-897 (2021).
- Nassiri, A. M., et al. Hearing preservation outcomes using a precurved electrode array inserted with an external sheath. Otol Neurotol. 41 (1), 33-38 (2020).
- O'Connell, B. P., et al. Electrode location and angular insertion depth are predictors of audiologic outcomes in cochlear implantation. Otol Neurotol. 37 (8), 1016-1023 (2016).
- Moteki, H., et al. Long-term results of hearing preservation cochlear implant surgery in patients with residual low frequency hearing. Acta Otolaryngol. 137 (5), 516-521 (2017).
- Von Ilberg, C. A., Baumann, U., Kiefer, J., Tillein, J., Adunka, O. F. Electric-acoustic stimulation of the auditory system: A review of the first decade. Audiol Neurootol. 16, 1-30 (2011).
- Ariyasu, L., Galey, F. R., Hilsinger, R., Byl, F. M. Computer-generated three-dimensional reconstruction of the cochlea. Otolaryngol Head Neck Surg. 100 (2), 87-91 (1989).
- Danielian, A., Ishiyama, G., Lopez, I. A., Ishiyama, A. Morphometric linear and angular measurements of the human cochlea in implant patients using 3-dimensional reconstruction. Hear Res. 386, 107874 (2020).
- Kawano, A., Seldon, H. L., Clark, G. M. Computer-aided three-dimensional reconstruction in human cochlear maps: Measurement of the lengths of organ of Corti, outer wall, inner wall, and Rosenthal's canal. Ann Otol Rhinol Laryngol. 105 (9), 701-709 (1996).
- Rask-Andersen, H., et al. Human cochlea: Anatomical characteristics and their relevance for cochlear implantation. Anat Rec (Hoboken). 295 (11), 1791-1811 (2012).
- Skarzynski, H., et al. Towards a consensus on a hearing preservation classification system. Acta Otolaryngol Suppl. 564, 3-13 (2013).
- Yoshimura, H., Watanabe, K., Nishio, S. Y., Takumi, Y., Usami, S. I. Determining optimal cochlear implant electrode array with OTOPLAN. Acta Otolaryngol. 143 (9), 748-752 (2023).
- Skarzynska, M. B., et al. Preservation of hearing following cochlear implantation using different steroid therapy regimens: a prospective clinical study. Med Sci Monit. 24, 2437-2445 (2018).
- Geerardyn, A., et al. Human histology after structure preservation cochlear implantation via round window insertion. Laryngoscope. 134 (2), 945-953 (2023).
- Campbell, L., et al. Intraoperative real-time cochlear response telemetry predicts hearing preservation in cochlear implantation. Otol Neurotol. 37 (4), 332-338 (2016).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved