Method Article
用于多模式单颗粒电感耦合等离子体质谱分析和验证的多功能双入口进样系统
摘要
在这里,我们提供了一种使用双入口系统进行单颗粒电感耦合质谱分析的方案,该系统允许进行标准的独立纳米颗粒表征。
摘要
使用仪器的单粒子模式 (spICP-MS),可以使用电感耦合等离子体质谱仪 (ICP-MS) 对含金属纳米颗粒 (NP) 的大小和数量浓度进行表征。测量的准确性取决于仪器的设置、作条件和用户设置的特定参数。ICP-MS 的传输效率对于 NP 的定量至关重要,通常需要具有均匀粒度分布和已知粒数浓度的参考材料。
目前,NP 参考材料仅适用于少数金属且尺寸有限。如果在没有参考标准品的情况下对颗粒进行表征,则粒径和颗粒数的结果都可能存在偏差。因此,开发了一种使用 spICP-MS 表征纳米颗粒的双入口设置来克服这个问题。该设置基于传统的引入系统,该系统由用于纳米颗粒溶液的气动雾化器 (PN) 和用于离子校准溶液的微滴发生器 (μDG) 组成。开发了一种新的灵活接口,以促进 μDG、PN 和 ICP-MS 系统的耦合。该接口由可用的实验室组件组成,允许在 ICP-MS 仪器仍在运行时进行校准、纳米颗粒 (NP) 表征和清洁装置。
有三种独立的分析模式可用于测定颗粒粒径和粒数浓度。每种模式都基于不同的校准原理。虽然模式I(计数)和模式III (μDG)从文献中已知,但模式II(灵敏度)仅用于确定无机离子标准溶液的传输效率。它独立于 NP 标准品。此处描述的基于 μDG 的进样口系统保证了卓越的分析物灵敏度,因此降低了检测限 (LOD)。对于所研究的所有 NP(Au、Ag、CeO2),所获得的尺寸依赖性 LOD 小于 15 nm。
引言
电感耦合等离子体质谱仪广泛用于定量各种样品和基质中 NP 的大小和数量,即所谓的单颗粒模式 1,2,3。单粒子模式是数据采集系统的一种作,积分或停留时间短。如果使用 NP 悬浮液的适当稀释以避免双重事件,则测量的每个 NP 都会在此时间间隔内产生一个积分信号(事件以每秒计数为单位:cps)。校准标准品和样品通常通过基于气动雾化 (PN) 的常规进样系统引入 ICP-MS 4。但是,作为先决条件,必须确定进样流速和传输效率 (η),以准确量化每 NP 的金属质量并确定它们在悬浮液中的数量浓度。传输效率描述了进样的质量数或颗粒数与 ICP-MS5 检测到的质量数(废液收集法)或颗粒数(计数法)的比值。运输效率最常使用基于纳米颗粒的参考物质来确定5。然而,传输特性取决于 NP 的结构,涉及成分和样品分散剂等特性。其他影响因素是仪器参数,如样品提升速率、雾化器气体流速、停留时间和总测量时间。
由于只有有限的纳米颗粒参考材料可用,因此由于参考颗粒和样品颗粒之间的元素组成存在差异,因此获得的 NP 分析结果可能会产生偏差。除了参考物质范围有限之外,每个探测器停留时间检测多个粒子事件也是一个进一步的挑战。这也可能会影响要确定的运输效率的准确性。
为了独立于参考材料,理想情况下,最好使用运输效率接近 100% 的样品引入系统。同时,与传统的引入系统相比,当使用低体积时,可以使用更高的颗粒数浓度。即使两个颗粒彼此靠近,也可以使用基于 μDG 的系统分别检测这两个颗粒。
μDG 能够生成 pL 范围内具有固定体积的单分散液滴,非常适合此目的 6,7,8,9。μDG 有助于将不同溶剂中的离子和颗粒样品注入 ICP-MS。对于离子金属样品,假设生成的液滴在到达 ICP 的途中已完全脱溶剂。因此,液滴失去了所有水分,并从剩余的盐中形成颗粒。该颗粒的直径与所使用的浓度成正比。因此,可以在内部生产相同基质、质量和大小的自制参比标准品,以及不同浓度的待研究 NP 离子溶液。液滴的体积可以根据 μDG 测量的液滴直径轻松计算。这对于产生不同直径10,11 的广泛液滴分布的 PN 来说是不可能的。由于在 100% μDG 的高传输效率下均匀进样,因此可以实现高仪器特异性分析物灵敏度。根据所使用的基质,与基于 PN12 的传统引入系统的结果相比,这会导致颗粒质量和尺寸的检测限 (LOD) 更低。然而,由于 μDG 的设计,当 ICP-MS 系统仍在运行时,无法轻松更换样品。在测量不同样品之间,必须清洁 μDG,然后用样品溶液冲洗以确保系统稳定。此外,它对重基质样品的耐受性尚未得到很大程度的测试。此外,由于流速极低,获得良好统计数据的分析时间将非常长,这限制了其实际应用,如果应该分析“真实”样品,例如环境水域。
为了克服这些限制,μDG 以前曾与基于传统气动雾化器的系统结合使用,该系统被命名为双入口系统13。通过气动雾化器将带有 μDG 和 NP 悬浮液的校准标准品引入 ICP-MS 中,Ramkorun-Schmidt 等人能够利用这两个系统13。实现了 Au 和 Ag NP 金属质量分数的高精度测定,无需测定运输效率。然而,使用这种双进样口系统无法确定颗粒数量浓度。此外,μDG 系统的清洁和校准也使常规分析的适用性变得复杂。
在本文中,我们提出了一种灵活的双入口接口,用于确定 NP 粒径和颗粒数浓度,并演示了它的组装和实际应用。与 Ramkorun-Schmidt 等人的系统一样,它由 μDG 和 PN 样品引入系统组成。我们证明,在目前的开发阶段,双入口系统允许应用三种独立的分析模式来研究和表征含金属的 NP。我们的双进样口系统简化了 NP 测定的校准程序,并提高了分析品质因数,特别是准确度14。即使 ICP-MS 仍在运行时,进样口系统也可以方便地更换样品和清洁 μDG,从而减少整体分析时间和错位风险。为了测试系统性能,使用经过充分表征的参比 NP(60 nm AuNP – NIST 8013、75 nm AgNP – NIST 8017)进行方法验证和可比性。
研究方案
1. 组装双进样口进样装置
注意: 有关不同部件的详细信息如 表 1 所示。
| 组件 | |||
| 第 1 部分 | 玻璃内螺纹球形接头,柄长约 10 mm | ||
| 玻璃外螺纹球形接头,柄长约 10 mm | |||
| 金属 T 形件(尺寸:1/4 英寸) | |||
| 玻璃-金属胶粘剂 | |||
| 两个用于球形玻璃接头的夹具 | |||
| 第 2 部分 | ICP-MS 雾化室(推荐类型:冲击珠雾化室、旋流雾化室或类似产品) | ||
| 气动雾化器(推荐类型:同心雾化器) | |||
| 钳 | |||
| 第 3 部分 | 无 O 形圈的石英炬管 | ||
| 气体管路连接器闭端 | |||
| 气体管路连接器 开口端 | |||
| 导电和柔性硅胶管 | |||
| 第 4 部分 | 压电式微型液滴发生装置 | ||
| 第 5 部分 | 微液滴控制单元 | ||
表 1:用于构建双入口设置的组件列表。
- T 形连接器单元的结构(图 1 第 1 部分)。
注:这部分连接传统的样品引入系统(步骤 1.2)和 μDG 运输单元(步骤 1.3)。- 将公头和母头球形接头插入 T 形接头的相对开口。
- 使用玻璃与金属的粘合剂(例如硅胶)固定公球接头和母球接头。
- 使用夹具将内螺纹球形接头连接到 ICP-MS 的进样器。
- 连接常规进样系统(图 1 第 2 部分)
注意: 此部件连接到 T 形连接器单元(步骤 1.1)- 将 ICP-MS 雾化室与气动雾化器 (PN) 相结合,使其适合所使用的雾化室。
- 使用夹子将雾化室出口连接到 T 形接头的外螺纹球形接头(如步骤 1.1 中所述)。
注意:雾化室出口通常配有一个内螺纹球形接头连接器。 图 1 所示的组合由雾化器和冲击珠雾化室组成。可以使用其他运输效率在 2% 至 10% 或更高的雾化室来代替冲击珠雾化室。
- 微滴传输单元的结构(图 1 第 3 部分)
注意:此部件连接 T 形连接器单元(步骤 1.1)和 μDG 单元(步骤 1.4)。- 使用适当的夹具将可拆卸的石英炬管(去除中心管)连接到实验室支架上,炬管入口位于顶部。
- 通过封闭端气体连接器堵塞炬管等离子体/辅助气体入口。
注:使用蠕动泵将样品输送到雾化器。氩气用于样品雾化到雾化室中,并进一步输送到等离子体中。 - 使用合适的气体连接器,通过冷却气体入口将氦气管线连接到炬管。
注:施加的氦气用于对生成的液滴进行脱溶剂气,并充当鞘气,防止液滴与装置壁碰撞,并防止 ICP-MS 仪器在必须拆下 μDG 的样品入口头进行清洁和样品更换时插入大气中的氧气。 - 使用适配器将一根 30 cm 长的导电柔性硅胶管(内径 0.75 cm)连接到手电筒的出口端(手电筒底部)。
- 通过将柔性硅胶管拉伸到其剩余的垂直金属连接上,将硅胶管的下端连接到 T 形件连接器单元。
注:柔性硅胶管允许使用连接的设置对 ICP-MS 仪器进行 x-y-z 调谐。
- 微液滴发生单元和微液滴发生控制单元的连接(图 1 第 4 部分、第 5 部分)
注意:此部件连接到 μDG 运输单元(步骤 1.3)- 将 μDG 头插入炬管的样品入口端,将准备好的 μDG 单元连接到微滴传输单元。
- 将电源连接到 μDG 控制单元。
注:此处描述的设置包括市售的 μDG 头和 μDG 电源。根据所使用的 μDG 头,必须相应地调整设置。
2. 液滴大小的定量
- 使用频闪仪灯和 CCD 相机(例如,在开放式配置中,参见 图 1 尺寸测量配置)拍摄 μDG 产生的液滴的图像。
- 通过拍摄 μm 范围内已知大小的物体(例如,直径为 150 μm 的铜线)的图像来校准 CCD 相机。
- 以用于实验的设置拍摄至少 1, 000 滴的图像(见 表 2)。
- 使用适当的图形软件程序(参见 材料表)在以下步骤中评估有关物体和液滴大小的图像:
- 单击 File 和 Open 以加载对象的图像。
- 点击 图片 |Adjust |阈值 通过移动滚动条来定义对象的区域。
- 单击 Apply 以应用设置。
- 单击 Straight segment 按钮。
- 单击并按住鼠标左键可在对象旁边绘制一条线。
- 按 Ctrl + M 测量对象大小。
- 测量物体在 5 个不同点的直径。
- 将 “Results” 表格复制并 粘贴到 电子表格软件中。
- 计算 “Length” 列的算术平均值。
- 计算像素长宽比 (PAR):实际物体大小 (μm)/图像中的平均物体大小 (px)。
- 单击 File (文件) |导入 |Image Sequence 导入和加载 Droplet 的图像。
- 单击 矩形 并标记第一个图像的液滴。
- 右键单击鼠标垫,然后选择 Duplicate (复制) 以将图像序列的液滴与图像的其余部分分开。
- 按照步骤 2.4.2 中的指定将水滴与背景分离。
- 单击 Process |二进制 |“Erode”(侵蚀 )可移除水滴表面上的光反射。
- 单击 Process |二进制 |扩张 以反转 “Erode” 步骤。
- 单击 Analyze |分析粒子 |确定 测量所有液滴。
- 将 “Summary” 或 “Result” 表格复制并 粘贴到 电子表格软件中。
- 计算雪貂直径的算术平均值(以 px 为单位)。
- 使用 PAR 转换以 μm 为单位的直径:以 px/PAR 为单位的雪貂直径。
注:μDG 形成的液滴的大小取决于施加到压电陶瓷元件7 的电流脉冲的选定长度和持续时间。
3. 样品制备
- 制备待测分析物的离子校准溶液,浓度范围为 0.2 至 20 μg/L 的稀酸(例如 HCl (0.5 v/v)、HNO3 (3.5 v/v))。
- 在稀酸中制备浓度范围为 1 至 10 μg/L 的离子溶液,用于单点校准。
- 根据制造商的说明或内部方案制备 NP 标准悬浮液。
注:步骤 3.3.1 – 3.3.4 以 Ag、Au、CeO2 NP 为例,解释了 NP 标准悬浮液的制备。- 为 PN 制备 10 mL 的 0.05 μg/L AuNP 溶液,在 μDG 的超纯水中制备 1 μg/L AuNP 溶液。使用前涡旋 20-60 秒。
- 为 μDG 制备 0.05 μg/L AgNP PN 溶液和 2 μg/L AgNP 溶液,均在超纯水中制备。使用15 号前摇匀 20-60 秒。
- 如前所述制备用于金属氧化物16,17 的 CeO2 NP 溶液。
- 为 PN 制备 0.05 μg/L CeO2 NP 溶液,为 μDG 制备 1 μg/L 溶液。
- 在总共 15 mL – 20 mL 的玻璃容器中称取 25.6 mg/mL CeO2 NP,并加入 10 mL 用超纯水中制备的 0.05 (v/v) BSA 溶液。
- 使用功率为 7.35 W 的指尖超声仪将颗粒溶液均质化 309 秒。
4. 乐器调音和参数
- 确保 MDG 发生器已关闭,并将步骤 1 中内置的双入口进样装置与带夹子的 ICP-MS 仪器进样器连接。用雾化器气体 (Ar) 和液滴输送气体 (He) 冲洗入口系统 5 – 10 分钟。
注:ICP-MS 仪器必须受到保护,防止高浓度氧气渗入等离子室。 - 关闭液滴输送气体 (He) 并启动 ICP-MS 系统
- 使用 ICP-MS 系统制造商指定的仪器标准调谐溶液,在想要使用的测量模式下调谐仪器。
注:标准调谐溶液包括钡、铈、铟、铀、铋、铋、钴、锂(均为 1 μg/L)在 2.5% (v/v) 硝酸和 0.5% (v/v) 盐酸的混合物中。 - 测定 PN 的样品摄取率。
- 在容器中装满 15 mL 水。
- 称量容器。
- 将容器连接到 PN 的管道。
- 单击仪器软件中的蠕动泵启动按钮,启动蠕动泵。
- 启动 5 分钟计时器。
- 5 分钟后从容器中取出提升线。再次称量容器。
- 使用以下公式计算样品摄取速率 (mL/min):之前的容器重量 - 之后的容器重量/持续时间。
- 必要时优化仪器参数以提高分析物灵敏度,例如雾化器气体流速、采样深度、等离子体功率。
注:参见 表 2 作为可在 ICP-MS 系统中优化的仪器参数示例。 - 调整 He 气体流量,直到可以检测到恒定的信号速率作为液滴形成速率的函数。
| 参数 | 价值 | ||
| ICP – MS: | |||
| 等离子功率 (W) | 1600 | ||
| 采样深度 (mm) | 4 | ||
| 流速 (L min-1): | |||
| 辅助气体 | 0.65 | ||
| 冷却气体 | 14 | ||
| 时间 (s) | |||
| 数据采集 (s) | 1200 | ||
| 停留时间 (s) | 0.01 | ||
| 接口: | |||
| PN 样品摄取率 (mL min-1) | 0.21 | ||
| 雾化器气体 (L min-1) | 0.92 | ||
| 微DG: | |||
| 毛细管直径 (μm) | 75 | ||
| 掉落率 (Hz) | 10 | ||
| He 补气 (L min-1) | 0.27 | ||
| 作模式 | 三脉冲 | ||
| 第 1 集 | 第 2 集 | 第 3 集 | |
| 电压 (V) | 53 | 51 | 47 |
| 脉冲宽度 (μs) | 20 | 25 | 12 |
| 脉冲延迟 (μs) | 4 | 2 | 1 |
表 2:使用的仪器参数值。
5. 纳米颗粒样品的多模式测量
- 准备 μDG 控制单元
- 打开 μDG 控制单元的电源开关。
- 单击第一个屏幕上的 Start 以启动控制单元。
- 单击 Global Settings 选择要使用的脉冲模式。
- 在脉冲模式下单击右侧图形按钮以选择三脉冲模式。
注意: 表 2 给出了三脉冲模式的设置。
- 准备 μDG 单元
- 单击 On/Off 启动 μDG。
- 将要测量的样品溶液填充样品容器。
- 将样品容器连接到 μDG 装置。
- 使用 10 mL 注射器吹扫通过容器和 μDG 装置的空气。
- 将注射器连接到样品容器上的注射器端口。
- 推动注射器柱塞,直到观察到恒定的液体流出 μDG 头。
- 保持压力 10 秒。
- 取出注射器。
- 将 μDG 单元放入 CCD 相机的聚焦区域,以观察形成的液滴。
- 将 CCD 相机连接到 PC 或笔记本电脑。
- 启动 CCD 相机软件以观察形成的液滴
- 单击 “开始 ”以获取快捷批处理的实时视图。
- 观察恒定的液滴形成。
- 将 μDG 头放在双入口进样系统上的倒置炬管上。
- 通过测量重复的多点校准来验证每个感兴趣元素的 μDG 单元和 PN。
注:对于 ICP-MS 数据采集,请使用与仪器关联的软件。 - 通过将实验数据导入电子表格软件来确定多点校准的线性范围。
- 计算每个校准点的算术平均值。
- 确定截距、斜率和相关系数。
注:对于 sp-ICP-MS,相关系数应为 >0.9918。
- 在校准曲线的线性范围内选择浓度,以便稍后进行单点校准。
- 按照以下步骤进行多模式纳米材料定量的测量和验证(通过使用 NIST 8012、NIST 8013 或 NIST 8017 等参考材料或类似材料)(图 2)。
- 根据目标分析物选择纳米颗粒和离子标准品。
- 根据 5.2 用离子标准溶液制备 μDG 单元。
- 通过 PN 添加稀酸溶液(例如,0.5% v/v HCl)。
- 在时间分辨模式下开始 ICP-MS 系统的测量。
- 120 秒后单击开 /关 以停止 μDG 并将 PN 处的稀酸溶液与离子标准品交换。
- 330 秒后,再次将 PN 处的离子标准品与稀酸溶液交换。
- 同时,从设置中删除 μDG 单元。
- 将 μDG 装置的样品容器(玻璃瓶)更换为含有稀酸溶液(例如 3.5% HNO3)的容器,以清洁 μDG 装置。
- 向 10 mL 注射器中注入空气。
- 将注射器连接到 μDG 装置的注射口并清空注射器,直到 μDG 头出现液体射流,并保持压力 30 秒。
- 按照步骤 5.2 中指定的 NP 样品准备 μDG,并在 510 秒时将 μDG 单元连接回设置中。
- 810 秒后单击 On/Off 以停止 μDG。
- 将 PN 处的稀酸溶液与 NP 样品交换,再测量 300 秒。
- 大约 1,200 秒后停止测量。
- 按照步骤 5.5.8 中的指定清洁 μDG 单元。
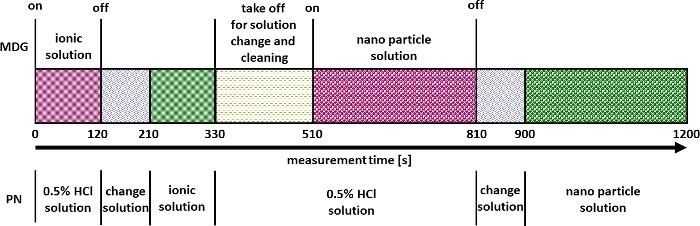
图 2:多模式纳米材料定量的测量策略。请单击此处查看此图的较大版本。
6. 数据分析
注意:为了简化所有计算步骤,准备了相应的电子表格(参见 补充文件)。
- 使用可以处理数据帧的电子表格或软件来处理数据并导入测量数据。将电子表格软件中整个测量的强度值(包含在电子补充中)粘贴到 A 列中,数据将被可视化。在“输入参数”表中输入所有必要的计算实验参数。
- 通过选择合适的电子表格单元格,定义 μDG 离子 (I)、PN 离子 (II)、μDG NP (III) 和 PN NP (IV) 的目标区域 (ROI)。使用准备好的工作表中的图表定义 ROI 的边界,并将值输入到“感兴趣区域的确定”表(单元格 C1:E7)中。
- 将每个数据集复制并粘贴到单独的列中。在准备好的工作表中按下按钮 Copy ROI(复制 ROI ),将测量拆分为四个 ROI(M:P 列)。
- 计算 I 和 II 的算术平均值。
- 应用迭代方法分离 III 和 IV 的颗粒或液滴信号和背景。
- 计算所有测量值的算术平均值和标准差。
- 通过平均值 + 5 * 标准差计算极限或临界值。
- 通过对已识别的粒子信号使用 Cut 命令,删除所有小于 III 和 IV 限值的信号。使用 Paste 将它们粘贴到单独的列中。
- 重复步骤 1-3,直到平均值和标准差保持不变。
注意:在准备好的纸张的 Q 到 BD 列中,分离背景和粒子信号的迭代方法执行了五次。
- 计算 III 和 IV 的已识别粒子信号的算术平均值。
- 通过使用分析物的仪器检测限(LOD - 计数)、分析物灵敏度(SC,离子 - 计数/(μg/L))、样品吸收速率(qs - mL/min)、运输效率(η - 相对单位)和散装材料密度(ρ - g/cm³),计算μDG NP和PN NP的最小可检测粒径(LOD大小 - nm):
- 根据应用的三种分析模式,计算 μDG NP 和 PN NP 的已鉴定粒子信号的质量 (ma,p) 和粒径 (d - nm,假设颗粒是球形的),同时考虑标准溶液的离子金属浓度 (ca - μg/L) 和等离子体中的离子通量 (计数/s):
- 质量:

- 大小:

- 质量:
- 使用检测到的颗粒数量 (qp)、样品的颗粒浓度 (cp,已使用 - 1/mL)、PN 和 MDG 的分析物灵敏度(Sm,离子,PN、Sm,离子、MDG – 计数/(μg/L))、液滴体积(V滴 – pL])计算分析模式的比传输效率, 停留时间 (td – ms)、PN 的传输效率 (ηPN)、μDG 的传输效率 (ημDG)、由 PN 和 μDG 测量的离子溶液强度(I离子、PN、I离子、μDG – 计数)以及用于两种进样系统的离子溶液浓度(c离子、PN、 c离子,μDG - μg/L):
- 模式一:

- 模式 II:

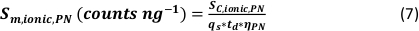

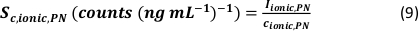
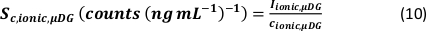
- 模式一:
- 假设 μDG 的传输效率等于 1:19
- 通过考虑测量过程中的进样体积(V 进样)来计算分析的 NP 溶液的颗粒数浓度:
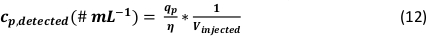
注意:在准备好的工作表中,所有计算都在拆分后自动执行。结果显示在表“输出参数”(单元格 BH7:BR35)中,并包含上述公式,包括各个计算步骤。
结果

图 3:使用 CCD 相机测定液滴大小。 使用 150 μm 铜线校准 CCD 相机 (A),并将获得的液滴图片转换为二进制彩色图片后测定液滴大小 (B)。 请单击此处查看此图的较大版本。
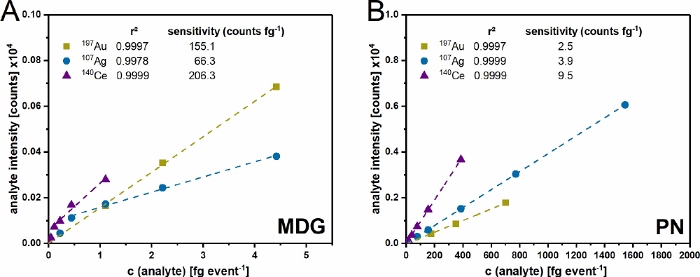
图 4:双进样口设置的验证。 对金 (Au)、银 (Ag) 和铈 (Ce) 的 μDG (A) 和 PN (B) 进样口系统进行多点校准。根据每个检测到事件的所用实验条件质量数,换算 0.2 – 20 μg mL-1 范围内的使用浓度。显示的数据是三个独立仿行的平均值。 请单击此处查看此图的较大版本。
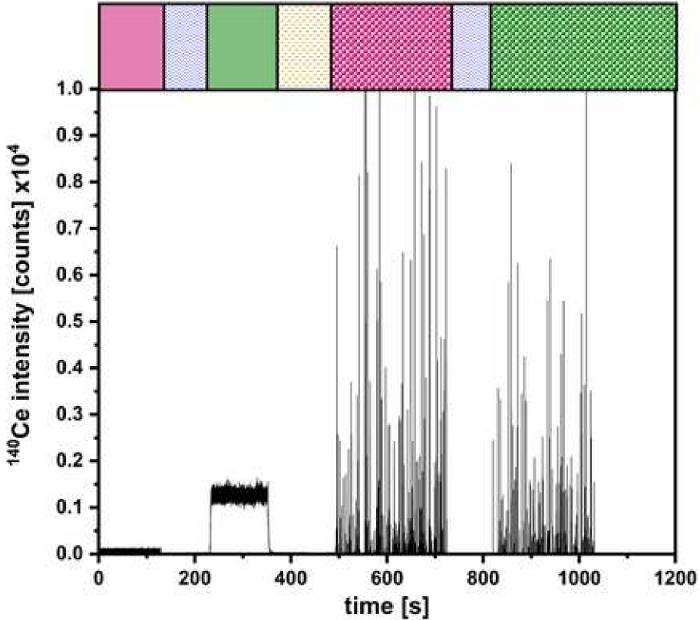
图 5:表示双入口设置的测量值。 如图 2 中所示,针对不同的进样步骤对 CeO2 NP 进行定量分析。请单击此处查看此图的较大版本。
| 样本 | 分析模式 / | NP 样品进样口 | 校准标准液进样口 | η | 米A, P | NP 尺寸 (d) | #NPs | 收入 (%) | |
| ηPN 测定 | (%) | (FG) | (纳米) | (毫升-1 x103) | |||||
| 金 56 nm | 模式-I / | PN | PN:Au离子和AuNP标准品 | 1.8 (0.1) | 1.9 (0.5) | 57.2 (4.3) | 28.1 (0) | 100 | |
| 美国国家标准研究院 (NIST 8013) | 计数方法 | ||||||||
| 模式 II / | PN | PN/μDG (注: | 1.9 (0.1) | 2 (0.4) | 58 (3.6) | 25.6 (1.6) | 91 | ||
| 灵敏度比 | 金离子标准品 | ||||||||
| 模式-III / | 微DG | 微DG: | 100 | 1.7 (0.2) | 55 (2.4) | 394.4 (29.3) | 70 | ||
| ημDG = 1 | Au 离子标准品 | ||||||||
| 预期尺寸 (nm) | 56.0 (0.5) | ||||||||
| 银 75 纳米 | 模式-I / | PN | PN:Ag离子和AgNP标准品 | 2.3 (0.2) | 1.9 (0.2) | 70.2 (2.3) | 21.6 (0) | 100 | |
| 美国国家标准研究院 (NIST 8017) | 计数方法 | ||||||||
| 模式 II / | PN | PN/μDG (注: | 2.5 (0.2) | 2 (0.2) | 71.5 (2.1) | 20.5 (1.9) | 95 | ||
| 灵敏度比 | Ag 离子标准品 | ||||||||
| 模式-III / | 微DG | 微DG: | 100 | 2.5 (0.2) | 76.7 (2.3) | 757.1 (68.7) | 88 | ||
| ημDG = 1 | Ag 离子标准品 | ||||||||
| 预期尺寸 (nm) | 74.6 (3.8) | ||||||||
| 二氧化硫 JRC NM212 | 模式-I / | PN | PN:Ce离子和AuNP标准 | 1.7 (0) | 0.90 (0.09) | 61.9 (2.0) | 7.59 (0.32) | - | |
| 10-100 纳米 | 计数方法 | ||||||||
| 模式 II / | PN | PN/μDG (注: | 4.9 (1.4) | 1.36 (0.35) | 70.6 (5.9) | 5.42 (1.7) | - | ||
| 灵敏度比 | Ce 离子标准品 | ||||||||
| 模式-III / | 微DG | 微DG: | 100 | 1.63 (0.62) | 74.4 (9.2) | 590 (168) | - | ||
| ημDG = 1 | Ce 离子标准品 | ||||||||
表 3:双入口设置的结果。 使用三种分析模式和三种运输效率测定方法,对 Au NIST 8013、Ag NIST 8017 和 CeO2 JRC NM 212 (n=3) NP 材料的运输效率、金属质量分数、直径和 NP 数浓度进行分析。回收率定义为确定 #NPs 与预期 #NPs 的比率。该表经参考文献14 许可转载。
此处介绍的方案允许测定颗粒质量和数量浓度。预先表征了 μDG 液滴的形成,包括液滴大小(图 3)(表 3)。
组装设置(图 1)并确定液滴大小后,使用离子标准品(图 4)验证两种进样系统。对于所有研究的元素,两种注射系统都可以实现 r² > 0.99 的精度。但是,由于引入和运输的分析物数量不同,两种系统存在差异。由于 μDG 具有非常高的传输效率(高达 100%),因此与 PN 相比,在低质量输入下观察到更高的分析物灵敏度。但是,μDG 引入的测量浓度必须分为两个线性范围。对于 Ag,第一个线性范围可以在 0 到 0.5 fg 事件-1 之间观察到,第二个线性范围在 0.5 和 fg 事件-1 之间。相比之下,Ce 的第一个线性范围介于 0 和 0.25 fg 事件-1 之间,第二个线性范围介于 0.25 和 3 fg 事件-1 之间。测量浓度的 PN 线性范围似乎更高。这很可能与每个检测事件引入 ICP-MS 的质量数的差异有关。与使用 PN 引入样品相比,μDG 每次液滴和检测事件以低体积进样恒定的绝对量,导致检测质量较低。
验证成功后,可以如图 2 所示进行实验。 图 5 举例说明了此类实验的结果,用于测定 CeO2 NP 的粒径和数量浓度。在这里,可以识别通过 μDG 和 PN 引入的离子和 NP 溶液的信号。对所有研究的颗粒进行了三重测定。
如上所述对所获得的数据进行评估,并在 表 3 中进行了总结。对于用于验证双入口设置和三种分析模式的 Au 和 Ag NP,在执行所有分析模式时都可以获得认证的粒径和数量浓度。CeO2 获得的平均粒径在 10 到 100 nm 之间,这是制造商指定的范围。
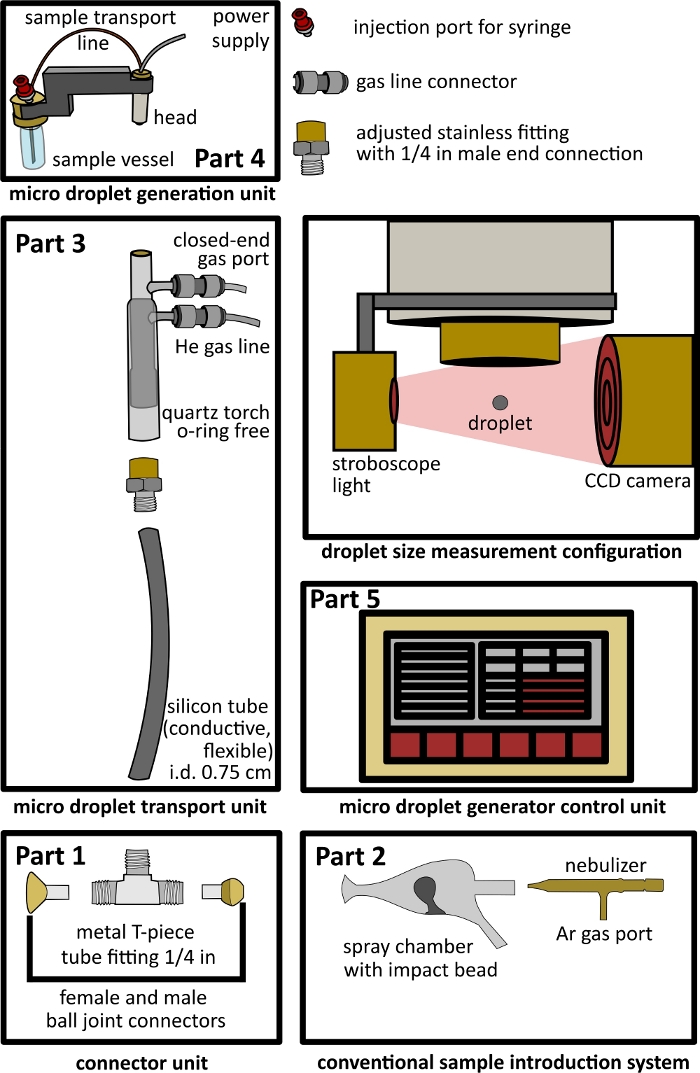
图 1:双入口接口设置的设计。 第 1 部分 - 连接器单元,第 2 部分 - 常规引入系统,第 3 部分 - 微液滴传输单元,第 4 部分 - 微液滴发生单元,第 5 部分 - 微液滴控制单元,以及用于液滴尺寸测量的开放式配置,包括频闪灯和 CCD 相机。 请单击此处查看此图的较大版本。
讨论
开发的双进样口设置的目的是使用不同的分析模式,独立于待研究的分析物,尽可能准确地表征和定量 NP 的大小和数量浓度。通过将低体积 (pL) 和高质量传输(高达 100%)引入系统 (μDG) 与传统引入系统 (PN) 相结合,这是可以实现的。通过使用本研究中介绍的设置,可以基于离子标准品确定定量颗粒质量所需的基于元素的特定传输效率,而不受 NP 参考物质的影响。此外,与 μDG 一起引入 ICP-MS 的 NP 具有较窄的 (AuNP) 或类似的 (AgNP) 粒径分布。否则,对于 CeO2 ,观察到 μDG 的尺寸分布更广,这可归因于分析样品的较高多分散性。由于引入了低体积,可以彼此单独检测两个 NP,否则在常规设置中会解释为一个 NP14。
μDG 运输单元的优势在于柔性硅管具有高度的灵活性,这简化了设置的对准。带中心管的炬管也可以在设置过程中进行调整,同时仍连接到 ICP-MS。额外的 He 气流可防止 μDG 头形成的液滴与管壁20 发生碰撞。此外,He 气体允许在样品更换过程中去除 μDG 头,即使 ICP-MS 仍在运行。保持 ICP 处于运行状态对于稳定和稳健的测量至关重要。由于每个新样品或标准品都必须清洁和冲洗 μDG 头,因此 He 流对于本研究中介绍的进样口系统的运行至关重要。此外,双入口装置的所有部分都必须正确连接,以防止氧气渗透到系统中。为了减少所提出的设置中的氧气,在等离子体点燃之前,用雾化器和液滴输送气体冲洗系统至少 5 到 10 分钟。
当形成的液滴到达连接器单元时,它们通过雾化液体流(也称为湿等离子体条件)输送到等离子体中。与使用干等离子体条件相比,这会导致等离子体的液体含量增加。因此,信号强度降低,信号波动增加,即平均测量信号的标准偏差较高13。但是,通过使用 μDG 和浓度,可以检测到高于背景 0.2 μg/L 的信号。每个液滴的相应进样质量具有较低的金属含量,接近某些元素(即 Au、Ag、Ce)的检测限。如果沿此限值使用不同的校准浓度,则可以观察到两个线性区域,Ce和Ag的重叠浓度分别约为0.05 μg/L和2 μg/L。在重叠区域以下,观察到的信号接近元素特异性背景21。超过这些限制,可以确定 μDG 的线性工作范围。即使能够测量低浓度,如果离子和NP同时存在,也无法区分液滴中相同分析物的离子和NP。否则,通过使用传统的引入系统,可以确定平均离子背景并从所有信号中减去,以仅得到粒子信号。
基于 MDG 的系统也有几个限制,可以通过应用拟议的双入口系统来部分避免。但是,如果 μDG 的液滴频率超过 50 Hz,则无法创建一致的液滴模式。形成的液滴可能会碰撞,因此会发生分析物交换。正确调整气体流速对于液滴可靠地输送到 ICP-MS 系统以及 PN 的正确作也很重要。拟议的双进样口系统目前不支持测量程序的自动化,因为需要手动更改样品溶液。
未来,μDG 可用于表征和定量复杂基质和环境样品中的 NP。为了防止 μDG 因较高的溶液粘度、复杂性和表面张力而堵塞,应使用适当的头部设计。根据 μDG 头的设计和电源的作,可能会生成包含颗粒状系统(如细胞、胶束或脂质载体)的液滴,而这些系统根本没有标准参考材料。
披露声明
所有作者均声明无利益冲突。
致谢
这项工作得到了 FLK 和 PR 的 BfR SFP 1322-642、DR 的 BfR SFP 1322-724 和 START 的 BfR 高级科学家奖学金的支持。
材料
| Name | Company | Catalog Number | Comments |
| Au ionic (1000 mg L-1 stock) | VWR, UK | 85550.18E | |
| Ag ionic (1000 mg L-1 stock) | Ultra Scientific, RI, USA | ICM-103 | |
| Ag NP (75nm, NIST 8017) | NIST, Gaithersburg, MD, USA | no longer available | |
| Au NP (60nm, NIST 8013) | NIST, Gaithersburg, MD, USA | no longer available | |
| Ce ionic (1000 mg L-1 stock) | VWR, UK | 85557.18E | |
| CeO2 (10-100nm, NM212) | EU Joint Research Centre | NM212 | |
| Excel 2016 | Microsoft | ||
| Fiji | ImageJ | ||
| Glass female spherical ball + Glass male ball | Fisher Scientific | 12499016 | |
| HCl (emprove bio) | Merck, Germany | 100317 | |
| ICP-MS spray chamber with ipact bead | LabKings | LK6-45013 (OEM 3600170) | |
| Metal clamps for spherical glass joint | Fisher Scientific | 11322015 | |
| Metal T-Piece | Swagelok | SS-4-VCR-T | |
| Microdrop Dispenser Head, non heated | microdrop Technologies | 944 | |
| Microdrop Dispensing System MD-E-3000 | microdrop Technologies | ||
| MilliQ water (MilliPore gradient) | Merck MilliPore, Darmstadt, Germany | ||
| O-ring free quartz torch | Analytical West | 450-301 | |
| PFA-ST concentric nebulizer | Elemental Scientific | ES-2042 | |
| Silicone Rubber Tubing - 60° Shore - Platinum Cured - Black | Silex | ||
| XIMEA Cam Tool | XIMEA |
参考文献
- Linsinger, T. P. J., Peters, R., Weigel, S. International interlaboratory study for sizing and quantification of Ag nanoparticles in food simulants by single-particle ICPMS. Analytical and Bioanalytical Chemistry. 406 (16), 3835-3843 (2014).
- Krystek, P., et al. Method development and inter-laboratory comparison about the determination of titanium from titanium dioxide nanoparticles in tissues by inductively coupled plasma mass spectrometry. Analytical and Bioanalytical Chemistry. 406 (16), 3853-3861 (2014).
- Degueldre, C., Favarger, P. Y., Bitea, C. Zirconia colloid analysis by single particle inductively coupled plasma-mass spectrometry. Analytica Chimica Acta. 518 (1-2), 137-142 (2004).
- Degueldre, C., Favarger, P. Y. Colloid analysis by single particle inductively coupled plasma-mass spectroscopy: a feasibility study. Colloid Surface A. 217 (1-3), 137-142 (2003).
- Pace, H. E., et al. Determining transport efficiency for the purpose of counting and sizing nanoparticles via single particle inductively coupled plasma mass spectrometry. Analytical Chemistry. 83 (24), 9361-9369 (2011).
- Verboket, P. E., Borovinskaya, O., Meyer, N., Gunther, D., Dittrich, P. S. A new microfluidics-based droplet dispenser for ICPMS. Analytical Chemistry. 86 (12), 6012-6018 (2014).
- Shigeta, K., et al. Application of a micro-droplet generator for an ICP-sector field mass spectrometer - optimization and analytical characterization. Journal of Analytical Atomic Spectrometry. 28 (5), 646-656 (2013).
- Gschwind, S., Hagendorfer, H., Frick, D. A., Gunther, D. Mass quantification of nanoparticles by single droplet calibration using inductively coupled plasma mass spectrometry. Analytical Chemistry. 85 (12), 5875-5883 (2013).
- Gschwind, S., et al. Capabilities of inductively coupled plasma mass spectrometry for the detection of nanoparticles carried by monodisperse microdroplets. Journal of Analytical Atomic Spectrometry. 26 (6), 1166-1174 (2011).
- Zarrln, F., K, S. L., Socha, J. R. Droplet size measurements of various nebulizers using differential electrical mobluty particle sizer. Journal of Aerosol Science. 22, 343-346 (1991).
- Geertsen, V., Lemaitre, P., Tabarant, M., Chartier, F. Influence of design and operating parameters of pneumatic concentric nebulizer on micro-flow aerosol characteristics and ICP-MS analytical performances. Journal of Analytical Atomic Spectrometry. 27 (1), 146-158 (2012).
- Mehrabi, K., Günther, D., Gundlach-Graham, A. Single-particle ICP-TOFMS with online microdroplet calibration for the simultaneous quantification of diverse nanoparticles in complex matrices. Environmental Science. Nano. 6, 3349-3358 (2019).
- Ramkorun-Schmidt, B., Pergantis, S. A., Esteban-Fernandez, D., Jakubowski, N., Gunther, D. Investigation of a combined microdroplet generator and pneumatic nebulization system for quantitative determination of metal-containing nanoparticles using ICPMS. Analytical Chemistry. 87 (17), 8687-8694 (2015).
- Rosenkranz, D., et al. Improved validation for single particle ICP-MS analysis using a pneumatic nebulizer/microdroplet generator sample introduction system for multi-mode nanoparticle determination. Analytica Chimica Acta. 1099, 16-25 (2020).
- National Institute of Standards and Technology. Report of investigation reference material. Reference material 8017. National Institute of Standards and Technology. , (2015).
- Tavares, A. M., et al. Genotoxicity evaluation of nanosized titanium dioxide, synthetic amorphous silica and multi-walled carbon nanotubes in human lymphocytes. Toxicology In Vitro. 28 (1), 60-69 (2014).
- Au-Kaur, I., et al. Dispersion of Nanomaterials in Aqueous Media: Towards Protocol Optimization. Journal of Visualized Experiments. (130), e56074(2017).
- Nanotechnologies. Size distribution and concentration of inorganic nanoparticles in aqueous media via single particle inductively coupled plasma mass spectrometry. ISO/TS19590 Nanotechnologies. , (2017).
- Shigeta, K., et al. Application of a micro-droplet generator for an ICP-sector field mass spectrometer - optimization and analytical characterization. Journal of Analytical Atomic Spectrometry. 28, 646-656 (2013).
- Koch, J., et al. Accelerated evaporation of microdroplets at ambient conditions for the on-line analysis of nanoparticles by inductively-coupled plasma mass spectrometry. Journal of Analytical Atomic Spectrometry. 28 (11), 1707-1717 (2013).
- Tuoriniemi, J., Cornelis, G., Hassellov, M. A new peak recognition algorithm for detection of ultra-small nano-particles by single particle ICP-MS using rapid time resolved data acquisition on a sector-field mass spectrometer. Journal of Analytical Atomic Spectrometry. 30 (8), 1723-1729 (2015).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。


