Method Article
マルチモード単粒子誘導結合プラズマ質量分析およびバリデーションのための汎用デュアルインレットサンプル導入システム
要約
ここでは、標準的な独立したナノ粒子の特性評価を可能にする、単一粒子誘導結合質量分析用のデュアルインレットシステムを使用するためのプロトコルを提供します。
要約
金属含有ナノ粒子(NP)は、誘導結合プラズマ質量分析計(ICP-MS)で、装置の単粒子モード(spICP-MS)を使用して、そのサイズと数濃度の点で特性評価できます。測定の精度は、セットアップ、機器の動作条件、およびユーザーが設定する特定のパラメータによって異なります。ICP-MSの輸送効率は、NPの定量にとって非常に重要であり、通常、均一なサイズ分布と既知の粒子数濃度を持つ標準物質が必要です。
現在、NP標準物質はごく一部の金属についてのみ入手可能で、サイズも限られています。参照標準なしで粒子を特性評価すると、サイズと粒子数の両方の結果に偏りが生じる可能性があります。そこで、この問題を克服するために、spICP-MSでナノ粒子を特性評価するためのデュアルインレットセットアップが開発されました。このセットアップは、ナノ粒子溶液用の空気圧ネブライザー(PN)とイオン校正溶液用のマイクロ液滴発生器(μDG)で構成される従来の導入システムに基づいています。μDG、PN、ICP-MSシステムの結合を容易にするために、新しい柔軟なインターフェースが開発されました。このインターフェースは、利用可能なラボ用コンポーネントで構成されており、ICP-MS装置が稼働している間に、キャリブレーション、ナノ粒子(NP)の特性評価、および配列の洗浄が可能です。
粒子サイズと数濃度を決定するために、3つの独立した分析モードが利用可能です。各モードは、異なるキャリブレーション原理に基づいています。モードI(計数)とモードIII(μDG)は文献から知られていますが、モードII(感度)は、無機イオン標準溶液のみによる輸送効率を決定するために使用されます。NP標準物質に依存しません。ここで説明するμDGベースのインレットシステムは、優れた分析物感度を保証し、したがって検出限界(LOD)を低く抑えます。達成されるサイズ依存のLODは、調査したすべてのNP(Au、Ag、CeO2)で15 nm未満です。
概要
誘導結合プラズマ質量分析計は、いわゆる単粒子モード1,2,3でさまざまなサンプルやマトリックス中のNPのサイズと数を定量するために広く使用されています。シングルパーティクルモードは、短い積分時間または滞留時間でデータ収集システムの操作です。測定された各NPは、NP懸濁液の適切な希釈が二重イベントを回避するために使用された場合、この時間間隔で積分信号(カウント/秒で測定されるイベント:cps)を生成します。キャリブレーション標準試料は、サンプルと同様に、通常、空気圧噴霧(PN)4に基づく従来のサンプル導入システムを介してICP-MSに導入されます。ただし、前提条件として、NPあたりの金属質量を正確に定量し、懸濁液中のそれらの数濃度を決定するためには、サンプル導入流量と輸送効率(η)を決定する必要があります。輸送効率とは、ICP−MS5によって検出される質量(廃棄物収集方法)または粒子数(計数方法)に対する注入された質量または粒子数の割合を表す。輸送効率は、ナノ粒子ベースの標準物質5を使用して最も頻繁に決定されます。ただし、輸送特性はNPの構造に依存し、組成やサンプル分散剤などの特性が関与します。その他の影響要因は、サンプルの取り込み率、ネブライザーのガス流量、滞留時間、合計測定時間などの機器パラメータです。
ナノ粒子標準物質は限られているため、参照粒子とサンプル粒子の元素組成の違いにより、得られたNP分析結果に偏りが生じる可能性があります。限られた範囲の標準物質が利用できることに加えて、検出器の滞留時間ごとに複数の粒子イベントを検出することは、さらなる課題を表しています。これは、決定される輸送効率の精度にも影響を与える可能性があります。
標準物質に依存しないためには、輸送効率がほぼ100%のサンプル導入システムが理想的です。同時に、従来の導入システムに比べて少量で使用する場合、より高い粒子数濃度を使用することができます。2つの粒子が互いに接近していても、μDGベースのシステムでは両方を別々に検出できます。
μDGは、pL範囲の固定容量で単分散液滴を生成することができ、この目的に適しています6,7,8,9。μDGは、異なる溶媒中のイオン性サンプルと微粒子性サンプルの両方をICP-MSに注入することを容易にします。イオン性金属サンプルの場合、生成された液滴はICPに向かう途中で完全に脱溶媒化されていると想定されます。したがって、液滴はすべての水を失い、残りの塩から粒子が形成されます。この粒子の直径は、使用される濃度に正比例します。したがって、同じマトリックス、質量、およびサイズの自家製の参照標準試料を、調査対象のNPのイオン溶液の濃度を変えて、社内で製造することができます。液滴の体積は、μDGで測定した液滴の直径に基づいて簡単に計算できます。これは、異なる直径10,11の液滴の広い分布を生成するPNでは不可能です。μDGの100%という高い輸送効率で均一なサンプル導入を行うことで、装置特異的な高い分析物感度を達成することができます。使用するマトリックスにもよりますが、PN12に基づく従来の導入システムの結果と比較して、粒子の質量とサイズの検出限界(LOD)が低くなります。しかし、μDGの設計上、ICP-MS装置が稼働している状態では、容易に試料交換を行うことができません。異なるサンプルの測定の合間には、μDGを洗浄し、その後、システムを安定させるためにサンプル溶液で洗い流す必要があります。さらに、重いマトリックスサンプルに対する耐性は、あまりテストされていません。また、流量が極端に少ないため、良好な統計を得るための分析時間が非常に長くなり、環境水などの「実際の」サンプルを分析する場合、その実用化が制限されます。
これらの制限を克服するために、μDGは、以前は、デュアルインレットシステム13の名称が与えられた従来の空気圧ネブライザーベースのシステムと組み合わせて運転されてきた。μDGおよびNP懸濁液を用いた較正標準を空圧ネブライザーを介してICP-MSに導入することにより、Ramkorun-Schmidtらは両方のシステムを利用することができた13。AuおよびAgNPの金属質量分率の高精度な測定が達成され、輸送効率の決定は必要ありませんでした。しかし、このデュアルインレットシステムでは粒子数濃度は測定されませんでした。また、μDGシステムのクリーニングとアライメントが、ルーチン分析への適用性を複雑にしていました。
この論文では、NP粒子サイズと粒子数濃度を決定するための柔軟なデュアルインレットインターフェースを提案し、その組み立てと実用化を示します。Ramkorun-Schmidtらのシステムと同様に、μDGとPNサンプル導入システムの両方で構成されています。デュアルインレットシステムは、開発の現在の段階では、金属含有NPを調査および特性評価するために3つの独立した分析モードを適用できることを示しています。当社のデュアルインレットシステムは、NP測定の校正手順を簡素化し、分析性能指数、特に精度14を向上させます。インレットシステムにより、ICP-MSが動作しているときでもμDGのサンプル交換と洗浄が容易になり、全体的な分析時間とミスアライメントのリスクが軽減されます。システム性能を試験するために、十分に特性評価されたリファレンスNP(60 nm AuNP – NIST 8013、75 nm AgNP – NIST 8017)を分析法のバリデーションと比較に使用します。
プロトコル
1. デュアルインレットサンプル導入セットアップの組み立て
メモ: さまざまなパーツの詳細を 表 1 に示します。
| コンポーネント | |||
| パート1 | シャンク長約10mmのガラスメス球面ボールジョイント | ||
| シャンク長約10mmのガラスオスボールジョイント | |||
| 金属製Tピース(寸法:1/4インチ) | |||
| ガラスと金属の接着剤 | |||
| 球面ガラスジョイント用の2つのクランプ | |||
| パート2 | ICP-MSスプレーチャンバー(推奨タイプ:インパクトビーズスプレーチャンバー、サイクロンスプレーチャンバーなど) | ||
| 空気圧ネブライザー(推奨タイプ:同心円状ネブライザー) | |||
| 鎹 | |||
| パート3 | Oリングフリークォーツトーチ | ||
| ガスラインコネクタクローズドエンド | |||
| ガスラインコネクタオープンエンド | |||
| 導電性で柔軟なシリコーンチューブ | |||
| パート4 | 圧電マイクロ液滴発生ユニット | ||
| パート5 | マイクロ液滴制御ユニット | ||
表1:デュアルインレットセットアップの構築に使用されるコンポーネントのリスト。
- Tピースコネクタユニットの構造(図1パート 1)。
注:従来のサンプル導入装置(ステップ1.2)とμDG搬送ユニット(ステップ1.3)を接続する部品です。- オスとメスのボールジョイントをTピースコネクタの反対側の開口部に挿入します。
- オスとメスのボールジョイントを、ガラスと金属の接着剤(シリコン接着剤など)を使用して固定します。
- メスボールジョイントをICP-MSのインジェクターにクランプで接続します。
- 従来のサンプル導入装置のアタッチメント(図1 パート2)
注意: この部品はTピースコネクタユニットに接続されています(ステップ1.1)- ICP-MSスプレーチャンバーと、使用するスプレーチャンバーに収まる空気圧ネブライザー(PN)を組み合わせます。
- clを使用しますamp スプレーチャンバーの出口をTピースコネクタのオスボールジョイントに接続します(手順1.1で説明)。
注:スプレーチャンバーの出口には、通常、メスのボールジョイントコネクタが装備されています。 図 1 に示す組み合わせは、ネブライザーとインパクト ビーズ スプレー チャンバーで構成されています。インパクトビーズスプレーチャンバーの代わりに、2〜10%以上の範囲の輸送効率を持つ他のスプレーチャンバーを使用することができます。
- 微小飛沫輸送ユニットの構造(図1 その3)
注意: この部品は、Tピースコネクタユニット(ステップ1.1)とμDGユニット(ステップ1.4)を接続します。- 取り外し可能なクォーツトーチを、インジェクターチューブを取り外した状態で、トーチインレットが上部にある実験室スタンドに適切なクランプを使用して取り付けます。
- トーチプラズマ/補助ガス入口をクローズドエンドガスコネクタで塞ぎます。
注:サンプルは、蠕動ポンプを使用してネブライザーに輸送されます。アルゴンガスは、サンプルをスプレーチャンバーに噴霧し、さらにプラズマに輸送するために使用されます。 - 適切なガスコネクタを使用して、冷却ガス入口を介してヘリウムガスラインをトーチに接続します。
注:印加されたヘリウムガスは、生成された液滴の脱溶媒に使用され、液滴がセットアップの壁に衝突するのを防ぎ、ICP-MS装置が大気中の酸素挿入を防ぐシースガスとして機能します。一方、μDGのサンプル入口ヘッドは洗浄とサンプル交換のために取り外す必要があります。 - アダプターを使用して、長さ30 cmの導電性および柔軟なシリコンチューブ(内径0.75 cm)をトーチの出口端(トーチの底)に接続します。
- シリコンチューブの下端をTピースコネクタユニットに接続します。これには、フレキシブルシリコンチューブを残りの垂直金属接続部に伸ばします。
注:柔軟なシリコンチューブにより、接続されたセットアップでICP-MS装置のx-y-zチューニングが可能になります。
- 微小飛沫発生ユニットと微小飛沫発生制御ユニットの接続(図1 パート4、パート5)
注:この部品はμDGトランスポートユニットに接続されています(ステップ1.3)- トーチのサンプル入口端にμDGヘッドを挿入して、準備したμDGユニットをマイクロ液滴輸送ユニットに接続します。
- μDGコントロールユニットに電源を接続します。
注:ここで説明するセットアップは、市販のμDGヘッドとμDG電源で構成されています。使用するμDGヘッドに応じて、セットアップを適宜調整する必要があります。
2. 液滴サイズの定量化
- ストロボスコープライトとCCDカメラ(たとえば、オープン構成では、 図1 サイズの測定構成を参照)を使用して、μDGによって生成された液滴の画像を撮影します。
- μmの範囲にある既知のサイズの物体(直径150μmの銅線など)の画像を撮影して、CCDカメラをキャリブレーションします。
- 実験に使用した設定で少なくとも1, 000滴の画像を撮影します( 表2を参照)。
- 適切なグラフィカルソフトウェアプログラム( 資料の表を参照)を使用して、次の手順でオブジェクトとドロップサイズに関する画像を評価します。
- 「ファイル」と「開く」をクリックして、オブジェクトのイメージをロードします。
- 画像をクリック |調整 |スクロールバーを移動してオブジェクトの領域を定義するしきい値。
- [適用] をクリックして設定を適用します。
- [直線セグメント]ボタンをクリックします。
- マウスの左ボタンをクリックしたままにすると、オブジェクトの横に線が引かれます。
- Ctrl + M を押して、オブジェクトのサイズを測定します。
- 5つの異なるポイントでオブジェクトの直径を測定します。
- 「結果」テーブルをコピーして、スプレッドシートソフトウェアに貼り付けます。
- 列 "Length"の算術平均を計算します。
- ピクセルアスペクト比(PAR)を計算します:実際のオブジェクトサイズ(μm)/画像内の平均オブジェクトサイズ(px)。
- [ファイル] |インポート |Image Sequence は、液滴の画像をインポートして読み込みます。
- 「長方形」をクリックし、最初の画像の液滴をマークします。
- マウスパッドを右クリックして [複製 ]を選択し、画像シーケンスの液滴を画像の残りの部分から分離します。
- ステップ2.4.2で指定されているように、液滴を背景から分離します。
- [プロセス] |バイナリ |侵食して、液滴表面の光の反射を取り除きます。
- [プロセス] |バイナリ |「侵食」ステップを逆にするために拡張します。
- [分析] |粒子の分析 |すべての液滴を測定しても大丈夫です。
- 「Summary」または「Result」の表をコピーして、表計算ソフトに貼り付けます。
- フェレットの直径の算術平均をpxで計算します。
- PARを使用して、直径をμmで変換します:フェレットの直径をpx/PARで変換します。
注:μDGによって形成される液滴のサイズは、ピエゾ素子7に適用される電流パルスの選択された長さと持続時間によって異なります。
3. サンプル調製
- 希酸(HCl(0.5 v/v)、HNO3 (3.5 v/v)など)中の0.2〜20 μg/Lの濃度範囲で測定する分析種のイオン性キャリブレーション溶液を調製します。
- 希酸中で1〜10μg/Lの濃度範囲でワンポイントキャリブレーション用のイオン溶液を調製します。
- NP標準サスペンションは、製造元の指示または社内プロトコルに従って調製します。
注:ステップ3.3.1〜3.3.4では、Ag、Au、CeO2 NPを例にとったNP標準懸濁液の調製について説明します。- PNには0.05 μg/L AuNP溶液10 mLを、超純水にはμDG溶液に1 μg/L AuNP溶液を調製します。使用する前に20〜60秒間渦巻きます。
- PNには0.05 μg/L AgNP溶液を、超純水中には2 μg/L AgNP溶液を調製します。15を使用する前に、20〜60秒間よく振ってください。
- 金属酸化物16,17について前述したように使用するCeO2 NP溶液を調製する。
- PNには0.05 μg/L CeO2 NP溶液を、μDGには1 μg/L溶液を調製します。
- 合計15 mL〜20 mLのガラス容器で25.6 mg/mL CeO2 NPを秤量し、超純水で調製した0.05(v / v)BSA溶液10 mLを加えます。
- 7.35 Wの電力を持つ指先の超音波発生器を使用して、粒子溶液を309秒間均質化します。
4. 楽器のチューニングとパラメータ
- MDGジェネレーターの電源がオフになっていることを確認し、ステップ1で作成したデュアルインレットサンプル導入セットアップをICP-MS装置のインジェクターとクランプで接続します。インレットシステムをネブライザーガス(Ar)と液滴輸送ガス(He)で5〜10分間洗い流します。
注:ICP-MS装置は、プラズマルームへの高レベルの酸素の侵入から保護する必要があります。 - 液滴輸送ガス(He)をOFFにし、ICP-MSシステムを起動します
- ICP-MSシステムの製造元が指定する装置標準チューニングソリューションを使用して、利用したい測定モードで装置をチューニングします。
注:標準的なチューニングソリューションは、バリウム、セリウム、インジウム、ウラン、ビスマス、コバルト、リチウム(すべて1μg / L)で構成され、2.5%(v / v)の硝酸と0.5%(v / v)塩酸の混合物に含まれています。 - PNのサンプル取り込み率の決定。
- 容器に15mLの水を入れます。
- 容器の重量を量ります。
- 容器をPNのチューブに接続します。
- 装置ソフトウェアの蠕動ポンプ開始ボタンをクリックして、蠕動ポンプを開始します。
- 5分間のタイマーを開始します。
- 5分後に正確に容器から取り込みラインを取り外します。再度容器の重量を量ります。
- サンプル取り込み速度(mL/min)を次の式で計算します:前の容器重量 - 後の容器重量/時間持続時間。
- 必要に応じて、ネブライザーのガス流量、サンプリング深度、プラズマ出力などの分析対象物の感度を向上させるために、機器パラメータを最適化します。
注:ICP-MS システムで最適化できる装置パラメーターの例として、 表 2 を参照してください。 - 液滴形成率の関数として一定の信号速度を検出できるようになるまで、Heガス流量を調整します。
| パラメーター | 価値 | ||
| ICP – MS: | |||
| プラズマ出力(W) | 1600 | ||
| サンプリング深さ(mm) | 4 | ||
| 流量(L最小-1): | |||
| 補助ガス | 0.65 | ||
| 冷却ガス | 14 | ||
| タイムズ (秒) | |||
| データ取得 | 1200 | ||
| 滞在時間 (秒) | 0.01 | ||
| インターフェイス: | |||
| PN サンプル取り込み速度 (mL min-1) | 0.21 | ||
| ネブライザーガス(L分-1) | 0.92 | ||
| μDGです。 | |||
| キャピラリー径(μm) | 75 | ||
| ドロップ率(Hz) | 10 | ||
| HEメイクアップガス(Lmin-1) | 0.27 | ||
| 動作モード | トリプルパルス | ||
| セット1 | セット2 | セット3 | |
| 電圧(V) | 53 | 51 | 47 |
| パルス幅(μs) | 20 | 25 | 12 |
| パルス遅延(μs) | 4 | 2 | 1 |
表2:使用されたインストゥルメンタルパラメータの値。
5. ナノ粒子試料のマルチモード測定
- μDGコントロールユニットを準備します
- μDGコントロールユニットの電源スイッチをONにします。
- 最初の画面で [開始 ]をクリックして、コントロールユニットを起動します。
- [グローバル設定]をクリックして、使用するパルスモードを選択します。
- パルスモードで右側のグラフィカルボタンをクリックして、トリプルパルスモードを選択します。
注意: トリプルパルスモードの設定を 表2に示します。
- μDGユニットの準備
- [オン/オフ]をクリックして、μDGを起動します。
- 測定するサンプル溶液をサンプル容器に充填します。
- サンプル容器をμDGユニットに接続します。
- 10mLシリンジを使用して、容器とμDGユニット内の空気をパージします。
- シリンジをサンプルコンテナ容器のシリンジポートに接続します。
- シリンジプランジャーを、μDGヘッドから一定の液体の流れが出るのが観察されるまで押します。
- 圧力を10秒間維持します。
- シリンジを取り外します。
- μDGユニットをCCDカメラのフォーカスゾーンに置き、形成された液滴を観察します。
- CCDカメラをPCまたはラップトップに接続します。
- CCDカメラソフトウェアを起動して、形成された液滴を観察します
- [開始] をクリックして、液滴のライブ ビューを取得します。
- 一定の液滴形成を観察します。
- μDGヘッドをデュアルインレットサンプル導入システムの倒立トーチに置きます。
- μDGユニットとPNの両方を、マルチポイントキャリブレーションの繰り返しを測定することにより、対象の各要素について検証します。
注:ICP-MSデータ取得には、装置に関連付けられているソフトウェアを使用してください。 - マルチポイントキャリブレーションの線形範囲を決定するには、実験データをスプレッドシートソフトウェアにインポートします。
- 各キャリブレーションポイントの算術平均を計算します。
- 切片、傾き、および相関係数を決定します。
注:sp-ICP-MSの場合、相関係数は>0.9918である必要があります。
- 検量線の線形範囲内の濃度を選択して、後でワンポイント校正を行います。
- 以下の手順に従って、マルチモードナノマテリアル定量(図2)の測定と検証(NIST 8012、NIST 8013、NIST 8017などの標準物質を使用)を行います。
- ナノ粒子とイオン性標準物質を、目的の分析種に応じて選択してください。
- μDGユニットを5.2に従ってイオン標準溶液で調製します。
- PNを介して希釈した酸溶液(例:0.5% v/v HCl)を添加します。
- ICP-MSシステムの測定を時間分解モードで開始します。
- 120秒後に On/Off をクリックすると、μDGが停止し、PNの希酸溶液がイオン標準と交換されます。
- 330 秒後、PN のイオン標準試料を再び希酸溶液と交換します。
- その間、μDGユニットをセットアップから取り外します。
- μDGユニットのサンプル容器(ガラスバイアル)を、希釈した酸溶液(3.5%HNO3など)を入れた容器と交換して、μDGユニットを洗浄します。
- 10mLのシリンジに空気を入れます。
- シリンジをμDGユニットの注入ポートに接続し、μDGヘッドから液体の噴流が出るまでシリンジを空にし、圧力を30秒間維持します。
- 手順5.2で指定されているように、NPサンプルを使用してμDGを準備し、μDGユニットを510秒でセットアップに取り付け直します。
- 810秒後に [オン/オフ ]をクリックして、μDGを停止します。
- PNで希酸溶液をNPサンプルと交換し、さらに300秒間測定します。
- 約1,200秒後に測定を停止します。
- 手順5.5.8で指定されているように、μDGユニットを清掃します。
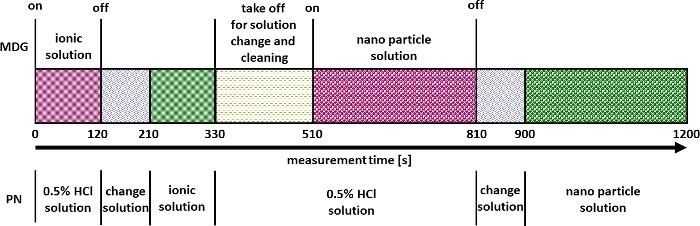
図2:マルチモードナノ材料定量のための測定戦略。この図の拡大版を表示するには、ここをクリックしてください。
6. データ分析
注:すべての計算手順を簡略化するために、対応するスプレッドシートが用意されました( 補足ファイルを参照)。
- データフレームを処理できるスプレッドシートまたはソフトウェアを使用して、データを処理し、測定データをインポートします。A列にスプレッドシートソフトウェア(電子サプリメントに含まれています)の測定値全体の強度値を貼り付けると、データが視覚化されます。計算に必要なすべての実験パラメータを「入力パラメータ」の表に入力します。
- 適切なスプレッドシートセルを選択して、μDG ionic (I)、PN ionic (II)、μDG NP (III)、PN NP (IV) の対象領域 (ROI) を定義します。準備されたシートのグラフを使用してROIの境界を定義し、「関心領域の決定」テーブル(セルC1:E7)に値を入力します。
- 各データセットをコピーして、別々の列に貼り付けます。準備したシートの Copy ROI ボタンを押して、測定値を4つのROI(列M:P)に分割します。
- IとIIの算術平均を計算します。
- 反復アプローチを適用して、IIIとIVの粒子または液滴信号とバックグラウンドを分離します。
- すべての測定値の算術平均と標準偏差を計算します。
- 制限値またはカットオフ値を平均値 + 5 x 標準偏差で計算します。
- III と IV の制限値より小さい信号をすべて削除します。識別された粒子信号に対して Cut コマンドを使用します。 [貼り付け] を使用して、それらを別の列に貼り付けます。
- 平均値と標準偏差が一定になるまで、手順1〜3を繰り返します。
注:準備したシートの列QからBDでは、バックグラウンド信号と粒子信号を分離するための反復アプローチが5回実行されます。
- 同定された粒子信号IIIとIVの算術平均を計算します。
- 分析対象物の検出限界(LOD - カウント)、分析対象物の感度(SC、イオン性 - カウント/(μg/L))、サンプル取り込み速度(qs - mL/min)、輸送効率(η - 相対単位)、およびバルク材料密度(ρ - g/cm³)を使用して、μDG NPおよびPN NPの最小検出可能粒子サイズ(LODサイズ - nm)を計算します。
- μDG NP と PN NP の同定された粒子信号の質量 (ma,p) と粒子サイズ (d – nm、粒子が球形であると仮定) を、標準溶液のイオン性金属濃度 (ca - μg/L) とプラズマ中のイオンフラックス (カウント/秒) を考慮して適用された 3 つの分析モードに従って計算します。
- 質量:

- 大きさ:

- 質量:
- 検出された粒子の数(qp)、サンプルの粒子濃度(cp、使用 済み - 1/mL)、PNおよびMDGの分析物感度(Sm、イオン性、PN型、Sm型、イオン性、MDG - カウント/(μg/L))、液滴の体積(V型ドロップ - pL)、 滞留時間(TD – ms)、PNの輸送効率(ηPN)、μDGの輸送効率(ημDG)、PNおよびμDGによって測定されたイオン溶液の強度(Iイオンc、PN、Iイオン性、μDG –カウント)、および両方の注入システムに使用されるイオン溶液の濃度(cイオン性、PN、 cイオン性、μDG - μg/L):
- モードI:

- モードII:

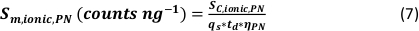

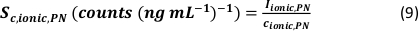
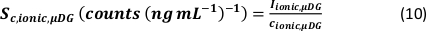
- モードI:
- μDGの伝送効率が1:19に等しいと仮定します
- 分析した NP 溶液の粒子数濃度は、測定中に注入されたサンプル量 (注入された V) を考慮して計算します。
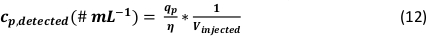
注:準備されたシートでは、分割後にすべての計算が自動的に実行されます。結果は表「出力パラメータ」(セルBH7:BR35)に表示され、個々の計算ステップを含む上記の式が含まれています。
結果

図3:CCDカメラによる液滴サイズの決定。 150μmの銅線によるCCDカメラのキャリブレーション(A)と、達成された液滴画像をバイナリカラー画像(B)に変換した後の液滴サイズの決定。 この図の拡大版を表示するには、ここをクリックしてください。
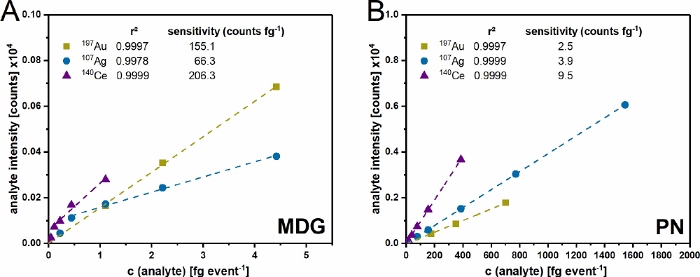
図4:デュアルインレットセットアップの検証。 金(Au)、銀(Ag)、セリウム(Ce)のμDG(A)およびPN(B)インレットシステムのマルチポイントキャリブレーション。0.2 〜 20 μg mL-1 の範囲の使用濃度は、検出されたイベントあたりの質量の使用実験条件に応じて変換されます。提示されたデータは、3つの独立した反復の平均値です。 この図の拡大版を表示するには、ここをクリックしてください。
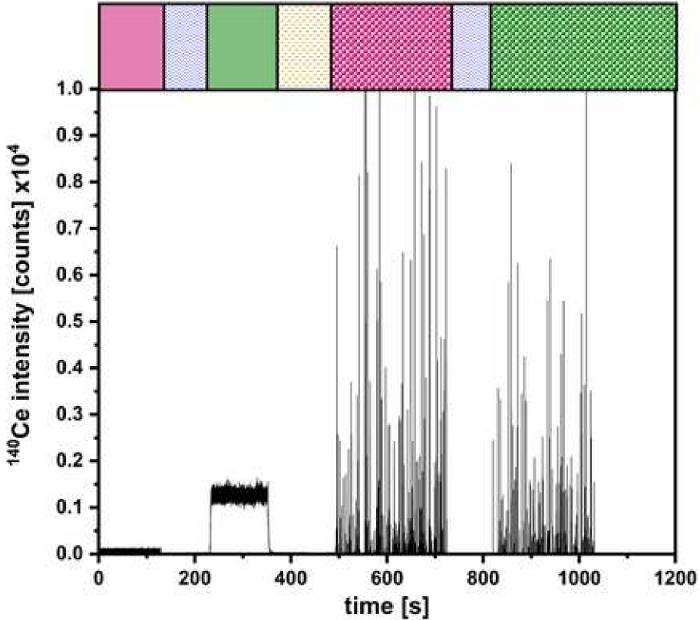
図5:デュアルインレットセットアップの測定を表しています。 CeO2 NP の定量は、 図 2 で行ったように、さまざまな注入ステップについて色付きのバーで行います。 この図の拡大版を表示するには、ここをクリックしてください。
| 見本 | 解析モード / | NPサンプル用インレット | 校正標準液用インレット | η | MA、P | NPサイズ(d) | #NPs | レコブリー (%) | |
| η PN決定 | (%) | (FGの) | (ナノメートル) | (mL-1 x103) | |||||
| Au 56 nm | モードI / | PNの | PN: Au イオン性 & AuNP 標準物質 | 1.8 (0.1) | 1.9 (0.5) | 57.2 (4.3) | 28.1 (0) | 100 | |
| NIST 8013 (英語) | カウント方法 | ||||||||
| モードII/ | PNの | PN/μDG: | 1.9 (0.1) | 2 (0.4) | 58 (3.6) | 25.6 (1.6) | 91 | ||
| 感度比 | Auイオン標準 | ||||||||
| モードIII/ | μDGの | μDGです。 | 100 | 1.7 (0.2) | 55 (2.4) | 394.4 (29.3) | 70 | ||
| ημDG = 1 | Auイオン標準 | ||||||||
| 予想サイズ (nm) | 56.0 (0.5) | ||||||||
| 銀 75 nm | モードI / | PNの | PN: AgイオンおよびAgNP標準 | 2.3 (0.2) | 1.9 (0.2) | 70.2 (2.3) | 21.6 (0) | 100 | |
| NIST 8017 (英語) | カウント方法 | ||||||||
| モードII/ | PNの | PN/μDG: | 2.5 (0.2) | 2 (0.2) | 71.5 (2.1) | 20.5 (1.9) | 95 | ||
| 感度比 | 銀イオン標準物質 | ||||||||
| モードIII/ | μDGの | μDGです。 | 100 | 2.5 (0.2) | 76.7 (2.3) | 757.1 (68.7) | 88 | ||
| ημDG = 1 | 銀イオン標準 | ||||||||
| 予想サイズ (nm) | 74.6 (3.8) | ||||||||
| CeO2 JRC NM212 | モードI / | PNの | PN: CeイオンおよびAuNP標準 | 1.7 (0) | 0.90 (0.09) | 61.9 (2.0) | 7.59 (0.32) | - | |
| 10-100 nm | カウント方法 | ||||||||
| モードII/ | PNの | PN/μDG: | 4.9 (1.4) | 1.36 (0.35) | 70.6 (5.9) | 5.42 (1.7) | - | ||
| 感度比 | Ceイオン標準 | ||||||||
| モードIII/ | μDGの | μDGです。 | 100 | 1.63 (0.62) | 74.4 (9.2) | 590 (168) | - | ||
| ημDG = 1 | Ceイオン標準 | ||||||||
表3:デュアルインレットセットアップの結果。 3つの分析モードと3つの輸送効率決定方法を使用した、Au NIST 8013、Ag NIST 8017、およびCeO2 JRC NM 212(n = 3)NP材料の輸送効率、金属質量分率、直径、およびNP数濃度。回復率は、予想 #NPs に対する決定された #NPs の比率として定義されます。この表は、参考文献14の許可を得て転載しています。
ここで紹介するプロトコールでは、粒子の質量と数濃度を決定することができます。液滴サイズ(図3)を含むμDG液滴形成は、事前に特徴付けました(表3)。
セットアップを組み立て(図 1)、液滴サイズを決定した後、両方の注入システムをイオン標準でバリデーションしました(図 4)。r² > 0.99 の精度は、調査したすべての要素について、両方の注入システムで達成できました。ただし、導入および輸送される分析物の量により、両方のシステムには違いがあります。μDGは非常に高い輸送効率(最大100%)を備えているため、PNと比較して高い分析種の感度が観察され、同時に低質量入力で観察されます。ただし、μDGによって導入される測定濃度は、2つの線形範囲に分離する必要があります。Agの場合、最初の線形範囲は0〜0.5 fgイベント-1 の間で観察でき、2番目の線形範囲は0.5〜fgイベント-1の間で観察できます。対照的に、Ce の最初の線形範囲は 0 から 0.25 fg event-1 の間であり、2 番目の線形範囲は 0.25 から 3 fg event-1 の間です。測定された濃度のPNの線形範囲は、より高く見えます。これは、検出イベントごとにICP-MSに導入される質量の違いに関連している可能性が最も高いです。μDGは、液滴および検出イベントごとに一定の絶対量を少量で注入するため、PNによるサンプルの導入と比較して検出質量が少なくなります。
検証が成功したら、図 2 に示すように実験を実行できます。このような実験の結果を、CeO2 NPの粒子サイズと数濃度を決定するための図5に例示されています。ここでは、導入されたイオン溶液とNP溶液のμDGおよびPNを介したシグナルを同定できます。調査したすべての粒子について、トリプルデスティネーションを実施しました。
得られたデータの評価は、上記のようにして行い、 表3にまとめられている。デュエルインレットのセットアップと3つの分析モードの検証に使用したAuおよびAgNPについては、すべての分析モードを実行して、認証された粒子サイズと数濃度を達成できました。CeO2 について得られる平均粒子サイズは10〜100nmであり、メーカーが指定した範囲です。
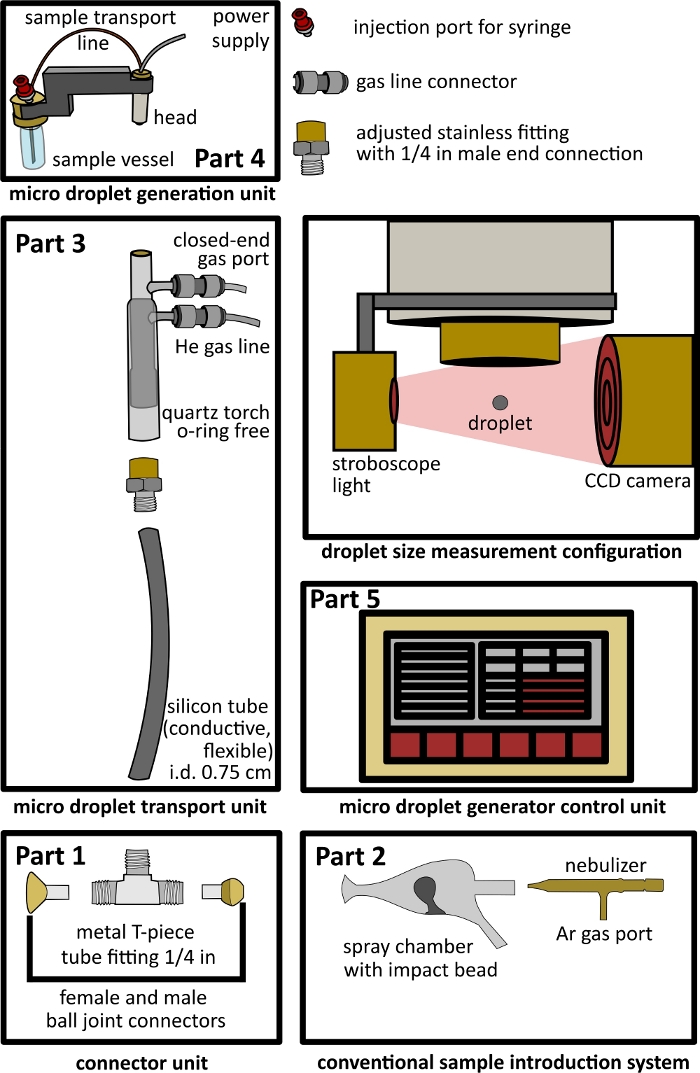
図1:デュアルインレットインターフェースセットアップの設計。 パート1 - コネクタユニット、パート2 - 従来の導入システム、パート3 - マイクロ飛沫輸送ユニット、パート4 - 微小飛沫発生ユニット、パート5 - 微小飛沫制御ユニット、ストロボスコープライトやCCDカメラなどの飛沫サイズ測定用のオープン構成。 この図の拡大版を表示するには、ここをクリックしてください。
ディスカッション
開発されたデュアルインレットセットアップの目的は、調査対象の分析物とは無関係に、さまざまな分析モードを使用して、NPのサイズと数濃度に関してNPを可能な限り正確に特性評価および定量することです。従来の導入システム(PN)と少量(pL)および高質量(最大100%)の導入システム(μDG)を組み合わせることで、これを実現できます。この研究で提示されたセットアップを使用することで、粒子質量の定量に必要な元素固有の輸送効率を、NP標準物質とは無関係にイオン標準に基づいて決定できます。さらに、μDGを使用してICP-MSに導入されたNPは、粒子サイズ分布が狭く(AuNP)、または類似の(AgNP)分布を示します。それ以外の場合、CeO2 では、μDGのより広いサイズ分布が観察され、分析されたサンプルの多分散性が高いことに起因している可能性があります。低ボリュームの導入により、2つのNPを互いに別々に検出することができ、これは、そうでなければ、従来のセットアップ14では1つのNPと解釈されるであろう。
μDGトランスポートユニットの利点は、柔軟なシリコンチューブによる高い柔軟性であり、セットアップのアライメントが簡素化されます。インジェクター付きのトーチは、ICP-MSに接続したままセットアップ中に調整することもできます。追加で印加されたHeガスの流れは、μDGヘッドによって形成された液滴とチューブ壁20との衝突を防止する。さらに、Heガスにより、ICP-MSが動作しているときでも、サンプル交換中にμDGヘッドを取り外すことができます。ICPを動作状態に保つことは、安定した堅牢な測定のために重要です。μDGヘッドは、新しいサンプルや標準試料ごとに洗浄およびすすぐ必要があるため、この作業で導入するインレットシステムの操作にはHeフローが不可欠です。さらに、システムへの酸素の浸透を防ぐために、デュアルインレットセットアップのすべての部分を正しく接続する必要があります。提示されたセットアップで酸素を減少させるために、プラズマの点火前に、システムをネブライザーと液滴輸送ガスで少なくとも5〜10分間洗い流します。
形成された液滴がコネクターユニットに到達すると、噴霧された液体の流れによってプラズマに運ばれます(湿式プラズマ状態とも呼ばれます)。ドライプラズマ条件の使用と比較して、これはプラズマの液体含有量の増加につながります。その結果、信号強度は減少し、信号の変動は増加し、すなわち、平均測定信号13の標準偏差が高くなる。しかし、μDGと0.2μg/Lの範囲の濃度を使用することで、バックグラウンドより上の信号を検出することができます。液滴あたりの対応する注入質量は金属含有量が低く、一部の元素(Au、Ag、Ceなど)の検出限界に近い値です。この限界に沿った異なる濃度の較正を使用する場合、Ceで約0.05μg/L、Agで約2μg/Lのオーバーラップを伴う2つの線形領域を観察することができる。これらの制限を超えると、μDGの線形動作範囲を特定できます。低濃度を測定する能力があっても、液滴内の同じ分析種のイオンとNPが同時に存在する場合、それらを区別することは不可能です。それ以外の場合、従来の導入システムを使用することにより、平均イオンバックグラウンドを決定し、すべての信号から減算して粒子信号のみを取得できます。
MDGベースのシステムには、提案されたデュアルインレットシステムの適用によって部分的に回避できるいくつかの制限もあります。しかし、μDGの液滴周波数が50Hzを超えると、一貫した液滴パターンを作成することはできません。形成された液滴が衝突する可能性があるため、分析物の交換が発生します。ガス流量の正しい調整は、液滴をICP-MSシステムに確実に輸送するため、およびPNの正しい操作のためにも重要です。提案されたデュアルインレットシステムは、サンプル溶液を手動で変更する必要があるため、現在、測定手順の自動化をサポートしていません。
将来的には、μDGは、複雑なマトリックスや環境サンプル中のNPの特性評価と定量に使用できるようになります。溶液の粘度、複雑さ、表面張力が高いためにμDGが目詰まりするのを防ぐためには、適切なヘッド設計を使用する必要があります。μDGヘッドの設計や電源の動作によっては、標準的な標準物質が全く入手できない細胞、ミセル、脂質キャリアなどの粒子様系を含む液滴を生成することができる場合があります。
開示事項
すべての著者は、利益相反を宣言しません。
謝辞
この研究は、F.L.K.およびP.R.のBfR SFP 1322-642、D.R.のBfR SFP 1322-724、S.A.P.のBfR senior scientist fellowshipの支援を受けました。
資料
| Name | Company | Catalog Number | Comments |
| Au ionic (1000 mg L-1 stock) | VWR, UK | 85550.18E | |
| Ag ionic (1000 mg L-1 stock) | Ultra Scientific, RI, USA | ICM-103 | |
| Ag NP (75nm, NIST 8017) | NIST, Gaithersburg, MD, USA | no longer available | |
| Au NP (60nm, NIST 8013) | NIST, Gaithersburg, MD, USA | no longer available | |
| Ce ionic (1000 mg L-1 stock) | VWR, UK | 85557.18E | |
| CeO2 (10-100nm, NM212) | EU Joint Research Centre | NM212 | |
| Excel 2016 | Microsoft | ||
| Fiji | ImageJ | ||
| Glass female spherical ball + Glass male ball | Fisher Scientific | 12499016 | |
| HCl (emprove bio) | Merck, Germany | 100317 | |
| ICP-MS spray chamber with ipact bead | LabKings | LK6-45013 (OEM 3600170) | |
| Metal clamps for spherical glass joint | Fisher Scientific | 11322015 | |
| Metal T-Piece | Swagelok | SS-4-VCR-T | |
| Microdrop Dispenser Head, non heated | microdrop Technologies | 944 | |
| Microdrop Dispensing System MD-E-3000 | microdrop Technologies | ||
| MilliQ water (MilliPore gradient) | Merck MilliPore, Darmstadt, Germany | ||
| O-ring free quartz torch | Analytical West | 450-301 | |
| PFA-ST concentric nebulizer | Elemental Scientific | ES-2042 | |
| Silicone Rubber Tubing - 60° Shore - Platinum Cured - Black | Silex | ||
| XIMEA Cam Tool | XIMEA |
参考文献
- Linsinger, T. P. J., Peters, R., Weigel, S. International interlaboratory study for sizing and quantification of Ag nanoparticles in food simulants by single-particle ICPMS. Analytical and Bioanalytical Chemistry. 406 (16), 3835-3843 (2014).
- Krystek, P., et al. Method development and inter-laboratory comparison about the determination of titanium from titanium dioxide nanoparticles in tissues by inductively coupled plasma mass spectrometry. Analytical and Bioanalytical Chemistry. 406 (16), 3853-3861 (2014).
- Degueldre, C., Favarger, P. Y., Bitea, C. Zirconia colloid analysis by single particle inductively coupled plasma-mass spectrometry. Analytica Chimica Acta. 518 (1-2), 137-142 (2004).
- Degueldre, C., Favarger, P. Y. Colloid analysis by single particle inductively coupled plasma-mass spectroscopy: a feasibility study. Colloid Surface A. 217 (1-3), 137-142 (2003).
- Pace, H. E., et al. Determining transport efficiency for the purpose of counting and sizing nanoparticles via single particle inductively coupled plasma mass spectrometry. Analytical Chemistry. 83 (24), 9361-9369 (2011).
- Verboket, P. E., Borovinskaya, O., Meyer, N., Gunther, D., Dittrich, P. S. A new microfluidics-based droplet dispenser for ICPMS. Analytical Chemistry. 86 (12), 6012-6018 (2014).
- Shigeta, K., et al. Application of a micro-droplet generator for an ICP-sector field mass spectrometer - optimization and analytical characterization. Journal of Analytical Atomic Spectrometry. 28 (5), 646-656 (2013).
- Gschwind, S., Hagendorfer, H., Frick, D. A., Gunther, D. Mass quantification of nanoparticles by single droplet calibration using inductively coupled plasma mass spectrometry. Analytical Chemistry. 85 (12), 5875-5883 (2013).
- Gschwind, S., et al. Capabilities of inductively coupled plasma mass spectrometry for the detection of nanoparticles carried by monodisperse microdroplets. Journal of Analytical Atomic Spectrometry. 26 (6), 1166-1174 (2011).
- Zarrln, F., K, S. L., Socha, J. R. Droplet size measurements of various nebulizers using differential electrical mobluty particle sizer. Journal of Aerosol Science. 22, 343-346 (1991).
- Geertsen, V., Lemaitre, P., Tabarant, M., Chartier, F. Influence of design and operating parameters of pneumatic concentric nebulizer on micro-flow aerosol characteristics and ICP-MS analytical performances. Journal of Analytical Atomic Spectrometry. 27 (1), 146-158 (2012).
- Mehrabi, K., Günther, D., Gundlach-Graham, A. Single-particle ICP-TOFMS with online microdroplet calibration for the simultaneous quantification of diverse nanoparticles in complex matrices. Environmental Science. Nano. 6, 3349-3358 (2019).
- Ramkorun-Schmidt, B., Pergantis, S. A., Esteban-Fernandez, D., Jakubowski, N., Gunther, D. Investigation of a combined microdroplet generator and pneumatic nebulization system for quantitative determination of metal-containing nanoparticles using ICPMS. Analytical Chemistry. 87 (17), 8687-8694 (2015).
- Rosenkranz, D., et al. Improved validation for single particle ICP-MS analysis using a pneumatic nebulizer/microdroplet generator sample introduction system for multi-mode nanoparticle determination. Analytica Chimica Acta. 1099, 16-25 (2020).
- National Institute of Standards and Technology. Report of investigation reference material. Reference material 8017. National Institute of Standards and Technology. , (2015).
- Tavares, A. M., et al. Genotoxicity evaluation of nanosized titanium dioxide, synthetic amorphous silica and multi-walled carbon nanotubes in human lymphocytes. Toxicology In Vitro. 28 (1), 60-69 (2014).
- Au-Kaur, I., et al. Dispersion of Nanomaterials in Aqueous Media: Towards Protocol Optimization. Journal of Visualized Experiments. (130), e56074(2017).
- Nanotechnologies. Size distribution and concentration of inorganic nanoparticles in aqueous media via single particle inductively coupled plasma mass spectrometry. ISO/TS19590 Nanotechnologies. , (2017).
- Shigeta, K., et al. Application of a micro-droplet generator for an ICP-sector field mass spectrometer - optimization and analytical characterization. Journal of Analytical Atomic Spectrometry. 28, 646-656 (2013).
- Koch, J., et al. Accelerated evaporation of microdroplets at ambient conditions for the on-line analysis of nanoparticles by inductively-coupled plasma mass spectrometry. Journal of Analytical Atomic Spectrometry. 28 (11), 1707-1717 (2013).
- Tuoriniemi, J., Cornelis, G., Hassellov, M. A new peak recognition algorithm for detection of ultra-small nano-particles by single particle ICP-MS using rapid time resolved data acquisition on a sector-field mass spectrometer. Journal of Analytical Atomic Spectrometry. 30 (8), 1723-1729 (2015).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved


