Method Article
重新审视镫骨手术中的显微经管入路
摘要
本文介绍了镫骨手术的显微镜经管技术,提供了分步手术说明,使外科医生熟悉这种方法。
摘要
显微镜经耳道(又名经鼻)手术方法在 60 年代首次被描述,提供了一种到达外耳道、中耳和 epitympanon 的微创手段。这种方法避免了耳后或耳内皮肤切口;然而,在狭窄的空间内工作需要倾斜的显微手术器械和耳科手术方面的特定培训。跨运河方法限制了工作空间;然而,它提供了进入中耳的双眼显微镜视野,而无需延长皮肤切口,从而减少了术后疼痛和出血。此外,这种微创方法避免了瘢痕组织并发症、耳廓感觉减退和耳廓的潜在突出。尽管有许多优点,但耳外科医生仍然不常规使用这种方法。由于这种微创技术更具挑战性,因此需要进行广泛的培训,以便被耳外科医生广泛采用。本文提供了镫骨手术的分步手术说明,并报告了使用这种显微镜经管技术的可能适应症、陷阱和局限性。
引言
1951年耳科手术中双目手术显微镜的出现1为侵入性较小的显微镜经管方法铺平了道路。替代方案是耳内切口或耳后入路,这些方法更具侵入性。罗森早在 1952 年就描述了第一次经管镫骨手术2,3,但当时镫骨是动员而不是移除的。1956年,Shea使用第一个Teflon假肢4彻底改变了镫骨手术。经耳管方法被证明适合这种技术,因为它提供了耳道后部、鼓膜和中耳的良好 3D 可视化。随着时间的推移,经管显微镜方法的适应症已经扩大,涵盖了大量的外科耳科干预措施:鼓室切开术5、鼓室成形术6、7、8、听骨成形术9、窦开术 10、胆脂瘤 11、12、13、鼓室球 14、迷路切除术 15、神经切除术 16,17、经海角入路18、19、20甚至人工耳蜗植入鼻蜗21。
这种具有挑战性的方法需要使用专门的器械进行经管手术(最初描述于60年代)22 和特定的外科培训。它限制了工作空间,但确实提供了进入中耳的双眼显微镜视野,而无需延长皮肤切口,从而减少了术后疼痛和出血。此外,这种微创方法避免了瘢痕组织并发症、耳廓感觉减退和耳廓突出。在本文中,我们提供了镫骨手术的分步手术说明,并报告了使用这种显微镜经管技术的可能适应症、陷阱和局限性。
研究方案
伯尔尼大学(伯尔尼大学)的地方审查委员会批准了本研究,这种类型的回顾性研究不需要正式的知情同意。
1. 适应症
- 如果耳道直径为 ≥5.5 mm,请使用经道入路。
注意:外耳道的解剖结构和形状可能会进一步限制工作空间。 - 通过放置直径为 5 mm 的耳窥器来评估管的直径。确保窥器舒适地放置在运河中。
- 在前缘不可见的前穿孔中,不要使用经管入路。
- 使用由内而外技术11 治疗中耳病变,例如胆脂瘤,其到达半规管以外的 epitympanon 处。
2. 准备
- 患者的定位:将手术台放在最低位置,倾斜在反向特伦德伦堡位置(图1A),头枕的角度(α)处于最大倾斜度(无头垂)。
注意:寰枢椎不稳定患者禁用此体位。最后,将头部朝对侧旋转(β, 图1B)。 - 仪器:使用弯曲的仪器保持工作区域开放。用手指正确握住仪器,从而防止任何视力受阻(图2 和 图3)。
注意:黑色仪器可减少光反射。 - 耳道消毒清洁:彻底清洁耳道,避免术中感染。用稀释的聚维酮碘(毒性为2.5%-5%)消毒运河。
3.局部麻醉
- 分两步进行局部麻醉:
- 将所有四个象限(23 G 针头)与 0.25% (50 mg/20 mL) 的碳骨素与肾上腺素 1 mg/mL(终浓度 1:200,000 肾上腺素)混合。
- 使用弯曲的小 27 G 针头在耳道内注射。在前下区注射时要小心,以避免面部麻痹。
4.鼓膜瓣和窥器支架
- 使用带镰刀的 U 形切口或圆刀从 6' 时钟位置(下前)开始进行鼓膜瓣。用罗森刀拆下耳道皮肤,直到到达下环边缘。
- 安装窥器支架(图4)。
- 插入尽可能大的耳窥器。确保方向正确。
注意:指示窥器大小的字母应放在上方。 - 用贝鲁奇剪刀剪断上后部,完成鼓膜U形瓣。用罗森刀拆下耳道皮肤,直到到达上环边缘。
- 此步骤可能会导致出血。
- 使用浸有肾上腺素的可吸收明胶海绵止血。
- 拆下整个翻盖,直到环形的边缘。
5.中耳夹层
- 在进入中耳之前,请确保面神经监测正常工作。
注意:患者应已从任何神经肌肉阻滞中恢复,这可以通过神经肌肉监测(4 TOF,四列)进行评估。 - 进入环后上部的中耳,因为在这个位置更容易分离。
注意:中耳听小骨周围的大胆脂瘤或肉芽组织可能会隐藏任何解剖标志。在这种情况下,建议中耳后下进入以找到其他标志(CAVE:颈静脉球)。 - 解剖并可视化解剖学中耳结构。可视化鼓索、海角、髫骨关节、镫骨肌腱和面神经(鼓膜段)。
- 如果上述任何结构未充分暴露,则用刮匙或 2 mm 金刚石粗钻(低速)加宽耳道后上部。在中耳中放入可吸收的明胶海绵,以防止骨尘进入中耳。
6. 镫骨上结构去除
- 用0.3-0.6毫米的小钩子或镰刀断开内髶关节,并向前运动以防止脚踏板断裂。
- 通过用针头触摸每个听小骨来测试所有三个听小骨的活动性,以确认镫骨的孤立性强直。
- 使用集成在显微镜中的防护眼镜或滤光片。
- 用激光(例如二极管激光、CO2 激光)解剖镫骨肌腱。在此过程中测试激光的强度。在脉冲模式(30-50 ms)下使用能量为 2.5-3 W 的 FOX 激光器;但是,此值取决于设备及其探测器。
- 如果脚踏板活动性太强,则解剖脚踏板±前胭关节附件附近的镫骨后痂。
- 移除镫骨上层结构。如果前痂仍然完好无损,则将镫骨从面神经制动到海角。保持踏板完好无损。
注意: 踏板在破坏上部结构时不应移动。在此过程中存在脚踏板纵向骨折的风险。
7. 踏板穿孔
- 使用 FOX 激光器通过制作玫瑰花图案来碳化/削弱踏板(2 W,30 ms 脉冲模式)。
- 使用穿孔器微钻(0.6 mm)在后第三部分对踏板的最后一个壳进行穿孔。
- 如果踏板太厚,请使用金刚石微钻使踏板变薄,直到可见蓝色闪光结构(也称为蓝色衬里)。
- 一旦脚踏板打开,请勿在踏板区域使用吸力。
8.镫骨假体插入
- 使用带有 4 毫米测量标记的测量仪器测量窦肌和脚踏板的长过程之间的距离。使用比测量值长 0.25 毫米的假肢。
- 插入前,使用小鳄鱼耳钳握住假体钩,使用预定义的方向角度 (~20°)。
- 将镫骨钩压在长长的镫骨过程上。
注意: 压接仪器的前齿移动,而后齿在内砌上保持稳定。 - 通过移动锤柄来检查假体的运动。
- 避免假体接触海角或面神经。
- 如果假体和烽肌过程之间存在相互作用,请考虑使用耳科骨水泥。
- 避免过度卷曲,因为长期存在矽肌坏死的风险。
- 用小的水浸泡可吸收明胶海绵密封穿孔的脚踏板。
9. 伤口闭合/敷料
- 重新定位鼓膜瓣,用真丝敷料适应,并用浸泡氢化可的松10mg(1%)/新霉素3.5mg/硫酸多粘菌素B溶液10,000单位的可吸收明胶海绵包装。
- 使用浸有相同溶液的 10 厘米带状纱布进行耳道包装。
结果
我们在此对66名年龄在9-68岁(平均46.3y,SD ±13.4y)接受镫骨手术(48例标准手术,18例修订,表1和表2)的患者(37名男性,29名女性)进行了回顾性横断面分析(2018年1月至2021年5月)。所有患者均由同一位外科医生(GM)手术。仪器弯曲且呈黑色(图3)。平均窥器尺寸为6.1毫米(范围5-8毫米,n = 51,图2),可以充分观察操作区域。66例中只有1例需要耳后切口(9岁儿童,管径<5毫米)。66例患者中有37例需要进行后管成形术。图2说明了如何用前三个指尖握住弯曲的器械,同时用剩下的两个手指将手稳定在患者的窥器或头部。窥器支架由安装在手术台上的移动扩展件组成(图4)。光暴露是有限的,需要通过显微镜和倾斜仪器的位置进行调整(图5)。坐着外科医生的测力位置和优化的手的角度(图6)可实现稳定的显微手术性能。58名患者接受了Richards活塞假体,1名患者接受了Matrix Slim Line KURZ假体,5名患者接受了malleo-vestibulo-pexy(MVP)假体(球形关节假体)。假体的平均尺寸为4.4毫米(范围4-5毫米,SD±0.2毫米),平均直径为0.46毫米(范围0.4-0.6毫米,SD±0.08毫米,表1)。在66例病例中,有33例还用耳科水泥固定了假体。在65例病例中,有55例保留了鼓弦鼓膜。
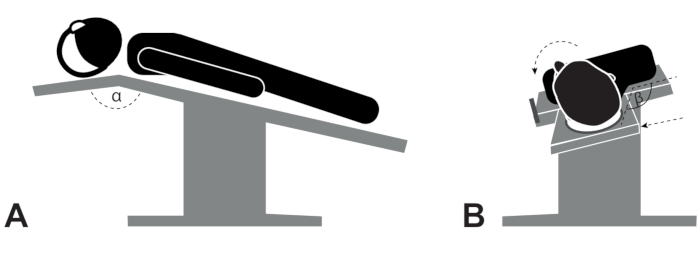
图1:患者的定位 。 (A)最低位置的操作台倾斜在反向特伦德伦堡位置。(B)头部/身体以侧卧姿势向健康耳朵旋转。 请点击此处查看此图的大图。
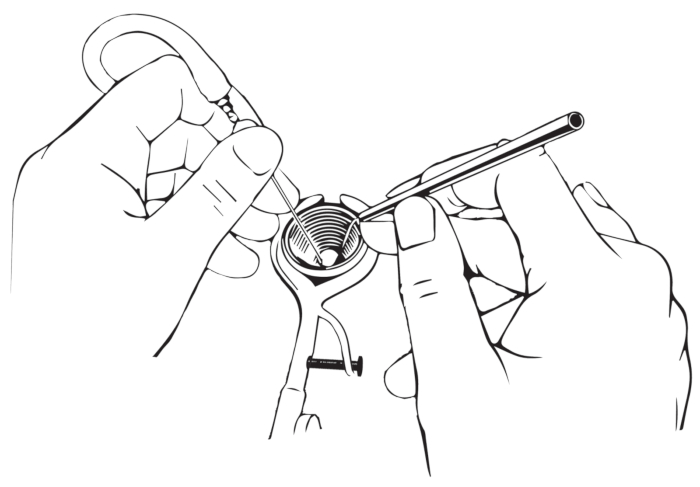
图 2:如何握持仪器。 乐器必须像铅笔一样握住;无名指应支撑在窥器边缘。 请点击此处查看此图的大图。

图3:用于经管显微方法的弯曲仪器。 该图显示了弯曲的器械,例如钩子、吸力器或耳窥器(从左到右)。 请点击此处查看此图的大图。
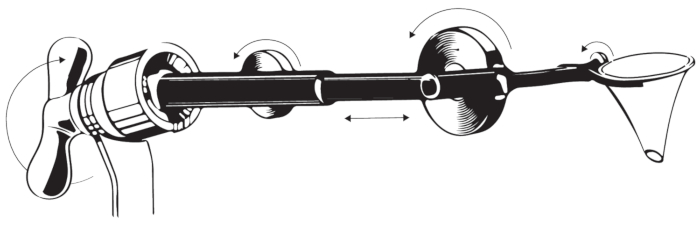
图 4:耳窥器支架。 该图说明了窥器支架的设计。 请点击此处查看此图的大图。
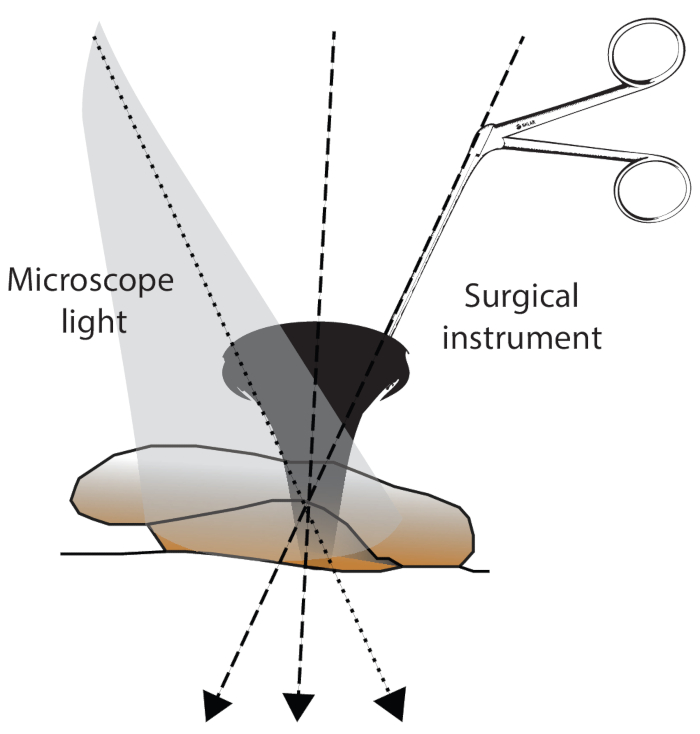
图5:手术视野暴露。 手术视野的暴露可能受到以下因素的影响:1)显微镜光线的角度,2)引入的器械的角度,以及3)耳道/头部位置的角度。 请点击此处查看此图的大图。
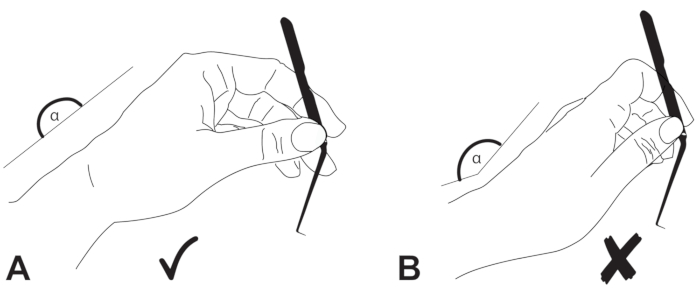
图 6:手的位置。 外科医生的手腕应处于(A)中立位置和(B)不伸展。 请点击此处查看此图的大图。
表1:研究摘要。该表总结了患者和操作特点 请点击这里下载此表格。
表2:患者和操作特征。该表显示了个别患者的详细信息和操作特征。 请按此下载此表格。
讨论
本文提供了有关镫骨手术经管显微镜方法的详细内幕信息。我们可以证明,在大多数情况下,使用锁孔技术进行显微手术是可行的,避免耳后或耳内切口。
然而,要实现成功的手术,必须满足一些先决条件。解剖器应该是弯曲的。刀、钩和针的角度(图1)以改善如此狭窄空间中的可视化和光线条件22。此外,仪器应为黑色,避免任何微观光反射。由于耳道是弯曲的,因此患者定位对于经管入路至关重要,并且显微镜的光束必须与耳道的纵轴完全对齐(图2)。此外,正确握住器械(图3)并保持合适的手部人体工程学姿势(图5)对于成功的经管手术至关重要。
如图3所示,窥器支架允许双手技术和直通鼓膜/中耳的路径。窥器还可以作为仪器指南。最后,应调整和优化手指/仪器的角度和显微镜光线的角度。鉴于所有这些参数,需要对经输管耳科手术进行广泛的培训,以提高手术性能。
替代方法包括耳内和耳后切口或内镜经管切路。对于无法接近的鼓膜前穿孔或次全穿孔,建议使用耳后切口。然而,只要耳道直径足够大(>5毫米),这种情况仍可以通过内窥镜方法23进入。如果需要打开乳突腔,耳后入路仍然是金标准。对于胆脂瘤联合手术(经鼻道和耳后经乳突入路),我们推荐由内而外的技术,该技术首先由Roth和Häusler11描述。该技术建议作为第一步,经管进入中耳,通过上膜切除术识别疾病扩展(胆脂瘤)后的所有解剖结构。作为第二步,如果根据胆脂瘤的延伸指示经乳突通路,则可能会进行耳后切口。这种两步法具有相当大的优势,因为基于疾病的有限扩展,有不可忽视的比例的患者不需要耳后切口(第二步)。
经管内镜方法使用相同的通路途径,并且也限制在耳道直径为 >5 mm。同样,这种方法是微创的,并提供更近的解剖结构广角视图。此外,内窥镜方法提供 45° 或 70° 的倾斜视图,这对于去除鼓室后24、阁楼区域 25 或前穿孔23 的胆脂瘤很有价值。在胆脂瘤手术中,与上述由内而外的技术类似,进行经管内镜下胆脂瘤切除术,然后根据需要从乳突中清除疾病。在这种情况下,最近描述了使用恒定抽吸骨钻孔技术的新型独家内窥镜技术26。然而,内窥镜手术是一种单手技术,在伴有出血的发炎情况下具有挑战性。因此,出血的管理在中耳的内窥镜入路中起着关键作用27。此外,内窥镜检查提供的景深有限,因为它不提供双目视图。新的3D内窥镜可能会改善景深28;但是,这种内窥镜的直径较大,为4毫米。
与耳后入路相比,显微镜下经管入路是微创的,具有避免耳后疼痛、瘢痕组织并发症、耳廓感觉减退和耳突出等优点。
经运河方法也有局限性。主要限制是耳道的直径,应至少为5毫米。任何没有直接或有限通过鼻道的疾病都不适合单独经管入路。该方法可以通过使用内窥镜或经乳突通路组合来扩展。
经管/经肉道显微方法已被证明已有70多年的历史;然而,尽管这种微创方法具有优势,但耳科医生仍然不常规使用这种方法。由于这种微创技术的性能更加困难和具有挑战性,因此需要进行广泛的培训,以促进耳外科医生的使用。这个说明性的教学视频提供了一个额外的工具,让耳科医生熟悉这种手术技术。
披露声明
L.A.是Stryker ENT的顾问。其他调查人员没有任何相关的经济利益、活动、关系或隶属关系,代表与这项工作相关的财务利益冲突。
致谢
GM得到了瑞士国家科学基金会#320030_173081的支持。
材料
| Name | Company | Catalog Number | Comments |
| Adrenalin | Sintetica | ||
| Belucci microscissors | Olympus (former Richards) | 8178100FX | |
| Betadine solution (Povidon iodine) | Mundipharma Medical Company | ||
| Carbostesin | Sintetica | Bupivacain 2.5 mg/mL | |
| Cup forceps | Olympus (former Richards) | ||
| Curette | Olympus (former Richards) | 13-0147 | |
| Curved suction tubes | Spiggle & Theis | 302007NV und6066500100 | |
| Drill | Bienair | 2 mm rough diamond drill | |
| FOX laser | A.R.C. Laser GmbH | ||
| Gelfoam (absorbable gelatine compressed sponge) | Pfizer Injectables | GS-010DP | absorbable gelatin sponge |
| Gloves | Sempermed | Appropriate size | |
| Hooks | Olympus (former Richards) | 13-0201, 13-0202, 13-0204, 13-0206 | 0.3–0.6 mm |
| Hydrocortison/neomycin/polymyxin otic /Cortisporin Otic Solution | Pfizer | ||
| Needle | Olympus (former Richards) | 13-0207 | 27 G |
| Operating Microscope | Leica | E 114637 | |
| Otologic dissectors | Olympus (former Richards) | ||
| Ribbon gauze | |||
| Round knifes | Olympus (former Richards) | 13-0211 13-0212 | |
| Silk dressing | Otosilk | ||
| Speculum | Olympus (former Richards) | OK 082R | |
| Surgical Mask | Halyard | 48247 | |
| Water to rinse | Ringer |
参考文献
- Mudry, A. The history of the microscope for use in ear surgery. Otology & Neurotology. 21 (6), 877-886 (2000).
- Rosen, S. The development of stapes surgery after five years: Mobilization-Fenestra Ovalis. AMA Archives of Otolaryngology. 67 (2), 129-141 (1958).
- Rosen, S., Bergmant, M. Improved hearing after mobilization of the stapes in otosclerotic deafness. The Journal of Laryngology & Otology. 69 (5), 297-308 (1955).
- Nazarian, R., McElveen, J. T., Eshraghi, A. A. History of otosclerosis and stapes surgery. Otolaryngologic Clinics of North America. 51 (2), 275-290 (2018).
- Jackson, M. Transmeatal tympanotomy. South African Medical Journal. 34, 983-984 (1960).
- Austin, D. F. Transcanal tympanoplasty. Otolaryngologic Clinics of North America. 5 (1), 127-143 (1972).
- de Savornin Lohman, E. A. J., Borgstein, J. Transmeatal tympanoplasty of subtotal and anterior perforations: a single-institution experience including 94 patients. Clinical Otolaryngology: Official Journal of ENT- UK; Official Journal of Netherlands Society for Oto-Rhino-Laryngology & Cervico-Facial Surgery. 42 (4), 920-923 (2017).
- Seidman, M. D. Anterior transcanal tympanoplasty: A novel technique to repair anterior perforations. Otolaryngology-Head and Neck Surgery: Official Journal of American Academy of Otolaryngology- Head and Neck Surgery. 138 (2), 242-245 (2008).
- Aslan, A., Tanyeri Toker, G., Ozgur, E. Transcanal approach for Type 2 tympanoplasty with incus interposition ossiculoplasty: Our experience on 134 patients. Clinical Otolaryngology. 43 (4), 1135-1139 (2018).
- Holt, J. J. Transcanal antrotomy. Laryngoscope. 118 (11), 2036-2039 (2008).
- Roth, T. N., Haeusler, R. Inside-out technique cholesteatoma surgery: a retrospective long-term analysis of 604 operated ears between 1992 and 2006. Otology & Neurotology: Official Publication of the American Otological Society, American Neurotology Socient [and] European Academy of Otology and Neurotology. 30 (1), 59-63 (2009).
- Roth, T. N., Ziglinas, P., Haeusler, R., Caversaccio, M. D. Cholesteatoma surgery in children: long-term results of the inside-out technique. International Journal of Pediatric Otorhinolaryngology. 77 (5), 843-846 (2013).
- Shah, N. Cholesteatoma surgery; transcanal approach. Advances in Oto-Rhino-Laryngology. 29, 216-223 (1983).
- Cannon, S. J. Glomus tympanicum removal by transmeatal approach. Laryngoscope. 72, 193-200 (1962).
- Gacek, R. R. Transcanal labyrinthectomy. Laryngoscope. 88 (10), 1707-1708 (1978).
- Jones, R., Silverstein, H., Smouha, E. Long-term results of transmeatal cochleovestibular neurectomy: an analysis of 100 cases. Otolaryngology-Head and Neck Surgery: Official Journal of American Academy of Otolaryngology- Head and Neck Surgery. 100 (1), 22-29 (1989).
- Kos, M. I., et al. Transcanal approach to the singular nerve. Otology & Neurotology. 27 (4), 542-546 (2006).
- Isaacson, B., Tolisano, A. M., Patel, A. R., Barnett, S. L. Transcanal microscopic transpromontorial approach for vestibular schwannoma. Journal of Neurological Surgery, Part B: Skull Base. 80, 279-280 (2019).
- Mazzoni, A., et al. Transmeatal microsurgery for intralabyrinthine and intrameatal schwannomas: a reappraisal. Acta Otorhinolaryngologica Italica. 40 (5), 390-395 (2020).
- Presutti, L., et al. Expanded transcanal transpromontorial approach to the internal auditory canal: Pilot clinical experience. Laryngoscope. 127 (11), 2608-2614 (2017).
- Kiratzidis, T., Arnold, W., Iliades, T. Veria operation updated. I. The trans-canal wall cochlear implantation. ORL; Journal for Oto-Rhino-Laryngology and its Related Specialties. 64 (6), 406-412 (2002).
- Dworacek, H. Instruments for transmeatal middle ear surgery. AMA Archives of Otolaryngology. 70, 510-511 (1959).
- Tseng, C. C., Lai, M. T., Wu, C. C., Yuan, S. P., Ding, Y. F. Endoscopic transcanal myringoplasty for anterior perforations of the tympanic membrane. JAMA Otolaryngology-Head & Neck Surgery. 142 (11), 1088-1093 (2016).
- Bonali, M., et al. Correlation of radiologic versus endoscopic visualization of the middle ear: implications for endoscopic ear surgery. Otology & Neurotology. 41 (9), 1122-1127 (2020).
- Presutti, L., et al. The impact of the transcanal endoscopic approach and mastoid preservation on recurrence of primary acquired attic cholesteatoma. Otology & Neurotology. 39 (4), 445-450 (2018).
- Gao, Z., Jia, X. H., Yuan, Y. S. Endaural endoscopic atticoantrotomy (retrograde mastoidectomy) using a constant suction bone-drilling technique. Journal of Visualized Experiments: JoVE. (171), e62450(2021).
- Anschuetz, L., et al. Management of bleeding in exclusive endoscopic ear surgery: Pilot clinical experience. Otolaryngology-Head and Neck Surgery. 157 (4), 700-706 (2017).
- Molinari, G., et al. Surgical implications of 3D vs 2D endoscopic ear surgery: a case-control study. European Archives of Oto-Rhino-Laryngology. 277 (12), 3323-3330 (2020).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。