Method Article
哺乳动物细胞 原位 冷冻断层扫描的样品制备
摘要
该方法为原 位 细胞冷冻断层扫描和相关光电子显微镜 (CLEM) 的电子显微镜 (EM) 网格的制备提供了一种可访问且灵活的协议。
摘要
原位 细胞冷冻断层扫描是一种强大的技术,用于在天然冷冻水合细胞环境中研究复杂物体,使其与细胞生物学和病毒学高度相关。将冷冻断层扫描与其他显微镜模式相结合的潜力使其成为综合和相关成像的完美技术。然而,原 位 细胞断层扫描的样品制备并不简单,因为细胞不容易附着在电子显微镜网格上并拉伸。此外,网格本身很脆弱,如果处理得太用力,可能会破裂,从而导致可成像区域的丢失。当用镊子操纵网格时,组织培养皿的几何形状也会带来挑战。在这里,我们描述了克服这些(和其他)挑战的技巧和窍门,并为贴壁哺乳动物细胞的 原位 细胞冷冻断层扫描和相关成像制备高质量的样品。随着冷冻显微镜技术的不断进步,这项技术在促进我们对复杂生物系统的理解方面具有巨大的前景。
引言
原位细胞冷冻断层扫描是一种强大的技术,无需化学固定即可研究细胞中的生物学相关结构。通过将细胞连接到EM网格并在制冷剂中对网格进行浸入冷冻,感兴趣的物体在其自然细胞环境中被冷冻,而不会从细胞内水中形成结晶冰1,2。化学固定和结晶冰的形成都会破坏相关分子的结构,例如蛋白质和脂质,从而降低使用这些技术获得的图像的生物学准确性3,4。在断层扫描中,使用电子显微镜以增量角度对网格进行成像,然后使用这些图像来构建成像的目标区域的三维表示5。原位冷冻断层扫描可与其他显微镜技术一起用于综合和相关成像,例如冷冻荧光成像、软 X 射线断层扫描和 cryoFIB/SEM(低温聚焦离子束/扫描电子显微镜)6,7,8,9,10,11 .与任何单一显微镜技术相比,集成多种技术可以获得更多关于结构或过程的信息。
尽管原 位 细胞冷冻断层扫描具有所有优点,但由于各种原因,样品制备可能具有挑战性。由于它们的脆弱性,强行操纵电子显微镜网格会导致损坏,特别是薄碳层很脆弱,容易撕裂,从而减小网格的可成像面积。由于尺寸小,电子显微镜网格也难以操作,并且容易与用于生长细胞的孔或微载玻片表面分离。由于井或微载玻片的几何形状,操作这些网格可能很困难。网格准备不当(例如,允许它们漂浮)会导致细胞密度低并减少潜在成像区域的数量,特别是当细胞不容易附着在网格本身时。对于直接细胞冷冻断层扫描,细胞必须扩散得非常薄,这可能会因多种原因而中断,包括温度不当或网格处理粗糙。
通过各种优化,本文介绍的技术旨在处理在制备冷冻断层扫描电子显微镜网格时出现的这些最常见的陷阱。使用 5/15 角镊子可以操纵孔板或微载玻片内的网格。在电镀前将纤连蛋白溶液涂在网格的两侧,可降低浮动网格的可能性,这有利于确保网格具有足够的细胞密度,并且网格不太可能因操作而损坏。通过将网格保持在 37°C 下孵育直到冷冻前,我们还确保细胞保持在舒适的环境中,以防止细胞缩回其薄边缘。从背面吸干网格还可以防止机械力对细胞的损坏。总之,这些措施提高了原 位 细胞冷冻断层扫描研究样品制备的成功率,增加了这种成像方法的可及性。
研究方案
1. 电网准备
注:在实验设计中,计划每次浸入冷冻期间最多 8-12 个网格,每孔最多 4-5 个网格。超过此值将导致非常长的冷冻过程,这可能会导致细胞压力增加、冰污染和用户错误。
- 辉光放电
- 在辉光放电装置中,用穿孔碳支撑膜加载适当数量的网格,以 15 mA 的电流在 0.39 mBar 气氛下以 0.39 毫秒的电流进行辉光放电。
- 确保电网的碳面朝上。完成后,将网格转移到衬有滤纸的干净容器中(图1A1)。
注意:只要材料对电池无毒(不包括任何铜网格),就可以使用其他网格。Finder 网格对于关联研究非常有用。也可以使用其他材料制成的网格。许多实验室在 SiO2 支持网格 8,9 上生长细胞取得了良好的结果。
- 依从性治疗
- 将网格、纤连蛋白、PBS、板和镊子转移到生物安全柜中。通过在无菌表面(例如 6 孔板的盖子)上微量移液两个大大小的贴壁溶液点,用 20 μg/mL 牛纤连蛋白处理网格的两侧。确保点足够大以包裹整个网格(建议约 100 μL)。
注:在用选定的贴壁溶液处理之前,可以选择在此处对网格进行光微图案化,以优化网格正方形中心细胞的附着。降低单元格附着到条形图的能力将增加可成像单元格的数量。这是涉及冷冻FIB研磨的实验的理想选择。 - 使用 5/15 镊子操作网格。确保在溶液中处理网格的两侧。
注意:可以使用其他粘合剂溶液(纤维蛋白原、胶原蛋白、其他细胞外基质成分等)。这里使用纤连蛋白,因为它在多种细胞系中都能获得良好的结果。(U2OS、HeLa、Vero、Calu-3、Tzm-bl)。5/15 镊子非常有用,因为它的几何形状可以提高 6 孔板、35 mm 培养皿和微型载玻片周围的可操作性。这样可以减少网格上的机械应力,并形成更完整的碳膜。确保在开始之前将所有必需的材料都放在生物安全柜中,因为这样可以减少网格污染的可能性。
- 将网格、纤连蛋白、PBS、板和镊子转移到生物安全柜中。通过在无菌表面(例如 6 孔板的盖子)上微量移液两个大大小的贴壁溶液点,用 20 μg/mL 牛纤连蛋白处理网格的两侧。确保点足够大以包裹整个网格(建议约 100 μL)。
- 附加网格
- 一旦用牛纤连蛋白处理,网格就会变得粘稠。使用 5/15 镊子,将网格的非碳表面轻轻接触空盘/盘子的底部,然后打开镊子。网格应易于附着在新表面上(图1A2)。
注意: 尽量避免将网格放在盘子/盘子的直接中心或边缘。添加细胞时,细胞密度有在板中心积聚的趋势。这可能导致网格具有过高的细胞密度。或者,这里可以使用3D打印的网格支架,而不是将细胞直接连接到培养皿/板12的表面。
- 一旦用牛纤连蛋白处理,网格就会变得粘稠。使用 5/15 镊子,将网格的非碳表面轻轻接触空盘/盘子的底部,然后打开镊子。网格应易于附着在新表面上(图1A2)。
- 孵化
- 将网格在纤连蛋白贴壁溶液(20μg/ mL)中孵育30分钟。为确保网格在此过程中不会变干,每15分钟将1-2滴更粘附的溶液直接滴在网格顶部(图1A3)。
注意:孵育期将根据所使用的贴壁溶液而有所不同。对于牛纤连蛋白,推荐时间为 30 分钟。
- 将网格在纤连蛋白贴壁溶液(20μg/ mL)中孵育30分钟。为确保网格在此过程中不会变干,每15分钟将1-2滴更粘附的溶液直接滴在网格顶部(图1A3)。
- 洗涤
- 孵育期过后,通过微量移液去除多余的粘附溶液。通过将PBS滴微量移液液直接在网格顶部来清洗网格。重复此操作 2-3 次。(图 1A4)。
- 灭菌
- 使用紫外线对生物安全柜中的网格进行消毒1小时。将网格放置在尽可能靠近紫外线源的位置,以最大限度地提高灭菌效果(图1A5)。为确保网格在此过程中不会变干,每 10 分钟将 1-2 滴 PBS 直接滴在网格顶部。
注意:步骤 1.4-1.6 可以同时执行。
- 使用紫外线对生物安全柜中的网格进行消毒1小时。将网格放置在尽可能靠近紫外线源的位置,以最大限度地提高灭菌效果(图1A5)。为确保网格在此过程中不会变干,每 10 分钟将 1-2 滴 PBS 直接滴在网格顶部。
2. 播种网格
- 细胞计数:
- 使用机械或酶法分离和计数细胞。在计数之前确定用于接种的最佳细胞数。对于接种在 6 孔板中的 U2OS,每孔使用 6 x 104 至 1.6 x 105 个细胞之间的任意位置(图 1B1)。
注:接种的细胞数量将根据细胞类型、孔的表面积、使用的培养皿或微载玻片、接种和浸入冷冻之间的时间以及实验设计而变化。测试一系列细胞数量,以确定在骤降冻结时将导致每个网格方块产生 0.25-1 个细胞的条件。需要注意的是,高细胞密度会降低传热速度,并可能影响玻璃化过程。为了解决这个问题,一些实验室已经发现使用细胞过滤器取得了成功,这种过滤器的作用是防止细胞团块形成13。最后,该协议导致细胞随机附着在碳层上。如果需要有针对性的附件,可以使用光微图案化(参见步骤 1.3)14。
- 使用机械或酶法分离和计数细胞。在计数之前确定用于接种的最佳细胞数。对于接种在 6 孔板中的 U2OS,每孔使用 6 x 104 至 1.6 x 105 个细胞之间的任意位置(图 1B1)。
- 添加细胞和生长培养基:通过微量移液管将细胞添加到孔中,避免气泡(图1B2)。在 6 孔板中,建议总孔体积为 1.5-2.0 mL。
注意: 建议在添加整个体积之前小心地弄湿网格周围。这将有助于防止网格在溶液中分离和浮动。轻轻地左右移动板,以促进孔上的细胞均匀分布。不要以圆周运动旋转板,因为这会导致孔中心分配过多的细胞密度。 - 孵育:根据实验设计,将载玻片在37°C下孵育适当的时间,这将取决于下游应用。对于本例(HIV分子克隆的转染),孵育16-24小时(图1B3)。
注意:较长的孵育时间将导致更多的细胞分裂周期。因此,请相应地调整接种的细胞起始数量。
3. 转染
- 制备转染混合物:
- 制备适当的阳离子脂质体试剂,用于将质粒转染到所选细胞系中。
- 在该转染示例中,每孔(在 6 孔板中)使用 1 μg 总质粒 DNA,以 1:3 的比例转染 HIViΔEnv 质粒与 psPAX2 质粒。对于每个孔,将 1 μg DNA 稀释到 50 μL 无血清 DMEM 中。通过反复微量移液或轻轻旋转板来匀浆混合物。
- 对于每个孔,在无血清DMEM中稀释3μL转染试剂,然后通过微量移液或轻轻旋转再次匀浆混合物。将整个稀释的转染试剂混合物加入稀释的DNA混合物中(步骤3.1.2),并在室温(RT)下孵育15分钟(图1C1)。
注意:当该混合物孵育时,用 1.5 mL 新鲜 DMEM 替换孔中的培养基。小心不要将格栅从井底移开。
- 为了应用转染混合物,将步骤3.1.3中的100μL混合物逐滴移液到每个孔中,将液滴集中在网格上以确保接触(图1C2)。转染后16-24小时更换生长培养基(图1C3)。
4.骤降冻结
注意:将细胞保持在37°C,直到需要印迹。此外,在整个过程中,请务必记下电网的碳侧。
- 细胞密度
- 在倒置光学显微镜中检查网格,并注意每个网格上的细胞密度。
注意:每个网格方块少于 0.25 个单元格(或每 4 个网格方块一个单元格)的网格被视为“空”。每个网格方格有 0.25-1 个像元的网格被认为是“正常”的。每个格子方块具有 1 个以上像元的格网被视为“已满”。 - 记下每个网格上的细胞密度,以便在速冻期间稍后调整印迹时间。将2-3mL PBS加入空板/培养皿中,并加热至37°C。
- 在倒置光学显微镜中检查网格,并注意每个网格上的细胞密度。
- 准备基准点
- 为了制备用于下游冷冻断层扫描应用的金基准点,将 50 μL 10 nm 胶体金珠溶液移液到干净的 1.5 mL 试管中。向试管中加入 2 μL 1 mg/mL BSA,并通过反复微量移液匀浆。
- 将试管以15,000-20,000× g 离心15分钟。微量移液器在不干扰沉淀的情况下尽可能多地去除上清液。
注意:颗粒会非常松散。 - 向沉淀中加入 50 μL PBS 并重悬。再次以15,000-20,000× g 离心管15分钟。
- 使用 10 μL 吸头,直接吸出 4 μL 沉淀,并将其转移到干净的 1.5 mL 管中(图 1D1)。每个网格使用 1 μL 洗涤和浓缩的金。
注意:使用的基准点类型取决于下游应用。对于 TEM 断层扫描,请使用 10 nm 金珠。对于软 X 射线断层扫描,请使用 200 nm 金珠。对于相关显微镜检查,请使用荧光乳胶珠。对于涉及冷冻FIB研磨的实验,基准点通常不是必需的,因为研磨过程会破坏它们。
- 杂交
- 将环境室设置为95%的湿度和30°C(图1D1)。使用 5/15 镊子选择网格。
- 用PBS清洗网格并将它们转移到插入镊子上(图1D2)。固定后,取出 5/15 镊子并滑动夹子amp 在插入镊子上。
- 将网格插入切入式冷冻机,保持夹子牢固(图 1D3)。向网格的背面加入1μL金基准点(图1D4)。将 2-3 μL PBS 添加到网格的碳侧。使用自动印迹法印迹网格的背面,并将冷冻液浸入液态乙烷中(图1D5)。
注:建议每个网格的体积在 3-4 μL 之间,以获得最佳印迹效果。洗涤后,网格可能会保留不同量的 PBS。调整增加的 PBS 体积,以考虑网格上预先存在的液体潴留。建议将黄金基准点添加到网格的背面。在前面加法会导致在插入点附近产生金基准点池,而从后面加法会导致更均匀的解决方案。印迹持续时间取决于网格的细胞牙科。空格格分别为 2 秒、正常格栅为 3 秒、全格格为 4 秒。可用的速冻仪类型可能决定了印迹的方法:徕卡GP2速冻仪是该协议中使用的速冻机,默认情况下能够进行自动单面印迹。Thermo Fisher Vitrobot 可进行自动双面印迹,但这通常会损坏附着在碳侧的细胞。也可以在 Vitrobot 中进行手动印迹,也可以使用手动重力柱塞。
结果
在HIViGFPΔEnv和psPAX2共转染后,所有网格在碳层中的撕裂最小。在与转染试剂孵育 24 小时后,使用相光显微镜和荧光显微镜对网格进行成像(图 2)。模拟网格和共转染网格上的细胞在多个网格方块中都包含活细胞。
psPAX2 编码 HIV-1 的所有结构蛋白和酶蛋白,无需任何荧光标记。HIViGFPΔEnv 与 psPAX2 相似,但具有 GFP 标记的 HIV Gag 蛋白的代码。两种质粒都是ΔEnvelope。共转染导致荧光 HIV-1 颗粒的天然样组装和出芽,使其成为在生物安全 1 级条件下进行 HIV CLEM 研究的绝佳系统。共转染网格显示一部分细胞表现出绿色荧光,表明共转染成功。模拟网格上没有细胞表现出荧光,进一步验证了使用 HIViGFPΔEnv 和 psPAX2 的共转染。使用基于光学的显微镜观察网格后,将网格冷冻并移至液氮中长期储存。
图 3 描述了使用相同实验方法但使用略有不同的质粒构建体产生的网格的结果。使用不同的HIV克隆(HIVmCherryΔEnv和NL4-3ΔEnvGFP)以1:6的比例共转染含U2OS的网格。由于使用了更高质量量的荧光标记质粒,这些网格能够观察到更多的转染细胞,在使用 cryoCLEM 和 cryoET 捕获图像时具有优势。使用 cryoCLEM,使用冷冻荧光显微镜为每个网格生成完整的网格图谱,以记录所有共转染细胞的位置。在已知细胞位置的情况下,进行冷冻ET。收集完整的低倍率网格图谱,并与冷冻荧光时收集的荧光图谱叠加(图3A)。在细胞位点收集冷冻造影,捕捉病毒生命周期的复杂细节,包括HIV从细胞中组装和出芽(图3B)。
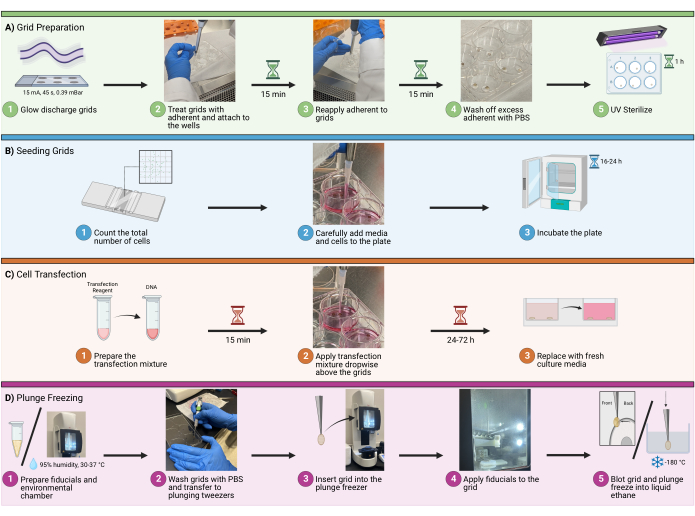
图 1:网格上的单元格播种工作流程。 在冷冻电镜网格上接种细胞的整个过程的示意图。该过程分为四个主要步骤,包括 (A) 在孔中制备用于接种的网格,(B) 向每个孔中添加适量的细胞,(C) 可选的细胞转染用于荧光成像,以及 (D) 网格的浸入冷冻以允许样品的玻璃化。 请点击这里查看此图的较大版本.

图 2:使用 HIViGFPΔEnv 和 psPAX2 共转染 U2OS。 U2OS 细胞与含 GFP 的 HIViGFPΔEnv 和 psPAX2 以 1:3 的比例共转染。通过相差和荧光显微镜对网格进行成像。显示具有GFP表达的细胞表明共转染成功。比例尺:500μm。比例尺(插图):100 μm。 请点击这里查看此图的较大版本.
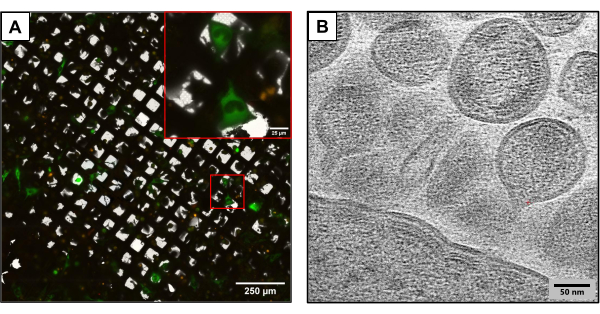
图 3:潜在的下游基于冷冻的方法 。 (A) 共转染 U2OS 细胞的 cryoCLEM 图像。绿色细胞代表产生HIV的细胞,用于测量共转染成功。红色点状物代表 mCherry 标记的 HIV-1 Gag。比例尺:250μm。比例尺(插图):25 μm (B) 从 U2OS 细胞质膜萌芽的多个 HIV 颗粒的冷冻 ET 图像。比例尺:50纳米 请点击这里查看此图的较大版本.
讨论
在这里,我们提供了一种可访问、灵活且可重复的方案,用于在原 位 冷冻电子断层扫描应用中的电子显微镜网格上接种细胞。该方法可以很容易地适应下游应用和/或实验要求的需求。除了极大的灵活性外,我们还描述了一种工作流程,该工作流程可以优化和减少网格接种中的常见缺陷,特别是对碳层的广泛破坏、低细胞密度和薄细胞突起的结构完整性差。
尽管此处描述的协议确实提供了几种替代方案,但应遵循一些关键步骤来优化一般结果。网格细胞接种的最大问题之一是网格从孔或微载玻片上分离和漂浮。因此,重要的是在两侧用粘附溶液完全润湿网格,并防止其在孵育期间干燥。如果使用 3D 打印的网格支架,请注意,对这些支架进行多次介质更换可能会产生浮动网格,因为被困在网格下方的空气会迫使其离开支架。
我们选择的镊子还提高了网格质量,因为它提供了一种几何上有利的方法来操纵网格,而不会造成会损坏碳层的大量网格弯曲。在坠入之前,将细胞保持在37°C下尽可能长的时间可以减少细胞的痛苦,并改善网格上薄的可成像细胞的数量。最后,从金侧进行印迹将保护细胞免受可能导致脆弱细胞结构受损的苛刻机械力的影响。
虽然不包括在该协议中,但网格光微图案化已被证明通过优化可成像细胞与网格方块14中心的附着来增加可成像细胞的数量。最后,3D打印的网格支架最近被用于通过限制直接的网格操作来减少网格损坏12。
需要注意的是,该协议针对细胞的薄边缘和突起的成像进行了优化,用于冷冻断层扫描的应用。我们建议根据协议中的建议对各种情况进行故障排除,以便为所选的下游应用找到最佳结果。总体而言,该协议提供了一种可靠而通用的方法,可以将细胞接种到网格上,可以根据特定需求进行调整。
披露声明
作者声明没有利益冲突。
致谢
我们要感谢 Mansky 实验室提供极速冻设备。这项工作的一部分是在明尼苏达大学的表征设施中进行的,该设施通过材料研究科学与工程中心(MRSEC;奖项编号 DMR-2011401) 和国家神经科学课程倡议 (NNCI;奖项编号 ECCS-2025124) 计划。我们要感谢病毒环境中的HIV行为中心(B-HIVE;1U54AI170855-01)和杜克大学HIV结构生物学中心(DCHSB;U54AI170752) 中心。
材料
| Name | Company | Catalog Number | Comments |
| 10 nm colloidal gold bead solution | Sigma-Aldrich | 741957 | |
| 6 well multidish, 100/CS | Fisher Scientific | FB012927 | |
| Allegra V-15R Benchtop Centrifuge, IVD 120 V 60 Hz | Beckman-Coulter | C63125 | |
| Au G300F1 with R2/2 Quantifoil carbon | Quantifoil | TEM-G300F1-AU | |
| Bovine serum albumin | MilliporeSigma | A9647 | |
| BRAND counting chamber BLAUBRAND Neubauer improved | Sigma-Aldrich | BR717805-1EA | |
| DMi1 Inverted Microscope | Leica | 22A00G119 | |
| Dulbecco's modified eagle's medium - high glucose, no glutamine | Gibco | 11-960-044 | |
| Dumont 5/15 tweezer | Electron Microscopy Sciences | 0103-5/15-PO | |
| EM GP2 | Leica | 587085 | Automated plunge freezer |
| Fetal Bovine Serum | Gibco | A5209 | |
| Fibronectin from bovine plasma, cell culture grade | MilliporeSigma | F1141 | |
| GenJet version II in vitro DNA transfection reagent | SignaGen Laboratories | SL100489 | |
| GlutaMAX I 100x | Fisher Scientific | 35050061 | Media supplement |
| Neslab EX-211 Heating Circulator | Neslab | Out of production | Water bath for media warming |
| Original Portable Pipet-Aid Pipette Controller | Drummond Scientific | 4-000-100 | |
| PBS, pH 7.4 | Gibco | 10010023 | |
| Pelco easyGlow device | Pelco | 91000S | Glow discharge device |
| Penicillin-Streptomycin | Sigma-Aldrich | P0781 | Media supplement |
| Pipetman P1000, 100–1000 µL, Metal Ejector | Gilson | F144059M | |
| Pipetman P2, 0.2–2 µL, Metal Ejector | Gilson | F144054M | |
| Pipetman P20, 2–20 µL, Metal Ejector | Gilson | F144056M | |
| Whatman number 2 filter paper, 55 mm | Whatman | 28455-041 | Blotting paper |
参考文献
- Zhang, P., Mendonça, L. Analysis of Viruses in the Cellular Context by Electron Tomography. Encyclopedia of Virology. 1, Elsevier, Academic Press. 242-247 (2021).
- Fäßler, F., Dimchev, G., Hodirnau, V. -V., Wan, W., Schur, F. K. M. Cryo-electron tomography structure of Arp2/3 complex in cells reveals new insights into the branch junction. Nature Communications. 11, 6437(2020).
- McDowall, A. W., et al. Electron microscopy of frozen hydrated sections of vitreous ice and vitrified biological samples. Journal of Microscopy. 131 (Pt 1), 1-9 (1983).
- Stewart, M., Vigers, G. Electron microscopy of frozen-hydrated biological material. Nature. 319 (6055), 631-636 (1986).
- Gan, L., Jensen, G. J. Electron tomography of cells. Quarterly Reviews of Biophysics. 45 (1), 27-56 (2012).
- Yang, J. E., Larson, M. R., Sibert, B. S., Shrum, S., Wright, E. R. CorRelator: Interactive software for real-time high precision cryo-correlative light and electron microscopy. Journal of Structural Biology. 213 (2), 107709(2021).
- Mendonça, L., et al. Correlative multi-scale cryo-imaging unveils SARS-CoV-2 assembly and egress. Nature Communications. 12 (1), 4629(2021).
- Klumpe, S., et al. A modular platform for automated cryo-FIB workflows. eLife. 10, e70506(2021).
- Wagner, F. R., et al. Preparing samples from whole cells using focused-ion-beam milling for cryo-electron tomography. Nature Protocols. 15 (6), 2041-2070 (2020).
- Klein, S., et al. IFITM3 blocks influenza virus entry by sorting lipids and stabilizing hemifusion. Cell Host & Microbe. 31 (4), 616.e20-633.e20 (2023).
- Shah, P. N. M., et al. Characterization of the rotavirus assembly pathway in situ using cryoelectron tomography. Cell Host & Microbe. 31 (4), 604.e4-615.e4 (2023).
- Fäßler, F., Zens, B., Hauschild, R., Schur, F. K. M. 3D printed cell culture grid holders for improved cellular specimen preparation in cryo-electron microscopy. Journal of Structural Biology. 212 (3), 107633(2020).
- Hoffmann, P. C., et al. Electron cryo-tomography reveals the subcellular architecture of growing axons in human brain organoids. eLife. 10, e70269(2021).
- Toro-Nahuelpan, M., et al. Tailoring cryo-electron microscopy grids by photo-micropatterning for in-cell structural studies. Nature Methods. 17 (1), 50-54 (2020).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。