Method Article
Bronchoalveoläre Lavage (BAL) für Forschung, Beschaffung angemessene Probenausbeute
In diesem Artikel
Zusammenfassung
Wir beschreiben eine Technik für die Forschung Bronchoskopie und BAL mit Niederdruck-Absaugung. Die Technik wird verwendet, um die Immunzellen aus der Lunge bronchoalveolären Oberflächen ernten. Lokalanästhesie und milden Sedierung (Midazolam) verwendet. Themen vertragen die Prozedur gut und Erfahrung minimalen Nebenwirkungen.
Zusammenfassung
Wir beschreiben eine Technik für die Forschung Bronchoskopie mit BAL (BAL) mit manuellen Hand Sog, um nicht-adhärenten Zellen und Lunge Futter Flüssigkeit aus der Schleimhautoberfläche zu entfernen. In Forschungsumgebungen ermöglicht BAL Abtastung angeborenen (Lunge Makrophagen), Mobil (B-und T-Zellen) und die humorale (Immunglobulin)-Antworten innerhalb der Lunge.
BAL ist international für Forschungszwecke akzeptiert und seit 1999 die Technik in> 1.000 Probanden in Großbritannien und Malawi von unserer Gruppe durchgeführt.
Unsere Technik nutzt sanfte Hand Absaugen von Flüssigkeit eingeflößt, dies ist für die Maximierung der BAL-Volumen zurückgeführt und gelten Mindestscherkraft auf Flimmerepithelien, um die Struktur und Funktion von Zellen in der BAL-Flüssigkeit erhalten und lebensfähig zu erhalten, um das Wachstum zu erleichtern von Zellen in ex-vivo-Kultur. Die Forschungstechnik verwendet daher ein größeres Volumen insDestillat (typischerweise in der Größenordnung von 200 ml) und beschäftigt manuelle Absaugung, um Zellschäden zu reduzieren.
Die Patienten werden Lokalanästhetikum gegeben, bot Sedierung (Midazolam), und gut vertragen das Verfahren mit minimalen Nebenwirkungen. Mündliche und schriftliche Fachinformationen verbessert die Toleranz und eine schriftliche Einverständniserklärung ist Pflicht. Sicherheit der Person im Vordergrund steht. Themen werden sorgfältig mit klarem und Ausschlusskriterien ausgewählt.
Dieses Protokoll enthält eine Beschreibung der möglichen Risiken und die Schritte unternommen, um sie zu mildern, eine Liste der Kontraindikationen, Pre-und Post-Prozedur überprüft, sowie präzise Bronchoskopie-und Labortechnik.
Einleitung
Hintergrund
Bronchoskopie wurde für die klinische Praxis entwickelt, es ist weit verbreitet sowohl diagnostisch als auch therapeutisch 1,2 verwendet. Bronchoalveoläre Lavage (BAL) entfernt nicht-adhärenten Zellen und Lunge Futter Flüssigkeit aus der Schleimhautoberfläche; Biopsie wird verwendet, um Schleimhaut und Submukosa Gewebe probieren. In Forschungsumgebungen ermöglicht BAL Abtastung angeborenen (Lungen-Makrophagen 3-5), Mobil (B-und T-Zellen, 6) und humorale (Immunglobulin 7) Reaktionen in der Lunge.
BAL ist international für Forschungszwecke 8 angenommen und seit 1999 die Technik in> 1.000 Probanden in Großbritannien und Malawi von unserer Gruppe durchgeführt. Wir verwenden diese Technik in den Studien der angeborenen zellulären und humoralen Immunantwort auf den Pneumokokken-Antigen einschließlich experimenteller menschlichen Pneumokokken-Wagen 9,17, Biomasse Rauch 5, HIV und die Impfung und Ergänzung der Behandlung stustirbt in Genesung von einer Lungenentzündung. Unsere Technik nutzt sanfte Hand Absaugen von Flüssigkeit eingeflößt, dies ist für die BAL-Volumen zurück maximieren und gelten Mindestscherkraft auf Flimmerepithelien, um die Struktur und Funktion von Zellen in der BAL-Flüssigkeit zu bewahren.
In einem Forschungskontext BAL nutzt eine andere Technik als die durch Atem-und Intensivmediziner (oft als bronchiale Wäsche, Wasch, Spülung, oder BAL), die darauf abzielen, diagnostischen oder therapeutischen Nutzen zu gewinnen praktiziert. Die Forschung Technik wurde entwickelt, um Zellen zu ernten und Lebensfähigkeit zu erhalten, um das Wachstum von Zellen in Kultur ex vivo zu erleichtern. Aus diesen Gründen ist die Forschung Technik verwendet ein größeres Volumen instillate (typischerweise in der Größenordnung von 200 ml) und beschäftigt manuellen Absaugung zu Zellschäden zu verringern. Die Patienten werden Lokalanästhetikum gegeben, bot Sedierung (Midazolam), und gut vertragen das Verfahren mit minimalen Nebenwirkungen. Mündliche und schriftliche subjektivent Informationen verbessert die Toleranz und eine schriftliche Einverständniserklärung ist zwingend ein.
Ziel
Das übergeordnete Ziel ist, dass das Verfahren sicher und wirksam zu sein. Themen sollten keine physiologische Störung erleben und Betreiber sollten konsequent von über 100 ml BAL von Patienten zu sammeln. Nach dem Eingriff sollten Themen minimalen Nebenwirkungen zu erleben.
Sicherheit
Sicherheit der Person im Vordergrund steht. Themen werden sorgfältig mit klarem und Ausschlusskriterien ausgewählt. Dieses Protokoll enthält eine Beschreibung der möglichen Risiken und die getroffenen Maßnahmen, um sie zu mildern.
Kontraindikationen für Forschung Bronchoskopie kann absolut oder relativ ausgedrückt werden kann, und werden in unserem Studienprotokoll als Ausschluss-und Einschlusskriterien enthalten. Unsere Themen sind alle abgeschirmt zu voller Gesundheit zu gewährleisten.
Absolute Kontraindikationengehören instabile Halswirbelsäule, reagiert Hypoxie, instabile Angina pectoris, Blutungsneigung, Herzrhythmusstörungen und bösartige.
Relative Kontraindikationen, einschließlich der Bedingungen mit erhöhten Komplikationsraten verbunden sind, gehören:
Allgemein: schlecht Genossenschaft ein Thema, eine signifikante allgemeine medizinische Problem zB Epilepsie, vorherige schlecht vertragen Bronchoskopie, bekannten Nebenwirkungen von Lidocain oder Midazolam, Schwangerschaft, schlechte Ernährung.
Atemwege: Hypoxie [Sättigungen (sats) on air <94%], Hyperkapnie, instabile Asthma 1, wesentlich beeinträchtigt Atemfunktion 1 (FEV 1 <1 l), Lungenbluthochdruck.
Herz-Kreislauf: Urämie, innerhalb von 6 Wochen nach Myokardinfarkt 1, obere Hohlvene Obstruktion.
Sonstiges: Immunsuppression (unsere Gruppe führt regelmäßig dieses Verfahdure bei HIV-positiven Patienten).
Siehe Tabelle 1 - Risiken mit BAL für Forschung verbunden.
Protokoll
1. Die Themen werden auf Anreise mit dem Atem Forschung Krankenschwester Met
- Das Thema wurde Fasten für> 4 h für feste Nahrung und 2 h für klare Flüssigkeiten ein.
- Das Verfahren wird als Tag Fall mit entsprechenden Pre-und Post-Prozedur überprüft (nach Standard-Krankenhauspolitik) durchgeführt.
- Das Thema trägt einen Krankenhauskittel.
- Eine kleine Gauge-Kanüle eingeführt wird (idealerweise in die linke Hand) und bleibt in situ bis zum Ende der Post-Verfahren Erholungsphase ein.
- Vorverfahren Beobachtungen getroffen werden (Blutdruck, Herzfrequenz, Sauerstoffsättigung [sats]).
- Das Thema ist mit der Bronchoskopie-Suite übertragen.
2. Das Thema ist für die Vorgehensweise in der Suite durch eine Atemforschungsmediziner in Bronchoskopie Erfahrene Vorbereitet
- Überwachungsgeräte angeschlossen ist, einschließlich, 3-Kanal-EKG, Pulsoximeter 1,10 und Blutdruckmessgerät. Anesthetic-Unterstützung ist nicht erforderlich einschließlich schriftlicher Einwilligung.
- Sauerstoff kann über eine Nasenkanüle mit bis zu 4 l / min geliefert werden, zu erreichen sats> 90% ein.
- Der Betreiber prüft die Bronchoskop, dies beinhaltet eine effektive Absaugung durch Absaugen sterile physiologische Kochsalzlösung.
- Lokalanästhesie mit Lidocain in die Nasenwege (mit Instillagel 1) und der Mundschleimhaut erreicht (mit Xylocain)
- Wenn Sedierung geeignete und von der Person beantragt, so wird die intravenöse Midazolam ein. Eine entsprechende Umkehrmittel (Flumazenil) ist ab sofort verfügbar.
- Reanimationsausrüstung sollten leicht zugänglich sein 1,10.
3. Das Bronchoskop wird eingefügt und positioniert,
- Intubation ist in der Regel über die Nase. Ist dies nicht möglich, da Nasenpolypen, entzündeten Nasenmuscheln oder irgendwelche Beschwerden dann das Motiv über den Mund intubiert (ein Mundschutz verwendet wird, um zu verhindern,Schäden an Rahmen oder der Person Zähne).
- Lokalanästhesie an der Kehlkopf wird mit 4% Lidocain abgeschlossen, in der Regel insgesamt von 4-6 ml verwendet. Häufig dies verursacht Husten auf Instillation.
- Die Stimmbänder übergeben werden, und ferner Schleimhautanästhesie mit 2 ml Aliquots von 2% Lidocain bei der Carina bei der Teilung des rechten Unterlappen (RLL) und rechte Mittellappen (RML) und an der RML Eingang.
- Das Bronchoskop wird innerhalb des RML positioniert, idealerweise im Mittelsegment in einer Position, wo es distal genug, um in einer sicheren Position ist, aber nicht zu, so daß die distalen Luftwege zusammenbricht, wenn ein Saugen angewandt unter Verwendung des Saug-Taste ("Wink-Test" ).
- Gute Positionierung während der Test Nachricht von einem Bronchoskop, die vollständig in Position durch den bronchoscopist und einem Atemwege, die nicht vollständig schließen sofort auf sanfte Saugwirkung tut aufrechterhalten werden kann angezeigt.
4. Die BAL durchgeführt
- Vier 60-ml-Spritzen sind vorge60 ml, 50 ml, 50 ml und 40 ml in aufeinander Spritzen - mit erwärmter physiologischer Kochsalzlösung gefüllt. Wenn das Motiv und bronchoscopist sind bereit die erste Spritze von Kochsalzlösung wird von der Bronchoskopie Assistent eingeflößt während die bronchoscopist hält die Position in der RML.
- Sanften Hand Sog wird dann vom Assistenten mit dem gleichen Port und 50-ml-Spritze durchgeführt.
- Dieses Verfahren wird dann wiederholt eine weitere 3x mit einem maximalen Volumen von 200 ml in den spezifischen Technik verwendet.
- Die abgerufenen BAL-Flüssigkeit wird sanft in gekennzeichneten Behältern bereits auf schmelzendem Eis gehalten ausgewiesen. Glasbehälter kann, um die Zellhaftung zu hemmen und zu maximieren Zellrück presiliconized werden.
- Die BAL-Flüssigkeit trüb erscheint gegen das Licht mit Oberflächen Seifenblasen durch Tenside gebildet.
- Das Bronchoskop wird langsam vollständig zurückgezogen.
- Die BAL-Flüssigkeit wird unverzüglich auf Eis zur sofortigen Verarbeitung transportiert.
5. Betreff Rettung
- Das Thema wird für 2-4 Stunden durch die Atemforschungs Krankenschwester auf einer Station erholt.
- Während dieser Zeit dürfen sie zur Ruhe und dann nur essen und trinken> 60 min 1 nach dem Eingriff (wenn ihre Schwalbe als sicher beurteilt), um das Risiko der Aspiration.
- Postprozedurale Beobachtungen werden überwacht und aufgezeichnet. Eine klinische Prüfung erfolgt vor der Entlassung.
- Das Thema wird Predischarge über die häufigsten Nebenwirkungen (Fieber, mild rechts submammary Beschwerden in der Brust, Halsschmerzen) informiert und angesichts einer Kontaktnummer für den Fall erhebliche Nebenwirkungen auftreten, ein.
- Das Thema wird an 1-5 Tagen nach dem Eingriff mit einer klinischen Kontakt Follow-up. Dies kann entweder über das Telefon oder in Person zu sein.
6. Die Zellen werden im Labor Isoliert - Führen auf Melting Ice Wo Mögliche
- Das Volumen der BAL-Flüssigkeit wird durch eine doppelte Schicht von steriler Gaze Tupfer aufgenommen und filtriert,Schleim-Stecker in vorgekühlte, sterile 50 ml Zentrifugenröhrchen entfernen.
- Zellen werden durch Zentrifugation bei 500 × g bei 4 ° C für 5-10 min pelletiert und durch Vortexen in 50 ml kalter physiologischer Kochsalzlösung gewaschen. Zentrifugation wird einmal wiederholt.
- Zellen werden in Kulturmedium resuspendiert (RPMI-1640 + 10% fötales Rinderserum + 2 mM L-Glutamin + Penicillin [40 IU / ml], Streptomycin [75 IU / ml], und Amphotericin B [0,5 IU / ml]) und Differenzzählung durchgeführt wird unter Verwendung eines gleichen Volumens von Trypanblau und einem Hämocytometer.
- Die Zellsuspension wird normalisiert auf die gewünschte Dichte (wir verwenden 1 x 10 6 Zellen / ml), durch Pipettieren in geeignete Gewebekulturplatten eingebracht und bei 37 ° C für 3 Stunden, um Haftung zu Makrophagen inkubiert. 1 ml dieser Zellsuspension pro Well für 24-Well-Kulturplatten geeignet.
- Für Lymphozyten-Arbeit, nach 3 Stunden Inkubation wird das Kulturmedium vorsichtig nach oben und unten 3x pipettiert und gesammelt. Dieses Medium enthält Lymphozytenund nicht-adhärenten Makrophagen und Lymphozyten verwendet werden, um Funktion zu beurteilen, sondern kann auch in Reinigungsschritten verwendet werden, z. B. mit CD14 magnetischen Kügelchen an Makrophagen zu entfernen.
- Makrophagen für Arbeit, nach 3 h Inkubation wird das Medium vorsichtig mit minimaler Pipettieren entfernt und mit frischem, warmem Medium ohne Antibiotika (RPMI 1640 + 10% fötales Rinderserum + 2 mM L-Glutamin) ersetzt. Die Makrophagen sind Anhänger der Gewebekulturplatte (siehe Fig. 1).
Ergebnisse
Gute klinische Ergebnisse sind ein BAL Volumen von über 100 ml und ein Thema, die in den meisten erlebt hat, kleinere Beschwerden (siehe Tabelle 1). Dies erfordert eine entspannte und kooperative Thema. Der Arzt muss sicher sein, voll und ganz bereit (Werkstoffe) und Verständnis gegenüber der Freiwilligen.
Inter-und intraindividuelle Variabilität in der Zellausbeute (einschließlich Differentialblut) beschrieben worden. Differentialzellzählungen von gesunden Probanden in der Regel> 90% Makrophagen, die mit einer kleinen Anzahl von Neutrophilen (<2%) und Lymphozyten (5-10%). BAL-Zellen auf Objektträger zentrifugiert, kann mit einem Differenzkernfärbung angefärbt werden, um diese Informationen (Abbildung 1) zu erhalten. In Fig. 1 sind BAL-Zellen wurden fixiert und gefärbt mit Hemacolor Färbung nach den Anweisungen des Herstellers. Mindestens 300 Zellen gezählt, um zuverlässige Ergebnisse zu erhalten, werden Makrophagen,Neutrophile und Lymphozyten; 500 Zellen für seltener Zelltypen.
| Gefahr | Risiko | In diesem Protokoll reduziert nach: |
| Wirkung der Bronchoskopie und BAL 1, 14 | ||
| Leichte Beschwerden | <25% 14 # | Entsprechende Analgesie und Sedierung. Zuversichtlich und fürsorgliche Umgang mit dem Thema. |
| Nasenbluten | <1% # | Mild Druck für nur nasale Intubation. Wenn unterliegen Beschwerden oder verengte Öffnung - orale Intubation statt. |
| Endobronchial Blutung (Bluthusten) | <0,1% * 15 | Keine Biopsien entnommen. Eine sorgfältige Kontrolle während der Bronchoskopie - Vermeidung Schleimhaut der Atemwege. |
| Nausea, Erbrechen und Aspiration Pneumonie | <0,02% 14, # | Fasten für feste Nahrung> 4 Std. Vorverfahren ein. Angemessene Lokalanästhesie. Semirecumbent Position während der Prozedur. Sorgfältige Beobachtung post-Verfahren. |
| Fieber | 0,01 14-1% #, 16 | Bezieht sich auf die Entzündung und kann durch maximal Sammlung von BAL minimiert. Einzellappen BAL nur. # |
| Wunde Nase / Rachen und Heiserkeit | <25% 14 # | Angemessene Lokalanästhesie von Nase, Rachen und Kehlkopf (Minimierung Husten). |
| Infektion | <0,1% der HIV-negativen, 1% der HIV-positiven 14, # | Standard-Bronchoskop Waschverfahren ein. Einzellappen BAL nur. # Frühzeitiges Erkennen der Infektion: klinische Prüfung innerhalb 1 Stunde eind klinischen Kontakt 1-5 Tage nach der Bronchoskopie. |
| Brustschmerzen / Husten | <0,2% 14, # | Einzellappen nur BAL. Maximal BAL-Sammlung. # |
| Auswirkungen von Drogen: Lidocain, Midazolam | ||
| Arrhythmie | Sehr selten * | Maximal 5 mg / kg 14 Lidocain verwendet. Erwärmt normaler Kochsalzlösung getropft. # Pulsoximetrie (sats> 90% mit Sauerstoff Ergänzung), Herzüberwachung im gesamten Verfahren. Benzodiazepine Antagonisten (Flumazenil) sofort verfügbar. |
| Desorientierung / Agitation | <0,1% † # | |
| Cardio Atemdepression | Sehr selten * | |
* Nicht in unserer Gruppe in über 1.500 Forschungsverfahren erlebt.
† idiosyncratic eher als Dosis-abhängige Reaktion.
# Erfahrung unserer Gruppe in über 1.500 Forschungsverfahren.
Tabelle 1. Risiken im Zusammenhang mit BAL für Forschung verbunden. Dies schließt die Gefahr oder ein Risiko und wie diese unter Verwendung der beschriebenen Technik reduziert. Auswirkungen der Bronchoskopie / BAL und Auswirkungen von Arzneimitteln verwendet werden, enthalten.
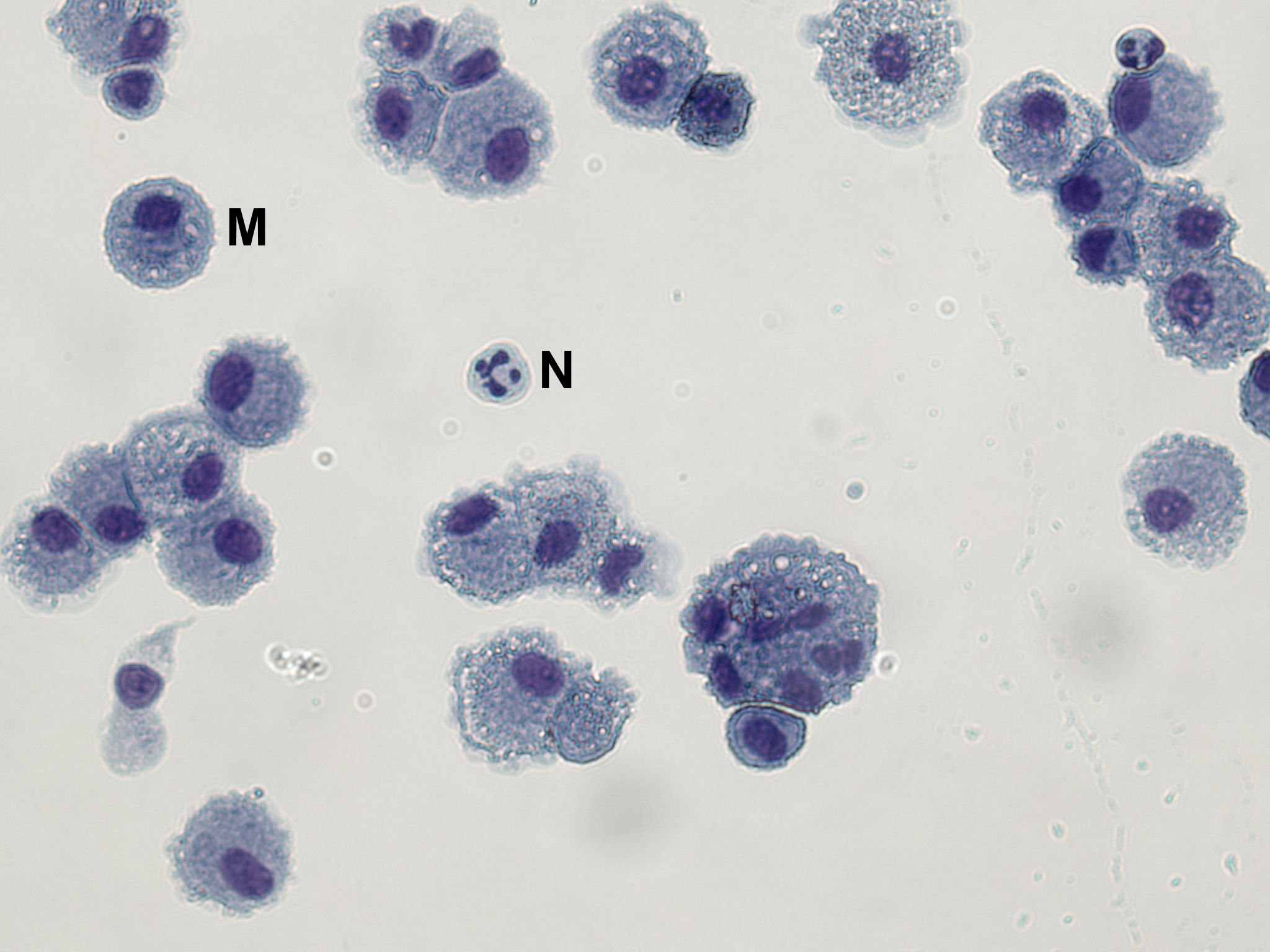
Fig. 1 ist. Ein Objektträger Zeige BAL Makrophagen und Neutrophile Gelegentliche. BAL-Zellen in Methanol fixiert und mit Hemacolor rot (Eosin Y) und Blau (Azur B) gefärbt.
Diskussion
Um gute Ergebnisse zu erzielen, die folgenden sind hilfreich:
- Gute anesthetisation an der Basis der Zunge und der hinteren Rachen. Dies ist wichtig, weil es Verfahrens Toleranz des Patienten und der Gesamtkomfort verbessert.
- Entweder ein pädiatrischer (Außendurchmesser 3,4-3,6 mm) oder erwachsenen Bronchoskop (Außendurchmesser 4,8 bis 5,9 mm) verwendet werden.
- Wenn es irgendein Unbehagen während nasale Intubation, bevorzugt orale Intubation. Im Allgemeinen Nasen Intubation ist entweder eine einfache Technik oder aufgegeben werden sollte.
- Nach der erstmaligen Einträufeln von Lidocain auf die Oropharynx, können Gegenstand der Bronchoskop zurückgenommen bevorzugen anhängigen dem Beginn der Anästhesie, insbesondere wenn das Bronchoskop oral eingeführt.
- Stellen Sie sicher, mindestens 10 x 10 ml-Spritzen sind mit nur 2-4 ml Lidocain vorgefüllt. Die Luft sollte in den Spritzen ermöglicht verbesserte Lieferung der Narkose direkt auf Schnüre und endobronchialer schleimig gelassen werdensa.
- Seit Husten während des Verfahrens deutlich reduziert BAL Ausbeute; erwärmt mit Kochsalzlösung und eine gute Schleimhautanästhesie sind wichtig, um diese zu reduzieren.
- Die 50-ml-Spritzen sind mit Kochsalzlösung vorgefüllt erwärmt werden. Es ist für die ersten 50 ml physiologischer Kochsalzlösung eingeflößt, zwischen 10-20 ml aufgrund dead-space Verlust und der Rest läuft in der terminalen Luftwege ergeben gemeinsam. Weitere Aliquots geben einen größeren Anteil der Flüssigkeit.
- Der Betreiber sollte immer die Bronchoskop vor der Intubation zu überprüfen, einschließlich der Gewährleistung effektiven Absaugung durch Absaugen sterile physiologische Kochsalzlösung. Verlust der Saugwirkung kann allgemein durch Abknicken des Schlauches oder Lecks um die Verbindungen mit dem Bronchoskop oder Saugvorrichtung auftreten.
- Bei der manuellen Absaugung, idealerweise der Atemwege sollten nicht zusammenbrechen. Wenn Sog immer wieder zusammenbricht, die Atemwege sind BAL kehrt zu einem Ventilmechanismus reduziert und lokale Entzündungen und Blutungen ist wahrscheinlicher: dies wiederum macht die Atemwege mErz reizbar und Husten wahrscheinlicher. Die Wahl der am besten geeigneten RML subsegmentalen Zweig und mit geringer Saugdrücke sind deshalb beide wichtig.
- Wenn Luft ständig abgesaugt überprüfen Sie die Verbindung der Spritze mit dem Bronchoskop und auch die Position des Bronchoskops im distalen Luftwege. Wenn dies ein wiederkehrendes Problem, post-Verfahren zu gewährleisten, dass keine Löcher in der Bronchoskop selber.
- BAL von Rauchern häufig dunkler aufgrund der Anwesenheit des intrazellulären Partikel. Raucher können die Bronchoskopie weniger gut vertragen und haben vermehrtes Husten.
- Die bevorzugte BAL Volumenausbeute> 100 ml. Eine Ausbeute von> 150 ml ist ausgezeichnet. Es wurden keine Erträge> 170 ml erlebt. Gibt es keine lineare Beziehung zwischen der Zellausbeute und BAL Volumenausbeute.
- Die Renditen von <100 ml sind, nach unserer Erfahrung eher zu Nebenwirkungen wie Husten, Brustschmerzen und Fieber führen. Wir beraten, dass Probanden mit Ausbeuten von <100 ml reco seinin Linksseitenlage Vered, kann diese Entwässerung eines verbleibenden Lungenflüssigkeit helfen.
- Klinische Kontakt sollte mit dem Thema innerhalb von 1-5 Tagen erfolgen, um keine Nebenwirkungen zu gewährleisten.
- Midazolam Sedierung ist für <50% der Patienten in Großbritannien und <5% in Malawi eingesetzt. Midazolam scheint nicht direkt die Verträglichkeit zu verbessern, einige Betreiber das Gefühl, dass Sedierung kann manchmal kontraproduktiv sein bei der Aufrechterhaltung einer kohärenten (und beruhigend) Dialog mit dem Thema.
- Nach unserer Erfahrung gibt es eine signifikante Lernkurve mit dieser Technik. Zum Beispiel die Koordination zwischen Arzt und Krankenschwester braucht Zeit, und die Renditen sind oft niedriger am Anfang des Lernprozesses.
- Bei HIV-positiven Patienten, verwenden wir Antibiotika prophylaktisch prebronchoscopy.
Offenlegungen
Andrea M. Collins wird von der Bill-und-Melinda-Gates-Stiftung, und keine potenziellen Interessenkonflikte finanziert. Sie hat Mittel von Merck (MSD) und GSK zu Konferenzen und Vortragshonorare zu besuchen. 50 Forschungs BALs unabhängig voneinander durchgeführt.
Jamie Rylance wird durch den Wellcome Trust finanziert und hat keinen Interessenkonflikt. Er hat keine anderen Mittel erhalten. 70 Forschungs BALs unabhängig voneinander durchgeführt.
Daniel G. Wootton wird von einem NIHR PhD Fellowship finanziert und hat keine Interessenkonflikte. 40 Forschungs BALs unabhängig voneinander durchgeführt.
Angela D. Wright hat keine potenzielle Interessenkonflikte. Mit über 100 Forschungs BALs unterstützt.
Adam Wright KA hat keine potenzielle Interessenkonflikte. Er hat über 50 BAL-Proben verarbeitet.
Duncan G. Fullerton Hat keine potenzielle Interessenkonflikte. 100 Forschungs BALs unabhängig voneinander durchgeführt.
Stephen B. Gordon hat keine potenzielle Interessenkonflikte. Er hat Mittel von Merck (MSD) und Novartis um an Konferenzen teilzunehmen. 400 Forschungs BALs unabhängig voneinander durchgeführt.
Danksagungen
Vielen Dank an Elena Mitsi (Wissenschaftlicher Mitarbeiter) und Sr. Carole Hancock (Research Krankenschwester) und OP-Personal für ihren Beitrag zu filmen, und David Shaw (Forschung Krankenschwester) für seine Unterstützung mit unseren Forschungs Bronchoskopien. Vielen Dank auch an unsere ehrenamtlichen Rebecca Dunphy dafür, dass dieses Verfahren, gefilmt zu werden.
Materialien
| Name | Company | Catalog Number | Comments |
Fiberoptic bronchoscope, light, and suction source | unspecified | ||
| Surgical gown, sterile gloves | unspecified | ||
| Sphygnomanometer | unspecified | For continuous patient monitoring | |
| Pulse oximeter | unspecified | For continuous patient monitoring | |
3-lead ECG monitor | unspecified | For continuous patient monitoring | |
Nasal oxygen delivery 2-4 L/min | unspecified | ||
| Lidocaine 10% spray (Xylocaine) | AstraZeneca | For topical anesthesia | |
| Lidocaine hydrochloride 2% | unspecified | For topical anesthesia | |
| Lidocaine gel (Instillagel) | Farco-Pharma, Germany | Alternative products available from other suppliers | |
Normal saline, sterile, 200 ml | unspecified | Warm to 30 °C | |
10 ml taper-end syringe (x10) | unspecified | For administration of lidocaine | |
Intravenous cannula 18 G | unspecified | For administration of midazolam | |
| Midazolam | unspecified | For sedation | |
| Flumazenil | unspecified | Reversal of benzodiazepine sedation (emergency use only) | |
60 ml taper-end syringes (x4) | unspecified | For normal saline injection and BAL fluid withdrawal. May require connector to attach to the injection port of the bronchoscope. | |
| Sterile gauze swab | Vernaid, UK | Alternative products available from other suppliers | |
| Sterile container for BAL fluid | See text and comments | Siliconized glass bottles reduce macrophage adherence. Alternatively, 50 ml centrifuge tubes may be used (total capacity 200 ml) | |
| Sigmacote | Sigma, UK | SL2 | Only if siliconised glass bottles used. NB: Harmful and flammable. If used, follow precautions detailed in manufacturer’s MSDS |
| Centrifuge | unspecified | At least 4 x 50 ml tube capacity. Refrigeration to 4 °C preferred. | |
| Shandon Cytospin centrifuge | Thermo Scientific, UK | For differential count only | |
| RPMI 1640 medium with L-glutamine | Sigma, UK | R8758 | Alternative products available from other suppliers |
| Fetal bovine serum | Sigma, UK | F6178 | Alternative products available from other suppliers |
| Penicillin-Streptomycin | Sigma, UK | P4333 | Alternative products available from other suppliers |
| Amphotericin B | Sigma, UK | A2942 | Alternative products available from other suppliers |
| Tissue culture plates | Greiner Bio-One, UK | 662160 | Alternative products available from other suppliers |
| Glass microscope slides | unspecified | For differential count only | |
| Shandon cytofunnel | Thermo Scientific, UK | A78710003 | For differential count only |
| Shandon cytoclip | Thermo Scientific, UK | 59910052 | For differential count only |
| Hemacolor staining set (fixative, red and blue reagents) | Merck, Germany | 111661 | Use according to manufacturer’s instructions |
Referenzen
- BTS, The British Thoracic Society Bronchoscopy Guideline Committee - A sub-Committee of the Standards of Care Committee of the British Thoracic Society. Thorax. 56 (Suppl I), 1-21 (2001).
- . Technical recommendations and guidelines for bronchoalveolar lavage (BAL) report of the European Society for Pneumology Task Group. Eur. Respir. , 561-585 (1989).
- Gordon, S. B., Irving, G. R., Lawson, R. A., Lee, M. E., Read, R. C. Intracellular trafficking and killing of Streptococcus pneumoniae by human alveolar macrophages are influenced by opsonins. Infect. Immun. 68, 2286-2293 (2000).
- Gordon, S. B., et al. Pulmonary immunoglobulin responses to Streptococcus pneumoniae are altered but not reduced in human immunodeficiency virus-infected Malawian adults. J. Infect. Dis. 188, 666-670 (2003).
- Fullerton, D. G., et al. Domestic smoke exposure is associated with alveolar macrophage particulate load. Trop. Med. Int. Health. 14, 349-354 (2009).
- Jambo, K. C., et al. Bronchoalveolar CD4+ T cell responses to respiratory antigens are impaired in HIV-infected adults. Thorax. 66, 375-382 (2011).
- Eagan, R., et al. Lung fluid immunoglobulin from HIV-infected subjects has impaired opsonic function against pneumococci. Clin. Infect. Dis. 44, 1632-1638 (2007).
- Rose, A. S., Knox, K. S. Bronchoalveolar lavage as a research tool. Sem. Respir. Crit. Care Med. 28, 561-573 (2007).
- Wright, A. K. A., et al. Human Nasal Challenge with Streptococcus pneumoniae is Immunising in the Absence of Carriage. PLoS Pathog. , (2012).
- Bolliger, C. T., et al. ERS/ATS statement on interventional pulmonology European Respiratory Society/American Thoracic Society. Eur. Respir. J. 19, 356-373 (2002).
- Ettensohn, D. B., Jankowski, M. J., Duncan, P. G., Lalor, P. A. Bronchoalveolar lavage in the normal volunteer subject. I. Technical aspects and intersubject variability. Chest. 94, 275-280 (1988).
- Ettensohn, D. B., Jankowski, M. J., Redondo, A. A., Duncan, P. G. Bronchoalveolar lavage in the normal volunteer subject. 2. Safety and results of repeated BAL, and use in the assessment of intrasubject variability. Chest. 94, 281-285 (1988).
- De Brauwer, E. I., Jacobs, J. A., Nieman, F., Bruggeman, C. A., Drent, M. Bronchoalveolar lavage fluid differential cell count. How many cells should be counted. Anal. Quant. Cytol. Histol. 24, 337-341 (2002).
- Mtunthama, N., et al. Malawians permit research bronchoscopy due to perceived need for healthcare. J. Med. Ethics. 34, 303-307 (2008).
- Pereira, W., Kovnat, D. M., Snider, G. L. A prospective cooperative study of complications following flexible fiberoptic bronchoscopy. Chest. 73, 813-816 (1978).
- Huang, Y. C., Bassett, M. A., Levin, D., Montilla, T., Ghio, A. J. Acute phase reaction in healthy volunteers after bronchoscopy with lavage. Chest. 129, 1565-1569 (2006).
- Gritzfeld, J. F., et al. Experimental Human Pneumococcal Carriage. J. Vis. Exp. (72), (2013).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten