Method Article
Lavagem Broncoalveolar (BAL) de Investigação; Obtenção adequada Rendimento Amostra
Neste Artigo
Resumo
Nós descrevemos uma técnica de pesquisa para fibrobroncoscopia e lavado bronco-alveolar utilizando baixa pressão de sucção. A técnica é utilizada para colher células do sistema imunológico das superfícies broncoalveolar de pulmão. A anestesia local e sedação consciente leve (midazolam) é usado. Assuntos toleram bem o procedimento e experimentar efeitos colaterais mínimos.
Resumo
Nós descrevemos uma técnica de pesquisa para fibrobroncoscopia com lavado bronco-alveolar (BAL), utilizando mão manual de sucção realizada, a fim de remover as células não aderentes e fluido de revestimento do pulmão a partir da superfície da mucosa. Em ambientes de pesquisa, BAL permite amostragem de inato (macrófagos do pulmão), celulares (B-e T-células), e humoral (imunoglobulina) respostas dentro do pulmão.
BAL é internacionalmente aceito para fins de pesquisa e, desde 1999, a técnica foi realizada em> 1.000 indivíduos no Reino Unido e Malawi por nosso grupo.
Nossa técnica utiliza sucção de mão suave do líquido instilado, o que é projetado para maximizar o volume BAL voltou e aplicar a força mínima de cisalhamento em epitélio ciliado, a fim de preservar a estrutura e função das células dentro do LBA e de preservar a viabilidade para facilitar o crescimento de células em cultura ex vivo. Assim, a técnica de pesquisa usa um maior volume de instillate (tipicamente na ordem de 200 ml) e emprega aspiração manual para reduzir os danos celulares.
Os pacientes recebem anestesia local, sedação consciente oferecido (midazolam), e toleram bem o procedimento com efeitos secundários mínimos. Informações sujeitas verbal e escrita melhora a tolerância e consentimento informado é obrigatório. Segurança do assunto é de suma importância. Os assuntos são cuidadosamente selecionados de acordo com critérios de inclusão e exclusão claras.
Este protocolo inclui uma descrição dos riscos potenciais, e as medidas tomadas para mitigá-los, uma lista de contra-indicações, pré e cheques pré-procedimento, bem como técnicas de broncoscopia e laboratoriais precisos.
Introdução
Fundo
A fibrobroncoscopia foi desenvolvido para a prática clínica, que é amplamente utilizado tanto para diagnóstico e terapêutica 1,2. A lavagem broncoalveolar (BAL) remove as células não aderentes e pulmão revestimento fluido a partir da superfície da mucosa, a biópsia é utilizado para recolher amostras de tecidos da mucosa e da submucosa. Em ambientes de pesquisa, BAL permite respostas de amostragem de inata (macrófagos pulmonares 3-5), celular (e B células T 6) e humoral (imunoglobulinas 7) dentro do pulmão.
BAL é internacionalmente aceito para fins de pesquisa e 8 desde 1999 a técnica foi realizada em> 1.000 indivíduos no Reino Unido e Malawi por nosso grupo. Nós usamos esta técnica em estudos de respostas imune inata, celulares e humoral ao antígeno pneumocócica incluindo experimental transporte humano pneumocócica 9,17, fumaça de biomassa 5, HIV e vacinação, e adjunto stu tratamentomorre em recuperação da pneumonia. Nossa técnica utiliza sucção de mão suave do líquido instilado, o que é projetado para maximizar o volume BAL voltou e aplicar a força mínima de cisalhamento em epitélio ciliado, a fim de preservar a estrutura e função das células dentro do LBA.
Em um contexto de pesquisa BAL utiliza uma técnica diferente daquela praticada por médicos de cuidados respiratórios e intensivos (muitas vezes chamado de lavagem brônquica, lavagens, lavagem, ou LBA) que desejem obter o benefício terapêutico ou diagnóstico. A técnica de pesquisa foi concebida para a colheita de células e preservar a viabilidade para facilitar o crescimento de células em cultura ex vivo. Por estas razões, a técnica de pesquisa utiliza um maior volume instilado (tipicamente na ordem de 200 ml) e emprega aspiração manual para reduzir os danos celulares. Os pacientes recebem anestesia local, sedação consciente oferecido (midazolam), e toleram bem o procedimento com efeitos secundários mínimos. Subjetividade verbal e escritainformações t melhora a tolerância e consentimento informado é obrigatória 1.
Objetivo
O objetivo geral é que o procedimento deve ser seguro e eficaz. Assuntos não deve sentir qualquer perturbação fisiológica e os operadores devem sempre coletar mais de 100 ml de BAL de indivíduos. Após o procedimento, os indivíduos devem experimentar efeitos secundários mínimos.
Segurança
Segurança do assunto é de suma importância. Os assuntos são cuidadosamente selecionados de acordo com critérios de inclusão e exclusão claras. Este protocolo inclui uma descrição dos riscos potenciais e as medidas tomadas para mitigá-los.
Contra-indicações para a broncoscopia pesquisa pode ser expressa como absoluto ou relativo, e estão incluídos em nosso protocolo de estudo como critérios de exclusão e inclusão. Nossos temas são todos selecionados para garantir plena saúde.
Contra-indicações absolutasincluir coluna cervical instável, a hipóxia sem resposta, angina instável, diátese hemorrágica, e arritmia cardíaca maligna.
Contra-indicações relativas, incluindo as condições associadas com o aumento das taxas de complicação, incluem:
Geral: mal cooperativa assunto 1, qualquer problema médico significativo geral por exemplo, epilepsia, anterior broncoscopia mal tolerada, conhecido reações adversas à lidocaína ou midazolam, gravidez, má nutrição.
Respiratória: hipoxia [saturações (SATS) no ar <94%], hipercapnia, asma instável 1, prejudicado significativamente a função respiratória 1 (FEV 1 <1 L), hipertensão pulmonar.
Cardiovascular: uremia, no prazo de 6 semanas de infarto do miocárdio 1, obstrução da veia cava superior.
Outros: imunossupressão (nosso grupo realiza regularmente este procemento em indivíduos HIV-positivos).
Ver Tabela 1 - Riscos associados a BAL para a pesquisa.
Protocolo
1. Os assuntos são recebido à chegada pela enfermeira Respiratory Research
- O assunto tem sido jejum de> 4 horas para alimentos sólidos e 2 horas para líquidos claros 1.
- O procedimento é realizado como um caso dia com cheques pré-e pós-procedimento adequado (de acordo com a política do hospital padrão).
- O sujeito usa um vestido hospital.
- É inserida uma cânula de pequeno calibre (idealmente para o lado esquerdo) e permanece in situ até ao final do período de recuperação pós-procedimento 1.
- Observações pré-procedimento são tomadas (pressão arterial, freqüência cardíaca, saturação de oxigênio [SATS]).
- O assunto é transferido para a suíte broncoscopia.
2. O assunto está preparado para o procedimento na Suite por uma Research Clínico Respiratório Experiente em broncoscopia
- O equipamento de monitorização está em anexo, incluindo, 3-lead ECG, oxímetro de pulso e 1,10 esfigmomanômetro. Anestésicosapoio ic não é necessária, incluindo consentimento informado por escrito.
- O oxigénio pode ser fornecido através de uma cânula nasal de até 4 L / min, para atingir sats> 90% 1.
- O operador verifica o broncoscópio, isso inclui a garantia de sucção eficaz por aspiração de soro fisiológico estéril.
- A anestesia tópica com lidocaína é atingida nas vias nasais (utilizando Instillagel 1) e da mucosa oral (usando xilocaína)
- Se a sedação é apropriado e solicitado pelo sujeito, midazolam é administrado 1. Um agente de reversão apropriado (flumazenil) está imediatamente disponível.
- Equipamento de reanimação devem estar prontamente disponíveis 1,10.
3. O broncoscópio é inserido e posicionado
- A intubação é geralmente através do nariz. Se isto não é possível devido a pólipos nasais, cornetos inflamados, ou qualquer desconforto, então o assunto é entubados através da boca (boca-guarda é usado para prevenirdanificar o âmbito ou os dentes do assunto).
- A anestesia tópica da laringe é completada usando 4% de lidocaína, geralmente um total de 4-6 mL é utilizado. Normalmente este provoca tosse em instilação.
- As cordas vocais são passados, e mais anestesia mucosas utilizando 2 ml alíquotas de lidocaína a 2% na carina, na divisão do lobo inferior direito (MID) e lobo médio direito (RML) e na entrada RML.
- O broncoscópio é posicionado dentro da RML, de preferência no segmento medial, numa posição em que é afastada o suficiente para estar em uma posição segura, mas não muito distante, de modo que as vias aéreas colapsa quando a sucção é aplicada ("teste de interesse" utilizando o botão de sucção ).
- Bom posicionamento é indicado durante o teste piscadela por um broncoscópio, que pode ser totalmente mantido em posição pelo broncoscopista e uma via aérea que não fechar totalmente imediatamente na sucção suave.
4. O LBA é realizado
- Quatro de 60 ml são seringas précheio com soro fisiológico normal aquecido - 60 ml, 50 ml, 50 ml e 40 ml em seringas sucessivas. Quando o assunto e broncoscopista estão prontos a primeira seringa de soro fisiológico é instilada pela assistente broncoscopia, enquanto o broncoscopista mantém a posição na RML.
- Sucção mão suave é então realizada pelo assistente usando a mesma porta e 50 ml seringa.
- Este procedimento é repetido mais uma 3x, com um volume máximo de 200 ml usados no nosso técnica específica.
- O LBA recuperado é expelido suavemente em recipientes rotulados já realizada no derretimento do gelo. Embalagens de vidro podem ser presiliconized, a fim de inibir a adesão celular e maximizar o retorno celular.
- O LBA parece nebuloso contra a luz com bolhas de sabão superfície formada por surfactantes.
- O broncoscópio é lentamente totalmente retirado.
- O LBA é transportado sem demora no gelo para processamento imediato.
5. Recuperação Assunto
- O assunto é recuperado para 2-4 hr pela enfermeira investigação respiratória em uma enfermaria.
- Durante esse tempo, eles estão autorizados a descansar e só então comer e beber> 60 min 1 após o procedimento (quando sua andorinha é avaliado como seguro), a fim de reduzir o risco de aspiração.
- Observações Mensagem processuais são monitorados e registrados. Um exame clínico ocorre antes da descarga.
- O assunto é informado predischarge sobre os efeitos colaterais comuns (febre, desconforto no peito submamária direita moderada, dor de garganta) e dado um número de contacto em caso efeitos colaterais significativos ocorrem 1.
- O assunto é acompanhado em 1-5 dias após o procedimento com um contato clínico. Isto pode ser por telefone ou pessoalmente.
6. As células são isoladas no Laboratório - Executar em Degelo Onde Possível
- O volume de fluido de BAL é gravado e filtrada através de uma camada dupla de gaze estéril cotoneteremover tampões de muco em previamente arrefecido, estéreis tubos de centrífuga de 50 ml.
- As células são sedimentadas por centrifugação a 500 xg, a 4 ° C durante 5-10 min e lavou-se por rotação em 50 ml de solução salina normal de frio. A centrifugação é repetida uma vez.
- As células são novamente suspensas em meio de cultura (RPMI-1640 + 10% de soro fetal de bovino + 2 mM de L-glutamina + penicilina [40 IU / ml], estreptomicina [75 IU / mL], e anfotericina B [0,5 IU / ml]) e contagem diferencial realizadas utilizando um volume igual de azul de tripano e um hemocitómetro.
- A suspensão de células é normalizado para a densidade necessária (usamos 1 x 10 6 células / ml), introduzido por pipeta em placas de cultura de tecidos adequados, e incubados a 37 ° C durante 3 horas para permitir a aderência de macrófagos. 1 ml desta suspensão de células por poço é adequado para placas de cultura de 24 poços.
- Para o trabalho de linfócitos, após 3 horas de incubação, o meio de cultura é suavemente pipetados para cima e para baixo 3x, e recolhida. Este meio contém linfócitose macrófagos não aderentes e podem ser utilizados para avaliar a função dos linfócitos, mas também pode ser usado em passos de purificação, por exemplo, com pérolas magnéticas CD14 para remover os macrófagos.
- Para o trabalho de macrófagos, após 3 horas de incubação, o meio é cuidadosamente removido com pipeta mínima e substituído com meio fresco, quente, sem antibióticos (RPMI 1640 + 10% de soro fetal de bovino + 2 mM de L-glutamina). Os macrófagos são aderentes à placa de cultura de tecido (ver Figura 1).
Resultados
Bons resultados clínicos são um volume de mais de BAL 100 ml e um sujeito que tenha experimentado na maior parte, menor desconforto (ver Tabela 1). Isso requer um sujeito relaxado e cooperativo. O médico deve ser confiante, totalmente preparado (Materiais), e compreensão para com o voluntário.
Variabilidade inter e intra-sujeito no rendimento celular (incluindo contagem diferencial) tem sido descrita. As contagens de células diferenciais de indivíduos saudáveis são geralmente> 90% de macrófagos com um pequeno número de neutrófilos (<2%) e os linfócitos (5-10%). Células do LBA centrifugadas em lâminas de microscópio pode ser manchado com uma mancha nuclear diferencial para obter essa informação (Figura 1). Na Figura 1, as células de BAL foram fixadas e coradas com Hemacolor coloração de acordo com as instruções do fabricante. Pelo menos 300 células devem ser contados para a obtenção de resultados confiáveis para os macrófagos,neutrófilos e linfócitos, células para 500 tipos de células mais raras.
| Perigo | Risco | Redução neste protocolo: |
| Efeito da broncoscopia e BAL 1, 14 | ||
| Leve desconforto | <25% 14, # | Analgesia e sedação adequada. Abordagem confiante e cuidar do assunto. |
| A epistaxe | <1% # | Pressão leve por apenas intubação nasal. Se o desconforto assunto ou abertura estreitada - intubação oral, em seu lugar. |
| Hemorragia endobrônquica (hemoptise) | <0,1% * 15 | Sem biópsias feita. O controle cuidadoso durante a broncoscopia - evitando mucosa respiratória. |
| Nausea, pneumonia vômito e aspiração | <0,02% 14, # | Jejum para o alimento sólido> 4 horas pré-procedimento 1. Anestesia tópica adequada. Posição Semirecumbent durante o procedimento. Observação pós-procedimento cuidadoso. |
| Febre | 0,01 14 - 1% #, 16 | Relaciona-se com a inflamação, e pode minimizado pela coleta máxima de BAL. Lóbulo único BAL só. # |
| Sore nariz / garganta e rouquidão | <25% 14, # | Anestesia tópica adequada do nariz, garganta e laringe (minimizando tosse). |
| Infecção | <0,1% em HIV negativo, 1% em HIV positivo 14, # | Procedimento de lavagem broncoscópio Standard 1. Lóbulo único BAL só. # O reconhecimento precoce da infecção: exame clínico dentro de 1 hora umad contato clínico de 1-5 dias após a broncoscopia. |
| Dor no peito / tosse | <0,2% 14, # | Lóbulo único BAL só. Coleção Maximal BAL. # |
| Efeitos das drogas: a lidocaína, midazolam | ||
| Arritmia | Muito raro * | Máximo de 5 mg / kg 14 de lidocaína utilizada. Soro fisiológico aquecido incutiu. # A oximetria de pulso (SATs> 90% com suplementação de oxigênio), monitorização cardíaca durante todo o procedimento. Antagonista de benzodiazepínicos (flumazenil) imediatamente disponível. |
| Desorientação / agitação | <0,1% † # | |
| Depressão respiratória Cardio | Muito raro * | |
* Não experientes no nosso grupo em mais de 1.500 procedimentos de pesquisa.
† idiosyncratic vez de reacção dependente da dose.
# Experiência do nosso grupo em mais de 1.500 procedimentos de pesquisa.
Tabela 1. Os riscos associados à BAL para a pesquisa. Isto inclui o perigo ou risco e como esta é reduzida por meio da técnica descrita. Efeitos da broncoscopia / BAL e também os efeitos de quaisquer medicamentos utilizados estão incluídos.
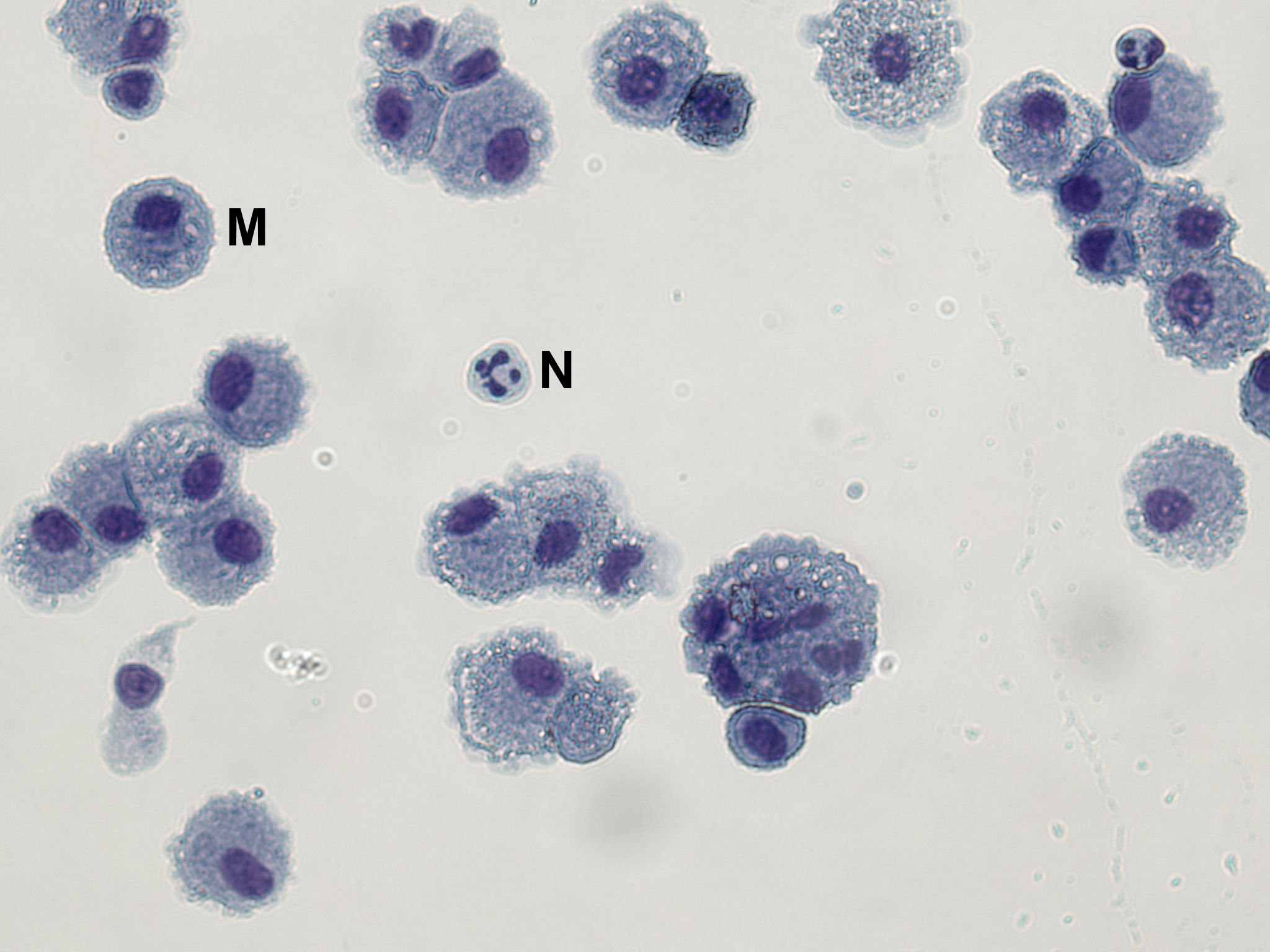
Figura 1. Uma lâmina de microscópio Mostrando BAL macrófagos e neutrófilos ocasionais. Células do LBA foram corrigidos em metanol e corados com Hemacolor vermelho (eosina Y) e azul (azul B).
Discussão
Para alcançar bons resultados a seguir são úteis:
- Bom anesthetisation na base da língua e posterior orofaringe. Isto é importante porque melhora a tolerância processual do sujeito e conforto geral.
- Ou um pediátrica (diâmetro externo 3,4-3,6 mm) ou broncoscópio adulto (4,8-5,9 mm de diâmetro externo) pode ser utilizado.
- Se não houver qualquer desconforto durante a intubação nasal, entubação oral é a preferida. Em geral intubação nasal ou é uma técnica simples ou deve ser abandonada.
- Após instilação inicial de lidocaína a orofaringe, o sujeito pode preferir broncoscópio de ser retirado pendente o início da anestesia, especialmente se o broncoscópio é inserido oralmente.
- Certifique-se de, no mínimo, 10 x 10 ml seringas são pré-preenchido com apenas 2-4 ml de lidocaína. O ar deve ser deixada nas seringas que permitam melhorar a entrega dos anestesia diretamente sobre os fios e muco endobrônquicasa.
- Desde tosse durante o procedimento reduz significativamente o rendimento BAL, usando salina aquecida e ter bons anestesia mucosas são importantes para reduzir isso.
- Os 50 ml seringas devem ser previamente preenchido com soro fisiológico aquecido. É comum que os primeiros 50 ml de soro fisiológico instilado para produzir entre 10-20 ml devido à perda de espaço morto eo restante em execução nas vias aéreas terminais. Mais alíquotas retornar uma proporção maior de fluido.
- O operador deve sempre verificar o broncoscópio antes da intubação, incluindo a garantia de sucção eficaz por aspiração de soro fisiológico estéril. A perda de sucção pode geralmente ocorrem devido à dobragem do tubo ou fugas em torno das ligações com o broncoscópio ou dispositivo de sucção.
- Durante sucção manual, de preferência a via aérea não deve entrar em colapso. Se sucção recorrentemente colapsa as vias aéreas, os retornos do LBA são reduzidos a um mecanismo de válvula, e inflamação local e sangramento é mais provável: que por sua vez faz com que as vias aéreas mminério irritável e tosse mais provável. Escolhendo o subsegmentares ramo RML mais adequada e utilizando baixas pressões de sucção, portanto, são ambos importantes.
- Quando o ar é constantemente aspirada verificar novamente a ligação da seringa para o broncoscópio e também a posição do broncoscópio nas vias aéreas distais. Se este é um problema recorrente, pós-procedimento garantir que não há buracos no próprio broncoscópio.
- BAL dos fumadores é muitas vezes mais escura, devido à presença de partículas intracelulares. Fumantes podem tolerar a broncoscopia menos bem, e têm aumento da tosse.
- O rendimento de volume preferível BAL é> 100 ml. Um rendimento de 150 ml> é excelente. Nós não tiveram quaisquer rendimentos> 170 ml. Não existe uma relação linear entre o rendimento das células e BAL rendimento volume.
- Rendimentos de <100 ml são, em nossa experiência, mais propensos a levar a efeitos colaterais, como tosse, dor torácica e febre. Aconselhamos que os indivíduos com rendimentos de <100 ml ser recoVered em decúbito lateral esquerdo, isso pode ajudar a drenagem de todo o líquido do pulmão remanescente.
- Contato clínico deve ser feita com o assunto dentro de 1-5 dias para garantir que não haja efeitos colaterais.
- Midazolam sedação é usada para <50% dos indivíduos no Reino Unido e <5% no Malawi. Midazolam não parece melhorar diretamente a tolerabilidade; alguns operadores acham que a sedação pode às vezes ser contraproducente na manutenção de um diálogo coerente (e reconfortante) com o assunto.
- Na nossa experiência, não é uma curva de aprendizagem significativa com esta técnica. Por exemplo coordenação entre médico e enfermeiro, leva tempo e os rendimentos são muitas vezes inferiores no início do processo de aprendizagem.
- Em indivíduos HIV positivos, usamos antibióticos profilaticamente prebronchoscopy.
Divulgações
Andrea M. Collins é financiada pela Fundação Bill e Melinda Gates, e sem conflito de interesses em potencial. Ela recebeu fundos da Merck (MSD) e GSK para participar de conferências e taxas de palestras. 50 BALs pesquisa realizada de forma independente.
Jamie Rylance é financiado pelo Wellcome Trust, e não tem nenhum conflito de interesse. Ele não recebeu outros fundos. 70 BALs pesquisa realizada de forma independente.
Daniel G. Wootton é financiado por uma NIHR PhD Fellowship, e não tem conflitos de interesse. 40 BALs pesquisa realizada de forma independente.
Angela D. Wright não tem conflito de interesses em potencial. Assistido com mais de 100 BALs pesquisa.
Adam KA Wright não tem conflito de interesses em potencial. Ele processou mais de 50 amostras de LBA.
Duncan G. Fullerton Não tem conflito de interesses em potencial. 100 BALs pesquisa realizada de forma independente.
Stephen B. Gordon não tem conflito de interesses em potencial. Ele recebeu fundos da Merck (MSD) e Novartis para participar de conferências. 400 BALs pesquisa realizada de forma independente.
Agradecimentos
Obrigado a Elena Mitsi (assistente de Investigação) e Ir. Carole Hancock (enfermeira Research) eo pessoal do teatro para a sua contribuição para as filmagens, e David Shaw (enfermeira da pesquisa) por seu apoio com os nossos bronchoscopies pesquisa. Agradeço também ao nosso Rebecca Dunphy voluntário para permitir que este procedimento a ser filmado.
Materiais
| Name | Company | Catalog Number | Comments |
Fiberoptic bronchoscope, light, and suction source | unspecified | ||
| Surgical gown, sterile gloves | unspecified | ||
| Sphygnomanometer | unspecified | For continuous patient monitoring | |
| Pulse oximeter | unspecified | For continuous patient monitoring | |
3-lead ECG monitor | unspecified | For continuous patient monitoring | |
Nasal oxygen delivery 2-4 L/min | unspecified | ||
| Lidocaine 10% spray (Xylocaine) | AstraZeneca | For topical anesthesia | |
| Lidocaine hydrochloride 2% | unspecified | For topical anesthesia | |
| Lidocaine gel (Instillagel) | Farco-Pharma, Germany | Alternative products available from other suppliers | |
Normal saline, sterile, 200 ml | unspecified | Warm to 30 °C | |
10 ml taper-end syringe (x10) | unspecified | For administration of lidocaine | |
Intravenous cannula 18 G | unspecified | For administration of midazolam | |
| Midazolam | unspecified | For sedation | |
| Flumazenil | unspecified | Reversal of benzodiazepine sedation (emergency use only) | |
60 ml taper-end syringes (x4) | unspecified | For normal saline injection and BAL fluid withdrawal. May require connector to attach to the injection port of the bronchoscope. | |
| Sterile gauze swab | Vernaid, UK | Alternative products available from other suppliers | |
| Sterile container for BAL fluid | See text and comments | Siliconized glass bottles reduce macrophage adherence. Alternatively, 50 ml centrifuge tubes may be used (total capacity 200 ml) | |
| Sigmacote | Sigma, UK | SL2 | Only if siliconised glass bottles used. NB: Harmful and flammable. If used, follow precautions detailed in manufacturer’s MSDS |
| Centrifuge | unspecified | At least 4 x 50 ml tube capacity. Refrigeration to 4 °C preferred. | |
| Shandon Cytospin centrifuge | Thermo Scientific, UK | For differential count only | |
| RPMI 1640 medium with L-glutamine | Sigma, UK | R8758 | Alternative products available from other suppliers |
| Fetal bovine serum | Sigma, UK | F6178 | Alternative products available from other suppliers |
| Penicillin-Streptomycin | Sigma, UK | P4333 | Alternative products available from other suppliers |
| Amphotericin B | Sigma, UK | A2942 | Alternative products available from other suppliers |
| Tissue culture plates | Greiner Bio-One, UK | 662160 | Alternative products available from other suppliers |
| Glass microscope slides | unspecified | For differential count only | |
| Shandon cytofunnel | Thermo Scientific, UK | A78710003 | For differential count only |
| Shandon cytoclip | Thermo Scientific, UK | 59910052 | For differential count only |
| Hemacolor staining set (fixative, red and blue reagents) | Merck, Germany | 111661 | Use according to manufacturer’s instructions |
Referências
- BTS, The British Thoracic Society Bronchoscopy Guideline Committee - A sub-Committee of the Standards of Care Committee of the British Thoracic Society. Thorax. 56 (Suppl I), 1-21 (2001).
- . Technical recommendations and guidelines for bronchoalveolar lavage (BAL) report of the European Society for Pneumology Task Group. Eur. Respir. , 561-585 (1989).
- Gordon, S. B., Irving, G. R., Lawson, R. A., Lee, M. E., Read, R. C. Intracellular trafficking and killing of Streptococcus pneumoniae by human alveolar macrophages are influenced by opsonins. Infect. Immun. 68, 2286-2293 (2000).
- Gordon, S. B., et al. Pulmonary immunoglobulin responses to Streptococcus pneumoniae are altered but not reduced in human immunodeficiency virus-infected Malawian adults. J. Infect. Dis. 188, 666-670 (2003).
- Fullerton, D. G., et al. Domestic smoke exposure is associated with alveolar macrophage particulate load. Trop. Med. Int. Health. 14, 349-354 (2009).
- Jambo, K. C., et al. Bronchoalveolar CD4+ T cell responses to respiratory antigens are impaired in HIV-infected adults. Thorax. 66, 375-382 (2011).
- Eagan, R., et al. Lung fluid immunoglobulin from HIV-infected subjects has impaired opsonic function against pneumococci. Clin. Infect. Dis. 44, 1632-1638 (2007).
- Rose, A. S., Knox, K. S. Bronchoalveolar lavage as a research tool. Sem. Respir. Crit. Care Med. 28, 561-573 (2007).
- Wright, A. K. A., et al. Human Nasal Challenge with Streptococcus pneumoniae is Immunising in the Absence of Carriage. PLoS Pathog. , (2012).
- Bolliger, C. T., et al. ERS/ATS statement on interventional pulmonology European Respiratory Society/American Thoracic Society. Eur. Respir. J. 19, 356-373 (2002).
- Ettensohn, D. B., Jankowski, M. J., Duncan, P. G., Lalor, P. A. Bronchoalveolar lavage in the normal volunteer subject. I. Technical aspects and intersubject variability. Chest. 94, 275-280 (1988).
- Ettensohn, D. B., Jankowski, M. J., Redondo, A. A., Duncan, P. G. Bronchoalveolar lavage in the normal volunteer subject. 2. Safety and results of repeated BAL, and use in the assessment of intrasubject variability. Chest. 94, 281-285 (1988).
- De Brauwer, E. I., Jacobs, J. A., Nieman, F., Bruggeman, C. A., Drent, M. Bronchoalveolar lavage fluid differential cell count. How many cells should be counted. Anal. Quant. Cytol. Histol. 24, 337-341 (2002).
- Mtunthama, N., et al. Malawians permit research bronchoscopy due to perceived need for healthcare. J. Med. Ethics. 34, 303-307 (2008).
- Pereira, W., Kovnat, D. M., Snider, G. L. A prospective cooperative study of complications following flexible fiberoptic bronchoscopy. Chest. 73, 813-816 (1978).
- Huang, Y. C., Bassett, M. A., Levin, D., Montilla, T., Ghio, A. J. Acute phase reaction in healthy volunteers after bronchoscopy with lavage. Chest. 129, 1565-1569 (2006).
- Gritzfeld, J. F., et al. Experimental Human Pneumococcal Carriage. J. Vis. Exp. (72), (2013).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados