Method Article
Lavage broncho-alvéolaire (LBA) pour la recherche; obtention adéquate rendement de l'échantillon
Dans cet article
Résumé
Nous décrivons une technique de recherche pour la fibroscopie bronchique et lavage broncho-alvéolaire en utilisant aspiration basse pression. La technique est utilisée pour récolter des cellules immunitaires à partir des surfaces de broncho-pulmonaire. L'anesthésie locale et sédation consciente légère (midazolam) est utilisé. Sujets tolèrent les effets secondaires minimes procédure ainsi et d'expérience.
Résumé
Nous décrivons technique recherche pour fibroscopie avec lavage bronchoalvéolaire (BAL) utilisant main manuel aspiration tenue pour éliminer cellules n'adhèrent et poumon fluide doublure partir la muqueuse. Dans les environnements de recherche, BAL permet échantillonnage de innée (macrophages du poumon), cellulaires (B et cellules T), et humorale (immunoglobulines) réponses dans le poumon.
BAL est internationalement accepté à des fins de recherche et depuis 1999 la technique a été réalisée en 1000> sujets au Royaume-Uni et au Malawi par notre groupe.
Notre technique utilise une aspiration douce main de liquide instillé, ce qui est conçu pour maximiser le volume BAL retourné et appliquer une force de cisaillement minimum sur l'épithélium cilié afin de préserver la structure et la fonction des cellules dans le liquide de LBA et de préserver la viabilité de faciliter la croissance des cellules en culture ex vivo. La technique de recherche utilise donc un plus grand volume insdistillat (typiquement de l'ordre de 200 ml) et emploie aspiration manuel afin de réduire les dommages cellulaires.
Les patients reçoivent un anesthésique local, offerts sédation consciente (midazolam), et tolèrent la procédure bien avec des effets secondaires minimes. Informations sous réserve verbale et écrite améliore la tolérance et le consentement éclairé écrit est obligatoire. Sécurité du sujet est primordiale. Les sujets sont choisis avec soin en utilisant des critères d'inclusion et d'exclusion clairs.
Ce protocole comprend une description des risques potentiels et les mesures prises à les atténuer, une liste de contre-indications, et pré-contrôles post-procédure, ainsi que des techniques de bronchoscopie et de laboratoire précises.
Introduction
Fond
La fibroscopie bronchique a été développé pour la pratique clinique, il est largement utilisé à la fois diagnostique et thérapeutique 1,2. Lavage broncho-alvéolaire (BAL) élimine les cellules non adhérentes et les poumons revêtement fluide à partir de la surface muqueuse; biopsie est utilisée pour échantillonner les tissus des muqueuses et sous-muqueuses. Dans les environnements de recherche, BAL permet échantillonnage de innée (macrophages pulmonaires 3-5), cellulaire (et B et T-cellules 6), et humorale (immunoglobuline 7) réponses dans le poumon.
BAL est internationalement accepté à des fins de recherche et 8 depuis 1999 la technique a été réalisée en 1000> sujets au Royaume-Uni et au Malawi par notre groupe. Nous utilisons cette technique dans les études de la réponse immunitaire innée, cellulaires et humorales à l'antigène pneumococcique y compris expérimentale transport humain pneumocoque 9,17, la fumée de biomasse 5, le VIH et la vaccination, et complément étudiants de traitementmeurt dans la récupération de pneumonie. Notre technique utilise une aspiration douce main de liquide instillé, ce qui est conçu pour maximiser le volume BAL retourné et appliquer une force de cisaillement minimum sur l'épithélium cilié afin de préserver la structure et la fonction des cellules dans le liquide de LBA.
Dans un contexte de recherche BAL utilise une technique différente de celle pratiquée par les voies respiratoires et les médecins de soins intensifs (de lavage souvent appelée bronchique, lavages, lavage, ou LBA) qui visent à obtenir un avantage diagnostique ou thérapeutique. La technique de recherche est conçu pour récolter les cellules et de préserver la viabilité à faciliter la croissance de cellules dans une culture ex vivo. Pour ces raisons, la technique de recherche utilise un volume instillation plus grande (typiquement de l'ordre de 200 ml) et emploie aspiration manuel afin de réduire les dommages cellulaires. Les patients reçoivent un anesthésique local, offerts sédation consciente (midazolam), et tolèrent la procédure bien avec des effets secondaires minimes. Subjectives verbale et écriteinformations t améliore la tolérance et le consentement éclairé écrit est obligatoire 1.
Objectif
L'objectif global est que la procédure doit être sûr et efficace. Sujets devraient pas connaître de perturbation physiologique et les opérateurs devraient systématiquement collecter plus de 100 ml de BAL de sujets. Après la procédure, les sujets devraient ressentir des effets secondaires minimes.
Sécurité
Sécurité du sujet est primordiale. Les sujets sont choisis avec soin en utilisant des critères d'inclusion et d'exclusion clairs. Ce protocole comprend une description des risques potentiels et les mesures prises pour les atténuer.
Contre-indications à la bronchoscopie de recherche peuvent être exprimés en absolu ou relatif, et sont inclus dans notre protocole de l'étude que l'exclusion et les critères d'inclusion. Nos sujets sont tous examinés pour assurer la pleine santé.
Contre-indications absoluesinclure la colonne vertébrale cervicale instable, l'hypoxie ne répond pas, l'angine de poitrine instable, diathèse hémorragique, et une arythmie cardiaque maligne.
Contre-indications relatives, y compris les conditions associées à une augmentation du taux de complications, notamment:
Général: sujet 1, tout problème médical général, par exemple l'épilepsie importante, avant la bronchoscopie mal tolérée, réactions indésirables connues à la lidocaïne ou le midazolam, la grossesse, une mauvaise nutrition mal coopérative.
Respiratoire: hypoxie [saturations (CST) sur l'air <94%], l'hypercapnie, l'asthme instable 1, la fonction respiratoire altérée de manière significative 1 (FEV 1 <1 L), l'hypertension artérielle pulmonaire.
Cardiovasculaire: urémie, dans les 6 semaines de l'infarctus du myocarde 1, supérieure obstruction de la veine cave.
Autres: immunosuppression (notre groupe se produit régulièrement cette procéduredure chez les sujets VIH positifs).
Voir le Tableau 1 - Risques liés aux BAL pour la recherche.
Protocole
Une. Les sujets sont accueillis à leur arrivée par l'infirmière de recherche en santé respiratoire
- Le sujet a été à jeun depuis> 4 h pour les aliments solides et 2 h pour les liquides clairs 1.
- La procédure est réalisée comme un cas de jour avec des contrôles pré-et post-procédure appropriée (conformément à la politique standard de l'hôpital).
- Le sujet porte une chemise d'hôpital.
- Une canule de petit calibre est inséré (de préférence dans la main gauche) et reste en place jusqu'à la fin de la période de récupération post-procédure 1.
- Observations préprocédure sont prises (pression artérielle, fréquence cardiaque, saturation en oxygène [des] sats).
- Le sujet est transféré à la suite de la bronchoscopie.
2. Le sujet est-elle prête pour la procédure dans la suite par une recherche des cliniciens expérimentés dans respiratoire bronchoscopie
- L'équipement de surveillance est fixée notamment; 3 ECG, oxymètre de pouls 1,10 et sphygmomanomètre. Anesthésiqueappui d'ic n'est pas nécessaire, y compris le consentement éclairé.
- L'oxygène peut être administré via une canule nasale jusqu'à 4 L / min, pour atteindre sats> 90% 1.
- L'opérateur vérifie le bronchoscope, cela implique d'assurer aspiration efficace en aspirant une solution saline normale stérile.
- L'anesthésie topique avec de la lidocaïne est atteint dans les voies nasales (en utilisant Instillagel 1) et de la muqueuse buccale (à l'aide de la xylocaïne)
- Si la sédation est approprié et demandé par le sujet, le midazolam par voie intraveineuse est administré 1. Un agent de renversement approprié (flumazénil) est immédiatement disponible.
- Matériel de réanimation doit être disponible immédiatement 1,10.
3. Le bronchoscope est insérée et positionnée
- Intubation est généralement par le nez. Si ce n'est pas possible en raison de polypes nasaux, cornets enflammées, ou tout inconfort alors le sujet est intubé par la bouche (bouche-garde est utilisé pour prévenirnuire à la portée ou les dents de l'objet).
- L'anesthésie topique au niveau du larynx est réalisée en utilisant 4% de lidocaïne, généralement un total de 4-6 ml est utilisé. Généralement ce qui provoque la toux sur instillation.
- Les cordes vocales sont passés, et d'autres l'anesthésie de la muqueuse à l'aide de fractions de 2 ml de lidocaïne 2% à la carène, à la division du lobe inférieur droit (RLL) et lobe moyen droit (RML) et à l'entrée RML.
- Le bronchoscope est positionné à l'intérieur de la RML, de préférence dans le segment médian, dans une position où il suffit d'être dans une position sûre distale mais pas trop distale de telle sorte que les voies aériennes s'effondre lorsque l'aspiration est appliquée («test Clin 'à l'aide du bouton d'aspiration ).
- Bon positionnement est indiqué lors de l'essai de clin d'oeil d'un bronchoscope qui peut être entièrement maintenue en position par le bronchoscopiste et les voies respiratoires qui ne se ferme pas complètement immédiatement aspiration douce.
4. Le BAL est joué
- Quatre 60 ml seringues sont prérempli de solution saline normale réchauffé - 60 ml, 50 ml, 50 ml et 40 ml dans des seringues successives. Lorsque le sujet et sont prêts bronchoscopiste la première seringue de sérum physiologique est inculquée par l'assistant de bronchoscopie tandis que le bronchoscopiste maintient la position dans la RML.
- Aspiration de main douce est ensuite effectuée par l'assistant en utilisant le même port et seringue de 50 ml.
- Cette procédure est ensuite répétée en outre un 3x, avec un volume maximal de 200 ml utilisées dans notre technique spécifique.
- Le fluide BAL récupéré est ensuite expulsé doucement dans des conteneurs appropriés ont déjà eu lieu sur la fonte des glaces. Les récipients en verre peuvent être presiliconized afin d'inhiber la fixation cellulaire et de maximiser le rendement de la cellule.
- Le LBA semble brumeuse contre la lumière avec des bulles de savon de surface formés par des agents tensioactifs.
- Le bronchoscope est entièrement retirée lentement.
- Le LBA est transporté sans délai sur la glace pour un traitement immédiat.
5. Récupération Sujet
- Le sujet est récupérée pour 2-4 heures par l'infirmière de recherche en santé respiratoire dans un service.
- Pendant ce temps, ils sont autorisés à se reposer et seulement manger et boire> 60 min 1 après la procédure (lorsque leur hirondelle est évaluée comme sûr), afin de réduire les risques d'aspiration.
- Observations poste de procédure sont surveillés et enregistrés. Un examen clinique se produit avant la décharge.
- Le sujet est informé prédécharge quant aux effets secondaires courants (fièvre, doux droit submammary gêne thoracique, mal de gorge) et un numéro de contact en cas d'effets secondaires importants se produisent 1.
- Le sujet est un suivi à 1-5 jours après l'intervention d'un contact clinique. Cela peut être soit par téléphone ou en personne.
6. Les cellules sont isolés en laboratoire - Effectuer sur fonte des glaces, si possible,
- Le volume de fluide BAL est enregistré et filtré à travers une double couche de tampon de gaze stérilepour enlever les bouchons de mucus dans prérefroidie, tubes de 50 ml à centrifuger stériles.
- Les cellules sont sédimentées par centrifugation à 500 xg à 4 ° C pendant 5 à 10 min et lavées par vortex dans 50 ml de solution saline normale à froid. Centrifugation est répétée une fois.
- Les cellules sont remises en suspension dans du milieu de culture (RPMI-1640 + 10% de sérum bovin foetal + 2 mM de L-glutamine + pénicilline [40 UI / ml], de la streptomycine [75 UI / ml], et de l'amphotéricine B [0,5 UI / ml]) et comptage différentiel effectuée en utilisant un volume égal de bleu trypan et un hémocytomètre.
- La suspension cellulaire est normalisée à la densité requise (on utilise 1 x 10 6 cellules / ml), introduit à la pipette dans des plaques de culture tissulaire appropriées, et incubées à 37 ° C pendant 3 heures pour permettre l'adhérence des macrophages. 1 ml de cette suspension de cellules par puits est approprié pour des plaques de culture à 24 puits.
- Pour le travail de lymphocytes, après 3 h d'incubation, le milieu de culture est doucement à la pipette de haut en bas 3x, et recueilli. Ce milieu contient les lymphocyteset les macrophages non adhérentes et peut être utilisé pour évaluer la fonction des lymphocytes, il peut aussi être utilisé dans les étapes de purification, par exemple avec des billes magnétiques CD14 pour éliminer les macrophages.
- Pour le travail macrophage, après 3 h d'incubation, le milieu est soigneusement retiré avec un minimum de pipetage et remplacé par du frais, chaud milieu sans antibiotiques (RPMI 1640 + 10% de sérum bovin foetal + 2 mM de L-glutamine). Les macrophages sont adhérents à la plaque de culture de tissus (voir la figure 1).
Résultats
De bons résultats cliniques sont un volume BAL de plus de 100 ml et un sujet qui a connu tout au plus, un léger inconfort (voir le tableau 1). Cela exige un sujet détendue et coopérative. Le clinicien doit être confiant, tout à fait prêt (Matériaux), et de compréhension envers les bénévoles.
Inter-et intra-sujet variabilité du rendement cellulaire (y compris leucocytaire) a été décrite. Le nombre de cellules dérivées de sujets sains sont généralement> 90% de macrophages avec un petit nombre de neutrophiles (<2%) et les lymphocytes (5-10%). BAL cellules centrifugées sur des lames de microscope peut être teinté avec un colorant nucléaire différentiel pour obtenir cette information (figure 1). Sur la figure 1, les cellules BAL ont été fixées et colorées en utilisant Hemacolor coloration selon les instructions du fabricant. Au moins 300 cellules doivent être comptées pour obtenir des résultats fiables pour les macrophages,neutrophiles et les lymphocytes, cellules pour 500 types de cellules rares.
| Danger | Risque | Réduit dans ce protocole par: |
| Effet de la bronchoscopie et BAL 1, 14 | ||
| Léger malaise | <25% 14 # | Analgésie et la sédation appropriée. Approche confiante et bienveillante à l'objet. |
| Épistaxis | <1% # | Une légère pression pour l'intubation nasale seulement. Si le sujet ou l'inconfort ouverture rétrécie - intubation orale à la place. |
| Hémorragie endobronchique (hémoptysie) | <0,1% * 15 | Pas de biopsies prises. Un contrôle attentif pendant la bronchoscopie - éviter muqueuse respiratoire. |
| Nausea, des vomissements et une pneumonie par aspiration | <0,02% 14 # | Le jeûne pour la nourriture solide> 4 h préprocédure 1. Anesthésie topique adéquate. La position Semirecumbent durant la procédure. Attention, post-procédure observation. |
| Fièvre | 0,01 14-1% # 16 | Concerne l'inflammation, et peut minimisé par la collecte maximale de BAL. Seul lobe BAL seulement. # |
| Douleurs dans le nez / gorge et enrouement | <25% 14 # | Anesthésie topique adéquates du nez, de la gorge et du larynx (en minimisant la toux). |
| Infection | <0,1% en séronégatifs, 1% dans séropositifs 14, # | Norme bronchoscope procédure de lavage 1. Seul lobe BAL seulement. # La reconnaissance précoce de l'infection: l'examen clinique dans 1 heure und un contact clinique 1-5 jours après la bronchoscopie. |
| Douleur thoracique / toux | <0,2% 14, # | Seul lobe BAL seulement. Collection maximale BAL. # |
| Effets de la drogue: la lidocaïne, midazolam | ||
| Arythmie | Très rare * | Maximum de 5 mg / kg 14 lidocaïne utilisée. Sérum physiologique réchauffé inculqué. # L'oxymétrie de pouls (sats> 90% avec la supplémentation en oxygène), la surveillance cardiaque pendant toute la procédure. Antagoniste des benzodiazépines (flumazénil) disponible immédiatement. |
| Désorientation / agitation | <0,1% † # | |
| Dépression cardio-respiratoire | Très rare * | |
* Non connu dans notre groupe dans plus de 1500 procédures de recherche.
† idiosyncratic plutôt que la réaction dose-dépendante.
# L'expérience de notre groupe dans plus de 1500 procédures de recherche.
Tableau 1. Risques liés aux BAL pour la recherche. Cela comprend le danger ou de risque et comment cela se réduit en utilisant la technique décrite. Effets de la bronchoscopie / BAL et aussi les effets des drogues médicinales utilisées sont incluses.
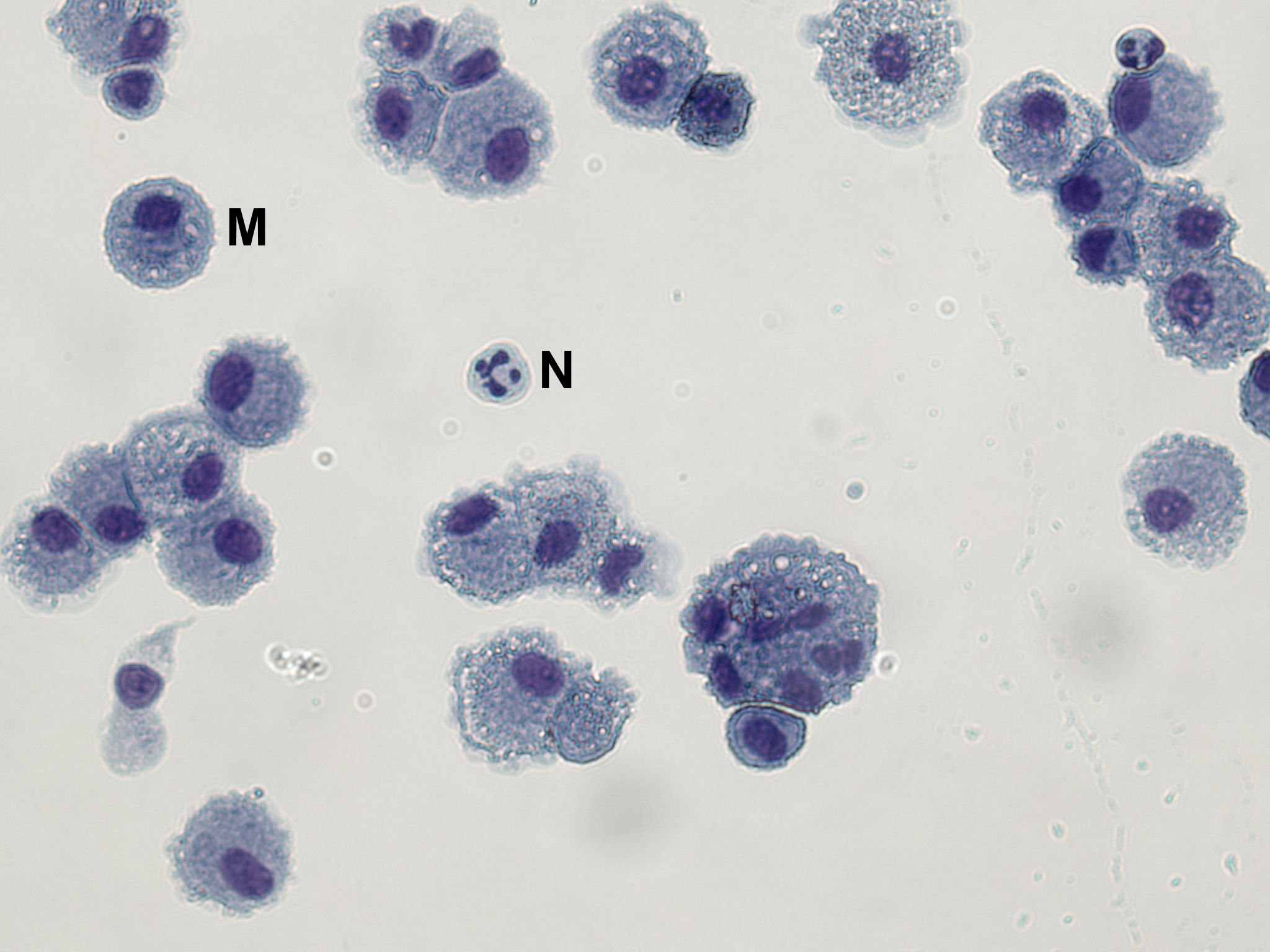
Figure 1. Glisser Microscope Affichage BAL macrophages et des neutrophiles occasionnel. BAL cellules ont été fixées au méthanol et colorées avec Hemacolor rouge (éosine Y) et bleu (azur B).
Discussion
Pour obtenir de bons résultats ce qui suit sont utiles:
- Bon anesthetisation à la base de la langue et de l'oropharynx postérieur. Ceci est important car il améliore la tolérance de la procédure de l'objet et de confort.
- Soit un pédiatrique (diamètre extérieur de 3.4 à 3.6 mm) ou bronchoscope adulte (diamètre extérieur de 4.8 à 5.9 mm) peuvent être utilisées.
- Si il n'y a aucune gêne lors de l'intubation nasale, intubation orale est préférée. En général intubation nasale est soit une technique simple ou devrait être abandonnée.
- Après instillation initiale de la lidocaïne à l'oropharynx, le sujet peut préférer le bronchoscope retirée en attendant le début de l'anesthésie, en particulier si le bronchoscope est inséré par voie orale.
- Veiller au moins 10 x 10 ml seringues préremplies sont à seulement 2-4 ml de lidocaïne. L'air doit être laissé dans les seringues permettant d'améliorer la prestation de l'anesthésie directement sur les cordons et les muco endobronchiquesa.
- Depuis la toux au cours de la procédure réduit significativement le rendement BAL; utilisant une solution saline chauffée et ayant de bonnes anesthésie des muqueuses sont importants pour réduire ce.
- Les seringues de 50 ml doivent être remplies au préalable avec une solution saline chauffée. Il est commun pour les 50 premiers ml de solution saline normale inculquées à donner entre 10-20 ml raison de la perte d'espace mort et le reste en cours d'exécution dans les voies aériennes terminales. D'autres aliquots de retour une plus grande proportion de fluide.
- L'opérateur doit toujours vérifier le bronchoscope avant l'intubation, notamment en veillant à aspiration efficace en aspirant une solution saline normale stérile. Perte d'aspiration peuvent souvent se produire en raison de vrillage du tube ou de fuites autour des connexions avec le bronchoscope ou dispositif d'aspiration.
- Au cours de l'aspiration manuelle, idéalement les voies aériennes ne devrait pas s'effondrer. Si l'aspiration s'effondre récurrente des voies respiratoires, les rendements BAL sont réduites à un mécanisme de soupape, et l'inflammation locale et des saignements est plus probable: à son tour, rend les voies respiratoires mminerai irritable et la toux plus probable. Choisir le RML sous-segmentaire branche la plus appropriée et l'utilisation de pressions d'aspiration faibles sont donc à la fois importante.
- Lorsque l'air est constamment aspiré revérifier la connexion de la seringue au bronchoscope et également la position du bronchoscope dans les voies aériennes distale. Si c'est un problème récurrent, post-procédure s'assurer qu'il n'y a pas de trous dans le bronchoscope lui-même.
- BAL de fumeurs est souvent plus foncée due à la présence de particules intracellulaires. Les fumeurs peuvent tolérer la bronchoscopie moins bien, et avoir augmentation de la toux.
- Le rendement préférable de volume BAL est> 100 ml. Un rendement de> 150 ml est excellent. Nous n'avons pas connu de rendements> 170 ml. Il n'y a pas de relation linéaire entre le rendement de la cellule et le rendement volumique BAL.
- Les rendements de <100 ml sont, dans notre expérience, plus susceptible de conduire à des effets secondaires tels que la toux, des douleurs thoraciques et de la fièvre. Nous conseillons que les sujets avec des rendements de <100 ml Soyez recoVERED dans la position latérale gauche, ce qui peut faciliter le drainage de tout fluide restant du poumon.
- Le contact clinique doit être faite avec le sujet dans les 1-5 jours pour assurer sans effets secondaires.
- Midazolam sédation est utilisée pour <50% des sujets dans le Royaume-Uni et <5% au Malawi. Le midazolam ne semble pas directement à améliorer la tolérance; certains opérateurs estiment que la sédation peut parfois être contre-productive dans le maintien d'un dialogue cohérent (et rassurant) avec le sujet.
- Dans notre expérience, il ya une courbe d'apprentissage importante avec cette technique. Par exemple la coordination entre le médecin et l'infirmière prend du temps et les rendements sont souvent plus bas au début du processus d'apprentissage.
- Chez les sujets séropositifs, nous utilisons des antibiotiques à titre prophylactique prebronchoscopy.
Déclarations de divulgation
Andrea M. Collins est financé par la Fondation Bill et Melinda Gates, et aucun conflits d'intérêts potentiels. Elle a reçu des fonds de Merck (MSD) et GSK pour assister à des conférences et des honoraires de conférencier. 50 LBA de recherche effectuées indépendamment.
Jamie Rylance est financé par le Wellcome Trust, et n'a aucun conflit d'intérêts. Il n'a pas reçu d'autres fonds. 70 LBA de recherche effectuées indépendamment.
Daniel G. Wootton est financé par une bourse de doctorat INDH, et n'a pas de conflits d'intérêts. 40 LBA de recherche effectuées indépendamment.
Angela D. Wright n'a pas de conflits d'intérêts potentiels. Assistée avec plus de 100 BAL de recherche.
Adam KA Wright n'a pas de conflits d'intérêts potentiels. Il a traité plus de 50 échantillons de LBA.
Duncan G. Fullerton N'a pas de conflits d'intérêts potentiels. 100 BAL de recherche effectuées indépendamment.
Stephen B. Gordon n'a pas de conflits d'intérêts potentiels. Il a reçu des fonds de Merck (MSD) et Novartis à assister à des conférences. 400 BAL de recherche effectuées indépendamment.
Remerciements
Merci à Elena Mitsi (assistant de recherche) et Sœur Carole Hancock (infirmière en recherche) et le personnel du théâtre pour leur contribution au tournage, et à David Shaw (infirmière en recherche) pour son soutien avec nos bronchoscopies de recherche. Merci également à notre bénévole Rebecca Dunphy pour permettre cette procédure pour être filmé.
matériels
| Name | Company | Catalog Number | Comments |
Fiberoptic bronchoscope, light, and suction source | unspecified | ||
| Surgical gown, sterile gloves | unspecified | ||
| Sphygnomanometer | unspecified | For continuous patient monitoring | |
| Pulse oximeter | unspecified | For continuous patient monitoring | |
3-lead ECG monitor | unspecified | For continuous patient monitoring | |
Nasal oxygen delivery 2-4 L/min | unspecified | ||
| Lidocaine 10% spray (Xylocaine) | AstraZeneca | For topical anesthesia | |
| Lidocaine hydrochloride 2% | unspecified | For topical anesthesia | |
| Lidocaine gel (Instillagel) | Farco-Pharma, Germany | Alternative products available from other suppliers | |
Normal saline, sterile, 200 ml | unspecified | Warm to 30 °C | |
10 ml taper-end syringe (x10) | unspecified | For administration of lidocaine | |
Intravenous cannula 18 G | unspecified | For administration of midazolam | |
| Midazolam | unspecified | For sedation | |
| Flumazenil | unspecified | Reversal of benzodiazepine sedation (emergency use only) | |
60 ml taper-end syringes (x4) | unspecified | For normal saline injection and BAL fluid withdrawal. May require connector to attach to the injection port of the bronchoscope. | |
| Sterile gauze swab | Vernaid, UK | Alternative products available from other suppliers | |
| Sterile container for BAL fluid | See text and comments | Siliconized glass bottles reduce macrophage adherence. Alternatively, 50 ml centrifuge tubes may be used (total capacity 200 ml) | |
| Sigmacote | Sigma, UK | SL2 | Only if siliconised glass bottles used. NB: Harmful and flammable. If used, follow precautions detailed in manufacturer’s MSDS |
| Centrifuge | unspecified | At least 4 x 50 ml tube capacity. Refrigeration to 4 °C preferred. | |
| Shandon Cytospin centrifuge | Thermo Scientific, UK | For differential count only | |
| RPMI 1640 medium with L-glutamine | Sigma, UK | R8758 | Alternative products available from other suppliers |
| Fetal bovine serum | Sigma, UK | F6178 | Alternative products available from other suppliers |
| Penicillin-Streptomycin | Sigma, UK | P4333 | Alternative products available from other suppliers |
| Amphotericin B | Sigma, UK | A2942 | Alternative products available from other suppliers |
| Tissue culture plates | Greiner Bio-One, UK | 662160 | Alternative products available from other suppliers |
| Glass microscope slides | unspecified | For differential count only | |
| Shandon cytofunnel | Thermo Scientific, UK | A78710003 | For differential count only |
| Shandon cytoclip | Thermo Scientific, UK | 59910052 | For differential count only |
| Hemacolor staining set (fixative, red and blue reagents) | Merck, Germany | 111661 | Use according to manufacturer’s instructions |
Références
- BTS, The British Thoracic Society Bronchoscopy Guideline Committee - A sub-Committee of the Standards of Care Committee of the British Thoracic Society. Thorax. 56 (Suppl I), 1-21 (2001).
- . Technical recommendations and guidelines for bronchoalveolar lavage (BAL) report of the European Society for Pneumology Task Group. Eur. Respir. , 561-585 (1989).
- Gordon, S. B., Irving, G. R., Lawson, R. A., Lee, M. E., Read, R. C. Intracellular trafficking and killing of Streptococcus pneumoniae by human alveolar macrophages are influenced by opsonins. Infect. Immun. 68, 2286-2293 (2000).
- Gordon, S. B., et al. Pulmonary immunoglobulin responses to Streptococcus pneumoniae are altered but not reduced in human immunodeficiency virus-infected Malawian adults. J. Infect. Dis. 188, 666-670 (2003).
- Fullerton, D. G., et al. Domestic smoke exposure is associated with alveolar macrophage particulate load. Trop. Med. Int. Health. 14, 349-354 (2009).
- Jambo, K. C., et al. Bronchoalveolar CD4+ T cell responses to respiratory antigens are impaired in HIV-infected adults. Thorax. 66, 375-382 (2011).
- Eagan, R., et al. Lung fluid immunoglobulin from HIV-infected subjects has impaired opsonic function against pneumococci. Clin. Infect. Dis. 44, 1632-1638 (2007).
- Rose, A. S., Knox, K. S. Bronchoalveolar lavage as a research tool. Sem. Respir. Crit. Care Med. 28, 561-573 (2007).
- Wright, A. K. A., et al. Human Nasal Challenge with Streptococcus pneumoniae is Immunising in the Absence of Carriage. PLoS Pathog. , (2012).
- Bolliger, C. T., et al. ERS/ATS statement on interventional pulmonology European Respiratory Society/American Thoracic Society. Eur. Respir. J. 19, 356-373 (2002).
- Ettensohn, D. B., Jankowski, M. J., Duncan, P. G., Lalor, P. A. Bronchoalveolar lavage in the normal volunteer subject. I. Technical aspects and intersubject variability. Chest. 94, 275-280 (1988).
- Ettensohn, D. B., Jankowski, M. J., Redondo, A. A., Duncan, P. G. Bronchoalveolar lavage in the normal volunteer subject. 2. Safety and results of repeated BAL, and use in the assessment of intrasubject variability. Chest. 94, 281-285 (1988).
- De Brauwer, E. I., Jacobs, J. A., Nieman, F., Bruggeman, C. A., Drent, M. Bronchoalveolar lavage fluid differential cell count. How many cells should be counted. Anal. Quant. Cytol. Histol. 24, 337-341 (2002).
- Mtunthama, N., et al. Malawians permit research bronchoscopy due to perceived need for healthcare. J. Med. Ethics. 34, 303-307 (2008).
- Pereira, W., Kovnat, D. M., Snider, G. L. A prospective cooperative study of complications following flexible fiberoptic bronchoscopy. Chest. 73, 813-816 (1978).
- Huang, Y. C., Bassett, M. A., Levin, D., Montilla, T., Ghio, A. J. Acute phase reaction in healthy volunteers after bronchoscopy with lavage. Chest. 129, 1565-1569 (2006).
- Gritzfeld, J. F., et al. Experimental Human Pneumococcal Carriage. J. Vis. Exp. (72), (2013).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon