Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Messung der Influenza neutralisierenden Antikörperantworten gegen a/H3N2-Viren im menschlichen Serum von Microneutralization Assays mit MDCK-SIAT1 Zellen
In diesem Artikel
Zusammenfassung
Grippe neutralisierende Antikörper korrelieren mit dem Schutz der Influenza-Infektionen. Microneutralization Assays messen neutralisierende Antikörper im menschlichen Serum und dienen oft der menschlichen Grippe-Serologie. Wir beschreiben einen Microneutralization-Assay mit MDCK-SIAT1 Zellen um zu messen, neutralisierende Antikörpertiter zu zeitgenössischen 3C.2a und 3C.3a a/H3N2-Viren nach Influenza-Impfung oder Infektion.
Zusammenfassung
Neutralisierende Antikörper gegen Hämagglutinin (HA) von Influenza-Viren werden die wichtigsten Immunmechanismus angesehen, die mit Schutz für Influenza-Infektionen korreliert. Microneutralization (MN) Assays werden häufig verwendet, um neutralisierende Antikörperreaktionen im menschlichen Serum nach Influenza-Impfung oder Infektion zu messen. Verdeckte Darby Canine Kidney (MDCK) Zellen sind die häufigsten verwendeten Zelle Substrat für MN-Assays. Allerdings verändert die derzeit zirkulierenden 3C.2a und 3C.3a a/H3N2 Influenza Viren erworbenen Rezeptorspezifität Bindung. Die MDCK-SIAT1-Zell-Linie mit erhöhten α-2,6 sialic Galaktose Moieties auf der Oberfläche erweist sich verbesserte Infektiosität und treuere Repliken als herkömmliche MDCK-Zellen für diese zeitgenössischen a/H3N2-Viren zur Verfügung. Hier beschreiben wir eine MN-Assay mit MDCK-SIAT1 Zellen, die zu neutralisierende Antikörpertiter zu dieser zeitgenössischen a/H3N2-Viren quantifizieren optimiert wurde. In diesem Protokoll sind Hitze inaktiviert Sera, neutralisierende Antikörper enthält zunächst seriell verdünnt dann inkubiert mit 100 TCID50/gut von Influenza a/H3N2-Viren Antikörper im Sera binden an die Viren ermöglichen. MDCK-SIAT1 Zellen sind dann die Virus-Antikörper-Mischung hinzugefügt und inkubiert für 18-20 h bei 37 ° C, 5 % CO2 , a/H3N2-Viren MDCK-SIAT1 Zellen infizieren können. Nach der Inkubation über Nacht, sind Platten fixiert und der Virusmenge in jedem gut durch ein Enzym-linked Immunosorbentprobe Assay (ELISA) mit Anti-Grippe quantifiziert ist ein monoklonaler Antikörper Nucleoprotein (NP). Neutralisierende Antikörpertiter ist definiert als der Kehrwert der höchsten Serum Verdünnung, die ≥50 % Hemmung der Virus Infektiosität bereitstellt.
Einleitung
Influenza-Viren weiterhin Morbidität und Mortalität in der Bevölkerung jedes Jahr verursachen. HA ist die große Oberfläche Glykoprotein von Influenza-Viren. Neutralisierende Antikörper gezielt HA sind die wichtigsten Immunmechanismus, die mit dem Schutz der Influenza-Infektion1,2korreliert. Hämagglutination Inhibition (HI) Assays und MN-Assays sind zwei Methoden, die häufig verwendet, um Antikörperreaktionen im menschlichen Serum nach Grippe-Infektion oder Impfung3messen. Die HI-Assay misst Antikörper Hemmung der Virus Hämagglutination der roten Blutkörperchen und gilt als einen Surrogat-Assay. Im Gegensatz zu HI kann die MN-Assay direkt die Ebenen von Antikörpern im menschlichen Serum messen, die Influenza-Infektion in Zellkulturen zu neutralisieren. MDCK-Zellen dienen häufig Influenza Virus isoliert und MN assays4.
Influenza-Viren werden ständig Antigendrift und Shift, Erwerb von Mutationen auf HA-Proteine, die verbindliche Rezeptorspezifität Viren verändern können. Seit 2014 neue Cluster a/H3N2-Viren entstanden und weiter bis zur aktuellen Saison zirkulieren. Die meisten dieser Viren gehören zu den genetischen Gruppe 3C.2a und 3C.3a basierend auf phylogenetische Analyse der HA Proteine. Viele der zirkulierenden Viren 3C.2a Fähigkeit, die roten Blutkörperchen hemagglutinate reduziert hatte und daher können nicht von HI-Assays5geprägt sein. Neutralisation Assays müssen verwendet werden, um die Antikörperreaktionen auf diese Viren zu messen, die nicht6hemagglutinate. Darüber hinaus haben Studien gezeigt, dass diese zeitgenössischen a/H3N2-Viren Rezeptor bindende Eigenschaften im Vergleich zu früheren a/H3N2-Viren verändert und neigen dazu haben, Kultur angepasst Mutationen und Polymorphismus bei in in-vitro- Zellen passagiert akkumulieren Kulturen7,8,9. Verglichen mit konventionellen MDCK-Zellen, ist MDCK-SIAT1 eine Zell-Linie von Matrosovich Et Al. entwickelt durch stabile Transfektion von MDCK Zellen mit cDNA des menschlichen α2, 6-Sialtransferase (SIAT1). Diese Zelllinie drückt erhöhte Mengen an α2, 6-sialic Galaktose Moieties und geringere Mengen an α2, 3 sialic Acid Moieties als das übergeordnete Element MDCK Zellen10. MDCK-SIAT1 Zellen haben gezeigt, um Isolierung Preise für a/H3N2-Viren im Vergleich zu MDCK Zellen11zu verbessern. Vor kurzem, Lin Et al. berichtet, dass für frisch geschlüpfte 3C.2a und 3C.3a menschlichen a/H3N2 Influenzaviren, treuer Virus Replikationen und bessere Virus Infektiosität erreicht wurden, wenn Viren in MDCK-SIAT1-Zell-Linien im Vergleich zu MDCK Zellen7kultiviert wurden. Somit eignen sich die MDCK-SIAT1 Zellen besser in MN-Assays Antikörperantworten den jüngsten Clustern von a/H3N2-Viren zu charakterisieren.
Hier beschreiben wir eine MN-Assay mit MDCK-SIAT1 Zellen zu Antikörperreaktionen auf zeitgenössische 3C.2a und 3C.3a a/H3N2-Viren im menschlichen Serum messen. Viren, die in Eiern oder Zellen gewachsen können in diesem Test verwendet werden. Hitze inaktiviert Sera, neutralisierende Antikörper enthält sind zunächst seriell verdünnt, dann inkubiert mit 100 TCID50/gut von Influenza-a/H3N2-Virus Antikörper im Serum, um das Virus zu binden zu ermöglichen. MDCK-SIAT1 Zellen sind dann die Virus-Antikörper-Mischung hinzugefügt und für 18-20 h bei 37 ° C, 5 % CO2 erlauben das a/H3N2 Virus MDCK-SIAT1 Zellen infizieren und replizieren inkubiert. Nach der Inkubation über Nacht die Platten werden fixiert und der Virusmenge in jede Vertiefung wird von einem ELISA mit Anti-Grippe A NP monoklonalen Antikörpern quantifiziert. Die Erkennung von NP zeigt das Vorhandensein des Virus-Infektion und das Fehlen von neutralisierenden Antikörpern. Neutralisierende Antikörpertiter ist definiert als der Kehrwert der höchsten Serum Verdünnung, die ≥ 50 % Hemmung der Virus Infektiosität bereitstellt.
Protokoll
Alle Influenzaviren behandelt werden, nach geeigneten Biosafety Level-Anforderungen (BSL-2 oder höher) wie in der Biosicherheit auf Mikrobiologie und biomedizinischen Labors (BMBL)12definiert.
1. Vorbereitung der Reagenzien und Ausgangsmaterial
-
MDCK-SIAT1 Zellen und sterile Zellkulturmedium vorbereiten
- Bereiten Sie das Zellkulturmedium MDCK-SIAT1 mit 500 mL von Dulbeccos geändert Eagle Medium (DMEM) mit hoher Glucose, 10 % V/V Hitze inaktiviert fetalen bovine Serum (FBS), 2 mM L-Glutamin, 1 mM Natrium Pyruvat, 1 mg/mL G418 Sulfat (z.B. Geneticin), und 100 U/ml Penicillin mit 100 µg/mL Streptomycin (optional). Sterilisieren Sie durch Filtration durch einen 0,2 µM Porengröße Membran. G418 Sulfat wird hinzugefügt, um Plasmid Stabilität in den MDCK-SIAT1 Zellen zu gewährleisten.
- Bereiten Sie die MDCK-SIAT1 -Zell-Linie. In einer 162 cm2- Gewebekultur Flask(s) mit 30 mL sterile Zellkulturmedien, Saatgut Flaschen mit 2-2,5 x 106 MDCK-SIAT1 Zellen und Inkubation bei 37 ° C in 5 % CO2 für 2 Tage; Hiermit werden für Gewebekultur infektiöse Dosis (TCID) Bestimmung und MN Assays.
Hinweis: MDCK-SIAT1 Zellen wurden freundlicherweise von Dr. M. Matrosovich, Marburg, Deutschland10zur Verfügung gestellt. Diese Zelllinie auch kommerziell erhältlich (siehe Tabelle der Materialien).
- Bereiten Sie der sterile Virus Vermehrungsmedien mit 500 mL DMEM hohe Glukose, 0,3 % Rinderserumalbumin (BSA) Teil V, 100 U/mL Penicillin, 100 µg/mL Streptomycin und 20 mM HEPES vor. Sterilisieren Sie durch Filtration durch einen 0,2 µM Porengröße Membran.
- Bereiten Sie 0,75 % (V/V) Meerschweinchen roten Blutkörperchen (GpRBCs) in Phosphat gepufferte Kochsalzlösung (PBS) mit 0,01 M PBS, bei pH 7,2 vor.
- Bereiten Sie das sterile Virus Verdünnungsmittel verwenden DMEM hohe Glukose, 1 % Bovine Albumin Fraktion V (BSA), 100 U/mL Penicillin, 100 µg/mL Streptomycin und 20 mM HEPES vor. Sterilisieren durch Filtration mit 0,2 µm Porengröße Membran, und bereiten Sie frisch für jedes Assay.
- Bereiten Sie die kalte Zelle Fixiermittel als 80 % kaltem Aceton mit PBS-Puffer (0,01 M PBS, pH 7,2).
- Bereiten Sie den Puffer zu waschen mit PBS (0,01 M PBS pH 7,2) und 0,3 % (V/V) Tween-20.
- Bereiten Sie die Antikörper Verdünnungsmittel mit PBS (0,01 M PBS, pH 7,2), 0,3 % (V/V) Tween-20 und 5 % fettfreie trockene Milch.
- Verwenden Sie Anti-Grippe A NP Maus monoklonaler Antikörper Klon A1 und A3-Pool als den primären Antikörper. Verdünnen Sie die Antikörper Verdünnungsmittel in der optimalen Konzentration durch Titration bestimmt.
- Verwendung Ziege konjugierten Anti-Maus IgG zu Pferd Rettich Peroxidase (HRP) als sekundäre Antikörper. Verdünnen Sie die Antikörper Verdünnungsmittel in der optimalen Konzentration durch Titration bestimmt.
- Bereiten Sie das Substrat der Peroxidase mit o- Phenylendiamin Dihydrochloride (OPD) in 0,05 M Phosphat-Citrat-Puffer bei pH 5. Vorbereiten von 0,05 M Phosphat-Citrat-Puffer durch Auflösen von 1 Kapsel/100 mL entionisiertem H2O. auflösen 1 OPD-Tablette (10 mg) / 20 mL Citrat Phosphatpuffer unmittelbar vor der Anwendung.
- Verwenden Sie 0,5 M Schwefelsäure als der OPD stop-Lösung. 972 mL entionisiertem H2O in einer chemischen Kapuze 28 mL 18 M Schwefelsäure Aktie hinzufügen.
-
Behandlung von menschlichen und tierischen Seren
- Wärme zu inaktivieren die menschliche Seren in die MN-Assays in einem Wasserbad bei 56 ° C für 30 min vor der Assay verwendet. Verwenden Sie sofort oder bei Bedarf speichern Sie aufgetauten Sera bei 4 ° C für höchstens 24 h; ggf. längere Lagerzeit speichern Sie Sera gefroren bei-20 ° C oder kälter.
- Behandeln der tierischen Seren in die MN-Assays mit Rezeptor zerstören Enzym (RDE) verwendet und Hitze inaktivieren vor der Test wie folgt.
- Der Sera in einem 37 ° c Wasserbad Auftauen dann auf Eis legen. Mischen Sie 1 Volumen von tierischen Serumprobe mit 3 Bände von RDE. Inkubation bei 37 ° c für 18-20 h.
- Wärme zu inaktivieren die RDE behandelt Sera bei 56 ° c für 30 min. hinzufügen 6 Bände von PBS, pH 7,2, jede Probe für eine endgültige Vorverdünnung von 01:10. Bei Bedarf speichern Sie aufgetauten Sera bei 4 ° C für höchstens 24 h; ggf. längere Lagerzeit speichern Sie Sera gefroren bei-20 ° C oder kälter.
Hinweis: Tierische Seren enthalten verschiedene Sialinsäure Säure-Glykane an die HAs von Influenza-Viren binden und hemmen die Bindung von Grippe-spezifischen Anti-HA Antikörper. Daher ist es notwendig, RDE behandeln alle tierische Seren vor die MN-Assays, diese unspezifischen virale HA Bindemittel in die Serumproben zu entfernen.
2. Durchgang der Zellkultur MDCK-SIAT1
Hinweis: In einer biologischen Sicherheitsschrank um Kontaminationen zu vermeiden müssen alle Zellkulturen durchgeführt werden.
- Dekantieren Sie Zellkulturmedium aus der Zelle Monolayer in 162 cm2 Flaschen. Trypsinize der Zellen durch Spülen der Monolage mit Trypsin-EDTA. Fügen Sie 5 mL Trypsin-EDTA zur Deckung der Zelle monomolekularen Film hinzu. Inkubation bei 37 ° C, 5 % CO2 bis der Monolayer (5-10 min) löst. Jede Flasche enthält trypsiniert Zellen, Pipette rauf und runter, um Zellen zu trennen fügen Sie 15 mL MDCK-SIAT1 Zellkulturmedien hinzu.
- Verwenden Sie einen Hemocytometer und Trypan blau, um festzustellen, dass die Zelle zählt und Lebensfähigkeit. Die Zellen im neuen 162 cm2 Gewebekultur Fläschchen mit 30 mL von Zellkulturmedien mit 2-2,5 x 106 Zellen /flask Saatgut und Inkubation bei 37 ° C mit 5 % CO2 für 2 Tage für den Einsatz in TCID und MN-Assays. Samen Zellen bei 4-5 x 106 Zellen/Kolben und Inkubation bei 37 ° C mit 5 % CO2 für 2 Tage für den Einsatz in Virus-Vermehrung.
Hinweis: Die Aussaatdichte kann angepasst werden, wenn Kultur für kürzere oder längere Zeiträume sind erwünscht. Für die Vermehrung der Viren, Zellen über 100 % erreichen Konfluenz. Für Gewebekultur Infektion Dosis (TCID) und MN Assays sollte die Zellen 75-95 % Konfluenz (Abbildung 1).
(3) Verbreitung von a/H3N2-Viren in MDCK-SIAT1 Zellen
Hinweis: A/H3N2 Virus kann entweder im 10. / 11. Tag vermehrt werden alte embryonierten Henne nach Standardprotokoll3oder MDCK-SIAT1 Zelle Kulturen Eiern. MDCK-SIAT1 Zellen über 100 % erreichen confluency Virus Impfung. Virus-Saatgut kann mit mehreren Verdünnungen des Inokulums geimpft werden. Das Inokulum Verdünnungen mit die beste Ernte HA und Infektiosität können für weitere MN Assays verwendet werden.
- Entfernen Sie das Zellkulturmedium aus der Zelle Monolayer (> 100 % Konfluenz) in 162 cm2 Flaschen. Die monomolekularen Film zweimal mit 15 mL sterile 0,01 M PBS, pH 7,2, waschen und dekantieren.
- Kennzeichnen Sie 1 Flasche als Kontrolle zu und 20 mL Virus Vermehrungsmedien. Inkubation bei 37 ° C mit 5 % CO2Flasche. Lassen Sie dieses Fläschchen unangetastet und benutzen Sie zum Vergleich nach Tag 1 der Virus-Vermehrung.
- Die Flask(s) 10 mL sterile Virus Vermehrungsmedien hinzu und inkubieren Sie alle Flask(s) bei 37 ° C, 5 % CO2. Ein Fläschchen mit Influenza-Virus-Lager bei Raumtemperatur auftauen dann auf Eis legen. Mit den Virus Vermehrungsmedien, die Ziel-Verdünnungen verdünnen.
Hinweis: Ziel Verdünnungen einstellbar ist basiert auf HA-Titer von Virus-Aktien. Zur Vorbereitung einer 1: 1000 verdünnt Inokulum, 100 µL des Virus zu 9,9 mL sterile Virus Vermehrungsmedien hinzufügen. Invertieren Sie sanft zu, entfernen Sie 1 mL 1: 100 Verdünnung bis 9 mL sterile Virus Vermehrungsmedien, invertieren Sie sanft für eine 1: 1000 verdünnt Inokulum zu. Auf Eis legen. - Entfernen Sie alle Flaschen außer Kontrolle-Kolben aus dem Inkubator. Entfernen Sie die Virus-Vermehrung-Medien aus Flask(s) MDCK-SIAT1 Zellen und impfen Sie jede Flasche mit 10 mL der verdünnten Virus zu. Inkubieren Sie die Fläschchen bei 37 ° C, 5 % CO2 für 1 h, rotierenden Flask(s) alle 15 min.
- Entfernen Sie 5 mL Inokulum aus der Flask(s) und ersetzen Sie durch 15 mL Virus Vermehrungsmedien mit 1 µg/mL TPCK-Trypsin. Inkubieren Sie die Flask(s) bei 37 ° C, 5 % CO2 für 16-18 h.
- Nach der Übernachtung Inkubation beobachten die Flask(s) unter 100 X Mikroskop-Vergrößerung und suchen nach zytopathischen Effekte (CPE) auf die Zellen. Entfernen Sie 15-17 mL überstand-Virus aus der Flask(s) und ersetzen Sie durch 15-17 mL frisch zubereitete Virus Vermehrungsmedien mit 2 µg/mL TPCK-Trypsin.
- Inkubieren Sie die Fläschchen bei 37 ° C, 5 % CO2. Überwachen Sie CPE Monolayer (im Vergleich zu der Zelle Kontrolle Küvette) zu und überprüfen Sie die HA in regelmäßigen Abständen (alle 4 h) mit 0,75 % GpRBC bis zur Ernte.
- Richten Sie eine HA-96-Well Mikrotiterplatte. Fügen Sie 50 µL 0,01 M PBS, pH 7,2 bis Brunnen A2 - A12 und B2 - B12 (Duplikate), und Wells H1 - H12 für Kontrolle.
- A1 und A2 fügen Sie 100 µL des Virus überstand hinzu, führen Sie eine 2-fold serielle Verdünnung von A1 und B1 durch A12 und B12. Nach dem Mischen in A12 und B12 50 µL zu verwerfen. Fügen Sie 50 µL von 0,75 % GpRBCs Reihen A, B und H hinzu.
- Tippen Sie auf die Platte und Inkubation bei Raumtemperatur für 1 h.
- HA des Virus Überstand durch Kippen der 96-Well Mikrotiterplatte auf 45°, 60° Winkel zu bestimmen.
- Platten für Hämagglutination zu lesen; die höchsten Verdünnung des Virus, das komplette Hämagglutination erreicht gilt HA Titration Endpunkt für die spezifischen Virus. Aufzeichnung der Kehrwert der höchsten Virus Verdünnung mit vollständigen Hämagglutination als HA-Titer des Virus.
Hinweis: Die sesshaften RBCs in Reihe H (Steuerelemente) sollte anfangen zu "laufen" und eine kleine Träne-form aufgrund der Schwerkraft. Warten Sie, bis der Erythrozyten in der Steuerung, die Brunnen zu beenden lesen ausgeführt, dann die RBC-Schaltflächen in der Virus Titration Brunnen. Diejenigen, die zeigen RBC Tasten und "Run", erzielen nicht Hämagglutination. Suchen Sie die höchsten Verdünnung des Virus, die völlig Hämagglutination als Endpunkt HA Titer des Virus hemmen.
- Das Virus zu ernten, wenn HA der Virus Kultur Hochebenen oder Virus-Kultur das Ziel HA erreicht (z. B. > 16 HAU), aber vor der Zelle monomolekularen Film beginnt zu erheblichen CPE angezeigt.
- Zentrifugieren Sie die Virus-Kultur bei 300 X g für 10 min bei 4 ° C, die Zelltrümmer pellet überstand. Den geklärten überstand mit der Virus-Ernte in ein sauberes Röhrchen zu übertragen. Aliquoten der Überstand mit dem Virus in Einweg-sterile kryogenen Fläschchen zu ernten und Einfrieren sofort bei-70 ° C oder kälter.
Hinweis: Der Virus-Bestände für die MN-Assays verwendet sollte hoch infektiöse Titer und minimalen defekten Partikel haben. Die minimale Verdünnung des Virus Aktien zu 100 TCID5050 µL für MN-Assay ist 1: 100.
Hinweis: Der Virus-Bestände in die MN-Assays verwendet sollte nicht aufgetaut eingefroren und.
- Zentrifugieren Sie die Virus-Kultur bei 300 X g für 10 min bei 4 ° C, die Zelltrümmer pellet überstand. Den geklärten überstand mit der Virus-Ernte in ein sauberes Röhrchen zu übertragen. Aliquoten der Überstand mit dem Virus in Einweg-sterile kryogenen Fläschchen zu ernten und Einfrieren sofort bei-70 ° C oder kälter.
4. Bestimmung der TCID des Virus
- Tag 1: Virus titration
- Tauen Sie ein Fläschchen des Virus bei Raumtemperatur auf und sofort auf Eis.
- Testen Sie das Virus bei zwei verschiedenen ab Verdünnungen: 10-2 und 10-3. 9,9 mL Virus Verdünnungsmittel für 10-2 Verdünnung 100 µL des Virus hinzufügen. 1 mL 10-2 Verdünnung bis 9,0 mL des Virus Verdünnungsmittel für 10-3 Verdünnung zugeben.
- Mit zwei Mikrotiter hinzufügen Platten (Platte 1 für 10-2 Verdünnung) und Platte 2 für 10-3 Verdünnung 100 µL des Virus Verdünnungsmittel in alle Vertiefungen mit Ausnahme der Spalte 1 von 96-Well Mikrotiterplatte.
- Führen Sie ½log10 Verdünnungen (10-2, 10-2,5, 10-3, etc.). Fügen Sie 146 µL des Virus ab Verdünnung in alle Vertiefungen in Spalte 1 und übertragen Sie 46 µL von Säule 1 durch Spalte 11 (Abbildung 2) seriell. Änderung Pipettenspitzen zwischen Brunnen. Nach dem Mischen Spalte 11, verwerfen Sie die Spitzen mit 46 µL Verdünnung.
- Verwenden Sie Spalte 12 als Cell Control (CC); Es enthält nur Virus Verdünnungsmittel. Inkubation für 1 h bei 37 ° C, 5 % CO2.
- Tag 1: Vorbereitung der MDCK-SIAT1 Zellen
Hinweis: Die MDCK-SIAT1 Cell Monolayer sollte 75-95 % Konfluenz für TCID und MN Assays erreichen. Ein 162 cm2 Kolben bei 95 % Konfluenz sollte genügend Zellen Samen liefern ~ 4-5 Mikrotiter-Platten.- Waschen Sie die 75-95 % konfluierende Monolage mit 20 mL PBS, der FBS in der Kulturmedien zu entfernen. Trypsinize die Zellen wie folgt.
- Spülen Sie der Monolage mit sterilen PBS, fügen Sie 7 mL Trypsin-EDTA zur Deckung der Zelle monomolekularen Film hinzu. Legen Sie den Kolben flach und Inkubation bei 37 ° C, 5 % CO2 bis der Monolayer (ca. 5-10 min) löst. Jede Flasche enthält die trypsiniert Zellen fügen Sie 7 mL Virus Verdünnungsmittel hinzu.
- Waschen Sie die Zellen mit Virus Verdünnungsmittel, die FBS zu entfernen.
- Pipette vorsichtig nach oben und unten um die Zellen zu trennen. Übertragen Sie die Zellen auf ein 50 mL konische Rohr; Füllen Sie das Rohr mit Virus Verdünnungsmittel.
- Zentrifugieren bei 485 X g für 5 min. Dekantieren das Virus Verdünnungsmittel, ersetzen mit frischen 50 mL Virus Verdünnungsmittel und Zentrifugieren bei 485 X g für 5 min. Dekantieren Verdünnungsmittel Virus und durch frische Virus Verdünnungsmittel (10 mL/Flasche), das Pellet aufzuwirbeln.
- Verwenden Sie einen Hemocytometer und Trypan blau um die Zellzahl und die Lebensfähigkeit zu bestimmen. Passen Sie die Zellkonzentration mit dem Virus auf 1,5 x 105 Zellen/mL Verdünnungsmittel.
- Fügen Sie 100 µL verdünnter MDCK-SIAT1 Zellen in jede Vertiefung der Mikrotiterplatten (1,5 x 104 Zellen/Brunnen) und Deckplatten Sie die ab. Inkubation bei 37 ° C, 5 % CO2 für 18-20 h.
- Waschen Sie die 75-95 % konfluierende Monolage mit 20 mL PBS, der FBS in der Kulturmedien zu entfernen. Trypsinize die Zellen wie folgt.
- Tag 2: ELISA
-
Fixierung der Zellen
- Entfernen Sie das Medium aus der Mikrotiter-Platten. Waschen Sie jeweils gut mit 200 µL PBS. Jedes gut 300 µL kaltem 80 % Aceton hinzu und Inkubation bei Raumtemperatur für 10 min. das Fixiermittel zu entfernen und die Platten an der Luft trocknen lassen.
-
ELISA
-
Primärantikörper Zusatz
Hinweis: Anti-Grippe A NP monoklonaler Antikörper sollte als den primären Antikörper im ELISA im Übermaß verwendet werden. Bestimmen Sie die optimale Antikörper-Verdünnung für jede Menge Primärantikörper indem Sie Antikörper Titrationen in MN ausführen. Wählen Sie die primären Antikörper-Konzentration, die im Übermaß und mit der besten Signal-Hintergrund-Verhältnis ist.- Der Anti-Grippe A NP monoklonale Antikörper (Primärantikörper) um die Zielkonzentration in der Antikörper Verdünnungsmittel verdünnen (z. B. hinzufügen 30 µL Primärantikörper 30 mL des Antikörpers Verdünnungsmittel für eine Ziel-Verdünnung von 1: 1000).
- Waschen Sie Platten 3-Mal mit 300 µL Waschpuffer. Fügen Sie 100 µL verdünnter Primärantikörper in jede Vertiefung. Inkubation bei Raumtemperatur für 1 h.
-
Sekundärantikörper Zusatz
Hinweis: Ziege anti-Maus IgG, Meerrettich konjugiert Peroxidase (HRP) sollte im Übermaß als Sekundärantikörper in ELISA verwendet werden. Bestimmen Sie die optimale Antikörper-Verdünnung für jede Menge sekundäre Antikörper durch Antikörper Titrationen durchführen. Wählen Sie die sekundäre Antikörper-Konzentration im Übermaß und mit der besten Signal-Hintergrund-Verhältnis.- Verdünnen Sie die Ziege Anti-Maus, die IgG an HRP Antikörper (Sekundärantikörper) konjugiert, die Zielkonzentration in der Antikörper Verdünnungsmittel (z.B. hinzufügen 7,5 µL Sekundärantikörper bis 30 mL des Antikörpers Verdünnungsmittel für ein Ziel 1:4000 Verdünnung).
- Waschen Sie die Platten 3 Mal mit 300 µL Waschpuffer. Jedes gut 100 µL verdünnter Sekundärantikörper hinzufügen. Inkubation bei Raumtemperatur für 1 h.
-
Zugabe von Substrat und Platte lesen
- Waschen Sie die Platten 5 Mal mit 300 µL Waschpuffer und tippen Sie auf ein fusselfreies Tuch.
- Jedes gut 100 µL der frisch zubereiteten Substrat hinzu und Inkubation bei Raumtemperatur bis die Farbentwicklung sättigt und die optische Dichte (OD) der Zelle Kontroll-Vertiefungen < 0,2.
- Alle Brunnen 100 µL Stopplösung hinzufügen. Lesen die OD Wells in 490 nm mit einer Mikrotestplatte Spektralphotometer.
-
Primärantikörper Zusatz
-
Fixierung der Zellen
- TCID 50 Berechnung
- Berechnen Sie den Median OD490 der Zelle Steuerelemente (Spalte 12).
- Betrachten Sie alle Test gut mit einem OD-490 größer als zweimal den Median OD490 der CC Brunnen als "positiv"; Andernfalls gilt es "negativ".
- Berechnen Sie die TCID50 das Virus mit dem Reed-Muench Methode13.
- Bestimmen Sie die Anzahl der positiven und negativen bei jeder Verdünnung.
- Berechnen Sie die "kumulative positiv", "Kumulierte negative", "Ratio" und "% positiv" als in Tabelle 1dargestellt.
- Berechnen Sie den "proportionalen Abstand" zwischen der Verdünnung mit > 50 % positive und Verdünnung zeigt < 50 % positive unter Verwendung der folgenden:
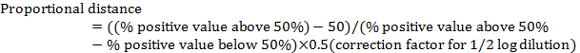
Hinweis: Der Korrekturfaktor für ½ Log Verdünnung ist 0,5. Zum Beispiel in Tabelle 1: (80 − 50) /(80 − 20) x 0,5 = 0,25 - Berechnen Sie das Virus TCID50 , indem der proportionalen Abstand zur Verdünnung mit > 50 % positiv.
Hinweis: zum Beispiel in Tabelle 2, TCID50 ist 10-5+(-0.25) = 10-5.25. Hinweis: Dies ist die neue50 des Virus pro 100 µL (oder 10-5.25100 µL).
- Berechnen Sie die Virus-Verdünnung. Verdünnen Sie für MN-Assays das Virus auf 200 TCID50100 µL (entspricht 100 TCID5050 µL pro Well).
Hinweis: Im Beispiel in Tabelle 1ist 1 TCID50 10-5.25 in 100 µL und die Verdünnung 200 TCID50100 µL zu erreichen ist 1:891 auf der Grundlage der Berechnungen: 200 x 10-5.25 = 10-2.95 = 1/102,95 = 1 / 891
(5) MN-Assay mit MDCK-SIAT1 Zellen
-
Tag 1: Prüf-, Steuer- und Sera Vorbereitung und Platte layout
- Der Sera in 37 ° C Wasserbad Auftauen und sofort nach dem Auftauen zu entfernen. Aliquot den Betrag von Seren, die getestet werden soll; ein Minimum von 10 µL des ursprünglichen Sera ist erforderlich, mit einem Virus im Unterhemd zu testen. Testen Sie wenn möglich Sera in Duplikate.
- Wärme zu inaktivieren die menschliche Seren für 30 min im Wasserbad 56 ° C wie in Schritt 1.12.1. Ort Sera am Eis post Hitzeinaktivierung, fügen Sie das Virus Verdünnungsmittel Seren Erreichung einer 01:10 Vorverdünnung.
- RDE zu behandeln und vor tierischen Seren um 01:10 für Steuerelemente pro 1.12.2 verdünnen.
Hinweis: Aufgetaut und behandelten menschliche und tierische Seren können bei 4 ° C gespeichert werden, für nicht mehr als 24 Std. Sera bei-20 ° C eingefroren gelagert werden sollte oder kälter, wenn längere Lagerzeit vor der Test benötigt wird. - Um mit einem Virus zu testen, fügen 100 µL 01:10 verdünnt Sera Spalten A1 bis A10 (Abbildung 4). Hinzu kommt 50 µL des Virus Verdünnungsmittel Reihen B und H, mit Ausnahme von Spalten 11 und 12 (Abbildung 4). Führen Sie eine 2-fold serielle Verdünnung von Zeilen A bis H, und entsorgen Sie die letzten 50 µL in Reihe H (Abbildung 4).
Hinweis: Wenn mehrere Viren getestet werden sollen, können Sera in Titer Röhren verdünnt werden. Die Verdünnung des Serums, für der Zweck der Bestimmung der Serum-Titer, gut a 01:10, gut B 01:20, na C 01:40, gut D 1: 80, gut E 1: 160, gut F 1:320, gut G 1:640, auch H 1:1,280 (Abbildung 4). - Für das Virus-Steuerelement hinzufügen 50 µL des Virus Verdünnungsmittels Brunnen A12, B12, C12 und D12 (keine Sera). Die Zellkontrolle hinzufügen 100 µL des Virus Verdünnungsmittels Brunnen E12, F12 und G12 H12 (keine Viren, keine Sera).
- Fügen Sie für die Kontrolle Sera (z. B. Frettchen Seren Kontrollen) 100 µL verdünnter Kontrolle Sera nun eine Spalte 11 und Brunnen B11 - H11 50 µL des Virus Verdünnungsmittel hinzufügen hinzu. Serielle verdünnte nach unten.
- Die Abdeckplatten, Inkubation bei 37 ° C, 5 % CO2 bis bereit für den Virus-Zusatz.
-
Tag 1: Virus Zusatz
- Verdünnen Sie das Virus auf 100 TCID5050 µL mit Virus Verdünnungsmittel.
- Fügen Sie 50 µL verdünnter Virus in alle Vertiefungen, mit Ausnahme der Spalte 11 auf die hinteren Titration (BT)-Platten und die Zelle-Kontroll-Vertiefungen E12, F12 und G12 H12 auf allen Platten (Abbildung 4). Fügen Sie Virus für diese Platten mit Kontrolle Sera in Spalte 11 hinzu Spalte 11.
- Titration (BT) zurück
- Schließen Sie eine BT in Spalte 11 aus einer Reihe von doppelten Platten (z. B. Platte 1A und 1 b). Alle Brunnen in Spalte 11 50 µL des Virus Verdünnungsmittel hinzufügen. Die erste Bohrung (A11) 50 µL des Virus bei 100 TCID5050 µL hinzufügen. Mischen von Pipettieren rauf und runter.
- Mischen und 50 µL in aufeinander folgenden Vertiefungen 2-fold Verdünnungsreihen durchführen zu übertragen. Ändern Sie die Pipettenspitzen zwischen Brunnen, Virus Verschleppung zu vermeiden. Entsorgen Sie 50 µL aus gut H11.
- Fügen Sie 50 µL des Virus Verdünnungsmittel, Spalte 11 bringen das Endvolumen in 100 µL. Tippen Sie auf die Platten zu mischen.
- Inkubieren Sie Platten bei 37 ° C, 5 % CO2 für 1 h.
- Führen Sie MDCK-SIAT1 Zelle neben am 1. Tag und ELISA am Tag 2 wie in 4.2 und 4.3 (auch in 5.3 und 5.4 beschrieben) beschrieben
-
1. Tag: MDCK-SIAT1 Zelle neben
- Bereiten Sie die MDCK-SIAT1-Zellen wie unter Punkt 4.2 beschrieben. 100 µL MDCK-SIAT1 Zellen bei 1,5 x 105 Zellen/mL in jede Vertiefung (1,5 x 104 Zellen/Brunnen) hinzufügen. Inkubieren Sie die Platten bei 37 ° C, 5 % CO2 für 18-20 h.
-
Tag 2: ELISA
- Befestigen Sie nach Übernachtung Inkubation, am zweiten Tag die Zellen mit 80 % kaltem Aceton, wie unter Punkt 4.3 beschrieben.
-
Primärantikörper Zusatz
- Waschen Sie die Platten 3 Mal mit 300 µL Waschpuffer. Der Anti-Grippe A NP monoklonale Antikörper (Primärantikörper) zur optimalen Konzentration bestimmt durch Titration in Antikörper Verdünnungsmittel verdünnen (z. B. hinzufügen 30 µL Primärantikörper 30 mL des Antikörpers Verdünnungsmittel für eine Ziel-Verdünnung von 1: 1000).
Hinweis: 100 µL Primärantikörper wird pro Bohrloch benötigt. ~ 10 mL braucht man pro Platte. - Fügen Sie 100 µL verdünnter Primärantikörper in jede Vertiefung. Inkubation bei Raumtemperatur für 1 h.
- Waschen Sie die Platten 3 Mal mit 300 µL Waschpuffer. Der Anti-Grippe A NP monoklonale Antikörper (Primärantikörper) zur optimalen Konzentration bestimmt durch Titration in Antikörper Verdünnungsmittel verdünnen (z. B. hinzufügen 30 µL Primärantikörper 30 mL des Antikörpers Verdünnungsmittel für eine Ziel-Verdünnung von 1: 1000).
-
Sekundärantikörper Zusatz
- Waschen Sie Platten 3-Mal mit 300 µL Waschpuffer. Verdünnen Sie die Ziege anti-Maus IgG konjugiert an HRP Antikörper (sekundäre Antikörper), die Zielkonzentration in Antikörper Verdünnungsmittel (z.B. hinzufügen 7,5 µL Sekundärantikörper bis 30 mL des Antikörpers Verdünnungsmittel für ein Ziel-1:4000.)
Hinweis: 100 µL der Sekundärantikörper ist auch pro 96 erforderlich. ~ 10 mL braucht man pro Platte. - Jedes gut 100 µL verdünnter Sekundärantikörper hinzufügen. Inkubation bei Raumtemperatur für 1 h.
- Waschen Sie Platten 3-Mal mit 300 µL Waschpuffer. Verdünnen Sie die Ziege anti-Maus IgG konjugiert an HRP Antikörper (sekundäre Antikörper), die Zielkonzentration in Antikörper Verdünnungsmittel (z.B. hinzufügen 7,5 µL Sekundärantikörper bis 30 mL des Antikörpers Verdünnungsmittel für ein Ziel-1:4000.)
-
Zugabe von Substrat und Platte lesen
- Waschen Sie die Platten 5 Mal mit 300 µL Waschpuffer und tippen Sie auf fusselfreien Tuch.
- Jedes gut 100 µL der frisch zubereiteten Substrat hinzu und bei Raumtemperatur inkubieren, bis die Virus-Kontroll-Vertiefungen eine OD490 erreichen = 0,8 - 3, mit der Zelle-Steuerung auf einem niedrigen Hintergrund OD490 < 0,2.
- Alle Brunnen 100 µL der Stopplösung hinzufügen. Lesen die OD Wells in 490 nm mit einer Mikrotestplatte Spektralphotometer.
-
Datenanalyse
Hinweis: Die MN-Berechnungen werden für jede Platte individuell festgelegt.- Neutralisierende Antikörpertiter von jeder Serumprobe zu bestimmen.
- Berechnen Sie die OD490 Cut-off von 50 % Virus Neutralisierung für jede Platte unter Verwendung der folgenden Gleichung:
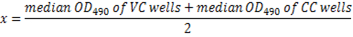
Hinweis: Hier X = 50 % von der Neutralisation Cut-off. Die gegenseitige Serum Verdünnung entspricht der höchsten Verdünnung mit OD490 gilt weniger als 50 % der Cut-Off (≥50 % Inhibition) die Neutralisation Antikörpertiter für die Serumprobe (Abbildung 5).
- Berechnen Sie die OD490 Cut-off von 50 % Virus Neutralisierung für jede Platte unter Verwendung der folgenden Gleichung:
- Überprüfen Sie, ob die Zelle-Kontroll-Vertiefungen eine OD490 haben < 0,2 und die Virus-Kontroll-Vertiefungen haben eine OD490 = 0,8 - 3.
- Überprüfen Sie, ob die Virus-Infektiosität in jedem Assay (100 X TCID50) durch Virus BT der zulässige Bereich der BT 50, 100 oder 200 TCID ist. Wenn mit der gleichen Cut-off wie im Schritt 4.4.2 definiert, sollte die höchste Virus Verdünnung in der BT-Spalte mit OD über der Cut-off in Brunnen E11, F11, G11.
Hinweis: Die Serum Positivkontrollen sollten geben Titer innerhalb 2-Fach der in den vorangegangenen Tests ermittelten Werte. Der OD-490 des Kontrollstreifens negativen Serum sollte ähnlich wie bei der Viruskontrolle.
- Neutralisierende Antikörpertiter von jeder Serumprobe zu bestimmen.
Ergebnisse
Bestimmung der die Infektiosität der Virus Bestände ist der erste Schritt bei der MN-Assay. Abbildung 2 veranschaulicht die Platte Layout um die TCID50 der Virus Bestände zu bestimmen. Für Virus Bestände mit unbekannten Infektiosität kann das Virus aus mehreren Pre-Verdünnungen, z.B. 10-2 und 10-3, titriert werden, um die beste Titration Kurve zur Berechnung der Infektiosität des Virus zu erfassen. Die Virus-Menge in d...
Diskussion
Die MN-Assay ist eines der wichtigsten Assays für Influenza Serologie zur Antikörperantworten nach Influenza-Infektion oder Impfung eingesetzt. Titer von MN-Assays generiert werden oft als die primären Endpunkt vieler Grippe Seroepidemiology Studien verwendet. MN-Assays sind auch für Sero-Diagnostik und der Bewertung der Impfstoff Immunogenität verbreitet. Internationalen Inter Lab Studien wurden durchgeführt, um MN Assays trat in mehreren Laboratorien14zu vergleichen.
Offenlegungen
Die Autoren berichten keinen Interessenskonflikt. Die Ergebnisse und Schlussfolgerungen in dieser Publikation sind diejenigen der Autoren und repräsentieren nicht unbedingt die Ansichten der Centers for Disease Control and Prevention und die Leistungsträger.
Danksagungen
Wir danken Dr. Xiuhua Lu, Dr. Feng Liu und Frau Ashley Burroughs aus der Influenza-Division des CDC für ihre kritische Überprüfung und Unterstützung bei der Vorbereitung dieser Handschrift. Wir danken Dr. Adrian Reber von Influenza Division des CDC für seine Hilfe bei der Vorbereitung der Grafik in Abbildung 3. Zu guter Letzt bedanken wir uns bei Dr. M. Matrosovich, Marburg, Deutschland für die Bereitstellung der MDCK-SIAT1-Zellen.
Materialien
| Name | Company | Catalog Number | Comments |
| Dulbecco’s Modified Eagle Medium (DMEM) with high Glucose | Life Science | 11965 | A critical component of Sterile Cell Culture, Virus Propagation and Virus Diluent Media |
| Fetal bovine serum (FBS) | Hyclone | SH30070.03 | |
| Bovine Serum Albumin (BSA) Fraction V, Protase Free | Sigma-Aldrich | 3117332001 | |
| L-Glutamine | Life Science | 25030-081 | |
| Sodium pyruvate | Life Science | 11360-070 | |
| Geneticin G-418 disulfate salt | Sigma-Aldrich | A1720-5G | |
| HEPES | Life Science | 15630-080 | |
| Penicillin/Streptomycin | Life Science | 15140-122 | |
| Acetone | VWR | 67-64-1 | Used at an 80% concentration |
| Phosphate-Citrate Buffer with Sodium Perborate | Sigma-Aldrich | SLBF2806V | |
| O-Phenylenediamine Dihydrochloride tablet | Sigma-Aldrich | SLBQ1086V | 1 tablet per 100ml of cell culture grade water |
| Sulfuric Acid | Fisher Scientific | A510-P500 | Used 0.5M final concentration |
| Ethanol, Denatured, 4L | VWR | EM-AX0422-3 | Used at an 70% concentration |
| Trypsin-EDTA | Life Science | 1748048 | |
| RDE II "Seiken" | Denka Seiken | 370013 | |
| Tween 20 | Sigma-Aldrich | P1379-500ml | |
| Anti-NP mouse monoclonal Ab | Millipore pool | MAB 8257 MAB 8258 | |
| Anti-mouse IgG HRP | KPL | 074-1802 | |
| 96-well flat-bottom plates | Thermo Scientific | 3455 | |
| Plate reader | Molecular Device | Spectromax 384 plus | |
| Cell Culture Flask 162 cm2/Vent Cap | Corning/VWR | 3151 |
Referenzen
- Reber, A., Katz, J. Immunological assessment of influenza vaccines and immune correlates of protection. Expert Rev of Vaccines. 12, 519-536 (2013).
- Li, C. K., Rappuoli, R., Xu, X. N. Correlates of protection against influenza infection in humans--on the path to a universal vaccine?. Curr Opin in Immunol. 25, 470-476 (2013).
- WHO Global Influenza Surveillance Network. . Manual for the labratory diagnosis and virological surveillence of influenza. , (2011).
- Govorkova, E. A., Kodihalli, S., Alymova, I. V., Fanget, B., Webster, R. G. Growth and immunogenicity of influenza viruses cultivated in Vero or MDCK cells and in embryonated chicken eggs. Dev Biological Stand. 98, 39-51 (1999).
- Levine, M. Z., et al. Neutralizing Antibody Responses to Antigenically Drifted Influenza A(H3N2) Viruses among Children and Adolescents following 2014-2015 Inactivated and Live Attenuated Influenza Vaccination. Clin Vaccine Immunol : CVI. 23, 831-839 (2016).
- Lin, Y., et al. The characteristics and antigenic properties of recently emerged subclade 3C.3a and 3C.2a human influenza A(H3N2) viruses passaged in MDCK cells. Influenza Other Respir Viruses. , (2017).
- Lin, Y. P., et al. Neuraminidase receptor binding variants of human influenza A(H3N2) viruses resulting from substitution of aspartic acid 151 in the catalytic site: a role in virus attachment?. J of Virol. 84, 6769-6781 (2010).
- Skowronski, D. M., et al. Mutations acquired during cell culture isolation may affect antigenic characterisation of influenza A(H3N2) clade 3C.2a viruses. Euro Surveillance. 21, 30112 (2016).
- Matrosovich, M., Matrosovich, T., Carr, J., Roberts, N. A., Klenk, H. D. Overexpression of the alpha-2,6-sialyltransferase in MDCK cells increases influenza virus sensitivity to neuraminidase inhibitors. J of Virol. 77, 8418-8425 (2003).
- Oh, D. Y., Barr, I. G., Mosse, J. A., Laurie, K. L. MDCK-SIAT1 cells show improved isolation rates for recent human influenza viruses compared to conventional MDCK cells. J Clin Microbiol. 46, 2189-2194 (2008).
- US Department of Health and Human Services. . Biosafety in Microbiological and Biomedical Laboratories. , (2009).
- Reed, H. M. A simple method of estimating fifty percent endpoints. The American Journal of Hygiene. 27, (1938).
- Laurie, K. L., et al. International Laboratory Comparison of Influenza Microneutralization Assays for A(H1N1)pdm09, A(H3N2), and A(H5N1) Influenza Viruses by CONSISE. Clinical Vaccine Immunol : CVI. 22, 957-964 (2015).
- Lin, Y., Gu, Y., McCauley, J. W. Optimization of a Quantitative Micro-neutralization Assay. J Vis Exp : JoVE. , (2016).
- van Baalen, C. A., et al. ViroSpot microneutralization assay for antigenic characterization of human influenza viruses. Vaccine. 35, 46-52 (2017).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten