Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Grippe neutralisante d’anticorps aux virus a (H3N2) dans le sérum humain par micro-neutralisation de mesure des analyses utilisant des cellules de MDCK-SIAT1
Dans cet article
Résumé
Les anticorps neutralisants de grippe sont en corrélation avec protection des infections grippales. Tests de micro-neutralisation mesurent les anticorps neutralisants dans des sérums humains et sont souvent utilisés pour la sérologie humaine de la grippe. Nous décrivons un essai de micro-neutralisation en utilisant des cellules de MDCK-SIAT1 pour mesurer les titres d’anticorps neutralisants à virus a (H3N2) 3C.2a et 3C.3a contemporains après vaccination contre la grippe ou une infection.
Résumé
Des anticorps neutralisants dirigés contre l’hémagglutinine (HA) des virus grippaux sont considérés comme le principal mécanisme immunitaire qui est en corrélation avec la protection pour les infections grippales. Tests de micro-neutralisation (MN) sont souvent utilisés pour mesurer la production d’anticorps neutralisants dans des sérums humains après vaccination contre la grippe ou une infection. Les cellules de Madine Darby Canine Kidney (MDCK) sont le substrat de la cellule utilisée couramment pour des dosages de MN. Toutefois, 3C.2a et 3C.3a la grippe a (H3N2) ont acquis des virus actuellement en circulation modifiée spécificité de liaison du récepteur. La lignée de cellules de MDCK-SIAT1 avec portions accrue α-2,6 sialique galactose sur la surface s’est avéré d’infectiosité améliorée et réplications plus fidèles que les cellules MDCK conventionnelles prévoient ces virus a (H3N2) contemporains. Nous décrivons ici un essai de MN en utilisant des cellules de MDCK-SIAT1 qui a été optimisé afin de quantifier les titres d’anticorps neutralisants de ces virus a (H3N2) contemporains. Dans ce protocole, sérums de chaleur inactivé contenant les anticorps neutralisants sont tout d’abord dilués en série, puis incubées avec 100 TCID50/bien des virus de la grippe a (H3N2) pour permettre des anticorps dans le sérum pour lier aux virus. Des cellules de MDCK-SIAT1 sont ensuite ajoutées au mélange des anticorps du virus et incubés pendant 18 à 20 h à 37 ° C, 5 % de CO2 pour permettre à des virus a (H3N2) d’infecter des cellules de MDCK-SIAT1. Après une nuit d’incubation, les plaques sont fixées et la quantité de virus dans chaque bien est quantifiée par un dosage immuno-enzymatique (ELISA) à l’aide contre la grippe une nucléoprotéine (NP) des anticorps monoclonaux. Titre d’anticorps de neutralisation est définie comme l’inverse de la plus forte dilution de sérum qui fournit ≥50 % d’inhibition de l’infectiosité du virus.
Introduction
Virus de la grippe continuent à cause de morbidité et mortalité chez l’homme chaque année. HA est la glycoprotéine de surface importante des virus grippaux. Les anticorps neutralisants ciblant HA constituent le principal mécanisme immunitaire qui est en corrélation avec la protection de l’influenza infection1,2. Tests d’hemagglutination inhibition (HI) et MN essais sont deux méthodes largement utilisés pour mesurer la production d’anticorps dans le sérum humain après grippe infection ou la vaccination3. Le test HI mesure inhibition des anticorps d’hémagglutination virus des globules rouges et est considéré comme un test de substitution. Contrairement à HI, le dosage de MN peut mesurer directement le taux d’anticorps dans le sérum humain qui neutralisent l’infection grippale dans des cultures cellulaires. Des cellules de MDCK sont souvent utilisés dans l’isolement du virus grippal et MN essais4.
Virus de l’influenza subissent constamment la dérive antigénique et Maj, acquérir des mutations sur les protéines HA pouvant modifier la spécificité de liaison du récepteur du virus. Depuis 2014, nouveaux groupes de virus a (H3N2) ont émergé et ont continué à circuler jusqu'à la saison en cours. La majorité de ces virus appartiennent au groupe génétique 3C.2a et 3C.3a, basée sur l’analyse phylogénétique des protéines HA. Beaucoup de virus circulants 3C.2a avaient réduit la capacité de résultats des globules rouges et donc ne peuvent être qualifiées de HI essais sur5. Tests de neutralisation doivent être utilisés pour mesurer la production d’anticorps à ces virus que résultats pas6. En outre, des études ont montré que ces virus a (H3N2) contemporains ont modifié les propriétés de liaison du récepteur par rapport aux précédents virus a (H3N2) et ont tendance à accumuler les mutations de la culture adaptée et polymorphisme lorsque repiquées dans in vitro de cellules cultures7,8,9. Par rapport aux traditionnelles cellules MDCK, MDCK-SIAT1 est une lignée cellulaire développée par Matrosovich et al. par le biais de transfection stable des cellules MDCK avec l’ADNc de α2 humaine, 6-sialtransferase (SIAT1). Cette lignée cellulaire exprime des quantités accrues de α2, fractions 6-sialique galactose et une diminution de α2, les moitiés acides sialique-3 que le parent de cellules MDCK10. Des cellules de MDCK-SIAT1 ont montré pour améliorer les taux de l’isolement des virus a (H3N2) par rapport à des cellules MDCK11. Récemment, Lin et al. a signalé que pour nouvellement écloses 3C.2a et 3C.3a humaine a (H3N2) virus de l’influenza, les réplications de virus plus fidèles et meilleure infectiosité du virus ont été atteints lorsque les virus ont été cultivées dans des lignées de cellules de MDCK-SIAT1 comparées à celle des cellules MDCK7. Ainsi, les cellules de MDCK-SIAT1 conviennent mieux dans MN essais pour caractériser les réponses anticorps aux clusters récentes du virus a (H3N2).
Nous décrivons ici un essai de MN en utilisant des cellules de MDCK-SIAT1 pour mesurer les réponses immunitaires à 3C.2a contemporaines et le virus a (H3N2) 3C.3a dans le sérum humain. Virus cultivés dans des oeufs ou des cellules peuvent être utilisés dans cet essai. Sérum de chaleur inactivé contenant les anticorps neutralisants est tout d’abord dilués en série, puis incubées avec 100 TCID50/bien des virus de la grippe a (H3N2) pour permettre des anticorps à lier le virus vaccinal. Des cellules de MDCK-SIAT1 sont ensuite ajoutées au mélange des anticorps du virus et incubés pendant 18 à 20 h à 37 ° C, 5 % de CO2 à permettent au virus a (H3N2) infecter des cellules de MDCK-SIAT1 et reproduire. Après une nuit d’incubation, les plaques sont fixées et la quantité de virus dans chaque puits est quantifiée par une technique ELISA utilisant des anticorps monoclonaux contre la grippe A NP. La détection du NP indique la présence d’infection par le virus et l’absence d’anticorps neutralisants. Titre d’anticorps de neutralisation est définie comme l’inverse de la plus forte dilution de sérum qui fournit ≥ 50 % d’inhibition de l’infectiosité du virus.
Protocole
Tous les virus grippaux doivent être manipulés selon les exigences de niveau de biosécurité appropriées (BSL-2 ou supérieur) tel que défini dans la prévention des risques biotechnologiques sur Microbiological and Biomedical Laboratories (BMBL)12.
1. préparation des réactifs et des matériaux
-
Préparer des cellules de MDCK-SIAT1 et de milieu de culture cellulaire stérile
- Préparer le milieu de culture de cellules MDCK-SIAT1 à l’aide de 500 mL de Dulbecco modifié Eagle (DMEM) avec des taux de glycémie élevé, 10 % v/v chaleur inactivé sérum fœtal (SVF), de 2 mM de L-glutamine, de pyruvate de sodium 1 mM, sulfate 1 mg/mL G418 (par exemple, G418) et 100 U/ml de pénicilline avec 100 µg/mL de streptomycine (facultatif). Stériliser par filtration à travers une membrane de pores de 0,2 µM. G418 sulfate est ajouté pour garantir la stabilité des plasmides dans les cellules MDCK-SIAT1.
- Préparer la lignée de cellules MDCK-SIAT1 . En 162 cm2- Deutsch de culture tissulaire contenant 30 mL de milieu de culture de cellules stériles, flacons avec 2-2. 5 x 106 MDCK-SIAT1 cellules de graines et incuber à 37 ° C à 5 % de CO2 pendant 2 jours ; cela sera utilisé pour la détermination de la dose infectante (DECT) de culture tissulaire et MN essais.
Remarque : Les cellules MDCK-SIAT1 ont été gracieusement fournis par Dr M. Matrosovich, Marburg, Allemagne10. Cette lignée de cellules peut également être obtenue dans le commerce (voir la Table des matières).
- Préparer les milieux de propagation de virus stérile à l’aide de 500 mL d’hyperglycémie DMEM, fraction de l’albumine sérique bovine (BSA) 0,3 % V, 100 U/mL de pénicilline, 100 µg/mL de streptomycine et 20 mM HEPES. Stériliser par filtration à travers une membrane de pores de 0,2 µM.
- Préparer la cobaye des globules rouges (gpRBCs) de 0,75 % (v/v) dans une solution saline tamponnée au phosphate (PBS) contenant du PBS 0,01 M, pH 7,2.
- Préparer le diluant stérile de virus à l’aide de DMEM élevée de glucose, 1 % V de Fraction d’albumine Bovine (BSA), 100 U/mL de pénicilline, 100 µg/mL de streptomycine et 20 mM HEPES. Stériliser par filtration avec une membrane de pores 0,2 µm et préparer les frais pour chaque dosage.
- Préparer le fixateur de cellule glaciale comme l’acétone froid à 80 % dans du PBS (PBS 0,01 M, pH 7,2).
- Préparer le tampon de lavage à l’aide de PBS (0,01 M PBS pH 7,2) et 0,3 % (v/v) de tween-20.
- Préparer le diluant de l’anticorps à l’aide de PBS (PBS 0,01 M, pH 7,2), 0,3 % (v/v) de tween-20 et 5 % écrémé lait à sec.
- Contre la grippe A NP souris anticorps monoclonal clone A1 et A3 pool servir l' anticorps primaire. Diluer avec le diluant à la concentration optimale, telle que déterminée par titrage d’anticorps.
- Chèvre d’utilisation IgG anti-souris conjugués à la peroxydase de radis cheval (HRP) que l' anticorps secondaire. Diluer avec le diluant à la concentration optimale, telle que déterminée par titrage d’anticorps.
- Préparer le substrat peroxydase à l’aide de dichlorhydrate de o- phénylènediamine (DPO) dans un tampon citrate phosphate 0,05 M à pH 5. Préparer un tampon citrate phosphate 0,05 M en dissolvant 1 capsule/100 mL eau désionisée H2O. dissoudre 1 DPO comprimé (10 mg) / 20 mL de tampon citrate phosphate immédiatement avant l’emploi.
- Utiliser 0,5 M d’acide sulfurique dans solution d’arrêt DPO. Ajouter 28 mL de 18 M d’acide sulfurique étalon à 972 mL eau désionisée H2O sous une hotte chimique.
-
Traitement des sérums humains et animaux
- Chaleur inactiver les sérums humains utilisés dans les essais de MN dans un bain d’eau à 56 ° C pendant 30 min avant le dosage. Utiliser immédiatement ou le cas échéant, stocker des sérums décongelés à 4 ° C pendant pas plus de 24 h ; Si la plus longue période de stockage est nécessaire, stocker des sérums congelés à-20 ° C ou plus froids.
- Traiter les sérums animaux utilisés dans les essais de MN avec Enzyme détruisant du récepteur (RDE) et inactiver de chaleur avant l’essai comme suit.
- Décongeler les sérums dans un bain-marie à 37 ° c puis placez sur la glace. Mélanger 1 volume d’échantillon de sérum animal et 3 volumes de RDE. Incuber à 37 ° c pendant 18 à 20 h.
- Chaleur inactiver les sérums RDE traité à 56 ° c pour 30 min. ajouter les 6 volumes de PBS, pH 7,2 à chaque échantillon pour une dilution finale avant de 01:10. Le cas échéant, stocker des sérums décongelés à 4 ° C pendant pas plus de 24 h ; Si la plus longue période de stockage est nécessaire, stocker des sérums congelés à-20 ° C ou plus froids.
NOTE : Les sérums animaux peuvent contenir divers glycanes acide sialique qui peuvent se lier à la HAs des virus grippaux et inhiber la liaison de grippe spécifiques anti-HA anticorps. Par conséquent, il est nécessaire de RDE traiter tous les sérums animaux avant les essais de MN pour enlever ces liants HA virales non spécifiques dans les échantillons de sérum.
2. le passage de la Culture de cellules MDCK-SIAT1
Remarque : Toutes les cultures de cellules doivent être effectuées sous une hotte pour prévenir la contamination de la sécurité biologique.
- Décanter le milieu de culture cellulaire de la monocouche cellulaire dans des flacons de2 162 cm. Trypsinize les cellules en rinçant la monocouche avec la trypsine-EDTA. Ajouter 5 mL de trypsine-EDTA pour couvrir la monocouche de cellules. Incuber à 37 ° C, 5 % CO2 jusqu'à ce que la monocouche détache (5-10 min). Ajouter 15 mL de milieux de culture de cellules de MDCK-SIAT1 dans chaque fiole contenant des cellules de la trypsinisés, pipette de haut en bas pour séparer les cellules.
- Utiliser un hémocytomètre trypan blue pour déterminer que la numération des lymphocytes et viabilité. Les cellules dans les flacons de culture de tissus du nouveau 162 cm2 contenant 30 mL de milieux de culture cellulaire avec 2-2. 5 x 106 cellules /flask de graines et incuber à 37 ° C, avec 5 % de CO2 pendant 2 jours pour une utilisation dans des essais de dict et MN. Cellules à 4-5 x 106 cellules/flacon de graines et incuber à 37 ° C, avec 5 % de CO2 pendant 2 jours devant servir à la propagation du virus.
Remarque : La densité de semis peut être ajustée si vous désirez des périodes plus ou moins longue de la culture. Pour la propagation des virus, des cellules devraient atteindre plus de 100 % confluence. Pour les tests de Culture tissulaire Infection Dose (DECT) et MN, les cellules doivent être à la confluence de 75 à 95 % (Figure 1).
3. la propagation du virus a (H3N2) dans les cellules MDCK-SIAT1
Remarque : Les virus a (H3N2) peut être multiplié soit en 10-11, jour d’oeufs de poule embryonnés vieux selon le protocole standard3, ou cellules MDCK-SIAT1 cultures. Des cellules de MDCK-SIAT1 devraient atteindre plus de 100 % confluency pour l’inoculation du virus. Stocks de semences de virus peuvent être inoculés avec des dilutions multiples d’inoculum. Les dilutions d’inoculum avec la meilleure récolte HA et l’infectiosité peuvent être utilisés pour des dosages plus MN.
- Retirer le milieu de culture cellulaire de la monocouche cellulaire (> 100 % confluence) dans des flacons de2 162 cm. Lavez la monocouche deux fois avec 15 mL de PBS stérile de 0,01 M, pH 7,2 et décanter.
- 1 fiole en tant que contrôle l’étiquette et ajouter 20 mL de milieux de propagation des virus. Incuber le ballon à 37 ° C, avec 5 % de CO2. Laisser cette fiole intacte et utiliser pour la comparaison après le jour 1 de la propagation du virus.
- Ajouter 10 mL de milieux de propagation de virus stérile à la Deutsch et incuber tous Deutsch à 37 ° C, 5 % de CO2. Décongeler un flacon de stock de virus de la grippe à la température ambiante, puis placer sur la glace. Diluer avec les milieux de propagation du virus aux dilutions cible.
NOTE : Cible les dilutions peuvent être ajustées basée sur titres HA des stocks de virus. Pour préparer un 1/1000 dilué inoculum, ajouter 100 µL de virus à 9,9 mL de milieux de propagation de virus stérile. Inverser doucement, enlever 1 mL de dilution au 1/100 dans 9 mL de milieux de propagation de virus stérile, inverser doucement pour un inoculum de 1/1000 dilué. Placer sur la glace. - Sortir tous les flacons sauf flacon de contrôle de l’incubateur. Retirez le support de propagation du virus de Deutsch des cellules de MDCK-SIAT1 et inoculer chaque fiole 10 ml du virus dilué. Incuber les flacons à 37 ° C, 5 % de CO2 pendant 1 h, en tournant le Deutsch toutes les 15 min.
- Prélever 5 mL de l’inoculum de la Deutsch et remplacer par 15 mL de milieu de propagation virus contenant 1 µg/mL TPCK-trypsine. Incuber le Deutsch à 37 ° C, 5 % de CO2 pendant 16-18 h.
- Après l’incubation durant la nuit, observer la Deutsch sous 100 X grossissement du microscope et chercher des effets cytopathiques (CPE) sur les cellules. Prélever 15-17 mL du surnageant de virus de la Deutsch et remplacer par 15-17 mL de milieux de propagation de virus fraîchement préparés contenant 2 µg/mL TPCK-trypsine.
- Incuber les flacons à 37 ° C, 5 % de CO2. Contrôler le CPE de la monocouche (par comparaison avec le flacon de contrôle cellulaire) et de vérifier l’AP périodiquement (toutes les 4 h) avec 0,75 % gpRBC jusqu'à la récolte.
- Mettre en place une microplaque de 96 HA-puits. Ajouter 50 µL de PBS 0,01 M, pH 7,2 à puits A2 - A12 et B2 - B12 (doublons) et puits H1 - H12 pour contrôle.
- Ajouter 100 µL de virus surnageant sur A1 et A2, effectuer une dilution en série 2 fois de A1 et B1 à A12 et B12. Jetez 50 µL après mélange dans A12 et B12. Ajouter 50 µL de 0,75 % gpRBCs aux lignes A, B et H.
- Appuyez sur la plaque et incuber à température ambiante pendant 1 h.
- Déterminer HA du virus surnageant en inclinant la Microplaque 96 puits à un 45° d’angle de 60°.
- Lire les plaques d’hémagglutination ; la dilution la plus élevée du virus qui permet d’obtenir une hémagglutination complete est considéré comme le point de fin de titrage HA du virus spécifique. Enregistrer la réciproque de la plus forte dilution de virus avec hémagglutination complète sous le titre de la HA du virus.
NOTE : Les hématies sédentarisés dans la colonne H (contrôles) devraient commencer à « courir » et forme une petite larme-due à la pesanteur. Wait till RBCs contrôle puits terminer en cours d’exécution, puis lisez les boutons de RBC dans le virus puits de titrage. Ceux qui présentent des touches de RBC et « exécuter », n’obtiennent pas d’hémagglutination. Localiser la dilution la plus élevée du virus qui inhibent complètement l’hémagglutination comme le point de terminaison HA titre du virus.
- Récolter le virus lorsque les plateaux de l’AP de la culture de virus ou de la culture de virus n’atteigne sa cible HA (par exemple, > 16 HAU), mais avant la cellule monocouche commence à montrer des CPE significative.
- Centrifuger le surnageant à 300 x g pendant 10 min à 4 ° C pour granuler les débris cellulaires de culture de virus. Transférer le surnageant clarifié contenant la récolte de virus dans un tube propre. Aliquot le surnageant contenant le virus récolter en flacons cryogéniques stériles à usage unique et de geler immédiatement à-70 ° C ou plus froid.
Remarque : Les stocks de virus utilisés pour les essais de MN devraient avoir titre infectieux élevé et un minimum particules défectueux. La dilution minimale des stocks de virus pour atteindre 100 TCID5050 µL pour dosage de MN est 1/100.
Remarque : Les stocks de virus utilisés dans les essais de MN pas devraient être décongelés et recongelés.
- Centrifuger le surnageant à 300 x g pendant 10 min à 4 ° C pour granuler les débris cellulaires de culture de virus. Transférer le surnageant clarifié contenant la récolte de virus dans un tube propre. Aliquot le surnageant contenant le virus récolter en flacons cryogéniques stériles à usage unique et de geler immédiatement à-70 ° C ou plus froid.
4. détermination du dict du Virus
- Jour 1 : Titrage de Virus
- Décongeler une fiole de virus à la température ambiante et placer immédiatement sur la glace.
- Tester le virus à deux différentes dilutions de départ : 10-2 et 10-3. Ajouter 100 µL de virus à 9,9 mL de diluant pour 10-2 dilution de virus. Ajouter 1 mL de dilution 10 de-2 à 9,0 mL de diluant pour 10-3 dilution de virus.
- À l’aide de deux microplaques plaques (plaque de 1 à 10-2 dilution) et plaque 2 pour dilution de 10-3 , ajouter 100 µL de diluant de virus à tous les puits sauf colonne 1 de la Microplaque 96 puits.
- Effectuer des dilutions de10 ½log (10-2, 10-2,5, 10-3, etc.). Ajouter 146 µL du virus à partir de dilution dans toutes les loges dans la colonne 1 et 46 µL de transfert en série de colonne 1 colonne 11 (Figure 2). Pointes de pipette de changement entre les puits. Après avoir mélangé la colonne 11, jeter les bouts avec la dilution 46 µL.
- Utilisez la colonne 12 comme la cellule contrôle (CC) ; elle ne contient que diluant de virus. Incuber pendant 1 heure à 37 ° C, 5 % CO2.
- Jour 1 : Préparation des cellules de MDCK-SIAT1
Remarque : La monocouche de cellules MDCK-SIAT1 devrait atteindre confluence de 75 à 95 % pour les dosages dict et MN. Un flacon de 162 cm2 à 95 % confluence devrait produire suffisamment de cellules à graine ~ 4-5 plaques de microtitration.- Laver la monocouche confluente de 75 à 95 % avec 20 mL de PBS pour enlever la FBS dans les milieux de culture. Trypsinize les cellules comme suit.
- Rincer la monocouche avec du PBS stérile, ajouter 7 mL trypsine-EDTA pour couvrir la monocouche de cellules. Poser le ballon à plat et incuber à 37 ° C, 5 % CO2 jusqu'à ce que la monocouche détache (environ 5-10 min). Ajouter 7 mL de diluant de virus dans chaque fiole contenant les cellules trypsinisés.
- Laver les cellules avec le diluant de virus pour enlever la FBS.
- Pipetez doucement de haut en bas pour séparer les cellules. Transférer les cellules dans un tube conique de 50 mL ; remplir le tube avec diluant du virus.
- Centrifuger à 485 x g pendant 5 min. décanter le virus diluant, remplacer avec frais 50 mL virus de diluant et centrifuger à 485 x g pendant 5 min. décanter le virus diluant et remplacer avec diluant virus fraîches (10 mL/flacon) pour remettre en suspension l’extrait concentré.
- Utiliser un hémocytomètre et le bleu trypan pour déterminer le nombre de cellules et la viabilité. Ajuster la concentration en cellules par le virus du diluant à 1,5 x 105 cellules/mL.
- Ajouter 100 µL de cellules de MDCK-SIAT1 dilués dans chaque loge des microplaques (1,5 x 104 cellules/puits) et les plaques de recouvrement. Incuber à 37 ° C, 5 % CO2 pendant 18 à 20 h.
- Laver la monocouche confluente de 75 à 95 % avec 20 mL de PBS pour enlever la FBS dans les milieux de culture. Trypsinize les cellules comme suit.
- Jour 2 : ELISA
-
Fixation des cellules
- Retirer le support des plaques de microtitration. Laver chaque bien avec 200 µL de PBS. Ajouter froid 80 % acétone de 300 µL à chaque puits et incuber à température ambiante pendant 10 min. Retirer le fixateur et laisser les plaques à l’air sec.
-
ELISA
-
Ajout d’anticorps primaire
Remarque : Un anticorps monoclonal contre la grippe A NP devrait servir en excès l’anticorps primaire en ELISA. Déterminer la dilution optimale d’anticorps pour chaque lot d’anticorps primaires en effectuant des titrages d’anticorps dans MN. Sélectionnez la concentration d’anticorps primaire qui est en excès et avec le meilleur rapport signal sur arrière-plan.- Diluer l’anti-grippe NP A anticorps monoclonal (anticorps primaire) à la concentration de la cible dans l’anticorps diluant (par ex. ajouter 30 µL d’anticorps primaire à 30 mL d’anticorps diluant pour une dilution de 1/1000 de cible).
- Laver 3 fois avec 300 µL de tampon de lavage. Ajouter anticorps primaire dilué de 100 µL à chaque puits. Incuber à température ambiante pendant 1 h.
-
Ajout d’anticorps secondaire
Remarque : Chèvre anti souris IgG conjugué au raifort peroxydase de raifort (HRP) doit être utilisé en excès que l’anticorps secondaire en ELISA. Déterminer la dilution optimale d’anticorps pour chaque lot d’anticorps secondaires en effectuant des titrages d’anticorps. Sélectionnez la concentration d’anticorps secondaire en excès et avec le meilleur rapport signal sur arrière-plan.- Diluer la chèvre anti-souris Qu'igg conjugué d’anticorps HRP (anticorps secondaire) à la concentration cible dans le diluant anticorps (par exemple ajouter 7,5 µL d’anticorps secondaire à 30 mL d’anticorps diluant pour une dilution de 1:4000 de cible).
- Laver les plaques 3 fois avec 300 µL de tampon de lavage. Ajouter anticorps secondaire dilué de 100 µL à chaque puits. Incuber à température ambiante pendant 1 h.
-
Ajout du substrat et la lecture de la plaque
- Laver les plaques 5 fois avec 300 µL de tampon de lavage et tap sur un chiffon non pelucheux.
- Ajouter 100 µL de substrat fraîchement préparé dans chaque puits et incuber à température ambiante jusqu'à ce que les acides gras saturés par le développement de la couleur et la densité optique (do) de puits de contrôle cellulaire < 0,2.
- Ajouter 100 µL de solution d’arrêt dans chaque puits. Lire le diamètre extérieur des puits à 490 nm à l’aide d’un spectrophotomètre microplaques.
-
Ajout d’anticorps primaire
-
Fixation des cellules
- Calcul de TCID 50
- Calculer la médiane d’OD490 des contrôles cellule (colonne 12).
- Envisager un test bien avec un OD490 supérieure à deux fois la médiane OD490 des puits CC « positifs » ; dans le cas contraire, il est considéré comme « négatif ».
- Calculer la TCID50 du virus à l’aide de la méthode de Reed-Muench13.
- Déterminer le nombre de points positifs et négatifs à chaque dilution.
- Calculer le « cumulatif positif », « Cumul négatif », « Ratio » et « % positifs » comme illustré dans le tableau 1.
- Calculer la « distance proportionnelle » entre la projection de dilution > 50 % positifs et la projection de dilution < 50 % positifs en utilisant ce qui suit :
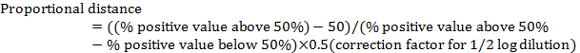
Remarque : Le facteur de correction pour la dilution ½ de journal est de 0,5. Par exemple, dans le tableau 1: (− 80 50) /(80 − 20) x 0,5 = 0,25 - Calculer le virus TCID50 en ajoutant la distance proportionnelle à la dilution montrant > 50 % positifs.
NOTE : par exemple, dans le tableau 2, TCID50 est 10-5+(-0.25) = 10-5,25. Remarque Il s’agit de la TCID50 du virus par 100 µL (ou 10-5,25100 µL).
- Calculer la dilution du virus. Pour les tests de MN, diluer le virus à 200 TCID50100 µL (équivalent à 100 TCID5050 µL / puits).
Remarque : Dans l’exemple dans le tableau 1, 1 TCID50 est 10-5,25 dans 100 µL et la dilution pour atteindre 200 TCID50100 µL est basé sur les calculs de 1:891 : 200 x 10-5,25 = 10-2.95 = 1/102,95 = 1 / 891
5. MN test en utilisant des cellules de MDCK-SIAT1
-
Jour 1 : Contrôler et sérums préparation et plaque de présentation
- Décongeler les sérums en bain-marie à 37 ° C et retirer immédiatement après décongélation. Aliquote la quantité de sérum qui doit être mis à l’essai ; Il faut un minimum de 10 µL de sérums originales à tester avec un virus dans l’état singulet. Tester les sérums des doublons si possible.
- Chaleur inactiver les sérums humains pendant 30 min dans un bain d’eau de 56 ° C comme à l’étape 1.12.1. Place sera sur la glace après inactivation par la chaleur, ajouter le diluant de virus de sérums pour atteindre une 01:10 une dilution préalable.
- RDE traiter et pré-diluer sérums animaux à 01:10 à utiliser pour les contrôles par 1.12.2.
Remarque : Les sérums humains et animaux décongelés et traitées peuvent être conservés à 4 ° C pendant n’est plus que 24 h. doivent être conservés congelés à-20 ° C ou plus froid si plus longue période de stockage est nécessaire avant le dosage. - Pour tester avec un virus, ajouter 100 µL 01:10 dilué sérums aux colonnes A1 à A10 (Figure 4). Ajouter 50 µL de diluant de virus dans les lignes B à H, à l’exception des colonnes 11 et 12 (Figure 4). Effectuer une dilution en série 2 fois à partir de lignes A à H et jeter la dernière 50 µL à colonne H (Figure 4).
Remarque : Lorsque plusieurs virus sont à tester, sérums peuvent être diluées dans des tubes de titre. La dilution du sérum, dans le but de déterminer le titre du sérum, l’A bien est 01:10, bien B 01:20, Eh bien C 01:40, bien D 1 : 80, bien E 1 : 160, bien F 1/320, bien 1/640 G, bien H 1:1,280 (Figure 4). - Pour le contrôle du virus, ajouter 50 µL de diluant de virus aux puits A12, B12, C12 et D12 (pas de sérum). Pour le contrôle de la cellule, ajouter 100 µL de diluant de virus à Herbert George wells E12, F12, G12 et H12 (aucun virus, aucun sérum).
- Pour les sérums de contrôle (par exemple, les contrôles de sérums furet), ajouter 100 µL de sérums dilués à bien une colonne 11 et ajouter 50 µL de diluant de virus dans les puits B11 - H11. Série dilué vers le bas.
- Recouvrir les plaques, incuber à 37 ° C, 5 % CO2 jusqu’au moment de l’ajout de virus.
-
Jour 1 : Ajout de Virus
- Diluer le virus à 100 TCID5050 µL avec virus diluant.
- Ajouter virus dilué de 50 µL dans toutes les loges, à l’exception de la colonne 11 sur les plaques de titrage en retour (BT) et les puits de contrôle cellulaire E12, F12, G12 et H12 sur toutes les plaques (Figure 4). Pour les plaques avec des sérums de contrôle à la colonne 11, ajouter le virus dans la colonne 11.
- Titrage en retour (BT)
- Inclure un BT dans la colonne 11 d’un ensemble de plaques en double (par exemple, plaque 1 a et 1 b). Ajouter 50 µL de diluant de virus dans tous les puits dans la colonne 11. Ajouter 50 µL du virus à 100 TCID5050 µL dans le premier puits (A11). La composition de pipetage de haut en bas.
- Mélanger et transférer 50 µL puits successifs pour effectuer des dilutions successives 2 fois. Changer les pointes de pipette entre les puits afin d’éviter le report de virus. Jetez 50 µL du puits H11.
- Ajouter 50 µL de diluant dans la colonne 11 pour porter le volume final à 100 µL. virus secouer les plaques pour mélanger.
- Incuber les plaques à 37 ° C, 5 % de CO2 pendant 1 h.
- Effectuer l’addition de cellules MDCK-SIAT1 le jour 1 et ELISA au jour 2 comme décrit aux points 4.2 et 4.3 (également décrit dans 5.3 et 5.4)
-
Jour 1 : Ajout de cellules MDCK-SIAT1
- Préparer les cellules MDCK-SIAT1 comme indiqué au point 4.2. Ajouter 100 cellules de MDCK-SIAT1 µL à 1. 5 x 105 cellules/mL dans chaque cupule (1,5 x 104 cellules/puits). Incuber les plaques à 37 ° C, 5 % CO2 pendant 18 à 20 h.
-
Jour 2 : ELISA
- Après incubation pendant la nuit, le deuxième jour, fixer les cellules avec 80 % d’acétone froid comme indiqué au point 4.3.
-
Ajout d’anticorps primaire
- Laver les plaques 3 fois avec 300 µL de tampon de lavage. Diluer l’anti-grippe NP A anticorps monoclonal (anticorps primaire) à la concentration optimale déterminée par titration en diluant anticorps (par ex. ajouter 30 µL d’anticorps primaire à 30 mL d’anticorps diluant pour une dilution de 1/1000 de cible).
Remarque : il faut 100 µL d’anticorps primaire / puits. ~ Il faut 10 mL par plaque. - Ajouter anticorps primaire dilué de 100 µL à chaque puits. Incuber à température ambiante pendant 1 h.
- Laver les plaques 3 fois avec 300 µL de tampon de lavage. Diluer l’anti-grippe NP A anticorps monoclonal (anticorps primaire) à la concentration optimale déterminée par titration en diluant anticorps (par ex. ajouter 30 µL d’anticorps primaire à 30 mL d’anticorps diluant pour une dilution de 1/1000 de cible).
-
Ajout d’anticorps secondaire
- Laver 3 fois avec 300 µL de tampon de lavage. Diluer la chèvre anti souris IgG conjugué d’anticorps HRP (anticorps secondaire) à la concentration cible en diluant anticorps (par exemple ajouter 7,5 µL d’anticorps secondaire à 30 mL d’anticorps diluant pour une 1:4000 de la cible.)
Remarque : 100 µL de l’anticorps secondaire est bien nécessaire par 96. ~ Il faut 10 mL par plaque. - Ajouter anticorps secondaire dilué de 100 µL à chaque puits. Incuber à température ambiante pendant 1 h.
- Laver 3 fois avec 300 µL de tampon de lavage. Diluer la chèvre anti souris IgG conjugué d’anticorps HRP (anticorps secondaire) à la concentration cible en diluant anticorps (par exemple ajouter 7,5 µL d’anticorps secondaire à 30 mL d’anticorps diluant pour une 1:4000 de la cible.)
-
Ajout du substrat et la lecture de la plaque
- Laver les plaques 5 fois avec 300 µL de tampon de lavage et appuyez sur non pelucheux.
- Ajouter 100 µL de substrat fraîchement préparé dans chaque puits et incuber à température ambiante jusqu'à ce que les puits de contrôle du virus atteint une OD490 = 0,8 - 3, avec le contrôle de la cellule à un faible fond OD490 < 0,2.
- Ajouter 100 µL de la solution d’arrêt dans chaque puits. Lire le diamètre extérieur des puits à 490 nm à l’aide d’un spectrophotomètre microplaques.
-
Analyse des données
Remarque : Les calculs de MN sont déterminées individuellement pour chaque plaque.- Déterminer le titre des anticorps neutralisants de chaque échantillon de sérum.
- Calculer le seuil de490 OD de séroneutralisation 50 % pour chaque plaque à l’aide de l’équation suivante :
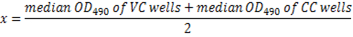
NOTE : Ici x = 50 % de la coupure de neutralisation. La dilution de sérum réciproque correspondant à la dilution la plus élevée avec OD490 inférieure à 50 % de la coupure (≥ 50 % d’inhibition) est considéré comme le titre d’anticorps de neutralisation pour cet échantillon de sérum (Figure 5).
- Calculer le seuil de490 OD de séroneutralisation 50 % pour chaque plaque à l’aide de l’équation suivante :
- Vérifiez que les puits de contrôle de cellules ont une OD490 < 0,2 et les puits de contrôle de virus ont une OD490 = 0,8 - 3.
- Vérifiez que l’infectiosité du virus dans chaque essai (100 x TCID50) par virus BT les limites acceptables de BT est de 50, 100 ou 200 DECT. Si vous utilisez la ligne de coupure même tel que défini à l’étape 4.4.2, la plus forte dilution du virus dans la colonne de BT de diamètre extérieur supérieur au seuil devrait être dans les puits E11, F11, G11.
Remarque : Les sérums de contrôle positif devraient donner 2 fois des titres au sein des valeurs obtenues dans les tests précédents. L' OD490 du contrôle sérum négatif doit être similaire à celle observée pour le contrôle du virus.
- Déterminer le titre des anticorps neutralisants de chaque échantillon de sérum.
Résultats
Détermination de l’infectiosité des stocks de virus est la première étape de l’analyse de MN. La figure 2 illustre le schéma pour déterminer la TCID50 des stocks de virus. Pour les stocks de virus avec l’infectivité inconnue, le virus peut être titré de multiples dilutions avant, par exemple les deux 10-2 et 10-3, afin de capturer la meilleure courbe de titrage pour calculer l’infectiosité du virus. La quanti...
Discussion
Le dosage de MN est l’un des dosages du principales utilisés pour une sérologie de la grippe pour détecter les réponses en anticorps après infection de la grippe ou la vaccination. Titres générés à partir des essais de MN sont souvent utilisés comme le principal résultat de nombreuses études séroépidémiologie de grippe. Tests de MN sont aussi couramment pour séro-diagnostic et l’évaluation de l’immunogénicité du vaccin. International inter-lab a été étudié afin de comparer les analyses de MN ...
Déclarations de divulgation
Les auteurs ne rapportent aucun conflit d’intérêts. Les constatations et conclusions dans la présente publication sont celles des auteurs et ne reflètent pas nécessairement les vues des Centers for Disease Control and Prevention et l’organisme de financement.
Remerciements
Nous remercions le Dr Xiuhua Lu, Dr Feng Liu et Mme Ashley Burroughs de la Division grippe des CDC pour leur examen critique et l’assistance dans la préparation de ce manuscrit. Nous remercions le Dr Adrian Reber de Division de la grippe des CDC pour son aide dans la préparation du graphique de la Figure 3. Enfin, nous remercions le Dr M. Matrosovich, Marburg, Allemagne pour fournir les cellules MDCK-SIAT1.
matériels
| Name | Company | Catalog Number | Comments |
| Dulbecco’s Modified Eagle Medium (DMEM) with high Glucose | Life Science | 11965 | A critical component of Sterile Cell Culture, Virus Propagation and Virus Diluent Media |
| Fetal bovine serum (FBS) | Hyclone | SH30070.03 | |
| Bovine Serum Albumin (BSA) Fraction V, Protase Free | Sigma-Aldrich | 3117332001 | |
| L-Glutamine | Life Science | 25030-081 | |
| Sodium pyruvate | Life Science | 11360-070 | |
| Geneticin G-418 disulfate salt | Sigma-Aldrich | A1720-5G | |
| HEPES | Life Science | 15630-080 | |
| Penicillin/Streptomycin | Life Science | 15140-122 | |
| Acetone | VWR | 67-64-1 | Used at an 80% concentration |
| Phosphate-Citrate Buffer with Sodium Perborate | Sigma-Aldrich | SLBF2806V | |
| O-Phenylenediamine Dihydrochloride tablet | Sigma-Aldrich | SLBQ1086V | 1 tablet per 100ml of cell culture grade water |
| Sulfuric Acid | Fisher Scientific | A510-P500 | Used 0.5M final concentration |
| Ethanol, Denatured, 4L | VWR | EM-AX0422-3 | Used at an 70% concentration |
| Trypsin-EDTA | Life Science | 1748048 | |
| RDE II "Seiken" | Denka Seiken | 370013 | |
| Tween 20 | Sigma-Aldrich | P1379-500ml | |
| Anti-NP mouse monoclonal Ab | Millipore pool | MAB 8257 MAB 8258 | |
| Anti-mouse IgG HRP | KPL | 074-1802 | |
| 96-well flat-bottom plates | Thermo Scientific | 3455 | |
| Plate reader | Molecular Device | Spectromax 384 plus | |
| Cell Culture Flask 162 cm2/Vent Cap | Corning/VWR | 3151 |
Références
- Reber, A., Katz, J. Immunological assessment of influenza vaccines and immune correlates of protection. Expert Rev of Vaccines. 12, 519-536 (2013).
- Li, C. K., Rappuoli, R., Xu, X. N. Correlates of protection against influenza infection in humans--on the path to a universal vaccine?. Curr Opin in Immunol. 25, 470-476 (2013).
- WHO Global Influenza Surveillance Network. . Manual for the labratory diagnosis and virological surveillence of influenza. , (2011).
- Govorkova, E. A., Kodihalli, S., Alymova, I. V., Fanget, B., Webster, R. G. Growth and immunogenicity of influenza viruses cultivated in Vero or MDCK cells and in embryonated chicken eggs. Dev Biological Stand. 98, 39-51 (1999).
- Levine, M. Z., et al. Neutralizing Antibody Responses to Antigenically Drifted Influenza A(H3N2) Viruses among Children and Adolescents following 2014-2015 Inactivated and Live Attenuated Influenza Vaccination. Clin Vaccine Immunol : CVI. 23, 831-839 (2016).
- Lin, Y., et al. The characteristics and antigenic properties of recently emerged subclade 3C.3a and 3C.2a human influenza A(H3N2) viruses passaged in MDCK cells. Influenza Other Respir Viruses. , (2017).
- Lin, Y. P., et al. Neuraminidase receptor binding variants of human influenza A(H3N2) viruses resulting from substitution of aspartic acid 151 in the catalytic site: a role in virus attachment?. J of Virol. 84, 6769-6781 (2010).
- Skowronski, D. M., et al. Mutations acquired during cell culture isolation may affect antigenic characterisation of influenza A(H3N2) clade 3C.2a viruses. Euro Surveillance. 21, 30112 (2016).
- Matrosovich, M., Matrosovich, T., Carr, J., Roberts, N. A., Klenk, H. D. Overexpression of the alpha-2,6-sialyltransferase in MDCK cells increases influenza virus sensitivity to neuraminidase inhibitors. J of Virol. 77, 8418-8425 (2003).
- Oh, D. Y., Barr, I. G., Mosse, J. A., Laurie, K. L. MDCK-SIAT1 cells show improved isolation rates for recent human influenza viruses compared to conventional MDCK cells. J Clin Microbiol. 46, 2189-2194 (2008).
- US Department of Health and Human Services. . Biosafety in Microbiological and Biomedical Laboratories. , (2009).
- Reed, H. M. A simple method of estimating fifty percent endpoints. The American Journal of Hygiene. 27, (1938).
- Laurie, K. L., et al. International Laboratory Comparison of Influenza Microneutralization Assays for A(H1N1)pdm09, A(H3N2), and A(H5N1) Influenza Viruses by CONSISE. Clinical Vaccine Immunol : CVI. 22, 957-964 (2015).
- Lin, Y., Gu, Y., McCauley, J. W. Optimization of a Quantitative Micro-neutralization Assay. J Vis Exp : JoVE. , (2016).
- van Baalen, C. A., et al. ViroSpot microneutralization assay for antigenic characterization of human influenza viruses. Vaccine. 35, 46-52 (2017).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon