Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Method Article
Estudio prospectivo, aleatorizado y controlado de una inyección de células madre mesenquimales del cordón umbilical humano para el tratamiento de las úlceras del pie diabético
* Estos autores han contribuido por igual
En este artículo
Resumen
El presente protocolo describe un estudio clínico prospectivo, aleatorizado y controlado que evalúa una inyección de células madre mesenquimales del cordón umbilical humano para el tratamiento de las úlceras crónicas del pie diabético.
Resumen
Con el desarrollo de la sociedad y la economía, la incidencia de úlceras del pie diabético sigue aumentando. Actualmente, el desbridamiento convencional con cambios de apósito, oxígeno hiperbárico y drenaje de sellado al vacío son los principales tratamientos conservadores en la práctica clínica, y las heridas grandes a menudo requieren injertos de piel o injertos de colgajo de piel. Sin embargo, los efectos del tratamiento no son ideales y existen muchas complicaciones. Debido a su compleja patogénesis, largo tiempo de tratamiento, dificultades asociadas significativas y alta tasa de discapacidad, las úlceras del pie diabético causan una pesada carga para los pacientes, la sociedad y la atención médica. Según nuestro estudio anterior, los efectos farmacológicos de las células madre de la sangre del cordón umbilical humano incluyen una regulación inmune inespecífica; aumento de la secreción de factores de crecimiento, factores vasoactivos y factores antiinflamatorios; mayor capacidad antiinfecciosa del cuerpo humano; eliminación de la inflamación; y la promoción de la angiogénesis y la cicatrización de úlceras. Estos efectos sugieren que las células madre pueden ser útiles como tratamiento autólogo o alogénico para heridas refractarias. Por lo tanto, estamos llevando a cabo un ensayo clínico para tratar heridas diabéticas refractarias con células madre de cordón umbilical humano en nuestra clínica para pacientes con úlcera de pie diabético que cumplen con los criterios de inclusión.
Introducción
La diabetes mellitus es una enfermedad que afecta a individuos en todo el mundo, y la Organización Mundial de la Salud (OMS) predice que el número de personas con diabetes mellitus aumentará de 285 millones en 2010 a 439 millones en 20301. Las úlceras del pie diabético (DFU) son una de las complicaciones más graves de la diabetes y son los principales contribuyentes a las amputaciones no traumáticas de las extremidades inferiores en todo el mundo 2,3,4,5.
Recientemente, las células madre han florecido como terapia debido a su pluripotencia, autorrenovación y capacidad para promover la secreción de citoquinas regenerativas 6,7. Un experimento clínico previo mostró que los geles de células madre derivadas de grasa tuvieron un efecto positivo en el tratamiento de las úlceras del pie en la diabetes crónica8. Los autores verificaron la efectividad del uso de células madre para tratar heridas diabéticas en 59 pacientes. En la semana 12, la tasa de cierre completo de la herida en los grupos de tratamiento y control fue del 82% y 53%, respectivamente, lo que indica que las células madre son efectivas para el tratamiento de heridas diabéticas refractarias. En general, la capacidad de las células madre para regenerarse, reemplazarse, repararse y diferenciarse ha dado una esperanza infinita a la comunidad de ciencias de la vida9.
En 2008, Dulchavsky et al.10 utilizaron injertos que contenían células autólogas del estroma de la médula ósea (BMSC) para tratar 20 casos de heridas no cicatrizantes de diferentes causas. Los exámenes histológicos mostraron que las heridas cutáneas de 18 pacientes fueron completamente reepitelizadas. Del mismo modo, el uso de células madre mesenquimales alogénicas no diabéticas (MSC) en andamios de gelatina para el tratamiento de heridas diabéticas sin unión puede promover la angiogénesis, aumentar la reepitelización y reducir el área de la úlcera11. Sin embargo, hay pocos casos de tratamiento con células madre de heridas del pie diabético en estudios de investigación clínica nacionales y extranjeros; La mayoría son solo informes de casos o investigaciones clínicas exploratorias que carecen de un diseño experimental estricto, y hay pocas muestras grandes con buen diseño o ensayos clínicos controlados aleatorios. Como las células madre no son fármacos o productos biológicos comunes, los métodos de preparación y los controles de calidad difieren entre los estudios. Los datos de un estudio pueden no reflejar completamente la seguridad de todas las células madre de la misma especie. Por lo tanto, resumimos la investigación básica relevante y los experimentos preclínicos con células madre mesenquimales del cordón umbilical humano (HUCMSCs) y evaluamos sistemáticamente la seguridad y eficacia de su aplicación clínica. Sobre esta base, se desarrolló como tratamiento la inyección de células madre mesenquimales del cordón umbilical humano para reparar heridas del pie diabético. Este estudio tiene como objetivo verificar la eficacia y seguridad de la reparación con células madre de las heridas del pie diabético en uso clínico.
En resumen, la terapia con células madre tiene un amplio espectro de aplicaciones y un gran potencial y representa un nuevo método de tratamiento médico prometedor. Con el apoyo continuo de la Fundación Nacional de Ciencias Naturales de China (No. 81571901, No. 81501671 y No. 82172224), realizamos una serie de estudios sobre el tratamiento de heridas diabéticas con HUCMSCs. Hemos publicado más de 20 artículos relacionados en el Journal of Investigative Dermatology, Stem Cell Research and Therapy, y Cell Death and Disease y hemos solicitado tres patentes nacionales de invención, acumulando así una gran base de investigación12,13. Aquí, proporcionamos un enfoque estándar para evaluar la inyección de HUCMSCs para la reparación de heridas del pie diabético. Este procedimiento estándar ha sido aprobado por ensayos clínicos de medicamentos chinos (Número de registro del ensayo: ensayos clínicos de medicamentos chinos: MR-32-21-015759, [Versión inicial: 20/10/2021]).
Protocolo
Este estudio clínico prospectivo, monocéntrico, aleatorizado y controlado fue aprobado por el Comité de Ética del Hospital Afiliado de la Universidad Médica de Xuzhou (XYFY2021-KL124-02). El estudio comenzó en julio de 2021 y continuará hasta julio de 2023; 60 pacientes fueron reclutados en este experimento. Todos los pacientes firmaron un consentimiento informado que permitió a los investigadores utilizar sus materiales clínicos y datos biológicos.
1. Reclutamiento de pacientes
- Criterios de inclusión:
- Asegurar que las edades de los pacientes estén entre 18 años y 80 años (inclusive), independientemente del género.
- Asegúrese de que los pacientes con diabetes tipo 2 y úlceras del pie diabético cumplan con los criterios diagnósticos de la OMS de 199914 y tengan un nivel de hemoglobina glucosilada (HbA1c) ≤10% según lo detectado durante el período de detección o dentro de los 3 meses anteriores a la aleatorización.
- Confirme que el índice tobillo-brazo15 de la extremidad objetivo es de al menos 0,8 sin claudicación intermitente.
- Asegúrese de que la úlcera de cada paciente tenga las siguientes características:
Grado 1 o grado 2 según el sistema de clasificación de Wagner16 para úlceras.
Ubicación en el pie, tobillo o espinilla delantera.
Área de sección transversal después del desbridamiento de 2-5 cm2.
No hay pus o sustancia necrótica visible a simple vista al menos 4 semanas antes de la aleatorización. - No incluya en el estudio a los pacientes sometidos a tratamiento rutinario de otras heridas.
- Si hay múltiples heridas presentes, seleccione la herida que cumpla con los criterios de inclusión y tenga el área de intervención y evaluación más grande.
- Si dos o más heridas son igualmente grandes, seleccione la que tenga el grado más grave.
- Si hay dos o más heridas con la misma área y grado, seleccione la que tenga la duración más larga de la herida.
- La participación en este estudio clínico es voluntaria. Asegúrese de que los pacientes cooperen con los médicos que realizan el estudio y firmen un formulario de consentimiento informado.
- Criterios de exclusión:
- Excluir pacientes con indicaciones quirúrgicas claras: oclusión vascular, exposición ósea, absceso, osteomielitis.
- Excluir a los pacientes con revascularización o angioplastia dentro de los 3 meses anteriores a la inscripción.
- Excluir a los pacientes con insuficiencia hepática; específicamente, excluir a los pacientes con niveles de ALT (aspartato aminotransferasa) y AST (alanina aminotransferasa) tres veces más altos que el límite superior de lo normal.
- Excluir a los pacientes con niveles de creatinina en sangre más de dos veces por encima del límite superior de lo normal; albúmina sérica <2,0 g/dL; tratamiento farmacológico inmunosupresor; varios tumores malignos; y embarazo, lactancia materna o un plan de parto reciente.
- Excluya a los pacientes con contraindicaciones, alergias o alergias conocidas a cualquier componente de los productos de preparación de células madre.
- Excluir a los pacientes en otras situaciones que hacen que el investigador crea que el paciente no debe participar en este estudio:
- Excluir a los pacientes si se descubre después de la admisión que no cumplen con los criterios de admisión más importantes.
- Excluir a los pacientes con reacciones adversas graves, a los pacientes que soliciten retirarse del estudio y a los pacientes cuyo tutor legal les solicite que se retiren del estudio.
- Excluir a los pacientes con falta de medicación o datos observacionales efectivos posteriores a la inscripción.
- Aleatorización y cegamiento
- Aleatorizar a los pacientes reclutados del departamento de pacientes ambulatorios del Hospital Afiliado de la Universidad Médica de Xuzhou en una base 1: 1 en el grupo de terapia con células madre y el grupo de tratamiento de heridas convencional.
- Realice un ensayo doble ciego para el tratamiento. Asegúrese de que un tercero mida el área de la herida de cada paciente.
2. Tratamiento preoperatorio
- Realizar exámenes de rutina previos al tratamiento para los pacientes después de la inscripción, incluyendo un análisis de sangre de rutina, análisis de orina, una evaluación de heces de rutina, una evaluación de la función bioquímica, una evaluación de la función de coagulación, virología, etc. Asegúrese de que los pacientes sean seguidos en el mismo hospital para garantizar la precisión de las pruebas.
- Incluya pacientes que cumplan con los criterios de inclusión y hayan firmado el consentimiento informado por escrito. Asigne cada sujeto al azar al grupo de terapia con células madre o al grupo de tratamiento de heridas convencional en una proporción de 1: 1 utilizando una técnica de muestreo proporcionada.
3. Procedimientos de tratamiento
NOTA: Los pacientes de ambos grupos reciben cambios sistemáticos de apósitos de rutina para heridas cada 3 días. Para el grupo de tratamiento con células madre, los pacientes reciben inyecciones locales de células madre cuatro veces (el día 1, el día 8, el día 15 y el día 22 después de la inscripción). En el grupo de tratamiento de heridas convencional, los pacientes son tratados con apósito de iones de plata cuatro veces (el día 1, el día 8, el día 15 y el día 22 después de la inscripción). Los pasos específicos son los siguientes.

Figura 1: Proceso de tratamiento. En cada grupo, 30 pacientes se someterán a tratamiento siguiendo estrictamente el protocolo descrito en este estudio. Haga clic aquí para ver una versión más grande de esta figura.
- Grupo de terapia con células madre
- Después de desinfectar localmente la herida con povidona yodada y eliminar el tejido necrótico de la superficie de la herida con tijeras quirúrgicas, use una jeringa para aspirar 50 ml de solución salina fisiológica para limpiar la superficie de la herida por dentro y por fuera.
- Mida el área de la herida utilizando el método de gancho de borde de lámina estéril17. Aplique el apósito transparente de película estéril con su rejilla de coordenadas a la superficie de la herida y delinee la forma de la superficie de la herida a lo largo de su borde con un marcador. Calcule el área de la herida de acuerdo con el área de cada cuadrícula de coordenadas de la película.
- Inyectar las células madre mesenquimales del cordón umbilical humano (2 x 105 células/cm 2; 0,4 ml/cm2) en la periferia y la base de la herida (espaciamiento de inyección: 0,75 cm; volumen de inyección: 0,1 ml/sitio).
NOTA: El número de inyecciones para cada paciente depende del área de la herida. - Recorte el apósito estéril al tamaño adecuado, cúbralo sobre la superficie de la herida y luego vendarlo.
- Grupo de tratamiento de heridas convencionales
- Después de desinfectar localmente la herida con yodóforo y extraer el tejido necrótico de la superficie de la herida con tijeras quirúrgicas, use una jeringa para aspirar 50 ml de solución salina fisiológica para limpiar la superficie de la herida por dentro y por fuera.
- Mida el área de la herida utilizando el método de gancho de borde de lámina estéril17. Aplique el apósito transparente de película estéril con su rejilla de coordenadas a la superficie de la herida y delinee la forma de la superficie de la herida a lo largo de su borde con un marcador. Calcule el área de la herida de acuerdo con el área de cada cuadrícula de coordenadas de la película.
- Recorte el apósito de iones de plata a un tamaño apropiado, cúbralo sobre la superficie de la herida y luego vendarlo.
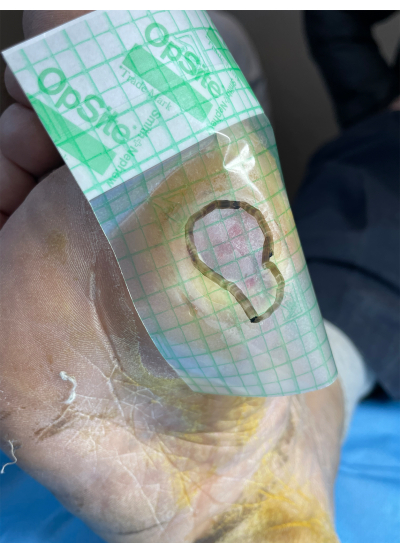
Figura 2: Diagrama esquemático de la medición del área de úlcera del pie. Haga clic aquí para ver una versión más grande de esta figura.
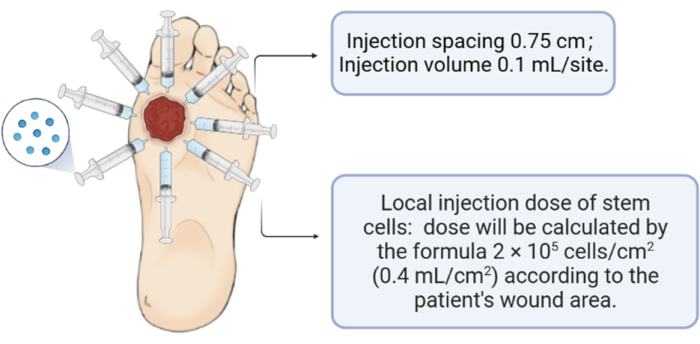
Figura 3: Esquema de la inyección de células madre mesenquimales del cordón umbilical humano. Haga clic aquí para ver una versión más grande de esta figura.
4. Indicadores de observación
- Obtener los datos demográficos de los sujetos.
- Registrar los tratamientos concomitantes; Específicamente, registre el estado de la herida (ubicación, área, profundidad, infección e isquemia), la tasa de cicatrización de la herida, el tiempo de curación y las complicaciones.
- Realizar pruebas de laboratorio. Tome la secreción de la herida para hisopos y cultivo bacteriológico. Realizar análisis de sangre de rutina y pruebas de función hepática y renal.
5. Seguimiento
- Examinar a los pacientes el primer día de terapia y durante las visitas de seguimiento 15 días y 30 días después de la última terapia.
- Realice seguimientos utilizando citas ambulatorias y telefónicas para registrar los efectos del tratamiento, los cambios de condición, la situación de recuperación y el estado de vida actual.
6. Evaluación de la eficacia de los resultados
- Realizar la evaluación clínica de acuerdo con los siguientes criterios.
- Calcular el índice de resultado primario:
La tasa de cicatrización de la herida a los 30 días = (área de la herida original − área de la herida no cicatrizada a los 30 días)/área de la herida original × del 100%. - Calcular el índice de resultados secundarios
- Tiempo de cicatrización de la herida: Defina el momento del cierre de la herida como el momento en que la herida se reepiteliza por completo.
- Calcule la tasa de curación completa:
La tasa de curación completa = el número de casos completos curados / el número total de casos × 100%
- Calcular la tasa de intervención quirúrgica:
Tasa de intervención quirúrgica = el número de intervenciones quirúrgicas/el número total de casos × del 100%.
NOTA: Los sujetos que se sometieron a uno de los siguientes procedimientos se registran como pacientes con intervenciones quirúrgicas: desbridamiento y drenaje, injerto de piel, colgajo de piel adyacente, colgajo de piel distal, colgajo de piel no anastomótico y amputación. - Realizar el cultivo bacteriano18 de acuerdo con los procedimientos estándar de inspección clínica y registrar los resultados del cultivo bacteriano de ≥1 patógeno como positivos. Calcule la tasa positiva de patógenos:
Tasa positiva de patógenos = el número de casos detectados patógenos positivos/el número total de casos × 100%.
- Calcular el índice de resultado primario:
7. Procedimientos de seguridad
- En el caso de un evento adverso (cualquier enfermedad, nuevos síntomas, signos o anomalías en el examen de laboratorio o el deterioro de los síntomas y signos originales que ocurren durante la investigación clínica con células madre, independientemente de si el evento está relacionado con el medicamento de investigación clínica o no), tome las medidas necesarias para el tratamiento y el rescate.
- Realice un seguimiento e investigue todos los eventos adversos y el proceso de tratamiento, y registre los resultados en detalle hasta que se resuelvan adecuadamente o hasta que la afección sea estable. Si una prueba es anormal y tiene importancia clínica, haga un seguimiento hasta que vuelva a la normalidad.
Resultados
En la actualidad, nuestra investigación todavía se encuentra en la fase de reclutamiento de pacientes, y ahora hemos completado tres pacientes en el grupo de tratamiento de HUCMSCs y tres pacientes en el grupo de control con apósitos de iones de plata, lo que da un total de seis pacientes con heridas crónicas en el pie diabético. El tamaño promedio del área de úlcera de un paciente en el grupo de tratamiento con HUCMSCs fue de 3,5 cm 2, y esto se redujo a 2,6 cm 2, 1,8 cm 2 y 1,25 cm 2<...
Discusión
Las DFU son un importante problema de salud pública mundial y una causa clave de amputaciones de miembros inferiores y mala calidad de vida relacionada con la salud19,20. En la actualidad, el manejo clínico todavía está dominado por el desbridamiento convencional, la oxigenoterapia hiperbárica, el drenaje con sellado al vacío (VSD) y el manejo conservador. Las heridas más grandes a menudo requieren el trasplante de piel y colgajos de piel. Muchos pacientes...
Divulgaciones
Los autores no tienen ningún conflicto de intereses que declarar.
Agradecimientos
Los autores agradecen al Hospital Afiliado de la Universidad Médica de Xuzhou por su cooperación, incluido el reclutamiento y seguimiento de pacientes con heridas en el pie diabético. Los autores también agradecen a los pacientes que participaron en la encuesta de necesidades de los pacientes durante el diseño de este estudio.
Los autores anuncian la recepción del siguiente apoyo financiero para la investigación, autoría y / o publicación de este artículo: Fundación Nacional de Ciencias Naturales de China 82172224, Programa de Investigación de Postgrado e Innovación de Práctica de la Provincia de Jiangsu (SJCX22-1271) y la Comisión de Innovación y Tecnología (Health@InnoHK).
Materiales
| Name | Company | Catalog Number | Comments |
| Silver Iin Wound Dressing | Shandong Cheerain Medical Co.,Ltd. | 20152640521 | Sterile silver ion dressing for medical use (Type F) 10 cm x 10 cm |
| Human Umbilical Cord Mesenchymal Stem Cells Injection | Shandong Qilu Cell Therapy Engineering Technology Co., Ltd. | 32183185-X | Main components: human umbilical cord mesenchymal stem cells. Pharmacological effect: non-specific immunomodulator can enhance the secretion of growth factor, vasoactive factor and anti-inflammatory factor, improve the anti infection ability of human body, eliminate inflammation, promote angiogenesis and ulcer healing. |
| Sterile mesh film transparent dressing | Smith & Nephew | 20162644490 | Sterile mesh film transparent dressing (used for wound area measurement) 6 cm x 7 cm |
Referencias
- Sun, H., et al. IDF diabetes atlas: Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045. Diabetes Research and Clinical Practice. 183, 109119 (2022).
- Volmer-Thole, M., Lobmann, R. Neuropathy and diabetic foot syndrome. International Journal of Molecular Sciences. 17 (6), 917 (2016).
- Boulton, A. J. The pathway to foot ulceration in diabetes. The Medical Clinics of North America. 97 (5), 7755-7790 (2013).
- Kumar, S., et al. The prevalence of foot ulceration and its correlates in type 2 diabetic patients: a population-based study. Diabetic Medicine. 11 (5), 480-484 (1994).
- Margolis, D. J., Jeffcoate, W. Epidemiology of foot ulceration and amputation: Can global variation be explained. The Medical Clinics of North America. 97 (5), 791-805 (2013).
- Burgess, J. L., Wyant, W. A., Abdo Abujamra, B., Kirsner, R. S., Jozic, I. Diabetic wound-healing science. Medicina. 57 (10), 1072 (2021).
- Behr, B., Ko, S. H., Wong, V. W., Gurtner, G. C., Longaker, M. T. Stem cells. Plastic and Reconstructive Surgery. 126 (4), 1163-1171 (2010).
- Moon, K. C., et al. Potential of allogeneic adipose-derived stem cell-hydrogel complex for treating diabetic foot ulcers. Diabetes. 68 (4), 837-846 (2019).
- Bacakova, L., et al. Stem cells: Their source, potency and use in regenerative therapies with focus on adipose-derived stem cells - A review. Biotechnology Advances. 36 (4), 1111-1126 (2018).
- Dulchavsky, D., et al. marrow-derived stromal cells (BMSCs) interact with fibroblasts in accelerating wound healing. Journal of Investigative Surgery. 21 (5), 270-279 (2008).
- Hu, Y., et al. Exosomes derived from pioglitazone-pretreated MSCs accelerate diabetic wound healing through enhancing angiogenesis. Journal of Nanobiotechnology. 19 (1), 150 (2021).
- Meng, F., et al. CircARHGAP12 triggers mesenchymal stromal cell autophagy to facilitate its effect on repairing diabetic wounds by sponging miR-301b-3p/ATG16L1 and miR-301b-3p/ULK2. The Journal of Investigative Dermatology. 142 (7), 1976.e4-1989.e4 (2022).
- Shen, C., et al. Exosomal microRNA rectangle93 rectangle3p secreted by bone marrow mesenchymal stem cells downregulates apoptotic peptidase activating factor 1 to promote wound healing. Bioengineered. 13 (1), 27-37 (2022).
- Alberti, K. G., Zimmet, P. Z. Definition, diagnosis and classification of diabetes mellitus and its complications. Part 1: Diagnosis and classification of diabetes mellitus provisional report of a WHO consultation. Diabetic Medicine. 15 (7), 539-553 (1998).
- Lijmer, J. G., Hunink, M. G., vanden Dungen, J. J., Loonstra, J., Smit, A. J. ROC analysis of noninvasive tests for peripheral arterial disease. Ultrasound in Medicine & Biology. 22 (4), 391-398 (1996).
- Wagner Jr, F. W. The dysvascular foot: A system for diagnosis and treatment. Foot & Ankle. 2 (2), 64-122 (1981).
- Griffin, J. W., Tolley, E. A., Tooms, R. E., Reyes, R. A., Clifft, J. K. A comparison of photographic and transparency-based methods for measuring wound surface area. Physical Therapy. 73 (2), 117-122 (1993).
- Lipsky, B. A., et al. Diagnosis and treatment of diabetic foot infections. Plastic and Reconstructive Surgery. 117 (7 Suppl), 212S-238S (2006).
- Huang, Y. Y., et al. Effect of a novel macrophage-regulating drug on wound healing in patients with diabetic foot ulcers: A randomized clinical trial. JAMA Network Open. 4 (9), e2122607 (2021).
- Yarahmadi, A., et al. The effect of platelet-rich plasma-fibrin glue dressing in combination with oral vitamin E and C for treatment of non-healing diabetic foot ulcers: A randomized, double-blind, parallel-group, clinical trial. Expert Opinion on Biological Therapy. 21 (5), 687-696 (2021).
- Virador, G. M., de Marcos, L., Virador, V. M. Skin wound healing: Refractory wounds and novel solutions. Methods in Molecular Biology. 1879, 221-241 (2019).
- Um, S., Ha, J., Choi, S. J., Oh, W., Jin, H. J. Prospects for the therapeutic development of umbilical cord blood-derived mesenchymal stem cells. World Journal of Stem Cells. 12 (12), 1511-1528 (2020).
- Xiao, M., et al. Dynamic biological characteristics of human bone marrow hematopoietic stem cell senescence. Scientific Reports. 12, 17071 (2022).
- Zhang, Z., et al. Safety and immunological responses to human mesenchymal stem cell therapy in difficult-to-treat HIV-1-infected patients. AIDS. 27 (8), 1283-1293 (2013).
- Wu, M., et al. Human umbilical cord mesenchymal stem cell promotes angiogenesis via integrin beta1/ERK1/2/HIF-1alpha/VEGF-A signaling pathway for off-the-shelf breast tissue engineering. Stem Cell Research & Therapy. 13 (1), 99 (2022).
- Li, K., et al. Anti-inflammatory and immunomodulatory effects of the extracellular vesicles derived from human umbilical cord mesenchymal stem cells on osteoarthritis via M2 macrophages. Journal of Nanobiotechnology. 20 (1), 38 (2022).
- Qin, H. L., Zhu, X. H., Zhang, B., Zhou, L., Wang, W. Y. Clinical evaluation of human umbilical cord mesenchymal stem cell transplantation after angioplasty for diabetic foot. Experimental and Clinical Endocrinology & Diabetes. 124 (8), 497-503 (2016).
- Cai, J., et al. Umbilical cord mesenchymal stromal cell with autologous bone marrow cell transplantation in established Type 1 diabetes: A pilot randomized controlled open-label clinical study to assess safety and impact on insulin secretion. Diabetes Care. 39 (1), 149-157 (2016).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados