JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
당뇨병성 족부궤양 치료를 위한 인간 탯줄 중간엽 줄기세포 주사의 전향적, 무작위 및 대조 연구
* 이 저자들은 동등하게 기여했습니다
요약
현재 프로토콜은 만성 당뇨병성 족부궤양 치료를 위한 인간 탯줄 중간엽 줄기 세포 주사를 평가하는 전향적, 무작위, 대조 임상 연구를 설명합니다.
초록
사회와 경제의 발전과 함께 당뇨병성 족부궤양의 발병률은 계속 증가하고 있습니다. 현재 드레싱 교체, 고압 산소 및 진공 밀봉 배액을 통한 기존의 괴사조직 제거술은 임상 실습에서 주요 보존적 치료법이며 큰 상처는 종종 피부 이식편 또는 피부 플랩 이식이 필요합니다. 그러나 치료 효과가 이상적이지 않고 많은 합병증이 존재합니다. 당뇨병성 족부궤양은 복잡한 발병기전, 긴 치료 시간, 심각한 관련 어려움, 높은 장애율로 인해 환자, 사회 및 의료에 큰 부담을 줍니다. 우리의 이전 연구에 따르면, 인간 제대혈 줄기 세포의 약리학 적 효과에는 비특이적 면역 조절이 포함됩니다. 성장 인자, 혈관 활성 인자 및 항염증 인자의 분비 증가; 인체의 항 감염 능력 향상; 염증 제거; 혈관 신생 및 궤양 치유 촉진. 이러한 효과는 줄기 세포가 난치성 상처에 대한 자가 또는 동종 치료제로 유용할 수 있음을 시사합니다. 따라서 본 클리닉에서는 선정 기준을 충족하는 당뇨성 족부궤양 환자를 대상으로 인간 탯줄 줄기세포로 난치성 당뇨 상처를 치료하기 위한 임상시험을 진행하고 있습니다.
서문
당뇨병은 전 세계적으로 개인에게 영향을 미치는 질병이며, 세계보건기구(WHO)는 당뇨병 환자의 수가 2010년 2억 8,500만 명에서 2030년 4억 3,900만 명으로 증가할 것으로 예측합니다1. 당뇨병성 족부궤양(DFU)은 당뇨병의 가장 심각한 합병증 중 하나이며 전 세계적으로 비외상성 하지 절단의 주요 원인입니다 2,3,4,5.
최근, 줄기 세포는 다능성, 자가 재생 및 재생 사이토카인의 분비를 촉진하는 능력으로 인해 치료제로 번성하고 있습니다 6,7. 이전의 임상 실험에서는 지방 유래 줄기세포 젤이 만성 당뇨병의 족부 궤양 치료에 긍정적인 영향을 미치는 것으로 나타났다8. 저자들은 59 명의 환자에서 당뇨병 상처를 치료하기 위해 줄기 세포를 사용하는 효과를 확인했습니다. 12주차에 치료군과 대조군의 완전한 상처 봉합률은 각각 82%와 53%로 줄기세포가 난치성 당뇨병성 상처 치료에 효과적임을 나타냅니다. 전반적으로, 줄기 세포의 재생, 대체, 복구 및 분화 능력은 생명 과학 커뮤니티에 무한한 희망을 주었습니다9.
2008년 Dulchavsky et al.10 은 자가 골수 기질 세포(BMSC)를 포함하는 이식편을 사용하여 다양한 원인의 치유되지 않는 상처 20건을 치료했습니다. 조직 학적 검사에서 18 명의 환자의 피부 상처가 완전히 재 상피화 된 것으로 나타났습니다. 유사하게, 불유합 당뇨병성 상처의 치료를 위해 젤라틴 스캐폴드에 동종 비당뇨병성 중간엽 줄기세포(MSC)를 사용하면 혈관신생을 촉진하고 재상피화를 증가시키며 궤양 면적을 감소시킬 수 있다11. 그러나 국내외 임상 연구에서 당뇨병성 족부 상처의 줄기세포 치료 사례는 거의 없습니다. 대부분은 엄격한 실험 설계가 결여된 사례 보고서 또는 탐색적 임상 연구일 뿐이며, 좋은 설계나 무작위 대조 임상 시험을 가진 대규모 샘플은 거의 없습니다. 줄기 세포는 일반적인 약물이나 생물학적 제제가 아니기 때문에 준비 방법과 품질 관리는 연구마다 다릅니다. 한 연구의 데이터는 동일한 종의 모든 줄기 세포의 안전성을 완전히 반영하지 못할 수 있습니다. 따라서 인간 탯줄 중간엽 줄기세포(HUCMSC)를 이용한 관련 기초 연구 및 전임상 실험을 추가로 요약하고 임상 적용의 안전성과 유효성을 체계적으로 평가했습니다. 이를 바탕으로 당뇨병성 족부 상처를 치료하기 위해 인간의 탯줄에서 중간엽 줄기세포를 주입하는 방법이 개발되었습니다. 본 연구는 임상에서 당뇨병성 족부상처의 줄기세포 복구의 효능과 안전성을 검증하는 것을 목적으로 한다.
요약하면, 줄기 세포 치료는 광범위한 응용 분야와 큰 잠재력을 가지고 있으며 유망한 새로운 치료 방법을 나타냅니다. 중국 국립 자연 과학 재단 (No. 81571901, No. 81501671, No. 82172224)의 지속적인 지원으로 HUCMSC로 당뇨병 성 상처 치료에 대한 일련의 연구를 수행했습니다. 우리는 Journal of Investigative Dermatology, Stem Cell Research and Therapy, Cell Death and Disease에 20편 이상의 관련 논문을 발표했으며 3개의 국가 발명 특허를 출원하여 연구의 큰 기반을 축적했습니다12,13. 여기에서 우리는 당뇨병성 발 상처 치료를 위한 HUCMSC 주사를 평가하기 위한 표준 접근 방식을 제공합니다. 이 표준 절차는 중국 약물 임상 시험(시험 등록 번호: 중국 약물 임상 시험: MR-32-21-015759, [초기 릴리스: 2021년 10월 20일])에 의해 승인되었습니다.
프로토콜
이 전향적, 단일 센터, 무작위, 통제 임상 연구는 쉬저우 의과대학 부속병원 윤리 위원회(XYFY2021-KL124-02)의 승인을 받았습니다. 이 연구는 2021년 7월에 시작되어 2023년 7월까지 계속됩니다. 이 실험에서 60명의 환자를 모집했습니다. 모든 환자는 연구자가 임상 자료와 생물학적 데이터를 사용할 수 있도록 정보에 입각한 동의서에 서명했습니다.
1. 환자 모집
- 포함 기준:
- 성별에 관계없이 환자의 연령이 18세에서 80세(포함) 사이인지 확인합니다.
- 제2형 당뇨병 및 당뇨병성 족부궤양 환자가 1999년 WHO 진단 기준14 를 충족하고 스크리닝 기간 동안 또는 무작위 배정 전 3개월 이내에 검출된 당화혈색소(HbA1c) 수치가 ≤10%인지 확인합니다.
- 표적 사지의 발목-상완 지수(15 )가 간헐적 파행 없이 0.8 이상인지 확인합니다.
- 각 환자의 궤양에 다음과 같은 특징이 있는지 확인하십시오.
궤양에 대한 Wagner 등급 시스템16 에 따른 등급 1 또는 등급 2.
발, 발목 또는 앞쪽 정강이의 위치.
괴사조직 제거 후 단면적 2-5 cm2.
무작위 배정 최소 4주 전에 육안으로 볼 수 있는 고름이나 괴사 물질이 없습니다. - 연구에서 다른 상처의 일상적인 치료를 받는 환자를 포함하지 마십시오.
- 여러 상처가 있는 경우 포함 기준을 충족하고 개입 및 평가 영역이 가장 큰 상처를 선택합니다.
- 두 개 이상의 상처가 비슷하게 크면 가장 심한 등급의 상처를 선택하십시오.
- 부위와 등급이 같은 상처가 두 개 이상 있는 경우 상처 지속 시간이 가장 긴 상처를 선택합니다.
- 이 임상 연구에 참여하는 것은 자발적입니다. 환자가 연구를 수행하는 의사와 협력하고 정보에 입각한 동의서에 서명하도록 합니다.
- 제외 기준:
- 혈관 폐색, 뼈 노출, 농양, 골수염과 같은 명확한 수술 적응증을 가진 환자는 제외하십시오.
- 등록 전 3개월 이내에 혈관재생술 또는 혈관성형술을 받은 환자는 제외합니다.
- 간 장애 환자는 제외합니다. 구체적으로는 ALT(아스파르테이트 아미노전이효소) 및 AST(알라닌 아미노전이효소) 수치가 정상 상한치보다 3배 높은 환자는 제외한다.
- 혈중 크레아티닌 수치가 정상 상한치보다 2배 이상 높은 환자는 제외합니다. 혈청 알부민<2.0g/dL; 면역 억제제 치료; 다양한 악성 종양; 임신, 모유 수유 또는 최근 출산 계획.
- 줄기 세포 준비 제품의 구성 요소에 대한 금기 사항, 알레르기 또는 알려진 알레르기가 있는 환자는 제외합니다.
- 연구자가 환자가 이 연구에 참여해서는 안 된다고 믿게 만드는 다른 상황에서 환자를 제외합니다.
- 입원 후 가장 중요한 입원 기준을 충족하지 못하는 것으로 밝혀지면 환자를 제외합니다.
- 심각한 부작용이 있는 환자, 연구 중단을 요청하는 환자, 법적 보호자가 연구 중단을 요청한 환자는 제외합니다.
- 약물이 부족하거나 효과적인 등록 후 관찰 데이터가 있는 환자를 제외합니다.
- 무작위화 및 눈가림
- 쉬저우 의과대학 부속병원 외래에서 모집한 환자를 줄기세포치료군과 기존 상처치료군으로 1:1로 무작위 배정한다.
- 치료를 위해 이중 맹검 시험을 실시하십시오. 제3자가 각 환자의 상처 부위를 측정하도록 합니다.
2. 수술 전 치료
- 등록 후 환자에 대한 일상적인 혈액 검사, 소변 검사, 일상적인 대변 평가, 생화학적 기능 평가, 응고 기능 평가, 바이러스학 등을 포함한 일상적인 전처리 검사를 수행합니다. 검사의 정확성을 보장하기 위해 환자가 같은 병원에서 추적 관찰되도록 합니다.
- 포함 기준을 충족하고 서면 동의서에 서명한 환자를 포함합니다. 비례 샘플링 기법을 사용하여 각 피험자를 줄기 세포 치료 그룹 또는 기존 상처 치료 그룹에 1:1 비율로 무작위로 할당합니다.
3. 치료 절차
참고: 두 그룹의 환자는 3일마다 체계적인 일상적인 상처 드레싱 교체를 받습니다. 줄기세포 치료군의 경우 환자는 줄기세포 국소주사를 4회(등록 후 1일, 8일, 15일, 22일) 투여한다. 기존의 상처 치료군에서 환자는 은 이온 드레싱으로 4회(등록 후 1일, 8일, 15일 및 22일) 치료됩니다. 구체적인 단계는 다음과 같습니다.

그림 1: 처리 과정. 각 그룹에서 30명의 환자는 이 연구에 설명된 프로토콜에 따라 엄격하게 치료를 받게 됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
- 줄기세포치료제
- 포비돈 요오드로 상처를 국소 소독하고 수술 용 가위로 상처 표면에서 괴사 조직을 제거한 후 주사기를 사용하여 생리 식염수 50mL를 흡인하여 상처 표면을 안팎으로 청소합니다.
- 멸균 호일 에지 후크 방법17을 사용하여 상처 부위를 측정합니다. 좌표 격자가 있는 멸균 필름 투명 드레싱을 상처 표면에 적용하고 마커로 가장자리를 따라 상처 표면의 모양을 윤곽을 그립니다. 필름의 각 좌표 격자의 면적에 따라 상처 면적을 계산하십시오.
- 인간 탯줄 중간엽 줄기세포(2 x 105 cells/cm2; 0.4 mL/cm2)를 상처 주변과 기저부에 주입합니다(주입 간격: 0.75 cm; 주입량: 0.1 mL/site).
참고: 각 환자의 주사 횟수는 상처 부위에 따라 다릅니다. - 멸균 드레싱을 적절한 크기로 다듬고 상처 표면에 덮은 다음 붕대를 감습니다.
- 종래의 상처 치료군
- iodophor로 상처를 국소 소독하고 수술 용 가위로 상처 표면에서 괴사 조직을 제거한 후 주사기를 사용하여 생리 식염수 50mL를 흡인하여 상처 표면을 안팎으로 청소합니다.
- 멸균 호일 에지 후크 방법17을 사용하여 상처 부위를 측정합니다. 좌표 격자가 있는 멸균 필름 투명 드레싱을 상처 표면에 적용하고 마커로 가장자리를 따라 상처 표면의 모양을 윤곽을 그립니다. 필름의 각 좌표 격자의 면적에 따라 상처 면적을 계산하십시오.
- 은이온 드레싱을 적당한 크기로 다듬고 상처 표면에 덮은 다음 붕대를 감습니다.
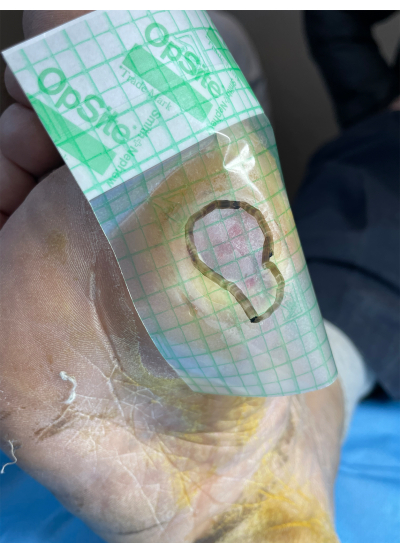
그림 2: 족부 궤양 면적 측정의 개략도. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
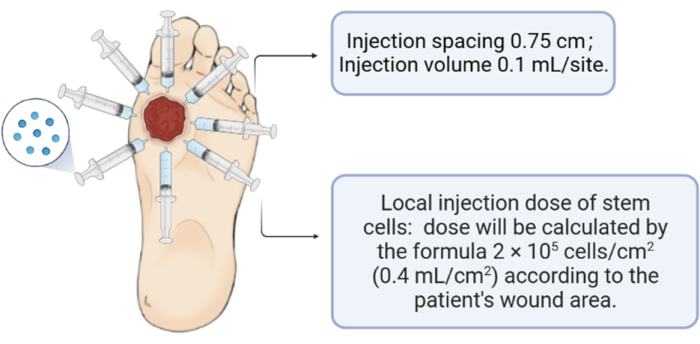
그림 3: 인간 탯줄 중간엽 줄기세포 주입의 개략도. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
4. 관측 지표
- 피험자의 인구 통계 학적 데이터를 얻습니다.
- 병용 치료를 기록하십시오. 구체적으로 상처 상태(위치, 면적, 깊이, 감염 및 허혈), 상처 치유 속도, 치유 시간 및 합병증을 기록합니다.
- 실험실 테스트를 수행합니다. 면봉과 세균 배양을 위해 상처 분비물을 섭취하십시오. 일상적인 혈액 검사와 간 및 신장 기능 검사를 실시하십시오.
5. 후속 조치
- 치료 첫날과 마지막 치료 후 15일 및 30일 후 후속 방문 동안 환자를 검사합니다.
- 외래 진료와 전화 예약을 모두 사용하여 후속 조치를 수행하여 치료 효과, 상태 변화, 회복 상황 및 현재 생활 상태를 기록합니다.
6. 결과 효능 평가
- 다음 기준에 따라 임상 평가를 수행합니다.
- 기본 결과 지수를 계산합니다.
30일 상처 치유율 = (원래 상처 부위 - 30일 후 치유되지 않은 상처 부위)/원래 상처 부위 × 100%. - 보조 결과 지수 계산
- 상처 치유 시간: 상처가 봉합되는 시간을 상처가 완전히 재상피화되는 시간으로 정의합니다.
- 전체 치유 속도를 계산하십시오.
완치율 = 완치된 건수/총 건수 × 100%
- 외과 개입 비율을 계산하십시오.
외과적 개입률 = 외과적 개입 횟수/총 사례 수 × 100%.
참고: 다음 절차 중 하나를 받은 피험자는 괴사조직 제거 및 배액, 피부 이식, 인접 피부 피판, 원위 피부 피판, 비문합 피부 피판 및 절단과 같은 외과적 개입이 있는 환자로 기록됩니다. - 표준 임상 검사 절차에 따라 세균 배양(18 )을 수행하고, ≥1 병원체의 세균 배양 결과를 양성으로 기록한다. 병원체 양성률을 계산하십시오.
병원체 양성률 = 병원체 양성 검출 사례 수/총 사례 수 × 100%.
- 기본 결과 지수를 계산합니다.
7. 안전 절차
- 이상반응(임상연구약물과의 연관 여부와 무관하게 줄기세포 임상연구 중 발생하는 질병, 새로운 증상, 징후 또는 검사실 검사 이상 또는 본래의 증상 및 징후의 악화)이 발생한 경우, 치료 및 구제에 필요한 조치를 취한다.
- 모든 부작용과 치료 과정을 추적 및 조사하고 적절하게 해결되거나 상태가 안정될 때까지 결과를 자세히 기록합니다. 검사가 비정상적이고 임상적으로 중요한 경우 정상으로 돌아올 때까지 후속 조치를 취하십시오.
결과
현재 우리의 연구는 아직 환자 모집 단계에 있으며, 현재 HUCMSC 치료군 환자 3명과 은이온 드레싱 대조군 환자 3명을 완료하여 만성 당뇨병성 족부 상처 환자 총 6명을 확보했습니다. HUCMSCs 치료군에서 환자의 궤양 면적의 평균 크기는 3.5 cm2이었고, 이것은 HUCMSCs로 치료한 후 8일째, 15일째 및 22일째에 각각 2.6 cm2, 1.8 cm2 및 1.25cm2로 감소되었다 (도 4A-D
토론
DFU는 전 세계의 주요 공중 보건 문제이며 하지 절단 및 건강 관련 삶의 질 저하의 주요 원인입니다19,20. 현재 임상 관리는 여전히 기존의 괴사조직 제거, 고압 산소 요법, 진공 밀봉 배액(VSD) 및 보존적 관리가 지배하고 있습니다. 더 큰 상처는 종종 피부와 피부 플랩의 이식이 필요합니다. 많은 환자들이 심각한 신체적, 정신적 고통을 유발하고 삶의 질을...
공개
저자는 선언할 이해 상충이 없습니다.
감사의 말
저자는 당뇨병성 족부 상처 환자의 모집 및 후속 조치를 포함하여 협력해 준 쉬저우 의과대학 부속병원에 감사를 표합니다. 저자는 또한 이 연구를 설계하는 동안 환자 요구 설문 조사에 참여한 환자들에게 감사를 표합니다.
저자는 이 논문의 연구, 저자 및/또는 출판을 위해 다음과 같은 재정 지원을 받았음을 발표합니다: 중국 국립 자연 과학 재단 82172224, 장쑤성 대학원 연구 및 실무 혁신 프로그램(SJCX22-1271) 및 혁신 및 기술 위원회(Health@InnoHK).
자료
| Name | Company | Catalog Number | Comments |
| Silver Iin Wound Dressing | Shandong Cheerain Medical Co.,Ltd. | 20152640521 | Sterile silver ion dressing for medical use (Type F) 10 cm x 10 cm |
| Human Umbilical Cord Mesenchymal Stem Cells Injection | Shandong Qilu Cell Therapy Engineering Technology Co., Ltd. | 32183185-X | Main components: human umbilical cord mesenchymal stem cells. Pharmacological effect: non-specific immunomodulator can enhance the secretion of growth factor, vasoactive factor and anti-inflammatory factor, improve the anti infection ability of human body, eliminate inflammation, promote angiogenesis and ulcer healing. |
| Sterile mesh film transparent dressing | Smith & Nephew | 20162644490 | Sterile mesh film transparent dressing (used for wound area measurement) 6 cm x 7 cm |
참고문헌
- Sun, H., et al. IDF diabetes atlas: Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045. Diabetes Research and Clinical Practice. 183, 109119 (2022).
- Volmer-Thole, M., Lobmann, R. Neuropathy and diabetic foot syndrome. International Journal of Molecular Sciences. 17 (6), 917 (2016).
- Boulton, A. J. The pathway to foot ulceration in diabetes. The Medical Clinics of North America. 97 (5), 7755-7790 (2013).
- Kumar, S., et al. The prevalence of foot ulceration and its correlates in type 2 diabetic patients: a population-based study. Diabetic Medicine. 11 (5), 480-484 (1994).
- Margolis, D. J., Jeffcoate, W. Epidemiology of foot ulceration and amputation: Can global variation be explained. The Medical Clinics of North America. 97 (5), 791-805 (2013).
- Burgess, J. L., Wyant, W. A., Abdo Abujamra, B., Kirsner, R. S., Jozic, I. Diabetic wound-healing science. Medicina. 57 (10), 1072 (2021).
- Behr, B., Ko, S. H., Wong, V. W., Gurtner, G. C., Longaker, M. T. Stem cells. Plastic and Reconstructive Surgery. 126 (4), 1163-1171 (2010).
- Moon, K. C., et al. Potential of allogeneic adipose-derived stem cell-hydrogel complex for treating diabetic foot ulcers. Diabetes. 68 (4), 837-846 (2019).
- Bacakova, L., et al. Stem cells: Their source, potency and use in regenerative therapies with focus on adipose-derived stem cells - A review. Biotechnology Advances. 36 (4), 1111-1126 (2018).
- Dulchavsky, D., et al. marrow-derived stromal cells (BMSCs) interact with fibroblasts in accelerating wound healing. Journal of Investigative Surgery. 21 (5), 270-279 (2008).
- Hu, Y., et al. Exosomes derived from pioglitazone-pretreated MSCs accelerate diabetic wound healing through enhancing angiogenesis. Journal of Nanobiotechnology. 19 (1), 150 (2021).
- Meng, F., et al. CircARHGAP12 triggers mesenchymal stromal cell autophagy to facilitate its effect on repairing diabetic wounds by sponging miR-301b-3p/ATG16L1 and miR-301b-3p/ULK2. The Journal of Investigative Dermatology. 142 (7), 1976.e4-1989.e4 (2022).
- Shen, C., et al. Exosomal microRNA rectangle93 rectangle3p secreted by bone marrow mesenchymal stem cells downregulates apoptotic peptidase activating factor 1 to promote wound healing. Bioengineered. 13 (1), 27-37 (2022).
- Alberti, K. G., Zimmet, P. Z. Definition, diagnosis and classification of diabetes mellitus and its complications. Part 1: Diagnosis and classification of diabetes mellitus provisional report of a WHO consultation. Diabetic Medicine. 15 (7), 539-553 (1998).
- Lijmer, J. G., Hunink, M. G., vanden Dungen, J. J., Loonstra, J., Smit, A. J. ROC analysis of noninvasive tests for peripheral arterial disease. Ultrasound in Medicine & Biology. 22 (4), 391-398 (1996).
- Wagner Jr, F. W. The dysvascular foot: A system for diagnosis and treatment. Foot & Ankle. 2 (2), 64-122 (1981).
- Griffin, J. W., Tolley, E. A., Tooms, R. E., Reyes, R. A., Clifft, J. K. A comparison of photographic and transparency-based methods for measuring wound surface area. Physical Therapy. 73 (2), 117-122 (1993).
- Lipsky, B. A., et al. Diagnosis and treatment of diabetic foot infections. Plastic and Reconstructive Surgery. 117 (7 Suppl), 212S-238S (2006).
- Huang, Y. Y., et al. Effect of a novel macrophage-regulating drug on wound healing in patients with diabetic foot ulcers: A randomized clinical trial. JAMA Network Open. 4 (9), e2122607 (2021).
- Yarahmadi, A., et al. The effect of platelet-rich plasma-fibrin glue dressing in combination with oral vitamin E and C for treatment of non-healing diabetic foot ulcers: A randomized, double-blind, parallel-group, clinical trial. Expert Opinion on Biological Therapy. 21 (5), 687-696 (2021).
- Virador, G. M., de Marcos, L., Virador, V. M. Skin wound healing: Refractory wounds and novel solutions. Methods in Molecular Biology. 1879, 221-241 (2019).
- Um, S., Ha, J., Choi, S. J., Oh, W., Jin, H. J. Prospects for the therapeutic development of umbilical cord blood-derived mesenchymal stem cells. World Journal of Stem Cells. 12 (12), 1511-1528 (2020).
- Xiao, M., et al. Dynamic biological characteristics of human bone marrow hematopoietic stem cell senescence. Scientific Reports. 12, 17071 (2022).
- Zhang, Z., et al. Safety and immunological responses to human mesenchymal stem cell therapy in difficult-to-treat HIV-1-infected patients. AIDS. 27 (8), 1283-1293 (2013).
- Wu, M., et al. Human umbilical cord mesenchymal stem cell promotes angiogenesis via integrin beta1/ERK1/2/HIF-1alpha/VEGF-A signaling pathway for off-the-shelf breast tissue engineering. Stem Cell Research & Therapy. 13 (1), 99 (2022).
- Li, K., et al. Anti-inflammatory and immunomodulatory effects of the extracellular vesicles derived from human umbilical cord mesenchymal stem cells on osteoarthritis via M2 macrophages. Journal of Nanobiotechnology. 20 (1), 38 (2022).
- Qin, H. L., Zhu, X. H., Zhang, B., Zhou, L., Wang, W. Y. Clinical evaluation of human umbilical cord mesenchymal stem cell transplantation after angioplasty for diabetic foot. Experimental and Clinical Endocrinology & Diabetes. 124 (8), 497-503 (2016).
- Cai, J., et al. Umbilical cord mesenchymal stromal cell with autologous bone marrow cell transplantation in established Type 1 diabetes: A pilot randomized controlled open-label clinical study to assess safety and impact on insulin secretion. Diabetes Care. 39 (1), 149-157 (2016).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유