Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Imagerie de cellules vivantes de la ségrégation des chromosomes pendant la mitose
Dans cet article
Résumé
Ce protocole décrit une méthode simple et pratique pour étiqueter et visualiser direct chromosomes dans les cellules mitotiques en utilisant l’étiquette Histone2B-GFP BacMam 2.0 et un système de microscopie confocale tourne disque.
Résumé
Chromosomes doivent être fiable et uniforme divisés en cellules filles pendant la division cellulaire mitotique. Fidélité de la ségrégation chromosomique est contrôlée par les mécanismes multiples qui incluent le Checkpoint de montage broche (SAC). Le SAC fait partie d’un système de rétroaction complexe qui est responsable de la prévention d’un progrès de cellulaire par mitose, à moins que tous les kinétochores chromosomiques ont joint à la broche de microtubules. Calorifugeage chromosomique et chromosome anormal est un indicateur des postes de contrôle dysfonctionnel cycle cellulaire de la ségrégation et peut être utilisée pour mesurer la stabilité génomique des cellules en division. Déréglementation du SAC peut entraîner la transformation d’une cellule normale en une cellule maligne à travers l’accumulation des erreurs au cours de la ségrégation chromosomique. Mise en œuvre du SAC et la formation du kinétochore complexe sont étroitement contrôlée par les interactions entre les kinases et phosphatases tels que de la protéine Phosphatase 2 a (PP2A). Ce protocole décrit l’imagerie de cellules vivantes des chromosomes dans les fibroblastes embryonnaires de souris isolés de souris qui avaient un masquage de la sous-unité régulatrice PP2A-B56γ à la traîne. Cette méthode permet de surmonter les défauts des autres cell cycle control techniques d’imagerie comme cytométrie ou immunocytochimie seulement présentent un portrait de cellulaire cytocinèse, au lieu d’une visualisation dynamique spatio-temporelle des chromosomes au cours de la mitose.
Introduction
Dans le protocole suivant, nous décrivons une méthode pratique pour visualiser la ségrégation chromosomique et la progression mitotique au cours du cycle cellulaire dans les fibroblastes embryonnaires de souris à l’aide d’Histone 2 b-GFP, marquage BacMam 2.0 et l’imagerie de cellules vivantes.
Points de contrôle de cycle cellulaire surveillent la ségrégation des chromosomes et jouent un rôle important dans le maintien de l’intégrité génétique de la cellule 1,2,3. Accumulation de mauvaise ségrégation chromosomes peut conduire à aneuploïdie, qui est une caractéristique de plus solides tumeurs 4. Par conséquent, détection des chromosomes traînards utilisable comme une méthode pour étudier l’instabilité chromosomique.
Fluorescent étiqueté protéines peuvent être utilisé pour visualiser la ségrégation des chromosomes vivants et chromosomiques en retard mais la génération de mCherry-tag ou protéine H2B-GFP Taggé nécessite des connaissances considérables de gène de biologie moléculaire et la livraison 5. Nous décrivons ici l’utilisation du réactif de CellLight Histone2B-GFP BacMam 2.0, ci-après appelé regent CL-HB, par souci de simplicité. Ce réactif peut être utilisé immédiatement et élimine donc les préoccupations concernant la qualité de vecteur et de l’intégrité. En outre, ce réactif ne nécessite pas l’utilisation des traitements potentiellement dangereux ou des lipides et des produits chimiques de colorant-chargement. À la différence des étiquettes fluorescentes conventionnelles, le régent de CL-HB taches indépendamment de fonction (i.e., potentiel membranaire). Le régent de CL-HB peut être simplement ajouté aux cellules et incubé durant une nuit à l’expression de la protéine. Le régent de CL-HB ne se réplique pas dans les cellules de mammifères et sont utilisables dans les paramètres de niveau 1 laboratoire (BSL) de prévention des risques biotechnologiques. Aussi, cette transfection transitoire peut être détectée après une nuit d’incubation jusqu'à 5 jours, suffisamment de temps pour procéder à des analyses cellulaires plus dynamiques.
Par ailleurs, les anomalies chromosomiques pourraient être étudiées par différentes techniques telles que la cytométrie en flux, immunohistochimie ou fluorescence in situ hybridation (poisson) 6. Cytométrie en flux peut être utilisée pour étudier l’aneuploïdie, qui peut être mesurée basée sur le contenu en ADN et la phase de cellules dans le cycle cellulaire. Bien que la cytométrie en flux peut être utilisée pour mesurer l’aneuploïdie, il ne fournit pas les informations sur la ségrégation chromosomique mauvaise. Techniques de poisson et l’immunohistochimie utilisent des sondes fluorescentes pour lier à l’ADN ou des chromosomes. Bien que ces techniques fournissent un instantané de l’état d’une population de cellules, ils ne permettent pas de cellules vivantes d’imagerie manquant ainsi toute information obtenue par le biais de visualisation spatio-temporelle de la cytokinèse dans certaines cellules suivies sur une période de temps.
Ce protocole a été utilisé pour étudier les chromosomes retardataires ou chromosomique mauvaise ségrégation dans la nocodazole traité fibroblastes embryonnaires de souris (MEFs) isolés de PP2A-B56γ-souris. Ce protocole prévoit, en plus de demande, un outil simple pour étiqueter et visualiser la ségrégation chromosomique dans divers types de cellules qui permet d’étudier la régulation du cycle cellulaire ou une instabilité chromosomique dans les cellules tumorales. En outre, il peut également être utilisé pour étudier l’instabilité chromosomique causée par différents traitements médicamenteux ou à étudier les effets du gène assommer résultant de la mis ségrégation chromosomique.
Protocole
Toutes les expériences menées dans ces études ont été effectuées conformément aux protocoles approuvés par le Comité de l’emploi et d’institutionnels animalier dans le centre de recherche de Food and Drug Administration (FDA).
1. isolement et Culture de fibroblastes embryonnaires de souris (MEFs)
- Isoler les fibroblastes embryonnaires de souris (MEFs) d’une souche de PP2A-B56γ-souris et ceux de type sauvage par le protocole standard 7,8,9.
- ExpandMEFs pour 3 passages, congeler et stocker jusqu'à ce que nécessaire pour expériences 8.
2. culture Mefs en lamelle couvre-lame 2 puits pour vivre d’imagerie
- Préparer 500 mL de milieu de culture de MEF contenant du milieu d’Eagle modifié Dulbecco (DMEM/F12) avec 10 % sérum bovin fœtal (SVF), 1 antibiotiques X pénicilline/streptomycine, L-Glutamine (200 mM) et 1 X des acides aminés non essentiels (NEAA) dans une bouteille de 500 mL de médias.
- Décongeler les flacons de MEFs congelés de type sauvage et PP2A-B56γ-souris au passage 3 de bain-marie préchauffé à 37 ° C.
- Transfert décongelés MEFs aux tubes de 15 mL et ajouter lentement goutte à goutte 20 mL de DMEM/F12 médias aux tubes de 15 mL à l’aide d’une pipette 10 mL.
- Transfert de MEFs avec 20 mL de milieu DMEM/F12 dans des flacons de T75 et développer jusqu'à ce que les cellules sont 70 % anastomosé. Confluence est estimé en utilisant un microscope inverse à 4 x ou un grossissement x 10.
- Aspirez le milieu de culture à l’aide d’un pâturage de verre Pipeter attaché à un système d’aspiration de la hotte, ajouter 3 mL de 0,25 % de trypsine/EDTA et incuber à 37 ° C pendant 5 min. Ajouter 3 mL de milieu DMEM/F12 pour arrêter la réaction.
- Centrifuger les cellules à basse vitesse (300 x g) pendant 5 min à température ambiante. Avec précaution, retirez le surnageant et Resuspendre le culot dans 1 mL de milieu DMEM/F12 préchauffée à 37 ° C dans un bain d’eau.
- Énumérer les cellules à l’aide de la méthode d’exclusion bleu trypan ou d’autres cellules appropriées, 8de la méthode de comptage.
- Graines d’environ 20 000 MEFs/puits dans un verre de couverture chambré 2 puits. Ajouter 200 µL/puits milieu DMEM/F12 et laisser les cellules à s’attacher en incuber une nuit à 37 ° C et 5 % de CO2.
3. synchronisation
- Synchroniser les MEFs en phase G0/G1 en incubant les cellules dans un milieu de croissance de DMEM/F12 contenant 0,1 % FBS pendant 24 h, afin d’obtenir un nombre maximal de cellules en phase G0/G1.
Remarque : Bien que le sérum était utilisée comme une méthode de préférence, diverses autres méthodes peuvent être utilisées selon le stade mitotique au cours de laquelle les cellules sont nécessaires pour être arrêtée 10.
4. étiquetage
- Préparer le 1,5 mg/mL solution de la nocodazole dans le DMSO. Nocodazole arrête les cellules en phase G2/M en inhibant la formation de microtubules 10.
- Trois jours après la synchronisation, ajouter 200 µL de milieu de culture (avec 10 % FCS), 200 ng/mL nocodazole et régent de CL-HB (Histone 2 b-GFP BacMam 2.0).
- Calculer le régent de CL-HB particules par cellule (PPC) à ajouter aux cellules comme suit :
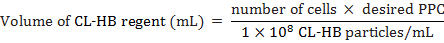
Lorsque le nombre de cellules est le nombre total estimé de cellules au moment de l’étiquetage, le CPMP est le nombre de particules par cellule, et 1 × 108 est le nombre de particules / mL de réactif. Par exemple, pour marquer 20 000 les cellules avec un PPC de 30
NOTE : Regent CL-HB fonctionne bien avec la plupart des types cellulaires entre 10 et 50 PPC. Cependant, 30 PPC travaille mieux pour cette étude. - Incuber les MEFs pendant 18 h à 37 ° C et 5 % de CO2.
Remarque : Pour l’expérience actuelle, visualisation des chromosomes dans les cellules mitotiques échapper le poste de contrôle de l’Assemblée de broche survint 18 h après l’arrêt du cycle cellulaire avec la nocodazole.
5. visualisation des Chromosomes traînards
- Visualiser les fibroblastes embryonnaires de souris (MEFs) en utilisant un système de microscope confocal de disque spinning équipé d’une chambre et une immersion dans l’huile, 63 x objectif.
- Utilisez onde d’excitation de 488 nm et d’émission d’onde 450 nm pour l’acquisition d’images canal GFP.
- Utiliser un système de microscope confocal tourne disque avec la capacité des stades de balayage motorisés, Z-Piezo insère, haut stade d’incubation et de récupération de fluorescence directe après le blanchiment de photo pour cette technique.
- Un jour avant l’imagerie, allumer le courant chambre environnementale et réchauffer la chambre entière à 37 ° C pendant la nuit.
- Mettez sous tension puissance de statif, caméra, unité de disque de filature, illuminateur, laser argon, ordinateur et platine motorisée.
- Laisser le système chauffer pendant 3 min ; commencer le laser argon en tournant sur la clé de contact. Basculer l’interrupteur à bascule pour laser à l’argon de « veille » à « laser run ».
- Lancer le logiciel d’acquisition et de traitement des données.
- Initialiser le contrôleur de CO2 pour l’incubateur haut de la scène et a fixé la concentration de CO2 à 5 %. Cela doit être fait avant le début de l’imagerie.
- Retirez le couvercle en verre chambré de l’incubateur et la place sur la scène pour la visualisation. Visualiser les cellules grâce à un huile d’immersion x 63 objectif (NA1.4).
- Découvre à travers les lentilles oculaires, mettre l’image et d’identifier une cellule en phase de décomposition (NEBD) enveloppe nucléaire.
- Initier approprié laser (laser à argon nm 488 pour visualiser Histone2B-GFP).
- Ouvrez la fenêtre de contrôle d’acquisition et régler la durée d’exposition pour le canal GFP. Identifier une cellule qui se trouve dans NEBD.
- Manuellement déterminer la partie supérieure de la cellule cible et plan focal bas et entrer dans l’optique de la section paramètres de xyz.
- Observez-la pendant 20 min ; Si la cellule ne se livre pas par le biais de la division cellulaire, arrêter après 20 min d’acquisition d’images et de passer à la cellule suivante qui se trouve dans NEBD.
- Environ 1 h par cellule est nécessaire aux chromosomes retardataires image au cours de la mitose chez PP2A-B56γ-cellules qui ont fui le SAC. Pour obtenir des données pour un film, prendre des photos toutes les 3 min.
Remarque : les cellules de type sauvage, arrêtent et progresse pas passé NEBD lorsque les traités avec la nocodazole. - Enregistrer des images au format de fichier de zvi pour une analyse ultérieure.
6. traitement et analyse d’images
Remarque : Effectuer le traitement de l’image en trois dimensions et de l’analyse à l’aide de tout logiciel disponible comme Axiovision version 4.8.2 ou Imaris version 8.2. Logiciel a été utilisé pour cette étude le ImageJ.
- Ouvrez la séquence d’images. Si les images sont déjà dans un format de pile, passez à l’étape suivante. Si non, combiner tous les images pertinentes dans une pile à l’aide de ' Image > cheminées > Images à pile ' dans la barre de menus.
- Effectuer les rajustements au besoin de luminosité/contraste et niveaux.
- Pour ajouter un horodatage pour le film :
- Allez dans "Image > cheminées > étiquette...' dans la barre de menus.
- Sélectionnez le format approprié, la valeur de temps de départ et intervalle de temps entre chaque image.
- Cochez la case « Aperçu » et ajuster les paramètres d’emplacement et le format. Appuyez sur « OK » pour appliquer l’horodatage.
- Pour ajouter une barre d’échelle pour le film :
- Définir l’image mise à l’échelle sous ' analyser > définissez échelle ' dans la barre de menus.
- Dans le champ « Distance en pixels », entrez un nombre de pixels lorsque la distance est connue et dans le domaine de la « Distance connue » entrez la distance. Définir la bonne unité de longueur pour la distance, par exemple, en µm. Appuyez sur « OK » pour appliquer le barème à la pile.
- Allez dans "Analyze > Outils > échelle bar..." pour ajouter la barre d’échelle. Définir la taille de la barre comme « Largeur en µm » et régler les autres options selon qu’il conviendra de formatage. Cochez la case « Label toutes tranches » pour ajouter la barre d’échelle à l’ensemble de la pile.
- Prévisualiser le film en cliquant sur le bouton de lecture triangulaire en bas à gauche de la fenêtre d’image. Ajuster le taux de trame à l’aide "Image > cheminées > Animation > Animation Options' dans la barre de menu.
- Exporter le fichier de film en sélectionnant ' fichier > Enregistrer sous > AVI... "et sélectionnez la fréquence d’images et de compression.
- Appuyez sur « OK » pour choisir l’enregistrement emplacement et nom du fichier. Appuyez sur « Enregistrer » pour enregistrer le fichier de film.
Résultats
MEFs de type sauvage et PP2A-B56γ-souris ont été ensemencées dans une chambre de 2 puits couvercle en verre et autorisés à fixer. Jour 2, MEFs ont été synchronisées à l’aide de 0,1 % FBS pendant 24 h. Jour 3, MEFs dans les médias, avec 200 ng/mL nocodazole et 30 CL de PPC-HB regentwere incubés pendant 18 h à 37° C et 5 % CO2. Jour 4, les cellules ont été projetés en utilisant un système de microscope confocal de disque de rotation (
Discussion
Points de contrôle de contrôle cycle cellulaire qui assurent la ségrégation des chromosomes précis empêchent aneuploïdie et cell transformation 1,2,3. Dans la présente étude, nous avons trouvé que l’inactivation de PP2A-B56γ a donné lieu à un poste de contrôle de l’Assemblée broche affaibli. L’imagerie de cellules vivantes nous a permis d’observer la mis-ségrégation chromosomique au cours de la mitose ch...
Déclarations de divulgation
Les auteurs déclarent qu’ils n’ont aucun intérêt financier concurrentes.
Remerciements
Nous tenons à remercier Dr Guo-Chiuan Hung et m. Bharatkumar Joshi de précieux commentaires qui ont amélioré le manuscrit.
matériels
| Name | Company | Catalog Number | Comments |
| DMEM/F12 | Gibco | 11320082 | |
| L-Glutamine | Gibco | 25030081 | |
| MEM Non-Essential amino acids solution (100X) | Gibco | 11140050 | |
| Penicillin-Streptomycin (10,000 U/mL) | Gibco | 15140122 | |
| Dulbecco’s Phosphate Buffered saline | Gibco | 14190144 | |
| Trypsin-EDTA | Gibco | 25300054 | |
| Fetal bovine serum | Atlanta Biologicals | S11150 | |
| DMSO | EMD Millipore | MX 1458-6 | |
| Cryogenic vial storage boxes | Fisherbrand | 10-500-28 | |
| Cryogenic vials | Corning/costar | 431416 | |
| T75 flasks | Cellstar | 658175 | |
| 2 well chambered cover glass | Nunc | 155380PK | |
| Cellometer Vision Cell Profiler | Nexcelom Bioscience LLC | Cellometer Vision Trio | |
| Nocodazole | Sigma | M1404 | |
| CellLight Histone 2B-GFP, BacMam 2.0 | Thermo Fisher Scientific Inc. | C10594 | |
| Zeiss Cell Observer Spinning Disk Confocal Microscope system | Carl Zeiss Microscopy | Zeiss Cell Observer SD | |
| Water Bath | Thermoscientific | 280 series | |
| Incubator | Sanyo commercial solutions | MCO-18AIC (UV) | |
| Class II Biological safety cabinet | The Baker Company | SterilGard | |
| Axiovision software | Zeiss | Ver.4.8.2 | |
| ImageJ software | National Institute of Health | Ver. 1.51r |
Références
- Funk, L. C., Zasadil, L. M., Weaver, B. A. Living in CIN: Mitotic Infidelity and Its Consequences for Tumor Promotion and Suppression. Dev Cell. 39, 638-652 (2016).
- Etemad, B., Kops, G. J. Attachment issues: kinetochore transformations and spindle checkpoint silencing. Curr Opin Cell Biol. 39, 101-108 (2016).
- Lara-Gonzalez, P., Westhorpe, F. G., Taylor, S. S. The spindle assembly checkpoint. Curr Biol. 22, 966-980 (2012).
- Jallepalli, P. V., Lengauer, C. Chromosome segregation and cancer: cutting through the mystery. Nat Rev Cancer. (2), 109-117 (2001).
- Zhu, L., et al. Mitotic protein CSPP1 interacts with CENP-H protein to coordinate accurate chromosome oscillation in mitosis. J Biol Chem. 290 (45), 27053-27066 (2015).
- Pikor, L., Thu, K., Vucic, E., Lam, W. The detection and implication of genome instability in cancer. Cancer Metastasis Rev. 32 (3-4), 341-352 (2013).
- Varadkar, P., Despres, D., Kraman, M., Lozier, J., Phadke, A., Nagaraju, K., McCright, B. The protein phosphatase 2A B56γ regulatory subunit is required for heart development. Dev Dyn. 243 (6), 778-790 (2014).
- Jozefczuk, J., Drews, K., Adjaye, J. Preparation of Mouse Embryonic Fibroblast Cells Suitable for Culturing Human Embryonic and Induced Pluripotent Stem Cells. J. Vis. Exp. (64), e3854 (2012).
- Varadkar, P., Abbasi, F., Takeda, K., Dyson, J. J., McCright, B. PP2A-B56γ is required for an efficient spindle assembly checkpoint. Cell Cycle. 18 (12), 1210-1219 (2017).
- Rosner, M., Schipany, K., Hengstschläger, M. Merging high-quality biochemical fractionation with a refined flow cytometry approach to monitor nucleocytoplasmic protein expression throughout the unperturbed mammalian cell cycle. Nat Protoc. 8 (3), 602-626 (2013).
- Jonkman, J., Brown, C. M. Any Way You Slice It-A Comparison of Confocal Microscopy Techniques. J Biomol Tech. 26 (2), 54-65 (2015).
- Versaevel, M., Braquenier, J. B., Riaz, M., Grevesse, T., Lantoine, J., Gabriele, S. Super-resolution microscopy reveals LINC complex recruitment at nuclear indentation sites. Sci Rep. 8 (4), 7362 (2014).
- Wild, T., Larsen, M. S., Narita, T., Schou, J., Nilsson, J., Choudhary, C. The Spindle Assembly Checkpoint Is Not Essential for Viability of Human Cells with Genetically Lowered APC/C Activity. Cell Rep. 1 (8), 1829-1840 (2016).
- Iuso, D., et al. Exogenous Expression of Human Protamine 1 (hPrm1) Remodels Fibroblast Nuclei into Spermatid-like Structures. Cell Rep. 1 (9), 1765-1771 (2015).
- Ratcliffe, E., Glen, K. E., Naing, M. W., Williams, D. J. Current status and perspectives on stem cell-based therapies undergoing clinical trials for regenerative medicine: case studies. Br Med Bull. 108, 73-94 (2013).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon