Method Article
Préparation des compartiments des chloroplastes d’Arabidopsis pour l’analyse de la localisation de la protéine par immunotransfert ou protéomique
Dans cet article
Résumé
Nous décrivons ici une méthode pour purifier les chloroplastes intacts des feuilles de l’Arabidopsis et leurs trois compartiments secondaires principaux (enveloppe, stroma et les thylakoïdes), en utilisant une combinaison de centrifugations différentielles, gradient de Percoll continue, et gradients de sucrose discontinu. La méthode est importante par subplastidial et localisation sous-cellulaire des protéines par immunotransfert et protéomique.
Résumé
Les chloroplastes sont des composants importants des cellules végétales. Ces plastes remplissent plusieurs fonctions cruciales, telles que l’assimilation du carbone, de soufre et d’azote ainsi que la synthèse de métabolites essentiels. Ces organites sont constitués des trois compartiments sous clés suivantes. L’enveloppe, caractérisée par deux membranes, entoure l’organite et contrôle de la communication de la plaste avec d’autres compartiments cellulaires. Le stroma est la phase soluble du chloroplaste et le site principal où le dioxyde de carbone est converti en hydrates de carbone. La membrane thylakoïde est le réseau de membrane interne composé de grana (plats Sakis compressés) et lamelles (moins structures denses), où la photosynthèse oxygénique a lieu. Le présent protocole décrit étape par étape les procédures requises pour la purification, à l’aide de centrifugations différentielles et gradient de Percoll, des chloroplastes intacts des Arabidopsiset leur fractionnement, utilisant des gradients de sucrose, dans trois compartiments secondaires (c.-à-d., enveloppe, stroma et les thylakoïdes). Ce protocole a également fournit des instructions sur comment évaluer la pureté de ces fractions à l’aide de marqueurs liés à différents compartiments des chloroplastes. La méthode décrite ici est précieuse pour la localisation subplastidial des protéines, immunoblotting, mais aussi pour subcellulaire et protéomique de subplastidial et d’autres études.
Introduction
Les chloroplastes sont des composants importants des cellules végétales. Ils dérivent d’un ancêtre de cyanobactéries qui a fait l’objet d’une endosymbiose et finalement évolué comme un organite au cours de l’évolution1,2. Ces organites contiennent trois compartiments principaux (Figure 1). Le système de l’enveloppe fait d’un intérieur et un extérieur les membranes entourant l’organite. Ce système de double membrane contient diverses enzymes impliquées dans le métabolisme des lipides et des pigments et est surtout consacré au contrôle de la communication entre le cytosol et les plastes. Il contient divers systèmes de transport qui permettent l’importation de protéines codées et l’échange d’ions et des métabolites entre le cytosol et le chloroplaste ainsi réguler des fonctions métaboliques essentielles du plant cell3,4 . Le stroma, la phase soluble du chloroplaste, contient des enzymes du cycle de Calvin (assimilation de CO2 ), la synthèse de divers métabolites, y compris les acides aminés et vitamines et les machines de transcription et de traduction du plaste. La membrane thylakoïde est un réseau de membrane interne largement organisé où s’effectue la phase légère de photosynthèse. Ainsi, les chloroplastes sont le lieu où trouvent les voies métaboliques essentielles5.
Afin de décrypter les nouveaux mécanismes de régulation qui contrôlent la dynamique des chloroplastes et la physiologie, définissant la localisation sup-plaste des protéines chloroplastique est donc essentiel de soutenir des études ciblées visant à mieux comprendre les fonctions des protéines dans le modèle organismes6. Pour avoir accès à la localisation de subplastidial véritable de ces protéines, il est donc essentiel pour démarrer à partir de fractions très pur subplastidial (membranes d’enveloppe, stroma et thylakoïdes). Dans ce contexte, le but du présent protocole est de purifier les chloroplastes intacts d’Arabidopsis feuilles à l’aide de centrifugations différentielles et des gradients Percoll continues et de fractionner les à l’aide de gradients de sucrose discontinu, dans trois compartiments secondaires (c.-à-d., enveloppe, stroma et les thylakoïdes). La méthode décrite ici fournit également des instructions pour évaluer la pureté des fractions de sub-organellar purifiées à l’aide de marqueurs liés à différents compartiments des chloroplastes. Ce protocole est utile pour subplastidial la localisation des protéines à l’aide d’immunotransfert et pour une analyse plus approfondie des fractions purifiées par spectrométrie de masse (MS)-basé des études protéomiques.
Protocole
1. préparation des tampons, des Solutions mères et dégradés
- Préparer les solutions suivantes qui peuvent être conservées jusqu'à 6 mois à 4 ° C.
- Préparer 1 L de buffer de Tricine (1 M, pH 8,4) et Tricine (1 M, pH 7,6). Ajuster le pH en ajoutant des boulettes de KOH.
- Préparer 1 L de l’acide éthylènediaminetétraacétique (EDTA, 0,5 M, pH 8) et 3-(N-morpholino) au propane sulfonique (MOPS) tampon (1 M, pH 7.8). Ajuster le pH en ajoutant des pastilles de NaOH.
- Préparation de 50 mL de MgCl2 (1 M).
- Préparer une 50 mL de protéase inhibiteurs : le fluorure de phénylméthylsulfonyle (PMSF mis en place dans l’isopropanol, 100 mM), hydrate de chlorhydrate de benzamidine (100 mM) et ε-aminé acide caproïque (50 mM).
Remarque : Bien que PMSF et amino acide caproïque sont stables en solution pendant des mois à 4 ° C, benzamidine solution doit être conservée à-20 ° C.
- Préparer les solutions suivantes la veille de l’expérience et stocker toutes les solutions à 4 ° C.
- Préparer 4 litres de mouture moyenne pH 8,4 contenant Tricine-KOH (20 mM, pH 8,4), sorbitol (0,4 M), l’EDTA (10 mM, pH 8) et NaHCO3 (10 mM). Ajuster le pH en ajoutant des pastilles de NaOH. Ajouter l’albumine sérique bovine (BSA) à 0,1 % (p/v) juste avant l’utilisation et bien mélanger.
- Préparer 500 mL de lavage pH moyen (x 2) 7,6 contenant Tricine-KOH (20 mM, pH 7,6), sorbitol (0,8 M), MgCl2 (5 mM) et l’EDTA (2,5 mM). Ajuster le pH en ajoutant des pastilles de NaOH. Diluer cette solution après préparation de solution de gradient de Percoll obtenir lavage moyen (1 x).
- Préparez 200 mL de solution de gradient de Percoll pour la purification des chloroplastes en mélangeant Percoll avec lavage moyen (x 2) à un volume égal d’obtenir une solution finale à 50 % (v/v) Percoll / 0,4 M sorbitol.
- Préparer 50 mL des solutions de saccharose pour fractionnement de chloroplastes en mélangeant MOPS (10 mM, pH 7,8), MgCl2 (4 mM) et différentes concentrations de saccharose (M 0,3, 0,6 M et 0,93 M).
- Préparer les dégradés et les tampons avant de commencer l’expérience suivantes.
- Préparer six tubes de gradients Percoll (chacun contenant 30 mL d’un 50 % Percoll / 0,4 M sorbitol) par centrifugation à 38 700 x g pendant 55 min à 4 ° C. Éloigner le frein pour éviter le mélange des gradients. Après centrifugation, ranger les tubes contenant les gradients préformés dans une chambre froide jusqu'à utilisation.
- Préparer quatre tubes de gradients de sucrose, avec chaque pente formée de trois couches de saccharose suivantes : 3 mL de 0,93 M, 2,5 mL de 0,6 M et 2 mL de saccharose de 0,3 M. Le recouvrement soigneusement chaque couche, à l’aide d’une pompe péristaltique commençant par 0,93 M en bas et en finissant par 0,3 M au sommet.
- Préparer 50 mL de milieu hypotonique à la lyse des chloroplastes contenant MOPS (10 mM, pH 7,8), MgCl2 (4 mM), PMSF (1 mM, mis en place dans l’isopropanol), hydrate de chlorhydrate de benzamidine (1 mM) et ε-aminé acide caproïque (0,5 mM). Stocker le tampon sur la glace jusqu'à l’utilisation.
- Préparation de 50 mL de membrane lavage tampon contenant MOPS (10 mM, pH 7,8), PMSF (1 mM), hydrate de chlorhydrate de benzamidine (1 mM) et ε-aminé acide caproïque (0,5 mM). Stocker le tampon sur la glace jusqu'à l’utilisation.
2. croissance et la récolte des feuilles de l’Arabidopsis
- Pour la croissance des plantes Arabidopsis , préparez 4 grandes casseroles en plastique (pour une surface totale de 0,5 à 1 m2) des plantes Arabidopsis en semant 30 mg de graines dans chaque casserole. Faire pousser des plantes Arabidopsis pendant 5 semaines au cycle de lumière de 12 h à 23 ° C (jour) / 18 ° C (nuit) avec une intensité lumineuse de 150 μM m-2 s-1.
- Incuber les plantes dans une pièce sombre et froide (4 ° C) pendant la nuit avant l’expérience (pour réduire la quantité de granules d’amidon dans les chloroplastes).
- Avant de peser un bécher de 1 L et puis placez-le sur la glace avant de commencer la récolte des feuilles.
- Récolter les feuilles de l’Arabidopsis en évitant les sols (compost). Réévaluer le bécher et noter le poids du tissu.
NOTE : 400 à 500 g de feuilles sont attendues de quatre casseroles. - Homogénéiser les feuilles dans une chambre froide avec 2 L de tampon de meulage (Ajouter BSA avant utilisation) trois fois / 2 s chaque fois, dans un mélangeur à haute vitesse.
- Filtrer l’homogénat dans une chambre froide à l’aide de 4 couches de mousseline et une couche de nylon blutex. Appuyer doucement sur les feuilles de l’homogénat à l’intérieur de la blutex de mousseline/nylon pour extraire tout le liquide.
- Récupérer le tissu restant dans la tasse du mélangeur pour une seconde extraction. Répétez les étapes 2.5 et 2.6 à l’aide de 2 L de broyage moyen et nouveaux 4-5 couches de mousseline (dans une chambre froide).
3. purification des chloroplastes bruts à l’aide de Centrifugation différentielle
- Tout aussi distribuer l’extrait cellulaire brut dans six bouteilles de 500 mL et placer les bouteilles sur la glace avant la centrifugation. Centrifuger pendant 2 min, dès que la vitesse maximale (2 070 x g) est atteinte (accélération maximale et frein, 4 ° C).
- Doucement, éliminer le surnageant.
- Aspirer le surnageant restant à l’aide d’une pompe à eau et garder des granulés contenant des chloroplastes bruts concentrés sur la glace.
- Resuspendre doucement les boulettes en ajoutant un volume minimal de lavage moyen (1 x) (volume final des suspensions combiné chloroplaste = 36 mL) à l’aide d’un pinceau ou une spatule en plastique incurvée. Utiliser une pipette de 10 mL pour ajouter 3 mL de milieu dans chaque bouteille de lavage.
Remarque : N’utilisez pas la pipette avec pointes très fines pour éviter la casse des chloroplastes. Vous pouvez également couper la pointe bleue d’une pipette avec une lame de rasoir pour générer un trou plus large. - Recueillir les chloroplastes remises en suspension dans un tube à l’aide d’une pipette 10 mL. Mélanger doucement en renversant le tube pour obtenir une suspension homogène avant leur chargement sur gradient de Percoll.
4. la purification des chloroplastes intacts sur Gradient de Percoll continu
- Lentement charger 6 mL de la suspension de chloroplastes sur le dessus de chacun des six gradients Percoll à l’aide d’une pipette de 10 mL pour éviter la casse des chloroplastes.
- Centrifuger les gradients pendant 10 min à 13 300 x g, 4 ° C à l’aide d’un rotor oscillant-seau.
Remarque : L’accélération doit être lente, et les freins doivent être débranchés (frein off ou décélération lente) pour éviter le mélange des gradients Percoll. - Aspirer la phase supérieure qui contient cassé les chloroplastes et les mitochondries intactes à l’aide d’une pompe à eau et ensuite récupérer les chloroplastes intacts présents dans la partie inférieure (la bande large de couleur vert foncé) de phase avec une pipette de 10 mL. Veillez à ne pas aspirer les noyaux et les débris cellulaires (qui se trouve au fond du tube) avec les chloroplastes intacts (Figure 2 a).
- Diluez 3 à 4 fois la suspension de chloroplastes intacts avec tampon de lavage (1 x). Centrifuger pendant 2 min, dès que la vitesse maximale (2 070 x g, 4 ° C) est atteinte (accélération maximale et frein).
- Soigneusement éliminer le surnageant.
- Totalement aspirer le surnageant restant avec une pompe à eau et garder le culot de concentré chloroplastes intacts sur la glace.
- Avant la lyse des chloroplastes, garder une partie aliquote de fraction de chloroplastes intacts dans environ 1 mL de lavage moyen (1 x) pour des analyses plus poussées à l’aide sur gel de polyacrylamide de sodium dodecyl sulfate (SDS-PAGE) et western blot. Garder une petite portion de ces chloroplastes intacts pour la détermination de la concentration de protéines. Stocker la fraction des chloroplastes intacts dans l’azote liquide pour d’autres expériences.
5. lyse des chloroplastes intacts à l’aide d’un tampon hypotonique et la Purification des chloroplastes des compartiments sur des Gradients de Sucrose discontinu
- Lyse des chloroplastes intacts purifiées par resuspendant le culot dans un milieu hypotonique contenant des inhibiteurs de la protéase (le volume final ne doit pas dépasser 12 mL).
Remarque : Cette étape, l’utilisation de la pipette avec pointes fines (bleus conseils) est possible puisque intact des chloroplastes est pas plus indispensable (pipetage chloroplastes haut et en bas aussi longtemps que le pellet n’est pas entièrement remis en suspension). Arabidopsis chloroplastes sont très fragiles (comparé aux chloroplastes de pois, par exemple) et leur lyse est presque immédiate après incubation dans un milieu hypotonique. - Lentement charger 3 mL des chloroplastes lysés sur le dessus de chaque gradients de sucrose préformé à l’aide d’une pompe péristaltique.
- Ultracentrifugeuse les gradients pendant 1 h (70 000 x g, 4 ° C). Équilibre entre paires de tubes à l’aide de tampon moyen hypotonique avant la centrifugation.
- Récupérer soigneusement les protéines solubles stromales en pipettant également, la phase supérieure du gradient (3 mL de chaque dégradé) (Figure 2 b). Prélever une partie aliquote de détermination de la concentration de protéine7. Stocker le stroma dans l’azote liquide pour d’autres expériences.
- Aspirer la phase supérieure restante de chaque dégradé jusqu'à la bande jaune à l’aide d’une pompe à eau.
- Récupérer la bande jaune (l’enveloppe) avec une pipette (environ 1 mL de chaque dégradé). Mettre en commun les enveloppes dans un tube.
- Supprimer la phase restante de chaque dégradé jusqu'à la pastille de thylakoïdes en utilisant une pompe à eau.
6. laver et Concentration des thylakoïdes et systèmes de Membrane d’enveloppe
- Resuspendre les thylakoïde pellets (granulés de verts) dans un volume minimum (2 mL) de membrane lavage tampon (1 x) (avec les inhibiteurs de la protéase).
- Diluer les suspensions de l’enveloppe et de thylakoïdes 3 à 4 fois dans le milieu de lavage de membranes (ajuster le volume à 10 mL) et ultracentrifugeuse pendant 1 h (110 000 x g, 4 ° C). Équilibre entre paires de tubes à l’aide de membranes lavage tampon avant la centrifugation.
- Soigneusement aspirer le surnageant à l’aide d’une pompe à eau.
- Ajouter environ 100 µL de tampon (avec les inhibiteurs de la protéase) au culot enveloppe de lavage de membranes. Prélever une partie aliquote de détermination de la concentration de protéine7. Stocker la préparation de membrane d’enveloppe purifiée dans l’azote liquide.
- Resuspendre les thylakoïdes culot dans 3 mL de membrane lavage tampon (avec les inhibiteurs de la protéase). Prélever une partie aliquote de détermination de la concentration de protéine7. Fraction des membranes thylakoïdes magasin dans l’azote liquide.
Résultats
Les étapes successives de la procédure qui aboutit en chloroplastes purifiée et leurs compartiments secondaires sont repris en Figure 2. Le gradient de Percoll (Figure 2 a) permet de distinguer les chloroplastes intacts de chloroplastes brisés et mitochondries (en haut de la pente) ou noyaux et débris cellulaires (en bas du gradient). Après rupture des organites purifiés Percoll grâce à un choc osmotique, les fractions qui en résultent sont séparées sur un gradient de saccharose (Figure 2 b). Le stroma (partie soluble du chloroplaste) est flottant à la surface de la pente de saccharose. Les vésicules de membrane légère enveloppe sont récupérés comme une discrète bande jaune à l’interface de saccharose de 0,6/0,93 M. Les vésicules de membranes thylakoïdes plus lourdes sont concentrées au fond du tube. Après récupération, lavage et concentration des fractions deux membranaires, les protéines sont quantifiés et la composition de tous les quatre fractions est analysée sur une SDS-PAGE (Figure 2). Les voies sont placées sur une base égale de protéines (20 µg de chaque fraction purifiée). Sachant que les chloroplastes contiennent seulement 1 % des protéines d’enveloppe et 50 % des protéines du stroma ou des thylakoïdes, ce qui tend à surestimer la contamination croisée des préparations enveloppe purifié avec autres compartiments des chloroplaste. Toutefois, cette méthode permet de détecter des quantités infimes de protéines contaminantes croix la fraction de l’enveloppe. Marqueurs de chaque compartiment (c'est-à-dire des protéines abondantes) sont très utiles pour évaluer la contamination croisée des fractions. En effet, les fractions de membranes thylakoïdes et enveloppe sont censées contenir des quantités très faibles de la grande sous-unité de RuBisCO (RBCL), la protéine la plus abondante du stroma (50 kDa). Chloroplastes brisés se distingués facilement de chloroplastes intacts en raison de la perte de cette protéine stromales8. La lumière récolte des protéines complexes (LHCP) sont des composants de thylakoïdes abondante de 25 kDa qui devraient à peine (moins de 3 %) contaminer enveloppe membranes9. Enfin, le translocator de phosphate-triose-phosphate (TPT) est une protéine de 30 kDa qui n’est visible dans la fraction purifiée enveloppe en raison de son fort enrichissement (c.-à-d., 50 à 100 x) dans la fraction de l’enveloppe par rapport aux chloroplastes entier extraits. En utilisant la méthode décrite ici, chloroplaste sous compartiments sont généralement mal contamination croisée comme l’a confirmé à l’aide d’analyses de western blot (Figure 2D) en s’appuyant sur des anticorps dirigés contre des marqueurs connus de tous les compartiments sous trois : la soluble cétol-acide reductoisomerase du (KARI) du stroma, l’enveloppe chloroplastique cuivre ATPase (HMA1) et la lumière récolte des protéines complexes (LHCP) des membranes thylakoïdes. La contamination croisée des trois compartiments sous peut être quantifiée à l’aide de tant d’immunobuvardage et masse spectrométrie analyses9. Alors que le stroma n’est habituellement pas contaminé par enveloppe ou thylakoïdes des fractions, fractions purifiées enveloppe contenant 3 % de protéines des thylakoïdes et jusqu'à 10 % des protéines du stroma. Les protéines du stroma peu contaminent les membranes thylakoïdes (moins de 1 %) mais les thylakoïdes contiennent jusqu'à 3 % de protéines de membrane d’enveloppe. Plus d’avoir un rôle crucial en identifiant l’emplacement véritable subplastidial de protéines de chloroplaste, la présente méthode donc limite également des conclusions erronées sur la localisation subplastidial des protéines résultant de traversent des contaminations.
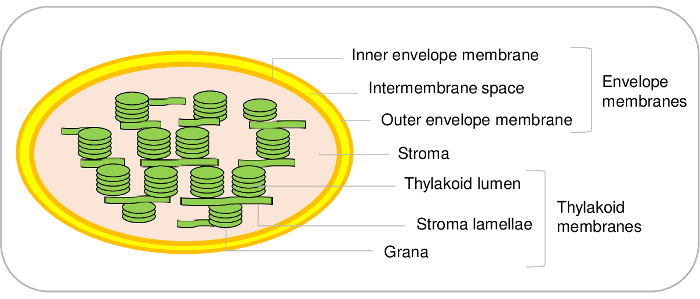
Figure 1 : Schéma représentatif du chloroplaste sous compartiments. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
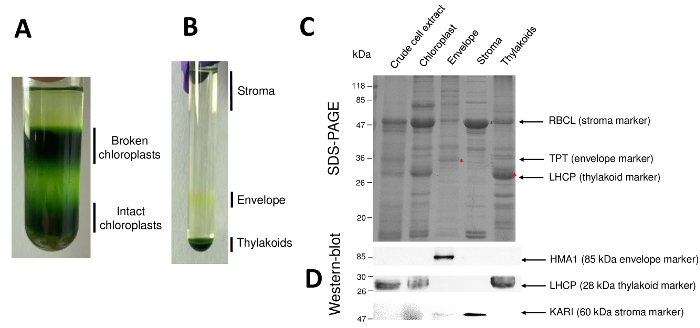
Figure 2 : Purification des chloroplastes intacts et leurs trois principales des compartiments avec des gradients Percoll et saccharose. A. gradient de Percoll permettant une séparation des chloroplastes brisés et intacts. B. gradient de saccharose qui permet la séparation des fractions stroma, enveloppe et thylakoïdes. C. représentant SDS-PAGE des protéines des chloroplastes intacts et leurs trois compartiments secondaires principales permettant de visualiser les marqueurs abondants de chaque compartiment secondaire. Chaque piste contient 10 µg de protéines. Marqueurs de poids moléculaire : RBCL, grandes sous-unités de la RuBisCO (marqueur pour le stroma) ; TPT, translocator Phosphate/triose-phosphate (marqueur de l’enveloppe) ; LHCP, léger, récolte des protéines complexes (marqueur pour les thylakoïdes). D. les expériences de Western blot permettant de détecter des marqueurs spécifiques (à l’aide d’anticorps spécifiques) de chaque compartiment secondaire : le chloroplaste enveloppe cuivre ATPase HMA110, la lumière récolte des protéines complexes LHCP partir du thylakoïde membranes11et le reductoisomerase de cétol-acide du KARI du stroma9. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
Discussion
Le présent article a pour but de détailler le protocole étape par étape utilisé pour purifier les chloroplastes (et leurs compartiments secondaires) d’Arabidopsis thaliana. Depuis la disponibilité de sa séquence complète du génome il y a près de vingt ans et de grandes collections de mutants d’insertion mises à la disposition de la Communauté, Arabidopsis est maintenant largement reconnue comme une plante modèle. Cependant, alors que cette plante était parfaitement adaptée pour des approches génétiques, plantez des scientifiques nécessaires pour adapter les outils biochimiques et physiologiques pour ce nouveau modèle. Protocoles permettant de purifier le rayonnement photosynthétiquement actifs chloroplastes des feuilles de modèles biochimiques bien établis comme épinards12 ou pois13 donc a dû être adaptée. La première méthode décrivant la purification des chloroplastes d’Arabidopsis a été publiée en 199814, juste avant la sortie de la séquence du génome d’Arabidopsis . Plusieurs années plus tard, simples méthodes pour isoler les chloroplastes d’Arabidopsis compatibles avec les études visant à analyser in vitro l’importation de protéines dans les organites purifiés ont fait disponible15,16. Cependant, ces méthodes ne permettaient pas de combiner le degré élevé de pureté et de la préservation de l’activité photosynthétique des chloroplastes purifiées. Plus récemment,17, une méthode rapide qui s’appuie sur l’utilisation de gradients Percoll et permet de conserver près de 90 % du taux de photosynthèse mesuré dans les feuilles de départ de l’Arabidopsis a été créé.
Le protocole décrit ici permet de purifier les chloroplastes d’Arabidopsis à un excellent niveau de pureté. En effet, détection immunologique de contaminants provenant des autres compartiments cellulaires ont démontré que les organites purifiés sont dépourvues de mitochondries et membrane plasmique marqueurs9,10. Ce protocole a été aussi efficace pour purifier les chloroplastes de plusieurs Arabidopsis écotypes18, comme la Colombie (Col) ou Wassilewskija (WS), c'est-à-dire les écotypes qui ont été utilisés pour génome ou exprimés sequence tags (ESTs) séquençage des projets mais aussi à générer des mutants d’insertion de l’ADN-T chez Arabidopsis. En d’autres termes, lorsque la protéomique des études doivent être effectuées, le présent protocole est compatible avec ces deux écotypes de référence d’Arabidopsis. Enfin, le rendement des chloroplastes en utilisant le présent protocole est similaire à celui obtenu lors du démarrage de feuilles d’épinards ou de pois (soit 3 %, mesuré par rapport à la teneur en chlorophylle dans les chloroplastes Percoll purifié par rapport au total quantité de chlorophylle présente à partir de feuilles). En termes de protéines, le rendement est proche de 50 mg de protéines de chloroplaste, lorsque les organites sont purifiés de 500 g de feuilles de Arabidopsis de 5 semaines.
Pour atteindre un bon rendement (et l’intégrité des chloroplastes), on devrait toutefois accorder une attention particulière à plusieurs étapes lors de l’utilisation du présent protocole. Le chloroplaste chez Arabidopsis est une structure extrêmement fragile (ce n’est pas le cas pour les chloroplastes de pois, par exemple). Il faut donc une attention particulière afin d’éviter une rupture à grande échelle des organites durant la purification. Le nombre et la taille des granules d’amidon présents dans les chloroplastes sont essentiels pour la préparation des chloroplastes intacts. En effet, chloroplastes contenant des grains d’amidon grand sera généralement cassés durant les étapes initiales centrifugations différentielles visant à concentrer le chloroplaste brut fractions12. Par conséquent, les plantes il faut toute la nuit dans une pièce sombre et froide (4 ° C) avant l’expérience, afin de réduire la quantité d’amidon.
Nouveaux utilisateurs du présent protocole soient tentées de lancer de plus grandes quantités de matériel foliaire (énormes rosettes de vieilles plantes Arabidopsis à grandes feuilles) essayer d’améliorer la récupération des chloroplastes purifiées. Toutefois, dans nos mains, à partir de jeunes feuilles (5 semaines) est le meilleur compromis pour combiner le rendement, la pureté et l’intégrité des organites purifiés. En effet, trop vieilles feuilles sont fortement enrichis en composés phénoliques qui ont un impact négatif sur les chloroplastes intégrité19.
Enfin, l’étape d’extraction initiale (broyage des tissus) est une autre étape critique. Le processus de fusion doit être limité à quelques secondes. Comme indiqué ci-dessus, nouveaux utilisateurs pourraient être tentés d’utiliser plus de mélange, espérant ainsi fortement améliorer le rendement des organites purifiés. Toutefois, si le mélange plus efficacement libère plus de matériel de feuilles, il semble que la proportion des chloroplastes cassés augmente rapidement dans l’extrait cellulaire brut. En raison de ce ratio élevé brisure à chloroplastes intacts dans le milieu, outre les étapes de purification (séparation sur gradient de Percoll) sont fortement affectées et le rendement de la purification est subitement plus faible.
Disponibilité des protocoles spécifiques pour purifier les organites ont permis une série de haut débit protéomique axée sur les expériences effectuées sur des échantillons de chloroplastes. Ces données ont été distribuées dans plusieurs bases de données publiques6, offrant ainsi aux biologistes sur le terrain une localisation subcellulaire (et subplastidial) précise pour plusieurs protéines chloroplastique. C’était particulièrement vrai pour les protéines de l’enveloppe dont l’identité et le lieu restée pratiquement inconnu avant ces analyses, membranes d’enveloppe représentent une composante mineure chloroplaste (1-2 % des protéines des chloroplastes) tout en jouant un rôle clé dans le chloroplaste métabolisme et biogenèse5,20. Utilisant le protocole décrit ici, nous avons récemment analysé la composition des trois compartiments principal chloroplastes d’Arabidopsis (c.-à-d., le stroma, les thylakoïdes et le système de membrane d’enveloppe)9. Basé sur une approche protéomique semi-quantitatif (comptage spectrale), nous avons pu évaluer le partitionnement de plusieurs centaines de protéines dans ces trois compartiments de chloroplastes.
Alors que le présent protocole permet de purifier les trois compartiments principaux du chloroplaste de l’Arabidopsis, il est également possible de distinguer des compartiments secondaires supplémentaires dans le chloroplaste. En effet, le système de membrane d’enveloppe fait de l’intérieur et les membranes de l’enveloppe extérieure (Figure 1). Cependant, au meilleur de nos connaissances, une méthode pour purifier les membranes de l’enveloppe intérieure et extérieure de chloroplastes d’Arabidopsis reste à établir. Membranes de l’enveloppe intérieure et extérieure peuvent être purifiés de chloroplastes d’épinard21 ou pois de22 . La principale limitation de Arabidopsis résulte principalement des montants limitatifs de matière première. À partir de 500 g de feuilles de l’Arabidopsis (qui exige déjà 1 m2 surface dans une chambre de croissance) permet de purifier seulement 100 µg de protéines de l’enveloppe. En revanche, il est facile de commencer avec des feuilles de 5 à 10 kg d’épinards du marché, pour purifier la grande quantité de chloroplastes8 et à la fin avec un rendement de 3 à 10 mg de protéines de l’enveloppe de ce matériau.
Il en va de même pour les compartiments des thylakoïdes. En effet, les thylakoïdes sont faites de la lumière des vésicules membranaires (lamelles) et des structures denses (grana) (Figure 1). Il existe des protocoles spécifiques distinguer ces deux compartiments dans Arabidopsis23,24. Encore une fois, basée sur une analyse protéomique quantitative, récemment inventorié les protéines présentes dans ces deux compartiments sous24. Ces approches, ainsi que d’une enquête approfondie de la littérature, a permis de valider, ou proposer des hypothèses pour, l’emplacement de subplastidial de centaines de protéines des thylakoïdes. Cependant, il est important de noter que les microdomaines membranaires supplémentaires sont présents à marge incurvée de thylakoïdes. Ces lipoprotéines compartiments secondaires, ou les plastoglobules, sont couplés en permanence aux membranes des thylakoïdes et contiennent un ensemble spécifique de protéines,25. En utilisant le présent protocole, il est donc pas possible de distinguer ces protéines spécifiques des autres composantes de thylakoïdes.
Certains composants d’enveloppe, stroma ou thylakoïdes (bien connus) véritables manquent encore dans les listes des protéines détectées. Ainsi que des analyses biochimiques et immunologiques ciblées, l’amélioration continue de la sensibilité de MS sera d’une grande aide de revenir sur le contenu de chloroplaste vers un répertoire complet de la composition de ses divers compartiments secondaires.
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ce travail a été soutenu par une bourse de doctorat conjointe à IB de la biologie végétale INRA et Division de l’élevage et des Labex GRAL (ANR-10-LABX-49-01). Nous tenons également à saluer le projet ANR ANR-15-IDEX-02, Dr. Olivier Vallon (IBPC Paris) pour les anticorps anti-LHCP et Dr Renaud Dumas (LPCV, Grenoble) des anticorps contre KARI.
matériels
| Name | Company | Catalog Number | Comments |
| Percoll | GE Healthcare | 17089101 | |
| Tricine | Roth | 6977.2 | |
| Sorbitol | Roth | 6213.1 | |
| Ethylenediaminetetraacetic acid (EDTA) | Promega | H5032 | |
| NaHCO3 | Roth | 8551.1 | |
| Bovine serum albumin (BSA) | Roth | 8076.5 | |
| MgCl2 | Roth | 2189.1 | |
| Phenylmethylsulfonyl fluoride (PMSF) | Sigma | P7626 | |
| Benzamidine | Sigma | B6506 | |
| ε-amino caproic acid | Fluka | 21530 | |
| 3-(N-morpholino) propane sulfonic acid (MOPS) | Roth | 6979.3 | |
| Sucrose | Roth | 9286.2 | |
| Acrylamide stock: 30% (w/v) acrylamide, 0.8% (w/v) bisacrylamide | Roth | 3029.1 | |
| Tris | Fisher | BP152-5 | |
| Sodium dodecyl sulfate (SDS) | Roth | 1057.1 | |
| Tetramethylethylenediamine (TEMED) | Sigma | T-8133 | |
| Ammonium persulfate (APS) | Roth | 9592.1 | |
| Glycerol | Roth | 3783.1 | |
| Bromophenol blue | USB | US12370 | |
| Glycin | Roth | 3908.3 | |
| Gel staining medium | Clini-sciences | GEN-QC-STAIN | |
| Ethanol | CARLO ERBA | 528151 | |
| NaCl | Euromedex | 1112-A | |
| Triton X-100 | Promega | H5141 | |
| Fat-free milk powder | Régilait | ||
| HCl | Fisher | H/1150/PB15 | |
| KOH pellets | Sigma | 1.05012 | |
| NaOH pellets | CARLO ERBA | 480507 | |
| Anti-HMA1 antibody | Seigneurin-Berny et al, 2006 | Used at a 1:1000 dilution | |
| Anti-KARI antibody | Ferro et al, 2010 | Used at a 1:1000 dilution | |
| Anti-LHCP antibody | Vallon et al, 1991 | Used at a 1:25,000 dilution | |
| P-coumaric acid | Sigma | C-9008 | |
| Luminol (3-aminophalhydrazin) | Fluka | 9253 | |
| Dimethyl sulfoxide (DMSO). | Sigma | D5879 | |
| Large (30 cm × 45 cm) plastic cases | Puteaux | 162135 | |
| A. thaliana seeds | Around 30 mg of seeds for a whole case | ||
| Compost "Floragard" | Puteaux | 16311770 | |
| Growth rooms | 12-h light cycle, set at 23°C (day) / 18°C (night) with a light intensity of 150 μmol/m2/s. | ||
| Muslin or cheesecloth | Raffin | 70116 | 80-cm-large |
| Nylon blutex 50 μm aperture | Tripette et Renaud, Sailly Saillisel | 50 μm aperture | |
| Motor-driven blender, three speeds, 1 gallon (4 L) capacity | Waring Blender | ||
| Fixed-angle rotors JLA-10.500 (6 × 500-mL plastic bottles) | Beckman Coulter | ||
| Beckman JA-20 rotor | Beckman Coulter | ||
| JA-20 (6 × 50 mL polypropylene tubes) | Sorvall instruments | ||
| Swinging-bucket rotor JS-13.1 (6 × 50 mL polycarbonate tubes) | Beckman Coulter | ||
| SW 41 Ti rotor (6 × 13.2 mL ultraclear tubes) | Beckman Coulter | ||
| SW 41 Ti rotor tubes (13.2 mL ultraclear tubes) | Beckman Coulter | ||
| Ultracentrifuge (Beckman L7) | Beckman Coulter | ||
| Centrifuge (Beckman JSE-06D18) | Beckman Coulter | ||
| Microcentrifuge | Eppendorf 5415D or equivalent | ||
| Water pump connected to a Pasteur pipette via a plastic tube. | |||
| Nitrocellulose membranes | BA85, Schleicher and Schuell | ||
| Filter paper | 3MM, Whatman, Maidstone | ||
| Liquid nitrogen | |||
| Peristaltic pump | Gilson | ||
| Gel electrophoresis apparatus with the various accessories needed for protein separation by electrophoresis (combs, plates and casting apparatus). | Bio-Rad Protean 3 or equivalent | ||
| System for protein transfer to nitrocellulose membranes | Bio-Rad Protean 3 or equivalent |
Références
- Zimorski, V., Ku, C., Martin, W. F., Gould, S. B. Endosymbiotic theory for organelle origins. Current Opinion in Microbiology. 22, 38-48 (2014).
- Gould, S. B., Waller, R. F., McFadden, G. I. Plastid evolution. Annual Review of Plant Biology. 59, 491-517 (2008).
- Linka, N., Weber, A. P. Intracellular metabolite transporters in plants. Molecular Plant. 3 (1), 21-53 (2010).
- Block, M. A., Douce, R., Joyard, J., Rolland, N. Chloroplast envelope membranes: a dynamic interface between plastids and the cytosol. Photosynthesis Research. 92 (2), 225-244 (2007).
- Rolland, N., et al. The biosynthetic capacities of the plastids and integration between cytoplasmic and chloroplast processes. Annual Review of Genetics. 46, 233-264 (2012).
- Agrawal, G. K., et al. Plant organelle proteomics: collaborating for optimal cell function. Mass Spectrometry Reviews. 30 (5), 772-853 (2011).
- Chua, N. -. H. [40] Electrophoretic analysis of chloroplast proteins. Methods in Enzymology. 69, 434-446 (1980).
- Seigneurin-Berny, D., Salvi, D., Joyard, J., Rolland, N. Purification of intact chloroplasts from Arabidopsis and spinach leaves by isopycnic centrifugation. Current Protocols in Cell Biology. , (2008).
- Ferro, M., et al. AT_CHLORO, a comprehensive chloroplast proteome database with subplastidial localization and curated information on envelope proteins. Molecular & Cell Proteomics. 9 (6), 1063-1084 (2010).
- Seigneurin-Berny, D., et al. HMA1, a new Cu-ATPase of the chloroplast envelope, is essential for growth under adverse light conditions. Journal of Biological Chemistry. 281 (5), 2882-2892 (2006).
- Vallon, O., et al. Lateral redistribution of cytochrome b6/f complexes along thylakoid membranes upon state transitions. Proceedings of the National Academy of Sciences of the United States of America. 88 (18), 8262-8266 (1991).
- Douce, R. J. J., Edelman, M., Hallick, R. B., Chua, N. -. H. Purification of the chloroplast. Methods in Chloroplast Molecular Biology. , 239-256 (1982).
- Cerovic, Z. G., Plesnicar, M. An improved procedure for the isolation of intact chloroplasts of high photosynthetic capacity. Biochemical Journal. 223 (2), 543-545 (1984).
- Kunst, L. Preparation of physiologically active chloroplasts from Arabidopsis. Methods in Molecular Biology. 82, 43-48 (1998).
- Aronsson, H., Jarvis, P. A simple method for isolating import-competent Arabidopsis chloroplasts. FEBS Letters. 529 (2-3), 215-220 (2002).
- Ling, Q., Jarvis, P. Analysis of Protein Import into Chloroplasts Isolated from Stressed Plants. Journal of Visualized Experiments. (117), (2016).
- Seigneurin-Berny, D., Salvi, D., Dorne, A. J., Joyard, J., Rolland, N. Percoll-purified and photosynthetically active chloroplasts from Arabidopsis thaliana leaves. Plant Physiology and Biochemistry. 46 (11), 951-955 (2008).
- Salvi, D., Rolland, N., Joyard, J., Ferro, M. Purification and proteomic analysis of chloroplasts and their sub-organellar compartments. Methods in Molecular Biology. 432, 19-36 (2008).
- Walker, D. . The use of the oxygen electrode and fluorescence probes in simple measurements of photosynthesis. , (1990).
- Jarvis, P., Lopez-Juez, E. Biogenesis and homeostasis of chloroplasts and other plastids. Nature Reviews Molecular Cell Biology. 14 (12), 787-802 (2013).
- Block, M. A., Dorne, A. J., Joyard, J., Douce, R. Preparation and characterization of membrane fractions enriched in outer and inner envelope membranes from spinach chloroplasts. II. Biochemical characterization. Journal of Biological Chemistry. 258 (21), 13281-13286 (1983).
- Soll, J. Phosphoproteins and protein-kinase activity in isolated envelopes of pea (Pisum sativum L.) chloroplasts. Planta. 166 (3), 394-400 (1985).
- Moyet, L., Salvi, D., Tomizioli, M., Seigneurin-Berny, D., Rolland, N. Preparation of Membrane Fractions (Envelope, Thylakoids, Grana, and Stroma Lamellae) from Arabidopsis Chloroplasts for Quantitative Proteomic Investigations and Other Studies. Methods in Molecular Biology. 1696, 117-136 (2018).
- Tomizioli, M., et al. Deciphering thylakoid sub-compartments using a mass spectrometry-based approach. Molecular & Cellular Proteomics. 13 (8), 2147-2167 (2014).
- Spicher, L., Kessler, F. Unexpected roles of plastoglobules (plastid lipid droplets) in vitamin K1 and E metabolism. Current Opinion in Plant Biology. 25, 123-129 (2015).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon