Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Thyroïdectomie endoscopique transbuccale Approche vestibulaire pour la lobectomie thyroïdienne
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Nous présentons ici un protocole pour décrire en détail la méthodologie de l’approche vestibulaire de thyroïdectomie endoscopique transbuccale.
Résumé
Le manuscrit décrit l’approche vestibulaire de thyroïdectomie endoscopique transorale (TOETVA) pour la lobectomie thyroïdienne. Le patient est placé en décubitus dorsal avec extension et fixation du cou. Une incision transversale de 20 mm et deux incisions de 5 mm sont pratiquées à travers la muqueuse du vestibule buccal pour le placement de la caméra et de l’instrument après désinfection de la peau et de la cavité buccale. L’espace de travail est établi et maintenu par le dispositif de suspension cutanée, qui est fait de ficelle non résorbable (3-0) et d’élastiques, et la pression d’insufflation CO2 . La lobectomie utilisant une technique médiale-latérale et un curage cervical central ipsilatéral prophylactique sont effectués simultanément sur des patients atteints d’un cancer papillaire de la thyroïde (PTC). L’échantillon est extrait à travers l’incision de 20 mm. La glande parathyroïde est immédiatement recherchée dans l’échantillon et auto-transplantée sur le brachioradialis gauche. Un tube de drainage est inséré à travers le trou de l’enrouleur dans le lit de la glande thyroïde, et des sutures résorbables sont utilisées pour fermer les incisions muqueuses dans le vestibule buccal et la linea alba cervicalis. Les prophylactiques administrés par voie intraveineuse sont recommandés pendant les 24 premières heures après la chirurgie et les antibiotiques oraux sont utilisés pendant 7 jours après l’opération.
Introduction
La thyroïdectomie ouverte conventionnelle est pratiquée en toute sécurité à l’aide d’une incision cervicale depuis plus de 100 ans1. Bien que la plupart des patients aient une cicatrisation efficace et que l’effet cosmétique soit généralement acceptable, une cicatrice permanente sur le cou attire toujours immédiatement l’attention des observateurs communs2. Près de 20% des patients post-thyroïdectomie éprouvent une conscience de soi et plus de 10% envisagent d’autres traitements pour enlever la cicatrice3. De plus, un impact négatif de l’incision cervicale sur la qualité de vie liée à la santé (QVLS) a également été signalé4. Diverses approches d’accès à distance pour la chirurgie de la thyroïde, telles que les approches axillo-mammaire, transaxillaire, rétroauriculaire et sous-clavière, ont été développées pour éviter une cicatrice visibledu cou 5,6,7,8 en déplaçant l’incision cutanée vers des endroits moins visibles. 9 Cependant, ces approches nécessitent une dissection à large lambeau pour accéder à la glande thyroïde tout en laissant des cicatrices cutanées aux sites d’incision10.
Depuis 2008, des techniques de chirurgie endoscopique transluminale à orifice naturel pour la chirurgie transbuccale de la thyroïde ont été développées. Celles-ci peuvent être réalisées via l’approche vestibulaire orale ou l’approche sublinguale. Le premier est plus populaire car il est associé à moins de complications. En 2016, Anuwong a publié la première série de cas de 60 patients subissant l’approche vestibulaire de thyroïdectomie endoscopique transorale (TOETVA) et a identifié un excellent pronostic11. En comparaison avec les méthodes d’accès à distance, TOETVA est considéré comme vraiment peu invasif parce que la zone du curage du lambeau est similaire à la thyroïdectomie ouverte conventionnelle, et il ne laisse aucune cicatrice sur le corps10.
TOETVA, une méthode endoscopique révolutionnaire, répond aux besoins cosmétiques des femmes et permet un accès facile à la thyroïde bilatérale et au compartiment central12. Il se distingue par l’exposition complète et le curage des ganglions lymphatiques centraux, ce qui est bénéfique dans le traitement différencié du cancer de la thyroïde avec cN1a10,13,14,15. Cependant, en raison de l’espace opératoire limité, le traitement des grosses tumeurs dans le pôle supérieur de la glande thyroïde est relativement difficile. La présente étude décrit les procédures étape par étape de TOETVA.
Protocole
L’étude a été approuvée par le comité d’éthique médicale de l’hôpital de Chine occidentale de l’Université du Sichuan (2018[457]), et le consentement éclairé écrit a été obtenu de tous les sujets.
1. Préparation préopératoire
- Admissibilité des patients
- Sélectionner des patients qui ont des exigences esthétiques strictes et qui répondent aux critères suivants: (1) un nodule bénin de <4 cm de diamètre; (2) un carcinome thyroïdien différencié (DTC) de <2 cm de diamètre sans métastases cliniques des ganglions lymphatiques latéraux ou à distance; et (3) aucune indication d’imagerie de métastases ganglionnaires centraux ou d’un ganglion lymphatique métastatique de <2 cm de diamètre sans fusion ni fixation.
- Exclure les patients qui répondent aux critères suivants : (1) carcinome médullaire ou carcinome thyroïdien indifférencié ; (2) infections buccales ou cervicales; (3) thyroïdite sévère qui a un impact aigu sur la fonction thyroïdienne; (4) invasion suspecte de la tumeur primaire ou du ganglion lymphatique métastatique vers les organes adjacents, tels que l’œsophage, la trachée ou le nerf laryngé récurrent (RLN); (5) localisation de la tumeur primaire dans le pôle supérieur; (6) antécédents de chirurgie cervicale, d’ablation ou de radiothérapie cervicale; (7) preuve biochimique d’hyperthyroïdie non contrôlée; 8° goitre substernal; et (9) intolérance à la chirurgie.
- Préparation du patient
- Évaluer les patients en préopératoire avec des tests cytologiques par aspiration à l’aiguille fine, des tests de la glande parathyroïde, des tests de la fonction thyroïdienne, une laryngoscopie et une échographie thyroïdienne16.
- Demandez au patient de préparer la cavité buccale en utilisant un rince-bouche (comme le tinidazole) avant et après les repas au moins 2 jours avant le TOETVA et en gardant le rince-bouche dans la bouche pendant au moins 15 s à chaque fois.
- Équipement
- Assurer la disponibilité des sutures résorbables (5-0) pour les plaies buccales.
- Assurer la disponibilité de tous les instruments et matériaux requis pour le protocole (voir le tableau des matériaux).
2. Préparation chirurgicale
- Préparation préopératoire
- Évaluer le risque d’anesthésie de la chirurgie selon la classification17 de l’American Society of Anesthesiologists.
- Induire une anesthésie générale avec intubation orotrachéale par neuromonitoring peropératoire (IONM).
- Scotchez les yeux et le nez et tamponnez la tête pour éviter tout traumatisme par inadvertance.
- Effectuer un cathétérisme.
- Champ d’opération
REMARQUE : La figure 1 montre le schéma de la disposition de la salle d’opération.- Laissez l’opérateur se tenir devant la tête du patient. Laissez le premier assistant se tenir sur le côté gauche de la tête du patient.
REMARQUE : Le premier assistant sera responsable de tenir l’endoscope. - Laissez le deuxième assistant se tenir à côté du corps du patient en fonction de l’emplacement de la lésion pour tenir le crochet. Laissez l’infirmière de gommage se tenir à côté de la jambe du patient.
- Placez l’équipement endoscopique et surveillez au-delà des pieds du patient.
- Placez le patient en décubitus dorsal avec le cou tendu. Fixez la tête du patient avec le brassard supérieur pendant l’opération pour éviter la rotation du cou.
- Laissez l’opérateur se tenir devant la tête du patient. Laissez le premier assistant se tenir sur le côté gauche de la tête du patient.
- Désinfection
- Désinfection de la peau: Préparez le haut de la poitrine, le cou et le bas du visage avec une solution d’iode trois fois selon le principe du top-down et in-out.
- Désinfection orale: Mettez la gaze d’iode diluée dans la bouche, désinfectez la cavité buccale avec elle trois fois et rincez-la avec une solution saline normale.

Figure 1 : Schéma de la disposition de la salle d’opération. Veuillez cliquer ici pour voir une version agrandie de cette figure.
3. Conception des incisions et établissement de l’espace de travail (Figure 2)
- Faites l’incision du port de la caméra avec un électrotome; Il devrait s’agir d’une incision transversale de 20 mm à 5 mm au-dessus du frein à travers la muqueuse alvéolaire du vestibule central de la lèvre inférieure.
- Avancez l’incision du port de la caméra jusqu’au menton avec un électrotome. Prenez soin d’éviter la pénétration de la peau mentum. Utilisez des pinces hémostatiques et une tige de décapage sous-cutanée pour créer un tunnel dans la ligne médiane du cou et s’étendre davantage au bas du cou.
- Placez une caméra 10 mm dans le port central. Insuffler l’espace de travail avec du dioxyde de carbone gazeux pour établir une pression de 4 mmHg.
REMARQUE: La pression du dioxyde de carbone gazeux doit être de <8 mmHg pour éviter les complications causées par une pression élevée. - Faites deux incisions verticales latérales de 5 mm à partir des premières prémolaires pour le placement des instruments.
- Utilisez un scalpel à ultrasons pour créer l’espace de travail et élargissez-le aux deux muscles sternocléidomastoïdiens latéralement et le long du plan sous-platysmal jusqu’à l’encoche sternale inférieurement. Utilisez la traction du dispositif de suspension cutanée, qui est constitué de sutures non résorbables (3-0) et d’élastiques, pour aider à élargir l’espace de travail (Figure 3).
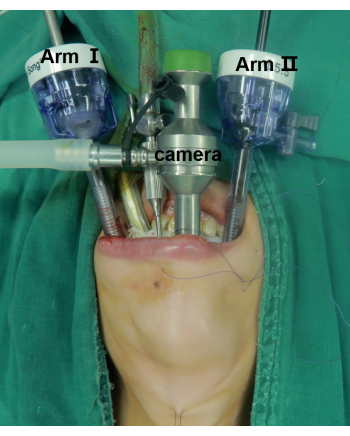
Figure 2 : Positionnement du patient et des orifices laparoscopiques. Celui du centre est le port de la caméra. Le bras I et le bras II sont destinés au placement des instruments. Veuillez cliquer ici pour voir une version agrandie de cette figure.
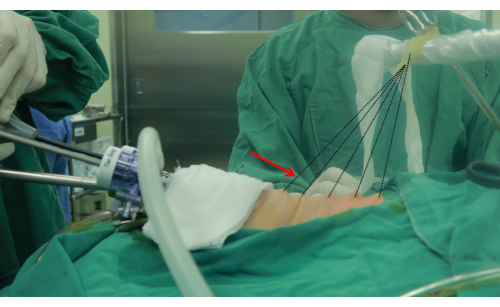
Figure 3 : Le dispositif de suspension de traction. La flèche pointe vers le dispositif de suspension de traction. Le dispositif de suspension est fait de ficelle non résorbable (3-0) et d’élastiques. Veuillez cliquer ici pour voir une version agrandie de cette figure.
4. Lobectomie thyroïdienne
- Diviser la linea alba coli avec un scalpel à ultrasons. Séparez une partie du muscle de la sangle de la glande thyroïde.
- Utilisez une aiguille de 20 ml pour percer la peau au niveau du coin inférieur du cartilage thyroïdien et placez un crochet de traction à travers le trou. Utilisez le crochet de traction pour saisir la partie séparée du muscle de la sangle.
- Utilisez le scalpel à ultrasons pour séparer la partie restante du muscle de la sangle et exposer l’artère carotide commune. Trouvez le nerf vague et utilisez l’IONM pour enregistrer le signal.
REMARQUE: La technologie IONM aide à localiser, identifier et protéger rapidement le nerf laryngé récurrent (RLN) et la branche externe du nerf laryngé supérieur (EBSLN). L’utilisation de l’IONM est encouragée; C’est un excellent outil auxiliaire, mais pas obligatoire. - Utilisez des pinces non traumatiques pour maintenir la marge inférieure de l’isthme. Utilisez le scalpel à ultrasons pour couper l’isthme de la partie inférieure du cartilage cricoïde et exposer la trachée. Pour la lobectomie de la TOETVA, localisez d’abord la trachée et prenez-la comme signe.
- Utilisez les pinces non traumatiques pour maintenir le pôle supérieur de la thyroïde et divisez l’espace cricothyroïdien avec le scalpel à ultrasons. Transect partie du muscle sternothyroïdien. Exposez le pôle supérieur de la thyroïde.
- Sectionner l’artère thyroïdienne supérieure et la veine. Libérez les glandes latérales du haut vers le bas. Soulevez le pôle supérieur de la glande, trouvez le RLN sous visualisation directe et utilisez l’IONM pour enregistrer le signal.
- Utilisez le scalpel à ultrasons pour séparer la capsule thyroïdienne de la trachée. Divisez les vaisseaux thyroïdiens inférieurs et coupez le ligament de la baie avec le scalpel à ultrasons.
- Retirez le lobe unilatéral de la glande thyroïde de la trachée. Utilisez l’IONM pour enregistrer à nouveau le signal du nerf vague et RLN.
5. Curage ganglionnaire central
- Localisez d’abord la glande parathyroïde inférieure et essayez de la retenir in situ.
REMARQUE: Le thymus doit être soigneusement identifié et protégé pour assurer la fonctionnalité de la glande parathyroïde inférieure de la source de l’apport sanguin du thymus et pour prévenir la résection accidentelle de la glande parathyroïde. Les nanoparticules de carbone peuvent être choisies pour faciliter l’identification des glandes parathyroïdes et le curage des ganglions lymphatiques. L’autotransplantation est possible pour les glandes parathyroïdes qui ne peuvent pas être retenues in situ. - Étirez les muscles de la sangle vers l’extérieur autant que possible pour exposer complètement le champ opératoire.
- Identifier le compartiment ganglionnaire central par l’os hyoïde (supérieur), la fosse suprasternale (inférieure), l’artère carotide (latérale), la couche superficielle du fascia cervical profond (antérieur) et l’œsophage (postérieur).
- Utilisez le scalpel à ultrasons pour disséquer les ganglions lymphatiques prétrachéaux et prélaryngés. Couper le tissu conjonctif devant l’artère carotide pour déterminer la limite latérale des ganglions lymphatiques centraux et le tissu conjonctif devant la trachée pour déterminer la limite médiale des ganglions lymphatiques centraux. Balayez la face antérieure du RLN gauche ou les faces antérieure et postérieure du RLN droit pour compléter le curage ganglionnaire central.
REMARQUE: La marge latérale ne doit pas être balayée trop profondément afin d’éviter d’endommager le nerf vague et le tronc sympathique. Lors du nettoyage de la marge inférieure, les blessures aux vaisseaux innominés et à la plèvre doivent être évitées.
6. Retrait de l’échantillon et fermeture
- Utilisez des poches endoscopiques pour retirer les échantillons.
REMARQUE: Pour éviter l’implantation extra-utérine, les échantillons doivent être complètement enlevés par les poches endoscopiques. - Lavez la plaie chirurgicale à plusieurs reprises avec une grande quantité d’eau distillée stérile tiède.
- Placez un drain chirurgical (4 #) à travers une petite ponction cutanée dans le cou antérieur.
- Re-approximez les muscles de la sangle. Fermez les plaies buccales avec des sutures résorbables 5-0.
7. Autotransplantation de la glande parathyroïde
- Conservez les glandes parathyroïdes avec une solution saline normale et examinez-les par biopsie de la section congelée.
- Couper la glande parathyroïde isolée en minuscules fragments de 1 mm x 1 mm x 1 mm avec des ciseaux ophtalmiques. Mélanger les fragments avec une solution saline normale. Injectez le mélange dans le muscle brachioradial de l’avant-bras.
Résultats
Nous avons mis en place un parcours clinique de routine pour les patients atteints de TOETVA au centre. Une laryngoscopie et une échographie thyroïdienne sont effectuées sur chaque patient avant l’opération. L’hormone parathyroïdienne (PTH), la fonction thyroïdienne, la 25-dihydroxyvitamine D (25-OH-VD) et le calcium sérique sont systématiquement mesurés avant l’opération, et tous, à l’exception de la fonction thyroïdienne, sont remesurés 1 jour après la chirurgie. Dans notre hôpital, les cathéter...
Discussion
TOETVA est caractérisé par l’exposition complète et le curage des ganglions lymphatiques centraux, ce qui est significativement avantageux dans le traitement du carcinome différencié de la thyroïde avec cN1a10,13,14,15. Cependant, il convient de noter qu’en raison de l’espace opératoire limité, il est relativement difficile de traiter les grosses tumeurs situées dans le pôle sup...
Déclarations de divulgation
Les auteurs ne déclarent aucun intérêt concurrent.
Remerciements
Nous remercions tous les patients qui ont participé à cette étude pour leur coopération. Cette recherche a été soutenue par le fonds de projet du Département de la science et de la technologie de la province du Sichuan. (Subvention n° 2021YFS0103).
matériels
| Name | Company | Catalog Number | Comments |
| Allis Grasping Forceps,310 mm x 5 mm | AESCULAP | PO111R | |
| Button Electrode Tip | AESCULAP | GK385R | |
| Ceramic Electrode | AESCULAP | GK384R | |
| Complete Trocar | AESCULAP | EJ751R | |
| Endoscope | Olympus | WA53005A | |
| IONM | Medtronic | NIM-3.0 | |
| Light Transmitting Bundle | Olympus | WA03310A | |
| Maryland Dissecting Forceps, 310 mm x 5 mm | AESCULAP | PO102R | |
| Monopolar Handle (5 mm diameter, 33 cm working length) | AESCULAP | GK372R | |
| Pneumoperitoneum tube,4 m | STRYKE | 620-240-223 | |
| Pyramidal Tip Obturator | AESCULAP | EJ755R | |
| Reusable Monopolar Cable | AESCULAP | GK245 | |
| Scissors | AESCULAP | P0004R | |
| Suction irrigation tube | AESCULAP | PG027R | |
| Super Righting Needle Holder, 5 mm | AESCULAP | PL414R | |
| Veress | TianSong | E2014.6 |
Références
- Latifi, R., et al. Outcomes of 1,327 patients operated on through twelve multispecialty surgical volunteerism missions: A retrospective cohort study. International Journal of Surgery. 60, 15-21 (2018).
- Liao, D., et al. Transoral neck surgery prevents attentional bias towards the neck compared to open neck surgery. Laryngoscope. 130 (6), 1603-1608 (2020).
- Best, A. R., Shipchandler, T. Z., Cordes, S. R. Midcervical scar satisfaction in thyroidectomy patients. Laryngoscope. 127 (5), 1247-1252 (2017).
- Choi, Y., et al. Impact of postthyroidectomy scar on the quality of life of thyroid cancer patients. Annals of Dermatology. 26 (6), 693-699 (2014).
- Kang, S. W., et al. Robotic thyroid surgery using a gasless, transaxillary approach and the da Vinci S system: The operative outcomes of 338 consecutive patients. Surgery. 146 (6), 1048-1055 (2009).
- Choe, J. H., et al. Endoscopic thyroidectomy using a new bilateral axillo-breast approach. World Journal of Surgery. 31 (3), 601-606 (2007).
- Inukai, M., Usui, Y. Clinical evaluation of gasless endoscopic thyroid surgery. Surgery Today. 35 (3), 199-204 (2005).
- Terris, D. J., Singer, M. C., Seybt, M. W. Robotic facelift thyroidectomy: II. Clinical feasibility and safety. Laryngoscope. 121 (8), 1636-1641 (2011).
- Russell, J. O., et al. Transoral thyroid and parathyroid surgery via the vestibular approach-a 2020 update. Gland Surgery. 9 (2), 409-416 (2020).
- Chai, Y. J., et al. Transoral endoscopic thyroidectomy for papillary thyroid microcarcinoma: Initial experience of a single surgeon. Annals of Surgical Treatment and Research. 93 (2), 70-75 (2017).
- Anuwong, A. Transoral endoscopic thyroidectomy vestibular approach: A series of the first 60 human cases. World Journal of Surgery. 40 (3), 491-497 (2016).
- Arora, A., et al. The perception of scar cosmesis following thyroid and parathyroid surgery: A prospective cohort study. International Journal of Surgery. 25, 38-43 (2016).
- Dionigi, G., Chai, Y. J., Tufano, R. P., Anuwong, A., Kim, H. Y. Transoral endoscopic thyroidectomy via a vestibular approach: Why and how. Endocrine. 59 (2), 275-279 (2018).
- Wang, Y., et al. Implementation of intraoperative neuromonitoring for transoral endoscopic thyroid surgery: A preliminary report. Journal of Laparoendoscopic and Advanced Surgical Techniques. Part A. 26 (12), 965-971 (2016).
- Wu, G. Y., et al. Endoscopic central lymph node dissection via breast combined with oral approach for papillary thyroid carcinoma: A preliminary study. World Journal of Surgery. 41 (9), 2280-2282 (2017).
- Yang, J., et al. Complete endoscopic thyroidectomy via oral vestibular approach versus areola approach for treatment of thyroid diseases. Journal of Laparoendoscopic and Advanced Surgical Techniques. Part A. 25 (6), 470-476 (2015).
- Su, A., et al. Does the number of parathyroid glands autotransplanted affect the incidence of hypoparathyroidism and recovery of parathyroid function. Surgery. 164 (1), 124-129 (2018).
- Doyle, D. J., Hendrix, J. M., Garmon, E. H. American Society of Anesthesiologists Classification. StatPearls. , (2022).
- Park, J. O., Kim, M. R., Kim, D. H., Lee, D. K. Transoral endoscopic thyroidectomy via the trivestibular route. Annals of Surgical Treatment and Research. 91 (5), 269-272 (2016).
- Dionigi, G., et al. Transoral endoscopic thyroidectomy: Preliminary experience in Italy. Updates in Surgery. 69 (2), 225-234 (2017).
- Udelsman, R., et al. Trans-oral vestibular endocrine surgery: A new technique in the United States. Annals of Surgery. 264 (6), 13-16 (2016).
- Choe, J. -. H., et al. Endoscopic thyroidectomy using a new bilateral axillo-breast approach. World Journal of Surgery. 31 (3), 601-606 (2007).
- Son, S. K., Kim, J. H., Bae, J. S., Lee, S. H. Surgical safety and oncologic effectiveness in robotic versus conventional open thyroidectomy in thyroid cancer: A systematic review and meta-analysis. Annals of Surgical Oncology. 22 (9), 3022-3032 (2015).
- Lee, K. E., et al. Robotic thyroidectomy by bilateral axillo-breast approach: Review of 1,026 cases and surgical completeness. Surgical Endoscopy. 27 (8), 2955-2962 (2013).
- Kim, M. J., et al. Yonsei experience of 5000 gasless transaxillary robotic thyroidectomies. World Journal of Surgery. 42 (2), 393-401 (2018).
- Jitpratoom, P., Ketwong, K., Sasanakietkul, T., Anuwong, A. Transoral endoscopic thyroidectomy vestibular approach (TOETVA) for Graves' disease: A comparison of surgical results with open thyroidectomy. Gland Surgery. 5 (6), 546-552 (2016).
- Yi, J. W., et al. Transoral endoscopic surgery for papillary thyroid carcinoma: Initial experiences of a single surgeon in South Korea. Annals of Surgical Treatment and Research. 95 (2), 73-79 (2018).
- Wang, D., et al. Transoral thyroidectomy vestibular approach versus non-transoral endoscopic thyroidectomy: A comprehensive systematic review and meta-analysis. Surgical Endoscopy. 36 (3), 1739-1749 (2022).
- Wang, T., et al. Safety of central compartment neck dissection for transoral endoscopic thyroid surgery in papillary thyroid carcinoma. Japanese journal of clinical oncology. 50 (4), 387-391 (2020).
- Sun, H., et al. Comparison of transoral endoscopic thyroidectomy vestibular approach, total endoscopic thyroidectomy via areola approach, and conventional open thyroidectomy: A retrospective analysis of safety, trauma, and feasibility of central neck dissection in the treatment of papillary thyroid carcinoma. Surgical Endoscopy. 34 (1), 268-274 (2020).
- Tanaka, K. Comparative study on bacterial flora of oral cavity and upper pharynx in healthy elderly. The Japanese Journal of Antibiotics. 54, 19-21 (2001).
- Guo, F., Wang, W., Zhu, X., Xiang, C., Wang, Y. Comparative study between endoscopic thyroid surgery via the oral vestibular approach and the areola approach. Journal of Laparoendoscopic and Advanced Surgical Techniques. 30 (2), 170-174 (2019).
- Chae, S., Min, S. Y., Park, W. S. Comparison study of robotic thyroidectomies through a bilateral axillo-breast approach and a transoral approach. Journal of Laparoendoscopic and Advanced Surgical Techniques. 30 (2), 175-182 (2020).
- Kim, W. W., et al. A comparison study of the transoral and bilateral axillo-breast approaches in robotic thyroidectomy. Journal of Surgical Oncology. 118 (3), 381-387 (2018).
- Nguyen, H. X., Long, T. N., Nguyen, H. V., Nguyen, H. X., Le, Q. V. Comparison of transoral thyroidectomy vestibular approach and unilateral axillobreast approach for endoscopic thyroidectomy: A prospective cohort study. Journal of Laparoendoscopic and Advanced Surgical Techniques. 31 (1), 11-17 (2020).
- Bhattacharyya, N. Surgical treatment of cervical nodal metastases in patients with papillary thyroid carcinoma. Archives of Otolaryngology - Head and Neck Surgery. 129 (10), 1101-1104 (2003).
- Lundgren, C. I., Hall, P., Dickman, P. W., Zedenius, J. Clinically significant prognostic factors for differentiated thyroid carcinoma: A population-based, nested case-control study. Cancer. 106 (3), 524-531 (2006).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon