Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Method Article
Approche chirurgicale et complications de la fusion intersomatique trans-psoas latérale autonome
Dans cet article
Résumé
La fusion intersomatique de la colonne lombaire peut être réalisée chirurgicalement à l’aide de différentes techniques. Des techniques peu invasives, y compris la fusion intersomatique latérale, ont été développées au cours des dernières décennies pour réduire les taux de complications et permettre un rétablissement plus rapide des patients. Nous donnons un aperçu de la fusion intersomatique trans-psoas latérale autonome, en mettant en évidence les complications et les pièges potentiels.
Résumé
La fusion intersomatique de la colonne lombaire est une procédure standard pour la maladie dégénérative symptomatique de la colonne lombaire en cas d’échec du traitement conservateur. La décompression chirurgicale et la fusion du segment peuvent être réalisées à l’aide de plusieurs techniques différentes. Au cours des dernières décennies, des techniques mini-invasives, telles que la fusion intersomatique latérale (LLIF), ont été développées pour réduire les lésions tissulaires et les complications et permettre un rétablissement plus rapide des patients. Avec la popularité croissante, les indications de la LLIF se sont élargies pour traiter les déformations de la colonne vertébrale et la sténose foraminale/centrale. Mécaniquement, il permet une fixation inégalée grâce au placement de l’anneau apophysaire de gauche à droite de la cage. Le LLIF utilise un couloir rétropéritonéal peu perturbateur et comprend à la fois des approches trans-psoas et pré-psoas. Pour l’approche pré-psoas, le risque de lésions dues à la manipulation du plexus lombaire intramusculaire est réduit par rapport à une approche trans-psoas. Cependant, des risques accrus de lésions vasculaires, urétérales, intestinales majeures et de lésions du plexus sympathique sont signalés.
Cet article vise à fournir un guide détaillé et complet sur la fusion intersoaque trans-psoas latérale autonome, y compris ses indications, son intervention chirurgicale, ses complications potentielles et ses résultats, sur la base d’une décennie d’expérience dans un seul centre.
Introduction
La lombalgie, symptôme important de la maladie lombaire dégénérative (TDL), est fréquente chez les patients de plus de 65 ans1. Les autres symptômes du TDL comprennent la radiculopathie et la claudication. En cas d’échec du traitement non chirurgical, la décompression chirurgicale ou, si indiquée, la fusion intersomatique de la colonne vertébrale peuvent être une option de traitement viable2. Plusieurs techniques et approches ont été développées pour réaliser la fusion intersomatique ou la décompression du segment. Les approches traditionnelles comprennent la fusion intersomatique lombaire postérieure (PLIF), la fusion intersomatique lombaire transforaminale (TLIF) et la fusion intersomatique lombaire antérieure (ALIF). Les approches de la colonne lombaire sont illustrées à la figure 1.
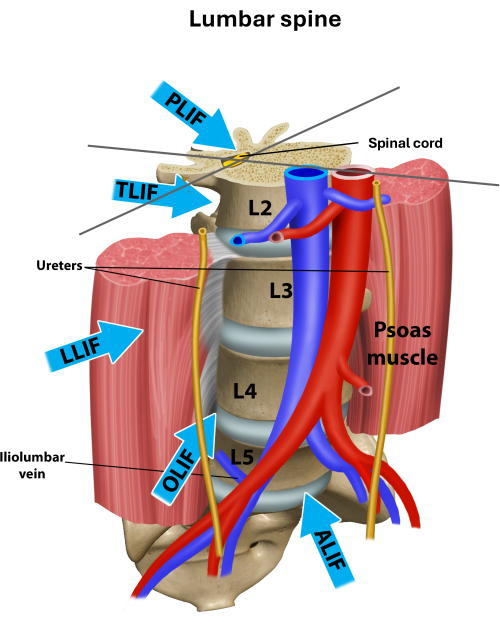
Figure 1 : Différentes approches de la colonne lombaire pour la fusion intersomatique12. Aperçu des différentes approches utilisées pour la fusion intersomatique lombaire. Le LLIF est une approche trans-psoas, et OLIF est une approche pré-psoas. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Au cours des dernières décennies, des techniques mini-invasives de fusion intersomatique de la colonne lombaire ont été développées pour réduire les lésions tissulaires et les complications, permettant un rétablissement plus rapide du patient, réduisant les complications et dépassant les limites techniques des approches traditionnelles de la colonne vertébrale. En 2001, Pimenta et al. ont introduit une approche rétropéritonéale peu invasive de la colonne lombaire en divisant le psoas, ce qui permet une exposition directe au disque en élargissant l’espace rétropéritonéal. Cela a été introduit lors de l’approche du trans-psoas latéral 3,4. Cette technique a été modifiée à l’aide d’écarteurs spéciaux et popularisée par Ozgur et al.5. Ces dernières années, une fusion intersomatique latérale extrême en position couchée a été développée. Cette technique offre une efficacité avec des procédures postérieures combinées et une lordose lombaire améliorée 6,7.
La fusion intersomatique latérale (LLIF) peut être réalisée en utilisant diverses approches. Il s’agit notamment d’approches trans-psoas (fusion intersomatique latérale extrême (XLIF8), fusion intersomatique latérale directe (DLIF9) à l’aide de différents instruments) et d’une approche pré-psoas (fusion intersomatique latérale oblique (OLIF10). L’approche utilisée pour l’intervention dépend, entre autres, du patient et de la formation du chirurgien. Les études anatomiques ont montré des avantages notables pour les approches trans-psoas (perte de sang minimale, préservation de la musculature postérieure et de la chaîne ligamentaire, capacité à effectuer une discectomie étendue et la mise en place d’une grande greffe intervertébrale) mais aussi des inconvénients (paralysie nerveuse postopératoire, lésions abdominales viscérales)11. Les complications majeures mais rares signalées comprennent une perforation intestinale, une lésion commune de la veine iliaque, un affaissement de la cage, des fractures du corps vertébral autour du dispositif intersomatique, un hématome rétropéritonéal et un pneumorétropéritoine associé à un pneumoscrotum12. Dans l’ensemble, les approches pré-psoas sont associées à un taux de complications légèrement plus faible et à moins de déficits neurologiques postopératoires13. Pour permettre un résultat optimal, l’indication d’une fusion intersomatique latérale doit être faite avec soin. Nous vous conseillons d’obtenir une tomodensitométrie (TDM) et une résonance magnétique (IRM) de la colonne lombaire. Pour évaluer l’hypermobilité ou l’instabilité du segment, obtenez des images radiographiques de flexion-extension en plus de l’antéropostérieure (AP) et latérale régulières. Les indications courantes sont les patients présentant une instabilité segmentaire et une radiculopathie concomitante qui ont échoué au traitement non chirurgical. Dans le cas d’une chirurgie d’instabilité segmentaire ou de déformation, une fixation interne supplémentaire peut être nécessaire. La LLIF peut être limitée dans la partie inférieure de la colonne lombaire, en fonction de la hauteur de la crête iliaque. Une fixation postérieure supplémentaire peut ajouter une rigidité de construction précieuse et une réduction des déformations pour les patients présentant une instabilité de haut grade, une déformation ou une stabilité osseuse douteuse. Les contre-indications à cette procédure sont généralement une tumeur maligne, des déformations de haut grade ou des anomalies de bifurcation. Des antécédents d’infection ou de maladie rétropéritonéale et une chirurgie ou une blessure rétropéritonéale antérieure sont des considérations importantes. Les facteurs de risque de mauvais résultats comprennent l’ostéoporose, le tabagisme, l’utilisation à long terme de stéroïdes, les malformations graves et l’hypermobilité segmentaire due à un épanchement facettaire ou à une laminectomie antérieure 14,15,16. De plus, les patients ayant un indice de masse corporelle très faible et une localisation antérieure du psoas sont des patients potentiellement indésirables pour une complexité d’accès accrue. En chirurgie de révision, une approche pré-psoas peut être favorable pour éviter le tissu cicatriciel.
L’objectif de cet article est de fournir des conseils étape par étape aux chirurgiens sur une fusion intersoasque trans-psoas latérale autonome, y compris les pièges et les taux de complications après 10 ans d’expérience monocentrique.
Protocole
L’étude rétrospective a été approuvée par notre comité d’examen institutionnel (STUDY2021000113), et une dérogation au consentement éclairé a été accordée en raison de la nature de l’étude. La procédure démontrée dans la vidéo a été réalisée sur un échantillon humain qui a été obtenu et utilisé conformément aux directives et protocoles éthiques établis par notre institution. L’échantillon a été manipulé avec respect et conformément à toutes les normes éthiques pertinentes.
1. Sélection des patients
- Sélectionner des patients atteints d’une maladie lombaire dégénérative et ayant échoué à un traitement non chirurgical.
- Évaluez l’hypermobilité ou l’instabilité du segment à l’aide d’images radiographiques de flexion-extension en plus des vues antéropostérieures et latérales normales (Figure 2). En cas d’instabilité segmentaire, effectuez une fixation postérieure supplémentaire.
- Obtenez une tomodensitométrie (TDM) et une résonance magnétique (IRM) de la colonne lombaire.
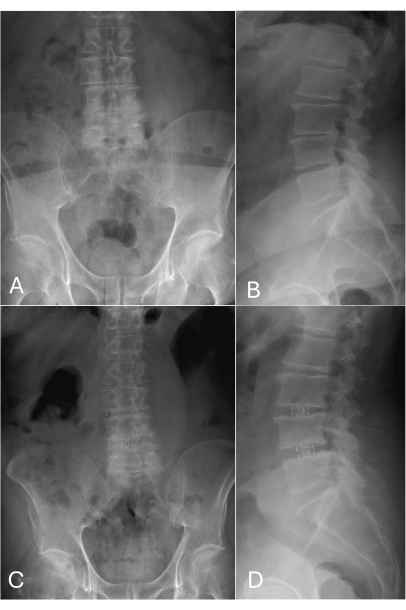
Figure 2 : Images radiographiques préopératoires et de suivi en A.P et en vue latérale. (A-B) Maladie dégénérative de la colonne lombaire à plusieurs niveaux avec affaissement de l’espace discal L3/4 ainsi que L4/5 et sténose neuroforaminale. Aucun signe d’instabilité ou d’hyperflexibilité n’a été observé. (C-D) Suivi postopératoire d’un an. Position correcte des cages en PEEK dans l’espace des disques L3/4 et L4/5 sans affaissement. La hauteur discale et neuroforaminale est restaurée. Veuillez cliquer ici pour voir une version agrandie de cette figure.
2. Positionnement
- Positionnez le patient, sous anesthésie générale, en position de décubitus du côté droit, avec les hanches et les genoux partiellement fléchis sur une table d’opération radiotransparente. Tamponnez les proéminences osseuses pour éviter d’endommager les tissus mous en raison de la pression.
- Sécurisez le patient avec du ruban chirurgical et des ceintures/coussinets pour empêcher tout mouvement et assurer la sécurité.
- Pliez la table d’opération pour générer plus d’espace si nécessaire.
3. Phase préopératoire
- Confirmez le niveau chirurgical souhaité avec des images de fluoroscopie AP/latérale.
- Utilisez des marqueurs cutanés pour visualiser l’espace discal et les corps vertébraux du niveau souhaité à la surface de la peau (Figure 3).
- Placez des électrodes d’électromyographie (EMG) sur les muscles de référence des nerfs qui pourraient être à risque pendant la chirurgie17.
4. Approche
- Après avoir désinfecté la peau et recouvert la zone avec le champ chirurgical, conformément aux normes institutionnelles, faites une incision cutanée de 3 à 5 cm de long à l’aide d’un scalpel stérile sur l’espace discal dans une chirurgie à un seul niveau.
- Utilisez l’électrocautérisation pour disséquer le fascia abdominal.
- Ouvrez le fascia et utilisez des pinces/écarteurs pour séparer brutalement les trois couches des obliques jusqu’à ce que l’espace rétropéritonéal soit atteint.
- Identifiez le psoas et fendez-le dans le sens longitudinal (par exemple, à l’aide d’enrouleurs).
5. Neuromonitoring
- Soyez à l’affût de toute modification des potentiels évoqués somatosensoriels (SSEP), des potentiels évoqués moteurs (MEP) et de l’électromyographie spontanée (EMG) lors de l’approche et de la dissection du psoas17.
- À l’aide d’une sonde EMG portable, identifiez la racine nerveuse sortante au niveau souhaité.
6. Enrouleurs
- Après avoir confirmé par fluoroscopie le niveau souhaité, placez un système d’enrouleur auto-retenant (Figure 4).
7. Préparation de l’espace intradiscale
- À l’aide d’un scalpel, effectuez une annulotomie et réséquez tout le matériel discale à l’aide d’un rongeur.
REMARQUE : Dans la dégénérescence sévère, l’espace discale peut être obscurci par des ostéophytes. Ceux-ci peuvent nécessiter une résection avant l’évacuation de l’espace discal. - Placez un écarteur pour ouvrir l’espace intervertébral effondré.
REMARQUE : En cas de dégénérescence sévère, seule une restauration partielle de l’espace intervertébral peut être possible. - Retirez avec précaution le matériau du disque et le cartilage des deux plaques d’extrémité à l’aide de curettes ou d’élévateurs Cobb (figure 4).
8. Placement de la cage de traînée
- Utilisez différents composants d’essai pour rétablir une hauteur normale du disque et pour soulager toute pression sur les racines nerveuses.
REMARQUE : La position de l’essai est vérifiée à l’aide de la fluoroscopie à partir des vues AP et latérale. Les plaques d’extrémité doivent être surélevées symétriquement (Figure 4).
9. Implantation en cage
- Après avoir identifié la bonne taille, implantez la cage sous guidage fluoroscopique (Figure 5).
- Obtenez des images fluoroscopiques finales en A.P. et en vue latérale.
10. Fermeture
- Utilisez l’irrigation et effectuez un dernier contrôle de l’hémostase.
- Retirez soigneusement tous les écarteurs et écarteurs.
- Fermez la plaie de manière multicouche.

Figure 3 : Identification du niveau du disque. (A-B) : Marquage du niveau souhaité en vue antéropostérieure (AP) et latérale. (C) Identification du niveau souhaité dans la fluoroscopie en vue latérale. Veuillez cliquer ici pour voir une version agrandie de cette figure.
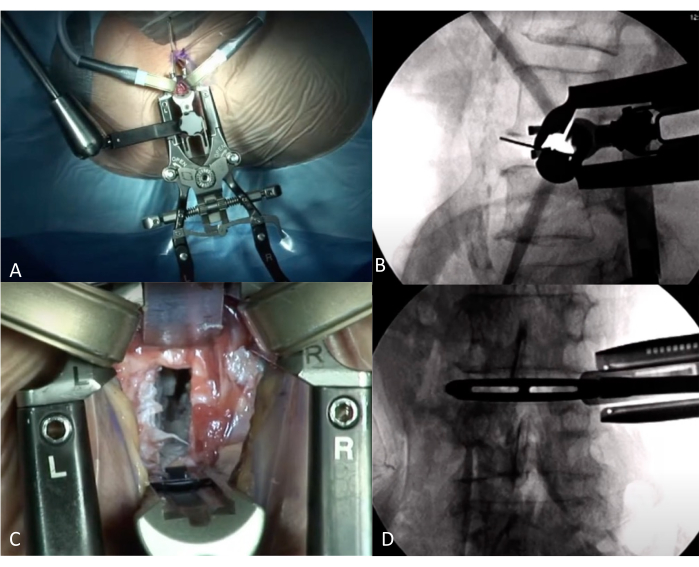
Figure 4 : Vue interopératoire pendant la LLIF. (A) Position des écarteurs sur la vue AP. (B) Vérification peropératoire du niveau correct à l’aide de la fluoroscopie, vue latérale avec écarteurs en place. (C) Vue au niveau du disque à travers les écarteurs. Le disque a été retiré, avec un peu de cartilage restant. (D) Vue AP de fluoroscopie peropératoire, avec une cage d’essai en place. Veuillez cliquer ici pour voir une version agrandie de cette figure.
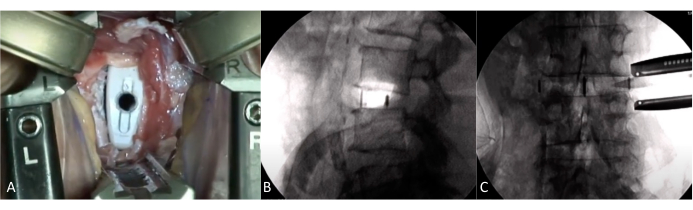
Figure 5 : Vue peropératoire avec cage implantée. (A) Vue peropératoire à travers des écarteurs. Visualisation de la cage implantée. (B-C) Fluoroscopie avec la cage en place. Positionnement correct de la cage avec restauration de la hauteur du disque. Veuillez cliquer ici pour voir une version agrandie de cette figure.
11. Phase postopératoire à l’hôpital
- Encouragez les patients à se mobiliser sans attelle dans les heures qui suivent en leur fournissant des analgésiques adéquats ou d’autres techniques de gestion de la douleur.
- Donnez au patient un régime alimentaire clair jusqu’à ce qu’il ait passé des flatulences, puis passez à un régime régulier.
- Effectuer l’inspection recommandée et la palpation manuelle des flancs ainsi qu’un pansement formel avant le congé.
12. Phase postopératoire ambulatoire
- Après deux semaines, effectuez un contrôle formel de la plaie.
- Conseillez aux patients de ne pas effectuer de mouvements de flexion/levage/torsion de plus de 15 lb.
13. Faites un suivi
- À six semaines, obtenez des radiographies postopératoires et commencez 6 semaines de physiothérapie formelle et d’éducation en mécanique du tronc (Figure 2).
- À 3 mois, effectuez une évaluation formelle. En cas de pseudoarthrose, obtenez une TDM avec des outils de post-traitement MPR (reformatage multiplanaire) ou MIP (projection d’intensité maximale) pour évaluer la continuité de la fusion.
- À six mois, effectuez une évaluation neurologique et obtenez des radiographies standard.
- Libérer le patient après un dernier suivi clinique et radiologique un an après l’intervention.
Résultats
Dans notre étude récente, nous avons étudié les taux de complications à la suite d’une fusion intersomatique latérale autonome12. Nous avons étudié rétrospectivement 158 patients (145 trans-psoas, 13 pré-psoas) qui ont reçu un LLIF entre 2016 et 2020, avec un suivi moyen de 14 mois (Tableau 1).
| Caractéristiques du pat... |
Discussion
La fusion intersomatique lombaire latérale (LLIF) est devenue une technique peu invasive populaire pour réaliser l’arthrodèse. Depuis son introduction, les indications se sont élargies pour le traitement de diverses affections lombaires telles que les maladies dégénératives, les déformations et les pathologies lombaires. Il permet l’implantation de cages intersomatiques plus grandes que le TLIF ou le PLIF à travers l’apophyse, ce qui permet une correction efficace des déf...
Déclarations de divulgation
Jens Chapman MD reçoit des honoraires de consultation de Globus Medical Inc. Rod Oskouian MD reçoit des redevances de Stryker et des honoraires de consultation de Seaspine, Globus Medical Inc., Stryker, DePuy Synthes, Medtronic et ATEC. Tous les autres auteurs n’ont aucun intérêt financier ou non financier pertinent à divulguer.
Remerciements
Aucun.
matériels
| Name | Company | Catalog Number | Comments |
| 100mm Aluminum Center Blade | Nuvasive | 3244100 | |
| 100mm Electrode Center Blade | Nuvasive | 3243100 | |
| 100mm Left Blade | Nuvasive | 3241100 | |
| 100mm Right Blade | Nuvasive | 3242100 | |
| 110mm Aluminum Center Blade | Nuvasive | 3244110 | |
| 110mm Electrode Center Blade | Nuvasive | 3243110 | |
| 110mm Left Blade | Nuvasive | 3241110 | |
| 110mm Right Blade | Nuvasive | 3242110 | |
| 120mm Aluminum Center Blade | Nuvasive | 3244120 | |
| 120mm Electrode Center Blade | Nuvasive | 3243120 | |
| 120mm Left Blade | Nuvasive | 3241120 | |
| 120mm Right Blade | Nuvasive | 3242120 | |
| 130mm Aluminum Center Blade | Nuvasive | 3244130 | |
| 130mm Electrode Center Blade | Nuvasive | 3243130 | |
| 130mm Left Blade | Nuvasive | 3241130 | |
| 130mm Right Blade | Nuvasive | 3242130 | |
| 140mm Aluminum Center Blade | Nuvasive | 3244140 | |
| 140mm Electrode Center Blade | Nuvasive | 3243140 | |
| 140mm Left Blade | Nuvasive | 3241140 | |
| 140mm Right Blade | Nuvasive | 3242140 | |
| 150mm Aluminum Center Blade | Nuvasive | 3244150 | |
| 150mm Electrode Center Blade | Nuvasive | 3243150 | |
| 150mm Left Blade | Nuvasive | 3241150 | |
| 150mm Right Blade | Nuvasive | 3242150 | |
| 160mm Aluminum Center Blade | Nuvasive | 3244160 | |
| 160mm Electrode Center Blade | Nuvasive | 3243160 | |
| 160mm Left Blade | Nuvasive | 3241160 | |
| 160mm Right Blade | Nuvasive | 3242160 | |
| 50mm Aluminum Center Blade | Nuvasive | 3244050 | |
| 50mm Left Blade | Nuvasive | 3241050 | |
| 50mm Right Blade | Nuvasive | 3242050 | |
| 60mm Aluminum Center Blade | Nuvasive | 3244060 | |
| 60mm Left Blade | Nuvasive | 3241060 | |
| 60mm Right Blade | Nuvasive | 3242060 | |
| 70mm Aluminum Center Blade | Nuvasive | 3244070 | |
| 70mm Left Blade | Nuvasive | 3241070 | |
| 70mm Right Blade | Nuvasive | 3242070 | |
| 80mm Aluminum Center Blade | Nuvasive | 3244080 | |
| 80mm Left Blade | Nuvasive | 3241080 | |
| 80mm Right Blade | Nuvasive | 3242080 | |
| 90mm Aluminum Center Blade | Nuvasive | 3244090 | |
| 90mm Electrode Center Blade | Nuvasive | 3243090 | |
| 90mm Left Blade | Nuvasive | 3241090 | |
| 90mm Right Blade | Nuvasive | 3242090 | |
| ALGI Penfield, Long Push | Nuvasive | 3300118 | |
| Anterior Crossbar | Nuvasive | 3240003 | |
| Bayonetted Shim Inserter | Nuvasive | 3200215 | |
| Blade Rotation Driver | Nuvasive | 3240005 | |
| Dilator - 12mm | Nuvasive | 1010968 | |
| Dilator - 6mm | Nuvasive | 1010966 | |
| Dilator - 9mm | Nuvasive | 1010967 | |
| Fixation Shim Screw Driver | Nuvasive | 3200052 | |
| Fluoro Modulator | Nuvasive | 3220131 | |
| Hex Driver (3/32”) | Nuvasive | 1011691 | |
| Hex Key (3/32”) | Nuvasive | 1011748 | |
| Initial Dilator Holder | Nuvasive | 3230140 | |
| K-wire (13.5”) | Nuvasive | 3230101 | |
| Light Cable Adapter, Storz | Nuvasive | 1011811 | |
| Lock Shim Inserter/Repositioning Tool | Nuvasive | 3240001 | |
| Lock Shim Inserter/Repositioning Tool, | Nuvasive | ||
| Low-Profile Shim | Nuvasive | 3240002 | |
| MaXcess 4 4th Blade Attachment | Nuvasive | 3240004 | |
| Maxcess 4 Access System | Nuvasive | Tray with XLIF Dilator and Retractors in different seizes | |
| MaXcess 4 Articulating Arm | Nuvasive | 3240121 | |
| MaXcess 4 Blade, 180mm Electrode Ctr | Nuvasive | 3243180 | |
| Needle Electrodes | Nuvasive | 8050029 | NVM5 System |
| Surface Electrodes | Nuvasive | 8020029 | NVM5 System |
| Targeting Instrument | Nuvasive | 3240000 | |
| XL (18mm wide) | Nuvasive | 1000-00-0716 | Implant |
| XL-F (18mm wide) | Nuvasive | 1000-00-0719 | Implant |
| XL-F Wide (22mm wide) | Nuvasive | 1000-00-0720 | Implant |
| XLIF Annulus Cutter, 4x14mm | Nuvasive | 6942414 | |
| XLIF Annulus Cutter, 4x16mm | Nuvasive | 6942416 | |
| XLIF Cobb, 12mm Straight | Nuvasive | 6940012 | |
| XLIF Cobb, 18mm Down | Nuvasive | 6940118 | |
| XLIF Cobb, 18mm Straight | Nuvasive | 6940018 | |
| XLIF Cobb, 22mm Straight | Nuvasive | 6940022 | |
| XLIF Cobb, Serrated | Nuvasive | 6940001 | |
| XLIF Cutter, 8mm Disc | Nuvasive | 6940151 | |
| XLIF Forceps, Bipolar Str Extra Long | Nuvasive | 3200322 | |
| XLIF Handle, Slide | Nuvasive | 6940004 | |
| XLIF Inserter, Angled XL | Nuvasive | D6904485 | |
| XLIF Kerrison, 2mm | Nuvasive | 6940132 | |
| XLIF Kerrison, 5mm | Nuvasive | 6940135 | |
| XLIF Nerve Retractor, Extra Long | Nuvasive | 3300319 | |
| XLIF Paddle Sizer, 4x16mm | Nuvasive | 6940416 | |
| XLIF Paddle Sizer, 6x18mm | Nuvasive | 6940618 | |
| XLIF Paddle Sizer, 6x22mm | Nuvasive | 6940622 | |
| XLIF Penfield, Pull Extra Long | Nuvasive | 3300318 | |
| XLIF Pituitary, Large | Nuvasive | 6940431 | |
| XLIF Pituitary, Medium | Nuvasive | 6940430 | |
| XLIF Pituitary, Small | Nuvasive | 6940429 | |
| XLIF Rasp | Nuvasive | 6940340 | |
| XLIF Scraper, Endplate | Nuvasive | 6940020 | |
| XLIF Slide, Bayonetted | Nuvasive | 6940063 | |
| XLIF Slide, XW Bayonetted | Nuvasive | 6940064 | |
| XLIF Suction, 12FR Extra Long | Nuvasive | 3300320 | |
| XLIF Suction, 15FR Extra Long | Nuvasive | 3300321 | |
| XL-W (22mm wide) | Nuvasive | 1000-00-0717 | Implant |
| XL-XW (26mm wide) | Nuvasive | 1000-00-0718 | Implant |
Références
- Luoma, K., et al. Low back pain in relation to lumbar disc degeneration. Spine. 25 (4), 487-492 (2000).
- Rabau, O., et al. Lateral lumbar interbody fusion (LLIF): An update. Global Spine J. 10 (2_suppl), 17S-21S (2020).
- Pimenta, L. Less-invasive lateral lumbar interbody fusion (XLIF) surgical technique: video lecture. Eur Spine J. 24 Suppl 3 (S3), 441-442 (2015).
- Pimenta, L. Lateral endoscopic transpsoas retroperitoneal approach for lumbar spine surgery. Presented at VIII Brazilian Spine Society Meeting. , (2001).
- Ozgur, B. M., Aryan, H. E., Pimenta, L., Taylor, W. R. Extreme lateral interbody fusion (XLIF): a novel surgical technique for anterior lumbar interbody fusion. Spine J. 6 (4), 435-443 (2006).
- Lamartina, C., Berjano, P. Prone single-position extreme lateral interbody fusion (Pro-XLIF): preliminary results. Eur Spine J. 29, 6-13 (2020).
- Walker, C. T., et al. Single-position prone lateral interbody fusion improves segmental lordosis in lumbar spondylolisthesis. World Neurosurg. 151, e786-e792 (2021).
- . XLIF Nuvasive Available from: https://www.nuvasive.com/procedures/spine/xlif20/ (2025)
- . DLIF Metronic Available from: https://thespinemarketgroup.com/wp-content/uploads/2020/07/Direct-Lateral-Surgical-Technique-Medtronic.pdf (2025)
- . OLIF Medtronic Available from: https://www.medtronic.com/me-en/healthcare-professionals/therapies-procedures/spinal-orthopaedic/olif.html (2025)
- Alonso, F., et al. The subcostal nerve during lateral approaches to the lumbar spine: an anatomical study with relevance for injury avoidance and postoperative complications such as abdominal wall hernia. World Neurosurg. 104, 669-673 (2017).
- Godolias, P., et al. Complication rates following stand-alone lateral interbody fusion: a single institution series after 10 years of experience. Eur J Orthop Surg Traumatol. 33 (5), 2121-2127 (2022).
- Walker, C. T., et al. Complications for minimally invasive lateral interbody arthrodesis: a systematic review and meta-analysis comparing prepsoas and transpsoas approaches. J Neurosurg Spine. 30 (4), 446-460 (2019).
- Amini, D. A., et al. Development of a decision-making pathway for utilizing standalone lateral lumbar interbody fusion. Eur Spine J. 31 (7), 1611-1620 (2022).
- Camino-Willhuber, G., et al. Lumbar lateral interbody fusion: step-by-step surgical technique and clinical experience. J Spine Surg. 9 (3), 294-305 (2023).
- Kwon, B., Kim, D. H. Lateral lumbar interbody fusion. J Am Acad of Orthop Surg. 24 (2), 96-105 (2016).
- Lall, R. R., et al. Intraoperative neurophysiological monitoring in spine surgery: indications, efficacy, and role of the preoperative checklist. Neurosurg Focus. 33 (5), E10 (2012).
- Taba, H. A., Williams, S. K. Lateral lumbar interbody fusion. Neurosurg Clin of N Am. 31 (1), 33-42 (2020).
- Rodgers, W. B., Gerber, E. J., Patterson, J. Intraoperative and early postoperative complications in extreme lateral interbody fusion. Spine. 36 (1), 26-32 (2011).
- Moro, T., Kikuchi, S., Konno, S., Yaginuma, H. An anatomic study of the lumbar plexus with respect to retroperitoneal endoscopic surgery. Spine. 28 (5), 423-427 (2003).
- Ng, J. P. H., Kaliya-Perumal, A. K., Tandon, A. A., Oh, J. Y. L. The oblique corridor at L4-L5: a radiographic-anatomical study into the feasibility for lateral interbody fusion. Spine. 45 (10), E552-E559 (2020).
- Huang, C., Xu, Z., Li, F., Chen, Q. Does the access angle change the risk of approach-related complications in minimally invasive lateral lumbar interbody fusion? An MRI study. J Korean Neurosurg Soc. 61 (6), 707-715 (2018).
- Kramer, D. E., Woodhouse, C., Kerolus, M. G., Yu, A. Lumbar plexus safe working zones with lateral lumbar interbody fusion: a systematic review and meta-analysis. Eur Spine J. 31 (10), 2527-2535 (2022).
- Godolias, P., et al. Lumbosacral plexus 3D printing with dissection validation - a baseline study with regards to lateral spine surgery. Interdiscip Neurosurg. 31, 101666 (2023).
- Agarwal, N., et al. Lateral lumbar interbody fusion in the elderly: a 10-year experience. J Neurosurg Spine. 29 (5), 525-529 (2018).
- Chen, E., et al. Cage subsidence and fusion rate in extreme lateral interbody fusion with and without fixation. World Neurosurg. 122, 969-977 (2019).
- Wang, Y., Beydoun, M. A., Min, J., Xue, H., Kaminsky, L. A., Cheskin, L. J. Has the prevalence of overweight, obesity and central obesity levelled off in the United States? Trends, patterns, disparities, and future projections for the obesity epidemic. Int J Epidemiol. 49 (3), 810-823 (2020).
- Barrie, U., et al. Impact of obesity on complications and surgical outcomes after adult degenerative scoliosis spine surgery. Clin Neurol Neurosurg. 226, 107619 (2023).
- Shasby, G. Erratum. Does minimally invasive spine surgery improve outcomes in the obese population? A retrospective review of 1442 degenerative lumbar spine surgeries. J Neurosurg Spine. 36 (6), 1035 (2022).
- Hijji, F. Y., et al. Lateral lumbar interbody fusion: a systematic review of complication rates. Spine J. 17 (10), 1412-1419 (2017).
- Hu, W. -. K., et al. An MRI study of psoas major and abdominal large vessels with respect to the X/DLIF approach. Eur Spine J. 20 (4), 557-562 (2011).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon