A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
Ex vivo החקיינות של hematopoiesis אנושיים בריאים חריגה
In This Article
Summary
מערכת התרבות 3D עבור hematopoiesis מתואר באמצעות דם טבורי האדם הנגועים מוח העצם. השיטה מבוססת על שימוש פוליאוריטן נקבובי הפיגום הסינתטי מצופה חלבונים תאי מטריקס. פיגום זה ניתנת להתאמה להכיל מגוון רחב של תאים.
Abstract
בתאי גזע hematopoietic דורשים microenvironment ייחודי כדי לקיים תא דם היווצרות 1, מח עצם (בע"מ) הינו קומפלקס תלת ממדי (3D) hematopoiesis שבו רקמת מוסדר על ידי microenvironments הסלולר מאורגנים במרחב כינה נישות 2-4. הארגון של נישות בע"מ היא קריטית לתפקוד או חוסר תפקוד של BM רגיל או ממאיר 5. לכן הבנה טובה יותר של ב microenvironment vivo באמצעות חיקוי vivo לשעבר יעזור לנו להבהיר את הגורמים המולקולריים, תאית microenvironmental של leukemogenesis 6.
נכון לעכשיו, תאים היווצרות הדם מתורבתים במבחנה ב דו מימדי (2D) תרבות צלוחיות רקמות / גם שלטי 7 הדורשים או שיתוף עם התרבות allogenic או תאים סטרומה xenogenic או תוספת של ציטוקינים אקסוגניים 8. תנאים אלה הם מלאכותיים שונים in vivo 9,10 pluripotency.
כאן, אנו מציגים מח עצם רומן 3D התרבות מערכת המדמה בסביבת הגידול 3D vivo ותומך hematopoiesis multilineage בהעדר גורמי צמיחה חיצוניים. פיגום נקבובי ביותר בשימוש במערכת זו עשוי פוליאוריטן (PU), מאפשר צפיפות גבוהה צמיחת תאים על פני שטח גבוהה יותר משטח ספציפי מאשר התרבות monolayer קונבנציונאלי ב 2 ד 11. העבודה שלנו ציינה כי מודל זה נתמך על צמיחה של דם טבורי האנושי (CB) תאים mononuclear (MNC) 12 תאים leukemic העיקריים בהיעדר ציטוקינים חיצוניים. זה חיקוי הרומן 3D מספק פלטפורמה מעשית עבור פיתוח של מודל ניסיוני האדם ללמוד hematopoiesis ולבחון טיפולים חדשניים בסרטן הדם.
Protocol
1. פיגום ייצור ביו functionalization של פיגומים
- כדי להמציא פו פיגומים (גודל הנקבוביות 100-250 מ"מ, נקבוביות 90-95%) בצורה של צלחת פטרי דיסקים, השתמש הפרדת פאזות המושרה תרמית 13 תהליך הכנת פתרון פולימר (5wt% ב Dioxan) ואחריו מקפיא לאחר מכן סובלימציה ממס (איור 1 א).
- חותכים את הדיסק פיגום לקוביות של 0.5 מ"מ x 0.5 x 0.5 לפני ציפוי עם ECM חלבונים (1B איור).
- טרום להרטיב את הפיגומים על ידי שיקוע שלהם אתנול (70%) עבור 1 דקות ולאחר מכן להעביר את הפוספט בופר סליין (PBS) עבור 20 דקות. אז סרכזת דקות 10 XG ב 3630 ולהוסיף את הפתרון חלבון.
- בצנטריפוגה פיגומים בתמיסה חלבון XG 1420 עבור 20 דקות.
- על מנת לבטל את חסימת הנקבוביות על פני השטח, ולאפשר את התאים שנזרעו לחדור עמוק יותר לתוך הפיגום, צנטריפוגה הפיגומים פעם נוספת על XG 910 דקות 10ב PBS.
- לחטא את הפיגומים באמצעות שילוב של חשיפה 8 דק 'ב 230 וולט, 50 הרץ, 0.14 מנורה, UV, עם טבילה עבור H 2 באתנול (70%). לאחר מכן לשטוף את הפיגומים פעמיים PBS לפני הוספת שינוי Iscove של Dulbecco בינוני (IMDM) השלימו עם סרום 30% שור עוברית (FBS) ו 1% פניצילין וסטרפטומיצין (P / S). מניחים את הפיגומים של חממה humidified במשך 3 ימים ב 37 מעלות צלזיוס, 5% CO 2 לפני השימוש. פיגומים סטריליים ממוקמים מספר 24 היטב רקמות צלחות תרבות (1 פיגום בכל טוב).
2. תא בידוד mononuclear ו זריעת הפיגום
- לחלץ אדם MNC מן הדם הטבורי או הנגועים דגימות מח עצם, באמצעות Ficoll-Paque שיפוע צפיפות צנטריפוגה (35 דק 'ב 1500 סל"ד) (איור 1 ג).
- Resuspend MNC ב IMDM המכיל 30 FBS% ו 1% P / S.
- זרעים 100μl של השעיה MNC (2 × 10 6 תאים / הפיגום) על גבי פיגומים באמצעות מיקרו פיפטה.
- דגירה פיגומים seeded על 37 מעלות צלזיוס מתחת CO 5% 2 במשך 10 דקות עבור התאים ליישב את הפיגומים.
- למעלה את כל טוב עם 1.5 מ"ל של IMDM המכיל 30% FBS וצלחות גם 1% P / S ומקום בחממה ב 37 מעלות צלזיוס, 5% CO 2 למשך כל הניסוי.
- את הפיגומים זרע לעבור שינוי יומי של כל מדיה.
3 ב התפשטות תאים באתרו ומורפולוגיה. MTS, SEM ו Cytospins
- Assay MTS: הסר מתרבות אחת בלתי seeded ושני פיגומים זרע ומכניסים 24 החדש נקי היטב את הצלחת. הוסף 1 מ"ל של מדיה 200 μl של פתרון MTS ו דגירה של 3 שעות ב 37 מעלות צלזיוס, 5% CO 2.
- קח 100 x 8 דגימות μl של supernatant: המקום בצלחת 96-היטב ספיגת מידה ב 490 ננומטר באמצעות קורא microplate.
- סריקה במיקרוסקופ אלקטרונים סורק (SEM): בנקודות זמן שונות של התרבות ה ', להסיר את הפיגומים שנזרעו עם MNC מהתקשורת, ולתקן את הפתרון 2.5%-PBS שנאגרו glutaraldehyde 40 דקות ב 4 ° C, ולאחר מכן לשטוף פעמיים עם PBS.
- מיובש על פיגומים בסדרה מדורג של אתנול (25, 50, 70, 80, 90, 95, ו - 100%), כל אחד 10 דקות ויבש בסביבה מזוהם במשך 4 שעות.
- דגימות מקטעים ולאחר מכן גמגום, מעיל אתם זהב באווירה ארגון 2 דקות קודם להערכה SEM, השתמש במתח האצה של kV 20.
- Cytospins: איסוף 2.0 x 10 4 תאים / שקופיות ידי aspirating את התאים מן הפיגום בנקודות זמן שונות בתרבות.
- בצנטריפוגה תאים על גבי זכוכית נושאת דקות 3 בסל"ד 1500.
- כתם על השקופיות עם רייט Giemsa כתמים השתנה ולבחון באמצעות מיקרוסקופ אופטי. F-להציג מערכת הדמיה רך ניתן להשתמש כדי לצלם תמונות.
- לשטוף מחליק לפני תצפית מיקרוסקופ.
- M ניתוח ultiphoton: פיגומים תקן בנקודות זמן שונות עם אדי אתנול (70%) למשך הלילה, ואז יבש החנות ב -20 ° C עד לניתוח נוסף. לפני להדמיה סעיף מיקרוסקופ multiphoton הפיגום לתוך 30 מיקרומטר בעובי שקופיות ורטוב עם PBS.
- חסום פיגומים seeded ב PBS עם סרום 10% שור עוברית למשך 30 דקות בטמפרטורת החדר.
- דגירה פיגומים את הלילה על 4 מעלות צלזיוס בחושך עם דילול 1:50 של נוגדן חד שבטי העיקרית: העכבר CD71 אדם אנטי.
- לשטוף דגימות שלוש פעמים PBS ואת הכתם עם נוגדנים משני: אנטי העכבר Alexa פלואוריד 488 עבור H 1 בטמפרטורת החדר בחושך.
- לשטוף דגימות שלוש פעמים עם PBS ולבחון באמצעות מיקרוסקופ confocal באמצעות פליטת מים X60 עדשה אובייקטיבי.
- Fluorophore Alexa פלואוריד 488 נרגש על 488 ננומטר על ידי לייזרים pulsatile. 5.3.2 התוכנה Volocity ניתן להשתמש ניתוח התמונה לאחר מכן.
- לפני ניתוח הסלולר cytometer את זרימת (FC), לתייג את התאים בעלי עניין עם נוגדנים immunofluorescence המתאימים לצורך זיהוי. מספר דגימות ערוכים לפי הנוגדנים שנבחרו לצורך זיהוי. לגילוי MNC השילוב הבא של נוגדנים משמשים: CD45-FITC/CD71-PE/CD235a-PE-Cy5.
- לשאוב את התאים מן הפיגום בנקודות זמן שונות צנטריפוגות. ממיסים תא גלולה של כ 1x10 6 תאים במאגר FC 100 μl (אזיד הנתרן PBS + 0.1%) ומוסיפים 10 μL של צבע פלואורסצנטי כל נוגדן. דגירה התאים למשך 30 דקות ב 4 ° C, לשטוף פעמיים עם PBS ולבסוף מחדש להשעות במאגר FC.
- טען את המדגם לתוך צבעונית cytometer הזרימה עם שליטה isotype להגדיר "השליליות" של הביטוי נוגדנים ו לכייל את ערוצי גילוי עם בקרת זרימה cytometer.
- לקרוא צבעונית מדגם W ith שלושת נוגדנים שונים ובסופו של דבר מייצגים את הנתונים באמצעות תוכנה WinList.
5. נציג תוצאות
למשל hematopoietic של קינטיקה הצמיחה הסלולר ללא תוספת של גורמי גדילה חיצוניים מוצגת באיור 2. בשל אופייה הטרוגנית של hematopoiesis, שני תאים שונים: רגילים ותאי היווצרות הדם תקינות באים לידי. איור 2 א, התרבות תאים של CBMNC האנושי בא לידי ביטוי לאחר 28 ימים בתרבית. 2B איור מראה את הקינטיקה הצמיחה באמצעות חיקוי אדם תאים leukemic ראשוניים. התרבות תאים נבחנת באמצעות assay MTS אשר מודד את פעילות חילוף החומרים התאי ביחס ספיגת. בשני המקרים, התאים התרבו והקימו במודל. הבדלים קינטיקה הצמיחה הם נצפו: היווצרות הדם לתאים נורמליים מקימים התרבות מהר יותר מאשר תאים leukemic.
"_content> מורפולוגיה של תאים שנקטפו גם לאחר 28 ימים של תרבות בהעדר גורמי צמיחה חיצוניים היה אופייני של היווצרות הדם תאים נורמליים (איור 3 א) ו תאים leukemic (איור 3 ב). חלקים מרכזיים של פיגומים נותחו על ידי SEM לאחר הפיגומים הוסרו מן התרבות והראה התפשטות התאים זרע לאורך הפיגום, לבסס את עצמם בקבוצות וכן "נישה כמו" מבנים (איור 3 א '& ב'). תרשים ג מציג את פיזור גודל הנקבוביות ב unseeded הפיגום משמש כביקורת. מיקרוסקופיה multiphoton לאחר 28 ימים שימש להדגיש את חלוקת התאים בתוך הפיגום 3D באתרו והוא הראה את הנוכחות של erythroid איים בסעיפים המרכזיים של הפיגום (איור 4) על ידי ביטוי של הסמן CD71 שהוא חיובי erythroblasts. זה מוכיח את החשיבות של דו בוגרים ותאי התבגרותטבעת erythropoiesis. לבסוף, cytometry זרימה גרפים של זריעת תאים לפני מראה את ההבדל הפנוטיפ של תאים היווצרות הדם, שבו ציור 5a מייצג היווצרות הדם תאים נורמליים: CBMNCs אדם איור 5 ב 'ממחיש את היווצרות הדם תאים לא תקינים: תאים leukemic ראשוניים. רמות CD235a + ו + CD45 המתאים אריתרוציטים ו Leukocytes בהתאמה גבוהות יותר מדגם הרגיל מאשר leukemic המדגיש את הטבע hemoblastic של לוקמיה את.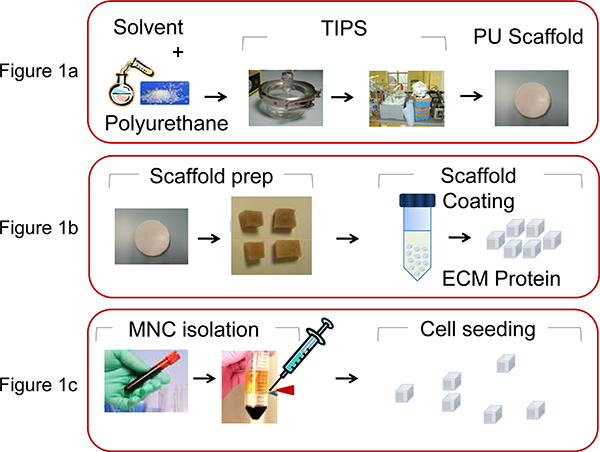
באיור 1. איור של התהליכים המעורבים PU פיגום ייצור ביו functionalization. א) פו הוא מומס Dioxan (5wt%) ועל ידי תהליך המושרה תרמית שלב ההפרדה סובלימציה ממס לאחר הפיגום מיוצר, כפי שתואר על ידי Safinia ואח' 13. ב) דיסק הפיגום אז הוא חתך intהו קוביות של 0.5 x 0.5 x 0.5 מ"מ ואז מצופה ידי צנטריפוגה עם תוספת הסלולר מטריקס (ECM) חלבונים. ג) MNC המחולצים הטבור CB אדם או השאיפה בע"מ באמצעות שיפוע צפיפות צנטריפוגה ו seeded (2x10 6 תאים / הפיגום) על פיגומים PU עם micropipette.
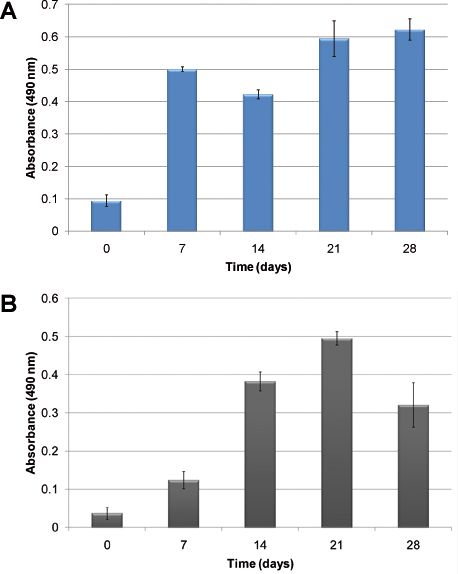
2. איור התרבות תאים נמדדת באמצעות assay MTS:) באמצעות אדם דם טבורי MNCs, ב ') באמצעות אדם תאים leukemic ראשוניים. העמודים להראות את הצמיחה של תאים לאורך זמן כאשר זרע של פיגומים PU ללא תוספת של ציטוקינים חיצוניים.
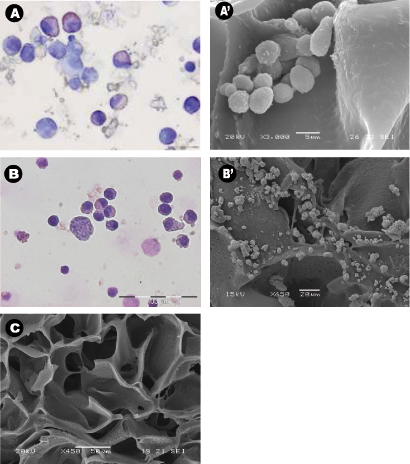
איור 3: מורפולוגיה תא והפצה ברחבי פיגומים באמצעות cytospins, scanniנג micrographs אלקטרונים. (AB) נציג רייט Giemsa cytospins צבעונית של מספר תאים) דם טבורי mononuclear שנאספו PU פיגומים לאחר 28 ימים של תרבות, ב) שאיפות עצם תאים leukemic שנאספו PU פיגומים לאחר 14 ימים של תרבות. שני הניסויים בוצעו במצב ציטוקינים חינם. (A'-B ") קטעים מרכזיים נציג של הפיגום micrographs יחידת השיטור של SEM) seeded דם טבורי MNCs ו 'ב') תאים leukemic לאחר בתרבית במשך 28 ימים, ו-C) שליטה פיגום עם תאים לא.
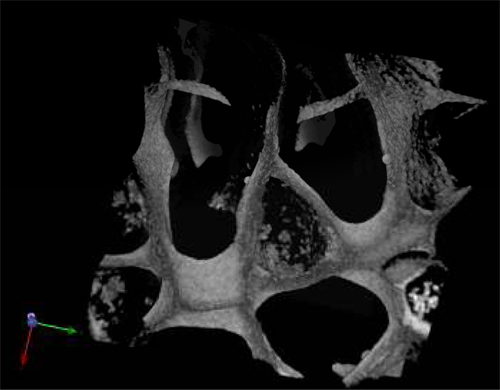
איור 4. מיקרוסקופ multiphoton של פיגום PU seeded עם דם טבורי לאחר MNCs ד 28 בתרבות צבעונית עם סמן erythroid CD71.

איור 5. תזרים cytometry 3D הדוט מגרשים מוכתם עבור CD45, CD71 וביטוי CD235a סמנים פני השטח. השליטה isotype לקבל מוצגת גם השוואה של עוצמת הקרינה היחסית. לוח מראה אדם דם טבורי תאים mononuclear חיוביות עבור סמנים ומעלה: ב 'לוח מראה האדם תאים leukemic ראשוניים.
Discussion
המערכת לשעבר vivo 3D התרבות המוצגת כאן מאפשרת לנו להקים ביומימטיקה 3D של hematopoiesis זה מסכם את הארכיטקטורה BM המקורי פנוטיפ הסלולר העצמאי של ציטוקינים חיצוניים. מודל 3D מספק את המבנה microenvironment המאפשרת היווצרות הדם לתאים נורמליים נורמלי להתרבות בתנאים דומים לאלה נתקל viv...
Disclosures
אין לנו מה למסור.
Acknowledgements
עבודה זו מומנה על ידי קרן ריצ'רד תומס לוקמיה, טאטא ליידי הזיכרון בנאמנות, פארק Northwick החולים קרן נאמנות לוקמיה מחקר במכון הלאומי לבריאות ומחקר (NIHR), בריטניה.
Materials
| Name | Company | Catalog Number | Comments |
| Name of the reagent | Company | Catalogue No | |
| Dioxan | Invitrogen | D20,186-3 | |
| PBS | Gibco | 14190-094 | |
| IMDM | Invitrogen | 12440-053 | |
| Ficoll-Paque | GE Healthcare | 17-1440-02 | |
| Penicillin/Streptomycin | Sigma-Aldrich | P4333 | |
| MTS | Promega | G3580 | |
| Glutaraldehyde | Fluka Biochemika | 49624 | |
| Wright-Giemsa | Sigma-Aldrich | WG32 | |
| Fetal bovine serum | Gibco | 10108-165 | |
| CD71 | Santa Cruz Biotechnology | sc-32272 | |
| Alexa Fluor 488 | Invitrogen | A11001 | |
| CD45-FITC | BD Pharmigen | 74895 | |
| CD71-PE | BD Pharmigen | 555537 | |
| CD235a-PE-Cy5 | BD Pharmigen | 555570 | |
| Sodium azide | Sigma-Aldrich | S-8032 |
References
- Orkin, S., Zon, L. Hematopoiesis: an evolving paradigm for stem cell biology. Cell. 132, 631-644 (2008).
- Spradling, A., Drummond-Barbosa, D., Kai, T. Stem cells find their niche. Nature. 414, 98-104 (2001).
- Panoskaltsis, N., Mantalaris, A., Wu, D. Engineering a mimicry of bone marrow tissue ex vivo. J Biosci. Bioeng. 100, 28-35 (2005).
- Lo Celso, C. Live-animal tracking of individual haematopoietic stem/progenitor cells in their niche. Nature. 457, 92-96 (2009).
- Mantalaris, A., Bourne, P., Wu, J. Production of human osteoclasts in a three-dimensional bone marrow culture system. Biochem. Eng. J. 20, 189-196 (2004).
- Placzek, M. Stem cell bioprocessing: fundamentals and principles. J. R. Soc. Interface. 6, 209-232 (2009).
- Dexter, T., Testa, N., Prescott, D. . Methods in Cell Biology. 14, 387-405 (1976).
- Piacibello, W. Differential growth factor requirement of primitive cord blood hematopoietic stem cell for self-renewal and amplification vs proliferation and differentiation. Leukemia. 12, 718-727 (1998).
- Yoshida, T., Takagi, M. Cell processing engineering for ex vivo expansion of hematopoietic cells: a review. Biochemical Engineering Journal. 20, 99-106 (2004).
- Lim, M. Intelligent bioprocessing for haemotopoietic cell cultures using monitoring and design of experiments. Biotechnol. Adv. 25, 353-368 (2007).
- Mortera-Blanco, T., Mantalaris, A., Bismarck, A., Panoskaltsis, N. The development of a three-dimensional scaffold for ex vivo biomimicry of human acute myeloid leukaemia. Biomaterials. 31, 2243-2251 (2010).
- Mortera-Blanco, T., Mantalaris, A., Bismarck, A., Aqel, N., Panoskaltsis, N. Long-term cytokine-free expansion of cord blood mononuclear cells in three-dimensional scaffolds. Biomaterials. 32, 9263-9270 (2011).
- Safinia, L., Datan, N., Hohse, M., Mantalaris, A., Bismarck, A. Towards a methodology for the effective surface modification of porous polymer scaffolds. Biomaterials. 26, 7537-7547 (2005).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved