このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
正常と異常ヒト造血のex vivoでの擬態
要約
造血のための3D培養系は、ヒト臍帯血および白血病骨髄細胞を用いて記述されています。方法は、細胞外マトリックスタンパク質でコーティングされた多孔質のポリウレタン合成足場の使用に基づいています。この足場は、細胞の広い範囲に対応するために適応可能である。
要約
造血幹細胞は、血液細胞の形成1を維持するためにユニークな微環境を必要とします。骨髄(BM)は、複雑な3次元(3D)ティッシュ式中、造血である空間的に組織化、細胞微小環境によって制御されているニッチ2-4と呼ばれる。 BMニッチの組織が 正常または悪性BM 5の機能または機能不全のために重要です。したがって、ex vivoでの擬態を用いたin vivo微小環境でのより良い理解は、私たちは、白血病6の分子、細胞と微小環境の決定要因を解明に役立つだろう。
現在、造血細胞のいずれか同種または異種間質細胞との共培養または外因性のサイトカインの8の加算を必要とする2次元(2D)の組織培養フラスコ/ウェルプレート7にin vitroで培養されています。これらの条件は、人工的であり、 生体内での異なる9,10が失われる可能性が異常に高いサイトカイン濃度に細胞をさらすという点で微小。
ここで、我々 は 、in vivo 3次元成長環境でシミュレートし、外因性成長因子の存在下で多系統造血をサポートして新たな3D骨髄培養系を提示します。ポリウレタン(PU)で作られたこのシステムで使用される非常に多孔性の足場は、2Dの11の従来の単層培養よりも高い比表面積にわたって高密度の細胞増殖を促進します。私たちの仕事は、このモデルはヒト臍帯血(CB)単核細胞(MNC)外因性のサイトカインの存在下で12および主要な白血病細胞の成長を支えたことを示した。この小説の3D擬態は、造血を勉強すると白血病の新しい治療法を探求する人間の実験モデルの開発のための実行可能なプラットフォームを提供します。
プロトコル
1。足場の足場製造·バイオ機能化
- ペトリ皿ディスクの形でPU足場を(孔径100〜250ミリメートル、気孔率90〜95%)を作製するには、凍結とその後に続くポリマー溶液(ジオキサン中の5重量%)を調製することにより、熱誘起相分離13プロセスを使用して溶剤昇華( 図1A)。
- ECMタンパク質( 図1B)でコーティングする前に0.5×0.5×0.5 mmの立方体に足場ディスクを切断します。
- 1分間エタノールでそれらを浸漬することによってプリウェット足場(70%)、続いてリン酸塩への転送は20分間緩衝生理食塩水(PBS)。その後、3630 xgで10分間遠心し、タンパク質溶液を追加します。
- 20分間1420×gで蛋白質溶液中で足場を遠心分離します。
- 表面の毛穴のブロックを解除し、足場の奥深くに浸透して播種した細胞を可能にするために、10分間910×gで1より多くの時間を足場遠心PBSインチ
- エタノール(70%)で2時間浸漬して、UVランプを0.14 230 V、50 Hzで、少なくとも8分露出の組み合わせを使用して足場を殺菌。その後、30%ウシ胎児血清(FBS)および1%ペニシリンおよびストレプトマイシン(P / S)を添加したイスコフ改変ダルベッコ培地(IMDM)を追加する前に、PBSで2回足場を洗う。 ℃、5%CO 2は、使用前に37℃で3日間の加湿インキュベーター中で足場を置きます。無菌の足場は、24ウェル組織培養プレート(ウェル当たり1足場)に配置されます。
2。単核細胞の単離と足場シード
- をFicoll-Paque密度勾配遠心分離(1500 rpmで35分)( 図1C)を使用して 、臍帯血または白血病骨髄サンプルから人間のMNCを抽出します。
- IMDMに再懸濁し、MNCは、30%FBSおよび1%P / Sを含む
- マイクロピペットを用いて足場の上にMNC懸濁液の100μlの種子(2×10 6細胞/足場)。
- 足場に解決するためにセルの10分間、5%CO 2下で37℃で播種足場をインキュベートします。
- 37℃インキュベーターで30%FBSおよび1%P / Sと場所ウェルプレートを含むIMDM 1.5 mlを各ウェルアップトップ℃、実験期間中5%CO 2。
- シード足場は、毎日すべてのメディアの変化を受けています。
3 In Situ細胞増殖と形態、次の操作を行います 。MTS、SEMとCytospins
- MTSアッセイ:培養1非シードとクリーンな新しい24ウェルプレートに2シードの足場と場所から削除します。 37メディアと3時間MTS溶液とインキュベートし、200μlの1 mlの℃、5%CO 2を追加します 。
- マイクロプレートリーダーを用いて490nmで96ウェルプレートおよび測定の吸光度で行われ、上清から8×100μlのサンプルを取る。
- 走査電子顕微鏡(SEM):番目の異なる時点でeの文化は、メディアからのMNCを接種した足場を削除して、4時40分°C、2.5%PBS-緩衝グルタルアルデヒド溶液で固定し、PBSで2回洗浄する。
- エタノールの段階的シリーズ(25、50、70、80、90、95、および100%)で脱水足場、各4時間の無菌環境で10分間、乾燥した。
- セクションの標本とし、前のSEM評価に2分間アルゴン雰囲気中での金のスパッタコートして、20 kVの加速電圧を使用しています。
- Cytospins:文化の異なる時点で足場から細胞を吸引することにより2.0×10 4細胞/スライドを収集します。
- 1500 rpmで3分間のガラススライド上に細胞を遠心分離します。
- ライト·ギムザ染色と変更された光学顕微鏡を用いて観察してスライドを染色。 F-VIEWソフトイメージングシステムは、写真を撮るために使用することができます。
- 顕微鏡観察の前にスライドを洗浄します。
- M ultiphoton分析:さらに分析まで-20℃でエタノール蒸気(70%)一晩乾燥した、店舗°Cで別の時点で修正足場。 30μmの厚さのスライドに多光子顕微鏡のセクション足場と可視化の前に、PBSでぬれた。
- 室温で30分間、10%ウシ胎児血清を含むPBS中に播種足場をブロックします。
- マウス抗ヒトCD71を:°C暗闇の中で主要なモノクローナル抗体の1:50希釈し4℃で足場は、一晩インキュベートします。
- サンプルをPBSで3回洗浄し、二次抗体で染色:暗闇の中で、室温で1時間インキュベートした抗マウスのAlexa Fluor 488。
- PBSでサンプルを3回洗浄し、水の排出X60対物レンズを用いた共焦点顕微鏡で観察します。
- 蛍光体のAlexa Fluor 488拍レーザーで488nmで励起されています。 Volocity 5.3.2ソフトウェアは、その後の画像解析に使用することができます。
- フローサイトメーター(FC)の細胞分析の前に、検出に対応する免疫抗体で目的の細胞にラベルを付けます。サンプル数は、検出のために選択された抗体に応じて用意されています。 MNC検出用抗体の次の組み合わせが使用されています。CD45-FITC/CD71-PE/CD235a-PE-Cy5。
- 異なる時間ポイントと遠心で足場から細胞を吸引します。 100μlのFC緩衝液(PBS + 0.1%アジ化ナトリウム)で6×10の周りの細胞の細胞ペレットを溶解し、各抗体の蛍光色素の10μLを追加します。 4℃で30分間細胞をインキュベートし、PBSで2回洗浄し、最終的にFCの緩衝液に再懸濁する。
- アイソタイプコントロール抗体発現の "否定"を設定し、フローサイトメーターの制御と検出チャネルを校正するためで染色しフローサイトメトリーにサンプルをロードします。
- wを染色したサンプルを読む i番目の3種の異なる抗体、最後にWinListソフトウェアを使用してデータを表します。
5。代表的な結果
外因性の成長因子を添加せずに、造血細胞の増殖動態の例を図2に示されています。造血の不均質な性質のために、二つの異なる細胞:正常と異常な造血細胞が示されている。 図2Aにおいて、ヒトCBMNCの細胞増殖は、培養28日後に明らかである。 図2Bは、ヒトの主要な白血病細胞を用いた擬態の成長速度を示しています。細胞増殖は、吸光度との関係で細胞の代謝活性を測定するMTSアッセイを用いて評価されています。両方のケースでは、細胞は増殖し、モデルに設立された。成長速度の違いが観察されています。文化を確立し、正常造血細胞より速い白血病細胞より。
外因性増殖因子の不在下でさえ文化の28日後に採取した細胞の形態が正常な造血細胞( 図3A)および白血病細胞( 図3B)の典型的だった。_content "は>足場の中央のセクションは、後のSEMで分析した足場は、培養液から除去し、クラスターおよび"ニッチのような"構造( 図3A '&B')の自分自身を確立し、足場全体に播種細胞の拡散を示した。 図Cは、シーディングの細孔サイズや分布を示した足場は、コントロールとして使用されます。多光子顕微鏡は、28日はその場で 3D足場内の細胞の分布を明らかにするために使用され、それがマーカーの発現により足場の中央セクション( 図4)赤芽球島の存在を示した後赤芽球で陽性である。これは、成熟した成熟細胞デュの重要性を証明するCD71リング赤血球。最後に、細胞のフローサイトメトリーのグラフ前の播種は 、 図5Aは、正常な造血細胞を表して造血細胞の表現型の違いを示しています。人間CBMNCsと図5Bは、異常な造血細胞を示しています。主要な白血病細胞。 CD235a赤血球と白血球+とCD45 +対応のレベルはそれぞれ白血病のhemoblastic性質を強調する白血病に比べて通常のサンプルでは高くなっています。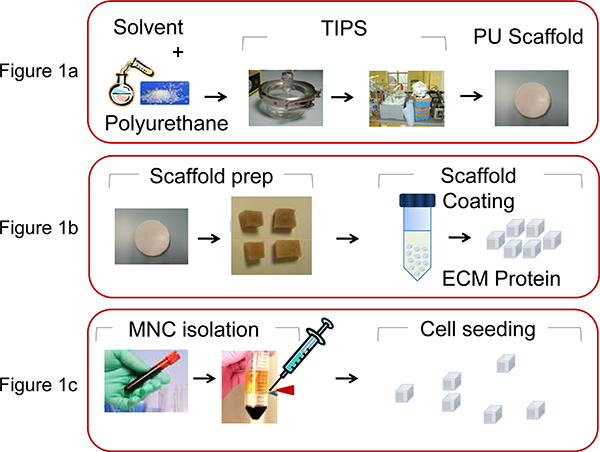
図1:PU足場製造·バイオ機能化に関与するプロセスのイラスト。 A)PUはジオキサン(5重量%)に溶解し、熱誘起相分離過程とその後の溶剤昇華によって足場はSafinia ら 13で説明したように、生成されます。 B)足場ディスクは、次にint切断されoののキューブ0.5×0.5細胞外マトリックス(ECM)タンパク質と、遠心分離により被覆された×0.5 mmとして。 C)MNCは、ヒト臍帯CBから、またはマイクロピペットで密度勾配遠心分離およびPU足場に播種し(2×10 6細胞/足場)を使用して、BM吸引から抽出されます。
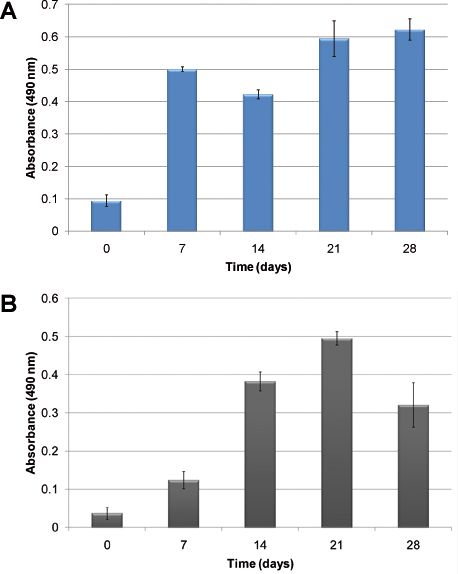
図2細胞の増殖はMTSアッセイを用いて測定しました。)は、ヒト臍帯血多国籍企業を使用して、B)ヒト初代白血病細胞を用いた。列には、外因性のサイトカインを添加せずにPU足場に播種時間をかけて細胞の成長を示しています。
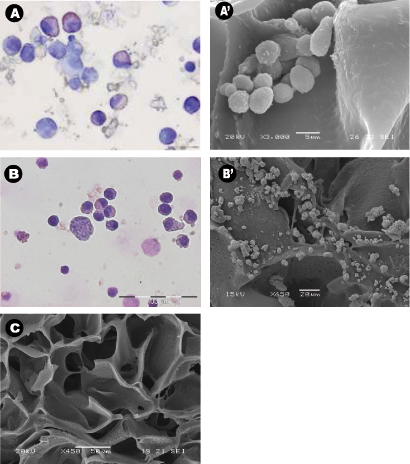
図3:cytospinsを使用して足場の周りの細胞の形態と分布、scanningの電子顕微鏡写真を示す。 (AB)培養28日後にPUの足場から収集された)臍帯血単核細胞の代表的なライト·ギムザ染色したcytospins、AとB)骨吸引白血病細胞は、培養14日後にPU足場から収集された。両方の実験は、サイトカイン遊離状態で行った。 (A'-B '))シード臍帯血多国籍企業とB')を28日間培養された後、白血病細胞、無細胞とC)コントロール足場のPU足場SEM写真の代表的な中央のセクション "。
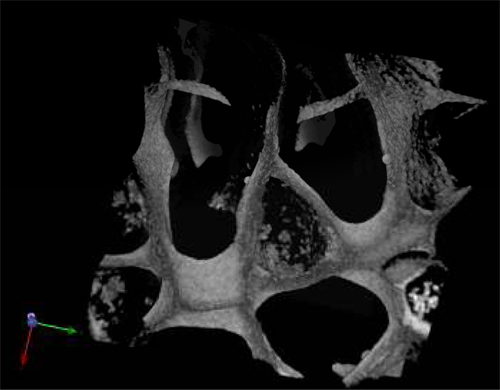
図4赤血球マーカーCD71との文化やステンドグラスの28日後に臍帯血多国籍企業のPU足場シードの多光子顕微鏡写真。

図5:フローサイトメトリー3Dのドットプロットは、CD45、CD71及びCD235a表面発現マーカーを染色した。得られたアイソタイプコントロールはまた、相対的な蛍光強度の比較のために提示されます。パネルは、上記のマーカーのヒト臍帯血単核細胞が陽性を示し、パネルBは、ヒト初代白血病細胞を示しています。
ディスカッション
ここで紹介するex vivoでの三次元培養システムは、外因性のサイトカインの元BMアーキテクチャと、細胞の表現型が独立して反復することが造血の3Dバイオミミクリーを確立することを可能にします。 3Dモデルの構造と正常および異常な造血細胞が in vivo で遭遇したと同様の条件で増殖することができます微小環境を提供しています。
高分子足場材料の...
開示事項
我々は、開示することは何もありません。
謝辞
この作品は、リチャード·トーマス白血病基金、レディタタメモリアルトラスト、ノースウィックパーク病院の白血病研究基金と保健研究(NIHR)の国立研究所、英国によって資金を供給された。
資料
| Name | Company | Catalog Number | Comments |
| Name of the reagent | Company | Catalogue No | |
| Dioxan | Invitrogen | D20,186-3 | |
| PBS | Gibco | 14190-094 | |
| IMDM | Invitrogen | 12440-053 | |
| Ficoll-Paque | GE Healthcare | 17-1440-02 | |
| Penicillin/Streptomycin | Sigma-Aldrich | P4333 | |
| MTS | Promega | G3580 | |
| Glutaraldehyde | Fluka Biochemika | 49624 | |
| Wright-Giemsa | Sigma-Aldrich | WG32 | |
| Fetal bovine serum | Gibco | 10108-165 | |
| CD71 | Santa Cruz Biotechnology | sc-32272 | |
| Alexa Fluor 488 | Invitrogen | A11001 | |
| CD45-FITC | BD Pharmigen | 74895 | |
| CD71-PE | BD Pharmigen | 555537 | |
| CD235a-PE-Cy5 | BD Pharmigen | 555570 | |
| Sodium azide | Sigma-Aldrich | S-8032 |
参考文献
- Orkin, S., Zon, L. Hematopoiesis: an evolving paradigm for stem cell biology. Cell. 132, 631-644 (2008).
- Spradling, A., Drummond-Barbosa, D., Kai, T. Stem cells find their niche. Nature. 414, 98-104 (2001).
- Panoskaltsis, N., Mantalaris, A., Wu, D. Engineering a mimicry of bone marrow tissue ex vivo. J Biosci. Bioeng. 100, 28-35 (2005).
- Lo Celso, C. Live-animal tracking of individual haematopoietic stem/progenitor cells in their niche. Nature. 457, 92-96 (2009).
- Mantalaris, A., Bourne, P., Wu, J. Production of human osteoclasts in a three-dimensional bone marrow culture system. Biochem. Eng. J. 20, 189-196 (2004).
- Placzek, M. Stem cell bioprocessing: fundamentals and principles. J. R. Soc. Interface. 6, 209-232 (2009).
- Dexter, T., Testa, N., Prescott, D. . Methods in Cell Biology. 14, 387-405 (1976).
- Piacibello, W. Differential growth factor requirement of primitive cord blood hematopoietic stem cell for self-renewal and amplification vs proliferation and differentiation. Leukemia. 12, 718-727 (1998).
- Yoshida, T., Takagi, M. Cell processing engineering for ex vivo expansion of hematopoietic cells: a review. Biochemical Engineering Journal. 20, 99-106 (2004).
- Lim, M. Intelligent bioprocessing for haemotopoietic cell cultures using monitoring and design of experiments. Biotechnol. Adv. 25, 353-368 (2007).
- Mortera-Blanco, T., Mantalaris, A., Bismarck, A., Panoskaltsis, N. The development of a three-dimensional scaffold for ex vivo biomimicry of human acute myeloid leukaemia. Biomaterials. 31, 2243-2251 (2010).
- Mortera-Blanco, T., Mantalaris, A., Bismarck, A., Aqel, N., Panoskaltsis, N. Long-term cytokine-free expansion of cord blood mononuclear cells in three-dimensional scaffolds. Biomaterials. 32, 9263-9270 (2011).
- Safinia, L., Datan, N., Hohse, M., Mantalaris, A., Bismarck, A. Towards a methodology for the effective surface modification of porous polymer scaffolds. Biomaterials. 26, 7537-7547 (2005).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved