A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
Supramaximal פעילות גופנית בעצימות ובשפתיים והערכת תפקוד כלי הדם בעכברים
In This Article
Summary
אימון בעצימות גבוהה ב היפוקסיה הוא פרוטוקול כי הוכח לזירוז שעשוי להיות מועיל אצל חלק מהחולים וסקולרית עיבודים וכדי לשפר ספורטאים חזר על יכולת הריצה. כאן, אנו לבחון את הכדאיות של עכברים הדרכה באמצעות פרוטוקול, לזהות את אלה עיבודים לכלי הדם באמצעות ex-vivo הערכת תפקוד כלי הדם.
Abstract
תרגיל אימון הוא לאסטרטגיה חשובה לשמירה על הבריאות ולמניעת מחלות כרוניות רבות. . זה הקו הראשון של הטיפול המומלץ על ידי הנחיות בינלאומיות עבור חולים הסובלים ממחלות לב וכלי דם, ליתר דיוק, להפחית מחלות עורקים הגפיים, איפה יכולת ההליכה המטופלים היא שונה במידה ניכרת, המשפיעים על שלהם איכות החיים.
באופן מסורתי, פעילות גופנית רציפה נמוכה והן מרווח אימון שימשו. לאחרונה, supramaximal הכשרה גם הוכח לשפר הופעות ספורטאים באמצעות עיבודים לכלי הדם, בין מנגנונים אחרים. השילוב של סוג זה של אימון עם היפוקסיה יכול להביא השפעה נוספים ו/או הסינרגי, אשר יכול להיות עניין של פתולוגיות מסוימות. כאן, אנו נתאר כיצד לבצע הדרכות אינטנסיביות supramaximal ב היפוקסיה על עכברים בריאים לפחות 150% של המהירות המקסימלית שלהם, בעזרת הליכון ממונע ותיבת ובשפתיים. אנו גם מראים כיצד לנתח את העכבר כדי לאחזר את האיברים של עניין, במיוחד את עורק הריאה, העורק הראשי, העורק iliac. לבסוף, אנו מראים כיצד לבצע ex-vivo הערכת תפקוד כלי הדם על מכלי הדם שאוחזרו באמצעות מחקרים איזומטרי מתיחות.
Introduction
היפוקסיה, השבר בהשראת ירידה של חמצן (O2) מוביל ל hypoxemia (הוריד לחץ עורקי היפוקסיה) שינו O2 התחבורה קיבולת1. היפוקסיה חריפה מעוררת פעילות מוגברת מצר את כלי הדם סימפטי מופנה כלפי שרירי השלד2 ו vasodilatation 'פיצוי' מתנגד.
בעוצמה submaximal ב היפוקסיה, זו vasodilatation 'פיצוי', יחסית באותה הרמה של פעילות גופנית בתנאים normoxic, הוא וותיקה3. התרחבות זו חיונית כדי להבטיח זרימת דם מוגבר ותחזוקה של (או להגביל את שינוי) של אספקת החמצן לשרירים הפעילים. אדנוזין הוצגה אין תפקיד עצמאי בתגובה זו, בעוד תחמוצת החנקן (NO) נראה אנדותל המקור העיקרי מאז blunting משמעותית של vasodilatation מוגבר דווח עם תחמוצת החנקן עיכוב סינתאז (NOS) במהלך ובשפתיים תרגיל4. מספר חומרים vasoactive אחרים הם ככל הנראה תפקיד vasodilatation המפצה בתרגיל ובשפתיים.
Hyperemia זה התרגיל ובשפתיים משופרת פרופורציונליים היפוקסיה-induced לסתיו בתוכן2 עורקים O והוא גדול יותר כמו עליות עוצמת פעילות גופנית, לדוגמה במהלך פעילות גופנית אינטנסיבית מצטבר של היפוקסיה.
הרכיב בתיווך לא של vasodilatation המפצה מוסדר דרך מסלולים שונים עם הגדלת פעילות גופנית בעוצמה3: אם β adrenergic קולטן-מגורה אין רכיב מופיעה עליונה בתרגיל ובשפתיים בעוצמה נמוכה , המקור לא לתרום הרחבה הבולמוס נראה פחות תלויים במנגנוני β adrenergic כפי מגביר עוצמת פעילות גופנית. ישנם מועמדים אחרים ולשם עירור אין שחרור בתרגיל ובשפתיים בעצימות גבוהה יותר, כגון ATP שוחרר אריתרוציטים ו/או אנדותל-derived פרוסטגלנדינים.
Supramaximal תרגיל היפוקסיה (בשם אימון ריצה חוזרת ונשנית של היפוקסיה [RSH] בספרות לפיזיולוגיה תרגיל) היא האחרונה הכשרה בשיטה5 מתן שיפור ביצועים שחקנים או רעש-ספורט קבוצתי. שיטה זו שונה מרווח הכשרה היפוקסיה בנטילת או ליד למהירות מירבית6 (Vmax) מאז RSH בנטילת בעוצמה מירבית מוביל זלוף השריר גדול יותר, חמצון7 , תעתיק ספציפיים שרירים תגובות8. מספר מנגנונים הוצעו להסביר את האפקטיביות של RSH: במהלך ספרינטים של היפוקסיה, הבולמוס vasodilation ואת משויכת זרימת הדם גבוה יותר יהנו הסיבים במהירות עווית יותר מאשר הסיבים איטי עווית. כתוצאה מכך, יעילות RSH צפוי להיות סלקטיבי הסיבים מסוג ועוצמה התלויים. אנו משערים כי התגובה משופר של מערכת כלי הדם הוא בעל חשיבות עליונה ב- RSH.
תרגיל אימון נחקרה בהרחבה בעכברים, גם אצל אנשים בריאים וגם העכבר פתולוגיים מודלים9,10. הדרך הנפוצה ביותר לאלף עכברים הוא באמצעות ההליכון מכרסמים, משטר מסורתי שימשה הוא אימון בעצימות נמוכה, ב 40%-60% של Vmax (שנקבע באמצעות מבחן הליכון מצטבר11), במשך 30-60 דקות12,13 14, ,15. מרווח אימון אינטנסיביות מקסימלי והשפעתה על פתולוגיות נרחב נחקרו עכברים16,17; לכן, פותחו מרווח אימון ריצה פרוטוקולים עבור עכברים. פרוטוקולים אלה מורכבות בדרך כלל כ-10 התקפי פועל ב 80%-100% של Vmax על הליכון ממונע מכרסמים, ' מזערי ' 1 – 4, וביניהם מנוחה פסיבית או אקטיבית16,18.
הריבית בעכברים פעילות גופנית בעוצמה supramaximal (קרי, מעל Vmax) ב היפוקסיה נובע תוצאות קודמות כי הפיצוי vasodilatory microvascular את הביצועים תרגיל לסירוגין הן יותר מוגבר- supramaximal מאשר על עוצמות מקסימלי או בינונית. עם זאת, הידע שלנו, יש אין הדו ח הקודם של פרוטוקול אימונים supramaximal בעכברים, גם normoxia או היפוקסיה.
המטרה הראשונה של המחקר הנוכחי הייתה לבחון את הכדאיות של supramaximal עוצמת האימון בעכברים ובבני הקביעה של פרוטוקול נסבל והולם (בעוצמה, משך הריצה, שחזור, וכו '.). המטרה השנייה הייתה להעריך את ההשפעות של אימון שונים משטר normoxia, היפוקסיה על הפונקציה כלי הדם. לכן, אנו לבחון את ההשערות (1) עכברים לסבול טוב supramaximal תרגיל היפוקסיה ומשרה (2) פרוטוקול זה שיפור גדול יותר בתפקוד כלי הדם מאשר תרגיל normoxia, אלא גם מאשר תרגיל היפוקסיה-בעוצמות נמוכות.
Protocol
הוועדה המקומית של המדינה טיפול בבעלי חיים (שירות de la Consommation et des המלון Vétérinaires [SCAV], לוזאן, שווייץ) אישר כל ניסויים (אישור VD3224; 01.06.2017) כל הניסויים בוצעו בהתאם הרלוונטי הנחיות ותקנות.
1. בעלי חיים דיור והכנות
- בית 6 זכר-לעכברים 8 של בת שבוע C57BL/6J, במתקן בבעלי חיים לפחות שבוע אחד לפני תחילת הניסויים על מנת העכברים להתרגל תנאי הדיור החדש שלהם. מטעמים פרקטיים, עכברים של קבוצת הניסוי אותו בדרך כלל שוכנות יחדיו.
- לשמור את העכברים בחדר מבוקרי טמפרטורה (22 ± 1 ° C) עם מחזור/כהה 12 שעות עם גישה ad libitum מזון ומים.
2. קביעת הערכה סטנדרטיים של שיפור ביצועים על-ידי. הבדיקה על ההליכון מצטבר ומהירות מירבית
הערה: השלבים הבאים הם קריטיים להשלמת הפרוטוקולים הכשרה.
- להשתמש הליכון ממונע עבור עכברים ניתן על נתיבים רבים לצד השני, עם נטייה 0° ואיפה רכוב עם רשת החשמל עכברים מוגדר כ- 0.2 mA בקצה השביל, על מנת לעודד את העכברים לפעול.
-
לפני המבחן הראשון, להגיש העכברים 4 ימים של הסתגלות על ההליכון, לפי הפרוטוקול הבא.
- יום 1, יש עכברים לרוץ 10 דקות ב- 4.8 מיליון/דקה.
- יום 2, יש העכברים לרוץ 10 דקות ב- 6 מטר/דקה.
- יום 3, יש העכברים לרוץ 10 דקות במהירות 7.2 m/min.
- יום 4, יש העכברים לרוץ 10 דקות ב- 8.4 מ'/דקה.
-
יום 5, להגיש עכברים מבחן מצטבר עד כדי אפיסת כוחות, לפי הפרוטוקול הבא.
- תן העכברים מתחממת 5 דקות ב- 4.8 מיליון/דקה (נטייה 0 °).
- להגדיל את המהירות של 1.2 מ' לדקה כל 3 דקות (למשל, 5 דקות ב- 4.8 מיליון/דקה, ואז 3 דקות ב- 6 מטר/דקה, 3 דקות ב- 7.2 m/דקה, 3 דקות ב- 8.4 מ'/min, וכו ') עד תשישות, אשר הגיע כאשר העכבר מקדיש גם 3 שניות רצופות רשת החשמל או מקבל 100 זעזועים (מוצג על ידי המנגנון).
- תרשום מהירות מושגת (נחשב את Vmax), משך זמן, מרחק, מספר בולמי זעזועים, הזמן הכולל שהושקע הרשת.
הערה: בדרך כלל, Vmax היה 28.8 ± 3.7 m/min. - באמצע אימון, שלח שוב עכברים הבדיקה על מנת להסתגל המהירויות של הדרכה מעודכן Vמקסימום של העכברים (למשל, אם פרוטוקול אימונים נמשך כשמונה שבועות, ולאחר מכן לבצע בדיקה מצטבר באמצע אימון ב- 4 שבועות. במקרה הזה, להחליף לאחד הדרכות סדירות על ידי המבחן), את כל-כך שוב בסוף המחקר כדי להעריך שיפורי ביצועים.
- ליישם את תקופת מנוחה 48 שעות לפני ואחרי בדיקה זו.
הערה: כל הבדיקות מצטבר בוצעו בבוקר.
3. חמצן בסביבה
- על ההדרכות על היפוקסיה, למקם את ההליכון בתיבת ובשפתיים (איור 1) קשורה מערבל גזים. השתמש oximeter מכויל לשלוט באופן קבוע השבר הסביבתית של חמצן (F. אניO2 [קרי, הרמה של היפוקסיה]) בתיבה.
- להגדיר את המיקסר גז ב- 100% של חנקן (N2) ולהשתמש דופק לבדוק את רמת של היפוקסיה. פעם FאניO2 = 0.13, לשנות את הפרמטר של המיקסר גז מ- 100% N2 ל- 13% O2.
- על מנת להימנע משהייה ממושכת פסיבי היפוקסיה, מקום העכברים בכלוב קטן זמני עם המלטה והעשרה, ומניחים במהירות אותו בתיבה פעם FאניO2 = 0.13 הגיעה. ודא כי הסביבה היא עדיין אצל 13% O2 אחרי ששמתי בכלוב; אם לא, להסתגל לזה.
- בקביעות לוודא שרמת O2 במהלך אימון כדי לוודא שהוא נשאר-FiO2 = 0.13 ± 0.002.
4. Normoxic הסביבה
- ההדרכות על normoxia, לשמור על ההליכון בתיבת שתקבעו, אלא להסיר את הכפפות, כך יש אויר (F. אניO2 = 0.21). המטרה היא ליצור מחדש באותה סביבה אימון כמו העכברים ב היפוקסיה.
5. Supramaximal עוצמת האימון
-
במקום העכברים על נתיבים נפרדים ההליכון (על נטייה 0°) ולהגיש אותם בפרוטוקול הבא.
- יש עכברים מתחממת 5 דקות ב- 4.8 מיליון/דקה, ואחריו 5 דקות ב- 9 מטר/דקה.
- הגדר את המהירות של ספרינטים 150% נחושה בעבר Vmax.
הערה: בדרך כלל, מהירות הריצה היה 42.1 ± 5.5 מ'/min. - הרכבת העכברים על ארבע קבוצות של 5 x 10 ספרינטים s עם 20 s של מנוחה בין כל ספרינט. השאר interset הוא 5 דקות (איור 2).
הערה: הוסף תקופה cooldown אם עומס העבודה הכולל של האימון עצמו צריך תואם לזה של קבוצת הכשרה נוספת.
- לבצע אימון x 3 בשבוע, עם רצוי 48 שעות בין אימון ההפעלות.
- השתמש ספוגיות כותנה כשיטה המשלימה כדי מכות חשמל כדי לעודד העכברים לפעול. הכנס חתך בחלק העליון של השביל, בין העכבר את רשת החשמל, ספוגית כותנה, להסיט בעדינות את העכבר כאשר הוא מגיע האחורי של ההליכון. זה למנוע המסירה של מכות חשמל, לעורר את העכברים לפעול בצורה רכה יותר.
6. בעוצמה נמוכה הכשרה
-
במקום העכברים על נתיבים נפרדים ההליכון (על נטייה 0°) ולהגיש אותם בפרוטוקול הבא.
- יש עכברים מתחממת 5 דקות ב- 4.8 מיליון/דקה, ואחריו 5 דקות ב- 7.2 m/דקה.
- הגדר את מהירות ההפעלה ריצה רציפה 40% נחושה בעבר Vmax.
הערה: בדרך כלל, מהירות ריצה רציפה היה 9.9 מ/דקה. - הרכבת העכברים למשך 40 דקות.
- לבצע אימון 3 x בשבוע עם רצוי 48 שעות בין אימון ההפעלות.
- השתמש ספוגיות כותנה כשיטה המשלימה כדי מכות חשמל כדי לעודד העכברים לפעול.
7. עכברים המתת חסד והפקת איברים
- בקצה של פרוטוקול אימונים, לפחות 24 שעות לאחר הבדיקה האחרונה מצטבר, עזים ומתנגד העכבר תא אינדוקציה באמצעות איזופלוריין (4% – 5% O2 כדי לגרום הרדמה, ו 1% – 2% 100% O2 כדי לשמור על הרדמה). לאשר ההרדמה המתאים באמצעות את רפלקס הכחשה של כף הרגל (בחוזקה קמצוץ כפת של החיה; ההרדמה נחשב תקין כאשר החיה אינו מגיב לגירויים).
- באמצעות מחט 25 גרם, לבצע ניקוב לב מלעורית, כדי לאסוף את נפח הדם המרבית כפי שתואר לעיל19.
- לבצע תאמת צוואר הרחם ולהסיר את העור של העכבר על ידי לחתוך השכבה הראשונה של העור על הבטן עם המספריים-סיבוב ומושך על שני הצדדים של החתך (לכיוון הראש, הזנב).
- לחתוך הצפק תחת קשת הצלעות בצד שמאל של העכבר במספריים דק-נקודת-טיפ כדי להגיע הטחול, לחלץ אותו במידת הצורך.
הערה: שווייץ השרירים במידת הצורך. -
שווייץ עורק הריאה.
- בעזרת מספריים קטנות וגם מלקחיים, להסיר את כלוב בית החזה ונקה את אזור לב-ריאה.
- עם פינצטה "עצמי הסגירה", לצבוט את הלב קרוב ככל האפשר איפקס, משוך בעדינות כדי למתוח את הבסיס ושל קשת אבי העורקים ועורק הריאה.
- בעזרת יד ימין, פינצטה מעוקל הוספה תחת לחץ הדם יורד אבי העורקים לבין אז לעבור הפינצטה בחזרה קצת להחזיק רק את עורק הריאה (איור 3).
- להשתמש ביד שמאל כדי להוסיף עוד זוג מלקחיים כדי להחליף את אחד שנערך עם יד ימין.
- שימוש microscissors ישר חדים בכף יד ימין, לנתח את עורק הריאה כמו בלב ככל האפשר על צד אחד, ולא רחוק ככל האפשר בצד השני.
הערה: לא משנה באיזו יד מחזיקה בכלי אילו, אמנם אנחנו מצאנו אותה קל יותר לחתוך עם יד ימין מאשר עם השמאל. - מכניסים אותו צינור 2 מ"ל עם קר מאגר מלוחים באגירה פוספט (PBS) ולשמור על קרח.
-
ביצוע של זלוף לכל הגוף.
- בחלק העליון של האיבר הימני התחתון של העכבר, השתמש פינצטה כדי לנקות את העורק iliac פנימי-חיצוני עד הירך נכון (תחת רצועה במפשעה). שימוש microscissors ישר חדה, גורם חתך מלאה בעורק הירך.
- הוספת מזרק 25 G מ ל מלא PBS קר החדר השמאלי של הלב, בעדינות להחדיר את PBS קר כדי להסיר את הדם שנותרו בכלי הדם.
הערה: בעקבות הפקת עורק הריאה, זה אפשרי PBS הפיצו לא עד הסוף החתך.
- באמצעות פינצטה, הסר את הרקמות הרכות שמסביב העורקים של הרצועות מפשעי ישר ושמאלה אל הלב יסודי ככל האפשר.
הערה: הלב ניתן לחלץ לניתוח נוסף במידת הצורך. - באמצעות פינצטה והן microscissors, שווייץ בלב עד לנקודה הנמוכה ביותר של העורק iliac חיצוני (ב הגפיים שמאלה וימינה) ומניחים את המקטע כולו גזור-אאוט בצלחת 10 ס מ קוטר עם PBS קר.
- באמצעות פינצטה ו/או microscissors, לסיים לנקות את השמן הנותר סביב אבי העורקים העורקים על ידי בעדינות משיכה או חיתוך זה מן כלי.
- שימוש microscissors, חותכים את העורק השמאלי iliac ההסתעפות עורק iliac משמאל ואחסן אותו לצורך ניתוח נוסף.
- שימוש microscissors, לחתוך את העורק הראשי תחת העורק הכליה השמאלית, הניחו את כלי הקיבול שחולצו במאגר PBS קר על קרח (איור 4).
- לשמור על הספינה נקי הנותרים, קשת אבי העורקים לימין מעל עורק הכליה השמאלית, אחסון לניתוח נוסף.
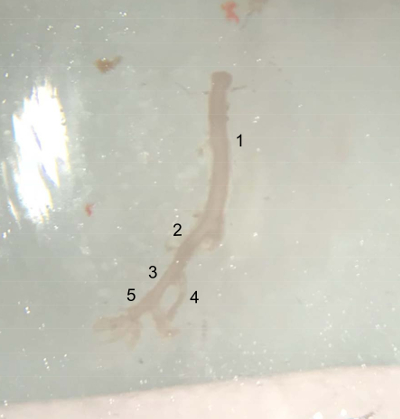
איור 4 : תמונה של כלי ניתוח. ספינת חילוץ מהחלק העליון של אבי העורקים בבטן (מתחת עורק הכליה השמאלית) לקצה של העורק iliac נכון, מוכנים להניח במאגר PBS קר על קרח. (1) Abdominal העורקים. עורק iliac משותף (2) נכון. (3) חיצוני iliac העורק. (4) פנימית iliac העורק. (5) בעורק הירך. אנא לחץ כאן כדי להציג גירסה גדולה יותר של הדמות הזאת.
8. ex-Vivo הערכת תפקוד כלי הדם
הערה: שטיפה מקביל כדי לרוקן ואת מילוי מחדש של התאים עם קרבס.
- על פי פרוטוקול שתואר לעיל20, חתך את עורק הריאה מבודד. העורק הראשי, עורק iliac מקטעי לטבעות כלי הדם של 1.0-2.0 מ מ אורך והר כל טבעת על שני 0.1 מ מ קוטר stirrups עברו לומן.
- להשעות את הטבעות כלי בתאי איברים אנכי מלא 10 מ"ל של קרבס-צלצול שונה ביקרבונט פתרון (118.3 מ מ NaCl, 4.7 מ מ אשלגן כלורי, 2.5 מ מ CaCl2, 1.2 מ מ MgSO4,2PO 1.2 מ מ ח'4, 25.0 מ"מ NaHCO3ו- 11.1 מ מ גלוקוז) שמרו ב 37 מעלות צלזיוס, מוגזים עם 95% O2-5% CO2 (pH 7.4). ארכוף אחת מעוגנת לחלק התחתון של החדר אורגן, השני מחובר לאמוד זן לשקילת כוח איזומטרי גרמים.
- להביא את כלי השיט שלהם מתח המנוחה אופטימלית: למתוח את הטבעות כדי 0.5 g עבור עורק הריאה, 1.5 g עבור העורק iliac ו- g 2 עבור העורק הראשי, ולשטוף אותם אחרי תקופה 20 דקות של equilibration. חזור על המתיחה-equilibration-לשטוף את השלבים 1 x.
- כדי לבדוק את הכדאיות של כלי, חוזה את הטבעות עם 235 µL של אשלגן כלורי (10-1 מ') למשך 10 דקות, לשטוף אותם עוד 10 דקות, ולכווץ שוב עם 235 µL של אשלגן כלורי (10-1 מ') במשך כ 20 דקות עד שהגיע מישור.
- לשטוף את כלי הדם שוב למשך 10 דקות ולהוסיף 58.4 µL של indomethacin (10-5 מ') (מעכב פעילות cyclooxygenase) לפחות 20 דקות על מנת למנוע הפרעות אפשריות של prostanoids אנדוגני.
- להוסיף מינונים מצטברים של phenylephrine (Phe) מ- 10-9 (10 µL) 10-4 מ' (או 10-9 עד 10-5 מ' עבור עורק ריאתי; µL 9 עבור כל ריכוזי מעל 10-9 מ') כדי לכווץ את כלי הדם.
- לאחר המנה האחרונה של Phe, חכו בערך 1 h עד כלי להגיע למצב יציב יחסית התכווצות (plateau).
- להוסיף מינונים מצטברים של אצטילכולין אנדותל תלוית מרחיב כלי דם (ACh), מ- 10-9 עד 10-4 מ' (µL 58.4 עבור 10-9 מ', ו לסירוגין 12.6 µL, µL 40 עבור כל ריכוזי מעל 10-9 מ'), כדי לעודד חנקתית אוקסיד (NO)-מתווכת הרפיה.
- בקצה של העקומה הרפיה, לשטוף את כלי הדם למשך 10 דקות, ולהוסיף 58.4 µL של indomethacin (10-5 מ'), וכן µL 184 של NG-ניטרו-L-ארגנין (NLA, 10-4 מ'), אשר הוא מעכב של ערימה, למשך 20 דקות לפחות.
- חוזה בכלי הדם שוב עם מנה ייחודית של µL 10 של Phe (10-5 , 10-4 M עבור עורק הריאה, 10-4 M עבור העורק והעורק iliac) לשעה לזירוז התכווצות יציב יחסית.
- להוסיף מנה ייחודית של µL 40 של ACh (10-4 מ') עד שהגיע מישור.
- לשטוף את כלי הדם שוב למשך 10 דקות, לפני הוספת 58.4 µL של indomethacin (10-5 מ'), 184 µL ה-NLA (10-4 מ') במשך 20 דקות.
- חוזה בכלי עם µL 10 של Phe (10-5 , 10-4 מ') לשעה.
- להוסיף מינונים מצטברים (10-9 [58.4 µL] כדי 10-4 מ' [40 µL עבור כל ריכוזי מעל 10-9 מ']) את לא תורם diethylamine (DEA) / לא, ב סדר כדי להעריך הרפיה לא-induced אנדותל-עצמאית.
- בסוף הניסוי, לאחסן בכלי הדם חנקן נוזלי עבור שניתוח במידת הצורך.
תוצאות
לידע שלנו, המחקר הנוכחי הוא הראשון לתאר את תוכנית של supramaximal עוצמת האימון ב- normoxia וב -היפוקסיה עבור עכברים. פרוטוקול זה, עכברים רצו ארבע קבוצות של 10 5 s ספרינטים עם החלמה s 20 בין כל ספרינט. הכסאות היו בשריקות 5 דקות של תקופות התאוששות. זה היה לא ידוע אם העכברים ניתן לשמר פרוטוקו?...
Discussion
המטרה הראשונה של מחקר זה היה כדי להעריך את הכדאיות של אימון בעצימות גבוהה ובשפתיים בעכברים וכדי לקבוע את המאפיינים נאותה של פרוטוקול זה להיות נסבל היטב על ידי עכברים. בכוונה, כיוון שאין נתונים באמצעות supramaximal (קרי, יותר מאשר Vmax) עוצמת האימון בעכברים, נאלצנו לבצע ניסויים על סמך הפרוטוק?...
Disclosures
המחברים אין לחשוף.
Acknowledgements
המחברים רוצה להודות דנילו Gubian, סטפן Altaus מבית חולים אוניברסיטת לוזאן (CHUV) המלאכה מכני שעזרת ליצור את תוכנית ההתקנה ובשפתיים. המחברים רוצה גם להודות Macabrey דיאן, מלאני Sipion על עזרתם באימון בעלי החיים.
Materials
| Name | Company | Catalog Number | Comments |
| Cotton swab | Q-tip | ||
| Gas mixer Sonimix 7100 | LSI Swissgas, Geneva, Switzerland | Gas-flow: 10 L/min and 1 L/min for O2 and CO2, respectively | |
| Hypoxic Box | Homemade | Made in Plexiglas | |
| Motorized rodents treadmill Panlab LE-8710 | Bioseb, France | ||
| Oximeter Greisinger GOX 100 | GREISINGER electronic Gmbh, Regenstauf, Germany | ||
| Sedacom software | Bioseb, France | ||
| Strain gauge | PowerLab/8SP; ADInstruments |
References
- Calbet, J. A., et al. Determinants of maximal oxygen uptake in severe acute hypoxia. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology. 284 (2), 291-303 (2003).
- Hanada, A., Sander, M., González-Alonso, J. Human skeletal muscle sympathetic nerve activity, heart rate and limb haemodynamics with reduced blood oxygenation and exercise. The Journal of Physiology. 551, 635-647 (2003).
- Casey, D. P., Joyner, M. J. Compensatory vasodilatation during hypoxic exercise: mechanisms responsible for matching oxygen supply to demand. The Journal of Physiology. 590 (24), 6321-6326 (2012).
- Casey, D. P., et al. Nitric oxide contributes to the augmented vasodilatation during hypoxic exercise. The Journal of Physiology. 588, 373-385 (2010).
- Girard, O., Brocherie, F., Millet, G. P. Effects of Altitude/Hypoxia on Single- and Multiple-Sprint Performance: A Comprehensive Review. Sports Medicine. 47 (10), 1931-1949 (2017).
- Faiss, R., Girard, O., Millet, G. P. Advancing hypoxic training in team sports: from intermittent hypoxic training to repeated sprint training in hypoxia. British Journal of Sports Medicine. 47, 45-50 (2013).
- Brocherie, F., Girard, O., Faiss, R., Millet, G. P. Effects of Repeated-Sprint Training in Hypoxia on Sea-Level Performance: A Meta-Analysis. Sports Medicine.(Auckland, N.Z). 47 (8), 1651-1660 (2017).
- Brocherie, F., et al. Repeated maximal-intensity hypoxic exercise superimposed to hypoxic residence boosts skeletal muscle transcriptional responses in elite team-sport athletes. Acta Physiologica. 222 (1), 12851 (2018).
- Pellegrin, M., et al. New insights into the vascular mechanisms underlying the beneficial effect of swimming training on the endothelial vasodilator function in apolipoprotein E-deficient mice. Atherosclerosis. 190 (1), 35-42 (2007).
- Picard, M., et al. Acute exercise remodels mitochondrial membrane interactions in mouse skeletal muscle. Journal of Applied Physiology. 115 (10), 1562-1571 (2013).
- Ayachi, M., Niel, R., Momken, I., Billat, V. L., Mille-Hamard, L. Validation of a Ramp Running Protocol for Determination of the True VO2max in Mice. Frontiers in Physiology. 7, (2016).
- Pellegrin, M., et al. Running Exercise and Angiotensin II Type I Receptor Blocker Telmisartan Are Equally Effective in Preventing Angiotensin II-Mediated Vulnerable Atherosclerotic Lesions. Journal of Cardiovascular Pharmacology and Therapeutics. 22 (2), (2016).
- Semin, I., Acikgöz, O., Gönenc, S. Antioxidant enzyme levels in intestinal and renal tissues after a 60-minute exercise in untrained mice. Acta Physiologica Hungarica. 88 (1), 55-62 (2001).
- Cho, J., et al. Treadmill Running Reverses Cognitive Declines due to Alzheimer Disease. Medicine & Science in Sports & Exercise. 47 (9), 1814-1824 (2015).
- Schill, K. E., et al. Muscle damage, metabolism, and oxidative stress in mdx mice: Impact of aerobic running. Muscle & Nerve. 54 (1), 110-117 (2016).
- Cho, J., Kim, S., Lee, S., Kang, H. Effect of Training Intensity on Nonalcoholic Fatty Liver Disease. Medicine & Science in Sports & Exercise. 47 (8), 1624-1634 (2015).
- Sabatier, M. J., Redmon, N., Schwartz, G., English, A. W. Treadmill training promotes axon regeneration in injured peripheral nerves. Experimental Neurology. 211 (2), 489-493 (2008).
- Rolim, N., et al. Aerobic interval training reduces inducible ventricular arrhythmias in diabetic mice after myocardial infarction. Basic Research in Cardiology. 110 (4), 44 (2015).
- Lab Animal Research. Blood Withdrawal I. JoVE Science Education Database Available from: https://www.jove.com/science-education/10246/blood-withdrawal-i (2018)
- Peyter, A. -. C., et al. Muscarinic receptor M1 and phosphodiesterase 1 are key determinants in pulmonary vascular dysfunction following perinatal hypoxia in mice. American Journal of Physiology-Lung Cellular and Molecular Physiology. 295 (1), 201-213 (2008).
- Faiss, R., et al. Significant Molecular and Systemic Adaptations after Repeated Sprint Training in Hypoxia. PLOS ONE. 8 (2), (2013).
- Faiss, R., et al. Repeated Double-Poling Sprint Training in Hypoxia by Competitive Cross-country Skiers. Medicine & Science in Sports & Exercise. 47 (4), 809-817 (2015).
- Billat, V. L., Mouisel, E., Roblot, N., Melki, J. Inter- and intrastrain variation in mouse critical running speed. Journal of Applied Physiology. 98 (4), 1258-1263 (2005).
- Ferguson, S. K., et al. Effects of living at moderate altitude on pulmonary vascular function and exercise capacity in mice with sickle cell anemia. The Journal of Physiology. , (2018).
- Lightfoot, J. T., Turner, M. J., Debate, K. A., Kleeberger, S. R. Interstrain variation in murine aerobic capacity. Medicine & Science in Sports & Exercise. 33 (12), (2001).
- Wojewoda, M., et al. Running Performance at High Running Velocities Is Impaired but V'O2max and Peripheral Endothelial Function Are Preserved in IL-6-/- Mice. PLOS ONE. 9 (2), (2014).
- Muller, C. R., Américo, A. L. V., Fiorino, P., Evangelista, F. S. Aerobic exercise training prevents kidney lipid deposition in mice fed a cafeteria diet. Life Sciences. 211, 140-146 (2018).
- Petrosino, J. M., et al. Graded Maximal Exercise Testing to Assess Mouse Cardio-Metabolic Phenotypes. PLOS ONE. 11 (2), 0148010 (2016).
- Poole, D. C., Jones, A. M. Oxygen Uptake Kinetics. Comprehensive Physiology. , (2012).
- Copp, S. W., Hirai, D. M., Musch, T. I., Poole, D. C. Critical speed in the rat: implications for hindlimb muscle blood flow distribution and fibre recruitment. The Journal of Physiology. 588, 5077-5087 (2010).
- Kregel, K., et al. . Resource Book for the Design of Animal Exercise Protocols. , (2006).
- Lamy, S., et al. Air puffs as refinement of electric shocks for stimulation during treadmill exercise test. The FASEB Journal. 30, 1014 (2016).
- Koenen, K., et al. Sprint Interval Training Induces A Sexual Dimorphism but does not Improve Peak Bone Mass in Young and Healthy Mice. Scientific Reports. 7, (2017).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved