A subscription to JoVE is required to view this content. Sign in or start your free trial.
Method Article
פיתוח ואפיון של סרט הידרוג'ל מבוסס אלגינט-אלוורה עמוס חומצה פוסידית
In This Article
Summary
פורמולה של סרט הידרוג'ל עמוס חומצה פוסידית פותחה עם יחסי אלוורה שונים ואופיינה במחקר זה.
Abstract
סרט הידרוג'ל חדש עמוס חומצה פוסידית הוכן בטכניקת יציקת הממס באמצעות אלגינט ואלוורה. סרטי ההידרוג'ל עברו אופטימיזציה באמצעות יחסים שונים של נתרן אלגינט, אלוורה וגליצרין. הסרטים המכילים 10% גליצרין (w/w של אלגינט) הציגו את המראה הטוב ביותר. שילוב אלוורה השפיע על העובי, התנהגות הנפיחות, חדירות אדי המים ופרופיל שחרור התרופות של סרטי ההידרוג'ל. תכולת אלוורה גבוהה יותר הביאה ליריעות עבות יותר (עד יחס מסוים), נפיחות מוגברת, חדירות אדי מים מופחתת ושחרור ממושך של תרופות של עד 93% במשך 12 שעות. ניתוח ספקטרוסקופיה אינפרא אדום של טרנספורמציה פורייה (FTIR) אישר את נוכחותן של קבוצות פונקציונליות מרכזיות ואת האינטראקציה בין רכיבי ההידרוג'ל. המחקר מצביע על כך שהשילוב של נתרן אלגינט, אלוורה וגליצרין יכול לשפר את התכונות המכניות ופרופילי שחרור התרופות של סרטי הידרוג'ל, מה שהופך אותם לאופציה מבטיחה לאספקת תרופות מקומיות משופרות ויישומי ריפוי פצעים.
Introduction
חומצה פוסידית היא אנטיביוטיקה סטרואידית עוצמתית המופקת מ-Fusidium coccineum. הוא נמצא בשימוש נרחב לטיפול בזיהומי עור סטפילוקוקליים ואימפטיגו. לתרופה זו יעילות גבוהה, אפילו נגד זנים עמידים לאנטיביוטיקה, ורעילות נמוכה, מה שהופך אותה לאופציה מתאימה לניהול זיהומי עור1. בניגוד לאנטיביוטיקה מקומית אחרת, חומצה פוסידית חודרת עמוק לתוך העור ומגבירה את ההשפעות האנטי-בקטריאליות שלה, במיוחד באזורים שבהם מחסום ההגנה של העור נפגע. המבנה שלו מאפשר מאפייני מסיסות מגוונים, המאפשרים פיזור נרחב בכל רקמות הגוף, אשר משופר עוד יותר בצורת הנתרן פוסידאט שלו למסיסות טובה יותר במים ושיעורי חדירה טובים יותר 2,3. ניתן לתת חומצה פוסידית בדרכים שונות, כולל דרך הפה, דרך הווריד ובאופן מקומי, תוך התאמה לצרכי טיפול שונים והפיכתה לבחירה גמישה לזיהומים שונים4.
הידרוג'לים, עם תכולת המים הגבוהה והתאימות הביולוגית שלהם, התגלו כנשאים חדשניים לאנטיביוטיקה בטיפול בפצעים, מספקים שימור לחות, שחרור תרופות מבוקר ותוצאות משופרות למטופלים. הם עשויים מפולימרים טבעיים או סינתטיים כמו אלגינט, המועדף בשל התאימות הביולוגית החזקה שלו, במחיר סביר ותכונות הג'לציה המחקות מטריצות חוץ-תאיות של רקמות טבעיות5. הידרוג'לים על בסיס אלגינט, במיוחד, מציעים סביבה לחה התורמת לריפוי פצעים, אינם נדבקים לפצע ומאפשרים הסרה קלה, מה שהופך אותם לאידיאליים לאספקת חומרים ביו-אקטיביים ותמיכה בהתחדשות רקמות. הפיתוח של הידרוג'לים המכילים אנטיביוטיקה מייצג התקדמות משמעותית בטיפול בפצעים, ומבטיח מתן תרופות ממוקד והשפעות טיפוליות מתמשכות 6,7.
הידרוג'ל האלגינט/אלוורה המוצע בחומצה פוסידית נועד להתגבר על אתגרי המסיסות של חומצה פוסידית ולשפר את החדירה העורית שלה. אלוורה, הידועה בתכונותיה הידידותיות לעור, הלחות והאנטיבקטריאליות, משמשת גם כמשפר חדירה כימית, מה שעשוי לשפר את יעילותה של חומצה פוסידית בטיפול בזיהומי עור 8,9. נוסחה חדשנית זו ממנפת את ההשפעות הסינרגטיות של אלוורה ואלגינט הידרוג'ל כדי ליצור סביבת ריפוי תומכת, לייעל את אספקת התרופות ולהציע פתרון מבטיח לטיפול משופר בזיהומי עור, תוך הפקת המרב מהפעילות האנטי-מיקרוביאלית העוצמתית של חומצה פוסידית עם תוצאות אספקה וריפוי משופרות10.
Protocol
פרטי הריאגנטים והציוד המשמשים במחקר זה מפורטים בטבלת החומרים.
1. הכנת סרטי הידרוג'ל חומצה פוסידית
- הכינו תמיסות של נתרן אלגינט (2.0% w/v) ואלוורה (1.0% w/v) על ידי המסתם במים מזוקקים.
- מוסיפים 200 מ"ג חומצה פוסידית לתמיסת הנתרן אלגינט ומערבבים במשך שעה.
- הוסיפו גליצרול לתמיסת האלגינט בריכוזים של 10%, 12% ו-14% (w/w, בהתבסס על מסת האלגינט).
- שלבו את תמיסות האלגינט והאלוורה כדי להשיג יחסי אלגינט/אלוורה סופיים (v/v) של 100:0, 90:10, 80:20 ו-75:25.
- יוצקים 25 מ"ל מכל תערובת לצלחות פטרי זכוכית (100 מ"מ על 20 מ"מ) ומניחים לייבוש בטמפרטורת החדר (25 מעלות צלזיוס) ולחות מבוקרת (50%) למשך יומיים.
- טבלו את הסרטים המיובשים בתמיסה מימית של סידן כלורי (CaCl2) (5.0% w/v) למשך 5 דקות כדי להשיג את סרטי ההידרוג'ל.
- שוטפים את הסרטים המתקבלים במים מזוקקים ומייבשים אותם בטמפרטורת החדר לפני השימוש.
2. קביעת עובי הסרט
- השתמש במיקרומטר דיגיטלי כדי למדוד את עובי הסרט11.
- בצעו מדידות בחמש נקודות נפרדות לאורך הסרט.
- רשום את המדידות המתקבלות מכל נקודה.
- חשב את עובי הסרט הממוצע על סמך המדידות שבוצעו.
3. קביעת מדד הנפיחות
- חותכים את דגימות הסרט לריבועים בגודל 2 ס"מ על 2 ס"מ בעזרת סכין מעבדה.
- שקלו כל דגימה במדויק.
- משרים את הדגימות במאגר PBS (pH 6.8) בטמפרטורת החדר למשך 24 שעות.
- ספוג עודפי מים על משטח הסרט באמצעות נייר פילטר.
- שקלו שוב את הדגימות.
- שקלו את הסרטים במרווחי זמן שונים. חשב את קיבולת הנפיחות באמצעות המשוואה הבאה:
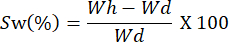
הערה: Wh מייצג את המשקל המיובש של הדגימה, ו-Wd מתאים למשקל היבש של הדגימה.
4. בדיקת חדירות אדי מים או חסימה
- מכסים את פתח זכוכית המכילה 50 מ"ל מים בנייר סינון11.
- החל תמיסה ליצירת סרט על אחד הניירות ואפשר לו לפתח סרט.
- אחסן את הכוס בטמפרטורת החדר ולחות.
- העריכו את חדירות הסרט למים על סמך הירידה במשקל המים בתוך הכוס.
- כדי לקבוע את הערכת חדירות אדי המים לסרט ההידרוג'ל המוכן, השתמש בנוסחה הבאה:
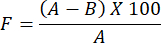
הערה: מקדם החסימה, F, מודד את החדירות של סרט. זה נקבע על ידי חישוב ההבדל במשקל המים בין זכוכית מכוסה בנייר פילטר ללא סרט לבין זכוכית מכוסה בנייר פילטר המצופה בסרט. ערך מקדם חסימה קטן יותר מצביע על חדירות סרט גדולה יותר.
5. ספקטרוסקופיה אינפרא אדום טרנספורמציה פורייה (FTIR)
- הנח את דגימת ההידרוג'ל על גביש ה-ATR של מכונת הספקטרוסקופיה FTIR.
- הגדר את טווח מספרי הגל ל-4000-400 ס"מ-1.
- הגדר את קצב הסריקה ל-60 סריקות לכל דגימה.
- הגדר את הרזולוציה ל-4 ס"מ-1.
- הקלט רקע אוויר לפני כל הפעלת דגימה.
- הפעל את הניתוח עבור כל דגימת הידרוג'ל בנפרד.
- נתח את ספקטרום ה-FTIR עבור כל דגימת הידרוג'ל כדי לאשר קבוצות פונקציונליות ולבחון אינטראקציות בין כל הרכיבים12.
- חזור על הניתוח עבור אלוורה גולמית, נתרן אלגינט, גליצרין וחומצה פוסידית בנפרד.
6. קלורימטריית סריקה דיפרנציאלית (DSC)
- השתמש במכשיר ניתוח תרמי זמין מסחרית כדי לרכוש פרופילים תרמיים.
- צור את דגימות המדידה ממספר חתיכות עגולות שנחתכו מסרט הפולימר.
- בדוק את טווח הטמפרטורות בין 25-230 מעלות צלזיוס.
- הגדר את קצב החימום/קירור על 20 מעלות צלזיוס לדקה.
- בצע כיול טמפרטורה ואנתלפיה באמצעות אינדיום סטנדרטי עם תוכנה תואמת.
7. מבחן שחרור סמים
- הכן תמיסה של 50 מ"ל PBS (pH = 7.4) כמדיום הפירוק.
- טבלו את סרטי ההידרוג'ל ב-PBS ב-37 מעלות צלזיוס למשך 24 שעות תוך ערבוב בקצב של 50 סל"ד.
- במרווחי זמן קבועים מראש, אספו 2 מ"ל מהדגימות.
- מדללים ומסננים את הדגימות שנאספו דרך פילטר מזרק.
- חדש מיד נפח שווה ערך של PBS.
- להעריך את ריכוזי החומצה הפוסידית המשתחררת באמצעות ספקטרופוטומטר UV, המודד ספיגה ב-285 ננומטר.
- הערך את קינטיקה השחרור של חומצה פוסידית באמצעות מודלים מסדר אפס, מסדר ראשון, היגוצ'י וקורסמאייר-פפאס4.
תוצאות
הכנת סרט הידרוג'ל אלגינט/אלוורה
יחסים שונים של נתרן אלגינט, אלוורה וגליצרין שימשו להכנת הפורמולה של סרט הידרוג'ל. ההכנה וההערכה הסופית של התכשירים בוצעו רק עם 10% גליצרין (w/w של אלגינט). איור 1 מציג את סרט ההידרוג'ל עם יחסי אלוורה שונ...
Discussion
חומצה פוסידית שולבה בסרטי הידרוג'ל אלגינט עם יחסים שונים של אלוורה וגליצרין. נוכחותו של אלוורה לא השפיעה על המראה, אך נצפתה ירידה בצמיגות בתמיסות המכילות אלוורה במהלך ההכנה. הממצאים מבדיקות עובי מצביעים על כך שלהכללת אלוורה עשויה להיות השפעה מסוימת ע...
Disclosures
למחברים אין מה לחשוף.
Acknowledgements
מחקר זה נתמך על ידי חוקרים תומכים בפרויקט מספר (PNURSP2024R30) של אוניברסיטת הנסיכה נורה בינת עבד אל-רחמן, ריאד, ערב הסעודית. מחקר זה מומן על ידי מספר פרויקט תומכי חוקרים (RSPD2024R811), אוניברסיטת המלך סעוד, ריאד, ערב הסעודית.
Materials
| Name | Company | Catalog Number | Comments |
| Aloe vera | Local supplier, Kuala Lumpur, Malaysia | It was raw aloe vera bark and prepared the materials in our lab | |
| Calcium Chloride | R&M Chemicals | ||
| Differential Scanning Calorimetry | Netzsch-Gruppe | DSC 300 Caliris | |
| FTIR spectroscopy | Perkin Elmer | 107914 | |
| Fusidic Acid | Sigma-Aldrich, St. Louis, MO, USA | PHR2810 | certified reference material, pharmaceutical secondary standard |
| Glycerin | Sigma-Aldrich, St. Louis, MO, USA | PHR1020 | United States Pharmacopeia (USP) Reference Standard |
| Micrometer Screw Gauge | Blomker Industries, Malaysia | ||
| NETZSCH proteus software | Netzsch-Gruppe | DSC 300 Caliris | |
| Phosphate Buffer Saline | Sigma-Aldrich, St. Louis, MO, USA | P4417 | Tablets |
| Sodium alginate | Sigma-Aldrich, St. Louis, MO, USA | W201502 | |
| thermal analysis instrument | NETZSCH | DSC Caliris | |
| UV-SPECTROPHOTOMETER / UV LINE-9400 | SECOMAM | / 8512047 |
References
- Bandyopadhyay, D. Topical antibacterials in dermatology. Indian J Dermatol. 66 (2), 117-125 (2021).
- Williamson, D. A., Carter, G. P., Howden, B. P. Current and emerging topical antibacterials and antiseptics: agents, action, and resistance patterns. Clin Microbiol Rev. 30, 827-860 (2017).
- Bonamonte, D., Belloni Fortina, A., Neri, L., Patrizi, A. Fusidic acid in skin infections and infected atopic eczema. G Ital Dermatol Venereol. 149 (4), 453-459 (2014).
- Curbete, M. M., Nunes, R. A. Critical review of the properties of fusidic acid and analytical methods for its determination. Crit Rev Anal Chem. 46 (4), 352-360 (2015).
- Zhao, C., Zhou, L., Chiao, M., Yang, W. Antibacterial hydrogel coating: Strategies in surface chemistry. Adv Colloid Interface. 285, 102280-102280 (2020).
- Ahmed, E. M. Hydrogel- Preparation, characterization, and applications: A review. J Adv Res. 6, 105-121 (2015).
- Stan, D., et al. Wound healing applications of creams and "smart" hydrogels. Exp Dermatol. 30 (9), 1218-1232 (2021).
- Cole, L., Heard, C. M. Skin permeation enhancement potential of Aloe vera and a proposed mechanism of action based upon size exclusion and pull effect. Int J Pharm. 333 (1-2), 10-16 (2007).
- Sharma, K., Mittal, A., Chauhan, N. Aloe vera as penetration enhancer. Int J Drug Dev Res. 7, 31-43 (2015).
- Parhi, R., Suresh, P., Mondal, S., Kumar, P. M. Novel penetration enhancers for skin applications: A Review. Curr Drug Deliv. 9 (2), 219-230 (2012).
- Hadi, A., Nawab, A., Alam, F., Zehra, K. Alginate/Aloe vera films reinforced with tragacanth gum. Food Chemistry: Mol Sci. 30 (4), 100105 (2022).
- Gull, N., et al. In vitro study of chitosan-based multi-responsive hydrogels as drug release vehicles: a preclinical study. RSC Adv. 9 (53), 31078-31091 (2019).
- Ciarleglio, G., Cinti, F., Toto, E., Santonicola, M. G. Synthesis and characterization of alginate gel beads with embedded zeolite structures as carriers of hydrophobic curcumin. Gels. 9 (9), 714 (2023).
- Dong, H., et al. Smart polycationic hydrogel dressing for dynamic wound healing. Small. 18 (25), 2201620 (2022).
- Giz, A. S., et al. A detailed investigation of the effect of calcium cross-linking and glycerol plasticizing on the physical properties of alginate films. Int J Biol Macromol. 148, 49-55 (2020).
- Fadhilah, S., Aisyah, N., Mohd, N., Mat, K. A. Sodium alginate film: The effect of crosslinker on physical and mechanical properties. IOP Conf Ser Mater Sci. 509, 012063 (2019).
- Kudłacik-Kramarczyk, S., et al. Investigations on the impact of the introduction of the Aloe vera into the hydrogel matrix on cytotoxic and hydrophilic properties of these systems considered as potential wound dressings. Mater Sci Eng C. 123, 111977 (2021).
- Pereira, R., et al. Development of novel alginate based hydrogel films for wound healing applications. Int J Biol Macromol. 52, 221-230 (2013).
- Hadi, A., Nawab, A., Alam, F., Zehra, K. Physical, mechanical, optical, barrier, and antioxidant properties of sodium alginate-Aloe vera biocomposite film. J Food Process. 45 (5), e15444 (2021).
- Yoshida, C. M., et al. Effect of chitosan and Aloe vera extract concentrations on the physicochemical properties of chitosan biofilms. Polymers. 13 (8), 1187 (2021).
- Nuutila, K., Eriksson, E. Moist wound healing with commonly available dressings. Adv Wound Care. 10 (12), 685-698 (2021).
- Naeem, F., et al. pH-responsive cross-linked polymeric matrices based on natural polymers: effect of process variables on swelling characterization and drug delivery properties. BioImpacts: BI. 7 (3), 177 (2017).
- Mahmood, A., et al. Aloe vera-based polymeric network: A promising approach for sustained drug delivery, development, characterization, and in vitro evaluation. Gels. 9 (6), 474 (2023).
- Kamaraj, N., Rajaguru, P. Y., Issac, P., Sundaresan, S. Fabrication, characterization, in vitro drug release and glucose uptake activity of 14-deoxy, 11, 12-didehydroandrographolide loaded polycaprolactone nanoparticles. Asian J Pharm Sci. 11 (4), 353-362 (2017).
- Chalitangkoon, J., Wongkittisin, M., Monvisade, P. Silver loaded hydroxyethylacryl chitosan/sodium alginate hydrogel films for controlled drug release wound dressings. Int J Biol Macromol. 159, 194-203 (2020).
- Laracuente, M. L., Yu, M. H., McHugh, K. J. Zero-order drug delivery: State of the art and future prospects. J Control Release. 327, 834-856 (2020).
- Wang, Y., et al. A sustained zero-order release carrier for long-acting, peakless basal insulin therapy. J Mater Chem B. 8 (9), 1952-1959 (2020).
- Unagolla, J. M., Jayasuriya, A. C. Drug transport mechanisms and in vitro release kinetics of vancomycin encapsulated chitosan-alginate polyelectrolyte microparticles as a controlled drug delivery system. Eur J Pharm Sci. 114, 199-209 (2018).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved