JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
Fusidic Acid-Loaded Alginate-Aloe vera 기반 하이드로겔 필름의 개발 및 특성화
요약
fusidic acid-loaded 하이드로겔 필름의 제형은 다른 알로에 베라 비율로 개발되었으며 본 연구에서 특성화되었습니다.
초록
새로운 푸시딕산이 로드된 하이드로겔 필름은 알긴산과 알로에 베라를 사용하는 용매 주조 기술을 통해 제조되었습니다. 하이드로겔 필름은 알긴산 나트륨, 알로에 베라 및 글리세린의 다양한 비율을 사용하여 최적화되었습니다. 10% 글리세린(알긴산 w/w)을 함유한 필름이 가장 좋은 외관을 나타냈습니다. 알로에 베라를 통합하면 하이드로겔 필름의 두께, 팽창 거동, 수증기 투과성 및 약물 방출 프로파일에 영향을 미쳤습니다. 알로에 베라 함량이 높을수록 필름이 더 두꺼워지고(특정 비율까지), 팽창이 증가하고, 수증기 투과성이 감소하고, 12시간 동안 최대 93%의 약물 방출이 연장되었습니다. 푸리에 변환 적외선 분광법(FTIR) 분석을 통해 주요 작용기의 존재와 하이드로겔 성분 간의 상호 작용을 확인했습니다. 이 연구는 알긴산 나트륨, 알로에 베라 및 글리세린의 조합이 하이드로겔 필름의 기계적 특성과 약물 방출 프로파일을 개선할 수 있음을 시사하여 향상된 국소 약물 전달 및 상처 치유 응용 분야에 대한 유망한 옵션이 될 수 있습니다.
서문
Fusidic acid는 Fusidium coccineum에서 파생 된 강력한 스테로이드 항생제입니다. 포도상구균 피부 감염 및 농가진을 치료하는 데 널리 사용됩니다. 이 약은 항생제 내성 균주에 대해서도 효능이 높고 독성이 낮아 피부 감염 관리에 적합한 옵션입니다1. 다른 국소 항생제와 달리 푸시딕산은 피부 깊숙이 침투하여 특히 피부의 보호 장벽이 손상된 부위에서 항균 효과를 향상시킵니다. 그 구조는 다양한 용해성 특성을 허용하여 신체 조직 전체에 널리 분포할 수 있으며, 이는 더 나은 수용성 및 침투율을 위해 소듐 퓨시데이트 형태로 더욱 향상됩니다 2,3. 푸시딕산은 경구, 정맥 주사, 국소 등 다양한 방법으로 투여할 수 있으며, 다양한 치료 요구에 적응하고 다양한 감염에 유연하게 선택할 수 있다4.
수분 함량이 높고 생체 적합성이 높은 하이드로겔은 상처 치료에서 항생제의 혁신적인 운반체로 부상하여 수분 유지, 약물 방출 조절 및 환자 결과 개선을 제공합니다. 알긴산염은 알긴산과 같은 천연 또는 합성 고분자로 만들어지며, 강력한 생체 적합성, 경제성 및 천연 조직 세포 외 기질을 모방한 겔화 특성으로 인해 선호됩니다5. 특히 알긴산 기반 하이드로겔은 상처 치유에 도움이 되는 습한 환경을 제공하고, 상처에 달라붙지 않으며, 쉽게 제거할 수 있어 생체 활성 물질을 전달하고 조직 재생을 지원하는 데 이상적입니다. 항생제를 캡슐화하는 하이드로겔의 개발은 상처 치료의 중요한 발전을 의미하며, 표적 약물 전달과 지속적인 치료 효과를 보장합니다 6,7.
제안된 푸시딕산 부하 알긴산/알로에 베라 하이드로겔은 푸시딕산의 용해성 문제를 극복하고 피부 침투를 향상시키는 것을 목표로 합니다. 피부 친화적이고 보습 및 항균 특성으로 알려진 알로에 베라는 화학적 침투 증진제 역할도 하여 피부 감염 치료에 대한 푸시딕산의 효능을 향상시킬 수 있습니다 8,9. 이 혁신적인 제형은 알로에 베라와 알긴산 하이드로겔의 시너지 효과를 활용하여 도움이 되는 치유 환경을 조성하고, 약물 전달을 최적화하며, 향상된 피부 감염 치료를 위한 유망한 솔루션을 제공하여 푸시딕산의 강력한 항균 활성을 극대화하고 전달 및 치유 결과를 개선합니다10.
Access restricted. Please log in or start a trial to view this content.
프로토콜
이 연구에 사용된 시약 및 장비의 세부 정보는 재료 표에 나열되어 있습니다.
1. 푸시딕산 하이드로겔 필름의 제조
- 알긴산 나트륨(2.0% w/v)과 알로에 베라 (1.0% w/v) 용액을 증류수에 용해하여 준비합니다.
- 알긴산 나트륨 용액에 푸시딕산 200mg을 넣고 1시간 동안 저어줍니다.
- 알긴산 용액에 글리세롤을 10%, 12% 및 14%(알긴산 질량 기준 w/w)의 농도로 추가합니다.
- 알긴산염과 알로에 베라 용액을 결합하여 100:0, 90:10, 80:20 및 75:25의 최종 알긴산/알로에 베라 비율(v/v)을 달성합니다.
- 각 혼합물 25mL를 유리 페트리 접시(100mm x 20mm)에 넣고 실온(25°C) 및 습도 조절(50%)에서 2일 동안 건조시킵니다.
- 건조된 필름을 염화칼슘(CaCl2) 수용액(5.0% w/v)에 5분 동안 담궈 하이드로겔 필름을 얻습니다.
- 생성된 필름을 증류수로 세척하고 사용하기 전에 실온에서 건조시킵니다.
2. 필름 두께 결정
- 디지털 마이크로미터를 사용하여 필름의 두께를 측정하십시오11.
- 필름 전체의 5개 지점에서 측정합니다.
- 각 점에서 얻은 측정값을 기록합니다.
- 측정한 값을 기준으로 평균 박막 두께를 계산합니다.
3. 팽창 지수 결정
- 실험용 칼을 사용하여 필름 샘플을 2cm x 2cm 정사각형으로 자릅니다.
- 각 샘플의 무게를 정확하게 측정합니다.
- 샘플을 PBS 버퍼(pH 6.8)에 실온에서 24시간 동안 담가둡니다.
- 여과지를 사용하여 필름 표면의 과도한 물을 흡수합니다.
- 샘플의 무게를 다시 잰다.
- 다른 시간 간격으로 필름의 무게를 잰다. 다음 방정식을 사용하여 팽창 용량을 계산합니다.
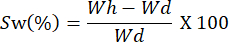
참고: Wh 는 샘플의 수화 중량을 나타내고 Wd 는 샘플의 건조 중량에 해당합니다.
4. 수증기 투과성 또는 폐색 시험
- 50mL의 물이 들어 있는 유리 비커의 입구를 여과지11로 덮습니다.
- 논문 중 하나에 필름 형성 용액을 바르고 필름을 현상하도록 합니다.
- 비커는 실온과 습도에 보관하십시오.
- 비커 내의 물 무게 감소를 기반으로 물에 대한 필름의 투과성을 평가합니다.
- 준비된 하이드로겔 필름에 대한 수증기 투과성 평가를 결정하려면 다음 공식을 사용하십시오.
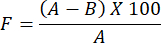
참고: 폐색률 계수 F는 필름의 투과성을 측정합니다. 필름이 없는 여과지로 덮인 유리 비커와 필름이 코팅된 여과지로 덮인 유리 비커의 물 무게 차이를 계산하여 결정됩니다. 폐색성 계수 값이 작을수록 필름 투과성이 더 크다는 것을 나타냅니다.
5. 푸리에 변환 적외선 분광법(FTIR)
- 하이드로겔 샘플을 FTIR 분광기의 ATR 결정에 놓습니다.
- 파수 범위를 4000-400cm-1로 설정합니다.
- 스캔 속도를 샘플당 60회 스캔으로 설정합니다.
- 해상도를 4cm-1로 설정합니다.
- 각 샘플 실행 전에 공기 배경을 기록합니다.
- 각 하이드로겔 샘플에 대해 개별적으로 분석을 실행합니다.
- 각 하이드로겔 샘플에 대한 FTIR 스펙트럼을 분석하여 작용기를 확인하고 모든 구성 요소 간의 상호 작용을 검사합니다12.
- 원시 알로에 베라, 알긴산 나트륨, 글리세린 및 푸시딕산에 대해 개별적으로 분석을 반복합니다.
6. 시차 주사 열량계(DSC)
- 시중에서 판매되는 열 분석 기기를 사용하여 열 프로파일을 획득하십시오.
- 고분자 필름에서 자른 여러 개의 원형 조각으로 측정 샘플을 제작합니다.
- 25-230 °C의 온도 범위를 조사하십시오.
- 가열/냉각 속도를 20°C/min으로 설정합니다.
- 호환 가능한 소프트웨어와 함께 표준 인듐을 사용하여 온도 및 엔탈피 교정을 수행합니다.
7. 약물 방출 검사
- 용해 매체로 50mL PBS(pH = 7.4) 용액을 준비합니다.
- 하이드로겔 필름을 37°C의 PBS에 24시간 동안 담그면서 50rpm의 속도로 교반합니다.
- 미리 결정된 간격으로 샘플 2mL를 수집합니다.
- 수집된 샘플을 주사기 필터를 통해 희석하고 여과합니다.
- 동일한 양의 PBS를 즉시 보충하십시오.
- 285nm에서 흡수를 측정하는 UV 분광 광도계를 사용하여 방출되는 푸시딕산의 농도를 평가합니다.
- 0차, 1차, Higuchi 및 Korsmeyer-Peppas 모델4를 사용하여 푸시딕산의 방출 역학을 평가합니다.
Access restricted. Please log in or start a trial to view this content.
결과
알긴산염/알로에 베라 하이드로겔 필름의 제조
알긴산 나트륨, 알로에 베라 및 글리세린의 다른 비율이 하이드로 겔 필름의 제형을 준비하기 위해 사용되었습니다. 제형의 최종 준비 및 평가는 10% 글리세린(알긴산 w/w)으로만 수행되었습니다. 그림 1 은 알로에 베라 비율이 다른 하이드로겔 필름을 보여줍니다. 이?...
Access restricted. Please log in or start a trial to view this content.
토론
Fusidic acid는 알로에 베라 와 글리세린의 다양한 비율로 알기네이트 하이드로겔 필름에 통합되었습니다. 알로에 베라 의 존재는 외관에 영향을 미치지 않았지만 준비 중에 알로에 베라 를 함유 한 용액에서 점도 감소가 관찰되었습니다. 두께 테스트의 결과는 알로에 베라 의 포함이 필름 두께에 어느 정도 영향을 미칠 수 있음을 시사하지만 중요...
Access restricted. Please log in or start a trial to view this content.
공개
저자는 공개할 내용이 없습니다.
감사의 말
이 연구는 사우디아라비아 리야드에 있는 Princess Nourah bint Abdulrahman University의 Princess Nourah bint Abdulrahman University Researchers Supporting Project 번호(PNURSP2024R30)의 지원을 받았습니다. 이 연구는 사우디아라비아 리야드에 있는 King Saud University의 Researchers Supporting Project 번호(RSPD2024R811)의 지원을 받았습니다.
Access restricted. Please log in or start a trial to view this content.
자료
| Name | Company | Catalog Number | Comments |
| Aloe vera | Local supplier, Kuala Lumpur, Malaysia | It was raw aloe vera bark and prepared the materials in our lab | |
| Calcium Chloride | R&M Chemicals | ||
| Differential Scanning Calorimetry | Netzsch-Gruppe | DSC 300 Caliris | |
| FTIR spectroscopy | Perkin Elmer | 107914 | |
| Fusidic Acid | Sigma-Aldrich, St. Louis, MO, USA | PHR2810 | certified reference material, pharmaceutical secondary standard |
| Glycerin | Sigma-Aldrich, St. Louis, MO, USA | PHR1020 | United States Pharmacopeia (USP) Reference Standard |
| Micrometer Screw Gauge | Blomker Industries, Malaysia | ||
| NETZSCH proteus software | Netzsch-Gruppe | DSC 300 Caliris | |
| Phosphate Buffer Saline | Sigma-Aldrich, St. Louis, MO, USA | P4417 | Tablets |
| Sodium alginate | Sigma-Aldrich, St. Louis, MO, USA | W201502 | |
| thermal analysis instrument | NETZSCH | DSC Caliris | |
| UV-SPECTROPHOTOMETER / UV LINE-9400 | SECOMAM | / 8512047 |
참고문헌
- Bandyopadhyay, D. Topical antibacterials in dermatology. Indian J Dermatol. 66 (2), 117-125 (2021).
- Williamson, D. A., Carter, G. P., Howden, B. P. Current and emerging topical antibacterials and antiseptics: agents, action, and resistance patterns. Clin Microbiol Rev. 30, 827-860 (2017).
- Bonamonte, D., Belloni Fortina, A., Neri, L., Patrizi, A. Fusidic acid in skin infections and infected atopic eczema. G Ital Dermatol Venereol. 149 (4), 453-459 (2014).
- Curbete, M. M., Nunes, R. A. Critical review of the properties of fusidic acid and analytical methods for its determination. Crit Rev Anal Chem. 46 (4), 352-360 (2015).
- Zhao, C., Zhou, L., Chiao, M., Yang, W. Antibacterial hydrogel coating: Strategies in surface chemistry. Adv Colloid Interface. 285, 102280-102280 (2020).
- Ahmed, E. M. Hydrogel- Preparation, characterization, and applications: A review. J Adv Res. 6, 105-121 (2015).
- Stan, D., et al. Wound healing applications of creams and "smart" hydrogels. Exp Dermatol. 30 (9), 1218-1232 (2021).
- Cole, L., Heard, C. M. Skin permeation enhancement potential of Aloe vera and a proposed mechanism of action based upon size exclusion and pull effect. Int J Pharm. 333 (1-2), 10-16 (2007).
- Sharma, K., Mittal, A., Chauhan, N. Aloe vera as penetration enhancer. Int J Drug Dev Res. 7, 31-43 (2015).
- Parhi, R., Suresh, P., Mondal, S., Kumar, P. M. Novel penetration enhancers for skin applications: A Review. Curr Drug Deliv. 9 (2), 219-230 (2012).
- Hadi, A., Nawab, A., Alam, F., Zehra, K. Alginate/Aloe vera films reinforced with tragacanth gum. Food Chemistry: Mol Sci. 30 (4), 100105(2022).
- Gull, N., et al. In vitro study of chitosan-based multi-responsive hydrogels as drug release vehicles: a preclinical study. RSC Adv. 9 (53), 31078-31091 (2019).
- Ciarleglio, G., Cinti, F., Toto, E., Santonicola, M. G. Synthesis and characterization of alginate gel beads with embedded zeolite structures as carriers of hydrophobic curcumin. Gels. 9 (9), 714(2023).
- Dong, H., et al. Smart polycationic hydrogel dressing for dynamic wound healing. Small. 18 (25), 2201620(2022).
- Giz, A. S., et al. A detailed investigation of the effect of calcium cross-linking and glycerol plasticizing on the physical properties of alginate films. Int J Biol Macromol. 148, 49-55 (2020).
- Fadhilah, S., Aisyah, N., Mohd, N., Mat, K. A. Sodium alginate film: The effect of crosslinker on physical and mechanical properties. IOP Conf Ser Mater Sci. 509, 012063(2019).
- Kudłacik-Kramarczyk, S., et al. Investigations on the impact of the introduction of the Aloe vera into the hydrogel matrix on cytotoxic and hydrophilic properties of these systems considered as potential wound dressings. Mater Sci Eng C. 123, 111977(2021).
- Pereira, R., et al. Development of novel alginate based hydrogel films for wound healing applications. Int J Biol Macromol. 52, 221-230 (2013).
- Hadi, A., Nawab, A., Alam, F., Zehra, K. Physical, mechanical, optical, barrier, and antioxidant properties of sodium alginate-Aloe vera biocomposite film. J Food Process. 45 (5), e15444(2021).
- Yoshida, C. M., et al. Effect of chitosan and Aloe vera extract concentrations on the physicochemical properties of chitosan biofilms. Polymers. 13 (8), 1187(2021).
- Nuutila, K., Eriksson, E. Moist wound healing with commonly available dressings. Adv Wound Care. 10 (12), 685-698 (2021).
- Naeem, F., et al. pH-responsive cross-linked polymeric matrices based on natural polymers: effect of process variables on swelling characterization and drug delivery properties. BioImpacts: BI. 7 (3), 177(2017).
- Mahmood, A., et al. Aloe vera-based polymeric network: A promising approach for sustained drug delivery, development, characterization, and in vitro evaluation. Gels. 9 (6), 474(2023).
- Kamaraj, N., Rajaguru, P. Y., Issac, P., Sundaresan, S. Fabrication, characterization, in vitro drug release and glucose uptake activity of 14-deoxy, 11, 12-didehydroandrographolide loaded polycaprolactone nanoparticles. Asian J Pharm Sci. 11 (4), 353-362 (2017).
- Chalitangkoon, J., Wongkittisin, M., Monvisade, P. Silver loaded hydroxyethylacryl chitosan/sodium alginate hydrogel films for controlled drug release wound dressings. Int J Biol Macromol. 159, 194-203 (2020).
- Laracuente, M. L., Yu, M. H., McHugh, K. J. Zero-order drug delivery: State of the art and future prospects. J Control Release. 327, 834-856 (2020).
- Wang, Y., et al. A sustained zero-order release carrier for long-acting, peakless basal insulin therapy. J Mater Chem B. 8 (9), 1952-1959 (2020).
- Unagolla, J. M., Jayasuriya, A. C. Drug transport mechanisms and in vitro release kinetics of vancomycin encapsulated chitosan-alginate polyelectrolyte microparticles as a controlled drug delivery system. Eur J Pharm Sci. 114, 199-209 (2018).
Access restricted. Please log in or start a trial to view this content.
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유