このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
フシジン酸を含有するアルギン酸-アロエベラ 系ハイドロゲル膜の開発と評価
要約
フシジン酸を充填したヒドロゲルフィルムの製剤を、異なる アロエベラ 比で開発し、この研究で特徴付けました。
要約
新しいフシジン酸を充填したヒドロゲルフィルムを、アルギン酸塩とアロエベラを用いた溶媒鋳造技術によって調製しました。ヒドロゲルフィルムは、アルギン酸ナトリウム、アロエベラ、グリセリンの異なる比率を使用して最適化しました。10%グリセリン(アルギン酸w/w)を含有するフィルムが最高の外観を示しました。アロエベラを組み込むと、ハイドロゲル膜の厚さ、膨潤挙動、水蒸気透過性、および薬物放出プロファイルに影響を与えました。アロエベラの含有量が高いと、フィルムが厚くなり(一定の割合まで)、膨潤が増加し、水蒸気透過性が低下し、12時間で最大93%の薬物放出が延長されました。フーリエ変換赤外分光法(FTIR)分析により、主要な官能基の存在とハイドロゲル成分間の相互作用が確認されました。この研究は、アルギン酸ナトリウム、アロエベラ、およびグリセリンの組み合わせが、ハイドロゲルフィルムの機械的特性と薬物放出プロファイルを改善できることを示唆しており、ハイドロゲルフィルムを局所薬物送達および創傷治癒アプリケーションの強化のための有望な選択肢にしています。
概要
フシジン酸は、Fusidium coccineumに由来する強力なステロイド系抗生物質です。ブドウ球菌性皮膚感染症や膿痂疹の治療に広く使用されています。本剤は、抗生物質耐性株に対しても高い有効性を有し、毒性も低いため、皮膚感染症1の管理に適した薬剤です1。他の局所抗生物質とは異なり、フシジン酸は皮膚の奥深くまで浸透し、特に皮膚の保護バリアが損傷している領域で抗菌効果を高めます。その構造は、汎用性の高い溶解性特性を可能にし、体組織全体に広く分布することを可能にし、これはさらに、より優れた水溶解性と浸透率2,3のために、そのフシジン酸ナトリウムの形で強化されます。フシジン酸は、経口、静脈内、局所など、さまざまな方法で投与でき、さまざまな治療ニーズに適応し、さまざまな感染症に柔軟に対応できます4。
ハイドロゲルは、その高い含水量と生体適合性により、創傷治療における抗生物質の革新的な担体として浮上し、水分保持、薬物放出の制御、および患者の転帰の改善を実現します。それらは、アルギン酸のような天然または合成ポリマーから作られており、アルギン酸は、その強力な生体適合性、手頃な価格、および天然組織の細胞外マトリックスを模倣するゲル化特性で好まれています5。特にアルギン酸ベースのハイドロゲルは、創傷治癒を助長する湿った環境を提供し、創傷に付着せず、容易に除去できるため、生理活性物質の送達や組織再生のサポートに最適です。抗生物質をカプセル化するハイドロゲルの開発は、創傷ケアにおける大きな進歩を表しており、標的薬物送達と持続的な治療効果を確保しています6,7。
提案されたフシジン酸を充填したアルギン酸/アロエベラハイドロゲルは、フシジン酸の溶解性の課題を克服し、その皮膚浸透を強化することを目的としています。肌にやさしく、保湿性があり、抗菌性があることで知られるアロエベラは、化学浸透促進剤としても機能し、皮膚感染症の治療におけるフシジン酸の有効性を向上させる可能性があります8,9。この革新的な製剤は、アロエベラとアルギン酸ヒドロゲルの相乗効果を活用して、治癒を助長する環境を作り出し、薬物送達を最適化し、皮膚感染症の治療を強化するための有望なソリューションを提供します。フシジン酸の強力な抗菌活性を最大限に活用し、送達と治癒結果を改善します10。
プロトコル
本試験で使用した試薬および装置の詳細は、 材料表に記載されています。
1. フシジン酸ハイドロゲル膜の作製
- アルギン酸ナトリウム(2.0%w / v)と アロエベラ (1.0%w / v)の溶液を蒸留水に溶解して調製します。
- アルギン酸ナトリウム溶液に200mgのフシジン酸を加え、1時間撹拌します。
- グリセロールを10%、12%、および14%の濃度でアルギン酸塩溶液に添加します(w / w、アルギン酸塩の質量に基づく)。
- アルギン酸と アロエベラ の溶液を組み合わせて、最終的なアルギン酸/アロエベラ 比(v / v)を100:0、90:10、80:20、および75:25にします。
- 各混合物25 mLをガラス製のペトリ皿(100 mm x 20 mm)に流し込み、室温(25 °C)および制御された湿度(50%)で2日間乾燥させます。
- 乾燥したフィルムを塩化カルシウム(CaCl2)水溶液(5.0%w / v)に5分間浸して、ヒドロゲルフィルムを得ます。
- 得られたフィルムを蒸留水で洗浄し、室温で乾燥させてから使用してください。
2. 膜厚の決定
- デジタルマイクロメータを使用して、フィルムの厚さを測定します11。
- フィルム全体の5つの異なるポイントで測定を行います。
- 各ポイントから取得した測定値を記録します。
- 取得した測定値に基づいて平均膜厚を計算します。
3.腫れ指数の決定
- ラボナイフを使用して、フィルムサンプルを2 cm x 2 cmの正方形にカットします。
- 各サンプルを正確に計量します。
- サンプルをPBS緩衝液(pH 6.8)に室温で24時間浸します。
- フィルム表面の余分な水分を濾紙で吸収します。
- サンプルを再度計量します。
- 異なる時間間隔でフィルムを計量します。次の式を使用して膨潤容量を計算します。
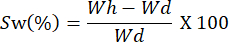
注: Wh はサンプルの水和重量を表し、 Wd はサンプルの乾燥重量に対応します。
4.水蒸気透過性または閉塞試験
- 50mLの水が入ったガラスビーカーの開口部を濾紙11で覆います。
- 紙の1つにフィルム形成溶液を塗布し、フィルムを現像できるようにします。
- ビーカーは室温と湿度で保管してください。
- ビーカー内の水重量の減少に基づいて、フィルムの水に対する透過性を評価します。
- 調製したヒドロゲルフィルムの水蒸気透過性の評価を決定するには、次の式を使用します。
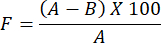
注:オクルーシビティ係数Fは、フィルムの透過性を測定します。フィルムを貼っていない濾紙で覆ったガラスビーカーと、フィルムを濾紙で覆ったガラスビーカーの水重量の差を計算して求めます。オクルーシビティ係数の値が小さいほど、フィルムの透過性が高いことを示します。
5. フーリエ変換赤外分光法(FTIR)
- ハイドロゲルサンプルをFTIR分光装置のATR結晶に置きます。
- 波数の範囲を4000-400 cm-1に設定します。
- スキャンレートをサンプルあたり60スキャンに設定します。
- 解像度を4cm-1に設定します。
- 各サンプル実行の前に空気の背景を記録します。
- 各ハイドロゲルサンプルについて個別に分析を実行します。
- 各ヒドロゲルサンプルのFTIRスペクトルを分析して、官能基を確認し、すべてのコンポーネント間の相互作用を調べます12。
- 生の アロエベラ、アルギン酸ナトリウム、グリセリン、およびフシジン酸について別々に分析を繰り返します。
6. 示差走査熱量測定(DSC)
- 市販の熱分析装置を使用して、熱プロファイルを取得します。
- ポリマーフィルムから切り出された複数の円形ピースから測定サンプルを作成します。
- 25〜230°Cの温度範囲を調査します。
- 加熱/冷却速度を20°C/minに設定します。
- 温度とエンタルピーのキャリブレーションは、互換性のあるソフトウェアを備えた標準インジウムを使用して行います。
7. 薬物放出試験
- 溶出液として50mLのPBS(pH = 7.4)の溶液を調製します。
- ヒドロゲルフィルムをPBSに37°Cで24時間浸漬し、50rpmの速度で攪拌します。
- 所定の間隔で、2 mLのサンプルを回収します。
- 収集したサンプルを希釈し、シリンジフィルターでろ過します。
- 同量のPBSを迅速に補充してください。
- UV分光光度計を使用して放出されるフシジン酸の濃度を評価し、285nmでの吸収を測定します。
- ゼロ次、1次、樋口モデル、およびKorsmeyer-Peppasモデル4を使用して、フシジン酸の放出速度を評価します。
結果
アルギン酸/アロエベラ ヒドロゲルフィルムの調製
アルギン酸ナトリウム、 アロエベラ、およびグリセリンの異なる比率を使用して、ヒドロゲルフィルムの製剤を調製しました。製剤の最終調製および評価は、10%グリセリン(アルギン酸w/w)のみを用いて行った。 図1 は、 アロエベラ の比率が異なるヒドロゲ?...
ディスカッション
フシジン酸は、 アロエベラ とグリセリンのさまざまな比率でアルギン酸ヒドロゲルフィルムに組み込まれました。 アロエベラ の存在は外観に影響を与えませんでしたが、調製中に アロエベラ を含有する溶液中の粘度の低下が観察されました。厚さ試験の結果は、 アロエベラ の含有がある程度フィルムの厚さに何らかの影響を与える可?...
開示事項
著者は何も開示していません。
謝辞
この研究は、サウジアラビアのリヤドにあるプリンセス・ヌーラ・ビント・アブドゥルラーマン大学のプリンセス・ヌーラ・ビント・アブドゥルラーマン大学の研究者支援プロジェクト番号(PNURSP2024R30)の支援を受けました。この研究は、サウジアラビアのリヤドにあるキングサウード大学の研究者支援プロジェクト番号(RSPD2024R811)によって資金提供されました。
資料
| Name | Company | Catalog Number | Comments |
| Aloe vera | Local supplier, Kuala Lumpur, Malaysia | It was raw aloe vera bark and prepared the materials in our lab | |
| Calcium Chloride | R&M Chemicals | ||
| Differential Scanning Calorimetry | Netzsch-Gruppe | DSC 300 Caliris | |
| FTIR spectroscopy | Perkin Elmer | 107914 | |
| Fusidic Acid | Sigma-Aldrich, St. Louis, MO, USA | PHR2810 | certified reference material, pharmaceutical secondary standard |
| Glycerin | Sigma-Aldrich, St. Louis, MO, USA | PHR1020 | United States Pharmacopeia (USP) Reference Standard |
| Micrometer Screw Gauge | Blomker Industries, Malaysia | ||
| NETZSCH proteus software | Netzsch-Gruppe | DSC 300 Caliris | |
| Phosphate Buffer Saline | Sigma-Aldrich, St. Louis, MO, USA | P4417 | Tablets |
| Sodium alginate | Sigma-Aldrich, St. Louis, MO, USA | W201502 | |
| thermal analysis instrument | NETZSCH | DSC Caliris | |
| UV-SPECTROPHOTOMETER / UV LINE-9400 | SECOMAM | / 8512047 |
参考文献
- Bandyopadhyay, D. Topical antibacterials in dermatology. Indian J Dermatol. 66 (2), 117-125 (2021).
- Williamson, D. A., Carter, G. P., Howden, B. P. Current and emerging topical antibacterials and antiseptics: agents, action, and resistance patterns. Clin Microbiol Rev. 30, 827-860 (2017).
- Bonamonte, D., Belloni Fortina, A., Neri, L., Patrizi, A. Fusidic acid in skin infections and infected atopic eczema. G Ital Dermatol Venereol. 149 (4), 453-459 (2014).
- Curbete, M. M., Nunes, R. A. Critical review of the properties of fusidic acid and analytical methods for its determination. Crit Rev Anal Chem. 46 (4), 352-360 (2015).
- Zhao, C., Zhou, L., Chiao, M., Yang, W. Antibacterial hydrogel coating: Strategies in surface chemistry. Adv Colloid Interface. 285, 102280-102280 (2020).
- Ahmed, E. M. Hydrogel- Preparation, characterization, and applications: A review. J Adv Res. 6, 105-121 (2015).
- Stan, D., et al. Wound healing applications of creams and "smart" hydrogels. Exp Dermatol. 30 (9), 1218-1232 (2021).
- Cole, L., Heard, C. M. Skin permeation enhancement potential of Aloe vera and a proposed mechanism of action based upon size exclusion and pull effect. Int J Pharm. 333 (1-2), 10-16 (2007).
- Sharma, K., Mittal, A., Chauhan, N. Aloe vera as penetration enhancer. Int J Drug Dev Res. 7, 31-43 (2015).
- Parhi, R., Suresh, P., Mondal, S., Kumar, P. M. Novel penetration enhancers for skin applications: A Review. Curr Drug Deliv. 9 (2), 219-230 (2012).
- Hadi, A., Nawab, A., Alam, F., Zehra, K. Alginate/Aloe vera films reinforced with tragacanth gum. Food Chemistry: Mol Sci. 30 (4), 100105 (2022).
- Gull, N., et al. In vitro study of chitosan-based multi-responsive hydrogels as drug release vehicles: a preclinical study. RSC Adv. 9 (53), 31078-31091 (2019).
- Ciarleglio, G., Cinti, F., Toto, E., Santonicola, M. G. Synthesis and characterization of alginate gel beads with embedded zeolite structures as carriers of hydrophobic curcumin. Gels. 9 (9), 714 (2023).
- Dong, H., et al. Smart polycationic hydrogel dressing for dynamic wound healing. Small. 18 (25), 2201620 (2022).
- Giz, A. S., et al. A detailed investigation of the effect of calcium cross-linking and glycerol plasticizing on the physical properties of alginate films. Int J Biol Macromol. 148, 49-55 (2020).
- Fadhilah, S., Aisyah, N., Mohd, N., Mat, K. A. Sodium alginate film: The effect of crosslinker on physical and mechanical properties. IOP Conf Ser Mater Sci. 509, 012063 (2019).
- Kudłacik-Kramarczyk, S., et al. Investigations on the impact of the introduction of the Aloe vera into the hydrogel matrix on cytotoxic and hydrophilic properties of these systems considered as potential wound dressings. Mater Sci Eng C. 123, 111977 (2021).
- Pereira, R., et al. Development of novel alginate based hydrogel films for wound healing applications. Int J Biol Macromol. 52, 221-230 (2013).
- Hadi, A., Nawab, A., Alam, F., Zehra, K. Physical, mechanical, optical, barrier, and antioxidant properties of sodium alginate-Aloe vera biocomposite film. J Food Process. 45 (5), e15444 (2021).
- Yoshida, C. M., et al. Effect of chitosan and Aloe vera extract concentrations on the physicochemical properties of chitosan biofilms. Polymers. 13 (8), 1187 (2021).
- Nuutila, K., Eriksson, E. Moist wound healing with commonly available dressings. Adv Wound Care. 10 (12), 685-698 (2021).
- Naeem, F., et al. pH-responsive cross-linked polymeric matrices based on natural polymers: effect of process variables on swelling characterization and drug delivery properties. BioImpacts: BI. 7 (3), 177 (2017).
- Mahmood, A., et al. Aloe vera-based polymeric network: A promising approach for sustained drug delivery, development, characterization, and in vitro evaluation. Gels. 9 (6), 474 (2023).
- Kamaraj, N., Rajaguru, P. Y., Issac, P., Sundaresan, S. Fabrication, characterization, in vitro drug release and glucose uptake activity of 14-deoxy, 11, 12-didehydroandrographolide loaded polycaprolactone nanoparticles. Asian J Pharm Sci. 11 (4), 353-362 (2017).
- Chalitangkoon, J., Wongkittisin, M., Monvisade, P. Silver loaded hydroxyethylacryl chitosan/sodium alginate hydrogel films for controlled drug release wound dressings. Int J Biol Macromol. 159, 194-203 (2020).
- Laracuente, M. L., Yu, M. H., McHugh, K. J. Zero-order drug delivery: State of the art and future prospects. J Control Release. 327, 834-856 (2020).
- Wang, Y., et al. A sustained zero-order release carrier for long-acting, peakless basal insulin therapy. J Mater Chem B. 8 (9), 1952-1959 (2020).
- Unagolla, J. M., Jayasuriya, A. C. Drug transport mechanisms and in vitro release kinetics of vancomycin encapsulated chitosan-alginate polyelectrolyte microparticles as a controlled drug delivery system. Eur J Pharm Sci. 114, 199-209 (2018).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved