Method Article
Cristallizzazione ABCG5/G8 in ambiente bicellare lipidico per cristallografia a raggi X
In questo articolo
Riepilogo
Questo protocollo descrive una configurazione per la cristallizzazione del trasportatore di steroli ABCG5/G8. ABCG5/G8 viene ricostituito in bicelle per la cristallizzazione a goccia sospesa. Il protocollo non richiede materiali o substrati specializzati, il che lo rende accessibile e facile da adattare in qualsiasi laboratorio per determinare la struttura della proteina attraverso la cristallografia a raggi X.
Abstract
I trasportatori a cassetta legante l'ATP (ABC) costituiscono proteine di membrana incorporate nei lipidi. L'estrazione di queste proteine di membrana dal doppio strato lipidico in un ambiente acquoso si ottiene in genere impiegando detergenti. Questi detergenti disintegrano il doppio strato lipidico e solubilizzano le proteine. L'habitat intrinseco delle proteine di membrana all'interno del doppio strato lipidico rappresenta una sfida nel mantenere la loro stabilità e uniformità in soluzione per la caratterizzazione strutturale. Le bicelle, che comprendono una miscela di fosfolipidi e detergenti a catena lunga e corta, replicano la struttura lipidica naturale. L'utilizzo di bicelle lipidiche e detergenti funge da sistema modello adatto per ottenere cristalli di diffrazione di alta qualità, in particolare per determinare la struttura ad alta risoluzione delle proteine di membrana. Attraverso questi microambienti sintetici, le proteine di membrana conservano la loro conformazione e funzionalità nativa, facilitando la formazione di cristalli tridimensionali. In questo approccio, l'eterodimerico solubilizzato ABCG5/G8 è stato reintegrato in bicelle DMPC/CHAPSO, integrate con colesterolo. Questa configurazione è stata impiegata nella procedura sperimentale di diffusione del vapore per la cristallizzazione delle proteine.
Introduzione
I trasportatori a cassetta legante l'ATP (ABC) costituiscono una superfamiglia di proteine di membrana responsabili di diversi processi di trasporto ATP-dipendenti attraverso le membrane biologiche 1,2,3,4,5. Queste proteine trasportatrici sono implicate nelle malattie cardiovascolari e svolgono un ruolo significativo nel facilitare l'efflusso di colesterolo nella bile per la successiva escrezione nel fegato. Di conseguenza, il metabolismo e l'equilibrio del colesterolo hanno suscitato un notevole interesse nel corso degli anni6. Un meccanismo specifico coinvolto nell'eliminazione del colesterolo e di altri steroli dall'organismo coinvolge i membri della sottofamiglia ABCG umana, in particolare l'eterodimerico ABCG5/G8 7,8,9,10. Le mutazioni in uno di questi geni interrompono l'eterodimero, portando alla perdita di funzione e causando sitosterolemia, una malattia che colpisce il traffico di steroli11,12,13. Data la rilevanza della malattia e il loro ruolo nel promuovere l'efflusso del colesterolo, i trasportatori di steroli hanno attirato un'attenzione significativa. Tuttavia, gli intricati dettagli del loro meccanismo molecolare e della selettività del substrato rimangono in gran parte non divulgati. Pertanto, la delucidazione della struttura cristallina di ABCG5/G8 è un passo cruciale verso la comprensione dei meccanismi e delle funzioni a valle nel trasporto del colesterolo.
Le proteine di membrana richiedono l'ancoraggio all'interno delle membrane per ripiegarsi e funzionare correttamente. Di conseguenza, l'estrazione delle proteine di membrana dal loro ambiente naturale spesso provoca instabilità proteica, misfolding e perdita di funzione14,15. Queste sfide sottolineano i principali ostacoli affrontati nella cristallizzazione delle proteine di membrana. Tuttavia, la ricostituzione delle proteine in doppi strati detergenti sintetici, come le bicelle, è emersa come una soluzione a questa situazione, consentendo il mantenimento delle proteine di membrana all'interno di un ambiente a doppio strato simile a quello nativo16. Le bicelle sono assemblaggi di fosfolipidi e detergenti sintetici sospesi e solubilizzati in acqua. In particolare, adottano una struttura a doppio strato che imita le membrane biologiche16,17,18. Le bicelle possono passare dalla fase liquida a quella gel in base alla temperatura e alla viscosità. La cristallizzazione bicellare sfrutta i piccoli dischi a doppio strato e la bassa viscosità a temperature ridotte, facilitando la miscelazione accurata di proteine e soluzioni bicellari. La dimensione delle bicelle dipende dal rapporto detergente/lipidi durante la preparazione19,20. I detergenti prevalenti per la formazione di bicelle includono il 3-[(3-colamidopropil)dimetilammonio]-2-idrossi-1-propansolfonato (CHAPSO), insieme al 3-[(3-colamidopropil)dimetilammonio]-1-propansolfonato (CHAPS) e all'1,2-ditridecanoil-sn-glicerolo-3-fosfocolina (DHPC)21. Questi detergenti sono utilizzati in combinazione con lipidi come la di-miristoil-fosfatidilcolina (DMPC) e la 1-palmitoil-2-oleoil-fosfatidilcolina (POPC). Inoltre, recenti studi hanno dimostrato la piena funzionalità delle proteine di membrana all'interno delle bicelle in condizioni fisiologiche. Ad esempio, Lee e colleghi hanno cristallizzato e riportato con successo la struttura cristallina di ABCG5/ABCG8 sulla base di un doppio strato lipidico22,23. Nel processo di cristallizzazione, le miscele proteina-bicelle possono essere adattate utilizzando attrezzature standard, compresi i robot di cristallizzazione ad alto rendimento24. La fattibilità dell'utilizzo delle bicelle, tuttavia, dipende dalla termostabilità delle proteine dovuta alle condizioni di cristallizzazione a temperature più elevate. Tuttavia, rispetto ad altre tecniche, le condizioni di cristallizzazione richieste per le proteine di membrana rimangono generalmente miti, coinvolgendo basse concentrazioni di precipitante, sale e tampone. Ciò rende sia le miscele proteina-bicelle che la diffusione del vapore strumenti efficaci e facilmente implementabili per gli studi strutturali delle proteine di membrana.
Questo protocollo delinea le fasi essenziali nella preparazione delle proteine e nella cristallizzazione bicellulare per determinare la struttura cristallina a raggi X di ABCG5/G8 ad alta risoluzione (Figura 1).
Protocollo
1. Clonaggio ed espressione proteica
- Clonare il gene umano ABCG5/G8 nel lievito Pichia pastoris seguendo i protocolli precedenti25,26. In breve, derivare i vettori di espressione pSGP18 e pLIC da pPICZB. Aggiungere un tag che codifica per un sito di proteasi 3C del rinovirus seguito da un peptide legante la calmodulina (CBP) all'estremità C del cDNA ABCG8 (pSGP18-G8-3C-CBP).
- Aggiungere un tag di sei-istidina separato da una glicina (His 6GlyHis6) al C-terminale del cDNA ABCG5 (pLIC-G5-H12). Co-trasformare i plasmidi nel ceppo Pichia KM71H utilizzando l'elettroporazione.
NOTA: Si prega di consultare la Tabella dei materiali per i dettagli dei plasmidi, dei terreni e dei tamponi utilizzati. - Coltivare cellule di lievito trasformate su piastre di agar MD a 28 °C.
- Aggiungere un tag di sei-istidina separato da una glicina (His 6GlyHis6) al C-terminale del cDNA ABCG5 (pLIC-G5-H12). Co-trasformare i plasmidi nel ceppo Pichia KM71H utilizzando l'elettroporazione.
- Dopo 1-2 giorni, selezionare 10-12 colonie e inocularle in 10 mL di terreno a base di azoto di lievito (MGY) a base minima di glicerolo utilizzando provette da centrifuga da 50 mL per colture su piccola scala.
- Praticare tre piccoli fori nel coperchio della provetta da centrifuga per una migliore aerazione. Lasciare crescere le cellule a 28 °C con agitazione costante a 250 giri/min fino a quando la densità ottica a 600 nm (OD600) raggiunge 10, di solito impiegando 1-2 notti.
NOTA: La crescita cellulare richiede solitamente tra le 12 e le 24 ore.
- Praticare tre piccoli fori nel coperchio della provetta da centrifuga per una migliore aerazione. Lasciare crescere le cellule a 28 °C con agitazione costante a 250 giri/min fino a quando la densità ottica a 600 nm (OD600) raggiunge 10, di solito impiegando 1-2 notti.
- Il giorno successivo, prelevare 1 litro di terreno MGY sterile e inoculare la coltura primaria in un pallone da 2,4 litri. Incubare il matraccio a 28 °C in un incubatore agitatore a 250 giri/min per 24 ore.
- Per mantenere il pH tra 5-6, aggiungere il 10% di idrossido di ammonio (NH4OH) fino a quando il pH non si stabilizza.
- Regolare il pH e indurre l'espressione proteica aggiungendo 1 mL di metanolo puro per 1 L di coltura (0,1 % (v/v) di metanolo).
NOTA: Alimentare le cellule successivamente con 5 mL di metanolo puro per litro di coltura (0,5 % (v/v) di metanolo) ogni 12 ore per una durata totale di 36-48 ore. - Raccogliere le cellule centrifugando a 15.000 x g per 30 minuti a 4 °C.
- Raccogliere i pellet cellulari e risospenderli in tampone di lisi (0,33 M di saccarosio, 0,3 M Tris-Cl pH 7,5, 0,1 M di acido amminoesanoico, 1 mM di EDTA e 1 mM di EGTA) a una concentrazione di 0,5 g/mL. Conservare la sospensione a -80 °C. Tipicamente, si possono recuperare 30 ± 5 g di massa cellulare da 1 L di cellule in coltura.
NOTA: Conservare i pellet cellulari direttamente nel congelatore o eseguire la risospensione immediata nel tampone di lisi per le preparazioni a membrana.
2. Preparazione della membrana microsomiale
- Scongelare le cellule e aggiungere inibitori della proteasi (2 μg/mL di leupeptina, 2 μg/mL di pepstatina A, 2 mM di PMSF, vedere la tabella dei materiali).
- Per lisare ulteriormente le cellule, utilizzare un emulsionante o un microfluidificatore ghiacciato (vedere la tabella dei materiali) a 25.000-30.000 psi. Ripeti questo processo 3-4 volte.
- Centrifugare per rimuovere i detriti cellulari: centrifugare a 3.500-4.000 x g per 15 min, seguita da una seconda centrifuga a 15.000 x g per 30 min. Mantenere entrambe le centrifughe a 4 °C.
- Per isolare le vescicole di membrana microsomiali, trasferire il surnatante in provette da ultracentrifuga e sottoporlo a ultracentrifugazione a 2.00.000 x g per 1,5 h a 4 °C.
- Risospendere il pellet di membrana in 50 mL di tampone A (50 mM Tris-Cl pH 8.0, 100 mM NaCl e 10% di glicerolo) utilizzando un omogeneizzatore dounce. Conservare la sospensione a -80 °C.
3. Preparazione-purificazione proteica di eterodimeri
- Scongelare le membrane microsomiali congelate e regolare la concentrazione a 4-6 mg/mL utilizzando il tampone di solubilizzazione. Il tampone deve contenere 50 mM di Tris-HCl, pH 8,0, 100 mM di NaCl, 10% di glicerolo, 1% (p/v) β-dodecil maltoside (β-DDM), 0,5% (p/v) colato, 0,1% (p/v) colesteril emisuccinato (CHS), 5 mM di imidazolo, 5 mM di β-mercaptoetanolo (β-ME), 2 μg/mL di leupeptina, 2 μg/mL di pepstatina A e 2 mM di PMSF (vedere la tabella dei materiali).
NOTA: Si possono miscelare volumi uguali della preparazione della membrana e del tampone di solubilizzazione, oppure utilizzare un tampone di solubilizzazione 2x senza inibitori della proteasi e agenti riducenti. Una breve ebollizione del tampone aiuta a sciogliere la CHS in modo efficiente. Per la purificazione, utilizzare solo il tampone raffreddato a 4 °C.- Mescolare il composto a velocità media per 1 h a 4 °C. Seguire con un'ulteriore agitazione a temperatura ambiente (RT) per 20-30 minuti.
- Centrifugare la miscela a 1,00,000 x g per 30 minuti a 4 °C per rimuovere le membrane insolubili. Raccogliere il surnatante solubilizzato e aggiungere 20 mM di imidazolo e 0,1 mM di TCEP.
- Eseguire la cromatografia su colonna di affinità26: legare il surnatante solubilizzato a microsfere di Ni-NTA pre-bilanciate (10-15 mL) (vedere Tabella dei materiali) nel tampone A (fase 2.2.1) durante la notte.
NOTA: Evitare l'uso di glicerolo nei tamponi in esecuzione da questo punto in poi.- Lavare due volte la colonna con 10 volumi di tampone B (50 mM di HEPES, pH 7,5, 100 mM di NaCl, 0,1 % (p/v) β-DDM, 0,05 % (p/v) di colato, 0,01 % (p/v) CHS, 0,1 mM di TCEP) contenente 25 mM di imidazolo.
- Lavare la colonna con 10 volumi di tampone B contenenti 50 mM di imidazolo.
- Eluire la proteina utilizzando il tampone C (tampone B con 200 mM di imidazolo).
- Aggiungere 1 mM di TCEP (vedi Tabella dei materiali) e 10 mM di MgCl2 alle proteine eluite.
- Convalidare le frazioni eluite su un gel SDS-PAGE per confermare la corretta dimensione della proteina26.
NOTA: Resa proteica tipica (1° Ni-NTA): 10-20 mg di proteine per coltura da 6 L. Utilizzare DDM a 10 o 5 volte la sua concentrazione di micelle critiche (CMC), circa lo 0,01%. Questo protocollo impiega lo 0,1% di DDM. - Diluire le frazioni di picco dall'eluizione Ni-NTA con un volume uguale di tampone D1 (tampone B con 1 mM CaCl 2, 1 mM MgCl2), mescolare e caricare le frazioni proteiche su una colonna CBP (3-5 mL) (vedere Tabella dei materiali) che è stata pre-bilanciata con il tampone di lavaggio CBP D1.
- Eseguire lavaggi sequenziali sulla colonna CBP per sostituire i detergenti utilizzando il Tampone D1 e D2 (Tampone B con 1 mM CaCl 2, 1 mM MgCl2, 0,1% (p/v) glicole neopentilico (DMNG) decil-maltosio (DMNG), senza β-DDM): lavare prima con 3 volumi di colonna di D1; in secondo luogo, lavare con 3 volumi di colonna di D1:D2 (3:1, v/v); terzo, lavare con 3 volumi di colonna di D1:D2 (1:1, v/v); quarta fase, lavaggio con 3 volumi di colonna di D1:D2 (1:3, v/v), seguiti da 6-10 volumi di colonna di D2.
- Eluire la proteina utilizzando il tampone D2 di lavaggio CBP con 300 mM di NaCl in frazioni da 1 mL dalla colonna CBP (totale 10 mL). Concentrare le frazioni eluite a 1-2 mL.
NOTA: La resa proteica tipica (1° CBP) è di 5-15 mg di proteine per 6 L di coltura. I detergenti a base di glicole neopentilico al maltosio (MNG) migliorano l'immagazzinamento delle proteine purificate a 4 °C. Sono stati utilizzati sia DMNG che Lauryl MNG (LMNG), con DMNG che produce migliori cristalli di diffrattazione dei raggi X. Utilizzare DMNG a 10-20 volte la sua concentrazione critica di micelle (CMC), circa lo 0,003%. Questo protocollo utilizzava lo 0,1% di DMNG. Una frazione dell'eluato CBP può essere ulteriormente purificata mediante cromatografia con filtrazione su gel (fase 4.4.) per analizzare l'attività dell'ATPasi delle proteine o valutare la monodispersione mediante microscopia elettronica a trasmissione (TEM).
4. Preparazione proteica-trattamento di pre-cristallizzazione
- Scindere i glicani legati all'N e i tag CBP utilizzando rispettivamente l'endoglicosidasi H (Endo H, ~0,2 mg per 10-15 mg di proteina purificata) e la proteasi HRV-3C (~2 mg per 10-15 mg di proteina purificata) (vedere la tabella dei materiali). Incubare una notte a 4 °C.
- Durante l'incubazione della proteasi Endo H e 3C, eseguire l'alchilazione riduttiva sulle proteine raggruppate. Iniziare incubando con iodoacetammide 20 mM (vedere Tabella dei materiali) per una notte a 4 °C. Seguire con un'incubazione di 1 ora con altri 2 mM di iodoacetammide su ghiaccio.
NOTA: Questo passaggio stabilizza ulteriormente la conservazione delle proteine per un massimo di un mese a 4 °C. - Utilizzare una seconda colonna CBP (1-2 mL) per separare il tag CBP scisso. Utilizzare il buffer D2 per questo processo.
NOTA: La resa proteica tipica (2° CBP) è di 5-10 mg di proteine per coltura da 6 L. - Purificare la proteina priva di tag CBP utilizzando la cromatografia con filtrazione su gel. Il tampone deve contenere 10 mM di HEPES, pH 7,5, 100 mM di NaCl, 0,1% (p/v) DMNG, 0,05% (p/v) colato e 0,01% (p/v) CHS.
NOTA: La resa proteica tipica (gel-filtrazione) è di 2-8 mg di proteine per coltura da 6 L. Durante questa fase, l'assenza di un picco DDM (~65 kD) durante la filtrazione del gel indica che il corretto scambio di detergente con DMNG è riuscito. - Modificare le frazioni proteiche aggregate attraverso la metilazione riduttiva: aggiungere 20 mM di dimetilammina borano (DMAB, vedi Tabella dei materiali) e 40 mM di formaldeide alla proteina. Incubare per 2 ore a 4 °C su agitatore oscillatorio. Aggiungere 10 mM di DMAB.
- Ripetere la fase 4.5, compresa l'aggiunta di 10 mM di DMAB, e incubare per una notte (12-18 ore) a 4 °C.
- Arrestare la reazione aggiungendo 100 mM di Tris-Cl, pH 7,5.
- Caricare la proteina metilata su una colonna Ni-NTA da 2 mL pre-bilanciata con 100 mM di Tris-Cl, pH 8,0 e 100 mM di NaCl.
- Lavare la colonna utilizzando 10 volumi di tampone di lavaggio (10 mM di HEPES, pH 7,5, 100 mM di NaCl, con 0,5 mg/mL DI DOPC: DOPE (3:1, p/p), 0,1% (p/v) DMNG, 0,05% (p/v) colato, 0,01% (p/v) CHS).
- Eluire la proteina relipidata utilizzando un tampone di eluizione (10 mM di HEPES, pH 7,5, 100 mM di NaCl, 200 mM di imidazolo, 0,5 mg/mL DI DOPC: DOPE (1:1, p/p), 0,1% (p/v) DMNG, 0,05% (p/v) di colato, 0,01% (p/v) CHS).
NOTA: La resa proteica tipica (2° Ni-NTA) è di 1-5 mg di proteine per coltura da 6 L. - Far passare gli eluati proteici attraverso una colonna di desalinizzazione PD-10 pre-bilanciata con il tampone utilizzato nella fase 4.4.
- Incubare la proteina dissalata e relipidata per una notte con colesterolo (preparato in isopropanolo o etanolo) fino a una concentrazione finale di ~20 μM.
- La mattina successiva, rimuovere il precipitante mediante ultracentrifugazione a 1,50,000 x g per 10 minuti a 4 °C. Raccogli il surnatante.
- Concentrare la proteina a una concentrazione finale di 30-50 mg/mL utilizzando un concentratore centrifugo cutoff da 100 kDa.
- Rimuovere il precipitante utilizzando una centrifuga refrigerata da banco alla massima velocità per 30 minuti a 4 °C.
- Mantenere il surnatante in ghiaccio a 4 °C e stabilire le condizioni di cristallizzazione nelle bicelle.
NOTA: Le proteine concentrate devono essere utilizzate per la crescita dei cristalli entro una settimana. Non congelare le proteine.
5. Cristallizzazione delle proteine nelle bicelle
- Preparare una soluzione madre bicellulare al 10% con lipidi DMPC e detergente CHAPSO in rapporto 3:1 (p/p) (vedere la tabella dei materiali).
NOTA: Utilizzare CHAPSO a 5 volte la sua concentrazione di micelle critiche (CMC), circa lo 0,5%. In questo modo si mantiene la concentrazione di detergente intorno al suo CMC nella miscela proteina-bicella (passaggio 5.2).- Aggiungere il detergente deionizzato H2O-disciolto (CHAPSO) ai lipidi pre-essiccati (miscela di 5 mol% di colesterolo e 95 mol% di DMPC).
NOTA: Preparare varie composizioni lipidiche in cloroformio e asciugarle in una provetta di vetro utilizzando un flusso di azoto gassoso a RT. Eliminare i solventi residui mettendoli in una camera a vuoto durante la notte, formando un sottile strato lipidico. - Sospendere i lipidi e il detergente utilizzando un sonicatore a bagnomaria.
- Sonicare la miscela bicellare in acqua ghiacciata utilizzando energia continua fino a quando la soluzione non diventa trasparente.
NOTA: Utilizzare protezioni per l'udito e garantire una fornitura di ghiaccio sufficiente per mantenere la miscela in fase liquida. - Rimuovere i componenti non disciolti con un filtro centrifugo da 0,2 μm (vedere la tabella dei materiali).
NOTA: Conservare la soluzione bicellulare aliquotata a -80 °C.
- Aggiungere il detergente deionizzato H2O-disciolto (CHAPSO) ai lipidi pre-essiccati (miscela di 5 mol% di colesterolo e 95 mol% di DMPC).
- Creare una miscela proteina/bicella su ghiaccio combinando delicatamente il 10% di bicelle (passaggio 5.1.4) e proteine (passaggio 4.7.4) in un rapporto 1:4 (v/v), ottenendo una concentrazione proteica finale compresa tra 5-10 mg/mL.
- Incubare la miscela proteica e bicellare su ghiaccio per 30 min.
- Impostare le condizioni di cristallizzazione in un formato di diffusione del vapore a goccia sospeso utilizzando piastre a 48 pozzetti.
- Miscelare volumi uguali (0,5 o 1 μL) di miscela proteina/bicella e soluzione serbatoio di cristallizzazione contenente 1,6 M-2,0 M solfato di ammonio, 100 mM MES (pH 6,5), 0%-4% PEG 400 e 1 mM TCEP (vedere la tabella dei materiali).
NOTA: Creare una matrice della soluzione serbatoio prima di ogni esperimento, regolando il solfato di ammonio (1,6-2,0 M) e il PEG 400 (0%-4%). - Incubare per la cristallizzazione a 20 °C.
- Controllare i vassoi di cristallizzazione il giorno successivo per garantire una corretta sigillatura del vetro di copertura.
- Monitorare la crescita dei cristalli almeno una volta al giorno. I cristalli di alta qualità di solito compaiono entro 1-2 settimane, misurando 50-150 μm x 20-50 μm x 2-5 μm.
NOTA: I cristalli possono richiedere più tempo per formarsi a concentrazioni proteiche inferiori. I cristalli maturi dovrebbero essere raccolti entro un mese. - Immergere i cristalli proteici in malonato di sodio 0,2 M e congelarli in azoto liquido utilizzando cryo-loop da 50 o 100 μm.
NOTA: Se è disponibile un diffrattometro a raggi X, testare alcuni cristalli con un'esposizione del fascio di raggi X di 15-30 minuti per rivelare una diffrazione fino a 5 Å. La diffrazione a risoluzione più elevata richiede una sorgente luminosa di sincrotrone. Utilizzando il malonato di sodio 0,2 M come crioprotettore, un cristallo di 100 μm x 50 μm x 2 μm può fornire circa 90 fotogrammi di immagini di diffrazione con raggi X di sincrotrone.
- Miscelare volumi uguali (0,5 o 1 μL) di miscela proteina/bicella e soluzione serbatoio di cristallizzazione contenente 1,6 M-2,0 M solfato di ammonio, 100 mM MES (pH 6,5), 0%-4% PEG 400 e 1 mM TCEP (vedere la tabella dei materiali).
Risultati
I semitrasportatori ABC ricombinanti, ABCG5 umano e ABCG8, sono co-espressi nel lievito Pichia pastoris . La frazione di membrana del lievito viene quindi frazionata mediante centrifugazione. Come indicato in questo protocollo, le proteine eterodimeriche vengono estratte utilizzando la cromatografia su colonna tandem. Successivamente, le proteine pretrattate chimicamente vengono cristallizzate incubandole con bicelle fosfolipidiche/colesterolo. Nella Figura 1 sono fornite panoramiche schematiche dei processi di purificazione e cristallizzazione.
Per valutare la monodispersità delle proteine purificate, i campioni contenenti 0,01-0,05 mg/mL di proteine vengono colorati con acetato di uranile all'1%-2%. Questi campioni vengono quindi esaminati utilizzando TEM con colorazione negativa (Figura 2A). Al fine di valutare la stabilità delle proteine senza subire cicli di gelo-disgelo, viene utilizzata la cromatografia analitica con filtrazione su gel. Questa analisi prevede il monitoraggio dell'immagazzinamento nel tempo delle proteine purificate attraverso l'uso di piccole aliquote di uguale volume delle proteine (Figura 2B). Dopo una settimana di incubazione a 4 °C, potrebbe verificarsi una leggera perdita di proteine nelle frazioni di picco, probabilmente a causa di aggregati proteici solubili residui. Ciononostante, la resa proteica complessiva rimane sufficiente per la crescita dei cristalli. L'uso del TEM a colorante negativo e della cromatografia analitica con filtrazione su gel è una pratica standard per valutare l'idoneità delle proteine per la cristallizzazione, in particolare da diversi costrutti ingegnerizzati.
Per la valutazione della qualità delle proteine in ogni fase del processo di cromatografia su colonna, nonché dopo il trattamento chimico di pre-cristallizzazione, aliquote di frazioni corrispondenti a due colonne Ni-NTA, due colonne CBP, una filtrazione su gel e alchilazione riduttiva vengono caricate su un gel SDS-PAGE al 10% (Figura 3). Inoltre, lo stesso ambiente di reazione utilizzato per l'alchilazione può essere applicato per la marcatura del mercurio con etilmercurio (EMTS), anche se questo esula dallo scopo del presente studio.
La crescita dei cristalli viene monitorata quotidianamente utilizzando uno stereomicroscopio da tavolo dotato di polarizzatore. I cristalli maturi e adatti alla raccolta dei dati raggiungono generalmente dimensioni di 50 μm x 100 μm x 2 μm (Figura 4). Durante il processo di raccolta dei cristalli, i cristalli più piccoli o i grappoli vengono deliberatamente evitati.
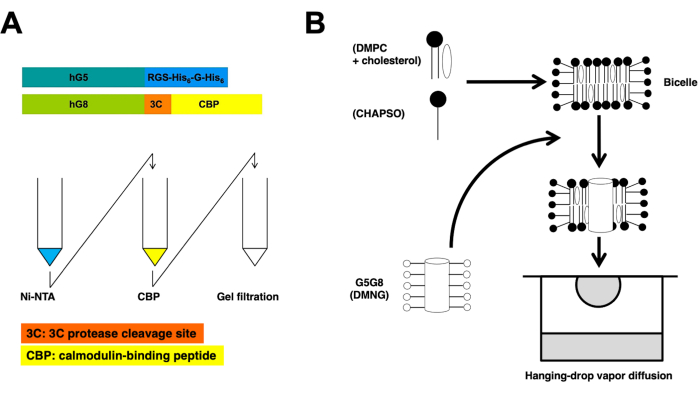
Figura 1: Panoramiche schematiche per la purificazione (A) e la cristallizzazione bicellulare (B) dell'eterodimerico ABCG5/G8. I costrutti di ABCG5 umano ricombinante (hG5) e ABCG8 (hG8) portano rispettivamente tag RGS-H 6-G-H6 e 3C-CBP (A, in alto). Cromatografia su colonna di affinità tandem, seguita da cromatografia con filtrazione su gel per ottenere la purificazione eterodimerica (A, in basso). Fare clic qui per visualizzare una versione più grande di questa figura.
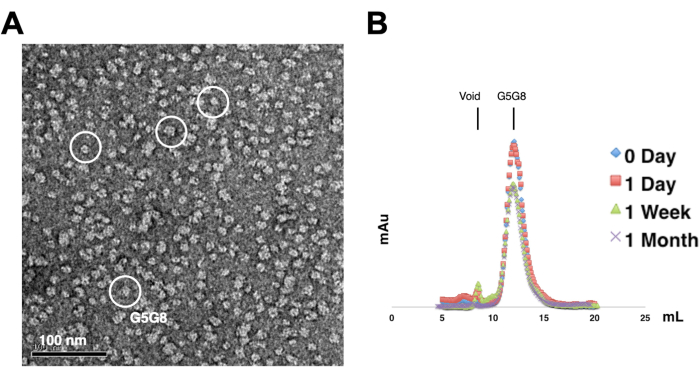
Figura 2: Valutazione della mono-dispersione (A) e della stabilità (B) di proteine purificate . (A) Micrografia elettronica di eterodimeri ABCG5/G8 (G5G8) colorati negativamente mediante TEM. Le particelle rappresentative sono evidenziate in cerchi bianchi pieni. Barra della scala = 100 nm. (B) Proteine alchilate conservate a 4 °C analizzate mediante cromatografia analitica con filtrazione su gel nel corso di un mese con una leggera perdita di proteine dopo una settimana. Fare clic qui per visualizzare una versione più grande di questa figura.
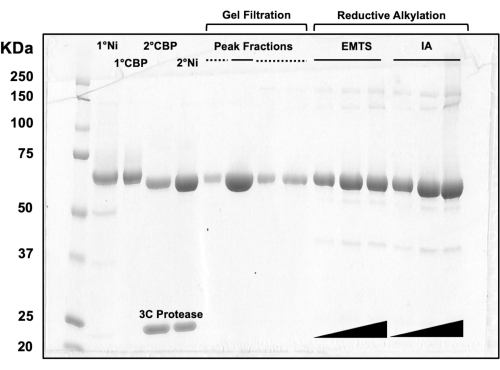
Figura 3: Analisi SDS-PAGE di eluati proteici di cromatografia su colonna e alchilazione riduttiva. Vari volumi (1-10 μL) di frazioni proteiche sono stati caricati su un gel di Tris/Glicina al 10% e fatti funzionare per 45 minuti a una tensione costante di 200 V. Il gel è stato colorato con blu Coomassie, decolorato, asciugato all'aria e scansionato da uno scanner da tavolo. 1° e 2° Ni: prima e seconda colonna Ni-NTA; 1° e 2° CBP: prima e seconda colonna CBP; Linea continua delle frazioni di picco: frazioni raggruppate per la cristallizzazione; Linea tratteggiata delle frazioni di picco: frazioni di spalla; EMTS: etilmercurio tiosalicinato; IA: iodoacedamide. Fare clic qui per visualizzare una versione più grande di questa figura.
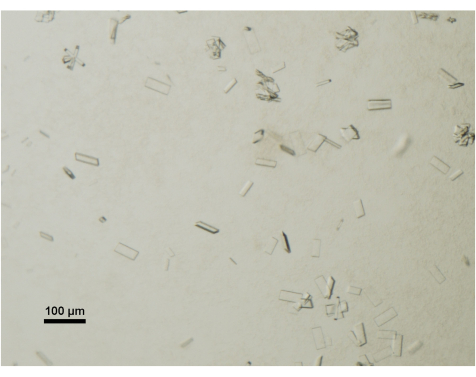
Figura 4: Valutazione della maturazione dei cristalli proteici mediante microscopia ottica. I cristalli maturi di ABCG5/G8 da una goccia di cristallizzazione sono stati visualizzati sotto un microscopio stereoscopico da tavolo e dotato di polarizzatore. Barra della scala = 100 μm. Fare clic qui per visualizzare una versione più grande di questa figura.
Discussione
Le sfide associate alla cristallizzazione delle proteine di membrana hanno spinto lo sviluppo di metodi di cristallizzazione guidati da doppio strato lipidico, come gli approcci bicellari27 o in fase cubica lipidica (LCP)14 . Tuttavia, il raggiungimento di una cristallizzazione di successo delle proteine di membrana dipende ancora dalla fase critica e talvolta strozzante della preparazione delle proteine. In particolare, i trasportatori ABC rappresentano un formidabile ostacolo nella crescita di cristalli adatti alla cristallografia a raggi X. Questo protocollo fornisce una guida pratica completa per semplificare la preparazione del trasportatore di steroli umano ABCG5/G8 e promuovere la crescita dei cristalli attraverso l'approccio di cristallizzazione bicellulare.
Una considerazione chiave nell'ideazione di questo protocollo è stata l'imperativo di una sostanziale resa proteica nelle fasi iniziali della purificazione proteica, consentendo un certo grado di perdita proteica durante il trattamento di pre-cristallizzazione (Figura 3). Le strategie comuni per affrontare questa sfida coinvolgono un'ampia ingegneria proteica, l'utilizzo di diversi ospiti di espressione e l'esplorazione di ortologhi o omologhi, tra gli altri approcci. Tuttavia, con questa procedura apparentemente intricata, sono stati identificati una serie di passaggi fondamentali che sono alla base del successo del protocollo e forniscono anche informazioni sui potenziali limiti che possono sorgere quando si studiano altri trasportatori ABC o proteine di membrana in generale.
In primo luogo, questo protocollo impiega un'accurata centrifugazione in ogni fase per ridurre al minimo l'aggregazione proteica. Inoltre, il monitoraggio continuo della termostabilità delle proteine purificate è fondamentale. La microscopia elettronica viene utilizzata per verificare la monodispersità delle proteine, mentre la filtrazione analitica su gel tiene traccia della stabilità delle proteine nel tempo (Figura 2). Potrebbero essere incorporate anche tecniche alternative come il dicroismo circolare (CD) o la calorimetria differenziale a scansione (DSC). Inoltre, l'incorporazione di lipidi in stadi specifici è essenziale per massimizzare sia l'attività che la cristallogenesi dell'ABCG5/G8 purificato. Ad esempio, il colato e la CHS sono necessari per esibire un'idrolisi misurabile dell'ATP; i fosfolipidi sono indispensabili per mantenere la stabilità delle proteine metilate; e il colesterolo è un componente necessario della soluzione bicellare, favorendo la crescita di cristalli adatti alla diffrazione di raggi X ad alta risoluzione (Figura 4).
In sostanza, l'intera procedura può essere eseguita in una settimana di sforzo. A differenza dell'LCP, il recupero dei cristalli dai vassoi di cristallizzazione a goccia sospesa è semplice. Guardando al futuro, con una notevole resa proteica (circa 10 mg), questo protocollo è facilmente adattabile per lo sviluppo di indagini cristallografiche che coinvolgono mutanti ABCG5/G8 o altre proteine trasportatrici. Ciò è particolarmente pertinente per i casi che attualmente sfuggono alla visualizzazione attraverso la microscopia elettronica.
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è supportato da una sovvenzione per la scoperta del Natural Sciences and Engineering Research Council (RGPIN 2018-04070) e da una sovvenzione per il progetto di ricerca del Canadian Institutes of Health (PJT-180640) a JYL. Questo protocollo si basa sui rapporti originali nelle strutture cristalline ABCG5/G8 riportati in precedenza da Farhat et al.22 e Lee et al.23.
Materiali
| Name | Company | Catalog Number | Comments |
| ABCG5 | National Institute of Health collection | NCBI accession number NM_022436 | |
| ABCG8 | National Institute of Health collection | NCBI accession number NM_022437 | |
| ÄKTA FPLC system | Cytiva (formerly GE Healthcare Life Sciences) | ||
| CaCl2 | Wisent | 600-024-CG | Anhydrous |
| CBP | Agilent | 214303 | Calmodulin binding peptide affinity resin |
| Centrifugal concentrators (Vivaspin) | Sartorius | ||
| CHAPSO | Anatrace | C317 | Anagrade |
| Cholesterol | Anatrace | CH200 | |
| CHS | Steraloids | C6823-000 | |
| DMAB | MilliporeSigma | 180238 | 97% |
| DMNG | Anatrace | NG322 | |
| DMPC | Anatrace | D514 | |
| DOPC | Avanti | 850375 | |
| DOPC | Anatrace | D518 | |
| DOPE | Avanti | 850725 | |
| DTT | Fisher | BP172 | |
| Dual Thickness MicroLoops | MiTeGen | ||
| EDTA | BioShop | EDT003 | Disodium salt, dihydrate |
| EGTA | MilliporeSigma | 324626 | |
| Emulsifier (EmulsiFex-C3) | Avestin | ||
| Endo H | New England Biolabs | P0702 | |
| Ethanol | Greenfield | P016EAAN | Ethyl Alcohol Anhydrous |
| Formaldehyde | MilliporeSigma | 252549 | ACS Reagent |
| Glycerol | BioShop | GLY004 | |
| HEPES | BioShop | HEP001 | |
| HRV-3C protease | Homemade | ||
| Imidazole | BioShop | IMD510 | Reagent grade |
| Iodoacetamide | MilliporeSigma | I1149 | BioUltra |
| Isopropanol | Fisher | BP2618212 | |
| Leupeptin | BioShop | LEU001 | |
| MES | MilliporeSigma | 69892 | BioUltra |
| Methanol | Fisher | A412P | |
| MgCl2 | Wisent | 800-070-CG | Hydrated |
| microfluidizer (LM 20) | Microfluidics | ||
| NaCl | BioShop | SOD002 | |
| NH4OH | Fisher | A669-212 | ACS Reagent |
| Ni-NTA superflow | Qiagen | 30430 | Nickel-charged resins |
| PEG 400 | MilliporeSigma | 202398 | |
| Pepstatin | BioShop | PEP605 | |
| PMSF | MilliporeSigma | P7626 | |
| pSGP18 and pLIC | Homemade (derived from pPICZ, Invitrogen) | ||
| SDS | BioShop | SDS003 | |
| Sodium cholate | Fisher | 229101 | |
| Sodium malonate | MilliporeSigma | 63409 | |
| Sucrose | Wisent | 800-081-WG | Ultra pure |
| Superdex 200 30/100 GL | Cytiva (formerly GE Healthcare Life Sciences) | 28990944 | Prepacked gel-filtration column |
| TCEP | |||
| TEM | FEI, Technai | ||
| Tris Base | Fisher | BP152 | |
| β-DDM | Anatrace | D310S | Sol Grade |
| β-mercaptoethanol | MilliporeSigma | ||
| ε-aminocaproic acid | Fisher | AAA1471936 |
Riferimenti
- Hamada, H., Tsuruo, T. Purification of the 170- to 180-kilodalton membrane glycoprotein associated with multidrug resistance. 170- to 180-kilodalton membrane glycoprotein is an ATPase. Journal of Biological Chemistry. 263 (3), 1454-1458 (1988).
- Higgins, F., Hiles, D., Whalley, K., Jamieson, J. Nucleotide binding by membrane components of bacterial periplasmic binding protein-dependent transport systems. The EMBO Journal. 4 (4), 1033-1039 (1985).
- Higgins, F., et al. A family of related ATP-binding subunits coupled to many distinct biological processes in bacteria. Nature. 323 (6087), 448-450 (1986).
- Horio, M., Gottesman, M., Pastan, I. ATP-dependent transport of vinblastine in vesicles from human multidrug-resistant cells. Proceedings of the National Academy of Sciences of the United States of America. 85 (10), 3580-3584 (1988).
- Mimmack, L., et al. Energy coupling to periplasmic binding protein-dependent transport systems: stoichiometry of ATP hydrolysis during transport in vivo. Proceedings of the National Academy of Sciences of the United States of America. 86 (21), 8257-8261 (1989).
- Grundy, M. Absorption and Metabolism of Dietary Cholesterol. Annual Review of Nutrition. 3 (1), 71-96 (1983).
- Berge, E., et al. Accumulation of dietary cholesterol in sitosterolemia caused by mutations in adjacent ABC transporters. Science. 290 (5497), 1771-1775 (2000).
- Repa, J., et al. Regulation of ATP-binding cassette sterol transporters ABCG5 and ABCG8 by the Liver X receptors α and β. Journal of Biological Chemistry. 277 (21), 18793-18800 (2002).
- Yu, L., et al. Stimulation of cholesterol excretion by the Liver X receptor agonist requires ATP-binding cassette transporters G5 and G8. Journal of Biological Chemistry. 278 (18), 15565-15570 (2003).
- Yu, L., et al. Expression of ABCG5 and ABCG8 is required for regulation of biliary cholesterol secretion. Journal of Biological Chemistry. 280 (10), 8742-8747 (2005).
- Lütjohann, D., Björkhem, I., Beil, F., von Bergmann, K. Sterol absorption and sterol balance in phytosterolemia evaluated by deuterium-labeled sterols: effect of sitostanol treatment. Journal of Lipid Research. 36 (8), 1763-1773 (1995).
- Miettinen, A. Phytosterolaemia, xanthomatosis and premature atherosclerotic arterial disease: a case with high plant sterol absorption, impaired sterol elimination and low cholesterol synthesis. European Journal of Clinical Investigation. 10 (1), 27-35 (1980).
- Salen, G., et al. Sitosterolemia. Journal of Lipid Research. 33 (7), 945-955 (1992).
- Caffrey, M. Membrane protein crystallization. Journal of Structural Biology. 142 (1), 108-132 (2003).
- Michel, H. Crystallization of membrane proteins. Trends in Biochemical Sciences. 8 (2), 56-59 (1983).
- Dürr, N., Gildenberg, M., Ramamoorthy, A. The magic of bicelleslights up membrane protein structure. Chemical Reviews. 112 (11), 6054 (2012).
- Dürr, N., Soong, R., Ramamoorthy, A. When detergent meets bilayer: Birth and coming of age of lipid bicelles. Progress in nuclear magnetic resonance spectroscopy. 69 (1), 1-22 (2013).
- Dufourc, J. Bicelles and nanodiscs for biophysical chemistry. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1863 (1), 183478 (2021).
- Beaugrand, M., et al. Lipid concentration and molar ratio boundaries for the use of isotropic bicelles. Langmuir. 30 (21), 6162-6170 (2014).
- Sanders, R., Schwonek, P. Characterization of magnetically orientable bilayers in mixtures of dihexanoylphosphatidylcholine and dimyristoylphosphatidylcholine by solid-state NMR. Biochemistry. 31 (37), 8898-8905 (1992).
- Seddon, M., Curnow, P., Booth, J. Membrane proteins, lipids and detergents: not just a soap opera. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1666 (1-2), 105-117 (2004).
- Farhat, D., et al. Structural analysis of cholesterol binding and sterol selectivity by ABCG5/G8. Journal of Molecular Biology. 434 (20), 167795 (2022).
- Lee, J. Y., et al. Crystal structure of the human sterol transporter ABCG5/ABCG8. Nature. 533 (7604), 561-564 (2016).
- Ujwal, R., Bowie, U. Crystallizing membrane proteins using lipidic bicelles. Methods. 55 (4), 337-341 (2011).
- Johnson, H., Lee, J. Y., Pickert, A., Urbatsch, L. Bile acids stimulate ATP hydrolysis in the purified cholesterol transporter ABCG5/G8. Biochemistry. 49 (16), 3403-3411 (2010).
- Wang, Z., et al. Purification and ATP hydrolysis of the putative cholesterol transporters ABCG5 and ABCG8. Biochemistry. 45 (32), 9929-9939 (2006).
- Faham, S. Crystallization of bacteriorhodopsin from bicelle formulations at room temperature. Protein Science. 14 (3), 836-840 (2005).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon