このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
ポリアクリルアミドゲルでのタンパク質の迅速かつ高感度コロイドクマG - 250染色
要約
このビデオでは、カンによるとコロイドクマG - 250染色プロトコールを普及するものとら。ゲルの平均4 ngのタンパク質の検出のための。染色は2時間以内と何の努力もせずに完了します。我々は日常的にゲルベースのプロテオミクス、分析目的のためにカンのプロトコルを使用してください。
要約
クマシーブリリアントブルー(CBB)は、一般的にシンプルな染色法と高い定量を提供し、SDS - PAGEにより分離されたタンパク質の可視化のために使用される色素です。さらに、質量分析、タンパク質の同定と完全に互換性があります。しかし、これらの利点にもかかわらず、CBBは、銀や蛍光stainingsよりも感度が低いとみなされるため、分析用ゲル電気泳動ベースのプロテオミクスのアプローチ中のタンパク質の検出に用いることはめったにありません。
オリジナルのクマプロトコル1のいくつかの改良がCBBの感度を高めるために行われています。二つの主要な変更は、コロイド粒子に色素分子を変換することにより、低濃度タンパク質の検出を強化するために導入されました:1988年、Neuhoffらは、CBB G - 250ベースの染色液2に20%メタノールおよび硫酸アンモニウムの高濃度を適用し、そして2004年にCandiano ら 。硫酸アンモニウムとメタノール3の存在下でリン酸とCBB G - 250を使用して確立されたブルーシルバー 。それにもかかわらず、これらすべての修正はわずか約10 ngのタンパク質の検出を可能にする。コロイドクマシー染色のための広くfamelessプロトコルは、Kang らによって出版された。彼らは錯化物質に関するNeuhoffのコロイドCBB染色のプロトコルを変更した2002年。代わりに硫酸アンモニウムを彼らは硫酸アルミニウムとメタノールが毒性の少ないエタノール4によって置き換えられたために使用。小説アルミベースのカンの研究では染色はタンパク質によって若干の感度のばらつきとは1 ng /バンド(ホスホリラーゼb)のように低い検出する優れた感度を示した。
ここでは、分析目的のタンパク質の迅速かつ高感度コロイドクマシー染色のためのカンのプロトコルのアプリケーションを示しています。我々は日常的に私たちのワーキンググループで行われる二次元のゲルを使って素早く簡単にプロトコルを説明します。
プロトコル
パート1:カップローディングを使用して二次元(2 - D)ゲル電気泳動
- IPGストリップの水和と等電点電気泳動(IEF)
- 125μlの補液でイモビのDryStripゲル、pHが6-11(7 cm)の水和する[7 M尿素、2 Mチオ尿素、4%CHAPS、50 mMリンhydroxyethyldisulfideと2%IPGの緩衝液pH 6月11日]のためにイモビDryStrip Reswellingトレイを使用して少なくとも10時間。
- [7 M尿素、2 Mチオ尿素、2%CHAPS、2%ASB - 14、50mMリンhydroxyethyldisulfideと2%IPGの緩衝液pH 6月11日]を100μl当たり60から100μgのタンパク質に対応するIEFサンプル緩衝液中で沈殿したタンパク質試料を溶かす。
- 可溶化(室温で少なくとも30分間)した後、サンプルカップを使用してカップローディング陽極を介してタンパク質のサンプルを適用する。カップの容量は100μlである(マニホールドのコップは150μLまでできます)。
注:あなたが焦点を当てプロトコルと詰め替えの先頭にカップを低電圧ステップを挿入するとカップの液膜が残っている間に、より大きなサンプルの量を読み込むことができます! - Multiphor II電気泳動ユニットの勾配モードで11.1 KVHのために等電点電気泳動法を実行します。
- 平衡とSDS - PAGE
- IEF後、IPGストリップを平衡化溶液中でそれぞれ1%ジチオスレイトール、2.5%のヨードアセトアミドを使用して、シェーカーにするたびに、減少してアルキル化するために15分を行った[50 mMのTris-HCl/pH 8.8、6 M尿素、30%グリセロールと2%SDS]。
- H 2 Oで平衡化したストリップをリンスし、余分な平衡化バッファーを削除するにはワットマンのペーパーにそれらを覆い隠す。その後、SDSランニングバッファー(1X)のストリップを浸し。
- 二次元目は12%の総アクリルアミド濃度の垂直電気泳動システムでSDS - PAGEによって実行されます。平衡化したIPGストリップは、[ブロモフェノールブルーを含むバッファ動作し、0.5%アガロース]を分離ゲルの上に置かれ、熱いアガロース溶液で固定した。
- タンパク質は、色素フロントがゲルカセットの底に達するまで、120 Vに続いて15分間80 Vから始まる、2.5時間のために分離した。
パート2:CBB G - 250コロイドCoomassie染色
1。染色液
注:ミリポアシステム(Milli - Q水)から取得として染色溶液の調製のために、このような分析グレード(PA)と高純度の水のような高品質で化学品を使用。
| クマのソリューション: | 広告2000ミリリットルH 2 O | |
| 0.02%(w / v)の | CBB G - 250 | 0,4グラム |
| 5%(w / v)の | 硫酸アルミニウム-(14-18) - 水和物 | 100グラム |
| 10%(v / v)の | エタノール(96%) | 200ミリリットル |
| 2%(v / v)の | オルトリン酸(85%) | 47ミリリットル |
注:染色溶液の調製のために、次の順序でコンポーネントを逐次添加を維持する必要がある。
- 第一Milli - Q水に硫酸アルミニウムを溶解する
- その後、エタノールを追加してホモジナイズし、解決するためにCBB G - 250を混在させる
- ソリューションが完全に溶解されているように、最近、リン酸を(アルコールのメディアへの酸の取り込みは、そのコロイド状態に集約し、クマシー分子をすることができます)を追加
- 最終的にMilli - Q水でいっぱいに
注:最終的な染色液は濃い緑、青味のある外観をして泳ぐの粒子に満ちている:
- ろ液は、このソリューションはいけない!
- あなたが準備の順序を変更した場合、あなたは、機密性の低い、よりバイオレット-青みがかったソリューションになるだろう。
| ソリューションを脱染: | 広告2000ミリリットルH 2 O | |
| 10%(v / v)の | エタノール(96%) | 200ミリリットル |
| 2%(v / v)の | オルトリン酸(85%) | 47ミリリットル |
2。染色手順
- 二次元目の分離後、慎重にガラス板からゲルを取り出して、Milli - Q水で満たされた染色皿にそれらを転送する。
- 水平シェーカーで10分間ゲルをMilli - Q水で3回洗浄し(ゲル上の残りのSDSは、タンパク質への染料の境界を乱すので、不十分な洗浄は貧しい感受性を引き起こす)。
- 均等にコロイド粒子を分散させるために使用する前に、クマシーソリューションを振る。
- よく2月12日時間シェーカー上で攪拌によってクマシーソリューションで覆われたゲルをインキュベートする。あなたが間に染色の進行状況を監視できるように、この染色は、マージナルな背景を生成します。
注:10分後には、インキュベーションの2時間以内に約80%がそれに染色、最初に表れるの蛋白質スポットを見ることができますsの最大レベルは完了です。ほぼ100%の染色の場合は、一晩インキュベーションすることをお勧めします。いくつかのケースでは、染色されるタンパク質の量は膨大であり、解決策が明るい青色に変わるときに、染色液のリフレッシュは必要です。 - 染色手順の後にクマの液を除去し、Milli - Q水で二回ゲルをすすぐ。
注:粒子が依然として残っているように限り、染色液を再利用できる、そうでなければ(あなたの研究室では廃棄物処理のための特別な規制があるかもしれないことに注意して)それを捨てる。 - 糸くずの出ないペーパータオルで染色皿から染料粒子を付着取り外し、10秒間汚れを除く - 60分。
注:またばかりMilli - Q水でゲルを洗浄することができますが、スキャン手順中に発生する予定ゲルで不規則な、弱いクマの映画をそこに続くので、これは我々が取ゲルのためにのみお勧めします。 - 最後にMilli - Q水で二回ゲルをすすぎ:ゲルは、元の厚さに達する(アルコール酸のメディアは、ゲルの縮小を行う)と中和水に加えてクマの色の強度を高めるでしょう。
パート3:代表的な結果
あなたが上記のプロトコルに従うのであれば、あなたの2次元ゲル独特の解決と同様ステンドダークブルーの蛋白質スポットを取得します。にもシェフチェンコら 5、質量分析との良好な感度との互換性を主張するプロトコルに応じて銀で染色した2 - Dゲルと比較して、我々は同じ染色の結果を達成する。
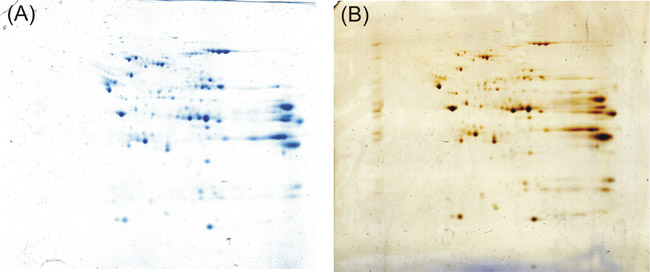
図1:上記の実験の最終結果。カン氏のクマシープロトコル()シェフチェンコらによれば、銀染色のように強く行います。(B)2 - Dゲル電気泳動後にタンパク質を検出する。
パート4:ヒントとテクニック
- 独自のサンプルを処理する前にいくつかのテストstainingsを実行します。説明のつかない理由のため私たちはミリグラムが適用された場合でも、目的のタンパク質が正常に検出できないことが時々報告。このケースでは、感度をテストするための希釈系列を用意することをお勧めします。
- あなたがゲル内の一般のタンパク質の検出(の)低いがある場合は、SDS - PAGE中に分離ゲルにスタッキングから失敗の転送は、おそらく理由になります。あなたは、スタッキングエリアを含む完全なゲルを染色することによってそのような粘着性のタンパク質を確認することができます。
- あなたの等電点電気泳動結果の高速な検証では、直接それ以上の二次元分離することなくIPGストリップを染色することができます。
- 彼らは(あなたがゲルに心を動かされない続ければ、色素がちょうどゲルの片側に結合する)両側から均等に染色されるので、時々染色手順の実行中にゲルを回します。
- 私たちは、暗い瓶の中に染色液のその記憶を経験し、その寿命を(透明ボトルで、最大4ヶ月間まで)増加する。
- 染色と文書化した後に、(あなたが酸性溶液を追加する場合には菌類による汚染を避けるために)数年間冷蔵庫でゲルを保つことができます。
- トリプシン消化物をゲルプラグの脱色は、ブロックヒーターで温暖化によって加速することができる。
ディスカッション
革新的なまたは単に別のクマのプロトコル?
現時点ではクマシーブリリアントブルーで手続きを染色するための複数のプロトコルが存在する。それらのほとんどはNeuhoffと同僚2で最も一般的に使用されるプロトコルのいずれかのマイナーまたはメジャーの変更に起因する。また、カンのプロトコルは、Neuhoffの式に基づいた。しかし、それは本当にプロテオミクス...
開示事項
謝辞
我々は1 - Dゲルの調製および染色のために博士ニコラWiethölterに感謝。
この作品は、ドイツ学術振興(NDとSMへのGRK 1089/project 5)からの助成金によって資金を供給され、NDに財団ユルゲンManchotから研究フェローシップによってサポートされていました。
資料
| 製品の名称 | 会社 | カタログ番号 | コメント |
| IEFとSDS - PAGE用: | |||
| イモビDryStripゲル | GEヘルスケア | 17-6001-94 | さらに有効期限を2年後に使用することができます。 |
| イモビDryStrip Reswellingトレイ | GEヘルスケア | 80-6371-84 | 有機溶剤で洗浄しないでください。 7〜18センチメートルIPGストリップのために設計されています。 |
| イモビDryStripキット | GEヘルスケア | 18-1004-30 | トレイ、電極ホルダー、アノードとカソード電極、アライナーとサンプルカップバーとサンプルカップを含みます。 |
| EPS 3501 XLの電源 | GEヘルスケア | 18-1130-05 | 消耗品は、3500までの電圧V |
| Multiphor II電気泳動ユニット | GEヘルスケア | 18-1018-06 | 可動電極は、すべての長さのIPGストリップにIEFを有効にする(7〜24センチメートルはストリップをIPG) |
| PerfectBlueゲルシステムツインS | Peqlab | 45から1010 - C | 10 × 10センチメートルミニゲルフォーマットでSDS - PAGE。ゲルチャンバーは、冷却システムが含まれています。 |
| コロイドクマG - 250染色の場合: | |||
| 蓋付染色皿 | VWR | 216-3412 | ミニゲルのはめあい。シェーカーでスタッカブル。 |
| 硫酸アルミニウム- 18 -水和物 | メルク | 1.01102.5000 | 我々は、メルクとの最高の体験をしました。 5kgのパッケージでだけ利用できる。 |
| オルトリン酸 | Prolabo | 20 624.295 | ガラスびんで販売。 |
参考文献
- Fazekas de St Groth, S., Webster, S. R. G., Datyner, A. Two new staining procedures for quantitative estimation of proteins on electrophoretic strips. Biochim. Biophys. Acta. 71, 377-391 (1963).
- Neuhoff, V., Arold, N., Taube, D., Ehrhardt, W. Improved staining of proteins in polyacrylamide gels including isoelectric focusing gels with clear background at nanogram sensitivity using Coomassie Brilliant Blue G-250 and R-250. Electrophoresis. 9, 255-262 (1988).
- Candiano, G., Bruschi, M., Musante, L., Santucci, L., Ghiggeri, G. M., Carnemolla, B., Orecchia, P., Zardi, L., Rigetti, P. G. Blue Silver: A very sensitive colloidal Coomassie G-250 staining for proteome analysis. Electrophoresis. 25, 1327-1333 (2004).
- Kang, D., Gho, S. G., Suh, M., Kang, C. Highly Sensitive and Fast Protein Detection with Coomassie Brilliant Blue in Sodium Dodecyl Sulfate-Polyacrylamide Gel Electrophoresis. Bull. Korean Chem. Soc. 11, 1511-1512 (2002).
- Shevchenko, A., Wilm, M., Vorm, O., Mann, M. Mass spectrometric sequencing of proteins silver-stained polyacrylamide gels. Anal. Chem. 68, 850-858 (1996).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved