このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
細胞輸送の陽電子放出断層撮影イメージング:細胞放射性標識法
要約
ここに示されるすぐに使用できるradiolabelingシントンを使用して陽電子放出断層撮影(ペット)の放射性同位体、 89Zr (t1/2 78.4 h)の放射性分類のセルにプロトコルはある、[89Zr] Zr-p-isothiocyanatobenzyl-desferrioxamine ([89Zr] Zr-DBN)。[89Zr]Zr-DBNを用いた放射性標識細胞は、投与後最大7日間、PETで体内に投与された放射性標識細胞の非侵襲的な追跡とイメージングを可能にします。
要約
幹細胞およびキメラ抗原受容体(CAR)T細胞療法は、臓器再生の有望な治療法として、またさまざまながんの免疫療法として浮上しています。これらの分野では大きな進歩が見られましたが、生体系で投与された治療細胞の薬物動態と薬力学をよりよく理解するためには、さらに多くのことを学ぶ必要があります。陽電子放射断層撮影法(PET)による細胞の非侵襲的in vivo追跡のために、89 Zr(t1/2 78.4 h)を利用して、新しい[89Zr]Zr-p-イソチオシアナトベンジル-デスフェリオキサミン([89Zr]Zr-DBN)を介した細胞放射性標識法が開発されました。現在のプロトコルは間葉系幹細胞、血統導かれた心poietic幹細胞、肝細胞、白血球、メラノーマの細胞および樹状細胞を再生するレバーを含むいろいろなセルの直接radiolabelingのための[89Zr] ZrDBN仲介された、すぐに使用できる、radiolabelingシントンを記述する。開発された方法論は、放射性標識細胞の性質や機能に影響を与えることなく、投与後最大7日間、細胞輸送の非侵襲的PETイメージングを可能にします。さらに、このプロトコルは[89Zr] Zr-DBN、[89 Zr] Zr-DBNのbiocompatible公式、radiolabelingのためのセルの準備、および最終的にセルの巧妙なradiolabelingに必要なすべての複雑な細部を含む[89Zr] ZrDBNのセルのradiolabelingのための段階的な方法を、記述する。
概要
幹細胞およびキメラ抗原受容体(CAR)T細胞療法は人気が高まっており、心筋不全1,2、網膜変性2、黄斑変性2、糖尿病2、心筋梗塞3,4,5、癌6,7,8,9などのさまざまな疾患の治療のために活発に研究されています。10.幹細胞療法の2つの妥当なアプローチのうち、幹細胞は疾患部位に直接生着して治療反応を引き起こすか、疾患部位に付着せずに疾患部位の微小環境に変化を引き起こして間接的な治療反応を開始することができます。間接的な治療反応は、疾患を修復または治療する因子を放出することにより、疾患部位の微小環境の変化を引き起こす可能性があります5。幹細胞治療のこれらのアプローチは、放射性標識幹細胞の非侵襲的イメージングによって評価できます。非侵襲的イメージングは、疾患部位上の放射性標識細胞の取り込みを治療反応と相関させて、直接的および間接的な治療的反応を解読することができます。
さらに、CAR-T細胞6,7,8,9,10および樹状細胞免疫療法11,12を使用して、さまざまな癌を治療するための免疫細胞ベースの治療法が開発されています。機構的には、CAR-T細胞免疫療法6,7,8,9,10では、T細胞は、治療が必要な腫瘍上の特定の抗原に結合するエピトープを発現するように操作されます。これらの改変されたCAR-T細胞は、投与されると、エピトープ-抗原相互作用を介して腫瘍細胞上に存在する特異的抗原に結合します。結合後、結合したCAR-T細胞は活性化を受け、増殖してサイトカインを放出し、宿主の免疫系に特定の抗原を発現する腫瘍を攻撃するように信号を送ります。対照的に、樹状細胞療法11,12の場合、樹状細胞は、その表面に特異的な癌抗原を提示するように操作される。これらの操作された樹状細胞は、投与されると、リンパ節に宿り、リンパ節のT細胞に結合します。T細胞は、投与された樹状細胞上の特定のがん抗原に結合すると、活性化/増殖を受け、その特定の抗原を発現する腫瘍に対する宿主の免疫応答を開始します。したがって、投与されたCAR-T細胞の腫瘍部位への輸送9,10およびリンパ節11,12への樹状細胞のホーミングの評価は、免疫療法の有効性を決定するために放射性標識CAR-T細胞および樹状細胞をイメージングすることによって可能である。さらに、非侵襲的細胞輸送は、治療の可能性をよりよく理解し、直接的および間接的な治療反応を明確にし、幹細胞および免疫細胞ベースの治療の両方の治療反応を予測および監視するのに役立ちます。
細胞輸送のためのさまざまなイメージングモダリティが検討されています3,4,9,10,12、これには、光イメージング、磁気共鳴画像法(MRI)、単一光子放出型コンピュータ断層撮影法(SPECT)、陽電子放射断層撮影法(PET)が含まれます。これらの手法には、それぞれ長所と短所があります。これらの中でも、PETは、その定量性と高感度により、最も有望なモダリティであり、イメージングベースの細胞輸送における細胞の信頼性の高い定量に不可欠です3,4,9,10。
半減期が78.4時間の陽電子放出放射性同位体89Zrは、細胞標識に適しています。1週間以上の細胞輸送のPETイメージングが可能で、広く入手可能な低エネルギー医療用サイクロトロン13,14,15,16,17で容易に製造できます。さらに、適切に官能基化されたp-イソチオシアナトベンジル-デスフェリオキサミン(DFO-Bn-NCS)キレート剤は、89 Zr標識、すぐに使用できる、細胞標識シントン、[89Zr]Zr-p-イソチオシアナトベンジル-デスフェリオキサミン([89Zr]Zr-DBN18,19,20,21,22,23,24としても知られる)の合成のために市販されている、25。[89 Zr]Zr-DBNを介した細胞標識の原理は、細胞膜タンパク質の第一級アミンと[89Zr]Zr-DBNのイソチオシアネート(NCS)部分との反応に基づいており、安定な共有結合チオ尿素結合を生成します。
[89ZR]幹細胞18,23,25、樹状細胞18、心形成幹細胞19、脱落間質細胞20、骨髄由来マクロファージ20、末梢血単核細胞20、Jurkat/CAR-T細胞21、肝細胞22,24、白血球25など、さまざまな細胞を追跡するために、Zr-DBNベースの細胞標識とイメージングが発表されています.次のプロトコルは[89Zr] Zr-DBNの調製そしてセルradiolabelingのステップバイステップ方法を提供し、特定のセルタイプのためのradiolabelingプロトコルで要求されるかもしれない変更を記述する。より明確にするために、ここで紹介する細胞放射性標識の方法は4つのセクションに分かれています。最初のセクションでは、DFO-Bn-NCSで89 Zrをキレート化することにより、[89Zr]Zr-DBNを調製します。第2章では、細胞放射性標識に容易に使用できる[89Zr]Zr-DBNの生体適合性製剤の調製について説明します。第3章では、放射性標識のための細胞のプレコンディショニングに必要なステップについて説明します。細胞のプレコンディショニングには、タンパク質を含まないリン酸緩衝生理食塩水(PBS)およびHEPES緩衝ハンクス平衡塩溶液(H-HBSS)で細胞を洗浄し、放射性標識中に細胞表面タンパク質に存在する第一級アミンと[89Zr]Zr-DBNの反応を妨害または競合する可能性のある外部タンパク質を除去することが含まれます。最後のセクションでは、細胞の実際の放射性標識と品質管理分析に関連するステップについて説明します。
プロトコル
樹状細胞およびメラノーマ細胞は商業的に得られた18。肝細胞は、腹腔鏡下肝部分切除術後にブタの肝臓から単離された22,24。幹細胞は骨髄吸引液から単離した18,19,26。脂肪組織由来幹細胞は、Human Cellular Therapy Laboratory, Mayo ClinicRochester 23から入手した。ヒト白血球は、輸血医学部門、メイヨークリニックロチェスター25から受け取った収集血液から分離されました。放射性標識に用いる各種細胞は、動物実験委員会、メイヨークリニック幹細胞研究監視分科会、輸血医学研究部会、バイオセーフティ委員会、放射線安全委員会が推奨するガイドラインに従って入手し、使用しました。
1. [89Zr]Zr-p-イソチオシアナトベンジル-デスフェリオキサミン([89Zr]Zr-DBN)の調製
タイミング:~160-220分
注:[89 Zr]Zr-DBNの調製では、ステップ1.1で述べたように、[89 Zr]Zr-リン酸水素([89Zr]Zr(HPO 4)2)または[89 Zr]Zr-塩化物([89 Zr]ZrCl4)の形で89Zrを単離します。
- 確立されたヒドロキサメート樹脂ベースの精製方法13,17を用いて、親89Yから89Zrを単離する。簡単に言うと、まず~100 mgのヒドロキサメート樹脂を含むカラムを調製し、次に8.0 mLの純粋な無水アセトニトリルでカラムを洗浄し、続いて5.0〜6.0 mLの空気でフラッシュしてヒドロキサメート樹脂を活性化します。次に、15 mL の脱イオン水でカラムを洗浄し、続いて 5.0-6.0 mL の空気で再度フラッシュし、次に 2.0 mL の 0.50 N HCl(微量金属ベーシスグレード)を通過させ、続いて 5.0-6.0 mL の空気でさらにフラッシュします。次に、89 Zrと89 Yの両方を含む溶液をヒドロキサメート樹脂にゆっくりとロードし、ヒドロキサメート樹脂から結合していない89Yを20 mLの2.0 N HClで洗浄し、続いて10 mLの脱イオン水と5.0〜6.0 mLの空気でフラッシュ洗浄します。
注:空気でフラッシュした後、 89Zrの溶出は以下に示すように実行できます。- 89Zr を [89 Zr]Zr(HPO 4)2 の形で溶出させるには、まず 0.50 mL の 1.2 M K 2 HPO 4/KH 2 PO 4 バッファー(pH 3.5)をステップ 1.1 のカラムに添加し、カラム上に 30 分間置いて、樹脂からの [89 Zr]Zr(HPO 4)2 としての 89Zr の放出を促進します。次に、1.2 M K 2 HPO 4/KH2PO4 バッファー(pH 3.5)を追加 1.50 mL でカラムから 89Zrを溶出します。[89Zr]Zr(HPO 4)2 の溶出後、図 1 に示すように、ステップ 1.2、1.2.1、および 1.2.2 に従って、[89 Zr]Zr(HPO 4)2 を使用して [89Zr]Zr-DBN を調製します。
- 89 Zrを[89 Zr]ZrCl4として得るには、まず89 Zrを[89Zr]Zr-シュウ酸塩として溶出する。
- 89Zr を [89 Zr]シュウ酸 Zr-シュウ酸塩の形で溶出させるには、ステップ 1.1 のカラムに 0.50 mL の 1.0 M シュウ酸を添加し、カラム上に 1 分間置いて、樹脂からの [89 Zr]-シュウ酸塩としての 89Zr の放出を促進します。次に、カラムから 89Zr を 2.50 mL の 1.0 M シュウ酸 (合計 3.0 mL) で溶出します17。
- 陰イオン交換カラムを用いて[89 Zr]シュウ酸Zr-シュウ酸を[89Zr]ZrCl4に変換するには、Larenkovら14によって記述されているように、まず6.0 mLのアセトニトリルで洗浄してカラムを活性化し、続いて5.0〜6.0 mLの空気でフラッシュします。次に、10.0 mLの生理食塩水でカラムを洗浄し、続いて5.0〜6.0 mLの空気を再度洗浄します。最後に、10.0 mLの脱イオン水を通し、続いて5.0〜6.0 mLの空気でフラッシュします。
- [89Zr]Zr-シュウ酸塩を含む3.0 mL溶液を活性化陰イオン交換カラムにゆっくりとロードし、続いて5.0〜6.0 mLの空気をフラッシュします。次に、 89Zr負荷カラムを50.0 mLの脱イオン水で洗浄して結合していないシュウ酸イオンを除去し、続いて5.0〜6.0 mLの空気でフラッシュします。
- [89 Zr]ZrCl4 の形で 89Zr を溶出させるには、0.10 mL の 1.0 N HCl をカラムに添加し、カラム上に 1.0 分間置いて樹脂から [89Zr]ZrCl4 として 89 Zr の放出を促進し、さらに 0.40 mL の 1.0 N HCl (合計 0.5 mL) でカラムから 89Zr を溶出します。溶出した[89Zr]ZrCl4をV字型バイアルに入れ、窒素ガスの定常流下で65°Cの加熱ブロックに入れて10〜30分間乾燥させます。乾燥後、乾燥した[89 Zr]ZrCl 4を水中で再溶解し、図1に示すように、手順1.3および1.3.1に従って[89 Zr]ZrCl4を使用して[89Zr]Zr-DBNを調製します。
- ステップ1.1.1から1.2 M K 2 HPO 4/KH 2 PO 4(pH 3.5)(10-25 MBq)に調製した[89Zr]Zr(HPO4)2~120 μLを取り、溶液を中和して、~100 μLの1.0 M HEPES-KOH(pH 7.5)および~65 μLの1.0 M K 2CO3でpH 7.5-8.0を達成します。
- 89Zrのさまざまな見かけ比活性を持つさまざまな89 Zr製剤について、ステップ1.2.2または1.3.1で適切な量のDFO-Bn-NCSを得るには、[89Zr]Zr(HPO 4)2または[89Zr]ZrCl4の中和製剤をDFO-Bn-NCS(7.5〜15 μg)の範囲で一定容量で一連のキレート反応を実行します。[89Zr]Zr(HPO4)2 の場合、37 °C のシェーカーで ~550 rpm で 60 分間、キレート反応をインキュベートします。一方、[89Zr]ZrCl4 の場合は、25 °C のシェーカー中で ~550 rpm のキレート反応を 30 分間インキュベートします。インキュベーション中またはインキュベーション終了時に沈殿物を示すキレート反応を廃棄します。インキュベーションの最後に、100 mM ジエチレントリアミン五酢酸(DTPA)、pH 7.0 を移動相として放射性薄層クロマトグラフィー(rad-TLC)を行い、後述のステップ 1.5 で説明するように、各キレート反応における DFO-Bn-NCS のキレート化効率を推定します。
注:キレート化効率に基づいて、[89Zr]Zr(HPO 4)2 または [89Zr]ZrCl4 の中和製剤で DFO-Bn-NCS を沈殿させることなく ≥97% のキレート化効率を達成するために必要なステップ 1.2.2 または 1.3.1 の最小量の DFO-Bn-NCS を使用します。ここで、[89Zr]Zr-DBNは、≥97%の放射化学的純度で合成された。 - 無水DMSO(3.76 mg/mL)で新鮮な5.0 mM DFO-Bn-NCSを調製し、4.0 μLの5.0 mM DFO-Bn-NCS(20 nmol または 15 μg)をステップ1.2で中和した[89Zr]Zr(HPO4)2 (10-25 MBq)~285 μLに加え、ピペッティングで溶液を混合します。キレート混合物中の最終的なDMSO濃度は、全容量の2%未満に保ちます。
- 89Zrのさまざまな見かけ比活性を持つさまざまな89 Zr製剤について、ステップ1.2.2または1.3.1で適切な量のDFO-Bn-NCSを得るには、[89Zr]Zr(HPO 4)2または[89Zr]ZrCl4の中和製剤をDFO-Bn-NCS(7.5〜15 μg)の範囲で一定容量で一連のキレート反応を実行します。[89Zr]Zr(HPO4)2 の場合、37 °C のシェーカーで ~550 rpm で 60 分間、キレート反応をインキュベートします。一方、[89Zr]ZrCl4 の場合は、25 °C のシェーカー中で ~550 rpm のキレート反応を 30 分間インキュベートします。インキュベーション中またはインキュベーション終了時に沈殿物を示すキレート反応を廃棄します。インキュベーションの最後に、100 mM ジエチレントリアミン五酢酸(DTPA)、pH 7.0 を移動相として放射性薄層クロマトグラフィー(rad-TLC)を行い、後述のステップ 1.5 で説明するように、各キレート反応における DFO-Bn-NCS のキレート化効率を推定します。
- ステップ 1.1.2.4 から 0.1 N HCl (40-80 MBq) に調製した [89Zr]ZrCl4 を ~180 μL 取り、得られた溶液を中和して、~25 μL の 1.0 M Na2CO3 で pH 7.5-8.0 を達成します。
- 無水ジメチルスルホキシド(DMSO)(1.88 mg/mL)で新鮮な 2.5 mM DFO-Bn-NCS を調製し、ステップ 1.3 で中和した [89Zr]ZrCl 4(40-80 MBq)に4.0 μL の 2.5 mM DFO-Bn-NCS (10 nmol または 7.5 μg) を加えます。ピペッティングで溶液を混合します。キレート混合物中の最終的なDMSO濃度は、全容量の2%未満に保ちます。
- [89Zr]Zr(HPO 4)2 の場合は ~550 rpm の加振機で 37 °C で 60分間、[89Zr]ZrCl4 の場合は 25 °C で ~550 rpm の加振機で 30 分間キレート化を進めます。
- 100 mM DTPA(pH 7.0)を rad-TLC 移動溶媒として rad-TLC により、89Zr のキレート化効率を測定します。[89Zr]Zr-DBN は ~0.021-0.035 の Rf を示し、[89 Zr]ZrCl 4 は ~1.0 の Rf を示し、[89Zr]Zr(HPO4)2 は ~1.0 の Rf を示すと予想されます。式(1)を使用してキレート化効率(%)を計算します。
[89Zr]Zr-DBN を形成するために DFO-NCS にキレート化された 89 Zr の割合 = [ ([89 Zr]Zr - DBN の Rf における放射能) / ([89 Zr]Zr - DBN の Rf における放射能と [89 Zr]Zr(HPO 4)2 または [89Zr]ZrCl4 の R f における放射能の合計 ] × 100 (1)
注:rad-TLCによって決定される、細胞放射性標識を続行するための許容可能な89Zrキレート化効率は≥97%です。[89Zr]Zr-DBNの提案された≥97%の放射化学的純度は、フィールドで使用される他の放射性医薬品の標準的な放射化学的純度要件に従って設定されました。代表的なrad-TLCについては、補足図S1および補足図S2を参照してください。

図1:[89Zr]Zr-DBN調製の概略図。 [89 Zr]Zr-DBNの調製には、事前に調合された[89Zr]Zr(HPO 4)2または[89Zr]ZrCl4をpH7.5〜8.0に中和します。中和した溶液をDFO-Bn-NCSでインキュベートします。rad-TLCによるDFO-Bn-NCSに対する89Zrのキレート化効率を確認します。この図の拡大版をご覧になるには、ここをクリックしてください。
2. 細胞放射性標識のための [ 89Zr ]Zr-DBN の生体適合性製剤 (図 2)
タイミング:~35分
注:ステップ3の細胞調製にかかる時間を考慮して、ステップ3はステップ2の開始の約20分前に開始し、~30分のインキュベーションを行います。これにより、ステップ4の細胞放射性標識は、ステップ2-3.2.2の完了後5~10分以内に開始することができます。
- [89Zr]ZrCl4から作製した[89Zr]Zr-DBN製剤の場合、~27.0 μLの1.2 M K 2 HPO 4/KH2PO4(pH 3.5)+~23.0 μLの1.0 M HEPES-KOH 緩衝液(pH 7.5)からなる50.0 μLの細胞適合性混合物を50.0 μLの[89 Zr]Zr-DBNに加えます。 [89Zr]Zr-DBN-細胞適合混合物を室温(25°C)で~30分間インキュベートします。
注:[89Zr]Zr(HPO4)2 から作られた [89Zr]Zr-DBN 製剤は、細胞の放射性標識に生体適合性があり、ステップ 2 を必要としません。
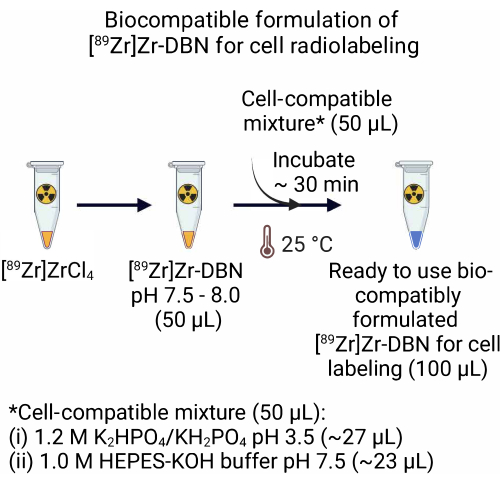
図2:細胞放射性標識用の[89Zr]Zr-DBNの生体適合性製剤の調製。 放射性標識シントンのすぐに使用できる生体適合性製剤を調製するには、1.2 M K 2 HPO 4/KH2PO4(pH 3.5)+ 1.0 M HEPES-KOHを含む等量の細胞適合性混合物を等容量の[89Zr]Zr-DBNに添加します。 25°Cで~30分間インキュベートします。 この図の拡大版を表示するには、ここをクリックしてください。
3. 放射性標識用細胞の調製
タイミング:~40-50分
- 6つの接着細胞(幹細胞、メラノーマがん細胞、心細胞造血幹細胞、樹状細胞、または肝細胞)を~12×10個の接着 細胞をトリプシン化し、15.0 mLのコニカル遠心チューブで~96 × g で4°Cで10分間遠心分離します。
- 上清を廃棄し、細胞ペレットを~500 μLのPBSに再懸濁し、細胞懸濁液を1.5 mLの微量遠心チューブに移します。細胞を~96 × g の微量遠心分離機で4°Cで10分間遠心分離します。
- 上清を廃棄し、細胞ペレットを~500 μLのH-HBSSに再懸濁します。1.5 mLの微量遠心分離機で、~96 × g で4°Cで10分間、細胞を遠心分離します。 手順3.1.2をもう一度繰り返して、手順4.1.1に進みます。
注:H-HBSSは、0.01 M HEPES(pH 8.0)のハンクス平衡塩溶液です。
- ヒト白血球(血液から新たに分離されたヒト白血球)などの非接着細胞の場合は、トリプシン処理をスキップし、~12×106 個の細胞を含む細胞懸濁液を1.5 mLの微量遠心分離機で~96 × g で4°Cで10分間遠心分離します。
- 上清を廃棄し、細胞ペレットを~500 μLのPBSに再懸濁し、1.5 mLの微量遠心分離機で~96 × g で4°Cで10分間遠心分離します。
- 上清を廃棄し、細胞ペレットを~500 μLのH-HBSSに再懸濁します。細胞を1.5 mLの微量遠心分離機で、~96 × g で4°Cで10分間遠心分離します。 手順3.2.2をもう一度繰り返して、手順4.1.1に進みます。
4. 細胞の放射性標識
タイミング:~125-155分
- 細胞放射性標識の開始(図3)
- ステップ3.1.2またはステップ3.2.2の細胞懸濁液を使用して、1.5 mLの微量遠心チューブ内で、pH 7.5-8.0の~500 μLのH-HBSSに約~6~6×10個の6個の細胞 を含む~500 μLの細胞懸濁液を調製します。
- これに、ステップ2で組成した生体適合性のある[89Zr]Zr-DBNを~100 μL添加します。
- 放射性標識のための細胞インキュベーション(図4)
- 生体適合性に調製した[89Zr]Zr-DBNと細胞懸濁液を、~500 μLに設定したマイクロピペットで静かにピペッティングして混合します。 89Zr同位体16の489設定の放射能線量校正器を使用して、インキュベーションチューブ内の放射能量を測定します。
- 細胞と[89Zr]Zr-DBN混合物をシェーカー中で、~550 rpm、25-37°C、30-45分間インキュベートし、細胞標識を行います。
注:インキュベーションの温度は、 表1に示すように、放射性標識に使用される細胞の種類によって異なります。 - ステップ4.2.2でインキュベーションした後、新たに調製したrad-TLC溶媒(20 mMクエン酸ナトリウム[pH 4.9-5.1]:メタノール[1:1、V:V])を使用して、細胞放射性標識反応でrad-TLCを実行します。 rad-TLC分析後、放射性標識細胞について、R f = ~0.73-0.81およびR f = ~0.01-0.02付近で[89 Zr]Zr-DBNおよび[89Zr]ZrCl4を探します。式(2)を使用して、R f = ~0.01-0.02 での放射能の割合を計算します。
Rf=~0.01-0.02における放射能の割合=[(Rf=~0.01-0.02における放射能)/(Rf=~0.01-0.02における放射能とRf=~0.73-0.81における放射能の合計)]×100(2)
注:R f = ~0.01-0.02 および R f = ~0.73-0.81 で可視化されたピークを理解するには、補足図 S3 の白血球放射性標識反応の rad-TLC を参照してください。 - 別の 1.5 mL 微量遠心チューブで、~100 μL の生体適合性調製 [89Zr]Zr-DBN と ~500 μL の H-HBSS を pH 7.5-8.0 で混合し、ステップ 4.2.5 のバックグラウンド補正用の無細胞コントロールとして使用します。ステップ4.2.2で使用したのと同様の温度と時間でインキュベートした後、rad-TLCを実行します。rad-TLCの実行後、Rf = ~0.73-0.81付近で[89 Zr]Zr-DBNと[89Zr]ZrCl4を探します。式(3)を用いて、R f = ~0.01-0.02における放射能の割合を計算する。
R f = ~0.01-0.02 = [ (R f= ~0.01 - 0.02 の放射能) / (R f= ~0.01 - 0.02 と R f= ~0.73 - 0.81 の放射能の合計) ] × 100 (3)
注: Rf = ~0.01-0.02 および ~0.73-0.81 で可視化されたピークを理解するには、 補足図 S4 の無細胞対照反応の rad-TLC を参照してください。 - (ステップ 4.2.3 の rad-TLC から) R f = ~0.01-0.02 の放射能率から Rf = ~0.01-0.02 (ステップ 4.2.4 の rad-TLC から) の放射能率を差し引いて、有効な細胞放射性標識 (%) を計算します。
- 放射性標識と細胞洗浄のクエンチング(図5)
- ステップ4.2.5でrad-TLCによる放射性標識の完了を確認した後、 表1に示すように、~600 μLの冷蔵した細胞に適した完全培地を添加するか、H-HBSSを添加して、放射性標識反応のクエンチングを行います。
- 細胞を~96 × g の微量遠心分離機で4°Cで10分間遠心分離します。 上澄みを捨てます。
- 表1に示すように、ペレット化した細胞を~500 μLの冷蔵培地(ダルベッコ改変イーグル培地(DMEM)+ウシ胎児血清10%+ペニシリン/ストレプトマイシン5%またはロズウェルパーク記念研究所-1640(RPMI-1640)+ウシ胎児血清10%+ペニシリン/ストレプトマイシン5%またはH-HBSS)に静かに再懸濁します。~500 μLに設定したマイクロピペットで静かにピペッティングして、細胞ペレットの再懸濁を行います。
- 細胞を微量遠心分離機で~96 × g で4°Cで10分間遠心分離します。
- 手順4.3.2〜4.3.4を2回繰り返して、結合していない放射能を洗い流します。
- 幹細胞またはH-HBSSの場合は、DMEM + 10%ウシ胎児血清+ 5%ペニシリン/ストレプトマイシンを含む新しい1.5 mL微量遠心チューブにペレットを移し、 89Zr-同位体16の489設定で線量校正器を使用して細胞ペレット内の放射能を測定します。
- 式(4)を使用して、すべての洗浄後の最終的な放射性標識効率を計算します。
放射性標識効率 = [(ステップ4.3.6における細胞ペレット中の崩壊補正放射能)/(ステップ4.2.1における細胞ペレットおよびH-HBSS中の崩壊補正放射能)] × 100 (4) - 放射性標識細胞の品質を確保するには、まず放射性標識細胞の最終懸濁液に凝集塊がないか目視検査します。塊がない場合は、この最終懸濁液を次のステップに進みます。塊があるが、ピペッティングまたは穏やかに振とうすることで再懸濁できる場合は、目視検査に合格するため、そうして次のステップに進みます。ただし、ピペッティングまたは穏やかな振とうによって凝集塊が再懸濁されない場合は、懸濁液を廃棄して最初からやり直してください。
- 目視検査に合格した場合は、放射性標識から1時間以内にPBSで調製した0.4%トリパンブルー溶液を使用してトリパンブルー排除生存率試験を実施し、放射性標識細胞の細胞生存率を評価するための洗浄ステップ(4.3.3-4.3.7)を実施します。
- 試験を実施するには、放射性標識細胞と非標識細胞の両方の10.0 μL細胞懸濁液に10.0 μLの0.4%トリパンブルー溶液を加え、10.0 μLに設定したマイクロピペットでトリパン青細胞懸濁液を上下にピペッティングして混合します。
- 血球計算盤に~10.0 μLのトリパン青細胞懸濁液混合物をロードし、すぐに顕微鏡で低倍率または自動セルカウンターを使用して、青色染色された細胞の数と血球計算盤内の細胞の総数をカウントします。式(5)を使用して、生細胞の割合を計算します。
生細胞の割合 = 100 - [(青色染色細胞数) / (総細胞数)] × 100 (5)
- 放射性標識細胞懸濁液中の生細胞の割合に変化がない場合は、非標識細胞を使用してください。生細胞の割合が標識されていない細胞よりも小さい場合は、放射性標識細胞を廃棄します。
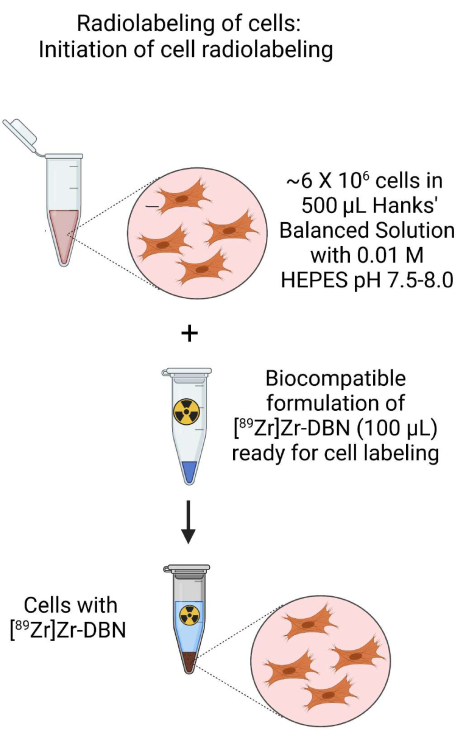
図3:細胞放射性標識の開始の概略図。HEPES緩衝ハンクス平衡塩溶液で調製した細胞懸濁液に生体適合性に調製された[89Zr]Zr-DBNを添加することにより、細胞の放射性標識を開始します。この図の拡大版をご覧になるには、ここをクリックしてください。
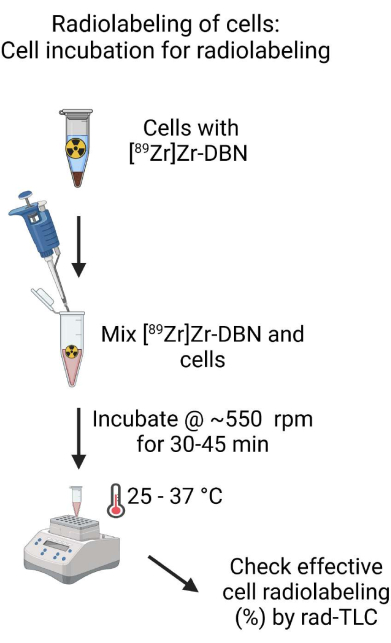
図4:放射性標識のための細胞インキュベーションの概略図。 生体適合性に調合された[89Zr]Zr-DBNを細胞懸濁液と完全に混合し、細胞懸濁液を温度制御された加熱ブロック中でシェーカー上で30〜60分間インキュベートします。
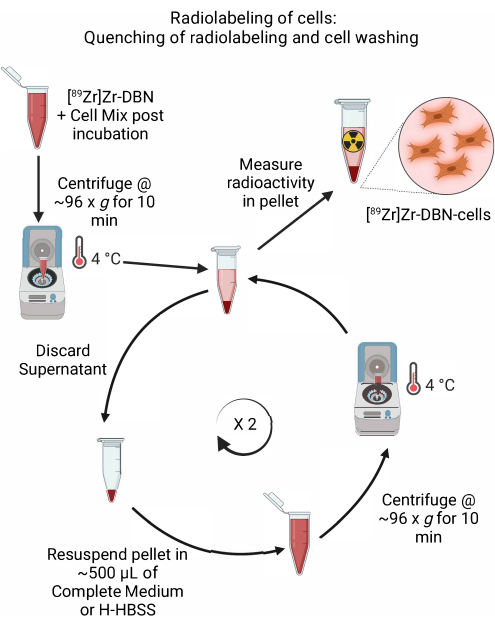
図5:放射性標識と細胞洗浄のクエンチングの概略図。 冷やした細胞培地またはH-HBSSを添加して細胞の放射性標識をクエンチし、続いて4°Cで遠心分離します。 細胞洗浄の場合は、上清を廃棄し、細胞ペレットを~500 μLのチルド細胞培地またはH-HBSSに再懸濁します。上清を廃棄し、細胞ペレットを新鮮な培地に再懸濁して、結合していない放射性標識シントンを除去するサイクルを繰り返します。この図の拡大版をご覧になるには、ここをクリックしてください。
結果
この原稿で提示された代表的な結果は、以前の[89Zr]Zr-DBN合成および細胞放射性標識研究18、19、22、23、24、25から編集されました。簡単に言うと、7.5-15 μgのDFO-Bn-NCSを用いて、25-37°Cで~30-60分で89ZrとDFO-Bn-NCSとの複合体形成に成功?...
ディスカッション
以下は、効果的な細胞放射性標識のために最適化が必要なプロトコルの重要なステップです。プロトコルステップ 1.2 および 1.3 では、使用する [89 Zr]Zr(HPO 4)2 または [89Zr]ZrCl4 の容量に応じて、適切な容量 (マイクロリットル) の塩基を使用する必要があります。1.0 M K 2 CO 3溶液を[89Zr]Zr(HPO 4)2の中和に使用し、[1.0 M Na 2CO 3...
開示事項
著者は金銭的な競合利害関係を有していないが、この技術の発明者である(特許#US20210330823A1)。
謝辞
この研究は、NIH 5R21HL127389-02、NIH 4T32HL007111-39、NIH R01HL134664、およびDOE DE-SC0008947助成金、国際原子力機関(ウィーン)、メイヨークリニック核医学部門、放射線科、およびメイヨークリニック再生医療センター(ミネソタ州ロチェスター)の支援を受けました。すべてのフィギュアは BioRender.com を使用して作成されました。
資料
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A996-4 | |
| Alpha Minimum Essential Medium | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 12571063 | |
| Anion exchange column | Macherey-Nagel, Inc., Düren, Germany | 731876 | Chromafix 30-PS-HCO3 SPE 45 mg cartridge |
| Conical centrifuge tubes (15 mL) | Corning Inc., Glendale, AZ, USA | 352096 | Falcon 15 mL high-clarity polypropylene (PP) conical centrifuge tubes |
| Dendritic cells | The American Type Culture Collection, Manassas, VA, USA | CRL-11904 | |
| DFO-Bn-NCS | Macrocyclics, Inc., Plano, TX, USA | B-705 | p-SCN-Bn-Deferoxamine |
| DMSO | Sigma-Aldrich, Inc., St. Louis, MO | 276855 | |
| Dose calibrator | Mirion Technologies (Capintec), Inc., Florham Park, NJ, USA | 5130-3234 | CRC -55tR Dose Calibrator |
| Dulbecco’s modified Eagle’s medium | The American Type Culture Collection, Manassas, VA, USA | 30-2002 | |
| Fetal Bovine Serum (FBS) | The American Type Culture Collection, Manassas, VA, USA | 30-2020 | |
| Hanks Balanced Salt solution (HBSS) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 14025092 | For preparation of H-HBSS |
| Hydrochloric Acid (trace metal basis grade) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A508P212 | |
| Melanoma cells | The American Type Culture Collection, Manassas, VA, USA | CRL-6475 | |
| Methanol | Sigma-Aldrich, Inc., St. Louis, MO | 34860 | |
| Microcentrifuge tube | Eppendorf, Hamburg, Germany | 30108442 | Protein LoBind microcentrifuge tube |
| Murine GM-CSF | R&D Systems, Inc., Minneapolis, MN USA | 415-ML-010 | |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 15140-122 | |
| Phosphate Buffered Saline without Ca2+ and Mg2+ | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 10010023 | For washing cells |
| Saline | Covidien LLC, Mansfield, MA, USA | 1020 | 0.9% Sterile Saline Solution |
| Shaker | Eppendorf, Hamburg, Germany | T1317 | Thermomixer |
| Silica gel-rad-TLC paper sheet | Agilent Technologies Inc., Santa Clara, CA, USA | SGI0001 | iTLC-SG |
参考文献
- Bhawnani, N., et al. Effectiveness of stem cell therapies in improving clinical outcomes in patients with heart failure. Cureus. 13 (8), e17236 (2021).
- Zakrzewski, W., Dobrzynski, M., Szymonowicz, M., Rybak, Z. Stem cells: past, present, and future. Stem Cell Research & Therapy. 10 (1), 68 (2019).
- Bukhari, A. B., Dutta, S., De, A. Image guidance in stem cell therapeutics: unfolding the blindfold. Current Drug Targets. 16 (6), 658-671 (2015).
- Momeni, A., Neelamegham, S., Parashurama, N. Current challenges for the targeted delivery and molecular imaging of stem cells in animal models. Bioengineered. 8 (4), 316-324 (2017).
- Gnecchi, M., Zhang, Z., Ni, A., Dzau, V. J. Paracrine mechanisms in adult stem cell signaling and therapy. Circulation Research. 103 (11), 1204-1219 (2008).
- D'Aloia, M. M., Zizzari, I. G., Sacchetti, B., Pierelli, L., Alimandi, M. CAR-T cells: the long and winding road to solid tumors. Cell Death & Disease. 9 (3), 282 (2018).
- Zhang, Q., et al. CAR-T cell therapy in cancer: tribulations and road ahead. Journal of Immunology Research. 2020, 1924379 (2020).
- Sterner, R. C., Sterner, R. M. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal. 11 (4), 69 (2021).
- Shao, F., et al. Radionuclide-based molecular imaging allows CAR-T cellular visualization and therapeutic monitoring. Theranostics. 11 (14), 6800-6817 (2021).
- Sakemura, R., Can, I., Siegler, E. L., Kenderian, S. S. In vivo CART cell imaging: Paving the way for success in CART cell therapy. Molecular Therapy Oncolytics. 20, 625-633 (2021).
- Wang, Y., et al. Dendritic cell biology and its role in tumor immunotherapy. Journal of Hematology & Oncology. 13 (1), 107 (2020).
- Bulte, J. W. M., Shakeri-Zadeh, A. In vivo MRI tracking of tumor vaccination and antigen presentation by dendritic cells. Molecular Imaging and Biology. 24 (2), 198-207 (2022).
- Holland, J. P., Sheh, Y., Lewis, J. S. Standardized methods for the production of high specific-activity zirconium-89. Nuclear Medicine and Biology. 36 (7), 729-739 (2009).
- Larenkov, A., et al. Preparation of zirconium-89 solutions for radiopharmaceutical purposes: interrelation between formulation, radiochemical purity, stability and biodistribution. Molecules. 24 (8), 1534 (2019).
- Pandey, M. K., et al. A new solid target design for the production of 89Zr and radiosynthesis of high molar activity [89Zr]Zr-DBN. American Journal of Nuclear Medicine and Molecular Imaging. 12 (1), 15-24 (2022).
- Pandey, M. K., et al. Improved production and processing of 89Zr using a solution target. Nuclear Medicine and Biology. 43 (1), 97-100 (2016).
- Pandey, M. K., Engelbrecht, H. P., Byrne, J. P., Packard, A. B., DeGrado, T. R. Production of 89Zr via the 89Y(p,n)89Zr reaction in aqueous solution: effect of solution composition on in-target chemistry. Nuclear Medicine and Biology. 41 (4), 309-316 (2014).
- Bansal, A., et al. Novel 89Zr cell labeling approach for PET-based cell trafficking studies. EJNMMI Research. 5, 19 (2015).
- Bansal, A., et al. 89Zr]Zr-DBN labeled cardiopoietic stem cells proficient for heart failure. Nuclear Medicine and Biology. 90-91, 23-30 (2020).
- Friberger, I., et al. Optimisation of the synthesis and cell labelling conditions for [89Zr]Zr-oxine and [89Zr]Zr-DFO-NCS: a direct in vitro comparison in cell types with distinct therapeutic applications. Molecular Imaging and Biology. 23 (6), 952-962 (2021).
- Lee, S. H., et al. Feasibility of real-time in vivo 89Zr-DFO-labeled CAR T-cell trafficking using PET imaging. PLoS One. 15 (1), e0223814 (2020).
- Nicolas, C. T., et al. Hepatocyte spheroids as an alternative to single cells for transplantation after ex vivo gene therapy in mice and pig models. Surgery. 164 (3), 473-481 (2018).
- Yang, B., et al. Tracking and therapeutic value of human adipose tissue-derived mesenchymal stem cell transplantation in reducing venous neointimal hyperplasia associated with arteriovenous fistula. Radiology. 279 (2), 513-522 (2016).
- Nicolas, C. T., et al. Ex vivo cell therapy by ectopic hepatocyte transplantation treats the porcine tyrosinemia model of acute liver failure. Molecular Therapy. Methods & Clinical Development. 18, 738-750 (2020).
- Bansal, A., Sharma, S., Klasen, B., Rosch, F., Pandey, M. K. Evaluation of different 89Zr-labeled synthons for direct labeling and tracking of white blood cells and stem cells in healthy athymic mice. Scientific Reports. 12 (1), 15646 (2022).
- Behfar, A., et al. Guided cardiopoiesis enhances therapeutic benefit of bone marrow human mesenchymal stem cells in chronic myocardial infarction. Journal of the American College of Cardiology. 56 (9), 721-734 (2010).
- Charoenphun, P., et al. 89Zr]oxinate4 for long-term in vivo cell tracking by positron emission tomography. European Journal of Nuclear Medicine and Molecular Imaging. 42 (2), 278-287 (2015).
- Sato, N., et al. In vivo tracking of adoptively transferred natural killer cells in rhesus macaques using 89zirconium-oxine cell labeling and PET imaging. Clinical Cancer Research. 26 (11), 2573-2581 (2020).
- Volpe, A., Pillarsetty, N. V. K., Lewis, J. S., Ponomarev, V. Applications of nuclear-based imaging in gene and cell therapy: probe considerations. Molecular Therapy Oncolytics. 20, 447-458 (2021).
- Fogli, L. K., et al. Challenges and next steps in the advancement of immunotherapy: summary of the 2018 and 2020 National Cancer Institute workshops on cell-based immunotherapy for solid tumors. Journal for Immunotherapy of Cancer. 9 (7), e003048 (2021).
- Li, X., Hacker, M. Molecular imaging in stem cell-based therapies of cardiac diseases. Advanced Drug Delivery Reviews. 120, 71-88 (2017).
- Puges, M., et al. Retrospective study comparing WBC scan and 18F-FDG PET/CT in patients with suspected prosthetic vascular graft infection. European Journal of Vascular and Endovascular Surgery. 57 (6), 876-884 (2019).
- Butterfield, L. H. Dendritic cells in cancer immunotherapy clinical trials: are we making progress. Frontiers in Immunology. 4, 454 (2013).
- de Vries, I. J. M., et al. Magnetic resonance tracking of dendritic cells in melanoma patients for monitoring of cellular therapy. Nature Biotechnology. 23 (11), 1407-1413 (2005).
- Gosmann, D., et al. Promise and challenges of clinical non-invasive T-cell tracking in the era of cancer immunotherapy. EJNMMI Research. 12 (1), 5 (2022).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved