Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Hücre Kaçakçılığının Pozitron Emisyon Tomografisi Görüntülemesi: Bir Hücre Radyo-Etiketleme Yöntemi
Bu Makalede
Özet
Burada sunulan, kullanıma hazır bir radyoetiketleme synthonu, [89 Zr]Zr-p-izotiyosiyatobenzil-desferrioksamin ([89Zr]Zr-p-izotiyosiyatobenzil-desferrioksamin ([89 Zr]Zr-DBN) kullanılarak bir pozitron emisyon tomografisi (PET) radyoizotopu, 89Zr (t1/2 78.4 h) ile radyoetiket hücrelerine yönelik bir protokoldür. [89Zr] Zr-DBN ile radyo-etiketleme hücreleri, uygulamadan sonra 7 güne kadar PET ile vücutta uygulanan radyoaktif işaretli hücrelerin invaziv olmayan izlenmesine ve görüntülenmesine izin verir.
Özet
Kök hücre ve kimerik antijen reseptörü (CAR) T hücresi tedavileri, organ rejenerasyonu için umut verici terapötikler ve çeşitli kanserler için immünoterapi olarak ortaya çıkmaktadır. Bu alanlarda önemli ilerlemeler kaydedilmiş olmasına rağmen, canlı sistemde uygulanan terapötik hücrelerin farmakokinetiğini ve farmakodinamiğini daha iyi anlamak için öğrenilecek daha çok şey vardır. Pozitron emisyon tomografisi (PET) ile hücrelerin noninvaziv, in vivo takibi için, 89 Zr (t1/2 78.4 saat) kullanılarak yeni bir [89Zr] Zr-p-izotiyosiyatobenzil-desferrioksamin ([89Zr] Zr-DBN) aracılı hücre radyoetiketleme yöntemi geliştirilmiştir. Mevcut protokol, mezenkimal kök hücreler, soy kılavuzluğunda kardiyopoietik kök hücreler, karaciğer yenileyici hepatositler, beyaz kan hücreleri, melanom hücreleri ve dendritik hücreler dahil olmak üzere çeşitli hücrelerin doğrudan radyoetiketlenmesi için [89Zr] Zr-DBN aracılı, kullanıma hazır, radyo-etiketleme synthonunu tanımlar. Geliştirilen metodoloji, radyoaktif işaretli hücrelerin doğasını veya işlevini etkilemeden, uygulamadan sonraki 7 güne kadar hücre trafiğinin noninvaziv PET görüntülemesini sağlar. Ek olarak, bu protokol, [89 Zr]Zr-DBN'nin radyosentezi, [89Zr]Zr-DBN'nin biyouyumlu formülasyonu, radyoetiketleme için hücrelerin hazırlanması ve son olarak hücrelerin [89Zr] Zr-DBN ile radyoetiketlenmesi için aşamalı bir yöntemi açıklar.
Giriş
Kök hücre ve kimerik antijen reseptörü (CAR) T hücresi tedavileri popülerlik kazanmakta ve miyokard yetmezliği1,2, retina dejenerasyonu 2, makula dejenerasyonu 2, diyabet 2, miyokard enfarktüsü 3,4,5 ve kanserler 6,7,8,9 gibi çeşitli hastalıkların tedavisi için aktif olarak araştırılmaktadır.10. Kök hücre tedavilerinin iki makul yaklaşımı arasında, kök hücreler ya terapötik bir yanıta neden olmak için doğrudan hastalık bölgesine aşılanabilir ya da dolaylı bir terapötik yanıt başlatmak için hastalık bölgesine bağlı kalmadan hastalık bölgesinin mikro çevresinde değişikliklere neden olabilir. Dolaylı bir terapötik yanıt, hastalığı onaracak veya tedavi edecek faktörleri serbest bırakarak hastalık bölgesinin mikro çevresinde değişikliklere neden olabilir5. Kök hücre tedavilerinin bu yaklaşımları, radyoaktif işaretli kök hücrelerin noninvaziv görüntülenmesi ile değerlendirilebilir. Noninvaziv görüntüleme, hastalık bölgesindeki radyoaktif işaretli hücrelerin alımını, doğrudan ve dolaylı terapötik yanıtı deşifre etmek için terapötik bir yanıtla ilişkilendirebilir.
Ek olarak, CAR T-hücresi 6,7,8,9,10 ve dendritik hücre immünoterapisi 11,12 kullanılarak çeşitli kanserleri tedavi etmek için bağışıklık hücresi bazlı tedaviler geliştirilmektedir. Mekanik olarak, CAR T hücresi immünoterapisi 6,7,8,9,10'da, T hücreleri, tedavi edilmesi gereken tümörler üzerindeki spesifik bir antijene bağlanan bir epitopu eksprese edecek şekilde tasarlanmıştır. Bu tasarlanmış CAR T hücreleri, uygulama üzerine, bir epitop-antijen etkileşimi yoluyla tümör hücrelerinde bulunan spesifik antijene bağlanır. Bağlandıktan sonra, bağlı CAR T hücreleri aktivasyona uğrar ve daha sonra çoğalır ve sitokinleri serbest bırakır, bu da konağın bağışıklık sistemine spesifik antijeni eksprese eden tümöre saldırması için sinyal verir. Buna karşılık, dendritik hücre tedavileri11,12 söz konusu olduğunda, dendritik hücreler, yüzeylerinde spesifik bir kanser antijeni sunacak şekilde tasarlanmıştır. Bu tasarlanmış dendritik hücreler, uygulandığında, lenf düğümlerine ev sahipliği yapar ve lenf düğümlerindeki T hücrelerine bağlanır. T hücreleri, uygulanan dendritik hücreler üzerindeki spesifik kanser antijenlerine bağlandıktan sonra, aktivasyon / proliferasyona uğrar ve bu spesifik antijeni eksprese eden tümöre karşı konakçının bir bağışıklık tepkisini başlatır. Bu nedenle, immünoterapinin etkinliğini belirlemek için radyoaktif işaretli CAR T hücrelerinin ve dendritik hücrelerin lenf nodlarına 11,12 yönlendirilmesinin değerlendirilmesi, uygulanan CAR T hücrelerinin bir tümör bölgesine9,10 ve dendritik hücrelerin 11,12 yönlendirilmesinin değerlendirilmesi mümkündür. Ayrıca, noninvaziv hücre kaçakçılığı, terapötik potansiyelin daha iyi anlaşılmasına, doğrudan ve dolaylı terapötik yanıtın netleştirilmesine ve hem kök hücre hem de bağışıklık hücresi bazlı tedavilerin terapötik yanıtının tahmin edilmesine ve izlenmesine yardımcı olabilir.
Optik görüntüleme, manyetik rezonans görüntüleme (MRI), tek foton emisyonlu bilgisayarlı tomografi (SPECT) ve pozitron emisyon tomografisi (PET) dahil olmak üzere hücre kaçakçılığı için farklı görüntüleme yöntemleri araştırılmıştır 3,4,9,10,12. Bu tekniklerin her birinin kendine göre avantajları ve dezavantajları vardır. Bunlar arasında PET, görüntülemeye dayalı hücre trafiğinde hücrelerin güvenilir bir şekilde ölçülmesi için gerekli olan kantitatif doğası ve yüksek duyarlılığı nedeniyle en umut verici yöntemdir 3,4,9,10.
Yarı ömrü 78.4saat olan pozitron yayan radyoizotop 89 Zr, hücre etiketlemesi için uygundur. 1 haftadan fazla bir süre boyunca hücre kaçakçılığının PET görüntülemesine izin verir ve yaygın olarak bulunan, düşük enerjili tıbbi siklotronlar 13,14,15,16,17 tarafından kolayca üretilir. Ek olarak, uygun şekilde işlevselleştirilmiş, p-izotiyosiyatobenzil-desferrioksamin (DFO-Bn-NCS) şelatörü, 89 Zr etiketli, kullanıma hazır, hücre etiketleme sentezi için ticari olarak mevcuttur, [89 Zr] Zr-p-izotiyosiyanosiyatobenzil-desferrioksamin, [89Zr] Zr-Zr-DBN 18,19,20,21,22,23,24 olarak da bilinir,25. [89Zr] Zr-DBN aracılı hücre etiketleme ilkesi, kararlı bir kovalent tiyoüre bağı üretmek için hücre zarı proteinlerinin birincil aminleri ile [89Zr] Zr-DBN'nin izotiyosiyanat (NCS) kısmı arasındaki reaksiyona dayanır.
[89Zr] Zr-DBN tabanlı hücre etiketleme ve görüntüleme, kök hücreler 18,23,25, dendritik hücreler 18, kardiyopoietik kök hücreler19, desidual stromal hücreler 20, kemik iliği kaynaklı makrofajlar 20, periferik kan mononükleer hücreleri 20, Jurkat/CAR T hücreleri 21, hepatositler 22,24 ve beyaz kan hücreleri 25 dahil olmak üzere çeşitli farklı hücreleri izlemek için yayınlanmıştır . Aşağıdaki protokol, [89Zr]Zr-DBN ile adım adım hazırlama ve hücre radyo-etiketleme yöntemlerini sağlar ve belirli bir hücre tipi için radyoetiketleme protokolünde gerekli olabilecek değişiklikleri açıklar. Daha fazla netlik için, burada sunulan hücre radyo-etiketleme yöntemi dört bölüme ayrılmıştır. İlk bölüm, 89Zr'yi DFO-Bn-NCS ile şelatlayarak [89Zr]Zr-DBN'nin hazırlanması ile ilgilidir. İkinci bölüm, hücre radyo-etiketleme için kolayca kullanılabilen [89Zr]Zr-DBN'nin biyouyumlu bir formülasyonunun hazırlanmasını açıklar. Üçüncü bölüm, radyo-etiketleme için hücrelerin ön koşullandırılması için gereken adımları kapsar. Hücrelerin ön koşullandırılması, hücrelerin proteinsiz fosfat tamponlu salin (PBS) ve HEPES tamponlu Hanks dengeli tuz çözeltisi (H-HBSS) ile yıkanmasını içerir, bu da [89Zr] Zr-DBN'nin radyoetiketleme sırasında hücre yüzey proteinlerinde bulunan birincil aminlerle reaksiyonuna müdahale edebilir veya bunlarla rekabet edebilir. Son bölüm, hücrelerin gerçek radyo-etiketleme ve kalite kontrol analizi ile ilgili adımları sağlar.
Protokol
Dendritik hücreler ve melanom hücreleri ticari olarak elde edildi18. Laparoskopik parsiyel hepatektomi sonrası domuzların karaciğerinden hepatositler izole edildi22,24. Kök hücreler kemik iliği aspiratlarındanizole edildi 18,19,26. Yağ dokusu kaynaklı kök hücreler, İnsan Hücresel Terapi Laboratuvarı, Mayo Clinic Rochester23'ten elde edildi. İnsan beyaz kan hücreleri, Transfüzyon Tıbbı Bölümü, Mayo Clinic Rochester25'ten alınan toplanan kandan izole edildi. Radyoetiketleme için kullanılan çeşitli hücreler, Kurumsal Hayvan Bakım ve Kullanım Komitesi, Mayo Clinic Kök Hücre Araştırma Gözetim Alt Komitesi, Transfüzyon Tıbbı Araştırma Komitesi, Kurumsal Biyogüvenlik Komitesi ve Radyasyon Güvenliği Komitesi tarafından önerilen yönergelere uygun olarak elde edildi ve kullanıldı.
1. [89 Zr] Zr-p-izotiyosiyatobenzil-desferrioksamin ([89Zr] Zr-DBN) hazırlanması
Süre: ~160-220 dk
NOT: [89 Zr]Zr-DBN'nin hazırlanması için, 89 Zr'yi [89 Zr]Zr-hidrojen fosfat ([89 Zr]Zr(HPO4)2) veya [89 Zr]Zr-klorür ([89Zr]ZrCl 4) formunda izole edin, adım 1.1'de belirtildiği gibi.
- Yerleşik bir hidroksamat reçinesi bazlı saflaştırma yöntemi13,17 kullanarak 89Zr'yi ana 89Y'den izole edin. Kısaca, önce ~100 mg hidroksamat reçinesi içeren bir kolon hazırlayın, ardından kolonu 8.0 mL saf susuz asetonitril ile yıkayarak ve ardından 5.0-6.0 mL hava ile yıkayarak hidroksamat reçinesini aktive edin. Daha sonra, kolonu 15 mL deiyonize su ile yıkayın, ardından 5.0-6.0 mL hava ile başka bir yıkama yapın ve ardından 2.0 mL 0.50 N HCl (eser metal bazlı derece) ve ardından 5.0-6.0 mL hava ile ek bir yıkama yapın. Daha sonra, hem 89 Zr hem de 89 Y içeren çözeltiyi yavaşça hidroksamat reçinesine yükleyin ve bağlanmamış 89Y'yi hidroksamat reçinesinden 20 mL 2.0 N HCl ile yıkayın, ardından 10 mL deiyonize su ve 5.0-6.0 mL hava ile yıkayın.
NOT: Hava ile yıkandıktan sonra, aşağıda gösterildiği gibi 89Zr elüsyon gerçekleştirilebilir.- 89Zr'yi [89 Zr]Zr(HPO 4)2 şeklinde ayrıştırmak için, önce 1.1. adımdan itibaren kolona 0.50 mL 1.2 MK2HPO 4/KH 2 PO 4 tamponu (pH 3.5) ekleyin ve 89Zr'nin reçineden [89Zr]Zr(HPO 4)2olarak salınmasını teşvik etmek için kolonda 30 dakika oturmasına izin verin. Ardından, 89Zr'yi kolondan ek bir 1.50 mL 1.2 M K 2 HPO 4 / KH2PO4 tamponu (pH 3.5)ile elüte edin. [89Zr]Zr(HPO 4)2'nin elüsyonundan sonra, Şekil 1.2.2'de gösterildiği gibi [1.2.1 Zr]Zr(HPO 1.2.2)89 kullanarak [89Zr]Zr-DBN'nin hazırlanması için 4,1 ve4 adımlarını izleyin.
- 89Zr'yi [89 Zr]ZrCl4 olarak elde etmek için, önce 89 Zr'yi [89Zr]Zr-oksalat olarak elute edin.
- 89Zr'yi [89 Zr]Zr-oksalat formunda ayrıştırmak için, 1.1. adımdan itibaren kolona 0.50 mL 1.0 M oksalik asit ekleyin ve 89Zr'nin reçineden [89Zr]-oksalat olarak salınmasını teşvik etmek için kolon üzerinde 1 dakika bekletin. Daha sonra, 89Zr'yi kolondan ek olarak 2.50 mL 1.0 M oksalik asit (toplam 3.0 mL) ile elüte edin17.
- Larenkov ve ark.14 tarafından tarif edildiği gibi bir anyon değişim kolonukullanarak [89Zr]Zr-oksalatı [89Zr]ZrCl4'e dönüştürmek için, önce 6.0 mL asetonitril ile yıkayarak kolonu etkinleştirin, ardından 5.0-6.0 mL hava ile yıkayın. Ardından, kolonu 10.0 mL tuzlu su ile yıkayın, ardından 5.0-6.0 mL hava ile yıkayın. Son olarak, 10.0 mL deiyonize su ve ardından 5.0-6.0 mL hava ile yıkayın.
- [89Zr]Zr-oksalat içeren 3.0 mL'lik çözeltiyi aktif anyon değişim kolonuna yavaşça yükleyin, ardından 5.0-6.0 mL hava yıkayın. Ardından, bağlanmamış oksalat iyonunu çıkarmak için 89Zr yüklü sütunu 50.0 mL deiyonize su ile yıkayın, ardından 5.0-6.0 mL hava ile yıkayın.
- 89Zr'yi [89 Zr]ZrCl 4 formunda ayrıştırmak için, kolona 0.10 mL 1.0 N HCl ekleyin, 89 Zr'nin reçineden [89 Zr] ZrCl4 olarak salınmasını teşvik etmek için kolonda 1.0 dakika oturmasına izin verin ve 89Zr'yi kolondan ek 0.40 mL 1.0 N HCl (toplam 0.5 mL) ile elüte edin. Ayrıştırılmış [89Zr] ZrCl4'ü V şeklinde bir şişede, 10-30 dakika boyunca sabit bir nitrojen gazı akışı altında 65 ° C'de bir ısıtma bloğuna yerleştirerek kurutun. Kuruduktan sonra, kurutulmuş [89 Zr]ZrCl4'ü suda sulandırın ve Şekil 1.3'de gösterildiği gibi [89Zr]ZrCl 1.3.1 kullanarak [89Zr]Zr-DBN'nin hazırlanması için 4 ve 1 adımlarını izleyin.
- Adım 1.1.1'den 1.2 MK2HPO 4 / KH 2 PO 4 (pH 3.5) (10-25 MBq) içinde formüle edilmiş ~ 120 μL [89Zr] Zr (HPO4) 2 alın ve ~ 100 μL 1.0 M HEPES-KOH (pH 7.5) ve ~65 μL 1.0 M K 2CO3 ile pH 7.5-8.0 elde etmek için çözeltiyi nötralize edin.
- 89Zr'lik çeşitli görünür spesifik aktiviteye sahip farklı 89 Zr formülasyonları için 1.2.2 veya 1.3.1 adımları için uygun miktarda DFO-Bn-NCS elde etmek için, sabit hacimde nötralize edilmiş bir formülasyon kullanarak bir dizi şelasyon reaksiyonu gerçekleştirin [89 Zr] Zr (HPO 4) 2 veya [89Zr] ZrCl 4 DFO-Bn-NCS (7.5-15 μg) aralığı ile. [89Zr]Zr(HPO4)2 durumunda, şelasyon reaksiyonunu 37 °C'de ~550 rpm'de bir çalkalayıcıda 60 dakika inkübe edin. Oysa [89Zr]ZrCl4durumunda, şelasyon reaksiyonunu 25 °C'de ~550 rpm'de bir çalkalayıcıda 30 dakika inkübe edin. İnkübasyon sırasında veya sonunda çökelti gösteren şelasyon reaksiyonunu atın. İnkübasyonun sonunda, aşağıda adım 1.5'te tartışıldığı gibi, her bir şelasyon reaksiyonu için DFO-Bn-NCS'nin şelasyon verimliliğini tahmin etmek için mobil faz olarak 100 mM dietilentriamin pentaasetat (DTPA), pH 7.0 ile radyoaktif ince tabaka kromatografisi (rad-TLC) gerçekleştirin.
NOT: Şelasyon verimliliğine bağlı olarak, [89Zr] Zr (HPO 4) 2 veya [89Zr] ZrCl4'ün nötralize edilmiş formülasyonunda DFO-Bn-NCS'nin çökelmesine neden olmadan% ≥97'lik bir şelasyon verimliliği elde etmek için gereken 1.2.2 veya 1.3.1 adımlarında minimum DFO-Bn-NCS miktarını kullanın. Burada, [89Zr]Zr-DBN, %≥97 radyokimyasal saflıkta sentezlendi. - Susuz DMSO'da (3.76 mg / mL) taze 5.0 mM DFO-BN-NCS hazırlayın ve Adım 1.2'den ~285 μL nötralize [89Zr] Zr (HPO 4) 2 (10-25 MBq) ila4.0 μL 5.0 mM DFO-Bn-NCS (20 nmol veya 15 μg) ekleyin ve çözeltiyi pipetleyerek karıştırın. Şelasyon karışımındaki son DMSO konsantrasyonunu toplam hacmin% 2'sinin altında tutun.
- 89Zr'lik çeşitli görünür spesifik aktiviteye sahip farklı 89 Zr formülasyonları için 1.2.2 veya 1.3.1 adımları için uygun miktarda DFO-Bn-NCS elde etmek için, sabit hacimde nötralize edilmiş bir formülasyon kullanarak bir dizi şelasyon reaksiyonu gerçekleştirin [89 Zr] Zr (HPO 4) 2 veya [89Zr] ZrCl 4 DFO-Bn-NCS (7.5-15 μg) aralığı ile. [89Zr]Zr(HPO4)2 durumunda, şelasyon reaksiyonunu 37 °C'de ~550 rpm'de bir çalkalayıcıda 60 dakika inkübe edin. Oysa [89Zr]ZrCl4durumunda, şelasyon reaksiyonunu 25 °C'de ~550 rpm'de bir çalkalayıcıda 30 dakika inkübe edin. İnkübasyon sırasında veya sonunda çökelti gösteren şelasyon reaksiyonunu atın. İnkübasyonun sonunda, aşağıda adım 1.5'te tartışıldığı gibi, her bir şelasyon reaksiyonu için DFO-Bn-NCS'nin şelasyon verimliliğini tahmin etmek için mobil faz olarak 100 mM dietilentriamin pentaasetat (DTPA), pH 7.0 ile radyoaktif ince tabaka kromatografisi (rad-TLC) gerçekleştirin.
- Adım 1.1.2.4'ten 0.1 N HCl'de (40-80 MBq) formüle edilmiş ~180 μL [89Zr]ZrCl4 alın ve elde edilen çözeltiyi ~25 μL 1.0 MNa2CO3ile pH 7.5-8.0 elde etmek için nötralize edin.
- Susuz dimetil sülfoksit (DMSO) (1.88 mg / mL) içinde taze 2.5 mM DFO-BN-NCS hazırlayın ve 4.0 μL 2.5 mM DFO-Bn-NCS (10 nmol veya 7.5 μg) ekleyin ~ 205 μL nötralize [89 Zr] ZrCl4 (40-80 MBq) adım 1.3'ten. Çözeltiyi pipetleyerek karıştırın. Şelasyon karışımındaki son DMSO konsantrasyonunu toplam hacmin% 2'sinin altında tutun.
- [89Zr]Zr(HPO 4)2 durumunda ~550 rpm'de ~550 rpm'de bir çalkalayıcıda 39 °C'de 89Zr şelasyonuna devam edin veya [89Zr]ZrCl4 durumunda ~550 rpm'de 30 dakika çalkalayıcıda 25 °C'de devam edin.
- Rad-TLC mobil çözücü olarak 100 mM DTPA (pH 7.0) ile rad-TLC ile 89Zr şelasyon verimliliğini belirleyin. [89Zr]Zr-DBN'nin ~0.021-0.035'lik bir R f göstermesini, [89 Zr]ZrCl 4'ün ~1.0'lık bir R f göstermesini ve [89Zr]Zr(HPO4)2'nin ~1.0'lık bir R f göstermesini bekleyin. Denklem (1)'i kullanarak şelasyon verimliliğini (%) hesaplayın:
[89Zr]Zr-DBN = [89Zr]Zr - DBN'nin R f'sinde Radyoaktivite) / ([89 Zr]Zr - DBN'nin R f'sinde ve [89 Zr]Zr(HPO 4)2 veya [89Zr]ZrCl 4'ün R f'sinde Radyoaktivitelerin Toplamı) ] × 100 (1)
NOT: rad-TLC ile belirlendiği üzere, hücre radyo-etiketlemesine devam etmek için kabul edilebilir 89Zr şelasyon verimliliği %≥97'dir. [89 Zr] Zr-DBN'nin önerilen %≥97radyokimyasal saflığı, sahada kullanılan diğer radyofarmasötikler için standart radyokimyasal saflık gereksinimine göre belirlenmiştir. Ek Şekil S1 ve Ek Şekil S2'deki temsili rad-TLC'ye bakın.

Şekil 1: [89Zr]Zr-DBN preparatının şeması. [89Zr]Zr-DBN'nin hazırlanması için, önceden formüle edilmiş [89 Zr]Zr(HPO4)2 veya [89Zr]ZrCl4'ü 7.5-8.0 pH'a kadar nötralize edin. Nötralize çözeltiyi DFO-Bn-NCS ile inkübe edin. Rad-TLC ile 89Zr'nin DFO-Bn-NCS'ye şelasyon verimliliğini kontrol edin. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
2. Hücre radyo-etiketleme için [89Zr] Zr-DBN'nin biyouyumlu formülasyonu (Şekil 2)
Süre: ~35 dk
NOT: 3. adımda hücrelerin hazırlanması için geçen süre göz önüne alındığında, ~30 dakikalık bir inkübasyon için 3. adımın başlangıcından yaklaşık 20 dakika önce 3. adıma başlayın. Bu, 4. adımdaki hücre radyo-etiketlemesinin 2-3.2.2 adımlarının tamamlanmasından sonra ~5-10 dakika içinde başlamasına izin verir.
- [89Zr]ZrCl4'ten yapılan [89Zr] Zr-DBN formülasyonu için, ~ 27.0 μL 1.2 M K 2 HPO 4 / KH2PO4 (pH 3.5) + ~23.0 μL 1.0 M HEPES-KOH tamponu (pH 7.5) ila 50.0 μL [89 Zr] Zr-DBN içeren hücre uyumlu bir karışımın 50.0 μL ekleyin. [89Zr] Zr-DBN hücre uyumlu karışımı oda sıcaklığında (25 ° C) ~ 30 dakika inkübe edin.
NOT: [89Zr]Zr(HPO4)2'den yapılan [89Zr]Zr-DBN formülasyonu, hücrelerin radyoaktif etiketlenmesi için biyouyumludur ve 2. adım gerektirmez.
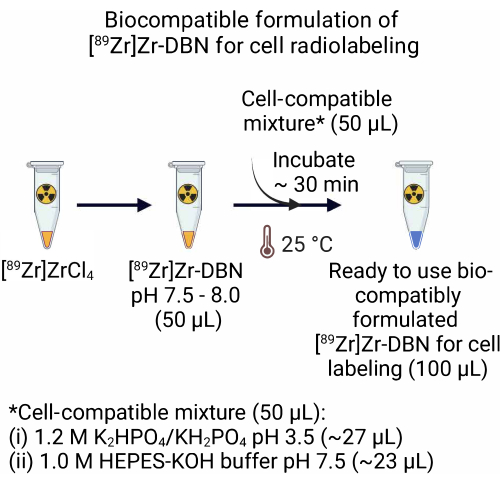
Şekil 2: Hücre radyo-etiketleme için [89Zr]Zr-DBN'nin biyouyumlu formülasyonunun hazırlanması. Radyoaktif işaretleme synthonunun kullanıma hazır biyouyumlu bir formülasyonunun hazırlanması için, eşit hacimde [89Zr]Zr-DBN'ye 1.2 MK2HPO4 / KH2PO4 (pH 3.5) + 1.0 M HEPES-KOH içeren eşit hacimde hücre uyumlu karışım ekleyin. 25 °C'de ~30 dakika inkübe edin. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
3. Radyo-işaretleme için hücrelerin hazırlanması
Süre: ~40-50 dk
- ~ 12 × 106 yapışık hücreleri (kök hücreler, melanom kanseri hücreleri, kardiyopoietik kök hücreler, dendritik hücreler veya hepatositler) tripsinize edin ve hücreleri 15.0 mL'lik bir konik santrifüj tüpünde ~ 96 × g'da 4 ° C'de 10 dakika boyunca santrifüjleyin.
- Süpernatanı atın, hücre peletini ~ 500 μL PBS'de yeniden süspanse edin ve hücre süspansiyonunu 1.5 mL'lik bir mikrosantrifüj tüpüne aktarın. Hücreleri bir mikrosantrifüjde ~96 × g'da 4 ° C'de 10 dakika santrifüjleyin.
- Süpernatanı atın ve hücre peletini ~ 500 μL H-HBSS içinde yeniden süspanse edin. Hücreleri 1.5 mL'lik bir mikrosantrifüjde ~ 96 × g'da 4 ° C'de 10 dakika santrifüjleyin. Adım 3.1.2'yi bir kez daha tekrarlayın ve adım 4.1.1'e geçin.
NOT: H-HBSS, 0.01 M HEPES (pH 8.0) içeren Hanks dengeli tuz çözeltisidir.
- İnsan beyaz kan hücreleri (kandan taze izole edilmiş insan beyaz kan hücreleri) gibi yapışık olmayan hücreler söz konusu olduğunda, tripsinizasyonu atlayın ve ~ 12 ×10 6 hücre içeren hücre süspansiyonunu 1.5 mL'lik bir mikrosantrifüjde ~ 96 × g'da 4 ° C'de 10 dakika boyunca santrifüjleyin.
- Süpernatanı atın, hücre peletini ~ 500 μL PBS'de yeniden süspanse edin ve hücreleri 4 ° C'de 10 dakika boyunca ~ 96 × g'de 1.5 mL'lik bir mikrosantrifüjde santrifüjleyin.
- Süpernatanı atın ve hücre peletini ~ 500 μL H-HBSS içinde yeniden süspanse edin. Hücreleri 1.5 mL'lik bir mikrosantrifüjde ~96 × g'da 4 ° C'de 10 dakika santrifüjleyin. Adım 3.2.2'yi bir kez daha tekrarlayın ve adım 4.1.1'e geçin.
4. Hücrelerin radyo-etiketlenmesi
Süre: ~125-155 dk
- Hücre radyo-işaretlemesinin başlatılması (Şekil 3)
- 1.5 mL'lik bir mikrosantrifüj tüpünde pH 7.5-8.0'da ~500 μL H-HBSS'de yaklaşık ~6 ×10 6 hücreli ~500 μL'lik bir hücre süspansiyonu hazırlamak için adım 3.1.2 veya adım 3.2.2'deki hücre süspansiyonunu kullanın.
- Buna, 2. adımdan itibaren biyouyumlu olarak formüle edilmiş [89Zr] Zr-DBN'den ~ 100 μL ekleyin.
- Radyoişaretleme için hücre inkübasyonu (Şekil 4)
- Biyouyumlu olarak formüle edilmiş [89 Zr] Zr-DBN ve hücre süspansiyonunu ~500 μL'ye ayarlanmış bir mikropipet ile hafifçe yukarı ve aşağı pipetleyerek karıştırın. 89Zr-izotop16 için 489ayarında bir radyoaktivite doz kalibratörü kullanarak inkübasyon tüpündeki radyoaktivite miktarını ölçün.
- Hücreleri ve [89Zr] Zr-DBN karışımını hücre etiketlemesi için 25-37 ° C'de ~550 rpm'de bir çalkalayıcıda 30-45 dakika inkübe edin.
NOT: İnkübasyonun sıcaklığı, Tablo 1'de gösterildiği gibi, radyoaktif işaretleme için kullanılan hücre tiplerine bağlı olarak değişecektir. - Adım 4.2.2'deki inkübasyondan sonra, yeni hazırlanmış rad-TLC çözücü (20 mM sodyum sitrat [pH 4.9-5.1]:metanol [1:1, V:V]) kullanarak hücre radyo-işaretleme reaksiyonu üzerinde rad-TLC gerçekleştirin. Rad-TLC çalışmasından sonra, radyoaktif işaretli hücreler için R f = ~0.73-0.81 ve Rf = ~0.01-0.02 civarında [89Zr]Zr-DBN ve [89Zr]ZrCl4'ü arayın. Denklem (2)'yi kullanarak Rf = ~0.01-0.02'deki radyoaktivite yüzdesini hesaplayın.
R f = ~0.01-0.02'deki radyoaktivite yüzdesi = [ (R f'deki radyoaktivite = ~0.01 - 0.02) / (R f = ~0.01 - 0.02 ve Rf= ~0.73 - 0.81'deki Radyoaktivitelerin Toplamı) ] × 100 (2)
NOT: R f = ~ 0.01-0.02 ve R f = ~ 0.73-0.81'de görselleştirilen pikleri anlamak için, Ek Şekil S3'teki beyaz kan hücresi radyoaktif etiketleme reaksiyonu için rad-TLC'ye bakın. - Ayrı bir 1.5 mL mikrosantrifüj tüpünde, adım 4.2.5'te arka plan düzeltmesi için hücresiz kontrol olarak kullanmak üzere biyouyumlu olarak formüle edilmiş [89Zr] Zr-DBN'nin ~ 500 μL H-HBSS ile pH 7.5-8.0'da ~ 100 μL karıştırılması. Adım 4.2.2'de kullanılana benzer bir sıcaklık ve sürede inkübasyondan sonra rad-TLC gerçekleştirin. Rad-TLC çalıştırmasından sonra, Rf = ~0.73-0.81 civarında [89Zr]Zr-DBN ve [89Zr]ZrCl4'ü arayın. Denklem (3)'ü kullanarak Rf = ~0.01-0.02'deki radyoaktivite yüzdesini hesaplayın.
R f = ~0.01-0.02'de radyoaktivite = [ (R f'de radyoaktivite = ~0.01 - 0.02) / (R f'de Radyoaktivite toplamı= ~0.01 - 0.02 ve Rf= ~0.73 - 0.81) ] × 100 (3)
NOT: Rf = ~ 0.01-0.02 ve ~ 0.73-0.81'de görselleştirilen tepe noktalarını anlamak için, Ek Şekil S4'teki hücresiz kontrol reaksiyonunun rad-TLC'sine bakın. - Rf = ~0.01-0.02'deki radyoaktivite yüzdesini (4.2.4 adımındaki rad-TLC'den) Rf = ~0.01-0.02'deki radyoaktivite yüzdesinden (4.2.3 adımındaki rad-TLC'den) çıkararak etkili hücre radyoetiketlemesini (%) hesaplayın.
- Radyoişaretleme ve hücre yıkamanın söndürülmesi (Şekil 5)
- Adım 4.2.5'te rad-TLC ile radyo-etiketlemenin tamamlandığını onayladıktan sonra, Tablo 1'de gösterildiği gibi ~600 μL soğutulmuş, hücreye uygun tam ortam ilavesiyle veya H-HBSS ilavesiyle radyo-etiketleme reaksiyonunun söndürülmesini gerçekleştirin.
- Hücreleri bir mikrosantrifüjde ~96 × g'da 4 ° C'de 10 dakika santrifüjleyin. Süpernatanı atın.
- Peletlenmiş hücreleri ~ 500 μL soğutulmuş ortamda (Dulbecco'nun modifiye kartal ortamı (DMEM) +% 10 fetal sığır serumu +% 5 penisilin / streptomisin veya Roswell Park Memorial Institute-1640 (RPMI-1640) +% 10 fetal sığır serumu +% 5 penisilin / streptomisin veya H-HBSS, Tablo 1'de gösterildiği gibi belirli bir hücre tipi için. ~500 μL'ye ayarlanmış bir mikropipet ile hafifçe yukarı ve aşağı pipetleyerek hücre peletinin yeniden süspansiyonunu gerçekleştirin.
- Hücreleri 4 ° C'de 10 dakika boyunca ~ 96 × g'de bir mikrosantrifüjde santrifüjleyin.
- Bağlanmamış radyoaktiviteyi yıkamak için 4.3.2-4.3.4 adımlarını iki kez tekrarlayın.
- Pelet, kök hücreler veya H-HBSS durumunda DMEM +% 10 fetal sığır serumu +% 5 penisilin / streptomisin içeren taze bir 1.5 mL mikrosantrifüj tüpüne aktarın ve 89Zr-izotop16 için 489 ayarında bir doz kalibratörü kullanarak hücre peletindeki radyoaktiviteyi ölçün.
- Denklem (4)'ü kullanarak tüm yıkamalardan sonra nihai radyoetiketleme verimliliğini hesaplayın.
Radyoetiketleme verimliliği = [(Adım 4.3.6'da hücre peletinde bozunma düzeltilmiş radyoaktivite) / (Adım 4.2.1'de hücre peletinde ve H-HBSS'de bozunma düzeltilmiş radyoaktivite) ] × 100 (4) - Radyoaktif işaretli hücrelerin kalitesinden emin olmak için, önce radyoaktif işaretli hücrelerin son süspansiyonunu herhangi bir küme varlığı açısından görsel olarak inceleyin. Küme yoksa, bu son askıya alma işlemine bir sonraki adımla geçin. Kümeler varsa, ancak pipetleme veya hafifçe çalkalama yoluyla yeniden askıya alınabiliyorsa, bunu yapın ve görsel incelemeden geçtiği için bir sonraki adıma geçin. Bununla birlikte, kümeler pipetleme veya hafifçe çalkalama yoluyla yeniden süspanse edilmezse, süspansiyonu atın ve baştan başlayın.
- Görsel inceleme geçilirse, radyo-etiketlemeden sonraki 1 saat içinde PBS'de hazırlanan% 0.4 tripan mavisi çözeltisi ve radyoaktif işaretli hücrelerin hücre canlılığını değerlendirmek için yıkama adımları (4.3.3-4.3.7) kullanarak bir tripan mavisi dışlama canlılık testi gerçekleştirin.
- Testi gerçekleştirmek için, hem radyoaktif işaretli hem de etiketsiz hücrelerin 10.0 μL'lik hücre süspansiyonuna 10.0 μL'lik %0.4 tripan mavisi çözeltisi ekleyin ve tripan mavi hücre süspansiyonunu 10.0 μL'ye ayarlanmış mikropipet ile yukarı ve aşağı pipetleyerek karıştırın.
- ~10.0 μL tripan mavi hücre süspansiyon karışımı içeren bir hemasitometre yükleyin, hemen mavi lekeli hücrelerin sayısını ve hematitometredeki toplam hücre sayısını mikroskop altında düşük büyütmede veya otomatik bir hücre sayacı kullanarak sayın. Denklem (5) kullanarak canlı hücrelerin yüzdesini hesaplayın.
Canlı hücrelerin yüzdesi = 100 - [(Mavi lekeli hücre sayısı) / (Toplam hücre sayısı)] × 100 (5)
- Radyoaktif işaretli hücre süspansiyonundaki canlı hücrelerin yüzdesinde, etiketlenmemiş muadili ile karşılaştırıldığında herhangi bir değişiklik yoksa, radyoaktif işaretli hücreleri kullanın. Canlı hücrelerin yüzdesi etiketlenmemiş muadilinden daha azsa, radyoaktif işaretli hücreleri atın.
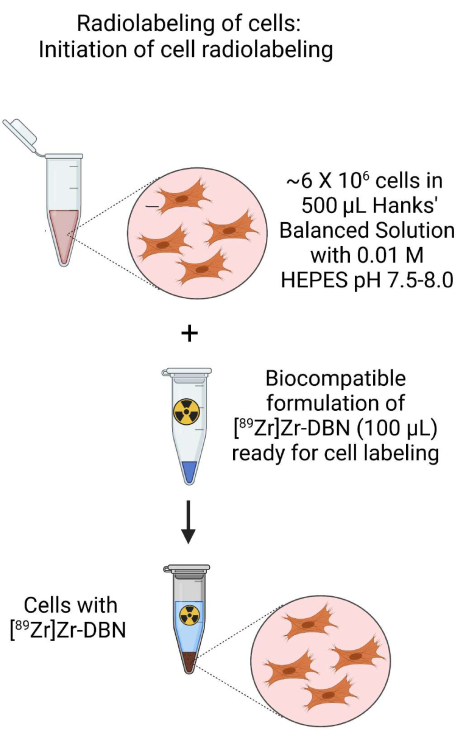
Şekil 3: Hücre radyoaktif etiketlemesinin başlatılmasının şeması. HEPES tamponlu Hanks dengeli tuz çözeltisinde hazırlanan hücre süspansiyonuna biyouyumlu olarak formüle edilmiş [89Zr] Zr-DBN'nin eklenmesiyle hücrelerin radyoaktif etiketlemesini başlatın. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
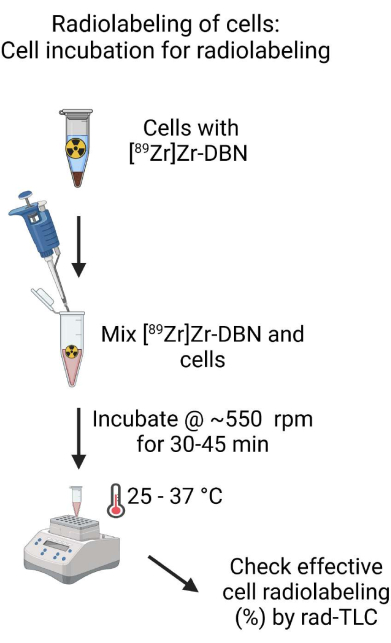
Şekil 4: Radyoetiketleme için hücre inkübasyonunun şeması. Biyouyumlu olarak formüle edilmiş [89Zr] Zr-DBN'yi hücre süspansiyonu ile iyice karıştırın ve hücre süspansiyonunu bir çalkalayıcı üzerinde sıcaklık kontrollü bir ısıtma bloğunda 30-60 dakika inkübe edin. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
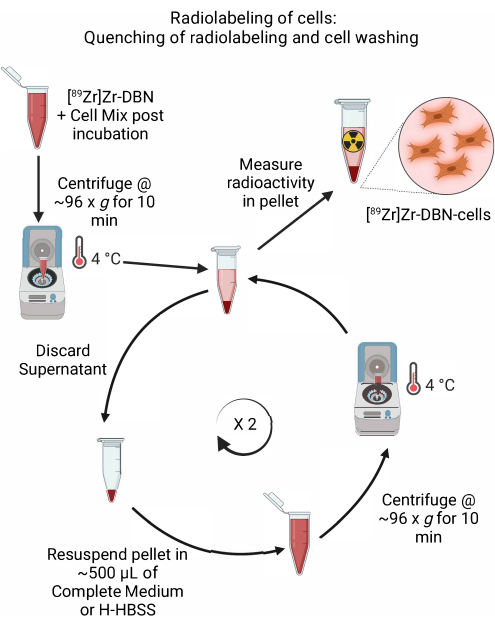
Şekil 5: Radyoişaretleme ve hücre yıkamanın söndürülmesinin şeması. Soğutulmuş hücre ortamı veya H-HBSS ilavesi ve ardından 4 ° C'de santrifüjleme ile hücrelerin radyoaktif etiketlemesini söndürün. Hücre yıkama için, süpernatanı atın ve hücre peletini ~ 500 μL soğutulmuş hücre ortamında veya H-HBSS'de yeniden süspanse edin. Bağlanmamış radyo-etiketleme synthonunu çıkarmak için süpernatanı atma ve hücre peletini taze ortamda yeniden süspanse etme döngüsünü tekrarlayın. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
Sonuçlar
Bu yazıda sunulan temsili sonuçlar, önceki [89Zr]Zr-DBN sentezi ve hücre radyo-etiketleme çalışmalarındanderlenmiştir 18,19,22,23,24,25. Kısaca, 89Zer, 7.5-15 μg DFO-Bn-NCS kullanılarak 25-37 ° C'de ~ 30-60 dakikada DFO-Bn-NCS ile başarılı bir şekilde komplekslenebilir (Tablo 2
Tartışmalar
Aşağıdakiler, etkili hücre radyo-etiketleme için optimizasyona ihtiyaç duyan protokoldeki kritik adımlardır. Protokol adımları 1.2 ve 1.3'te, kullanılan [89 Zr]Zr(HPO 4)2 veya [89Zr]ZrCl4 hacmine bağlı olarak, uygun bir hacim (mikrolitre) baz kullanılmalıdır; [89Zr]Zr(HPO4)2'nin nötralizasyonu için 1.0 MK2CO3çözeltisi ve 7.5-8.0 pH aralığına ulaşmak için [89Zr]ZrCl4'ün nötralizasyonu için 1.0 M
Açıklamalar
Yazarların finansal rekabet çıkarları yoktur, ancak bu teknolojinin mucitleridir (Patent # US20210330823A1).
Teşekkürler
Bu çalışma NIH 5R21HL127389-02, NIH 4T32HL007111-39, NIH R01HL134664 ve DOE DE-SC0008947 hibeleri, Uluslararası Atom Enerjisi Ajansı, Viyana, Mayo Clinic Nükleer Tıp Bölümü, Radyoloji Anabilim Dalı ve Mayo Clinic Rejeneratif Tıp Merkezi, Rochester, MN tarafından desteklenmiştir. Tüm figürler BioRender.com kullanılarak oluşturulmuştur.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A996-4 | |
| Alpha Minimum Essential Medium | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 12571063 | |
| Anion exchange column | Macherey-Nagel, Inc., Düren, Germany | 731876 | Chromafix 30-PS-HCO3 SPE 45 mg cartridge |
| Conical centrifuge tubes (15 mL) | Corning Inc., Glendale, AZ, USA | 352096 | Falcon 15 mL high-clarity polypropylene (PP) conical centrifuge tubes |
| Dendritic cells | The American Type Culture Collection, Manassas, VA, USA | CRL-11904 | |
| DFO-Bn-NCS | Macrocyclics, Inc., Plano, TX, USA | B-705 | p-SCN-Bn-Deferoxamine |
| DMSO | Sigma-Aldrich, Inc., St. Louis, MO | 276855 | |
| Dose calibrator | Mirion Technologies (Capintec), Inc., Florham Park, NJ, USA | 5130-3234 | CRC -55tR Dose Calibrator |
| Dulbecco’s modified Eagle’s medium | The American Type Culture Collection, Manassas, VA, USA | 30-2002 | |
| Fetal Bovine Serum (FBS) | The American Type Culture Collection, Manassas, VA, USA | 30-2020 | |
| Hanks Balanced Salt solution (HBSS) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 14025092 | For preparation of H-HBSS |
| Hydrochloric Acid (trace metal basis grade) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A508P212 | |
| Melanoma cells | The American Type Culture Collection, Manassas, VA, USA | CRL-6475 | |
| Methanol | Sigma-Aldrich, Inc., St. Louis, MO | 34860 | |
| Microcentrifuge tube | Eppendorf, Hamburg, Germany | 30108442 | Protein LoBind microcentrifuge tube |
| Murine GM-CSF | R&D Systems, Inc., Minneapolis, MN USA | 415-ML-010 | |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 15140-122 | |
| Phosphate Buffered Saline without Ca2+ and Mg2+ | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 10010023 | For washing cells |
| Saline | Covidien LLC, Mansfield, MA, USA | 1020 | 0.9% Sterile Saline Solution |
| Shaker | Eppendorf, Hamburg, Germany | T1317 | Thermomixer |
| Silica gel-rad-TLC paper sheet | Agilent Technologies Inc., Santa Clara, CA, USA | SGI0001 | iTLC-SG |
Referanslar
- Bhawnani, N., et al. Effectiveness of stem cell therapies in improving clinical outcomes in patients with heart failure. Cureus. 13 (8), e17236 (2021).
- Zakrzewski, W., Dobrzynski, M., Szymonowicz, M., Rybak, Z. Stem cells: past, present, and future. Stem Cell Research & Therapy. 10 (1), 68 (2019).
- Bukhari, A. B., Dutta, S., De, A. Image guidance in stem cell therapeutics: unfolding the blindfold. Current Drug Targets. 16 (6), 658-671 (2015).
- Momeni, A., Neelamegham, S., Parashurama, N. Current challenges for the targeted delivery and molecular imaging of stem cells in animal models. Bioengineered. 8 (4), 316-324 (2017).
- Gnecchi, M., Zhang, Z., Ni, A., Dzau, V. J. Paracrine mechanisms in adult stem cell signaling and therapy. Circulation Research. 103 (11), 1204-1219 (2008).
- D'Aloia, M. M., Zizzari, I. G., Sacchetti, B., Pierelli, L., Alimandi, M. CAR-T cells: the long and winding road to solid tumors. Cell Death & Disease. 9 (3), 282 (2018).
- Zhang, Q., et al. CAR-T cell therapy in cancer: tribulations and road ahead. Journal of Immunology Research. 2020, 1924379 (2020).
- Sterner, R. C., Sterner, R. M. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal. 11 (4), 69 (2021).
- Shao, F., et al. Radionuclide-based molecular imaging allows CAR-T cellular visualization and therapeutic monitoring. Theranostics. 11 (14), 6800-6817 (2021).
- Sakemura, R., Can, I., Siegler, E. L., Kenderian, S. S. In vivo CART cell imaging: Paving the way for success in CART cell therapy. Molecular Therapy Oncolytics. 20, 625-633 (2021).
- Wang, Y., et al. Dendritic cell biology and its role in tumor immunotherapy. Journal of Hematology & Oncology. 13 (1), 107 (2020).
- Bulte, J. W. M., Shakeri-Zadeh, A. In vivo MRI tracking of tumor vaccination and antigen presentation by dendritic cells. Molecular Imaging and Biology. 24 (2), 198-207 (2022).
- Holland, J. P., Sheh, Y., Lewis, J. S. Standardized methods for the production of high specific-activity zirconium-89. Nuclear Medicine and Biology. 36 (7), 729-739 (2009).
- Larenkov, A., et al. Preparation of zirconium-89 solutions for radiopharmaceutical purposes: interrelation between formulation, radiochemical purity, stability and biodistribution. Molecules. 24 (8), 1534 (2019).
- Pandey, M. K., et al. A new solid target design for the production of 89Zr and radiosynthesis of high molar activity [89Zr]Zr-DBN. American Journal of Nuclear Medicine and Molecular Imaging. 12 (1), 15-24 (2022).
- Pandey, M. K., et al. Improved production and processing of 89Zr using a solution target. Nuclear Medicine and Biology. 43 (1), 97-100 (2016).
- Pandey, M. K., Engelbrecht, H. P., Byrne, J. P., Packard, A. B., DeGrado, T. R. Production of 89Zr via the 89Y(p,n)89Zr reaction in aqueous solution: effect of solution composition on in-target chemistry. Nuclear Medicine and Biology. 41 (4), 309-316 (2014).
- Bansal, A., et al. Novel 89Zr cell labeling approach for PET-based cell trafficking studies. EJNMMI Research. 5, 19 (2015).
- Bansal, A., et al. 89Zr]Zr-DBN labeled cardiopoietic stem cells proficient for heart failure. Nuclear Medicine and Biology. 90-91, 23-30 (2020).
- Friberger, I., et al. Optimisation of the synthesis and cell labelling conditions for [89Zr]Zr-oxine and [89Zr]Zr-DFO-NCS: a direct in vitro comparison in cell types with distinct therapeutic applications. Molecular Imaging and Biology. 23 (6), 952-962 (2021).
- Lee, S. H., et al. Feasibility of real-time in vivo 89Zr-DFO-labeled CAR T-cell trafficking using PET imaging. PLoS One. 15 (1), e0223814 (2020).
- Nicolas, C. T., et al. Hepatocyte spheroids as an alternative to single cells for transplantation after ex vivo gene therapy in mice and pig models. Surgery. 164 (3), 473-481 (2018).
- Yang, B., et al. Tracking and therapeutic value of human adipose tissue-derived mesenchymal stem cell transplantation in reducing venous neointimal hyperplasia associated with arteriovenous fistula. Radiology. 279 (2), 513-522 (2016).
- Nicolas, C. T., et al. Ex vivo cell therapy by ectopic hepatocyte transplantation treats the porcine tyrosinemia model of acute liver failure. Molecular Therapy. Methods & Clinical Development. 18, 738-750 (2020).
- Bansal, A., Sharma, S., Klasen, B., Rosch, F., Pandey, M. K. Evaluation of different 89Zr-labeled synthons for direct labeling and tracking of white blood cells and stem cells in healthy athymic mice. Scientific Reports. 12 (1), 15646 (2022).
- Behfar, A., et al. Guided cardiopoiesis enhances therapeutic benefit of bone marrow human mesenchymal stem cells in chronic myocardial infarction. Journal of the American College of Cardiology. 56 (9), 721-734 (2010).
- Charoenphun, P., et al. 89Zr]oxinate4 for long-term in vivo cell tracking by positron emission tomography. European Journal of Nuclear Medicine and Molecular Imaging. 42 (2), 278-287 (2015).
- Sato, N., et al. In vivo tracking of adoptively transferred natural killer cells in rhesus macaques using 89zirconium-oxine cell labeling and PET imaging. Clinical Cancer Research. 26 (11), 2573-2581 (2020).
- Volpe, A., Pillarsetty, N. V. K., Lewis, J. S., Ponomarev, V. Applications of nuclear-based imaging in gene and cell therapy: probe considerations. Molecular Therapy Oncolytics. 20, 447-458 (2021).
- Fogli, L. K., et al. Challenges and next steps in the advancement of immunotherapy: summary of the 2018 and 2020 National Cancer Institute workshops on cell-based immunotherapy for solid tumors. Journal for Immunotherapy of Cancer. 9 (7), e003048 (2021).
- Li, X., Hacker, M. Molecular imaging in stem cell-based therapies of cardiac diseases. Advanced Drug Delivery Reviews. 120, 71-88 (2017).
- Puges, M., et al. Retrospective study comparing WBC scan and 18F-FDG PET/CT in patients with suspected prosthetic vascular graft infection. European Journal of Vascular and Endovascular Surgery. 57 (6), 876-884 (2019).
- Butterfield, L. H. Dendritic cells in cancer immunotherapy clinical trials: are we making progress. Frontiers in Immunology. 4, 454 (2013).
- de Vries, I. J. M., et al. Magnetic resonance tracking of dendritic cells in melanoma patients for monitoring of cellular therapy. Nature Biotechnology. 23 (11), 1407-1413 (2005).
- Gosmann, D., et al. Promise and challenges of clinical non-invasive T-cell tracking in the era of cancer immunotherapy. EJNMMI Research. 12 (1), 5 (2022).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır