È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Method Article
Tomografia a emissione di positroni Imaging del traffico cellulare: un metodo di radiomarcatura cellulare
In questo articolo
Riepilogo
Qui viene presentato un protocollo per radiomarcare le cellule con un radioisotopo per tomografia a emissione di positroni (PET), 89 Zr (t1/2 78,4 h), utilizzando un sintetizzatore radiomarcante pronto all'uso, [89 Zr]Zr-p-isotiocianatobenzil-desferrioxamina ([89Zr]Zr-DBN). La radiomarcatura delle cellule con [89Zr]Zr-DBN consente il monitoraggio e l'imaging non invasivi delle cellule radiomarcate somministrate nell'organismo con PET fino a 7 giorni dopo la somministrazione.
Abstract
Le terapie con cellule T con cellule staminali e recettori chimerici dell'antigene (CAR) stanno emergendo come terapie promettenti per la rigenerazione degli organi e come immunoterapia per vari tipi di cancro. Nonostante siano stati compiuti progressi significativi in queste aree, c'è ancora molto da imparare per comprendere meglio la farmacocinetica e la farmacodinamica delle cellule terapeutiche somministrate nel sistema vivente. Per il monitoraggio non invasivo e in vivo delle cellule con tomografia a emissione di positroni (PET), è stato sviluppato un nuovo metodo di radiomarcatura cellulare mediato da [89 Zr]Zr-p-isotiocianatobenzil-desferrioxamina ([89 Zr]Zr-DBN) utilizzando 89Zr (t1/2 78,4 h). Il presente protocollo descrive un synthon radiomarcato [89Zr]Zr-DBN-mediato, pronto all'uso, per la radiomarcatura diretta di una varietà di cellule, tra cui cellule staminali mesenchimali, cellule staminali cardiopoietiche guidate dal lignaggio, epatociti rigeneranti del fegato, globuli bianchi, cellule di melanoma e cellule dendritiche. La metodologia sviluppata consente l'imaging PET non invasivo del traffico cellulare fino a 7 giorni dopo la somministrazione senza influenzare la natura o la funzione delle cellule radiomarcate. Inoltre, questo protocollo descrive un metodo graduale per la radiosintesi di [89 Zr]Zr-DBN, la formulazione biocompatibile di [89 Zr]Zr-DBN, la preparazione delle cellule per la radiomarcatura e infine la radiomarcatura delle cellule con [89Zr]Zr-DBN, compresi tutti i dettagli intricati necessari per il successo della radiomarcatura delle cellule.
Introduzione
Le terapie a base di cellule T con cellule staminali e recettori chimerici dell'antigene (CAR) stanno guadagnando popolarità e sono in fase di studio attivo per il trattamento di varie malattie, come l'insufficienza miocardica1,2, la degenerazione retinica 2, la degenerazione maculare 2, il diabete 2, l'infarto del miocardio 3,4,5 e i tumori 6,7,8,9.10. Tra i due approcci plausibili delle terapie con cellule staminali, le cellule staminali possono essere innestate direttamente sul sito della malattia per causare una risposta terapeutica o causare cambiamenti nel microambiente del sito della malattia senza aderire al sito della malattia per avviare una risposta terapeutica indiretta. Una risposta terapeutica indiretta potrebbe causare cambiamenti nel microambiente della sede della malattia rilasciando fattori che potrebbero riparare o trattare la malattia5. Questi approcci di terapie con cellule staminali potrebbero essere valutati mediante imaging non invasivo di cellule staminali radiomarcate. L'imaging non invasivo potrebbe correlare l'assorbimento delle cellule radiomarcate nel sito della malattia con una risposta terapeutica per decifrare la risposta terapeutica diretta rispetto a quella indiretta.
Inoltre, sono in fase di sviluppo terapie basate sulle cellule immunitarie per il trattamento di vari tumori utilizzando le cellule T CAR 6,7,8,9,10 e l'immunoterapia con cellule dendritiche 11,12. Meccanicisticamente, nell'immunoterapia con cellule T CAR 6,7,8,9,10, le cellule T sono ingegnerizzate per esprimere un epitopo che si lega a un antigene specifico sui tumori che deve essere trattato. Queste cellule CAR-T ingegnerizzate, al momento della somministrazione, si legano all'antigene specifico presente sulle cellule tumorali attraverso un'interazione epitopo-antigene. Dopo il legame, le cellule CAR-T legate subiscono l'attivazione e quindi proliferano e rilasciano citochine, che segnalano al sistema immunitario dell'ospite di attaccare il tumore che esprime l'antigene specifico. Al contrario, nel caso delle terapie con cellule dendritiche11,12, le cellule dendritiche sono ingegnerizzate per presentare uno specifico antigene tumorale sulla loro superficie. Queste cellule dendritiche ingegnerizzate, quando somministrate, ospitano i linfonodi e si legano alle cellule T nei linfonodi. Le cellule T, legandosi agli antigeni tumorali specifici sulle cellule dendritiche somministrate, subiscono attivazione/proliferazione e avviano una risposta immunitaria dell'ospite contro il tumore che esprime quell'antigene specifico. Quindi, la valutazione del traffico di cellule CAR-T somministrate a un sito tumorale9,10 e l'homing delle cellule dendritiche ai linfonodi11,12 è possibile mediante imaging di cellule CAR-T radiomarcate e cellule dendritiche per determinare l'efficacia dell'immunoterapia. Inoltre, il traffico cellulare non invasivo può aiutare a comprendere meglio il potenziale terapeutico, chiarire la risposta terapeutica diretta rispetto a quella indiretta e prevedere e monitorare la risposta terapeutica delle terapie a base di cellule staminali e immunitarie.
Sono state esplorate diverse modalità di imaging per il traffico cellulare 3,4,9,10,12, tra cui l'imaging ottico, la risonanza magnetica (MRI), la tomografia computerizzata a emissione di singolo fotone (SPECT) e la tomografia a emissione di positroni (PET). Ognuna di queste tecniche ha i suoi vantaggi e svantaggi. Tra queste, la PET è la modalità più promettente grazie alla sua natura quantitativa e all'elevata sensibilità, che sono essenziali per la quantificazione affidabile delle cellule nel traffico cellularebasato sull'imaging 3,4,9,10.
Il radioisotopo che emette positroni 89Zr, con un'emivita di 78,4 ore, è adatto per la marcatura cellulare. Consente l'imaging PET del traffico cellulare per oltre 1 settimana ed è prontamente prodotto dai ciclotroni medici a bassa energia ampiamente disponibili 13,14,15,16,17. Inoltre, un chelante p-isotiocianatobenzil-desferrioxamina (DFO-Bn-NCS) opportunamente funzionalizzato è disponibile in commercio per la sintesi di un synthon marcato con 89 Zr, pronto all'uso, marcante con cellule, [89 Zr]Zr-p-isotiocianatobenzil-desferrioxamina, noto anche come [89Zr]Zr-DBN 18,19,20,21,22,23,24,25. Il principio della marcatura cellulare mediata da [89 Zr]Zr-DBN si basa su una reazione tra le ammine primarie delle proteine della membrana cellulare e la porzione isotiocianato (NCS) di [89Zr]Zr-DBN per produrre un legame tiourea covalente stabile.
[89Zr] L'etichettatura e l'imaging delle cellule basate su Zr-DBN sono state pubblicate per tracciare una varietà di cellule diverse, tra cui cellule staminali 18,23,25, cellule dendritiche18, cellule staminali cardiopoietiche19, cellule stromali deciduali 20, macrofagi derivati dal midollo osseo20, cellule mononucleate del sangue periferico 20, cellule T Jurkat/CAR 21, epatociti 22,24 e globuli bianchi 25. Il seguente protocollo fornisce metodi passo-passo per la preparazione e la radiomarcatura delle cellule con [89Zr]Zr-DBN e descrive le modifiche che possono essere richieste nel protocollo di radiomarcatura per un tipo di cellula specifico. Per maggiore chiarezza, il metodo di radiomarcatura delle cellule qui presentato è diviso in quattro sezioni. La prima sezione tratta della preparazione di [89 Zr]Zr-DBN mediante chelazione di 89Zr con DFO-Bn-NCS. La seconda sezione descrive la preparazione di una formulazione biocompatibile di [89Zr]Zr-DBN che può essere prontamente utilizzata per la radiomarcatura cellulare. La terza sezione riguarda le fasi necessarie per il precondizionamento delle cellule per la radiomarcatura. Il precondizionamento delle cellule comporta il lavaggio delle cellule con soluzione salina tamponata con fosfato privo di proteine (PBS) e soluzione salina bilanciata Hanks tamponata HEPES (H-HBSS) per rimuovere le proteine esterne, che potrebbero interferire o competere con la reazione di [89Zr]Zr-DBN con ammine primarie presenti sulle proteine della superficie cellulare durante la radiomarcatura. La sezione finale fornisce le fasi coinvolte nell'effettiva radiomarcatura delle cellule e nell'analisi del controllo di qualità.
Access restricted. Please log in or start a trial to view this content.
Protocollo
Le cellule dendritiche e le cellule di melanoma sono state ottenute commercialmente18. Gli epatociti sono stati isolati dal fegato dei suini dopo epatectomia parziale laparoscopica22,24. Le cellule staminali sono state isolate da aspirati di midollo osseo18,19,26. Le cellule staminali derivate dal tessuto adiposo sono state ottenute dal Laboratorio di Terapia Cellulare Umana, Mayo Clinic Rochester23. I globuli bianchi umani sono stati isolati dal sangue raccolto dalla Divisione di Medicina Trasfusionale, Mayo Clinic Rochester25. Varie cellule utilizzate per la radiomarcatura sono state ottenute e utilizzate in conformità con le linee guida raccomandate dal Comitato Istituzionale per la Cura e l'Uso degli Animali, dal Sottocomitato di Supervisione della Ricerca sulle Cellule Staminali della Mayo Clinic, dal Comitato di Ricerca della Divisione di Medicina Trasfusionale, dal Comitato Istituzionale per la Biosicurezza e dal Comitato per la Sicurezza delle Radiazioni.
1. Preparazione di [ 89 Zr ]Zr-p-isotiocianatobenzil-desferrioxamina ( [ 89Zr ]Zr-DBN)
Durata: ~160-220 min
NOTA: Per la preparazione di [89 Zr]Zr-DBN, isolare 89Zr sotto forma di [89 Zr]Zr-idrogeno fosfato ([89 Zr]Zr(HPO 4)2) o [89 Zr]Zr-cloruro ([89Zr]ZrCl4), come indicato al punto 1.1.
- Isolare 89 Zr dal genitore 89Y utilizzando un metodo di purificazione consolidato a base di resine di idrossimato13,17. In breve, preparare prima una colonna con ~100 mg di resina di idrossammato, quindi attivare la resina di idrossimato lavando la colonna con 8,0 mL di acetonitrile anidro puro, seguita da un lavaggio con 5,0-6,0 mL di aria. Quindi, lavare la colonna con 15 mL di acqua deionizzata, seguita da un altro lavaggio con 5,0-6,0 mL di aria, quindi passare 2,0 mL di HCl 0,50 N (grado di base di metallo in tracce) seguito da un ulteriore lavaggio con 5,0-6,0 mL di aria. Successivamente, caricare lentamente la soluzione contenente sia89 Zr che 89 Y nella resina di idrossamato e lavare l'89Y non legato dalla resina di idrossamato con 20 mL di HCl 2,0 N, seguito da 10 mL di acqua deionizzata e un lavaggio con 5,0-6,0 mL di aria.
NOTA: Dopo il lavaggio con aria, l'eluizione di 89Zr può essere eseguita come mostrato di seguito.- Per eluire 89 Zr sotto forma di [89 Zr]Zr(HPO 4)2, aggiungere prima 0,50 mL di tampone 1,2 M K 2 HPO 4/KH 2 PO 4 (pH 3,5) alla colonna dal passaggio 1.1 e lasciarlo riposare sulla colonna per 30 minuti per promuovere il rilascio di 89 Zr come [89Zr]Zr(HPO 4)2 dalla resina. Quindi, eluire gli 89Zr dalla colonna con altri 1,50 mL di tampone 1,2 M K 2 HPO 4/KH2PO4 (pH 3,5). Dopo l'eluizione di [89 Zr]Zr(HPO 4)2, seguire i passaggi 1.2, 1.2.1 e 1.2.2 per la preparazione di [89 Zr]Zr-DBN utilizzando [89Zr]Zr(HPO 4)2, come mostrato nella Figura 1.
- Per ottenere 89 Zr come [89 Zr]ZrCl4, eluire prima 89 Zr come [89Zr]Zr-ossalato.
- Per eluire 89 Zr sotto forma di [89 Zr]Zr-ossalato, aggiungere 0,50 mL di acido ossalico 1,0 M alla colonna dal passaggio 1.1 e lasciarlo riposare sulla colonna per 1 minuto per promuovere il rilascio di 89 Zr come [89Zr]-ossalato dalla resina. Quindi, eluire gli 89Zr dalla colonna con altri 2,50 mL di acido ossalico 1,0 M (totale di 3,0 mL)17.
- Per convertire [89 Zr]Zr-ossalato in [89Zr]ZrCl4 utilizzando una colonna a scambio anionico, come descritto da Larenkov et al.14, attivare prima la colonna lavando con 6,0 mL di acetonitrile, seguito da un lavaggio con 5,0-6,0 mL di aria. Quindi, lavare la colonna con 10,0 mL di soluzione fisiologica, seguita da un altro lavaggio di 5,0-6,0 mL di aria. Infine, passare 10,0 mL di acqua deionizzata, seguiti da un lavaggio con 5,0-6,0 mL di aria.
- Caricare lentamente la soluzione da 3,0 mL contenente [89Zr]Zr-ossalato sulla colonna di scambio anionico attivata, seguita da un lavaggio di 5,0-6,0 mL di aria. Quindi, lavare la colonna caricata con 89Zr con 50,0 mL di acqua deionizzata per rimuovere lo ione ossalato non legato, seguito da un lavaggio con 5,0-6,0 mL di aria.
- Per eluire 89 Zr sotto forma di [89 Zr]ZrCl 4, aggiungere 0,10 mL di HCl 1,0 N alla colonna, lasciarla riposare sulla colonna per 1,0 minuti per promuovere il rilascio di 89 Zr come [89 Zr]ZrCl4 dalla resina ed eluire gli 89Zr dalla colonna con ulteriori 0,40 mL di HCl 1,0 N (totale di 0,5 mL). Essiccare il [89Zr]ZrCl4 eluito in un flaconcino a forma di V mettendolo in un blocco riscaldante a 65 °C sotto un flusso costante di azoto gassoso per 10-30 minuti. Dopo l'asciugatura, ricostituire l'[89 Zr]ZrCl 4 essiccato in acqua e seguire i passaggi 1.3 e 1.3.1 per la preparazione di [89 Zr]Zr-DBN utilizzando [89Zr]ZrCl4, come mostrato nella Figura 1.
- Prelevare ~120 μL di [89Zr]Zr(HPO 4)2, formulato in 1,2 M K 2 HPO 4/KH 2 PO4 (pH 3,5) (10-25 MBq) dal passaggio 1.1.1 e neutralizzare la soluzione per ottenere pH 7,5-8,0 con ~100 μL di 1,0 M HEPES-KOH (pH 7,5) e ~65 μL di 1,0 M K 2CO3.
- Per ottenere la quantità appropriata di DFO-Bn-NCS per le fasi 1.2.2 o 1.3.1 per diverse formulazioni di 89 Zr con un'attività specifica apparente variabile di 89 Zr, eseguire una serie di reazioni chelanti utilizzando un volume fisso di una formulazione neutralizzata di [89 Zr]Zr(HPO 4)2 o [89Zr]ZrCl4 con un intervallo di DFO-Bn-NCS (7,5-15 μg). Nel caso di [89Zr]Zr(HPO4)2, incubare la reazione chelante a 37 °C in un agitatore a ~550 giri/min per 60 minuti. Mentre, nel caso di [89Zr]ZrCl4, incubare la reazione chelante a 25 °C in un agitatore a ~550 giri/min per 30 minuti. Scartare la reazione chelante che mostra precipitato durante o alla fine dell'incubazione. Al termine dell'incubazione, eseguire la cromatografia radioattiva su strato sottile (rad-TLC) con 100 mM di dietilentriamina pentaacetato (DTPA), pH 7,0, come fase mobile per stimare l'efficienza chelante di DFO-Bn-NCS per ciascuna reazione chelante, come discusso di seguito nel passaggio 1.5.
NOTA: In base all'efficienza di chelazione, utilizzare la quantità minima di DFO-Bn-NCS nei passaggi 1.2.2 o 1.3.1 necessaria per ottenere un'efficienza di chelazione del ≥97% senza causare precipitazioni di DFO-Bn-NCS nella formulazione neutralizzata di [89 Zr]Zr(HPO 4)2 o [89Zr]ZrCl4. Qui, [89Zr]Zr-DBN è stato sintetizzato in purezza radiochimica del ≥97%. - Preparare DFO-Bn-NCS fresco 5,0 mM in DMSO anidro (3,76 mg/mL) e aggiungere 4,0 μL di 5,0 mM di DFO-Bn-NCS (20 nmol o 15 μg) a ~285 μL di [89Zr]Zr(HPO4)2 neutralizzato (10-25 MBq) del passaggio 1.2 e miscelare la soluzione mediante pipettaggio. Mantenere la concentrazione finale di DMSO nella miscela chelante al di sotto del 2% del volume totale.
- Per ottenere la quantità appropriata di DFO-Bn-NCS per le fasi 1.2.2 o 1.3.1 per diverse formulazioni di 89 Zr con un'attività specifica apparente variabile di 89 Zr, eseguire una serie di reazioni chelanti utilizzando un volume fisso di una formulazione neutralizzata di [89 Zr]Zr(HPO 4)2 o [89Zr]ZrCl4 con un intervallo di DFO-Bn-NCS (7,5-15 μg). Nel caso di [89Zr]Zr(HPO4)2, incubare la reazione chelante a 37 °C in un agitatore a ~550 giri/min per 60 minuti. Mentre, nel caso di [89Zr]ZrCl4, incubare la reazione chelante a 25 °C in un agitatore a ~550 giri/min per 30 minuti. Scartare la reazione chelante che mostra precipitato durante o alla fine dell'incubazione. Al termine dell'incubazione, eseguire la cromatografia radioattiva su strato sottile (rad-TLC) con 100 mM di dietilentriamina pentaacetato (DTPA), pH 7,0, come fase mobile per stimare l'efficienza chelante di DFO-Bn-NCS per ciascuna reazione chelante, come discusso di seguito nel passaggio 1.5.
- Prelevare ~180 μL di [89Zr]ZrCl 4 formulato in HCl 0,1 N (40-80 MBq) dal passaggio 1.1.2.4 e neutralizzare la soluzione risultante per ottenere pH 7,5-8,0 con ~25 μL di 1,0 M Na2CO3.
- Preparare DFO-Bn-NCS fresco 2,5 mM in dimetilsolfossido anidro (DMSO) (1,88 mg/mL) e aggiungere 4,0 μL di 2,5 mM DFO-Bn-NCS (10 nmol o 7,5 μg) a ~205 μL di [89 Zr]ZrCl4 neutralizzato (40-80 MBq) dal passaggio 1.3. Miscelare la soluzione mediante pipettaggio. Mantenere la concentrazione finale di DMSO nella miscela chelante al di sotto del 2% del volume totale.
- Procedere con la chelazione di 89 Zr a 37 °C in agitatore a ~550 giri/min per 60 min nel caso di [89 Zr]Zr(HPO 4)2, o a 25 °C in agitatore a ~550 giri/min per 30 min nel caso di [89Zr]ZrCl4.
- Determinare l'efficienza di chelazione di 89Zr mediante rad-TLC con 100 mM DTPA (pH 7,0) come solvente mobile rad-TLC. Aspettatevi che [89 Zr]Zr-DBN mostri un R f di ~0.021-0.035, [89 Zr]ZrCl 4 mostri un R f di ~1.0 e [89Zr]Zr(HPO4)2 mostri un R f di ~1.0. Calcolare l'efficienza chelante (%) utilizzando l'equazione (1):
Percentuale di 89 Zr chelato a DFO-NCS per formare [89 Zr]Zr-DBN = [ (Radioattività a R f di [89 Zr]Zr - DBN) / (Somma delle radioattività a R f di [89 Zr]Zr - DBN e a R f di [89 Zr]Zr(HPO4)2 o [89Zr]ZrCl4) ] × 100 (1)
NOTA: L'efficienza chelante accettabile di 89Zr per procedere con la radiomarcatura cellulare, come determinato da rad-TLC, è del ≥97%. La purezza radiochimica suggerita del ≥97% di [89Zr]Zr-DBN è stata fissata in base ai requisiti di purezza radiochimica standard per altri radiofarmaci utilizzati sul campo. Vedere il rad-TLC rappresentativo nella Figura supplementare S1 e nella Figura supplementare S2.

Figura 1: Schema della preparazione di [89Zr]Zr-DBN. Per la preparazione di [89 Zr]Zr-DBN, neutralizzare [89 Zr]Zr(HPO 4)2 o [89Zr]ZrCl 4 preformulati a un pH di 7,5-8,0. Incubare la soluzione neutralizzata con DFO-Bn-NCS. Controllare l'efficienza chelante di 89Zr a DFO-Bn-NCS mediante rad-TLC. Fare clic qui per visualizzare una versione più grande di questa figura.
2. Formulazione biocompatibile di [ 89Zr ]Zr-DBN per la radiomarcatura cellulare (Figura 2)
Durata: ~35 min
NOTA: Dato il tempo necessario per la preparazione delle cellule nella fase 3, iniziare la fase 3 circa 20 minuti prima dell'inizio della fase 2 per un'incubazione di ~30 minuti. Ciò consente di avviare la radiomarcatura cellulare nella fase 4 entro ~5-10 minuti dal completamento delle fasi 2-3.2.2.
- Per la formulazione [89 Zr]Zr-DBN a base di [89 Zr]ZrCl 4, aggiungere 50,0 μL di una miscela compatibile con le cellule comprendente ~27,0 μL di 1,2 M K 2 HPO 4/KH2PO 4 (pH 3,5) + ~23,0 μL di tampone 1,0 M HEPES-KOH (PH 7,5) a 50,0 μL di [89 Zr]Zr-DBN. Incubare la miscela compatibile con le cellule [89Zr]Zr-DBN per ~30 minuti a temperatura ambiente (25 °C).
NOTA: La formulazione [89 Zr]Zr-DBN a base di [89Zr]Zr(HPO4)2 è biocompatibile per la radiomarcatura delle cellule e non richiede la fase 2.
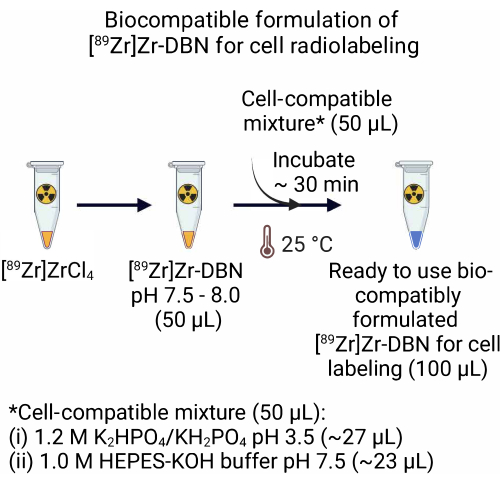
Figura 2: Preparazione della formulazione biocompatibile di [89Zr]Zr-DBN per la radiomarcatura cellulare. Per la preparazione di una formulazione biocompatibile pronta all'uso del sintetizzatore radiomarcante, aggiungere un volume uguale di miscela compatibile con le cellule, comprendente 1,2 M K 2 HPO 4/KH2PO4 (pH 3,5) + 1,0 M HEPES-KOH a un volume uguale di [89Zr]Zr-DBN. Incubare a 25 °C per ~30 min. Fare clic qui per visualizzare una versione più grande di questa figura.
3. Preparazione delle cellule per la radiomarcatura
Durata: ~40-50 min
- Tripsinizzare ~12 × 106 cellule aderenti (cellule staminali, cellule tumorali del melanoma, cellule staminali cardiopoietiche, cellule dendritiche o epatociti) e centrifugare le cellule in una provetta da centrifuga conica da 15,0 mL a ~96 × g per 10 minuti a 4 °C.
- Scartare il surnatante, risospendere il pellet cellulare in ~500 μL di PBS e trasferire la sospensione cellulare in una provetta per microcentrifuga da 1,5 mL. Centrifugare le cellule in una microcentrifuga a ~96 × g per 10 minuti a 4 °C.
- Scartare il surnatante e risospendere il pellet cellulare in ~500 μL di H-HBSS. Centrifugare le cellule in una microcentrifuga da 1,5 mL a ~96 × g per 10 minuti a 4 °C. Ripetere ancora una volta il passaggio 3.1.2 e procedere al passaggio 4.1.1.
NOTA: H-HBSS è una soluzione salina bilanciata Hanks con HEPES 0,01 M (pH 8,0).
- Nel caso di cellule non aderenti, come i globuli bianchi umani (globuli bianchi umani appena isolati dal sangue), saltare la tripsinizzazione e centrifugare la sospensione cellulare contenente ~12 × 106 cellule in una microcentrifuga da 1,5 mL a ~96 × g per 10 minuti a 4 °C.
- Scartare il surnatante, risospendere il pellet cellulare in ~500 μL di PBS e centrifugare le cellule in una microcentrifuga da 1,5 mL a ~96 × g per 10 minuti a 4 °C.
- Scartare il surnatante e risospendere il pellet cellulare in ~500 μL di H-HBSS. Centrifugare le cellule in una microcentrifuga da 1,5 mL a ~96 × g per 10 minuti a 4 °C. Ripetere ancora una volta il passaggio 3.2.2 e procedere al passaggio 4.1.1.
4. Radiomarcatura delle cellule
Durata: ~125-155 min
- Inizio della radiomarcatura cellulare (Figura 3)
- Utilizzare la sospensione cellulare del passaggio 3.1.2 o del passaggio 3.2.2 per preparare una sospensione cellulare da ~500 μL con circa ~6 × 106 cellule in ~500 μL di H-HBSS a pH 7,5-8,0 in una provetta per microcentrifuga da 1,5 mL.
- A questo, aggiungere ~100 μL di [89Zr]Zr-DBN biocompatibile dal passaggio 2.
- Incubazione cellulare per la radiomarcatura (Figura 4)
- Miscelare la formula biocompatibile [89Zr]Zr-DBN e la sospensione cellulare pipettando delicatamente su e giù con una micropipetta impostata a ~500 μL. Misurare la quantità di radioattività nella provetta di incubazione utilizzando un calibratore della dose di radioattività all'impostazione 489 per l'isotopo 89Zr16.
- Incubare le cellule e la miscela [89Zr]Zr-DBN in un agitatore a ~550 giri/min a 25-37 °C per 30-45 minuti per la marcatura cellulare.
NOTA: La temperatura dell'incubazione varia a seconda dei tipi di cellule utilizzate per la radiomarcatura, come mostrato nella Tabella 1. - Dopo l'incubazione nella fase 4.2.2, eseguire rad-TLC sulla reazione di radiomarcatura cellulare utilizzando un solvente rad-TLC appena preparato (20 mM di citrato di sodio [pH 4,9-5,1]:metanolo [1:1, V:V]). Dopo l'esecuzione di rad-TLC, cercare [89 Zr]Zr-DBN e [89 Zr]ZrCl4 intorno a R f = ~0.73-0.81 e R f = ~0.01-0.02 per le cellule radiomarcate. Calcolare la percentuale di radioattività a Rf = ~0.01-0.02 usando l'equazione (2).
Percentuale di radioattività a R f = ~0.01-0.02 = [ (Radioattività a R f= ~0.01 - 0.02) / (Somma delle radioattività a R f = ~0.01 - 0.02 e R f= ~0.73 - 0.81) ] × 100 (2)
NOTA: Per comprendere i picchi visualizzati a R f = ~0,01-0,02 e R f = ~0,73-0,81, vedere il rad-TLC per la reazione di radiomarcatura dei globuli bianchi nella Figura supplementare S3. - In una provetta separata per microcentrifuga da 1,5 mL, miscelare ~100 μL di [89Zr]Zr-DBN biocompatibile con ~500 μL di H-HBSS a pH 7,5-8,0 da utilizzare come controllo senza cellule per la correzione dello sfondo nel passaggio 4.2.5. Dopo l'incubazione a una temperatura e a un tempo simili a quelli utilizzati al punto 4.2.2, eseguire rad-TLC. Dopo l'esecuzione di rad-TLC, cercare [89 Zr]Zr-DBN e [89 Zr]ZrCl4 intorno a Rf = ~0.73-0.81. Calcolare la percentuale di radioattività a Rf = ~0.01-0.02 usando l'equazione (3).
Radioattività a R f = ~0.01-0.02 = [ (Radioattività a R f= ~0.01 - 0.02) / (Somma delle radioattività a R f= ~0.01 - 0.02 e R f= ~0.73 - 0.81) ] × 100 (3)
NOTA: Per comprendere i picchi visualizzati a Rf = ~0.01-0.02 e ~0.73-0.81, vedere il rad-TLC della reazione di controllo senza cellule nella Figura supplementare S4. - Calcolare l'effettiva radiomarcatura cellulare (%) sottraendo la percentuale di radioattività a R f = ~0.01-0.02 (da rad-TLC del passaggio 4.2.4) dalla percentuale di radioattività a R f = ~0.01-0.02 (da rad-TLC dal punto 4.2.3).
- Tempra della radiomarcatura e lavaggio delle cellule (Figura 5)
- Dopo aver confermato il completamento della radiomarcatura mediante rad-TLC nella fase 4.2.5, eseguire il quenching della reazione di radiomarcatura mediante l'aggiunta di ~600 μL di terreno completo refrigerato e appropriato per la cellula, o mediante l'aggiunta di H-HBSS, come mostrato nella Tabella 1.
- Centrifugare le cellule in una microcentrifuga a ~96 × g per 10 minuti a 4 °C. Scartare il surnatante.
- Risospendere delicatamente le cellule pellettate in ~500 μL di terreno refrigerato (Dulbecco's modified eagle medium (DMEM) + 10% di siero fetale bovino + 5% di penicillina/streptomicina o Roswell Park Memorial Institute-1640 (RPMI-1640) + 10% di siero fetale bovino + 5% di penicillina/streptomicina o H-HBSS per un particolare tipo di cellule, come mostrato nella Tabella 1. Eseguire la risospensione del pellet cellulare pipettando delicatamente su e giù con una micropipetta impostata a ~500 μL.
- Centrifugare le cellule in una microcentrifuga a ~96 × g per 10 minuti a 4 °C.
- Ripetere due volte i passaggi 4.3.2-4.3.4 per lavare via la radioattività non legata.
- Trasferire il pellet in una provetta fresca da microcentrifuga da 1,5 mL con DMEM + 10% di siero fetale bovino + 5% di penicillina/streptomicina nel caso di cellule staminali o H-HBSS e misurare la radioattività nel pellet cellulare utilizzando un calibratore di dose all'impostazione 489 per l'isotopo 89Zr16.
- Calcolare l'efficienza finale di radiomarcatura dopo tutti i lavaggi utilizzando l'equazione (4).
Efficienza di radiomarcatura = [(Radioattività corretta per il decadimento nel pellet cellulare al punto 4.3.6) / (Radioattività corretta per il decadimento nel pellet cellulare e H-HBSS al punto 4.2.1) ] × 100 (4) - Per garantire la qualità delle cellule radiomarcate, ispezionare prima visivamente la sospensione finale delle cellule radiomarcate per verificare la presenza di eventuali grumi. Se non ci sono grumi, procedere con questa sospensione finale al passaggio successivo. Se ci sono grumi, ma possono essere risospesi con il pipettaggio o con uno scuotimento delicato, farlo e procedere alla fase successiva, poiché questa supera l'ispezione visiva. Tuttavia, se i grumi non vengono risospesi né mediante pipettaggio né con un leggero scuotimento, scartare la sospensione e ricominciare da capo.
- Se l'ispezione visiva è superata, eseguire una prova di vitalità di esclusione del blu di tripano utilizzando una soluzione di blu di tripano allo 0,4% preparata in PBS entro 1 ora dalla radiomarcatura e dalle fasi di lavaggio (4.3.3-4.3.7) per valutare la vitalità cellulare delle cellule radiomarcate.
- Per eseguire il test, aggiungere 10,0 μL di soluzione di tripano blu allo 0,4% alla sospensione cellulare da 10,0 μL di cellule radiomarcate e non marcate e mescolarle pipettando la sospensione tripano di cellule blu su e giù con micropipetta impostata a 10,0 μL.
- Caricare un ematotometro con ~10,0 μL della miscela di sospensione di tripano di globuli blu, contare immediatamente il numero di cellule colorate di blu e il numero totale di cellule nell'ematotometro al microscopio a basso ingrandimento o utilizzando un contatore di cellule automatizzato. Calcolare la percentuale di cellule vitali utilizzando l'equazione (5).
Percentuale di cellule vitali = 100 - [(Numero di cellule colorate blu) / (Numero di cellule totali)] × 100 (5)
- Utilizzare le cellule radiomarcate se non vi è alcun cambiamento nella percentuale di cellule vitali nella sospensione cellulare radiomarcata rispetto alla controparte non marcata. Scartare le cellule radiomarcate se la percentuale di cellule vitali è inferiore alla controparte non marcata.
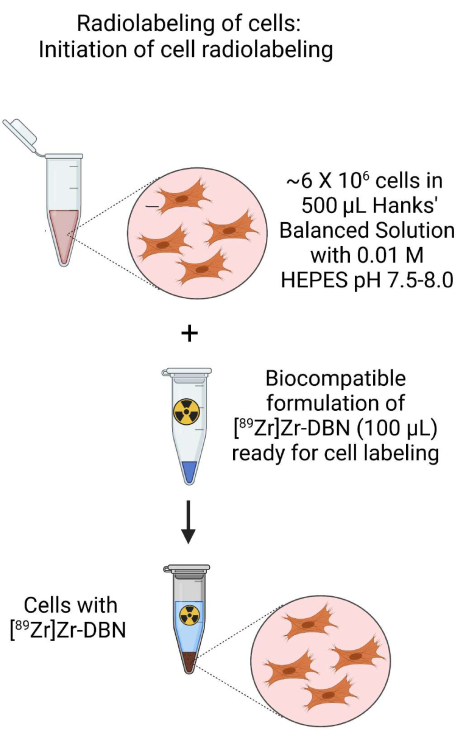
Figura 3: Schema dell'inizio della radiomarcatura cellulare. Avviare la radiomarcatura delle cellule mediante l'aggiunta del [89Zr]Zr-DBN biocompatibilmente formulato alla sospensione cellulare preparata in una soluzione salina bilanciata HEPES tamponata Hanks. Fare clic qui per visualizzare una versione più grande di questa figura.
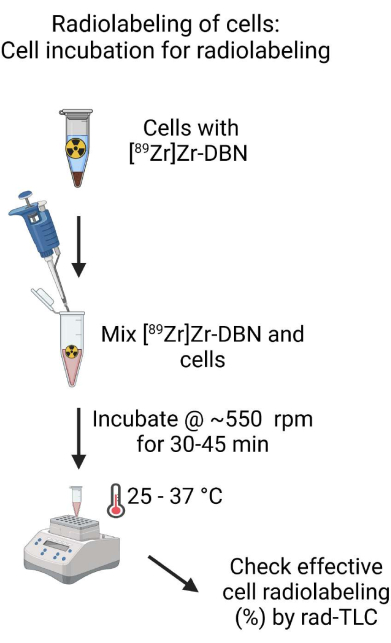
Figura 4: Schema dell'incubazione cellulare per la radiomarcatura. Miscelare accuratamente la formula biocompatibile [89Zr]Zr-DBN con la sospensione cellulare e incubare la sospensione cellulare in un blocco riscaldante a temperatura controllata su uno shaker per 30-60 minuti. Fare clic qui per visualizzare una versione più grande di questa figura.
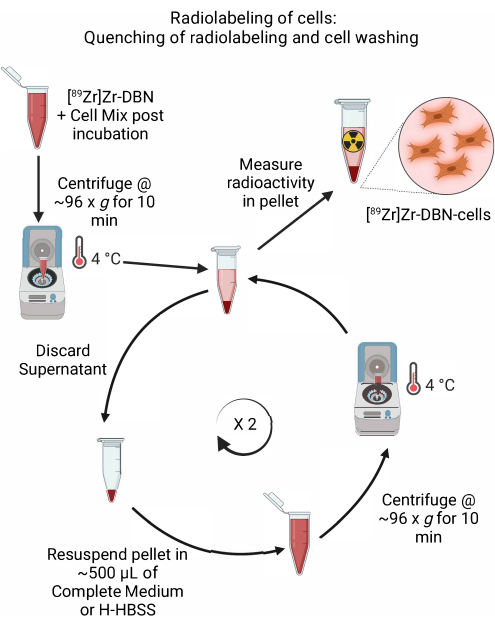
Figura 5: Schema dell'estinzione della radiomarcatura e del lavaggio delle cellule. Estinguere la radiomarcatura delle cellule mediante l'aggiunta di terreno cellulare refrigerato o H-HBSS, seguita da centrifugazione a 4 °C. Per il lavaggio delle cellule, scartare il surnatante e risospendere il pellet cellulare in ~500 μL di terreno cellulare refrigerato o H-HBSS. Ripetere il ciclo di eliminazione del surnatante e di risospensione del pellet cellulare in terreno fresco per rimuovere eventuali sintesi radiomarcanti non legate. Fare clic qui per visualizzare una versione più grande di questa figura.
Access restricted. Please log in or start a trial to view this content.
Risultati
I risultati rappresentativi presentati in questo manoscritto sono stati compilati dai precedenti studi di sintesi e radiomarcatura cellulare [89Zr]Zr-DBN 18,19,22,23,24,25. In breve, 89Zr può essere complessato con successo con DFO-Bn-NCS in ~30-60 minuti a 25-37 °C utilizzando 7,5-15 μg di DFO-Bn-NCS...
Access restricted. Please log in or start a trial to view this content.
Discussione
Di seguito sono riportati i passaggi critici del protocollo che devono essere ottimizzati per un'efficace radiomarcatura cellulare. Nelle fasi 1.2 e 1.3 del protocollo, a seconda del volume di [89 Zr]Zr(HPO 4)2 o [89Zr]ZrCl4 impiegato, deve essere utilizzato un volume appropriato (microlitri) di base; La soluzione di 1,0 MK 2 CO 3 deve essere utilizzata per la neutralizzazione di [89 Zr]Zr(HPO 4)2 e la soluzione 1,0 M Na2 CO3
Access restricted. Please log in or start a trial to view this content.
Divulgazioni
Gli autori non hanno alcun interesse finanziario in competizione, ma sono gli inventori di questa tecnologia (Brevetto # US20210330823A1).
Riconoscimenti
Questo lavoro è stato supportato da NIH 5R21HL127389-02, NIH 4T32HL007111-39, NIH R01HL134664 e sovvenzioni DOE DE-SC0008947, Agenzia Internazionale per l'Energia Atomica, Vienna, Mayo Clinic Division of Nuclear Medicine, Dipartimento di Radiologia e Mayo Clinic Center for Regenerative Medicine, Rochester, MN. Tutte le figure sono state create utilizzando BioRender.com.
Access restricted. Please log in or start a trial to view this content.
Materiali
| Name | Company | Catalog Number | Comments |
| Acetonitrile | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A996-4 | |
| Alpha Minimum Essential Medium | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 12571063 | |
| Anion exchange column | Macherey-Nagel, Inc., Düren, Germany | 731876 | Chromafix 30-PS-HCO3 SPE 45 mg cartridge |
| Conical centrifuge tubes (15 mL) | Corning Inc., Glendale, AZ, USA | 352096 | Falcon 15 mL high-clarity polypropylene (PP) conical centrifuge tubes |
| Dendritic cells | The American Type Culture Collection, Manassas, VA, USA | CRL-11904 | |
| DFO-Bn-NCS | Macrocyclics, Inc., Plano, TX, USA | B-705 | p-SCN-Bn-Deferoxamine |
| DMSO | Sigma-Aldrich, Inc., St. Louis, MO | 276855 | |
| Dose calibrator | Mirion Technologies (Capintec), Inc., Florham Park, NJ, USA | 5130-3234 | CRC -55tR Dose Calibrator |
| Dulbecco’s modified Eagle’s medium | The American Type Culture Collection, Manassas, VA, USA | 30-2002 | |
| Fetal Bovine Serum (FBS) | The American Type Culture Collection, Manassas, VA, USA | 30-2020 | |
| Hanks Balanced Salt solution (HBSS) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 14025092 | For preparation of H-HBSS |
| Hydrochloric Acid (trace metal basis grade) | Thermo Fisher Scientific, Inc., Waltham, MA, USA | A508P212 | |
| Melanoma cells | The American Type Culture Collection, Manassas, VA, USA | CRL-6475 | |
| Methanol | Sigma-Aldrich, Inc., St. Louis, MO | 34860 | |
| Microcentrifuge tube | Eppendorf, Hamburg, Germany | 30108442 | Protein LoBind microcentrifuge tube |
| Murine GM-CSF | R&D Systems, Inc., Minneapolis, MN USA | 415-ML-010 | |
| Penicillin/Streptomycin | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 15140-122 | |
| Phosphate Buffered Saline without Ca2+ and Mg2+ | Thermo Fisher Scientific, Inc., Waltham, MA, USA | 10010023 | For washing cells |
| Saline | Covidien LLC, Mansfield, MA, USA | 1020 | 0.9% Sterile Saline Solution |
| Shaker | Eppendorf, Hamburg, Germany | T1317 | Thermomixer |
| Silica gel-rad-TLC paper sheet | Agilent Technologies Inc., Santa Clara, CA, USA | SGI0001 | iTLC-SG |
Riferimenti
- Bhawnani, N., et al. Effectiveness of stem cell therapies in improving clinical outcomes in patients with heart failure. Cureus. 13 (8), e17236(2021).
- Zakrzewski, W., Dobrzynski, M., Szymonowicz, M., Rybak, Z. Stem cells: past, present, and future. Stem Cell Research & Therapy. 10 (1), 68(2019).
- Bukhari, A. B., Dutta, S., De, A. Image guidance in stem cell therapeutics: unfolding the blindfold. Current Drug Targets. 16 (6), 658-671 (2015).
- Momeni, A., Neelamegham, S., Parashurama, N. Current challenges for the targeted delivery and molecular imaging of stem cells in animal models. Bioengineered. 8 (4), 316-324 (2017).
- Gnecchi, M., Zhang, Z., Ni, A., Dzau, V. J. Paracrine mechanisms in adult stem cell signaling and therapy. Circulation Research. 103 (11), 1204-1219 (2008).
- D'Aloia, M. M., Zizzari, I. G., Sacchetti, B., Pierelli, L., Alimandi, M. CAR-T cells: the long and winding road to solid tumors. Cell Death & Disease. 9 (3), 282(2018).
- Zhang, Q., et al. CAR-T cell therapy in cancer: tribulations and road ahead. Journal of Immunology Research. 2020, 1924379(2020).
- Sterner, R. C., Sterner, R. M. CAR-T cell therapy: current limitations and potential strategies. Blood Cancer Journal. 11 (4), 69(2021).
- Shao, F., et al. Radionuclide-based molecular imaging allows CAR-T cellular visualization and therapeutic monitoring. Theranostics. 11 (14), 6800-6817 (2021).
- Sakemura, R., Can, I., Siegler, E. L., Kenderian, S. S. In vivo CART cell imaging: Paving the way for success in CART cell therapy. Molecular Therapy Oncolytics. 20, 625-633 (2021).
- Wang, Y., et al. Dendritic cell biology and its role in tumor immunotherapy. Journal of Hematology & Oncology. 13 (1), 107(2020).
- Bulte, J. W. M., Shakeri-Zadeh, A. In vivo MRI tracking of tumor vaccination and antigen presentation by dendritic cells. Molecular Imaging and Biology. 24 (2), 198-207 (2022).
- Holland, J. P., Sheh, Y., Lewis, J. S. Standardized methods for the production of high specific-activity zirconium-89. Nuclear Medicine and Biology. 36 (7), 729-739 (2009).
- Larenkov, A., et al. Preparation of zirconium-89 solutions for radiopharmaceutical purposes: interrelation between formulation, radiochemical purity, stability and biodistribution. Molecules. 24 (8), 1534(2019).
- Pandey, M. K., et al. A new solid target design for the production of 89Zr and radiosynthesis of high molar activity [89Zr]Zr-DBN. American Journal of Nuclear Medicine and Molecular Imaging. 12 (1), 15-24 (2022).
- Pandey, M. K., et al. Improved production and processing of 89Zr using a solution target. Nuclear Medicine and Biology. 43 (1), 97-100 (2016).
- Pandey, M. K., Engelbrecht, H. P., Byrne, J. P., Packard, A. B., DeGrado, T. R. Production of 89Zr via the 89Y(p,n)89Zr reaction in aqueous solution: effect of solution composition on in-target chemistry. Nuclear Medicine and Biology. 41 (4), 309-316 (2014).
- Bansal, A., et al. Novel 89Zr cell labeling approach for PET-based cell trafficking studies. EJNMMI Research. 5, 19(2015).
- Bansal, A., et al. 89Zr]Zr-DBN labeled cardiopoietic stem cells proficient for heart failure. Nuclear Medicine and Biology. 90-91, 23-30 (2020).
- Friberger, I., et al. Optimisation of the synthesis and cell labelling conditions for [89Zr]Zr-oxine and [89Zr]Zr-DFO-NCS: a direct in vitro comparison in cell types with distinct therapeutic applications. Molecular Imaging and Biology. 23 (6), 952-962 (2021).
- Lee, S. H., et al. Feasibility of real-time in vivo 89Zr-DFO-labeled CAR T-cell trafficking using PET imaging. PLoS One. 15 (1), e0223814(2020).
- Nicolas, C. T., et al. Hepatocyte spheroids as an alternative to single cells for transplantation after ex vivo gene therapy in mice and pig models. Surgery. 164 (3), 473-481 (2018).
- Yang, B., et al. Tracking and therapeutic value of human adipose tissue-derived mesenchymal stem cell transplantation in reducing venous neointimal hyperplasia associated with arteriovenous fistula. Radiology. 279 (2), 513-522 (2016).
- Nicolas, C. T., et al. Ex vivo cell therapy by ectopic hepatocyte transplantation treats the porcine tyrosinemia model of acute liver failure. Molecular Therapy. Methods & Clinical Development. 18, 738-750 (2020).
- Bansal, A., Sharma, S., Klasen, B., Rosch, F., Pandey, M. K. Evaluation of different 89Zr-labeled synthons for direct labeling and tracking of white blood cells and stem cells in healthy athymic mice. Scientific Reports. 12 (1), 15646(2022).
- Behfar, A., et al. Guided cardiopoiesis enhances therapeutic benefit of bone marrow human mesenchymal stem cells in chronic myocardial infarction. Journal of the American College of Cardiology. 56 (9), 721-734 (2010).
- Charoenphun, P., et al. 89Zr]oxinate4 for long-term in vivo cell tracking by positron emission tomography. European Journal of Nuclear Medicine and Molecular Imaging. 42 (2), 278-287 (2015).
- Sato, N., et al. In vivo tracking of adoptively transferred natural killer cells in rhesus macaques using 89zirconium-oxine cell labeling and PET imaging. Clinical Cancer Research. 26 (11), 2573-2581 (2020).
- Volpe, A., Pillarsetty, N. V. K., Lewis, J. S., Ponomarev, V. Applications of nuclear-based imaging in gene and cell therapy: probe considerations. Molecular Therapy Oncolytics. 20, 447-458 (2021).
- Fogli, L. K., et al. Challenges and next steps in the advancement of immunotherapy: summary of the 2018 and 2020 National Cancer Institute workshops on cell-based immunotherapy for solid tumors. Journal for Immunotherapy of Cancer. 9 (7), e003048(2021).
- Li, X., Hacker, M. Molecular imaging in stem cell-based therapies of cardiac diseases. Advanced Drug Delivery Reviews. 120, 71-88 (2017).
- Puges, M., et al. Retrospective study comparing WBC scan and 18F-FDG PET/CT in patients with suspected prosthetic vascular graft infection. European Journal of Vascular and Endovascular Surgery. 57 (6), 876-884 (2019).
- Butterfield, L. H. Dendritic cells in cancer immunotherapy clinical trials: are we making progress. Frontiers in Immunology. 4, 454(2013).
- de Vries, I. J. M., et al. Magnetic resonance tracking of dendritic cells in melanoma patients for monitoring of cellular therapy. Nature Biotechnology. 23 (11), 1407-1413 (2005).
- Gosmann, D., et al. Promise and challenges of clinical non-invasive T-cell tracking in the era of cancer immunotherapy. EJNMMI Research. 12 (1), 5(2022).
Access restricted. Please log in or start a trial to view this content.
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon