このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
光学分光ガス分析器を用いた水生生態系の溶存メタンの測定
要約
この研究では、閉ループの注入チャンバーに結合されたポータブル光学分析計を使用して、水性サンプル中のメタンガス濃度を測定するアプローチを示しています。結果は従来のガスクロマトグラフィーと同様であり、特に遠隔地でのフィールド研究に適した実用的で低コストの代替手段を提供します。
要約
生態系における温室効果ガス(GHG)フラックスとプールの測定は、気候変動との関連性から、生態学的研究においてますます一般的になりつつあります。それに伴い、研究グループ内のさまざまなプールやフラックスの測定に適応できる分析プラットフォームの必要性も高まっています。本研究では、ガスフラックス測定用に設計・販売された携帯型光学分光法を用いたガス分析計を用いて、水溶液中のGHG濃度を測定する方法を開発することを目的としています。このプロトコルには、従来のヘッドスペース平衡化技術と、それに続くガス分析器の入口ポートと出口ポートに閉ループで接続されたチャンバーにヘッドスペースガスサブサンプルを注入することが含まれます。チャンバーは、一般的なメイソンジャーと簡単な実験用品から製造されており、注射前の希釈が必要なサンプルに最適なソリューションです。チャンバーで測定されたメタン濃度は、同じバイアルのサブサンプルに対するガスクロマトグラフィー-水素炎イオン化検出(GC-FID)によって個別に決定された濃度と密接に相関しています(r2 > 0.98)。この手順は、クロマトグラフィー装置や消耗品が容易に入手できない遠隔地でのフィールド研究に特に関連しており、水系内のメタンやその他の溶存温室効果ガス濃度を測定するための実用的で安価で効率的なソリューションを提供します。
概要
湿地、湖沼、貯水池、河川、小川などの陸生-水生間期の生態系は、二酸化炭素(CO2)、メタン(CH4)、亜酸化窒素(N2O)1,2などの温室効果ガス(GHG)の重要な吸収源および発生源です。CH4は、特に、沈殿物細孔の飽和細孔空間での嫌気性呼吸中に生成されます。それが生成されると、画分は酸化されてCO2に変換され、残りは最終的に水柱や植生を通じて拡散するか、泡3に噴出します。ある時点で堆積物の細孔(すなわち、間隙水)を飽和させる水中のCH4の濃度は、CH4が生成、消費、および輸送される4のバランスを垣間見ることができます。垂直方向のプロファイルまたは時間で測定すると、間隙水濃度により、CH4の生産と消費、およびそれらの季節変動により活発なゾーンを特定することもできます。
従来、生態系の細孔水からのGHG濃度を決定する方法は、野外で収集された水サンプルを処理して、作成されたヘッドスペース内のガスを平衡化することを含みました。次に、ヘッドスペースをガスクロマトグラフィーで分析して、濃度を決定します5。この方法は生態学的研究に広く適用されていますが、ベンチトップガスクロマトグラフィー-水素炎イオン化検出(GC-FID)システムが必要であり、従来のラボスペースと、キャリブレーションと操作に高度な専門知識(例6)を割り当てる必要があります。また、キャリアガス(窒素(N2)やヘリウム(He)など)の大型タンクなど、遠隔地では容易に入手できない特殊な消耗品の使用も必要です。これらの要件と、それに伴うラボへのサンプル輸送のロジスティクスがサンプリング設計を制約し、場合によっては、クロマトグラフィー装置が利用できない場合に研究の範囲を制限する可能性があります。
この研究は、ポータブル光学分光法ベースのガス分析計を使用して、水溶液のヘッドスペースサンプルから溶存温室効果ガス濃度を測定するための代替方法を開発することを目的としています。このタイプの光ガス分析器は、標準的なGC-FIDシステムに代わる費用対効果の高いシステムであり、その携帯性により、フィールドワークアプリケーションに最適です。ポータブル光学分光法ベースのガス分析計は、ブランドやモデルにもよりますが、2〜5秒の応答時間で高周波ガス濃度測定(~1 s-1)を行います。これらの機器は、主に土壌、水、植生などのGHG排出表面からのガスフラックスを測定するために設計および販売されています7,8,9。光学分析装置は、対象の発光面上に展開された非定常状態のヘッドスペースチャンバーでの連続濃度測定から磁束計算を可能にします。表面チャンバでの通常の使用意図では、チャンバ内で観察される濃度の変化率、および既知のチャンバの寸法、圧力、および温度の高周波測定により、表面積(すなわち、表面フラックス)当たりの放出(または取り込み)の速度に関するこれらのデータの解釈が可能になる10。しかし、ポータブルガス分析計は、水性媒体中の溶存濃度に対応できておらず、最適化もされていないため、この種の分析には追加の適応と解釈が必要です。
ヘッドスペース8からの離散サンプルの濃度を決定するために光学分析器を使用するという以前のデモンストレーションを活用して、閉じたループで分析器に接続する小さな閉じたチャンバー(つまり、放出面がない)を設計しました。ヘッドスペースガスサブサンプルの注入後の濃度の変化とそれに続く希釈計算により、元のヘッドスペースの濃度を決定することができます。このアプローチの精度は、同じサンプルでGC-FIDによって得られた結果と結果を比較することによって評価されました。この方法は、ルイジアナ州の淡水湿地の実験サイトから収集された間孔水サンプル中のCH4 の垂直プロファイルを分析したユースケースを通じてさらに実証されています。
プロトコル
1. 間隙水のサンプリングと分析
- 細孔水透析サンプラー(のぞき見)11を使用してサンプルを収集します。調査サイトの関連する場所に覗き見を配置します。実証研究では、淡水湿地の2つの主要な植生パッチに6つのピーパーが配置されました:3つは Sagitaria lancifolia が優勢なパッチに、残りの3つは S.lancifolia と Typha latifolia の植生が共優勢なパッチに配置されました。
- 6月、9月、10月、12月に4回サンプルを収集します。土壌表面からその下~50cmまで10の異なる深さでサンプルを収集します。サンプリングは、12,13で説明されている方法に従いました。
- サンプリングの~20日前に、サンプリングセルに61mLの脱イオン水を入れます。実験室でN2 で脱イオン水を5分間泡立てて、酸素を除去してから現場で使用します。
- サンプリング中に、細胞の抽出ラインに接続されたシリンジを使用して、細胞から25 mLの水を引き出します。次に、二次セル再充電ラインを介してN2 で事前に泡立たせた新鮮な脱イオン水をセルに補充します。収集直後に濃度測定が必要な場合は、ステップ2.1に進みます。
- 0.2 mLの0.1 M HClで保存した10 mLガラスバイアルに抽出した水を加え、セプタムでキャップをし、実験室で分析するまで冷蔵します。
注:この方法のユーザーは、特定の研究ニーズに基づいて、収集深度、サンプリングスケジュール、および頻度を変更することができます。
2. 温室効果ガス濃度測定
- シリンジ内の間隙水サンプルのヘッドスペース平衡化の実施
- 平衡化技術を使用してヘッドスペースガスサンプルを作成します14。30 mLシリンジを使用して、現場で収集したサンプルから5 mLの水(Vpw)を採取し、15 mLのN2 (超高純度99.999%)を加えてヘッドスペース(Vhs)を作成します。
- シリンジを5分間激しく一貫して攪拌します、手動で、またはロッキングシェーカー(利用可能な場合)を使用して。次の手順で、光学分析器によるガス濃度測定に使用する10 mLの真空済みバイアルに12 mLのヘッドスペースガスサブサンプルを注入します(図1)。蠕動ポンプ15 でバイアルを排気するか、閉じたバイアル上の60mLシリンジのプランジャーを手動で引き抜き、空気を3回排出します。
注:彼はN2 の代わりにヘッドスペースを作成するために使用できます。シリンジにN2 またはHeを追加する手順は、ユーザーが利用できる実際のタンクの特定の適応またはレギュレーターによって異なります。この追加には、通常、マッチングチューブを使用してシリンジをタンクに結合するか、タンクに適合したサンプリングポートからシリンジを使用して抽出することが含まれます。現場の状況や関連する物流によっては、ユーザーは周囲の空気を使用してヘッドスペースを作り出すことができます。
- インジェクションチャンバーの作成
- 少量の空気(~1 - 5 mL)を密閉された空気に受け入れ、ガス分析器の流入と流出に接続して閉ループを形成できる注入チャンバーを製造します(材料表)。注入チャンバーと分析器は、システムの2つの主要な要素です(図2)。
- 365 mLメイソンジャーの金属製の蓋を変更するには、注入ポートとして1つのセプタムに収まるように直径11 mmの穴を1つ開け、アナライザーに接続するストップコックバルブを挿入するための直径7 mmの穴を2つ開けます。エポキシ接着剤を使用して注入ポートとフィッティングを締め、チャンバーの密閉を確保します。
- 注入チャンバーを光学分析器に接続します
- 5/32インチの内径(ID)と1/4インチの外径(OD)を使用して、ジャーを光学アナライザーの入口ポートと出口ポートに接続します。PFAプラスチックチューブであり、その追加体積を占めています。チューブが機器メーカーの推奨に従い、結露がなく清潔で乾燥していることを確認してください。
- 注入チャンバーを装置に接続するバルブを開いて、閉ループの空気回路を作成します。ガス濃度が安定するのを待ちます。
- チャンバーにサンプルを注入します
- チャンバー内の濃度と分析器内の信号が安定したら(つまり、標準偏差<0.03 ppm)、ステップ2.1.2で作成したヘッドスペースサンプルを含むバイアルから2 mLのサブサンプルを注入します。分析装置の濃度が再び安定するのを待ってから、次のサブサンプルを注入します(図3)。
- 濃度が 100 ppm に近づくと、最大 20 個のサブサンプルを連続して注入します (このしきい値を超える精度への影響については8を参照してください)。5サンプルごとにCH4 チェック標準を分析し、相対標準偏差(RSD)を使用して実際の測定値との違いを評価します。
- 積み重ねられた注入のセットが完了したら、装置に接続されているラインの 1 つを抜いてチャンバーを周囲圧力にリセットし、圧力とメタン濃度の大幅な蓄積を回避します。
注:複数回のテスト実行に基づいて、注入後~15秒で信号が安定することが決定されましたが、他の機器の記録仕様に応じて異なる時間が必要になる場合があります(図3)。使用した装置の流量は ~1 L/min、応答時間は 5 秒、異なる日の異なる分析中のキャビティ圧力は 720 から 745 Torr の範囲でした。
- ヘッドスペース内のCH4 濃度を計算する
- 各サブサンプルについて、式1を使用して、ヘッドスペース内の目標GHG(CH4、CO2、 N2Oなど)の濃度(Chs - μmol/mol)を計算します。
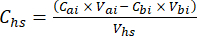 方程式 [1]
方程式 [1]
ここで、V hs はヘッドスペースサブサンプルのボリュームです。 - 注入前(Cbi - μmol mol-1)と注入後(Cai - μmol mol-1)の濃度を、注入前の 15 回の測定(~15 秒)と注入後の信号の安定化後の 15 回の平均として計算します。式 2 と 3 を使用して、注入前(Vbi)と注入後(Vai)の容量を mL 単位で計算します。
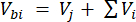 [2]
[2]
そして
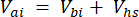 [3]
[3]
ここで、Vj (mL) はジャー (365 mL) とホース (125.4 mL) の添加量であり、Vi (mL) は注入されたサブサンプルの蓄積量です。
- 各サブサンプルについて、式1を使用して、ヘッドスペース内の目標GHG(CH4、CO2、 N2Oなど)の濃度(Chs - μmol/mol)を計算します。
- 間隙水濃度の計算
- ヘッドスペース内のCO2、CH4、またはN2Oの分圧(Pi - MPa)を、ヘッドスペース内のガスのモル分率と、式4を使用してサンプルの処理中の大気圧(P)を使用して計算します。
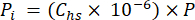 [4]
[4] - ヘッドスペースと水等価濃度と体積を指定した希釈方程式(式5)を使用して、間隙水中のGHGの水等価濃度を計算します。
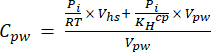 [5]
[5]
ここで、Rは万能気体定数(0.008314 L MPa mol−1 K−1)、は気温(K)、Vhsはヘッドスペースの体積(mL)、KHcpはCO2、CH4、またはN2Oのヘンリーの揮発性定数(それぞれ2.96、67.13、および3.82 L MPa/mol)16、Vpwはヘッドスペースを作成するために使用された液体サブサンプルの体積(mL)です。 - 測定中は記録されたTとPを使用してください。実証プロジェクトサンプルの分析中の平均TとPは、それぞれ295.15 Kと0.101325 MPaでした。
- ヘッドスペース内のCO2、CH4、またはN2Oの分圧(Pi - MPa)を、ヘッドスペース内のガスのモル分率と、式4を使用してサンプルの処理中の大気圧(P)を使用して計算します。
3. 標準的なクロマトグラフィー測定に対するバリデーション
- 従来のガスクロマトグラフで、10 mLバイアル中のさまざまな既知のCH4 濃度を分析します。それぞれ 20 個の標準からなる 3 つの同一のグループを使用します。最低濃度は5〜100ppmの範囲で、5ppm刻みで増加しました。
- ガスクロマトグラフでの水素炎イオン化検出により、CH4 濃度を測定します。クロマトグラフは、He(25 mL/min)をキャリアガスとして多孔質ポリマー吸収剤充填カラムを使用しました。標準濃度の測定を実行するには、クロマトグラフを0.99>カーブフィット(r2)に較正します。
- クロマトグラフィー後、製造業者によって較正された光学分析器(すなわち、精度(300s、1σ):0.3ppb CH4)を用いて、上記の方法を用いて同じ標準バイアル中のCH4濃度を決定することに進む。
- 3 つの標準グループのクロマトグラフィーおよび光学分析装置の結果に線形回帰を当てはめることにより、分析法の精度を評価します。各標準グループ内で実行された回帰の傾きと切片を比較することにより、分析法の再現性を評価します。効果のてこ比に重点を置いた標準最小二乗モデルを使用して比較を評価します。すべての回帰と比較を有意水準0.05で評価します。
結果
光学分析装置とガスクロマトグラフィーの比較
3 つの標準グループのガスクロマトグラフィーと光学分析装置で得られた結果は、傾きが 1 に近い良好な線形近似( r2 > 0.98)を示しました(図 4)。3つの実験における回帰の傾きは統計的に類似しており(F(2) = 0.478、p = 0.623)、結果の再現性が示唆されました。3つのケースす...
ディスカッション
この研究では、カスタムメイドの注入チャンバーと組み合わせたポータブル光学分光法ベースのガス分析計が、水サンプルから作成されたヘッドスペースを分析するための適用性を実証しました。このデモンストレーションはCH4に焦点を当てていましたが、このプロトコルは、CO2やN2O8などの他の関連するGHGの分析にも適用できます。
開示事項
著者は、利益相反を宣言しません。
謝辞
この研究は、DOE の賞 DE-SC0021067、DE-SC0023084、および DE-SC0022972 を通じて資金提供されました。湿原で採取した地点の間間水濃度データは、ESS-DIVE Data Archive(https://data.ess-dive.lbl.gov/view/doi:10.15485/1997524、2024年6月21日アクセス)で公開されています
資料
| Name | Company | Catalog Number | Comments |
| 1/4 in. I.D. x 3/8 in. O.D. Clear Vinyl Tubing | Home Depot | SKU # 702098 | Use to couple stopcocks and tubing connected to the instrument. Two short pieces (~4 cm). |
| 5/16 - 5/8 in. Stainless Steel Hose Clamp | Everbilt | 6260294 | Use to secure tubing connecting the stopcock valves and tubing connected to the instrument. |
| Crack-Resistant Teflon PFA Semi-Clear Tube for chemicals, 5/32" ID, 1/4" OD | McMaster-Carr | 51805K86 | Use to connect the injection chamber to the inlet and outlet ports of the instrument. We used two 0.68 m-long tubing in our experiment. |
| Drill with titanium step drillbit | Multiple companies | Use to drill the holes for septum and stopcocks in the jar's metallic lid. | |
| Gay butyl septum (stopper) | Weathon Microliter | 20-0025-B | Use as injection port and as vial septum (if compatible). |
| Headspace vials 20ml (23x75mm), Clear, Crimp Rounded Bottom | Restek | 21162 | Use to store the headspace sample. |
| Heavy Duty Steel Bond Epoxy GorillaWeld | Gorilla | 4330101 | Use to glue stopcock valves and septum to the jar's metallic lid. |
| Hypodermic Needles | Air-Tite Products Co. | N221 | Use to extract water from field vials, inject heaspace sample in vial and inject subsample to the injection chamber. |
| Mason jar (12 oz) | Ball, Kerr, Jarden | Larger or smaller chamber volumes can be chosen depending on sample concentrations. | |
| Optical spectroscopy-based gas analyzer | Multiple companies | Picarro G4301, Licor 7810, Licor 7820, ABB GLA131-GGA | These are some specific examples of analyzers that could be coupled to the injection chamber. We recognize that it is not an extensive list and other optical spectroscopy analyzers may also be suitable for the method. |
| Stopcock valve | DWK Life Sciences | 420163-0001 | Keep the valves open during normal operation. |
| Syringe (2.5 mL) | Air-Tite Products Co. | R2 | Use to extract subsamples from the headspace vials and inject them in the injecion chamber for analysis. |
| Syringe (30 mL) | Air-Tite Products Co. | R30HJ | Use to create headspace for gas analysis. |
参考文献
- Bastviken, D., Tranvik, L. J., Downing, J. A., Crill, P. M., Enrich-Prast, A. Freshwater methane emissions offset the continental carbon sink. Science. 331 (6013), 50 (2011).
- Quick, A. M., et al. Nitrous oxide from streams and rivers: A review of primary biogeochemical pathways and environmental variables. Earth-Sci Rev. 191, 224-262 (2019).
- Bridgham, S. D., Cadillo-Quiroz, H., Keller, J. K., Zhuang, Q. Methane emissions from wetlands: biogeochemical, microbial, and modeling perspectives from local to global scales. Glob Chang Biol. 19 (5), 1325-1346 (2013).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- McAuliffe, C. Gas chromatographic determination of solutes by multiple phase equilibrium. Chem Technol. 1, 46-51 (1971).
- Hoyos Ossa, D. E., Gallego Rios, S. E., Rodríguez Loaiza, D. C., Peñuela, G. A. Implementation of an analytical method for the simultaneous determination of greenhouse gases in a reservoir using FID/µECD gas chromatography. Int J Environ Anal Chem. 103 (12), 2915-2929 (2023).
- Kittler, F., et al. Long-term drainage reduces CO2 uptake and CH4 emissions in a Siberian permafrost ecosystem. Glob Biogeochem Cycles. 31 (12), 1704-1717 (2017).
- Wilkinson, J., Bors, C., Burgis, F., Lorke, A., Bodmer, P. Measuring CO2 and CH4 with a portable gas analyzer: Closed-loop operation, optimization and assessment. PLoS One. 13 (4), e0193973 (2018).
- Villa, J. A., et al. Ebullition dominates methane fluxes from the water surface across different ecohydrological patches in a temperate freshwater marsh at the end of the growing season. Sci Tot Environ. 767, 144498 (2021).
- Holland, E. A., et al. Soil CO2, N2O and CH4 exchange. Std Soil Meth Long-Term Ecol Res. , 185-201 (1999).
- MacDonald, L. H., Paull, J. S., Jaffé, P. R. Enhanced semipermanent dialysis samplers for long-term environmental monitoring in saturated sediments. Environ Monitor Assess. 185 (5), 3613-3624 (2013).
- Villa, J. A., et al. Plant-mediated methane transport in emergent and floating-leaved species of a temperate freshwater mineral-soil wetland. Limnol Oceanography. 65, 1635-1650 (2020).
- Villa, J. A., et al. Methane and nitrous oxide porewater concentrations and surface fluxes of a regulated river. Sci Tot Environ. 715, 136920 (2020).
- Kampbell, D. H., Wilson, J. T., Vandegrift, S. A. Dissolved oxygen and methane in water by a GC headspace equilibration technique. Int J Environ Anal Chem. 36 (4), 249-257 (1989).
- Rochette, P., Bertrand, N. Soil air sample storage and handling using polypropylene syringes and glass vials. Canadian J Soil Sci. 83 (5), 631-637 (2003).
- Sander, R. Compilation of Henry's law constants (version 4.0) for water as solvent. Atmos Chem Phys. 15 (8), 4399-4981 (2015).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- Comer-Warner, S. A., et al. Seasonal variability of sediment controls of carbon cycling in an agricultural stream. Sci Total Environ. 688, 732-741 (2019).
- U.S. Government Publishing Office. Title 42 - The Public Health and Wefare. U.S. Government Publishing Office. , (2009).
- Magen, C., et al. A simple headspace equilibration method for measuring dissolved methane. Limnol Oceanography Meth. 12 (9), 637-650 (2014).
- Regmi, B. P., Agah, M. Micro gas chromatography: An overview of critical components and their integration. Anal Chem. 90 (22), 13133-13150 (2018).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved