Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Optik Spektroskopi Gaz Analizörü Kullanarak Sucul Ekosistemlerde Çözünmüş Metanın Ölçülmesi
Bu Makalede
Özet
Bu çalışma, kapalı bir döngüde bir enjeksiyon odasına bağlı taşınabilir optik analizörler kullanılarak sulu numunelerdeki metan gazı konsantrasyonlarını ölçmek için bir yaklaşım göstermektedir. Sonuçlar, geleneksel gaz kromatografisine benzer ve özellikle uzak saha çalışmaları için uygun, pratik ve düşük maliyetli bir alternatif sunar.
Özet
Ekosistemlerdeki sera gazı (GHG) akışlarının ve havuzlarının ölçülmesi, iklim değişikliği ile ilgileri nedeniyle ekolojik çalışmalarda giderek daha yaygın hale gelmektedir. Bununla birlikte, araştırma grupları içindeki farklı havuzları ve akışları ölçmek için uyarlanabilen analitik platformlara olan ihtiyaç da artmaktadır. Bu çalışma, sulu numunelerdeki sera gazı konsantrasyonlarını ölçmek için orijinal olarak gaz akışı ölçümleri için tasarlanmış ve pazarlanan taşınabilir optik spektroskopi tabanlı gaz analizörlerini kullanmak için bir prosedür geliştirmeyi amaçlamaktadır. Protokol, geleneksel üst boşluk dengeleme tekniğini ve ardından bir üst boşluk gaz alt numunesinin, gaz analizörünün giriş ve çıkış portlarına kapalı bir döngü aracılığıyla bağlanan bir odaya enjeksiyonunu içerir. Hazne, jenerik bir mason kavanozundan ve basit laboratuvar malzemelerinden üretilmiştir ve enjeksiyon öncesi seyreltme gerektirebilecek numuneler için ideal bir çözümdür. Oda ile ölçülen metan konsantrasyonları, aynı şişelerden alınan alt numuneler üzerinde gaz kromatografisi-alev iyonizasyon tespiti (GC-FID) yoluyla ayrı ayrı belirlenen konsantrasyonlarla sıkı bir şekilde ilişkilidir (r2 > 0.98). Prosedür, özellikle kromatografi ekipmanının ve malzemelerinin hazır bulunmadığı uzak bölgelerdeki saha çalışmaları için geçerlidir ve su sistemlerindeki metan ve diğer çözünmüş sera gazı konsantrasyonlarını ölçmek için pratik, daha ucuz ve daha verimli bir çözüm sunar.
Giriş
Sulak alanlar, göller, rezervuarlar, nehirler ve dereler gibi karasal-sucul kesişim evresindeki ekosistemler, karbondioksit (CO2), metan (CH4) ve azot oksit (N2O) gibi sera gazlarının (GHG) önemli yutakları ve kaynaklarıdır1,2. CH4, özellikle, tortu gözeneklerinin doymuş gözenek boşluklarında anaerobik solunum sırasında üretilir. Üretildikten sonra, bir kısım oksitlenir ve CO2'ye dönüştürülürken, geri kalanı sonunda su sütunu ve bitki örtüsü boyunca yayılır veya kabarcıklar halinde patlar3. Belirli bir zamanda tortu gözeneklerini (yani gözenek suyunu) doyuran sudaki CH4 konsantrasyonu, üretilen, tüketilen ve taşınanCH 4 arasındaki dengeye bir bakış sunar 4. Dikey profiller veya zaman üzerinden ölçüldüğünde, gözenek suyu konsantrasyonu, CH4 üretimi ve tüketiminde daha aktif olan bölgelerin ve bunların mevsimsel değişimlerinin belirlenmesine de olanak tanır.
Geleneksel olarak, ekosistemlerdeki gözenek suyundan kaynaklanan sera gazı konsantrasyonunu belirleme yöntemleri, oluşturulan bir üst boşluktaki gazları dengelemek için sahada toplanan su örneklerinin işlenmesini içerir. Daha sonra, konsantrasyonları5 belirlemek için üst boşluk gaz kromatografisi ile analiz edilir. Bu yöntem ekolojik çalışmalarda yaygın olarak uygulanmakla birlikte, geleneksel laboratuvar alanı tahsis etmeyi ve kalibre etmek ve çalıştırmak için yüksek derecede uzman bilgisi gerektiren tezgah üstü gaz kromatografisi-alev iyonizasyon algılama (GC-FID) sistemleri gerektirir (örneğin6). Ayrıca, uzak yerlerde kolayca bulunamayan büyük taşıyıcı gaz tankları (yani Nitrojen (N2) ve Helyum (He)) gibi özel sarf malzemelerinin kullanılmasını gerektirir. Bu gereklilikler ve numunenin laboratuvara taşınmasının ilgili lojistiği, numune alma tasarımını kısıtlayabilir ve bazı durumlarda kromatografi ekipmanı mevcut olmadığında çalışmanın kapsamını sınırlayabilir.
Bu çalışma, taşınabilir optik spektroskopi tabanlı gaz analizörleri kullanarak sulu çözeltilerin üst boşluk örneklerinden çözünmüş sera gazı konsantrasyonlarını ölçmek için alternatif bir yöntem geliştirmeyi amaçlamıştır. Bu tip optik gaz analizörü, standart GC-FID sistemlerine uygun maliyetli bir alternatiftir ve taşınabilirliği, onu saha çalışması uygulamaları için ideal bir seçim haline getirir. Portatif optik spektroskopi tabanlı gaz analizörleri, marka ve modellere bağlı olarak 2 - 5 s tepki süreleriyle yüksek frekanslı gaz konsantrasyonu ölçümleri (yani ~ 1 s-1) üretir. Bu araçlar, öncelikle toprak, su ve bitki örtüsü gibi sera gazı yayan yüzeylerden gaz akışlarını belirlemek için tasarlanmış ve pazarlanmaktadır 7,8,9. Optik analizörler, ilgili yayan yüzeyler üzerine yerleştirilen kararlı olmayan durumdaki üst boşluk odalarındaki sürekli konsantrasyon ölçümlerinden akı hesaplamasına izin verir. Yüzey odaları ile düzenli amaçlanan kullanımlarında, odada gözlemlenen konsantrasyonlardaki değişim oranının ve bilinen oda boyutlarının, basıncın ve sıcaklığın yüksek frekanslı ölçümleri, bu verilerin yüzey alanı başına emisyon (veya alım) oranı (yani yüzey akışları) olarak yorumlanmasına izin verir10. Bununla birlikte, portatif gaz analizörleri, sulu ortamdaki çözünmüş konsantrasyonlar için ne donatılmıştır ne de optimize edilmiştir, bu da bu tür analizler için ek uyarlamalar ve yorumlar gerektirir.
Üst boşluklardan8 ayrı numunelerdeki konsantrasyonları belirlemek için optik analizörlerin kullanımına ilişkin önceki gösterilerden yararlanarak, analizöre kapalı bir döngüde bağlanan küçük, kapalı bir oda (yani yayan yüzeyler olmayan) tasarladık. Üst boşluk gazı alt numunesinin enjeksiyonundan sonra konsantrasyonlardaki değişiklik ve ardından seyreltme hesaplamaları, orijinal üst boşluğun konsantrasyonlarının belirlenmesine izin verir. Bu yaklaşımın kesinliği, sonuçları aynı numunelerde GC-FID yoluyla elde edilenlerle karşılaştırılarak değerlendirildi. Yöntem ayrıca, Louisiana'daki bir tatlı su bataklığındaki deney alanlarından toplanan gözenek suyu örneklerinde CH4'ün dikey profillerini analiz eden bir kullanım durumu ile gösterilmiştir.
Protokol
1. Gözenek suyu örneklemesi ve analizi
- Gözenekli diyaliz örnekleyicileri (gözetleyiciler) kullanarak örnekleri toplayın11. Gözetleyenleri çalışma alanının ilgili yerlerine yerleştirin. Gösteri çalışmasında, bir tatlı su bataklığının iki baskın bitki örtüsü yaması üzerinde 6 gözetleyici konuşlandırıldı: üçü Sagitaria lancifolia'nın hakim olduğu bir yama üzerinde ve diğer üçü S. lancifolia ve Typha latifolia bitki örtüsünün birlikte hakim olduğu bir yama üzerinde.
- Haziran, Eylül, Ekim ve Aralık aylarında 4 kez numune toplayın. Toprak yüzeyinden ~50 cm altına kadar 10 farklı derinlikte numune toplayın. Örnekleme, 12,13'te açıklanan yöntemi izlemiştir.
- Numune alma hücrelerini, numune almadan ~ 20 gün önce 61 mL deiyonize su ile doldurun. Sahada kullanmadan önce oksijeni çıkarmak için laboratuvarda 5 dakika boyunca N2 ile deiyonize su kabarcıklandırın.
- Numune alma sırasında, hücrenin ekstraksiyon hattına bağlı bir şırınga ile hücreden 25 mL su çekin. Ardından, hücreleri ikincil bir hücre şarj hattı aracılığıylaN2 ile önceden köpürtülmüş taze deiyonize su ile doldurun. Toplama işleminden hemen sonra konsantrasyon ölçümleri gerekiyorsa, adım 2.1'e geçin.
- Ekstrakte edilen suyu, 0.2 mL 0.1 M HCl ile korunmuş 10 mL cam şişelere ekleyin, septum ile kapatın ve laboratuvarda analiz edilene kadar buzdolabında saklayın.
NOT: Bu yöntemin kullanıcıları, belirli çalışma ihtiyaçlarına göre toplama derinliklerini, örnekleme programını ve sıklığı değiştirebilir.
2. Sera gazı konsantrasyonu ölçümü
- Bir şırıngadaki gözenek suyu numunelerinin üst boşluk dengesini gerçekleştirin
- Dengeleme tekniğini kullanarak üst boşluk gaz örnekleri oluşturun14. Sahada toplanan örneklerden 5 mL su (Vpw) çekmek için 30 mL'lik bir şırınga kullanın ve ardından üst boşluğu (Vhs) oluşturmak için 15 mLN2 (Ultra Yüksek Saflıkta %99.999) ekleyin.
- Şırıngayı manuel olarak veya sallanan bir çalkalayıcı (varsa) kullanarak 5 dakika boyunca kuvvetli ve tutarlı bir şekilde çalkalayın. Aşağıdaki adımlarda optik analizör ile gaz konsantrasyonu ölçümleri için kullanılan 10 mL'lik önceden boşaltılmış bir şişeye 12 mL üst boşluk gazı alt numunesi enjekte edin (Şekil 1). Şişeleri peristaltik bir pompa15 ile boşaltın veya kapalı şişenin üzerindeki 60 mL'lik bir şırınganın pistonunu manuel olarak çekin ve havayı 3 kez dışarı pompalayın.
NOT: Headspace'i oluşturmak için N2 yerine kullanılabilir. ŞırıngayaN2 veya He ekleme prosedürü, kullanıcılara sunulan gerçek tankın özel adaptasyonuna veya regülatörüne bağlıdır. Bu ilave, tipik olarak, şırınganın uygun boru kullanılarak tanka bağlanmasını veya şırınga ile tanka uyarlanmış bir numune alma portundan ekstraksiyonu içerir. Saha koşullarına ve ilgili lojistiğe bağlı olarak, kullanıcılar üst boşluğu oluşturmak için ortam havasını kullanabilir.
- Enjeksiyon odasını oluşturun
- Kapalı bir döngü oluşturmak için gaz analizörü giriş ve çıkışına bağlanan kapalı bir hava hacmine küçük bir hacimde havayı (~ 1 - 5 mL) kabul edebilen bir enjeksiyon odası üretin (Malzeme Tablosu). Enjeksiyon odası ve analizör, sistemin iki ana unsurudur (Şekil 2).
- 365 mL'lik bir mason kavanozun metal kapağını, enjeksiyon portu olarak bir septuma uyacak şekilde 11 mm çapında bir delik ve analizöre bağlanan vanaları yerleştirmek için iki adet 7 mm çapında delik açarak değiştirin. Enjeksiyon portunu ve bağlantı parçalarını sıkmak ve haznenin sızdırmazlığını sağlamak için epoksi yapıştırıcı kullanın.
- Enjeksiyon odasını optik analizöre bağlayın
- 5/32 inç iç çap (ID) ve 1/4 inç dış çap (OD) kullanarak kavanozu optik analizörün giriş ve çıkış portlarına bağlayın. PFA plastik boru ve eklenen hacimlerini hesaba katın. Borunun cihaz üreticisinin tavsiyesine uyduğundan ve yoğuşma olmadan temiz ve kuru olduğundan emin olun.
- Kapalı döngü bir hava devresi oluşturmak için enjeksiyon odasını cihaza bağlayan valfleri açılacak şekilde ayarlayın. Gaz konsantrasyonlarının stabilize olmasını bekleyin.
- Odaya bir numune enjekte edin
- Odadaki konsantrasyon ve analizördeki sinyal stabilize olduğunda (yani standart sapma <0.03 ppm), adım 2.1.2'de oluşturulan üst boşluk örneğini içeren şişelerden 2 mL'lik bir alt numune enjekte edin. Bir sonraki alt numuneyi enjekte etmeden önce analizördeki konsantrasyonların tekrar stabilize olmasını bekleyin (Şekil 3).
- Konsantrasyon 20 ppm'ye yaklaşırsa art arda 100'ye kadar veya daha az alt numune enjekte edin (bu eşiğin üzerindeki doğruluk üzerindeki etkiler için8'ebakın). Her 5 numune için CH4 kontrol standartlarını analiz edin ve nispi standart sapmayı (RSD) kullanarak gerçek ölçümlerle farkı değerlendirin.
- İstiflenmiş enjeksiyon seti ile işiniz bittiğinde, hazneyi ortam basıncına sıfırlamak ve önemli basınç ve metan konsantrasyonu oluşumunu önlemek için cihaza bağlı hatlardan birinin fişini çekin.
NOT: Birden fazla test çalışmasına dayanarak, sinyalin enjeksiyondan ~ 15 s sonra stabilize olduğu belirlendi, ancak diğer cihaz kayıt özelliklerine yanıt olarak farklı süreler gerekebilir (Şekil 3). Kullanılan cihazın akış hızı, 5 s'lik bir tepki süresi ve 720 ila 745 Torr arasında değişen farklı günlerde yapılan farklı analizler sırasında boşluk basıncı ile ~ 1 L / dak idi.
- Üst boşluktaki CH4 konsantrasyonlarını hesaplayın
- Her bir alt numune için, denklem 1 ile üst boşluktaki (Chs - μmol / mol) hedef sera gazı (örn. CH4, CO2, N2O) konsantrasyonunu hesaplayın:
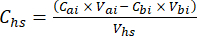 Denklem [1]
Denklem [1]
Burada Vhs , üst boşluk alt örneğinin hacmidir. - Enjeksiyondan önce (Cbi - μmol mol-1) ve enjeksiyondan sonra (Cai - μmol mol-1) konsantrasyonları, enjeksiyondan önce 15 ölçümün (~ 15 s) ve enjeksiyon sonrası sinyalin stabilizasyonundan sonra 15 ölçümün ortalaması olarak hesaplayın. Denklem 2 ve 3 ile enjeksiyonlardan önce (Vbi) ve sonra (Vai) mL cinsinden hacimleri hesaplayın:
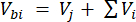 [2]
[2]
ve
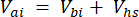 [3]
[3]
Burada Vj (mL), kavanozun (365 mL) ve hortumun (125.4 mL) eklenen hacmidir ve Vi (mL), enjekte edilen alt numunelerin birikmiş hacmidir.
- Her bir alt numune için, denklem 1 ile üst boşluktaki (Chs - μmol / mol) hedef sera gazı (örn. CH4, CO2, N2O) konsantrasyonunu hesaplayın:
- Gözenek suyu konsantrasyonunu hesaplayın
- Denklem 2'ü kullanarak numunenin işlenmesi sırasında üst boşluktaki gazın mol fraksiyonunu ve atmosferik basıncı (P) kullanarak üst boşluktaki CO2, CH4 veya N4O'nun kısmi basıncını (P i - MPa) hesaplayın:
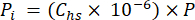 [4]
[4] - Üst boşluk ve sulu eşdeğer konsantrasyonlar ve hacimler ile bir seyreltme denklemi (denklem 5) kullanarak gözenekli sudaki sera gazlarının sulu eşdeğer konsantrasyonunu hesaplayın:
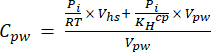 [5]
[5]
R, evrensel gaz sabiti (0.008314 L MPa mol−1 K-1) olduğunda, hava sıcaklığıdır (K), Vhs, üst boşluğun hacmidir (mL), KHcp, Henry'nin CO2, CH4 veya N2O (sırasıyla 2.96, 67.13 ve 3.82 L MPa/mol) uçuculuk sabitidir.16 ve Vpw, üst boşluğu (mL) oluşturmak için kullanılan sıvı alt numunenin hacmidir. - Ölçümler sırasında kaydedilen T ve P'yi kullanın. Demonstrasyon projesi örneklerinin analizi sırasında ortalama T ve P sırasıyla 295.15 K ve 0.101325 MPa idi.
- Denklem 2'ü kullanarak numunenin işlenmesi sırasında üst boşluktaki gazın mol fraksiyonunu ve atmosferik basıncı (P) kullanarak üst boşluktaki CO2, CH4 veya N4O'nun kısmi basıncını (P i - MPa) hesaplayın:
3. Standart kromatografi ölçümlerine karşı doğrulama
- Konvansiyonel bir gaz kromatografında 10 mL'lik şişelerde bilinen farklıCH4 konsantrasyonlarını analiz edin. Her biri 20 standarttan oluşan üç özdeş grup kullanın. En düşük konsantrasyonlar 5 ila 100 ppm arasında değişmiş ve 5 ppm'lik artışlarla artmıştır.
- Bir gaz kromatografında alev iyonizasyon tespiti ile CH4 konsantrasyonlarını belirleyin. Kromatograf, taşıyıcı gaz olarak He (25 mL / dak) ile gözenekli bir polimer emici paketlenmiş kolon kullandı. Standartların konsantrasyonlarının ölçümlerini yapmak için kromatografı 2 > 0.99 eğrisine uyacak şekilde kalibre edin.
- Kromatografiden sonra, üretici tarafından kalibre edilmiş bir optik analizör kullanarak (yani hassasiyet (300 s, 1σ): 0,3 ppb CH4) yukarıda açıklanan yöntemi kullanarak aynı standart şişelerde CH4 konsantrasyonunu belirlemeye devam edin.
- Üç standart grubun kromatografi ve optik analizör sonuçlarına doğrusal bir regresyon uydurarak yöntemin doğruluğunu değerlendirin. Her bir standart grubu içinde gerçekleştirilen regresyonların eğimlerini ve kesişimlerini karşılaştırarak yöntemin tekrarlanabilirliğini değerlendirin. Efekt Kaldıracına vurgu yaparak Standart En Küçük Kareler Modeli kullanarak karşılaştırmayı değerlendirin. Tüm regresyonları ve karşılaştırmaları 0,05 anlamlılık düzeyinde değerlendirin.
Sonuçlar
Optik analizöre karşı gaz kromatografisi
Üç standart grubu için gaz kromatografisi ve optik analizör yoluyla elde edilen sonuçlar, bire yakın eğimlerle iyi doğrusal uyumlar (yani, r2 > 0.98) gösterdi (Şekil 4). Üç deneydeki regresyonların eğimleri istatistiksel olarak benzerdi (F (2) = 0.478, p = 0.623), bu da sonuçların tekrarlanabilirliğini düşündürdü. Her üç durumda da eğimlerin birden b?...
Tartışmalar
Bu çalışma, su örneklerinden oluşturulan üst boşlukları analiz etmek için özel yapım bir enjeksiyon odasına bağlı taşınabilir optik spektroskopi tabanlı gaz analizörlerinin uygulanabilirliğini göstermiştir. Gösteri CH4'e odaklandı, ancak protokol CO2 ve N2O8 gibi diğer ilgili sera gazlarını analiz etmek için uygulanabilir. Amaç, sera gazı konsantrasyon ölçüm çalışmalarında geleneksel gaz kromatog...
Açıklamalar
Yazarlar herhangi bir çıkar çatışması beyan etmemektedir.
Teşekkürler
Bu çalışma, DOE ödülleri DE-SC0021067, DE-SC0023084 ve DE-SC0022972 aracılığıyla finanse edildi. Bataklıkta örneklenen alanların gözenek suyu konsantrasyonu verileri, ESS-DIVE Veri Arşivi'nde (https://data.ess-dive.lbl.gov/view/doi:10.15485/1997524, 21 Haziran 2024'te erişildi) kamuya açıktır
Malzemeler
| Name | Company | Catalog Number | Comments |
| 1/4 in. I.D. x 3/8 in. O.D. Clear Vinyl Tubing | Home Depot | SKU # 702098 | Use to couple stopcocks and tubing connected to the instrument. Two short pieces (~4 cm). |
| 5/16 - 5/8 in. Stainless Steel Hose Clamp | Everbilt | 6260294 | Use to secure tubing connecting the stopcock valves and tubing connected to the instrument. |
| Crack-Resistant Teflon PFA Semi-Clear Tube for chemicals, 5/32" ID, 1/4" OD | McMaster-Carr | 51805K86 | Use to connect the injection chamber to the inlet and outlet ports of the instrument. We used two 0.68 m-long tubing in our experiment. |
| Drill with titanium step drillbit | Multiple companies | Use to drill the holes for septum and stopcocks in the jar's metallic lid. | |
| Gay butyl septum (stopper) | Weathon Microliter | 20-0025-B | Use as injection port and as vial septum (if compatible). |
| Headspace vials 20ml (23x75mm), Clear, Crimp Rounded Bottom | Restek | 21162 | Use to store the headspace sample. |
| Heavy Duty Steel Bond Epoxy GorillaWeld | Gorilla | 4330101 | Use to glue stopcock valves and septum to the jar's metallic lid. |
| Hypodermic Needles | Air-Tite Products Co. | N221 | Use to extract water from field vials, inject heaspace sample in vial and inject subsample to the injection chamber. |
| Mason jar (12 oz) | Ball, Kerr, Jarden | Larger or smaller chamber volumes can be chosen depending on sample concentrations. | |
| Optical spectroscopy-based gas analyzer | Multiple companies | Picarro G4301, Licor 7810, Licor 7820, ABB GLA131-GGA | These are some specific examples of analyzers that could be coupled to the injection chamber. We recognize that it is not an extensive list and other optical spectroscopy analyzers may also be suitable for the method. |
| Stopcock valve | DWK Life Sciences | 420163-0001 | Keep the valves open during normal operation. |
| Syringe (2.5 mL) | Air-Tite Products Co. | R2 | Use to extract subsamples from the headspace vials and inject them in the injecion chamber for analysis. |
| Syringe (30 mL) | Air-Tite Products Co. | R30HJ | Use to create headspace for gas analysis. |
Referanslar
- Bastviken, D., Tranvik, L. J., Downing, J. A., Crill, P. M., Enrich-Prast, A. Freshwater methane emissions offset the continental carbon sink. Science. 331 (6013), 50 (2011).
- Quick, A. M., et al. Nitrous oxide from streams and rivers: A review of primary biogeochemical pathways and environmental variables. Earth-Sci Rev. 191, 224-262 (2019).
- Bridgham, S. D., Cadillo-Quiroz, H., Keller, J. K., Zhuang, Q. Methane emissions from wetlands: biogeochemical, microbial, and modeling perspectives from local to global scales. Glob Chang Biol. 19 (5), 1325-1346 (2013).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- McAuliffe, C. Gas chromatographic determination of solutes by multiple phase equilibrium. Chem Technol. 1, 46-51 (1971).
- Hoyos Ossa, D. E., Gallego Rios, S. E., Rodríguez Loaiza, D. C., Peñuela, G. A. Implementation of an analytical method for the simultaneous determination of greenhouse gases in a reservoir using FID/µECD gas chromatography. Int J Environ Anal Chem. 103 (12), 2915-2929 (2023).
- Kittler, F., et al. Long-term drainage reduces CO2 uptake and CH4 emissions in a Siberian permafrost ecosystem. Glob Biogeochem Cycles. 31 (12), 1704-1717 (2017).
- Wilkinson, J., Bors, C., Burgis, F., Lorke, A., Bodmer, P. Measuring CO2 and CH4 with a portable gas analyzer: Closed-loop operation, optimization and assessment. PLoS One. 13 (4), e0193973 (2018).
- Villa, J. A., et al. Ebullition dominates methane fluxes from the water surface across different ecohydrological patches in a temperate freshwater marsh at the end of the growing season. Sci Tot Environ. 767, 144498 (2021).
- Holland, E. A., et al. Soil CO2, N2O and CH4 exchange. Std Soil Meth Long-Term Ecol Res. , 185-201 (1999).
- MacDonald, L. H., Paull, J. S., Jaffé, P. R. Enhanced semipermanent dialysis samplers for long-term environmental monitoring in saturated sediments. Environ Monitor Assess. 185 (5), 3613-3624 (2013).
- Villa, J. A., et al. Plant-mediated methane transport in emergent and floating-leaved species of a temperate freshwater mineral-soil wetland. Limnol Oceanography. 65, 1635-1650 (2020).
- Villa, J. A., et al. Methane and nitrous oxide porewater concentrations and surface fluxes of a regulated river. Sci Tot Environ. 715, 136920 (2020).
- Kampbell, D. H., Wilson, J. T., Vandegrift, S. A. Dissolved oxygen and methane in water by a GC headspace equilibration technique. Int J Environ Anal Chem. 36 (4), 249-257 (1989).
- Rochette, P., Bertrand, N. Soil air sample storage and handling using polypropylene syringes and glass vials. Canadian J Soil Sci. 83 (5), 631-637 (2003).
- Sander, R. Compilation of Henry's law constants (version 4.0) for water as solvent. Atmos Chem Phys. 15 (8), 4399-4981 (2015).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- Comer-Warner, S. A., et al. Seasonal variability of sediment controls of carbon cycling in an agricultural stream. Sci Total Environ. 688, 732-741 (2019).
- U.S. Government Publishing Office. Title 42 - The Public Health and Wefare. U.S. Government Publishing Office. , (2009).
- Magen, C., et al. A simple headspace equilibration method for measuring dissolved methane. Limnol Oceanography Meth. 12 (9), 637-650 (2014).
- Regmi, B. P., Agah, M. Micro gas chromatography: An overview of critical components and their integration. Anal Chem. 90 (22), 13133-13150 (2018).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır