JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
광학 분광학 가스 분석기를 사용한 수생 생태계의 용존 메탄 측정
요약
이 연구는 폐쇄 루프의 주입 챔버에 연결된 휴대용 광학 분석기를 사용하여 수성 샘플의 메탄 가스 농도를 측정하는 방법을 보여줍니다. 그 결과는 기존 기체 크로마토그래피와 유사하며, 특히 원격 현장 연구에 적합한 실용적이고 저렴한 대안을 제시합니다.
초록
생태계의 온실 가스(GHG) 플럭스와 웅덩이를 측정하는 것은 기후 변화와의 관련성으로 인해 생태학 연구에서 점점 더 보편화되고 있습니다. 이와 함께 연구 그룹 내의 다양한 풀과 플럭스를 측정하는 데 적용할 수 있는 분석 플랫폼의 필요성도 커지고 있습니다. 본 연구는 원래 가스 플럭스 측정을 위해 설계 및 시판된 휴대용 광학 분광학 기반 가스 분석기를 사용하여 수성 시료의 GHG 농도를 측정하는 절차를 개발하는 것을 목표로 합니다. 이 프로토콜에는 기존의 헤드스페이스 평형 기법과 헤드스페이스 가스 서브샘플을 주입하는 과정이 포함되며, 그 후 폐쇄 루프를 통해 가스 분석기의 입구 및 출구 포트에 연결된 챔버에 주입합니다. 챔버는 일반 메이슨 항아리와 간단한 실험실 용품으로 제작되었으며 주입 전 희석이 필요할 수 있는 샘플에 이상적인 솔루션입니다. 챔버로 측정된 메탄 농도는 동일한 바이알의 하위 샘플에서 가스 크로마토그래피-화염 이온화 검출(GC-FID)을 통해 별도로 측정된 농도와 밀접한 상관관계(r2 > 0.98)를 갖습니다. 이 절차는 크로마토그래피 장비 및 소모품을 쉽게 구할 수 없는 외딴 지역의 현장 연구와 특히 관련이 있으며, 수생 시스템에서 메탄 및 기타 용존 온실 가스 농도를 측정하기 위한 실용적이고 저렴하며 효율적인 솔루션을 제공합니다.
서문
습지, 호수, 저수지, 강 및 개울과 같은 육지-수생 계면의 생태계는 이산화탄소 (CO2 ), 메탄 (CH4 ) 및 아산화 질소 (N2O)와 같은 온실 가스 (GHG)의 중요한 흡수원이자 공급원입니다 1 , 2 . 특히 CH4 는 퇴적물 공극의 포화 기공 공간에서 혐기성 호흡 중에 생성됩니다. 일단 생성되면 일부는 산화되어 CO2 로 변환되고 나머지는 결국 물기둥과 식물을 통해 확산되거나 거품3 으로 폭발합니다. 주어진 시간에 퇴적물 공극 (즉, 공극수)을 포화시키는 물에서 CH4 의 농도는 CH4 생산, 소비 및 수송4 사이의 균형을 엿볼 수 있습니다. 수직 프로파일 또는 시간에 걸쳐 측정할 때 공극수 농도를 통해 CH4 생산 및 소비에서 더 활발한 구역과 계절적 변화를 식별할 수 있습니다.
전통적으로 생태계의 공극수에서 GHG의 농도를 측정하는 방법은 현장에서 수집된 물 샘플을 처리하여 생성된 상부 공간에서 가스를 평형화하는 것입니다. 그런 다음 가스 크로마토그래피를 통해 헤드스페이스를 분석하여 농도를 결정합니다5. 이 방법은 생태학적 연구에 널리 적용되지만, 기존 실험실 공간을 할당하는 벤치탑 가스 크로마토그래피-화염 이온화 검출(GC-FID) 시스템과 보정 및 작동을 위한 높은 수준의 전문 지식이 필요합니다(예:6). 또한 운반 가스(예: 질소(N2) 및 헬륨(He))이 담긴 대형 탱크와 같은 특수 소모품을 사용해야 하는데, 이는 원격 위치에서 쉽게 구할 수 없습니다. 이러한 요구 사항 및 실험실로의 샘플 운송과 관련된 물류는 샘플링 설계를 제한할 수 있으며, 경우에 따라 크로마토그래피 장비를 사용할 수 없을 때 연구 범위를 제한할 수 있습니다.
이 연구는 휴대용 광학 분광법 기반 가스 분석기를 사용하여 수용액의 헤드스페이스 샘플에서 용존 온실 가스 농도를 측정하는 대체 방법을 개발하는 것을 목표로 했습니다. 이 유형의 광학 가스 분석기는 표준 GC-FID 시스템에 대한 비용 효율적인 대안이며, 휴대성이 뛰어나 현장 작업 Application에 이상적인 선택입니다. 휴대용 광학 분광법 기반 가스 분석기는 브랜드 및 모델에 따라 2 - 5초의 응답 시간으로 고주파 가스 농도 측정(즉, ~ 1 s-1)을 생성합니다. 이러한 기기는 주로 토양, 물 및 식물과 같은 GHG 배출 표면에서 가스 플럭스를 측정하기 위해 설계 및 판매됩니다 7,8,9. 광학 분석기를 사용하면 관심 있는 방출 표면 위에 배치된 비정상 상태 헤드스페이스 챔버에서 연속 농도 측정을 통해 플럭스를 계산할 수 있습니다. 표면 챔버와 함께 정기적으로 사용되는 경우, 챔버에서 관찰된 농도의 변화율과 알려진 챔버 치수, 압력 및 온도의 고주파 측정을 통해 표면적(즉, 표면 플럭스)당 방출(또는 흡수)율에 대한 데이터를 해석할 수 있습니다10. 그러나 휴대용 가스 분석기는 수성 매체의 용존 농도에 맞게 장비되거나 최적화되어 있지 않기 때문에 이러한 유형의 분석을 위해 추가적인 조정과 해석이 필요합니다.
Headspaces8에서 개별 샘플의 농도를 결정하기 위해 광학 분석기를 사용하는 이전 시연을 활용하여 폐쇄 루프에서 분석기에 연결되는 작은 폐쇄형 챔버(즉, 방출 표면 없음)를 설계했습니다. 헤드스페이스 가스 서브 샘플 주입 후 농도 변화와 희석 계산을 통해 원래 헤드스페이스의 농도를 결정할 수 있습니다. 이 접근법의 정밀도는 동일한 샘플에서 GC-FID를 통해 얻은 결과와 결과를 비교하여 평가되었습니다. 이 방법은 루이지애나의 담수 습지의 실험 현장에서 수집한 공수 샘플에서 CH4 의 수직 프로파일을 분석한 사용 사례를 통해 추가로 입증되었습니다.
프로토콜
1. Porewater 샘플링 및 분석
- 공수 투석 샘플러(엿보기)를 사용하여 샘플을 수집합니다.11. 연구 사이트의 해당 위치에 엿보는 사람을 배치합니다. 시범 연구에서, 6 마리의 엿보는 사람은 담수 습지의 두 개의 우세한 식생 패치에 배치되었습니다 : 3 개는 Sagitaria lancifolia 가 우세한 패치에, 다른 3 개는 S. lancifolia 와 Typha latifolia 식생이 공동 우세한 패치에 배치되었습니다.
- 6월, 9월, 10월, 12월에 4번 샘플을 수집합니다. 토양 표면에서 그 아래 ~50cm까지 10가지 깊이에서 샘플을 수집합니다. 샘플링은12,13에 설명된 방법을 따랐습니다.
- 샘플링 전에 61mL의 탈이온수 셀에 채움 ~20일. 실험실에서 N2 로 탈이온수를 5분 동안 거품을 일으켜 현장에서 사용하기 전에 산소를 제거합니다.
- 샘플링하는 동안 세포의 추출 라인에 연결된 주사기를 사용하여 세포에서 25mL의 물을 추출합니다. 그런 다음 2차 세포 충전 라인을 통해 N2 로 미리 기포된 신선한 탈이온수로 셀을 다시 채웁니다. 채취 직후 농도 측정이 필요한 경우 2.1단계를 계속합니다.
- 추출된 물을 0.2mL의 0.1M HCl로 보존된 10mL 유리 바이알에 넣고 격막으로 뚜껑을 씌운 다음 실험실에서 분석할 때까지 냉장 보관합니다.
참고: 이 방법의 사용자는 특정 연구 요구 사항에 따라 수집 깊이, 샘플링 일정 및 빈도를 수정할 수 있습니다.
2. 온실 가스 농도 측정
- 주사기에서 공극수 샘플의 헤드스페이스 평형 수행
- 평형 기법14를 사용하여 헤드스페이스 가스 샘플을 생성합니다. 30mL 주사기를 사용하여 현장에서 수집된 샘플에서 5mL의 물(Vpw)을 추출한 다음 15mL의 N2 (초고순도 99.999%)를 첨가하여 헤드스페이스(V, hs)를 만듭니다.
- 주사기를 5분 동안 강력하고 일관되게 교반하며, 수동으로 또는 흔들리는 셰이커(사용 가능한 경우)를 사용하여 교반합니다. 다음 단계에 따라 광학 분석기를 사용한 가스 농도 측정에 사용되는 10mL 사전 진공 바이알에 12mL의 헤드스페이스 가스 서브샘플을 주입합니다(그림 1). 연동 펌프15 로 바이알을 비우거나 밀폐된 바이알에 있는 60mL 주사기의 플런저를 수동으로 당겨 공기를 3번 펌핑합니다.
참고: N2 대신 He를 사용하여 헤드스페이스를 만들 수 있습니다. 주사기에N2 또는 He를 추가하는 절차는 사용자가 사용할 수 있는 실제 탱크의 특정 적응 또는 조절기에 따라 다릅니다. 이 추가에는 일반적으로 일치하는 튜브를 사용하여 주사기를 탱크에 결합하거나 탱크에 맞게 조정된 샘플링 포트에서 주사기와 추출하는 작업이 포함됩니다. 현장 조건 및 관련 물류에 따라 사용자는 주변 공기를 사용하여 헤드 스페이스를 만들 수 있습니다.
- 주입실 만들기
- 가스 분석기 유입 및 유출에 연결되어 폐쇄 루프를 형성하는 밀폐된 부피의 공기에 소량의 공기(~1 - 5 mL)를 수용할 수 있는 주입 챔버를 제조합니다(재료 표). 주입 챔버와 분석기는 시스템의 두 가지 주요 요소입니다(그림 2).
- 11mm 직경의 구멍 1개를 뚫어 1개의 격막을 주입 포트로 맞게, 7mm 직경의 구멍 2개를 뚫어 분석기와 연결되는 스톱콕 밸브를 삽입하여 365mL 메이슨 용기의 금속 뚜껑을 수정합니다. 에폭시 접착제를 사용하여 주입 포트와 피팅을 조이고 챔버 밀봉을 확인합니다.
- 주입 챔버를 광학 분석기에 연결합니다.
- 5/32인치 내경(I.D.) 및 1/4인치 외경(O.D.)을 사용하여 jar를 광학 분석기의 입구 및 출구 포트에 연결합니다. PFA 플라스틱 튜브 및 추가 부피를 설명합니다. 튜브가 기기 제조업체의 권장 사항을 따르고 결로 없이 깨끗하고 건조한지 확인하십시오.
- 주입 챔버를 기기에 연결하는 밸브를 열어 폐쇄 루프 공기 회로를 생성하도록 설정합니다. 가스 농도가 안정될 때까지 기다립니다.
- 챔버에 시료 주입
- 챔버의 농도와 분석기의 신호가 안정화되면(즉, 표준 편차 <0.03ppm) 2.1.2단계에서 생성된 헤드스페이스 샘플이 들어 있는 바이알에서 2mL의 하위 샘플을 주입합니다. 다음 하위 샘플을 주입하기 전에 분석기의 농도가 다시 안정화될 때까지 기다립니다(그림 3).
- 농도가 100ppm에 가까워지면 최대 20개의 하위 시료를 연속적으로 또는 그 이하로 주입합니다(이 임계값을 초과하는 정확도에 미치는 영향은8개 참조). 5개 샘플마다 CH4 check 표준물질을 분석하고 상대 표준 편차(RSD)를 사용하여 실제 측정값과의 차이를 평가합니다.
- 적층형 주입 세트를 사용하면 기기에 연결된 라인 중 하나를 분리하여 챔버를 주변 압력으로 재설정하고 상당한 압력 및 메탄 농도 축적을 방지합니다.
참고: 여러 번의 테스트 실행을 기반으로 주입 후 신호가 ~15초 후에 안정화된 것으로 확인되었지만 다른 기기 기록 사양에 따라 다른 시간이 필요할 수 있습니다(그림 3). 사용된 기기의 유속은 ~1L/min이었고 응답 시간은 5초였으며 720에서 745Torr 범위의 다른 날에 다른 분석을 수행하는 동안 캐비티 압력이 있었습니다.
- 헤드스페이스의 CH4 농도 계산
- 각 하위 샘플에 대해 방정식 1을 사용하여 헤드스페이스(Chs - μmol/mol)에서 목표 GHG(예: CH4, CO2, N2O)의 농도를 계산합니다.
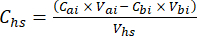 방정식 [1]
방정식 [1]
여기서 Vhs 는 헤드스페이스 하위 샘플의 부피입니다. - 주입 전 (C, bi - μmol mol-1) 및 (C, ai - μmol mol-1) 주입 전 15회 측정의 평균으로 농도를 계산합니다. 방정식 2와 3을 사용하여 주입 전(V,bi) 및 주입 후(V,ai) 부피를 mL 단위로 계산합니다.
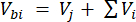 [2]
[2]
그리고
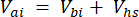 [3]
[3]
여기서, Vj(mL)는 jar(365 mL) 및 hosing(125.4 mL)의 첨가 부피이고, Vi(mL)는 주입된 subsamples의 누적 부피이다.
- 각 하위 샘플에 대해 방정식 1을 사용하여 헤드스페이스(Chs - μmol/mol)에서 목표 GHG(예: CH4, CO2, N2O)의 농도를 계산합니다.
- 공극수 농도 계산
- 방정식 4를 사용하여 시료 처리 중 헤드스페이스 내 가스의 몰 분율과 대기압(P)을 사용하여 헤드스페이스에서 CO2, CH4 또는 N2O의 분압(Pi - MPa)을 계산합니다.
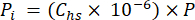 [4]
[4] - 헤드스페이스와 수성 등가 농도 및 부피가 있는 희석 방정식(방정식 5)을 사용하여 공극수 내 GHG의 수성 등가 농도를 계산합니다.
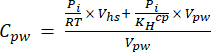 [5]
[5]
여기서 R은 범용 기체 상수(0.008314 L MPa mol-1 K-1)이고, 는 공기 온도(K), V hs는 헤드스페이스의 부피(mL), K Hcp는 CO2, CH4 또는 N2O(각각 2.96, 67.13 및 3.82 L MPa/mol)16의 헨리 휘발성 상수이며, Vpw는 헤드 스페이스를 생성하는 데 사용되는 액체 서브 샘플의 부피(mL)입니다. - 측정하는 동안 기록된 T와 P를 사용합니다. 시연 프로젝트 샘플 분석 중 평균 T와 P는 각각 295.15K와 0.101325MPa였습니다.
- 방정식 4를 사용하여 시료 처리 중 헤드스페이스 내 가스의 몰 분율과 대기압(P)을 사용하여 헤드스페이스에서 CO2, CH4 또는 N2O의 분압(Pi - MPa)을 계산합니다.
3. 표준 크로마토그래피 측정에 대한 검증
- 기존 가스 크로마토그래프에서 10mL 바이알의 다양한 알려진 CH4 농도를 분석합니다. 각각 20개의 표준으로 구성된 세 개의 동일한 그룹을 사용합니다. 최저 농도는 5에서 100ppm 사이였으며 5ppm 단위로 증가했습니다.
- 가스 크로마토그래프에서 화염 이온화 검출을 통해 CH4 농도를 측정합니다. 크로마토그래프는 He(25mL/분)를 캐리어 가스로 하는 다공성 폴리머 흡수성 충전 컬럼을 사용했습니다. 표준물질의 농도 측정을 실행하려면 크로마토그래프를 곡선 피팅(r2) > 0.99로 보정합니다.
- 크로마토그래피 후, 제조업체가 보정한 광학 분석기를 사용하여 위에서 설명한 방법을 사용하여 동일한 표준 바이알에서 CH4 농도를 측정하십시오(즉, 정밀도(300 s, 1σ): 0.3 ppb CH4).
- 3개의 표준 그룹의 크로마토그래피 및 광학 분석기 결과에 선형 회귀를 피팅하여 방법의 정확도를 평가합니다. 각 표준 그룹 내에서 수행된 회귀 분석의 기울기와 절편을 비교하여 방법의 재현성을 평가합니다. 효과 레버리지에 중점을 둔 표준 최소 제곱 모형을 사용하여 비교를 평가합니다. 모든 회귀 분석 및 비교를 0.05의 유의 수준에서 평가합니다.
결과
광학 분석기와 기체 크로마토그래피 비교
세 가지 표준 그룹에 대한 가스 크로마토그래피와 광학 분석기를 통해 얻은 결과는 1에 가까운 기울기에서 우수한 선형 맞춤( 즉, r2 > 0.98)을 보여주었습니다(그림 4). 세 가지 실험에서 회귀의 기울기는 통계적으로 유사하여(F(2) = 0.478, p = 0.623) 결과의 재현성을 시사합니다. 세 ?...
토론
이 연구는 물 샘플에서 생성된 헤드 스페이스를 분석하기 위해 맞춤형 주입 챔버에 결합된 휴대용 광학 분광학 기반 가스 분석기의 적용 가능성을 보여주었습니다. 시연은 CH4에 초점을 맞췄지만, 이 프로토콜은 CO2 및 N2O8과 같은 다른 관련 GHG를 분석하는 데 적용될 수 있습니다. 목표는 GHG 농도 측정 연구에서 기존 가스 크로마토...
공개
저자는 이해 상충이 없음을 선언합니다.
감사의 말
이 작업은 DOE 상인 DE-SC0021067, DE-SC0023084 및 DE-SC0022972를 통해 자금을 지원받았습니다. 습지에서 샘플링된 사이트의 공극수 농도 데이터는 ESS-DIVE Data Archive(https://data.ess-dive.lbl.gov/view/doi:10.15485/1997524, 2024년 6월 21일 액세스)에서 공개적으로 사용할 수 있습니다.
자료
| Name | Company | Catalog Number | Comments |
| 1/4 in. I.D. x 3/8 in. O.D. Clear Vinyl Tubing | Home Depot | SKU # 702098 | Use to couple stopcocks and tubing connected to the instrument. Two short pieces (~4 cm). |
| 5/16 - 5/8 in. Stainless Steel Hose Clamp | Everbilt | 6260294 | Use to secure tubing connecting the stopcock valves and tubing connected to the instrument. |
| Crack-Resistant Teflon PFA Semi-Clear Tube for chemicals, 5/32" ID, 1/4" OD | McMaster-Carr | 51805K86 | Use to connect the injection chamber to the inlet and outlet ports of the instrument. We used two 0.68 m-long tubing in our experiment. |
| Drill with titanium step drillbit | Multiple companies | Use to drill the holes for septum and stopcocks in the jar's metallic lid. | |
| Gay butyl septum (stopper) | Weathon Microliter | 20-0025-B | Use as injection port and as vial septum (if compatible). |
| Headspace vials 20ml (23x75mm), Clear, Crimp Rounded Bottom | Restek | 21162 | Use to store the headspace sample. |
| Heavy Duty Steel Bond Epoxy GorillaWeld | Gorilla | 4330101 | Use to glue stopcock valves and septum to the jar's metallic lid. |
| Hypodermic Needles | Air-Tite Products Co. | N221 | Use to extract water from field vials, inject heaspace sample in vial and inject subsample to the injection chamber. |
| Mason jar (12 oz) | Ball, Kerr, Jarden | Larger or smaller chamber volumes can be chosen depending on sample concentrations. | |
| Optical spectroscopy-based gas analyzer | Multiple companies | Picarro G4301, Licor 7810, Licor 7820, ABB GLA131-GGA | These are some specific examples of analyzers that could be coupled to the injection chamber. We recognize that it is not an extensive list and other optical spectroscopy analyzers may also be suitable for the method. |
| Stopcock valve | DWK Life Sciences | 420163-0001 | Keep the valves open during normal operation. |
| Syringe (2.5 mL) | Air-Tite Products Co. | R2 | Use to extract subsamples from the headspace vials and inject them in the injecion chamber for analysis. |
| Syringe (30 mL) | Air-Tite Products Co. | R30HJ | Use to create headspace for gas analysis. |
참고문헌
- Bastviken, D., Tranvik, L. J., Downing, J. A., Crill, P. M., Enrich-Prast, A. Freshwater methane emissions offset the continental carbon sink. Science. 331 (6013), 50 (2011).
- Quick, A. M., et al. Nitrous oxide from streams and rivers: A review of primary biogeochemical pathways and environmental variables. Earth-Sci Rev. 191, 224-262 (2019).
- Bridgham, S. D., Cadillo-Quiroz, H., Keller, J. K., Zhuang, Q. Methane emissions from wetlands: biogeochemical, microbial, and modeling perspectives from local to global scales. Glob Chang Biol. 19 (5), 1325-1346 (2013).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- McAuliffe, C. Gas chromatographic determination of solutes by multiple phase equilibrium. Chem Technol. 1, 46-51 (1971).
- Hoyos Ossa, D. E., Gallego Rios, S. E., Rodríguez Loaiza, D. C., Peñuela, G. A. Implementation of an analytical method for the simultaneous determination of greenhouse gases in a reservoir using FID/µECD gas chromatography. Int J Environ Anal Chem. 103 (12), 2915-2929 (2023).
- Kittler, F., et al. Long-term drainage reduces CO2 uptake and CH4 emissions in a Siberian permafrost ecosystem. Glob Biogeochem Cycles. 31 (12), 1704-1717 (2017).
- Wilkinson, J., Bors, C., Burgis, F., Lorke, A., Bodmer, P. Measuring CO2 and CH4 with a portable gas analyzer: Closed-loop operation, optimization and assessment. PLoS One. 13 (4), e0193973 (2018).
- Villa, J. A., et al. Ebullition dominates methane fluxes from the water surface across different ecohydrological patches in a temperate freshwater marsh at the end of the growing season. Sci Tot Environ. 767, 144498 (2021).
- Holland, E. A., et al. Soil CO2, N2O and CH4 exchange. Std Soil Meth Long-Term Ecol Res. , 185-201 (1999).
- MacDonald, L. H., Paull, J. S., Jaffé, P. R. Enhanced semipermanent dialysis samplers for long-term environmental monitoring in saturated sediments. Environ Monitor Assess. 185 (5), 3613-3624 (2013).
- Villa, J. A., et al. Plant-mediated methane transport in emergent and floating-leaved species of a temperate freshwater mineral-soil wetland. Limnol Oceanography. 65, 1635-1650 (2020).
- Villa, J. A., et al. Methane and nitrous oxide porewater concentrations and surface fluxes of a regulated river. Sci Tot Environ. 715, 136920 (2020).
- Kampbell, D. H., Wilson, J. T., Vandegrift, S. A. Dissolved oxygen and methane in water by a GC headspace equilibration technique. Int J Environ Anal Chem. 36 (4), 249-257 (1989).
- Rochette, P., Bertrand, N. Soil air sample storage and handling using polypropylene syringes and glass vials. Canadian J Soil Sci. 83 (5), 631-637 (2003).
- Sander, R. Compilation of Henry's law constants (version 4.0) for water as solvent. Atmos Chem Phys. 15 (8), 4399-4981 (2015).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- Comer-Warner, S. A., et al. Seasonal variability of sediment controls of carbon cycling in an agricultural stream. Sci Total Environ. 688, 732-741 (2019).
- U.S. Government Publishing Office. Title 42 - The Public Health and Wefare. U.S. Government Publishing Office. , (2009).
- Magen, C., et al. A simple headspace equilibration method for measuring dissolved methane. Limnol Oceanography Meth. 12 (9), 637-650 (2014).
- Regmi, B. P., Agah, M. Micro gas chromatography: An overview of critical components and their integration. Anal Chem. 90 (22), 13133-13150 (2018).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유