JoVE 비디오를 활용하시려면 도서관을 통한 기관 구독이 필요합니다. 전체 비디오를 보시려면 로그인하거나 무료 트라이얼을 시작하세요.
Method Article
손목과 원위 요골 관절을 연구하기 위한 양평면 비디오 방사선 촬영
요약
이평면 비디오방사선 촬영(BVR)은 골격계와 임플란트의 3차원 움직임을 이해하기 위한 고급 이미징 기술입니다. BVR은 밀도 기반 이미지 볼륨과 원위 상지의 비디오 방사선 사진을 결합하여 손목 및 원위 요골 관절의 생체 내 움직임과 관절 치환술을 연구하는 데 사용됩니다.
초록
생체 내에서 골격 운동학의 정확한 측정은 정상적인 관절 기능, 병리학의 영향, 질병 진행 및 치료 효과를 이해하는 데 필수적입니다. 골격 움직임을 추론하기 위해 피부 표면 마커를 사용하는 측정 시스템은 정상 및 병리학적 운동학에 대한 중요한 통찰력을 제공했지만, 특히 동적 활동 중에는 이러한 시스템을 사용하여 정확한 관절운동학을 얻을 수 없습니다. 지난 20년 동안 이평면 비디오방사선 촬영(BVR) 시스템을 통해 많은 연구자들이 일상 생활 활동 중 관절의 골격 운동학을 직접 연구할 수 있게 되었습니다. 원위 상지에 대한 BVR 시스템을 구현하기 위해 피험자가 지정된 작업을 수행하는 동안 두 개의 보정된 X선 소스에서 원위 반경과 손의 비디오 방사선 사진을 획득합니다. 3차원(3D) 강체 위치는 각 BVR 뷰에 대한 3D 모델 투영의 최적 등록을 통해 비디오 방사선 사진에서 계산됩니다. 3D 모델은 독립적으로 획득한 컴퓨팅 단층 촬영 데이터에서 파생된 특정 뼈의 밀도 기반 이미지 볼륨입니다. 그래픽 프로세서 장치와 고성능 컴퓨팅 시스템을 활용하는 이 모델 기반 추적 접근 방식은 손목 및 원위 요골 관절 생체 역학을 빠르고 정확하게 평가하는 것으로 나타났습니다. 본 연구에서는 먼저 손목 및 원위 요골 관절 운동학을 평가할 때 BVR과 체외 광학 모션 캡처 시스템의 서브밀리미터 및 서브도 일치를 확립한 이전 연구를 요약했습니다. 또한 BVR을 사용하여 손목 관절의 회전 중심 거동을 계산하고, 임플란트 구성 요소의 관절 패턴을 평가하고, 팔뚝 돌출 중 척골 변화의 동적 변화를 평가했습니다. 미래에는 평판 X선 검출기, 더 많은 X선 소스(즉, 다평면 비디오 방사선 촬영) 또는 고급 컴퓨터 비전 알고리즘이 추가되어 손목 뼈를 더 자세히 캡처할 수 있습니다.
서문
in vivo에서 골격 운동학의 정확한 측정은 건강하고 대체된 관절 기능, 병리학의 영향, 질병 진행 및 치료 효과를 이해하는 데 필수적입니다. 관절 표면에서 비침습적으로 골격 운동학을 정량화하는 것(관절 운동학)은 관절 병리학 및 골관절염과 같은 질병을 이해하는 데 중요하지만 기술적으로는 어렵습니다. 이전에는 피부 표면 마커를 사용하여 골격 움직임을 추론하는 기술이 건강하고 병리적인 운동학에 대한 중요한 통찰력을 제공했습니다. 그러나 이러한 기술을 사용하여 정확한 관절 운동학을 얻을 수 없으며, 특히 일상 생활 활동과 같은 역동적인 활동 중에는 더욱 그렇습니다. 이러한 광학 시스템은 인간의 움직임 분석에서 오류의 주요 원인인 기본 뼈에 대한 상대적인 피부 움직임으로 인해 본질적으로 정확도가 제한됩니다 1,2.
3차원(3D) 골격 운동학을 정량화하기 위한 현재 최첨단 방법은 이미지 기반 추적, 즉 복엽면 비디오방사선 촬영(BVR)3 및 직렬 컴퓨터 단층 촬영(CT) 볼륨4 및 자기 공명 영상(MRI)5입니다. 일반 3D CT 및 MRI 기반 기술은 매우 정확하고 전 세계 많은 병원에서 액세스할 수 있지만 관절의 동적 움직임을 측정할 수는 없습니다. 이러한 단점을 해결하기 위해 최근 몇 년 동안 4DCT 스캐닝6 및 동적 MRI7 과 같은 이미징 기술이 개발되었습니다. 그러나 이러한 방법은 환자를 높은 방사선 선량에 노출시키거나 낮은 시간 해상도로 인해 어려움을 겪습니다.
새로운 컴퓨터 비전 알고리즘과 기존 X-ray 시스템을 결합한 BVR은 동물과 인간의 여러 관절에 대해 정확한 것으로 나타났습니다. 마커 기반 또는 모델 기반 추적 알고리즘으로 해결됩니다. 마커 기반 접근법은 뼈 또는 연조직에 삽입된 탄탈륨 비드를 추적하며 동물 및 체외 테스트에 최적입니다. 그러나 그들은 생체 내 인간 연구를 위해 엄청나게 침습적입니다. 다행히도 모델 기반 추적 알고리즘의 개선으로 실행 가능한 대안이 제공됩니다. 인간을 대상으로 한 모델 기반 BVR 추적 접근 방식에는 정적인 자세에서 CT 또는 MRI로 획득한 체적 이미지 세트를 준비하고 두 X선의 시야에서 관심 있는 움직임을 캡처하는 것이 포함됩니다. 그런 다음 대부분의 모델 기반 추적 애플리케이션은 정적 CT 또는 MR 이미지로부터 뼈 또는 임플란트의 디지털 재구성 방사선 사진(DRR)을 생성하고, DRR과 비디오 방사선 사진 간의 유사성을 입증하는 메트릭을 사용하여 기능이 향상된 비디오 방사선 사진과 일치시킵니다8. 이 과정을 뼈 또는 임플란트의 "추적"이라고 합니다.
뼈 또는 임플란트 추적의 주요 출력 변수는 관절 운동학, 인대 연신율 9,10, 연골 두께에 대한 대리물로서의 관절 간격11, 관절 접촉12,13 및 기타 바이오마커를 계산할 수 있는 강체 운동학입니다. 최근에는 손목의 생체 역학, 손목 관절 전치환술(TWA) 및 원위 요골 관절(DRUJ)을 계산하는 데 있어 모델 기반 추적 BVR의 정확성을 문서화했습니다14,15. 다음 섹션에서는 다양한 작업 중 골격 손목, 손목 관절 전치환술 및 원위 요골 관절의 움직임을 연구하기 위한 이 검증된 방법의 자세한 프로토콜이 제시됩니다. CT 이미지 볼륨에서 뼈와 임플란트의 밀도 기반 이미지 볼륨을 분할하고, 비디오 방사선 사진 내에서 이러한 부분 이미지 볼륨을 추적하고, 회전 중심, 접촉 패턴 및 척골 분산과 같은 결과를 결정하여 이 방법의 강점과 한계를 입증합니다.
프로토콜
이 연구는 AAHRPP 인증 IRB인 Lifespan - Rhode Island Hospital의 IRB(Institutional Review Board)의 승인을 받았습니다. 총 16명의 환자가 기관 지침에 따라 서명된 정보에 입각한 동의서를 제공했습니다.
1. 데이터 수집
- 컴퓨터 단층 촬영(CT)
- CT를 위한 표본 또는 피험자를 준비합니다.
참고: 정확도 평가14,15를 위해 4개의 온전한 시체 표본(70.5 ± 12.3세, 권리 4명, 여성 2명)의 온전한 팔뚝 6개와 손목 관절 전치환술이 있는 팔뚝 1개(49세, 오른쪽, 여성)가 사용되었습니다. in vivo 연구16을 위해 손목 관절 전치환술을 받은 건강한 손목 환자 10명(57.0 ± 5.2세, 여성 8명, 우측 우세 9명)과 손목 전치환술을 받은 환자 6명(74.7± 5.6세, 여성 2명, 우측 손목 2명, 우측 손목 4명)이 등록되었다. - 각 피험자4를 이미지화하기 위해 데이터 수집 직경이 25cm인 원위 팔뚝의 CT 스캔을 획득하고 16슬라이스 임상 CT 스캐너를 사용하여 Bone Plus 컨볼루션 알고리즘을 사용하여 20cm 시야각으로 재구성합니다. 80kVp 및 80mA의 튜브 설정을 사용합니다. 팔뚝 노출을 원위 요골 표면에서 원위 지골까지 약 7cm 근위부로 제한합니다.
참고: 이 연구에서 이미지의 복셀 치수는 팔뚝의 횡단면에서 0.39 × 0.39 mm2 , 팔뚝의 긴 축을 따라 0.625 mm였습니다. - 획득한 CT 이미지를 DICOM(Digital Imaging and Communications in Medicine) 형식의 HIPPA 승인 프로토콜을 사용하여 실험실의 컴퓨터로 전송합니다.
- CT를 위한 표본 또는 피험자를 준비합니다.
- 이평면 비디오방사선 촬영(BVR)
- 실험 설정 (그림 1). 다양한 손목 자세에서 뼈 폐색을 최소화할 수 있는 원근감뿐만 아니라 원위 요골, 원위 척골 및 중수골을 캡처할 수 있는 시야 직경을 가능하게 하려면 팔뚝 아래에 이미지 증폭기(II)를 배치하고 그 사이의 각도를 110°로 설정합니다(X선 소스는 지면을 기준으로 55° 방향에서 해당 II를 향해 아래쪽을 향함).
- 뼈/임플란트의 가시성에 따라 65-75kV 사이의 노출 설정과 80mA로 연속 모드에서 X-ray를 생성합니다. 두 X-Ray-II 쌍의 소스-이미지 거리를 약 130cm로 조정하고 소스-핸드 거리를 90cm로 조정합니다.
참고: 이 연구에서 피험자들은 실험실에서 X선 보호 납 앞치마, 갑상선 칼라 보호대 목 덮개 및 디지털 선량계를 착용했습니다. 실험이 진행되는 동안 모든 연구원들은 납 차폐 유리 뒤에 서 있었습니다. - II 사이에 가대나 유사한 구조를 배치하고 피험자를 위한 항목(예: 문 손잡이, 망치, 주전자)을 배치하는 데 사용합니다.
- 뼈/임플란트의 가시성에 따라 65-75kV 사이의 노출 설정과 80mA로 연속 모드에서 X-ray를 생성합니다. 두 X-Ray-II 쌍의 소스-이미지 거리를 약 130cm로 조정하고 소스-핸드 거리를 90cm로 조정합니다.
- 실험 설정 (그림 1). 다양한 손목 자세에서 뼈 폐색을 최소화할 수 있는 원근감뿐만 아니라 원위 요골, 원위 척골 및 중수골을 캡처할 수 있는 시야 직경을 가능하게 하려면 팔뚝 아래에 이미지 증폭기(II)를 배치하고 그 사이의 각도를 110°로 설정합니다(X선 소스는 지면을 기준으로 55° 방향에서 해당 II를 향해 아래쪽을 향함).
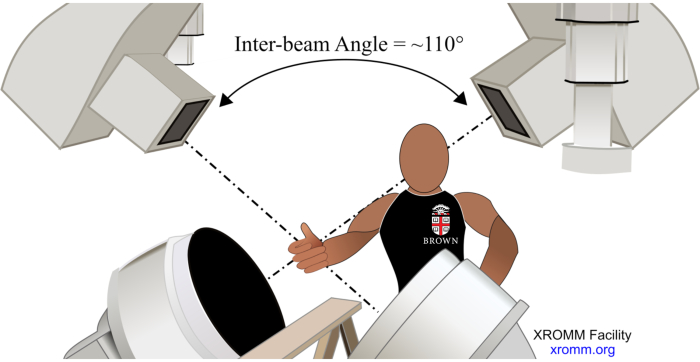
그림 1. 실험적 설정. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
- 왜곡 방지 그리드(그림 2A). 외부 전자기장이 X선 빔(즉, 전자 경로)의 동작에 영향을 미치기 때문에 방사선 이미지는 비선형 핀쿠션 및 S자형 왜곡17으로 어려움을 겪습니다. 이러한 왜곡을 제거하려면 정밀 천공 판금(즉, 왜곡되지 않은 그리드)의 평평한 조각 이미지를 사용하십시오18,19. II에 왜곡되지 않은 그리드를 배치하고 비디오 방사선 촬영 데이터 전후의 이미지를 캡처합니다. 이러한 이미지를 두 X선 소스에 대해 8비트 TIFF 이미지로 저장합니다.
- 보정 (그림 2B). X선 소스의 보정은 물체(뼈 또는 임플란트)의 3D 좌표를 계산하는 데 필요합니다(20). 일정한 간격의 무선 불투명 구가 있는 알려진 형상을 가진 3D 개체의 이미지를 사용하여 3D 공간에서 X선 소스의 위치 및 방향과 이미지 공간(즉, 방사선 사진) 간의 관계를 생성합니다. 강철 구가 있는 아크릴 시트와 스페이서로 만든 입방체 물체(즉, 캘리브레이션 큐브)는 BVR 설정에 효과적이고 정확합니다19.
- 실험 수행 전 4회, 실험 후 4회 다양한 방향으로 캘리브레이션 큐브18 의 방사선 사진을 캡처합니다. 실험 후 보정은 실험 설정이 실험 전반에 걸쳐 변경되지 않은 상태로 유지되는지 확인하는 역할을 합니다. 두 X선 소스에 대해 모든 이미지를 8비트 TIFF 이미지로 저장합니다.
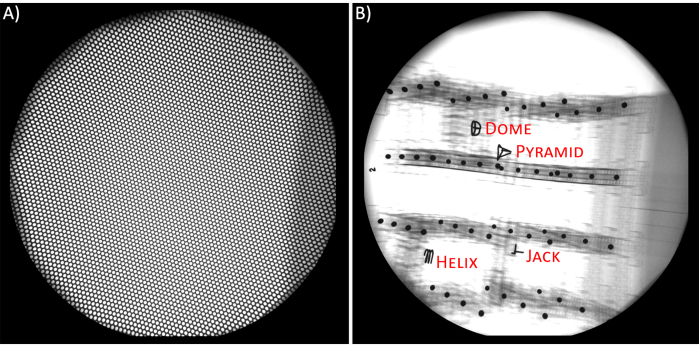
그림 2. A) 왜곡 방지 그리드. B) 캘리브레이션 큐브 및 참조 항목. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
- 작업 설명. 굴곡-신전, 요골-척골 이탈 및 외주 중 손목 움직임을 캡처하기 위한 다양한 작업을 정의합니다16. DRUJ 모션 작업을 팔뚝 회전, 유지 자세에서 전체 내전으로의 회전 또는 T 핸들 문 손잡이를 시계 방향 및 시계 반대 방향으로 회전하는 것으로 정의되는 완전 외전으로의 회전으로 설명21. 중립 자세(즉, 중립 정적 작업)에서 손목의 비디오 방사선 사진을 획득합니다. 팔뚝 뒤쪽과 같은 평면상의 손등으로 중립적인 포즈를 포착합니다.
참고: 모든 작업의 시작 자세에서 어깨는 내전을 하고 팔꿈치는 관절 수준에서 지지되며 팔뚝은 구속되지 않고 중립 회전을 합니다. 굴곡-신전(flexion-extension)과 요골-척골 편향(radical-ulnar deviation)의 과제는 각각 손의 볼라-등쪽(volar-dorsal sides)과 요골-척골(radial -ulnar) 측면에 대한 손바닥의 회전으로 설명되었습니다. 외곡은 모든 방향에서 최대한의 활성 운동 범위를 달성하는 것을 목표로 하는 손목 동작으로 설명되었습니다. - 비디오 방사선 사진 획득. 카메라 셔터 속도를 500μs로 설정하고 200Hz의 속도로 비디오 방사선 사진을 획득합니다. 각 작업에 대해 2초 분량의 이미징을 기록하여 2회 반복을 얻습니다. 각 X-ray 소스에서 획득한 비디오 방사선 사진을 8비트 형식의 CINE 비디오로 저장합니다.
참고: 이 연구에서 방사선 사진은 이미지 크기가 1760×1760픽셀이었고 픽셀당 약 0.22mm×0.22mm의 해상도를 가졌습니다.
참고: 현재 X선 소스에는 시야(FOV)를 확대할 수 있는 옵션이 있습니다. 그러나 본 연구에서는 하드웨어가 제공하는 확대 모드를 사용하지 않았다. 작업 설명에 따라 이 기능을 사용하면 더 높은 해상도의 출력을 얻을 수 있습니다. 이 기능을 사용하는 경우 이 모드에서 왜곡 그리드 및 보정 단계를 캡처해야 합니다.
- 광학 모션 캡처(OMC) - 정확도 연구
- 이전 연구14,15에서 설명한 광학 모션 캡처(OMC) 데이터 수집 프로토콜을 사용합니다. 각각 9.5mm 직경의 역반사 마커 구체 4개가 있는 2개의 마커 클러스터를 세 번째 중수골 및 반경 뼈에 직접 부착합니다. 8개의 광학 모션 캡처 카메라를 사용하여 마커의 움직임을 캡처합니다. 활성 로우 외부 트리거에 의해 OMC 데이터 수집의 시작을 BVR과 동기화합니다.
2. 데이터 처리
- 컴퓨터 단층 촬영(CT)
- DICOM 익명화. DICOM을 익명화하고 3D 모델링을 위한 이미지 처리 소프트웨어(예: Mimics Materialise)로 가져옵니다. Mimics Materialise 소프트웨어의 파일 도구 모음에서 Anonymize 창을 엽니다. 새 창이 열리면 왼쪽 탭에서 모든 이미지 익명화를 선택하고 오른쪽 하단의 익명화 버튼을 누릅니다.
- 세분화(그림 3). 앞서 설명한 방법론 16,22,23에 따라 관심 있는 뼈 또는 임플란트를 분할합니다.
- 간단히 말해서 세그먼트(Segment) 툴바에서 임계값(Threshold ) 옵션을 선택하고 창이 열릴 때 본(Bone )에 대해 미리 정의된 임계값 세트를 선택합니다. 임계값이 있는 마스크를 만든 후 Split Mask 옵션을 사용하고 뼈 또는 임플란트의 구성 요소의 영역을 수동으로 페인팅합니다.
- 모든 영역에 색상이 지정되면 확인을 클릭하고 소프트웨어가 각 뼈와 임플란트 구성 요소에 대한 마스크를 자동으로 생성할 때까지 기다립니다. 모든 마스크가 의도한 영역을 완전히 덮고 있는지 확인하십시오. 그렇지 않은 경우 Edit Masks 옵션을 사용하여 영역을 수동으로 하나씩 수정합니다.
참고: 손목 관절을 연구하려면 2번째 및 3번째 중수골과 요골을 분할하여 나머지 뼈와 분리해야 합니다. 선택적으로, capitate 및 다른 뼈는 후처리 단계를 위해 세그먼트화할 수 있습니다.
참고: DRUJ를 연구하려면 요골과 척골을 분할하여 나머지 뼈와 분리해야 합니다.
참고: 임플란트의 경우 방사형 구성 요소와 나사가 있는 수근 구성 요소를 분할해야 합니다.
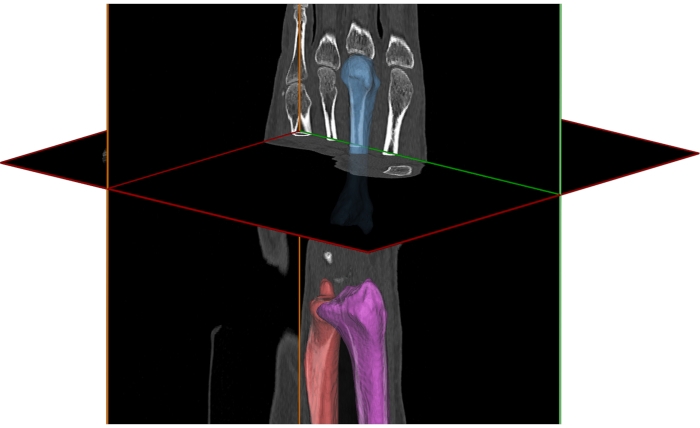
그림 3. 손목의 컴퓨터 단층 촬영 이미지와 요골, 제3 중수골 및 척골의 재구성 모델. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
- Segmentation - 방사형 구성 요소만 해당됩니다. CT 이미지에서 방사형 구성 요소 표면의 밀도 기반 줄무늬 아티팩트로 인해 방사형 구성 요소 모델을 이미지에서 분할할 수 없습니다. 따라서 CAD 모델 또는 3D 표면 스캐너를 사용하여 이식된 방사형 구성 요소의 3D 모델을 생성합니다. Mimics Materialise default의 방법을 사용하여 이 모델을 방사형 구성 요소의 대략적인 분할에 등록합니다.
참고: 이 연구에서는 해상도가 0.1mm인 표면 스캐너를 사용했습니다. 임플란트를 테이블 위에 놓고 3D 스캐너를 임플란트 주위로 수동으로 움직여 모든 외부 표면을 캡처했습니다. - 부분 이미지 볼륨. 추적 소프트웨어는 세그먼트화된 관심 물체가 밀도 기반 이미지 볼륨으로 입력되어야 합니다. 이 부분 볼륨을 만들려면 세그먼트 도구 모음에서 Threshold 옵션을 선택하여 모든 회색 값을 포함하는 이미지 볼륨의 전체 마스크를 생성합니다. 임계값을 최소값에서 최대 회색 값으로 조정합니다.
- 그런 다음 Boolean Operators 옵션을 사용하고 생성된 전체 마스크에서 관심 있는 뼈 또는 임플란트의 세그먼트화된 볼륨을 뺍니다 . 이 부분 볼륨의 마스크 색상을 검은색(RGB: 0.0/0.0/0.0)으로 변경하면 등록 소프트웨어는 회색 음영 이미지 볼륨만 허용하기 때문입니다. Export DICOM을 선택하여 마스크를 DICOM으로 내보냅니다. 소프트웨어에서. 출력은 분리된 뼈 또는 임플란트의 이미지 볼륨입니다.
- 3차원 모델. 최적 해상도(Optimal Resolution)와 함께 3D 계산(Calculate 3D) 옵션을 선택하여 세그먼트화된 마스크를 삼각형 메쉬 3D 표면 모델로 변환합니다. 이러한 모델을 정점(점)의 3D 위치와 연결 순서를 포함하는 VRML 형식으로 내보냅니다. 모델은 좌표계 구성 및 추가 시각화를 위해 생성됩니다.
- 비디오 방사선 촬영 전처리
- XMALab18 가져오기. 각 피험자에 대해 XMALab 소프트웨어에서 새 임상시험을 생성합니다. 폴더 경로를 Undistortion Grid 이미지에 할당하고 New Trial 대화 상자에서 8개의 보정 이미지 세트를 할당합니다.
참고: 캡처 내내 X선 소스가 뒤집히는 경우 XMALab 소프트웨어에서 뒤집기 옵션을 확인해야 합니다. - 왜곡 제거. 방사선 사진의 왜곡을 제거하려면 시험판을 만들고 소프트웨어가 Undistortion 작업 공간에서 그리드 이미지를 연 후 Compute Undistortion 버튼을 클릭합니다. XMALab은 그리드의 왜곡되지 않은 이미지를 자동으로 결정하고 표시합니다. 소프트웨어가 모든 구멍의 중심을 감지하면 왼쪽 상단 메뉴의 작업 공간을 보정 작업 공간으로 변경합니다. 자세한 내용 및 잠재적 문제 디버깅에 대한 지원은 참조24를 참조하십시오.
- 보정. 이 단계에서 XMALab 소프트웨어는 검량 매트릭스를 결정합니다. XMALab에서 X-ray 소스는 초점 거리, 소스의 중심, 소스-이미지 거리와 같은 고유 및 외부 매개변수가 있는 핀홀 카메라로 모델링되며, 보정 단계는 이러한 메트릭을 결정하는 프로세스입니다18. 보정하려면 모든 이미지 세트와 각 보기에 대해 보정 큐브에 배치된 4개의 참조 항목을 각각 선택합니다. 설정에서 이러한 참조는 피라미드, 잭, 돔 및 나선이었습니다(그림 2B). 소프트웨어가 자동으로 점을 찾지 못하면 Compute Calibration을 누릅니다. 모든 보정 이미지가 보정된 후 카메라 설정 최적화를 선택합니다.
- 캘리브레이션 매트릭스 내보내기. 최적화 후 8개의 보정 세트(즉, 실험 전에 캡처된 4개 세트와 실험 후에 캡처된 4개 세트)를 모두 정렬하고 왜곡되지 않은 오류가 가장 작은 이미지 세트를 선택합니다. 각 보정 창의 오른쪽 상단 모서리에 있는 정보 옵션을 눌러 이 값을 찾습니다. 오류가 가장 낮은 이미지에서 File-Export 메뉴에서 MayaCams 2.0 옵션을 선택하여 이미지를 내보냅니다. 자세한 내용 및 가능한 문제점을 디버그하려면 참조20을 참조하십시오.
- 비디오 방사선 촬영 왜곡 없음. 작업 공간을 마커 추적으로 변경하고 + 아이콘을 눌러 CINE 형식으로 캡처된 비디오 방사선 사진을 로드합니다. 로드 프로세스가 완료된 후 파일 내보내기(File-Export) 메뉴에서 왜곡되지 않은 체험판 이미지(Undistorted Trial Images)를 선택하여 왜곡되지 않은 체험판 이미지를 내보냅니다.
- XMALab18 가져오기. 각 피험자에 대해 XMALab 소프트웨어에서 새 임상시험을 생성합니다. 폴더 경로를 Undistortion Grid 이미지에 할당하고 New Trial 대화 상자에서 8개의 보정 이미지 세트를 할당합니다.
- 모델 기반 추적(그림 4)
- 방사선 사진/DRR의 기능 향상(그림 4A-B). 필터를 사용하여 이미지 기능을 향상시키는 것은 정확한 일치를 얻기 위해 필요한 단계입니다. 소프트웨어에서 contrast(intensity detection), Sobel(edge detection), Gaussian(blurring/smoother), Sharpen(가장자리 굵게)을 포함한 4가지 필터의 매개변수를 정의할 수 있습니다. 이러한 필터는 왼쪽 위 위젯에 표시된 Rad Renderer 또는 DRR Renderer 개체를 마우스 오른쪽 버튼으로 클릭하여 선택할 수 있습니다.
참고: 이 연구에서는 방사선 사진의 뼈 이미지 가장자리를 스케일 팩터 3과 블렌드 값 0.4의 Sobel 필터를 사용하여 향상시켰습니다. 또한 알파(이미지 대비)가 2.5이고 베타(이미지 밝기)가 0.9인 대비 필터를 사용하여 방사선 사진의 품질을 더욱 향상시켰습니다. DRR을 방사선 사진과 일치시키기 위해 0.1 블렌드 값과 1.7 스케일 팩터를 가진 Sobel 필터와 함께 0.35의 광선 강도 값을 사용했습니다. - 수동 초기화. 피벗 포인트를 사용하여 각 뼈와 구성 요소의 DRR을 이동하여 DRR과 방사선 사진 간에 가능한 최상의 일치를 얻습니다. 피벗 포인트 는 사용자가 왼쪽 하단 위젯에서 선택한 DRR을 회전하고 변환하는 데 도움이 됩니다. 이 단계가 필요한 이유는 최적화를 수행하기 전에 뼈 또는 임플란트의 위치를 최소 한 번, 적어도 첫 번째 프레임에 대해 초기화해야 하기 때문입니다. W 를 눌러 DRR을 변환 모드로 이동하고 E 를 눌러 DRR을 회전합니다.
참고: 피벗 포인트 위치 변경은 일반적으로 필요하지 않지만 도구 모음의 피벗 이동 옵션을 사용하여 변경할 수 있습니다. - 최적화. C를 누르거나 도구 모음에서 Track Current(현재 추적) 버튼을 클릭하여 DRR과 방사선 사진 간에 가장 일치하는 항목을 찾습니다. 소프트웨어의 기본 절차는 NCC(Normalized Cross-Correlation) 비용 함수와 입자 군집 최적화 방법 및 내리막 심플렉스 절차26,27을 모두 사용합니다. 이 프로세스를 매칭 또는 추적 단계라고도 합니다. 최적화 절차는 추적 대화 상자를 통해 실행할 수도 있습니다. 이렇게 하려면 도구 모음에서 Tracking Dialog 옵션을 누릅니다. 새 창이 열리면 From Frame 및 To Frame을 0으로 변경하고 OK를 누릅니다.
참고: NCC는 방사선 사진과 DRR 간의 유사성을 측정하는 기능이며, NCC 값이 0에 가까울수록 더 나은 일치를 보여주었습니다. 그러나 이 값을 달성하는 것은 전적으로 이미지 필터와 캡처 품질에 따라 달라집니다. NCC의 값은 "터미널 창"에서 확인할 수 있습니다. - 매칭 프로세스 - 첫 번째 패스. 첫 번째 프레임이 자동으로 최적화된 후 추적 대화 상자를 열고 시작 프레임을 0으로 변경하고 종료 프레임을 마지막 프레임 번호(오른쪽 하단에 위치할 수 있음)로 변경합니다. 소프트웨어의 기본 일치 프로세스는 현재 프레임을 일치 프로세스에 대한 DRR의 초기 위치로 사용합니다. 최적화 프로세스는 초기 위치의 3mm 및 3° 영역 내에서 입자 군집 최적화(PSO) 방법을 사용합니다.
- 매칭 프로세스 - 최종 패스 (그림 4C). 잘못된 초기화 또는 필터로 인해 자동 일치 프로세스가 실패할 수 있으므로 모든 프레임을 수동으로 확인하여 최적화가 올바르게 실행되었는지 확인하십시오. DRR과 방사선 사진이 올바르게 일치하지 않으면 섹션 2.3.2 및 2.3.3에 설명된 단계를 반복합니다.
참고: 손목 추적은 뼈 겹침의 영향을 줄이고 일치 정확도를 향상시키기 위해 두 번째 및 세 번째 중수골(MC2-MC3)을 포함하는 모델에서 처음 수행되었습니다. 방사선 사진에서 결합된 DRR 위치와 회전을 찾은 후, 일치하고 최적화된 MC2-MC3 위치를 MC3 부분 이미지 볼륨으로 변환하고 MC3의 초기 위치를 시딩했습니다. 이러한 시드 위치를 사용하여 MC3를 추적했습니다. MC3와 유사하게, 모든 작업 중 비디오 방사선 사진에서 요골, 척골, 요골 구성 요소 및 수근 구성 요소도 추적되었습니다.
- 방사선 사진/DRR의 기능 향상(그림 4A-B). 필터를 사용하여 이미지 기능을 향상시키는 것은 정확한 일치를 얻기 위해 필요한 단계입니다. 소프트웨어에서 contrast(intensity detection), Sobel(edge detection), Gaussian(blurring/smoother), Sharpen(가장자리 굵게)을 포함한 4가지 필터의 매개변수를 정의할 수 있습니다. 이러한 필터는 왼쪽 위 위젯에 표시된 Rad Renderer 또는 DRR Renderer 개체를 마우스 오른쪽 버튼으로 클릭하여 선택할 수 있습니다.
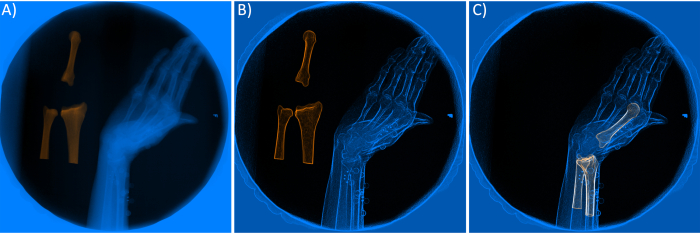
그림 4. A) 뼈의 DRR(Digital Reconstructed Radiographs)을 사용하여 X선 소스의 캡처된 방사선 사진. B) 향상된(필터링된) 방사선 사진 및 DRR.C) 최적화 프로세스 후 일치하는 DRR. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
- 데이터 감소. 프레임 속도와 방사선 촬영 이미지 품질을 기반으로 이동 평균 방법(5프레임 범위)과 같은 필터링 접근 방식을 활용할 수 있습니다. 이렇게 하려면 도구 모음 메뉴에서 Tracking-Advanced Dialog를 선택하고 Smooth 버튼을 클릭합니다. 이 접근 방식은 이 연구의 모든 캡처에 사용되었습니다.
- 뼈/임플란트 위치 내보내기. 각 뼈가 방사선 사진과 일치하고 모든 프레임이 최적화된 후 Save Tracking 버튼을 클릭하고 매트릭스 형식 출력을 선택하여 X-ray 세계에서 DRR의 4x4 변환 매트릭스를 내보냅니다. 이 변환 매트릭스는 보정된 X-ray 세계 좌표계에서 뼈/임플란트의 부분 이미지 볼륨의 회전 및 변환을 정의하며 추가 처리 및 모션 계산에 사용할 수 있습니다. 부분 이미지 볼륨의 좌표계는 의미 있는 생체 역학적 분석을 위해 해부학적 좌표계로 전송되어야 합니다.
3. 데이터 분석
- 좌표계 (그림 5). 운동학을 보고하려면 해부학적 및 기하학적 랜드마크를 기반으로 뼈와 임플란트 구성 요소에 대한 좌표계(CS)를 구성합니다. 이러한 CS를 구성한 후 반복 최근접점 알고리즘을 사용하여 새 CS에 있는 모델을 섹션 2.1.4 에서 생성된 표면 모델에 등록합니다. 이 일대일 등록은 운동학 계산에 사용될 새로운 4x4 변환 행렬을 계산합니다.
참고: 본 연구에서는 요골, 척골, 제3 중수골, 손목 성분, 요골 성분, 폴리에틸렌 캡 및 capitate에 대한 CS는 이전에 설명된 방법을 사용하여 생성되었습니다 16,22,23.
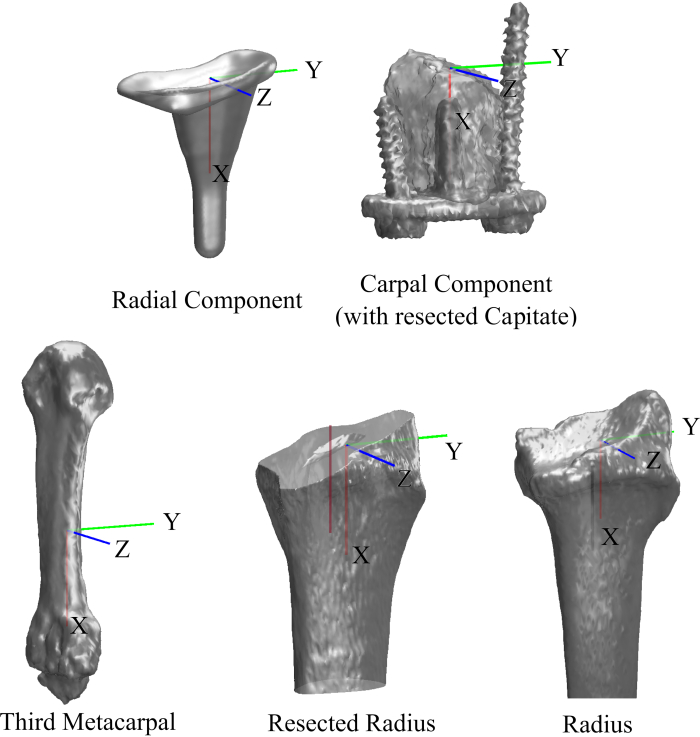
그림 5. 뼈와 임플란트 구성 요소의 좌표계. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
- 운동학. 이 연구에서는 손목 움직임을 반경에 대한 MC3의 움직임으로 정의하고, 운동학적 데이터는 중립 손목 위치에 상대적인 것으로 보고되었습니다.
- DRUJ 해석의 경우, 헬리컬 모션 축(HAM) 매개변수28 을 계산하여 운동학을 중립 포즈에 대한 척골 CS에서 반지름 CS의 상대 운동으로 설명합니다.
- HAM 분석을 사용하여 굴곡-신전 및 요골-척골 편차에서 손목의 회전 중심(COR)을 결정합니다.
- COR의 1차원 근위-원위 이동을 설명하기 위해, 건강한 손목에 대해 투영된 COR을 회전16의 나사 축에서 가장 짧은 거리를 가진 capitate 뼈의 중심 축에 있는 점으로 정의합니다.
- HAM 나사 축을 사용하여 척골 좌표계에서 HAM 회전을 분해하고 팔뚝의 내전(양)과 외전(음)을 계산합니다. 중립 포즈는 내전-외전(pronation-supination, PS)이 0일 때 정의되었습니다.
- 마지막으로, 척골 분산(UV)을 척골 중심와와 요골의 시그모이드 노치 사이의 거리로 정의합니다.
- 조음 패턴
- 폴리에틸렌 캡과 방사형 구성 요소 사이의 접촉 패턴을 wrist kinematics 및 구성 요소별 거리 필드29를 사용하여 계산합니다.
- 각 3D 표면 모델에 대한 거리 필드를 표면에서 부호 있는 거리의 체적 배열로 계산합니다.
- 각 자세에 대한 폴리에틸렌 캡 및 방사형 구성 요소의 표면에 있는 거리 필드의 근접 값을 계산합니다.
- 구성 요소 간의 접촉 패치를 얻으려면 이러한 근접 값을 획득 시스템의 해상도에 맞게 조정합니다(이 연구에서는 거리 제외 임계값을 0.70mm로 선택함).
- 통계 분석
- Bland-Altman 분석을 사용하여 BVR과 OMC14, 30 간의 치우침(평균 차이)과 95% 일치 한계(치우침 ± 1.96SD)를 입증하여 정확도를 평가합니다.
- 일반화 선형 모델(GLM)을 사용하여 건강한 손목의 회전 중심 거동을 설명하고, UV와 PS의 변화(UV = p1×PS2 + p2×PS) 사이의 관계를 구합니다. 여기서 p1 및 p2 는 선형 회귀를 사용하여 최적화된 계수입니다. RMSE(제곱 평균 제곱 오차) 메트릭을 사용하여 모델의 정확도를 평가합니다.
결과
모델 기반 추적을 위한 2D-3D 이미지 정합 소프트웨어의 선택은 부분적으로 GPU(그래픽 프로세서 장치) 및 HPC(고성능 컴퓨팅) 시스템에 대한 액세스에 따라 달라집니다. 이러한 프로그램에는 서로 다른 파이프라인이 있으며 현재로서는 프로그램 간에 공통된 방법론이 없습니다. 이 연구에서는 Brown University25에서 개발한 오픈 소스 2D-3D 이미지 등록 프로그?...
토론
BVR(Biplanar videoradiography)은 손목과 원위 요골 관절의 뼈 및 임플란트 움직임을 밀리미터 이하 및 미만 각도의 정확도로 측정하는 데 사용할 수 있는 이미지 기반 방법입니다. 여기에서 설명한 연구에서 BVR은 건강한 손목에 대한 투영된 COR의 정확한 패턴과 TWA 접촉 패턴을 식별하는 데 사용되었습니다. 이러한 발견은 차세대 전체 손목 치환술의 설계에 영향을 미칠 수 있으?...
공개
우리는 선언할 이해 상충이 없습니다.
감사의 말
저자는 의정서를 수정한 Josephine Kalshoven과 Lauren Parola에게 감사를 표합니다. 저자는 또한 데이터 수집 전반에 걸쳐 도움을 준 Erika Tavares와 Rohit Badida, 데이터 해석에 도움을 준 Kalpit Shah, Arnold-Peter Weiss, Scott Wolfe에게 감사를 표합니다. 이 연구는 미국 국립보건원(National Institutes of Health P30GM122732, COBRE Bio-engineering Core)의 지원과 미국 손 수술 재단(American Foundation for Surgery of the Hand, AFSH)의 보조금으로 가능했습니다.
자료
| Name | Company | Catalog Number | Comments |
| 3D Surface Scanner | Artec 3D | Artec Space SpiderTM | Luxembourg |
| Autoscoper | Brown University | https://simtk.org/projects/autoscoper | https://doi.org/10.1016/j.jbiomech.2019.05.040 |
| CT Scanner | General Electric (GE) | Lightspeed 16 | Milwaukee, WI, USA |
| Geomagic Wrap 3D | 3DSystems | Version 2017 | Rock Hill, SC, USA |
| Graphics Processing Unit (GPU) | Nvidia | GeForce GTX 1080 | CUDA-enabled GPU |
| High-speed Video Cameras | Phantom | Version 10 | Vision Research, Wayne, NJ, USA |
| Image Intensifier | Dunlee | 40 cm diameter | Aurora, IL, USA |
| ImageJ | Open-source (Brown University) | https://imagej.net/Fiji | https://doi.org/10.1038/nmeth.2019 |
| Matlab | The MathWorks, Inc. | R2017a to R2020a | Natick, MA, USA |
| Mimics | Materialise | Version 19.0 to 22.0 | Leuven, Belgium |
| Motion Capture Cameras | Qualisys | Oqus 5+ | Gothenburg, Sweden |
| Pulsed X-ray Generators | EMD Technologies | EPS 45–80 | Saint-Eustache, Quebec, QC, Canada |
| Undistortion Grid | McMaster-Carr | 9255T641 | Steel Perforated Sheet Staggered Holes, 0.048" Thk, 0.125" Hole Dia, 36" X 40" |
| Wrist Implant (In-vitro Study) | Integra LifeSciences | Universal 2 | Plainsboro, NJ, USA |
| Wrist Implant (In-vivo Study) | Integra LifeSciences | Freedom | Plainsboro, NJ, USA |
| WristViz | Open-source (Brown University) | https://github.com/DavidLaidlaw/WristVisualizer/tree/master | Open-source software |
| X-ray Tubes | Varian Medical Systems | Model G-1086 | Palo Alto, CA, USA |
| XMALab | Open-source (Brown University) | https://www.xromm.org/xmalab/ | https://doi.org/10.1242/jeb.145383 |
참고문헌
- Leardini, A., Chiari, L., Croce, U. D., Cappozzo, A. Human movement analysis using stereophotogrammetry: Part 3. Soft tissue artifact assessment and compensation. Gait & Posture. 21 (2), 212-225 (2005).
- Miranda, D. L., Rainbow, M. J., Crisco, J. J., Fleming, B. C. Kinematic differences between optical motion capture and biplanar videoradiography during a jump-cut maneuver. Journal of biomechanics. 46 (3), 567-573 (2013).
- Tashman, S., Anderst, W. In vivo measurement of dynamic joint motion using high speed biplane radiography and CT: application to canine ACL deficiency. Journal of Biomechanical Engineering. 125 (2), 238-245 (2003).
- Moore, D. C., et al. Computed Tomography Image-Based Kinematic Analysis: An Overview. Handbook of Imaging in Biological Mechanics. , 115-126 (2014).
- Fedorov, A., et al. 3D Slicer as an Image Computing Platform for the Quantitative Imaging Network. Magnetic resonance imaging. 30 (9), 1323-1341 (2012).
- Choi, Y. S., et al. Four-dimensional real-time cine images of wrist joint kinematics using dual source CT with minimal time increment scanning. Yonsei medical journal. 54 (4), 1026-1032 (2013).
- Boutin, R. D., et al. Real-Time Magnetic Resonance Imaging (MRI) during Active Wrist Motion-Initial Observations. PLoS ONE. 8 (12), 84004 (2013).
- Miranda, D. L., et al. Static and Dynamic Error of a Biplanar Videoradiography System Using Marker-Based and Markerless Tracking Techniques. Journal of Biomechanical Engineering. 133 (12), 121002-121008 (2011).
- Englander, Z. A., et al. In Vivo Anterior Cruciate Ligament Deformation During a Single-Legged Jump Measured by Magnetic Resonance Imaging and High-Speed Biplanar Radiography , In Vivo Anterior Cruciate Ligament Deformation During a Single-Legged Jump Measured by Magnetic Resonance Imaging and High-Speed Biplanar Radiography. The American Journal of Sports Medicine. 47 (13), 3166-3172 (2019).
- Englander, Z. A., Garrett, W. E., Spritzer, C. E., DeFrate, L. E. In vivo attachment site to attachment site length and strain of the ACL and its bundles during the full gait cycle measured by MRI and high-speed biplanar radiography. Journal of Biomechanics. 98, 109443 (2020).
- Anderst, W. J., Les, C., Tashman, S. In vivo serial joint space measurements during dynamic loading in a canine model of osteoarthritis. Osteoarthritis and cartilage: Osteoarthritis Research Society. 13 (9), 808-816 (2005).
- Bey, M. J., Kline, S. K., Zauel, R., Kolowich, P. A., Lock, T. R. In Vivo Measurement of Glenohumeral Joint Contact Patterns. EURASIP journal on advances in signal processing. 2010, (2010).
- Anderst, W. J., Tashman, S. A method to estimate in vivo dynamic articular surface interaction. Journal of Biomechanics. 36 (9), 1291-1299 (2003).
- Akhbari, B., et al. Accuracy of biplane videoradiography for quantifying dynamic wrist kinematics. Journal of Biomechanics. 92, 120-125 (2019).
- Akhbari, B., et al. Kinematic Accuracy in Tracking Total Wrist Arthroplasty with Biplane Videoradiography using a CT-generated Model. Journal of Biomechanical Engineering. , (2019).
- Akhbari, B., et al. Proximal-distal shift of the center of rotation in a total wrist arthroplasty is more than twice of the healthy wrist. Journal of Orthopaedic Research: Official Publication of the Orthopaedic Research Society. 38 (7), 1575-1586 (2020).
- Wang, J., Blackburn, T. J. The AAPM/RSNA Physics Tutorial for Residents. RadioGraphics. 20 (5), 1471-1477 (2000).
- Knörlein, B. J., Baier, D. B., Gatesy, S. M., Laurence-Chasen, J. D., Brainerd, E. L. Validation of XMALab software for marker-based XROMM. The Journal of Experimental Biology. 219 (23), 3701-3711 (2016).
- Brainerd, E. L., et al. X-ray reconstruction of moving morphology (XROMM): precision, accuracy and applications in comparative biomechanics research. Journal of experimental zoology. Part A, Ecological genetics and physiology. 313 (5), 262-279 (2010).
- X-ray Camera Calibration. XROMM / XMALab / wiki Available from: https://bitbucket.org/xromm/xmalab/wiki/X-ray%20Camera%20Calibration (2020)
- Akhbari, B., et al. Biomechanics of the Distal Radioulnar Joint in In vivo Forearm Pronosupination. Journal of Wrist Surgery. , (2020).
- Akhbari, B., et al. Predicting carpal bone kinematics using an expanded digital database of wrist carpal bone anatomy and kinematics. Journal of Orthopaedic Research: Official Publication of the Orthopaedic Research Society. , (2019).
- Moore, D. C., et al. Three-dimensional in vivo kinematics of the distal radioulnar joint in malunited distal radius fractures. The Journal of Hand Surgery. 27 (2), 233-242 (2002).
- Knörlein, B. J. Correct for Fluoroscope Distortion (X-ray images). XROMM / XMALab / wiki. , (2020).
- . Autoscoper Available from: https://simtk.org/projects/autoscoper (2019)
- Kennedy, J., Eberhart, R. . Particle swarm optimization. , (1995).
- Nelder, J. A., Mead, R. A Simplex Method for Function Minimization. The Computer Journal. 7, 308 (1965).
- Panjabi, M. A Mathematical Approach for three-dimensional analysis of the mechanics of the spine. J Biomechanics. 4, 203-211 (1971).
- Marai, G. E., et al. Estimating joint contact areas and ligament lengths from bone kinematics and surfaces. IEEE transactions on bio-medical engineering. 51 (5), 790-799 (2004).
- Bland, J. M., Altman, D. G. Measuring agreement in method comparison studies. Statistical methods in medical research. 8 (2), 135-160 (1999).
- . Camera calibration With OpenCV Available from: https://docs.opencv.org/master/index.html (2020)
- Anderst, W. J., Lee, J. Y., Kang, J. D. In Vivo Cervical Facet Joint Capsule Deformation During Flexion-Extension. Spine. 39 (8), 514-520 (2014).
- Anderst, W. J., Vaidya, R., Tashman, S. A technique to measure three-dimensional in vivo rotation of fused and adjacent lumbar vertebrae. The Spine Journal. 8 (6), 991-997 (2008).
- Mozingo, J. D., et al. Validation of imaging-based quantification of glenohumeral joint kinematics using an unmodified clinical biplane fluoroscopy system. Journal of Biomechanics. 71, 306-312 (2018).
- Akbari-Shandiz, M., et al. MRI vs CT-based 2D-3D auto-registration accuracy for quantifying shoulder motion using biplane video-radiography. Journal of Biomechanics. 82, 375-380 (2019).
- Bey, M. J., et al. In vivo shoulder function after surgical repair of a torn rotator cuff: glenohumeral joint mechanics, shoulder strength, clinical outcomes, and their interaction. The American journal of sports medicine. 39 (10), 2117-2129 (2011).
- Bey, M. J., Kline, S. K., Zauel, R., Kolowich, P. A., Lock, T. R. In Vivo Measurement of Glenohumeral Joint Contact Patterns. EURASIP journal on advances in signal processing. 2010, (2010).
- Bey, M. J., Zauel, R., Brock, S. K., Tashman, S. Validation of a New Model-Based Tracking Technique for Measuring Three-Dimensional, In Vivo Glenohumeral Joint Kinematics. Journal of biomechanical engineering. 128 (4), 604-609 (2006).
- Fu, E., et al. Elbow Position Affects Distal Radioulnar Joint Kinematics. The Journal of Hand Surgery. 34 (7), 1261-1268 (2009).
- Martin, D. E., et al. Model-Based Tracking of the Hip: Implications for Novel Analyses of Hip Pathology. The Journal of Arthroplasty. 26 (1), 88-97 (2011).
- Miranda, D. L., et al. Static and Dynamic Error of a Biplanar Videoradiography System Using Marker-Based and Markerless Tracking Techniques. Journal of Biomechanical Engineering. 133 (12), 121002-121008 (2011).
- Stentz-Olesen, K., et al. Validation of static and dynamic radiostereometric analysis of the knee joint using bone models from CT data. Bone & Joint Research. 6 (6), 376-384 (2017).
- Anderst, W., Zauel, R., Bishop, J., Demps, E., Tashman, S. Validation of Three-Dimensional Model-Based Tibio-Femoral Tracking During Running. Medical engineering & physics. 31 (1), 10-16 (2009).
- Kessler, S. E., et al. A Direct Comparison of Biplanar Videoradiography and Optical Motion Capture for Foot and Ankle Kinematics. Frontiers in Bioengineering and Biotechnology. 7, 199 (2019).
- Maharaj, J. N., et al. The Reliability of Foot and Ankle Bone and Joint Kinematics Measured With Biplanar Videoradiography and Manual Scientific Rotoscoping. Frontiers in Bioengineering and Biotechnology. 8, 106 (2020).
- Ito, K., et al. Direct assessment of 3D foot bone kinematics using biplanar X-ray fluoroscopy and an automatic model registration method. Journal of Foot and Ankle Research. 8, 21 (2015).
- Wang, B., et al. Accuracy and feasibility of high-speed dual fluoroscopy and model-based tracking to measure in vivo ankle arthrokinematics. Gait & Posture. 41 (4), 888-893 (2015).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유